一种快速识别苯硫酚的荧光探针的制作方法
本发明涉及化学分析技术领域,具体涉及一种快速识别苯硫酚的荧光探针。
背景技术:
苯硫酚(phsh)是一种广泛存在于医药、农药及化工中间体制备过程中的高毒性污染物。苯硫酚可通过吸入、食入、经皮吸收等途径对人、老鼠及鱼等其他生物造成一系列的严重危害。苯硫酚对眼睛、皮肤产生强烈的刺激作用;可造成呼吸困难、昏迷甚至死亡;高浓度的苯硫酚能够导致鱼和老鼠的死亡。因此,建立一种可用于环境及生物体中苯硫酚的特异性检测方法具有重要的实际应用价值。
目前,苯硫酚的检测方法有高效液相色谱法、气相色谱法、电化学法、紫外分光光度法和荧光探针分析法等。其中,荧光探针分析法因其操作简单、灵敏度高、检测限低、响应快、抗干扰能力强以及可在活细胞、组织或生物体中直接检测等优点而受到广泛关注。由于苯硫酚是一种易挥发的化学物质,所以为保证检测的高时效性,这就要求探针对苯硫酚具有快速响应的功能。并且,目前的苯硫酚荧光探针虽然都实现了对活细胞中苯硫酚的检测,但是,在检测过程中对苯硫酚的响应速度不够快,同时,大多荧光探针的水溶性较差以及抗干扰能力不强,进而导致其使用范围受到局限。
技术实现要素:
本发明的目的在于,针对上述现有技术的不足,提出一种快速识别苯硫酚的荧光探针,该种荧光探针在检测过程中对苯硫酚的响应速度较快、水溶性较强以及很好的抗干扰性,进而大大的提高了该种荧光探针的适用范围。
本发明提出一种快速识别苯硫酚的荧光探针,通过与苯硫酚反应,生成具有强荧光性的反应产物,具有如下所示的结构式:
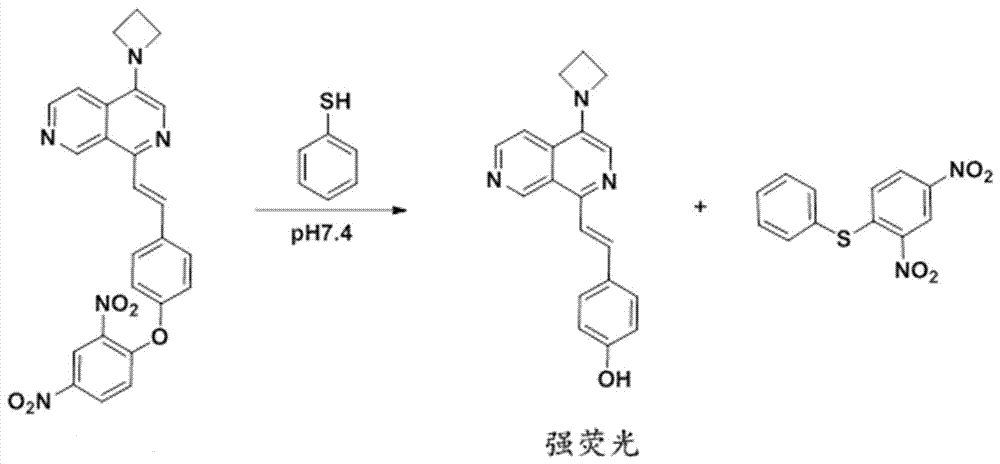
本发明的荧光探针由于含有吸电子的2,4-二硝基苯醚基识别基团,使荧光探针处于荧光淬灭状态。当荧光探针检测到苯硫酚时,苯硫酚首先亲核进攻识别基团,并发生苯醚键断裂,得到具有强荧光的反应产物,通过监测产物的荧光强度,可以实时检测苯硫酚的浓度。
由于2,4-二硝基苯醚基识别基团具有较强的吸电子能力,同时由于在本发明的荧光探针一侧具有氮杂环丁烷基,其对整个共轭体系的电子云密度发生变化,使苯醚键断裂速度较快,所以在检测苯硫酚时,本发明提供的荧光探针能够与苯硫酚快速响应,再者本荧光探针具有萘啶类衍生物结构,萘啶类衍生物的发射波长在近红外区域,而且具有较大的stokes位移(225nm),具有很强的抗干扰能力,进而对苯硫酚识别针对性较强,从而达到灵敏度高、响应速度快的特点。
由于本发明的荧光探针具有较强的抗干扰能力和响应速度,所以可以适用于干扰性较强的样品检测,例如水环境以及各种生物样品(细胞、斑马鱼)。
进一步的,所述反应产物的检测波长为575nm~585nm。该反应产物在580nm处具有最大发射波长。
进一步的,一种快速识别苯硫酚的荧光探针的制备方法,包括以下步骤:
(1)、将2,7-萘啶-1(2h)-酮与三溴氧磷的反应物经过萃取、干燥、分离纯化,制得中间体a;
(2)、将步骤(1)的中间体a与甲基硼酸和碳酸氢钠发生反应,得到中间体b;
(3)、将步骤(2)中的中间体b与液溴在乙酸溶液中反应,得到中间体c;
(4)、将步骤(3)的中间体c、氮杂环丁烷和2-二环己基磷-2,4,6-三异丙基联苯混合反应得到中间体d;
(5)、将步骤(4)的中间体d、对羟基苯甲醛、哌啶和乙酸溶于甲苯中,反应得到中间体e;
(6)、将步骤(5)的中间体e、2,4-二硝基氟苯和碳酸钾溶于n,n-二甲基甲酰胺中,反应得到荧光探针。
进一步的,步骤(1)中所述分离纯化采用硅胶色谱法。
进一步的,步骤(2)还包含pd(pph3)cl2。
进一步的,步骤(3)中所述中间体c通过二氯甲烷萃取后制得。
进一步的,步骤(4)还包含催化剂。
进一步的,所述催化剂为叔丁醇钠和pd(dba)2。
进一步的,步骤(4)中所述反应溶剂为二氧六烷。
进一步的,步骤(5)中所述反应试剂为甲苯。
本发明的一种快速识别苯硫酚的荧光探针,该种荧光探针通过具有较强吸电子能力的2,4-二硝基苯醚基识别基团能够快速识别苯硫酚,反应迅速,同时生产具有强荧光性的反应产物,灵敏度高,响应速度快;由于该荧光探针具有较强的抗干扰能力,能够特异性识别苯硫酚,适用于各种干扰强度较大样品的苯硫酚检测。
附图说明
图1为本发明荧光探针对苯硫酚的识别机理反应示意图;
图2为为本发明荧光探针的1hnmr谱图;
图3为本发明荧光探针的1cnmr谱图;
图4为本发明荧光探针与苯硫酚反应前后的荧光光谱图;
图5为本发明荧光探针与不同浓度的苯硫酚反应的荧光光谱图;
图6为本发明荧光探针与苯硫酚反应不同时间的荧光光谱图;
图7为本发明荧光探针和苯硫酚分别在不同巯基化合物、氨基酸和阴离子共存条件下反应后在580nm处荧光强度的柱形图;
图8为本发明荧光探针在活细胞中的荧光成像;
图9为本发明荧光探针在活体斑马鱼中的荧光成像。
具体实施方式
为下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外,本领域技术人员对本发明所做的各种改动或修改,这些等价形式同样落于本申请所要求保护的范围内。本发明实施例中的配比均为以重量计。
实施例1
一种快速检测苯硫酚的荧光探针的制备方法,具体包括以下步骤:
中间体a的合成:将1g(6.84mmol)的2,7-萘啶-1(2h)-酮和9.81g(34.21mmol)的三溴氧磷溶于10ml的乙腈中,加热到80℃反应1h。向反应体系中加入冰水使三溴氧磷淬灭,然后调ph至中性。将溶液用二氯甲烷萃取3次,然后用na2so4干燥二氯甲烷萃取液,经过减压蒸馏得到红色粗产品,继续硅胶柱色谱纯化,制得白色固体,即为中间体a(980mg,yield69%)。1hnmr(400mhz,cdc13):δ9.76(s,1h),8.82(d,j=4hz,1h),8.48(d,j=4hz,1h),7.68(d,j=8hz,1h),7.61(d,j=8hz,1h)。
中间体b的合成:在氩气条件下,将400mg(1.91mmol)的中间体a和134mg(0.19mmol)的pd(pph3)cl2溶解于10ml的二氧六烷。然后依次加入已溶解了138mg(2.3mmol)甲基硼酸的10ml的二氧六烷溶液和209mg(2.5mmol)的碳酸氢钠,在130℃搅拌反应1h。然后减压蒸馏除溶剂,残留液经硅胶柱色谱法纯化,制得黄色稠状液体,即为中间体b(180mg,yield66%)。1hnmr(400mhz,cdc13):δ9.59(s,1h),8.71(d,j=5.6hz,1h),8.57(d,j=6hz,1h),7.61(d,j=5.6hz,1h),7.48(d,j=6hz,1h),3.06(s,3h)。
中间体c的合成:将144mg(1mmol)的中间体b溶于10ml的乙酸中,向反应液中滴加211mg(1.2mmol)的液溴,室温下搅拌5小时。反应完毕后用nahco3调至中性,然后用二氯甲烷多次萃取,萃取液用na2so4干燥,经过减压蒸馏和硅胶柱色谱法纯化制得黄色油装液体,即为中间体c(154mg,yield69%)。
1hnmr(400mhz,dmso-d6)δ9.66(s,1h),9.02(s,1h),8.73(d,j=5.7hz,1h),7.78(d,j=5.5hz,1h),3.04(s,3h)。
中间体d的合成:将100mg(0.45mmol)的中间体c、77.1mg(1.35mmol)的氮杂环丁烷、53mg(0.54mmol)的叔丁醇钠、51.8mg(0.09mmol)的pd(dba)2和85.8mg(0.18mmol)的2-二环己基磷-2,4,6-三异丙基联苯溶解于二氧六烷,在氩气保护下100℃反应12h。反应完毕后,将反应液冷却至室温,经过滤、50ml二氯甲烷洗涤、减压蒸馏制得粗产品。粗产品经硅胶柱色谱法纯化制得黄色油状液体,即为中间体d(53.8mg,yield60%)。1hnmr(400mhz,dmso-d6)δ8.97(s,1h),8.41(d,j=5.4hz,1h),7.83(s,1h),7.63(d,j=5.7hz,1h),4.21(t,j=6.9hz,5h),2.91(s,3h),2.43-2.33(m,2h)。
中间体e的合成:将199mg(1mmol)的中间体d、112mg(0.92mmol)的对羟基苯甲醛、0.5ml哌啶和0.5ml的乙酸溶于30ml的甲苯中,140℃反应12h。反应液经减压蒸馏、硅胶柱色谱法纯化制得黄色固体,即为中间体e(146mg,yield48%)。1hnmr(400mhz,dmso-d6)δ9.50(s,1h),8.93(d,j=2.8hz,1h),8.62(d,j=5.6hz,1h),8.49-8.46(m,1h),8.38(d,j=15.2hz,1h),8.08(t,j=11.7hz,3h),7.87(s,1h),7.72(d,j=5.6hz,1h),7.35(d,j=8.4hz,2h),7.28(d,j=9.2hz,1h),4.25(t,j=7.2hz,4h),2.45-2.38(m,2h)。
荧光探针的合成:将50mg(0.16mmol)的中间体e、37mg(0.2mmol)的2,4-二硝基氟苯和碳酸钾溶于10ml干燥的n,n-二甲基甲酰胺中。室温搅拌1h。将反应液倒入冰水中,经过过滤、洗涤、硅胶柱色谱法纯化制得黄色固体,即得荧光探针(58mg,yield75%)。1hnmr(600mhz,dmso-d6)δ=9.46(s,1h),9.13(s,1h),8.61(t,j=7.4hz,2h),8.36(d,j=15.5hz,1h),8.29(d,j=8.3hz,1h),8.00(d,j=8.9hz,3h),7.86(s,1h),7.72(d,j=5.2hz,1h),7.26(d,j=7.6hz,2h),4.24(t,j=6.6hz,4h),2.44-2.38(m,2h)。
实施例2
测定实施例1所得荧光探针与苯硫酚反应的效果。
使用10mmpbs(ph=7.4)缓冲液配置100μm的实施例1中荧光探针溶液,用乙腈配置10mm的苯硫酚储液。取100μl上述荧光探针的溶液和900μlpbs(ph=7.4)缓冲液于比色皿中,检测其355nm激发下的荧光光谱图,如图4实线部分;取100μl上述化合物f的溶液、895μlpbs(ph=7.4)缓冲液和5μl的苯硫酚储液于比色皿中,检测其355nm激发下的荧光光谱图,如图4虚部分。
从图4虚线和实线对比可以看出,荧光探针背景低,并且对苯硫酚响应强,是一种荧光增强型的苯硫酚探针。
实施例3
测定实施例1所得荧光探针与不同浓度苯硫酚反应的分析。
向比色皿中加入100μl荧光探针溶液和pbs(ph=7.4)缓冲液,再分别加入工作浓度分为0,2,4,6,8,10,20,40,60,80,90,100μm的苯硫酚,配制成1ml的反应体系,测定不同浓度的苯硫酚与荧光探针反应30秒后的荧光光谱图,如图5所示。
从图5可以看出,在一定浓度范围内,反应体系在580nm处的荧光强度随苯硫酚的浓度增加而增加,说明该探针可以检测不同浓度下的苯硫酚。
实施例4
测定实施例1所得荧光探针与苯硫酚反应强度随时间的变化。
向比色皿中加入100μl上述荧光探针溶液、890μl的pbs(ph=7.4)缓冲液,10μl的苯硫酚储液,确保反应体系中探针的工作浓度为10μm,苯硫酚的工作浓度为100μm。每隔2秒检测该反应体系在355nm激发下的荧光光谱图,如图6所示。
从图6可以看出,在20秒内,反应体系在580nm处的荧光强度随与苯硫酚的反应时间成正比关系,说明该探针可以快速检测苯硫酚,响应速度快。
实施例5
测定实施例1所得荧光探针检测苯硫酚时的抗干扰能力。
向比色皿中加入100μl荧光探针溶液,然后分别加入200μm干扰试剂,如c6h5nh2、cys、hcy、gsh、ala、ki、nan3、nascn、nahs、c6h5oh、nano2,分别测试加入不同干扰试剂后反应体系在580nm的荧光强度,如图7中黑色柱形;图7中白色柱形表示再分别向不同体系中加入100μm的苯硫酚,检测其在580nm的荧光强度。
从图7中可以看出在存在不同的干扰试剂下,探针对苯硫酚仍然具有较准确的检测效果,说明该探针的抗干扰能力强。
实施例6
测定实施例1所得荧光探针检测实际水环境中的苯硫酚。
分别从武汉市东湖、南湖和长江中取500ml水样,用不同的水样将苯硫酚储液稀释成0,10,30,100μm的浓度。分别向比色皿中加入100μl荧光探针溶液、800μl的pbs(ph=7.4)缓冲液和100μl含不同浓度苯硫酚的水样,检测其在580nm处的荧光强度,根据荧光强度计算出水样中苯硫酚的浓度,如表1所示。
从表1中可以看出利用荧光探针测定实际水样中苯硫酚的理论含量和苯硫酚的实际含量具有较好的一致性,说明该荧光方法测定实际水样具有较好的准确度。
实施例7
测定实施例1所得荧光探针对活细胞中苯硫酚的成像检测。
将hepg2细胞种于六孔板中,设置实验组和对照组。对照组中加入荧光探针溶液,使探针工作浓度为10μm,直接用荧光倒置显微镜进行明场成像和红色通道的荧光成像;实验组中先加入mtp使其工作浓度为30μm,孵育30min后洗涤,再向hepg2细胞中加入荧光探针溶液,使探针工作浓度为10μm,分别孵育10min,20min,30min后,对孵育不同时间的hepg2细胞进行明场成像和红色通道的荧光成像,如图8所示。
从图8中可以看出探针孵育时间越长,细胞的荧光强度越大,说明该探针可以实时检测细胞中的苯硫酚。
实施例8
测定实施例1所得荧光探针对活体斑马鱼中苯硫酚的成像检测。
将生长0~7天的斑马鱼幼苗培养于6孔板中分成两组,即实验组和空白对照组,每组5条斑马鱼幼苗。空白对照组中加入荧光探针溶液,使探针工作浓度为10μm,孵育30min后直接用荧光倒置显微镜进行明场成像和红色通道的荧光成像;实验组中先加入mtp使其工作浓度分别为50μm、100μm,孵育6h后洗涤,再向斑马鱼培养液中加入荧光探针溶液,使探针工作浓度为10μm,孵育30min后,对孵育不同浓度mtp的斑马鱼幼苗进行明场成像和红色通道的荧光成像,如图9所示。
从图9中可以看出,孵育的mtp浓度越高,斑马鱼的荧光强度越强,说明该探针可以检测斑马鱼中的苯硫酚并进行荧光成像检测。
实施例9
本发明荧光探针与目前现有其他探针的检测参数、斯托克斯位移、响应时间以及应用范围对比,对比结果见表2。
通过表2可知,本发明苯硫酚荧光探针相比其他探针,响应时间短,斯托克斯位移大,具有快速并且较强的抗干扰能力,应用范围广泛。
以上对本发明的实施例进行了示例性说明,但所述内容仅为本发明的较佳实施例,不能被认为用于限定本发明的实施范围。凡依据本发明申请范围的均等变化与改进等,均应归属于本发明的专利涵盖范围之内。
- 还没有人留言评论。精彩留言会获得点赞!