一种以噻唑为母体的丙烯酰酯类化合物作为荧光探针的应用及其制备方法与流程
本发明涉及生物分析技术领域,特别涉及一种以噻唑为母体的丙烯酰酯类化合物作为荧光探针的应用及其制备方法。
背景技术:
硫醇类化合物(gsh,cys,hcy)在人体生理学方面扮演着重要角色chemicalsocietyreview,2013,(44):6019-6031.谷胱甘肽(gsh)是最丰富的细胞内非蛋白质硫醇,参与很多细胞内的活动,包括维持细胞内氧化还原活性,细胞内信号转导和基因调控。半胱氨酸(cys)的异常水平与和许多疾病相关,如生长缓慢,脱发,水肿,嗜睡,肝脏损伤,肌肉和脂肪的损失,皮肤病变等。同型半胱氨酸(hcy)含量异常可能导致认知障碍,心血管疾病,阿尔茨海默病等。更具体地说,在细胞中,gsh是小分子中最丰富的硫醇(1-10mmol),和氧化性谷胱甘肽(gssg)之间存在氧化还原平衡巯基。据了解,gsh在其中起着关键作用,控制氧化应激以维持细胞内环境稳定。此外,它的含量异常可能导致很多疾病,其中包括癌症,阿尔茨海默病和心血管疾病等angewandtechemieinternationaledition,2011,(50):10690-10693.因此,检测环境样品和生物体中硫醇一直备受关注。
荧光分析法是指荧光分子/探针与分析物发生作用后,根据其光谱的特性或强度变化对物质进行定性或定量分析的一种重要的光谱分析手段,具有灵敏度高、选择性好、方法简便、快速准确、线性范围宽等优点chemistry,2009,(15):5096–5103;organicletters,2008,(10):49-51.近年来,随着计算机技术、材料科学、生命科学等的快速发展,荧光分析技术在众多领域(如医学研究、生命科学等)中发挥着越来越重要的作用,成为环境监测、药物筛选和重大疾病的诊断等领域的有效手段chemicalsocietyreviews,2011,(40):3483-3495;chemicalsocietyreviews,2013,(42):622—661.基于此,通过荧光分析手段对于gsh,cys,hcy的选择性检测是十分重要的,并且,已报道的探针大都不能区分检测这三种生物体内常见氨基酸,本文报道的探针能比率比色对gsh进行检测,且能区分检测gsh,cys,hcy三种常见氨基酸。
技术实现要素:
为了克服上述现有技术的缺点,本发明的目的在于提供一种以噻唑为母体的丙烯酰酯类化合物作为荧光探针的应用及其制备方法,能够将以噻唑为母体的丙烯酰酯类化合物(btha)作为荧光探针,高选择性、比率检测gsh,高灵敏性检测cys、hcy,具有合成简单、检验灵敏、选择性专一的特点。
为了达到上述目的,本发明采取的技术方案为:
一种荧光探针,所述荧光探针是以噻唑为母体的丙烯酰酯类化合物(btha),其结构式如下所示:
所述荧光探针在二甲亚砜和hepes混合溶液体系中对gsh实现选择性、比率检测的应用。
所述荧光探针btha为5μmol/l时,能够在10mmol/l的hepes和体积/体积=9:1的dmso的体系中比率检测gsh,所述gsh为5-60μmol/l。
所述荧光探针与gsh、cys、hcy室温下反应,荧光性质变化差异明显,具体现象为:btha与10当量gsh作用时,在507nm处草绿色荧光淬灭,460nm处蓝色荧光出现;btha与10当量cys作用时,在507nm处产生草绿色荧光淬灭,460nm处没有新峰出现;btha与10当量hcy作用时,500nm处草绿色荧光只是减弱并没有完全淬灭,460nm处没有新峰出现。
所述荧光探针能够对溶液中的gsh、cys、hcy实现特异性、可视化检测,且对于其他的氨基酸、阴离子和金属阳离子没有响应。
一种以噻唑为母体的丙烯酰酯类化合物作为荧光探针的制备方法,其步骤如下:
步骤1:2-羟基-3-甲氧基苯并噻唑(btmt)的合成:将4.2mmol、0.3ml的2-氨基苯硫酚和3.2mmol、0.48g的邻香草醛在10ml乙醇中溶解后,加入质量分数为30%、1.9ml的h2o2溶液和质量分数为37%、0.79ml的hcl溶液中在室温下搅拌,反应结束后,反应液用水淬灭,真空干燥后乙醇重结晶得到亮黄色固体btmt;
步骤2:2,3-二羟基苯并噻唑(btdh)的合成:btmt在冰浴下加入bbr3,btmt与bbr3质量比为2:3,氮气保护下反应1-2h,然后室温下反应22-26h,反应结束后,反应液用水淬灭,得到黄色固体,经过柱层析得到纯化后的btdh;
步骤3:2-羟基-3-丙烯酯苯并噻唑(btha):将1mmol的btdh溶解在10ml二氯甲烷中,0℃下加入1mmol三乙胺和1mmol丙烯酰氯,三乙胺、丙烯酰氯、btdh物质的量比为1.1:1:1,反应1-2h,继而在室温下反应过夜;
步骤4:反应后处理:反应液用二氯甲烷萃取,水洗,继而柱层析得到纯净的btha。
所述步骤1反应时间为1-2h。
所述步骤1淬灭用水量为10-15ml。
所述步骤2淬灭用水量为10-15ml。
本发明与现有技术相比的有益效果为:
本发明所制备的荧光探针btha在二甲亚砜和4-羟乙基哌嗪乙磺酸(hepes)缓冲盐和dmso混合溶液中,只在507nm处有荧光峰,在逐渐加入gsh后,507nm处的荧光强度不断减弱,在460nm处出现一个新的荧光峰,并且随着gsh加入峰强度随着增强,从而实现比例检测gsh,进而消除了背景荧光的干扰,与之前检测gsh探针相比,本探针具有比率比色,高选择性检测gsh的特点。该荧光探针能够与溶液中的三个氨基酸gsh,cys,hcy作用,对gsh,cys,hcy实现特异性检测,产生不同的荧光信号,从而实现对三者进行高选择性地辨别可视化检测,且对于其他的氨基酸、阴离子和金属阳离子没有响应,具有选择性好、灵敏度高的特点。本发明制备方法简单,易于合成。
附图说明
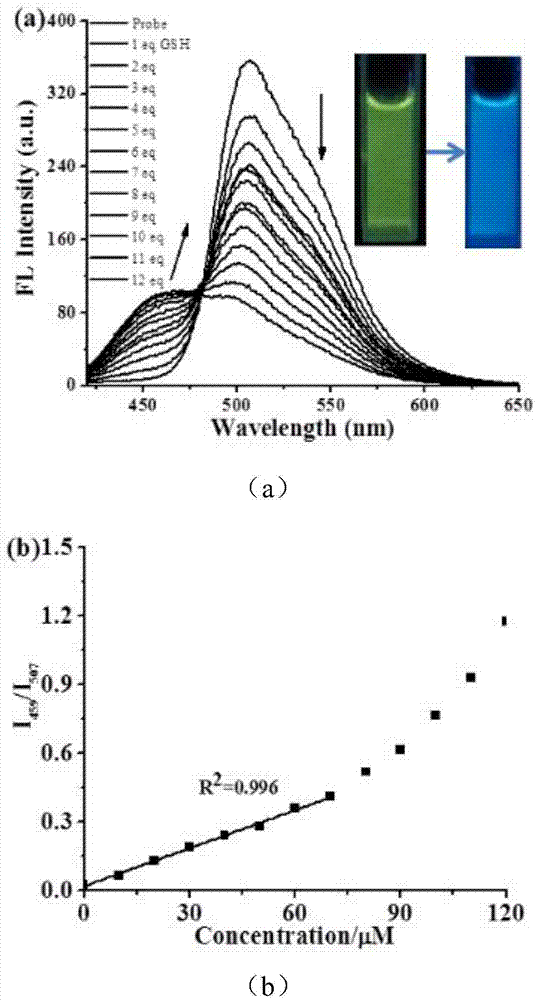
图1是探针btha加入不同浓度gsh的荧光变化图(a)及其线性关系(b)。
图2是探针btha加入不同浓度cys的荧光变化图(a)及其线性关系(b)。
图3是探针btha加入不同浓度hcy的荧光变化图(a)及其线性关系(b)。
图4是探针btha分别加入100μmcys,gsh,hcy的荧光光谱随时间变化图。
图5是探针btha的荧光性质随ph变化的谱图。
图6是探针btha分别先加入100μm生物分子(空白对照,三磷酸腺苷,维生素c,半胱氨酸,高半胱氨酸,谷氨酸,亮氨酸,缬氨酸,组氨酸),再加入100μmgsh在λ459/λ507比值处荧光强度柱状图。
具体实施方式
下面结合实施例对本发明做进一步详细说明。
一种以噻唑为母体的丙烯酰酯类化合物作为荧光探针的制备方法,其步骤如下:
步骤1:2-羟基-3-甲氧基苯并噻唑(btmt)的合成:将4.2mmol、0.3ml的2-氨基苯硫酚和3.2mmol、0.48g的邻香草醛在10ml乙醇中溶解后,加入质量分数为30%、1.9ml的h2o2溶液和质量分数为37%、0.79ml的hcl溶液中在室温下搅拌,反应时间为1-2h,反应结束后,反应液用水淬灭,淬灭用水量为10-15ml,真空干燥后乙醇重结晶得到亮黄色固体btmt。
步骤2:2,3-二羟基苯并噻唑(btdh)的合成:btmt在冰浴下加入bbr3,btmt与bbr3质量比为2:3,氮气保护下反应1-2h,然后室温下反应22-26h,反应结束后,反应液用水淬灭,淬灭用水量为10-15ml,得到黄色固体,经过柱层析得到纯化后的btdh。
步骤3:2-羟基-3-丙烯酯苯并噻唑(btha):将1mmol的btdh溶解在10ml二氯甲烷中,0℃下加入1mmol三乙胺和1mmol丙烯酰氯,三乙胺、丙烯酰氯、btdh物质的量比为1.1:1:1,反应1-2h,继而在室温下反应过夜。
步骤4:反应后处理:反应液用二氯甲烷萃取,水洗,继而柱层析得到纯净的btha。
所制备的探针btha核磁共振氢谱及碳谱数据如下:
1hnmr(500mhz,cdcl3)δ7.99(d,j=8.1hz,1h),7.95(d,j=8.0hz,1h),7.66(d,j=7.9hz,1h),7.55(t,j=7.7hz,1h),7.47(t,j=7.6hz,1h),7.27(d,j=7.9hz,1h),7.02(t,j=7.9hz,1h),6.74(d,j=17.3hz,1h),6.48(dd,j=17.3,10.5hz,1h),6.12(d,j=10.5hz,1h).13cnmr(126mhz,cdcl3)δ168.74,163.95,151.57,150.21,139.53,132.90,132.68,127.50,126.89,125.83,125.73,122.25,121.59,119.09,118.22.
反应化学方程式如下:
探针btha的性能实验。
将合成的探针btha溶解到无水乙腈溶液中配成5mm母液,然后用hepes(10mm)和dmso(v/v=9:1)的混合溶液稀释至相应的浓度对后期研究进行测试。
(1)对gsh响应灵敏性分析
探针btha浓度为1×10-6m加入到hepes/dmso混合(ph=7.4,v/v,1:1)测试体系中,在λ507处有较强荧光,在λ459处无荧光;加入gsh后由图1(a)箭头指示可以看出随着gsh浓度增大,λ507荧光强度逐渐减弱,λ459处荧光强度逐渐增强,当gsh浓度达到120μm时,荧光强度趋于稳定,λ459/λ507的荧光比值随gsh浓度线性变化如图1(b)。
(2)对cys响应灵敏性分析
探针btha浓度为1×10-6m加入到hepes/dmso混合(ph=7.4,v/v,1:1)测试体系中,在λ507处有较强荧光,在λ459处无荧光;加入cys后由图2(a)箭头指示可以看出随着cys浓度增大,λ507荧光强度逐渐减弱,λ459处荧光强度无明显变化;当cys浓度达到120μm时,λ507荧光强度几乎被完全淬灭,λ459处荧光强度增强微弱增强。λ459/λ507的荧光比值随cys浓度线性变化如图2(b)。
(3)对hcy响应灵敏性分析
探针btha浓度为1×10-6m加入到hepes/dmso混合(ph=7.4,v/v,1:1)测试体系中,在λ507处有较强荧光,在λ459处无荧光;加入hcy后由图3(a)箭头指示可以看出随着hcy浓度增大,λ507荧光强度逐渐减弱,λ459处荧光强度无明显变化;当cys浓度达到100μm时,λ507荧光强度减弱至起始一半左右,λ459处荧光强度无增强。λ459/λ507的荧光比值随hcy浓度线性变化如图3(b)。
(4)对gsh/cys/hcy响应动力学研究
探针btha浓度为1×10-6m加入到hepes/dmso混合(ph=7.4,v/v,1:1)测试体系中,在λ507处有较强荧光,在λ459处无荧光。如图4所示,对探针btha检测这三种氨基酸的动力学进行研究,在上述测试体系中,在分别加入gsh,cys,hcy(c=100μm)后,λ459的荧光强度在t=25min左右达到稳定。
(5)探针btha的酸碱稳定性
探针btha浓度为1×10-6m在不同ph溶液中,检测其ph稳定性,由图5可以看出探针在生理环境ph范围内(ph=6-8)荧光强度变化不大,且本发明的测试体系是缓冲溶液中比率检测,固此探针能够在测试体系中不受ph影响高选择性,高灵敏性检测gsh、cys、hcy。
(6)对gsh检测选择性分析
探针btha浓度为1×10-6m在测试体系中加入各种生物分子,由图6可以看出只有gsh加入时,探针荧光(λ459/λ507)增强明显。另外,图6左侧黑色实心柱是探针btha的浓度为1×10-6m先加入其它生物分子(空白对照,三磷酸腺苷,维生素c,半胱氨酸,高半胱氨酸,谷氨酸,亮氨酸,缬氨酸,组氨酸)的荧光强度,可以看出几乎没有荧光,右侧虚线柱是再加入gsh的荧光强度,明显看出荧光增强显著增强,说明对gsh有很好的选择性。
综上所述,本发明的探针btha具有较好的灵敏性和选择性,通过在507nm和460nm两处荧光的比率变化从而实现高准确度和高灵敏度的检测gsh,而且由于加入gsh后,探针荧光颜色发生从草绿色到蓝色的直观变化,从而实现了直观简单地检测gsh。本发明的探针能够高灵敏性检测cys、hcy,且能够高选择性检测这三种生物体内常见氨基酸。且此探针合成方法简单,操作方便,可应用于体外对gsh、hcy、cys的分别检测。
- 还没有人留言评论。精彩留言会获得点赞!