嘧啶并1,2,4–三氮唑类化合物及其制备方法和应用与流程
本发明属于药物化学领域,具体涉及一种嘧啶并1,2,4-三氮唑类化合物及其制备方法,以及其在制备抗肿瘤药物中的应用。
背景技术:
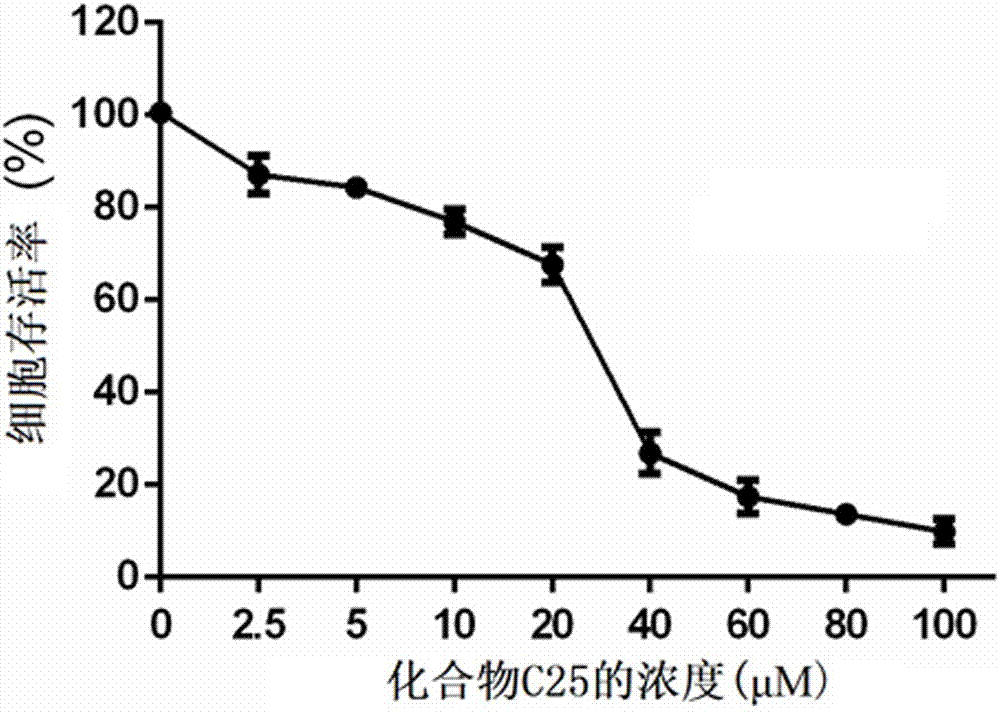
:表观遗传(epigenetics)是指基因的dna序列没有发生改变的情况下,基因表达与功能在发育和细胞增殖过程中发生了可逆的能稳定可遗传的改变,并最终导致表型的变化。表观遗传调控的分子机制包括dna甲基化修饰、组蛋白修饰、双链rna诱发的基因沉默和染色质重塑,这些机制调控着基因的表达与功能,并在多种疾病(如癌症、心血管疾病、神经紊乱、代谢失调及老龄化等)的发生发展过程中起到重要作用。肿瘤的发生发展是一个涉及多因素、多过程和多阶段的复杂过程,除遗传性改变外,异常的表观遗传调控通过改变dna甲基化水平和组蛋白修饰等影响基因的表达水平,进而影响肿瘤的发生发展。其中,表观遗传调控组蛋白赖氨酸特异性去甲基化酶1(以下简称lsd1)在较多肿瘤细胞中高表达,小分子抑制剂或rna干扰技术抑制或降低表观遗传调控蛋白lsd1的活性或表达水平可抑制癌细胞的增殖、侵袭与转移,加之表观遗传调控的可逆性,使基于lsd1的靶向药物设计成为抗肿瘤药物研发的一个重要研究方向。目前,oryzon、gsk和incyte公司分别研发的lsd1不可逆抑制剂ory-1001、gsk2879552及incb059872已进入临床试验用于急性白血病和小细胞肺癌的治疗,其中gsk-2879552和ory-1001均于2017年1月进入临床1期实验,用于治疗反复性和难治性小细胞肺癌(nct02034123)。以上信息说明lsd1是可用于癌症治疗的潜在靶点,靶向lsd1治疗癌症具有较高的可行性。设计靶向lsd1的用于肿瘤治疗的新型小分子化合物具有重大的科学意义和实际应用价值。技术实现要素:有鉴于此,本发明确有必要提供一类具有嘧啶并1,2,4-三氮唑结构单元的化合物及其制备方法和其在制备抗肿瘤药物中的应用。本发明提供一种嘧啶并1,2,4-三氮唑类化合物,结构式为:其中,所述结构式i中的基团r1代表烷基或芳基,基团r2代表氢原子或含硫取代基;基团r3代表氢原子或烷基。基于上述,所述结构式i中的基团r1代表甲基、乙基或苯基。基于上述,所述结构式i中的基团r3代表氢原子、甲基或正戊烷基。基于上述,结构式为所述结构式i的嘧啶并1,2,4-三氮唑类化合物为具有下列基团的化合物之一:c1:r1=ch3-,r3=h-;c2:r1=ch3ch2-,r2=h-,r3=h-;c3:r1=ph-,r2=h-,r3=h-;c4:r1=ch3-,r2=h-,r3=h-;c5:r1=ch3-,r3=h-;c6:r1=ch3-,r3=h-;c7:r1=ch3-,r3=h-;c8:r1=ch3-,r3=h-;c9:r1=ch3-,r3=h-;c10:r1=ch3-,r3=h-;c11:r1=ch3-,r3=h-;c12:r1=ch3-,r3=h-;c13:r1=ch3-,r3=h-;c14:r1=ch3-,r3=h-;c15:r1=ch3-,r3=h-;c16:r1=ch3-,r3=h-;c17:r1=ch3-,r3=h-;c18:r1=ch3-,r3=h-;c19:r1=ch3-,r3=h-;c20:r1=ch3-,r3=h-;c21:r1=ch3-,r3=h-;c22:r1=ch3-,r3=h-;c23:r1=ch3-,r3=h-;c24:r1=ch3-,r3=h-;c25:r1=ch3-,r3=h-;c26:r1=ch3-,r3=h-;c27:r1=ch3-,r3=ch3-;c28:r1=ch3-,r3=ch3(ch2)4-;本发明还提供一种上述所述嘧啶并1,2,4-三氮唑类化合物的制备方法,包括步骤:以乙醇为溶剂,以乙醇为溶剂,将化合物b与4-(n-甲基哌嗪)苯胺在碱性环境中,于70℃-90℃进行回流反应,制得所述嘧啶并1,2,4-三氮唑类化合物;其中,所述化合物b为化合物b1或化合物b2,且所述化合物b1的结构式为该所述合物b2的结构式为当所述嘧啶并1,2,4-三氮唑类化合物的结构式为结构式i时,其制备路线如下所示:当所述嘧啶并1,2,4-三氮唑类化合物的结构式为结构式ii时,其制备路线如下所示:基于上述,提供所述碱性环境的物质为三乙胺或碳酸钠。基于上述,所述化合物b的制备方法包括:所述化合物b的制备方法包括:化合物a与三氯氧磷于85℃-95℃进行回流反应,制得所述化合物b;其中,所述化合物a为化合物a1或化合物a2,且所述化合物a1的结构式为所述化合物a2的结构式为所述化合物b1的制备路线如下所示:所述化合物b2的制备路线如下所示:基于上述,所述化合物a1的制备方法包括:化合物q1与β-酮酸酯类化合物r1cochr3cooc2h5在115℃-125℃温度下于冰醋酸中进行反应,制得所述化合物a1;其中,所述化合物q1的结构式为其制备路线如下所示:其中,所述化合物q1的制备方法包括:以丙酮为溶剂,将2-氨基-5-巯基-1,2,4-三氮唑在碱性条件下与氯化物r4cl于55℃-65℃反应,制得所述化合物q1,其中,所述氯化物中的基团r4代表烷基,所述基团r2为r4s-。本文中“具有烷基的基团”包括烷基、具有烷基的烯烃基团、具有烷基的炔烃基团、具有烷基的环烃基团以及它们的各种取代基团。其中,该化合物的制备路线如下所示:基于上述,所述化合物a2的制备方法包括:化合物q2与β-酮酸酯类化合物c4h7(co)2och3在115℃-125℃温度下于冰醋酸中进行反应,制得所述化合物a2;其中,所述化合物q2的结构式为其制备路线如下所示:本发明还提供一种嘧啶并1,2,4-三氮唑类化合物在制备以lsd1为靶点的抗肿瘤药物中的应用。因此,本发明提供的嘧啶并1,2,4-三氮唑类化合物具有嘧啶环并1,2,4-三氮唑的结构单元,该类化合物可以用于以lsd1为靶点的抗肿瘤药物中,为寻找针对lsd1为靶点的新型抗肿瘤药物开辟新途径。另外,本发明提供的嘧啶并1,2,4-三氮唑类化合物的合成方法可行,收率高;当以2-氨基-5-巯基-1,2,4-三氮唑为原料、化合物q1或q2、a及b为中间体时,合成嘧啶并1,2,4-三氮唑类目标化合物的总收率可达48%以上。附图说明图1为本发明实施例25提供的化合物c25对肺癌细胞a549的增殖抑制曲线图。具体实施方式下面通过具体实施方式,对本发明的技术方案做进一步的详细描述。实施例1本实施例提供一种化合物c1,该化合物c1的结构式如下所示:该化合物c1的制备方法包括以下步骤:(1)制备化合物q1将1g(约8.61mmol)的2-氨基-5-巯基-1,2,4-三氮唑和1.37g(约12.92mmol)的碳酸钠分别加入到反应瓶中,然后加入约20ml丙酮,缓慢滴加1.13ml(约9.47mmol)卞氯,并在60℃下回流反应,采用薄层层析tlc监测反应。反应结束后,直接抽滤,滤液经柱层析(二氯甲烷:甲醇=20:1)得到纯品化合物q1。经测量计算:化合物q1的收率约为67%。外观:白色固体。1hnmr(400mhz,dmso-d6)δ7.41-7.18(m,5h),4.34(s,2h);13cnmr(100mhz,dmso-d6)δ152.19,147.08,136.55,128.79,128.43,127.48,35.41;hrms(esi):m/zcalcdforc9h9n4s(m-h)-,205.0548;found,205.0548;因此,可以确定所述化合物q1的结构式为(2)制备化合物a1将1g(约4.85mmol)化合物q1加入反应瓶中,再加入20ml冰醋酸,然后缓慢滴加612.57μl(约4.85mmol)乙酰乙酸乙酯并在120℃加热回流,采用tlc监测反应。反应结束后,将该反应体系投入冰水中,有大量白色固体析出,直接抽滤得白色固体。将该白色固体置于60℃烘箱中干燥6h得纯品化合物a1。经测量计算:该化合物a1的收率约为84%。该化合物a1为白色固体,熔点240℃-245℃。1hnmr(400mhz,dmso-d6)δ13.17(s,1h),7.44(d,j=7.1hz,2h),7.32(t,j=7.3hz,2h),7.26(d,j=7.2hz,1h),5.80(s,1h),4.43(s,2h),2.29(s,3h);13cnmr(100mhz,dmso-d6)δ161.92,154.75,151.09,150.63,137.35,128.77,128.38,127.22,98.46,34.48,18.43;hrms(esi):m/zcalcdforc13h11n4os(m-h)-,271.0654;found,271.0660;因此,可以确定所述化合物a1的结构式为(3)制备化合物b1将1.12g(约4.11mmol)化合物a1加入反应瓶中后,再缓慢滴加20ml三氯氧磷,并在90℃加热回流下;采用tlc监测该反应体系,待反应结束后,依次经ea萃取、无水硫酸镁干燥2h后,再经抽滤、浓缩得化合物b1。经测量计算:该化合物b1的收率约为91%。该化合物b1为浅绿色固体,且该化合物不稳定。hrms(esi):m/zcalcdforc13h12cln4s(m-h)-,291.0471;found,291.0463;因此,可以确定所述化合物b1的结构式为(4)制备化合物c1将150mg(约515.87μmol)化合物b1,和98.68mg(约515.87μmol)4-(n-甲基哌嗪)苯胺加入反应瓶中,再加入2ml乙醇后加入143.81mml(约1.03mmol)三乙胺,并于常温下反应;采用tlc监测该反应体系。待反应结束后,经柱层析处理得到纯化合物c1。该化合物c1为白色固体,且经检测计算其收率约为52%,熔点为155℃-158℃。1hnmr(400mhz,dmso-d6)δ7.49(d,j=7.3hz,2h),7.30(m,5h),7.10(d,j=8.9hz,2h),6.15(s,1h),4.55(s,2h),3.84(s,2h),3.60-3.43(m,2h),3.19(d,j=9.8hz,4h),2.81(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ164.43,163.68,155.77,147.98,145.57,138.02,128.90,128.50,128.42,127.20,126.03,116.61,88.93,51.99,45.36,41.89,34.50,24.63;hrms(esi):m/zcalcdforc24h28n7s(m+h)+,446.2126;found,446.2094;因此,可以确定所述化合物c1的结构式如上所示。实施例2本实施例提供一种化合物c2,该化合物c2的结构式如下所示:该化合物c2的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r1和r2不同,本实施例中的基团r1为烷基:ch3ch2-,基团r2为氢:h-。该化合物c2为白色固体,且经检测计算其收率约为61%,熔点为153℃-156℃;1hnmr(400mhz,dmso-d6)δ8.48(s,1h),7.27(d,j=8.7hz,2h),7.03(d,j=8.6hz,2h),6.17(s,1h),3.19(s,4h),2.66(dd,j=14.8,7.3hz,2h),2.26(s,3h),1.18(t,j=7.5hz,3h);13cnmr(100mhz,dmso-d6)δ154.34,125.88,115.85,54.43,47.80,45.56,30.97,12.98;hrms(esi):m/zcalcdforc18h24n7(m+h)+,338.2093;found,338.2059;因此,可以确定所述化合物c2的结构式如上所示。实施例3本实施例提供一种化合物c3,该化合物c3的结构式如下所示:该化合物c3的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r1和r2不同,本实施例中的基团r1为苯基:ph-,基团r2为氢:h-。该化合物c3为白色固体,且经检测计算其收率约为58%,熔点为176℃-179℃;1hnmr(400mhz,dmso-d6)δ8.59(s,1h),7.99(dd,j=6.4,2.9hz,2h),7.58-7.47(m,3h),7.43(d,j=8.8hz,2h),7.14(d,j=8.8hz,2h),6.74(s,1h),3.87(s,2h),3.47(s,2h),3.17(s,4h),2.82(s,3h);13cnmr(100mhz,dmso-d6)δ160.48,155.88,155.01,147.94,147.15,137.45,130.35,128.80,128.56,127.13,125.88,116.64,85.68,55.99,52.06,45.36,41.94,18.52;hrms(esi):m/zcalcdforc22h24n7(m+h)+,386.2093;found,386.2092;因此,可以确定所述化合物c3的结构式如上所示。实施例4本实施例提供一种化合物c4,该化合物c4的结构式如下所示:该化合物c4的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为h-。该化合物c4为白色固体,且经检测计算其收率约为48%,熔点为162℃-166℃;1hnmr(400mhz,dmso-d6)δ7.03(d,j=8.8hz,2h),6.94(d,j=8.9hz,2h),5.84(s,1h),3.16-3.06(m,5h),2.48-2.41(m,4h),2.22(d,j=3.5hz,6h);13cnmr(100mhz,dmso-d6)δ161.34,156.47,152.96,147.82,124.56,116.28,88.26,54.69,48.55,45.74,24.48;hrms(esi):m/zcalcdforc17h22n7(m+h)+,324.1936;found,324.1907;因此,可以确定所述化合物c4的结构式如上所示。实施例5本实施例提供一种化合物c5,该化合物c5的结构式如下所示:该化合物c5的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c5为白色固体,且经检测计算其收率约为43%,熔点为182℃-184℃;1hnmr(400mhz,dmso-d6)δ7.52(d,j=8.4hz,2h),7.37(d,j=8.4hz,2h),7.30(d,j=8.8hz,2h),7.10(d,j=8.9hz,2h),6.14(s,1h),4.52(s,2h),2.81(s,3h),2.35(s,3h);13cnmr(100mhz,dmso-d6)δ164.14,163.76,155.77,148.00,145.55,137.43,131.78,130.78,128.44,128.33,126.05,116.61,88.96,52.07,45.43,41.98,33.58,24.62;hrms(esi):m/zcalcdforc24h27fn7s(m+h)+,464.2032;found,464.1995;因此,可以确定所述化合物c5的结构式如上所示。实施例6本实施例提供一种化合物c6,该化合物c6的结构式如下所示:该化合物c6的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c6为白色固体,且经检测计算其收率约为58%,熔点为172℃-175℃;1hnmr(400mhz,dmso-d6)δ7.54(dd,j=8.6,5.6hz,2h),7.30(d,j=8.9hz,2h),7.19-7.06(m,4h),6.14(s,1h),4.53(s,2h),2.82(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ164.27,163.74,160.10,155.77,147.98,145.55,134.49,130.95,130.87,128.47,126.03,116.62,115.26,115.05,88.94,52.10,45.45,42.00,33.56,24.63;hrms(esi):m/zcalcdforc24h27cln7s(m+h)+,480.1737;found,480.1697;因此,可以确定所述化合物c6的结构式如上所示。实施例7本实施例提供一种化合物c7,该化合物c7的结构式如下所示:该化合物c7的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c7为白色固体,且经检测计算其收率约为62%,熔点为162℃-165℃;1hnmr(400mhz,dmso-d6)δ7.48(q,j=8.5hz,4h),7.30(d,j=8.8hz,2h),7.09(d,j=8.9hz,2h),6.14(s,1h),4.51(s,2h),3.27(s,8h),2.77(s,3h),2.35(s,3h);13cnmr(100mhz,dmso-d6)δ164.12,163.74,155.77,148.09,145.57,137.86,131.24,131.13,128.37,126.04,120.29,116.56,88.95,52.20,45.55,42.18,33.66,24.63;hrms(esi):m/zcalcdforc24h27brn7s(m+h)+,524.1232;found,524.1182;因此,可以确定所述化合物c7的结构式如上所示。实施例8本实施例提供一种化合物c8,该化合物c8的结构式如下所示:该化合物c8的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c8为白色固体,且经检测计算其收率约为41%,熔点为142℃-146℃;1hnmr(400mhz,dmso-d6)δ7.72(d,j=6.6hz,1h),7.65(d,j=7.8hz,1h),7.33(dd,j=14.9,8.0hz,3h),7.23(t,j=7.0hz,1h),7.10(d,j=8.8hz,2h),6.15(s,1h),4.62(s,2h),2.80(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ164.00,163.79,155.80,148.03,145.59,136.92,132.72,131.42,129.59,128.43,127.90,126.06,124.02,116.60,89.00,52.05,45.41,41.97,35.23,24.64;hrms(esi):m/zcalcdforc24h27brn7s(m+h)+,524.1232;found,524.1192;因此,可以确定所述化合物c8的结构式如上所示。实施例9本实施例提供一种化合物c9,该化合物c9的结构式如下所示:该化合物c9的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c9为白色固体,且经检测计算其收率约为59%,熔点为163℃-169℃;1hnmr(400mhz,dmso-d6)δ7.80(s,1h),7.57(d,j=7.7hz,1h),7.53-7.47(m,1h),7.34(d,j=7.8hz,1h),7.32-7.26(m,2h),7.07(d,j=9.0hz,2h),6.17(s,1h),4.58(s,2h),3.29-3.18(m,4h),2.54-2.49(m,4h),2.40(s,3h),2.28(s,3h);13cnmr(100mhz,dmso-d6)δ163.99,163.70,155.80,149.47,145.68,141.25,131.63,130.53,130.01,128.03,127.20,126.02,121.43,115.79,88.89,54.53,47.89,45.72,33.57,24.62;hrms(esi):m/zcalcdforc24h27brn7s(m+h)+,524.1232;found,524.1192;因此,可以确定所述化合物c9的结构式如上所示。实施例10本实施例提供一种化合物c10,该化合物c10的结构式如下所示:该化合物c10的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c10为白色固体,且经检测计算其收率约为86%,熔点为172℃-175℃;1hnmr(400mhz,dmso-d6)δ8.18(d,j=8.7hz,2h),7.79(d,j=8.7hz,2h),7.27(d,j=8.8hz,2h),7.07(d,j=8.9hz,2h),6.13(s,1h),4.65(s,2h),3.35(s,4h),2.96(s,4h),2.58(s,3h),2.35(s,3h);13cnmr(100mhz,dmso-d6)δ163.75,155.79,148.63,146.69,146.55,145.64,130.17,127.88,126.06,124.50,123.48,116.27,88.99,53.13,46.48,33.54,24.61;hrms(esi):m/zcalcdforc24h27n8o2s(m+h)+,491.1977;found,491.1933;因此,可以确定所述化合物c10的结构式如上所示。实施例11本实施例提供一种化合物c11,该化合物c11的结构式如下所示:该化合物c11的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c11为白色固体,且经检测计算其收率约为76%,熔点为167℃-175℃;1hnmr(400mhz,dmso-d6)δ8.13-8.04(m,1h),7.92(d,j=7.7hz,1h),7.71(m,1h),7.62-7.51(m,1h),7.31(d,j=8.9hz,2h),7.10(d,j=8.9hz,2h),6.15(s,1h),4.83(s,2h),3.49(s,8h),2.77(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ163.97,163.83,155.78,148.15,147.93,145.59,133.90,133.63,132.50,129.01,128.30,126.07,124.99,116.55,89.03,52.20,45.56,42.20,31.79,24.62;hrms(esi):m/zcalcdforc24h27n8o2s(m+h)+,491.1977;found,491.1929;因此,可以确定所述化合物c11的结构式如上所示。实施例12本实施例提供一种化合物c12,该化合物c12的结构式如下所示:该化合物c12的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c12为白色固体,且经检测计算其收率约为76%,熔点为161℃-165℃;1hnmr(400mhz,dmso-d6)δ7.41(d,j=8.7hz,2h),7.30(d,j=8.9hz,2h),7.10(d,j=9.0hz,2h),6.88(d,j=8.7hz,2h),6.14(s,1h),4.48(s,2h),3.72(s,4h),2.82(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ164.56,163.68,158.46,155.77,147.95,145.53,130.13,129.72,128.52,126.01,116.63,113.83,55.04,52.12,45.47,34.06,24.64;hrms(esi):m/zcalcdforc25h30n7os(m+h)+,476.2232;found,476.2190;因此,可以确定所述化合物c12的结构式如上所示。实施例13本实施例提供一种化合物c13,该化合物c13的结构式如下所示:该化合物c13的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c13为白色固体,且经检测计算其收率约为59%,熔点为158℃-167℃;1hnmr(400mhz,dmso-d6)δ7.60(dd,j=10.5,1.7hz,1h),7.53(t,j=8.1hz,1h),7.42-7.36(m,1h),7.29(d,j=8.8hz,2h),7.09(d,j=8.8hz,2h),6.14(s,1h),4.53(s,2h),3.19(s,8h),2.73(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ163.91,155.79,148.23,145.60,140.39,130.46,126.07,124.51,117.42,116.51,88.98,52.51,45.84,33.22,24.62;hrms(esi):m/zcalcdforc24h26clfn7s(m+h)+,498.1643;found,498.1597;因此,可以确定所述化合物c13的结构式如上所示。实施例14本实施例提供一种化合物c14,该化合物c14的结构式如下所示:该化合物c14的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c14为白色固体,且经检测计算其收率约为67%,熔点为172℃-175℃;1hnmr(400mhz,dmso-d6)δ7.78(dd,j=7.2,2.1hz,1h),7.58-7.48(m,1h),7.41-7.26(m,3h),7.10(d,j=8.9hz,2h),6.14(s,1h),4.52(s,2h),3.21(s,8h),2.74(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ163.97,163.78,157.55,155.80,155.10,148.22,145.59,136.55,130.98,129.69,129.62,128.26,126.08,119.12,116.86,116.66,116.51,88.96,52.39,45.74,42.46,32.99,24.63;hrms(esi):m/zcalcdforc24h26clfn7s(m+h)+,498.1643;found,498.1600;因此,可以确定所述化合物c14的结构式如上所示。实施例15本实施例提供一种化合物c15,该化合物c15的结构式如下所示:该化合物c15的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c15为白色固体,且经检测计算其收率约为66%,熔点为191℃-196℃;1hnmr(400mhz,dmso-d6)δ7.54(d,j=8.1hz,2h),7.44-7.36(m,1h),7.25(d,j=8.9hz,2h),7.02(d,j=9.0hz,2h),6.15(s,1h),5.76(s,1h),4.83(s,2h),3.20-3.12(m,4h),2.49-2.44(m,4h),2.37(s,3h),2.23(s,3h);13cnmr(100mhz,dmso-d6)δ163.80,155.81,149.41,145.74,135.09,132.23,130.45,128.79,127.23,125.92,115.78,89.00,59.72,54.87,54.52,47.88,45.69,31.49,24.66,20.72,14.05;hrms(esi):m/zcalcdforc24h26cl2n7s(m+h)+,514.1347;found,514.1304;因此,可以确定所述化合物c15的结构式如上所示。实施例16本实施例提供一种化合物c16,该化合物c16的结构式如下所示:该化合物c16的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c16为白色固体,且经检测计算其收率约为75%,熔点为188℃-192℃;1hnmr(400mhz,dmso-d6)δ7.36(d,j=8.0hz,2h),7.24(d,j=8.9hz,2h),7.12(d,j=7.9hz,2h),7.01(d,j=9.0hz,2h),6.11(s,1h),4.49(s,2h),3.21-3.11(m,4h),2.49-2.43(m,4h),2.35(s,3h),2.26(s,3h),2.23(s,3h);13cnmr(100mhz,dmso-d6)δ164.45,163.61,155.78,149.42,145.64,136.40,134.82,128.97,128.82,127.23,125.97,115.78,88.81,54.52,47.88,45.69,34.29,24.62,20.65;hrms(esi):m/zcalcdforc25h30n7s(m+h)+,460.2283;found,460.2260;因此,可以确定所述化合物c16的结构式如上所示。实施例17本实施例提供一种化合物c17,该化合物c17的结构式如下所示:该化合物c17的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c17为白色固体,且经检测计算其收率约为67%,熔点为172℃-176℃;1hnmr(400mhz,dmso-d6)δ7.71(dd,j=23.9,8.2hz,4h),7.30(d,j=8.8hz,2h),7.10(d,j=8.9hz,2h),6.14(s,1h),4.62(s,2h),2.81(s,3h),2.35(s,3h);13cnmr(100mhz,dmso-d6)δ163.98,163.78,155.79,148.03,145.59,143.41,129.69,128.43,127.87,127.56,126.06,125.24,125.20,122.86,116.60,88.99,52.05,45.40,41.96,33.72,24.61;hrms(esi):m/zcalcdforc25h27f3n7s(m+h)+,514.2000;found,514.1956;因此,可以确定所述化合物c17的结构式如上所示。实施例18本实施例提供一种化合物c18,该化合物c18的结构式如下所示:该化合物c18的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c18为白色固体,且经检测计算其收率约为58%,熔点为161℃-165℃;1hnmr(400mhz,dmso-d6)δ7.31(t,j=4.3hz,6h),7.27-7.21(m,1h),7.10(d,j=8.4hz,2h),6.13(s,1h),3.67-3.48(m,10h),3.05(t,j=7.5hz,2h),2.81(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ164.68,163.60,155.83,147.99,145.57,140.00,128.62,128.52,128.32,126.31,126.07,116.62,88.87,52.12,45.47,42.03,35.43,31.88,24.61;hrms(esi):m/zcalcdforc25h30n7s(m+h)+,460.2283;found,460.2242;因此,可以确定所述化合物c18的结构式如上所示。实施例19本实施例提供一种化合物c19,该化合物c19的结构式如下所示:该化合物c19的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c19为白色固体,且经检测计算其收率约为77%,熔点为152℃-156℃;1hnmr(400mhz,dmso-d6)δ7.24(m,7h),7.01(d,j=9.0hz,2h),6.10(s,1h),3.25(t,j=7.1hz,2h),3.20-3.11(m,4h),2.82-2.69(m,2h),2.50-2.43(m,4h),2.34(s,3h),2.23(s,3h),2.05(m,2h);13cnmr(100mhz,dmso-d6)δ164.68,163.48,155.80,149.41,145.65,141.16,128.32,128.30,127.27,126.01,125.84,115.78,88.76,54.52,47.88,45.69,33.99,31.12,30.20,24.61;hrms(esi):m/zcalcdforc26h32n7s(m+h)+,474.2439;found,474.2399;因此,可以确定所述化合物c19的结构式如上所示。实施例20本实施例提供一种化合物c20,该化合物c20的结构式如下所示:该化合物c20的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c20为白色固体,且经检测计算其收率约为73%,熔点为192℃-197℃;1hnmr(400mhz,dmso-d6)δ7.23(d,j=8.9hz,2h),7.02(d,j=9.0hz,2h),6.09(s,1h),3.27-3.20(m,2h),3.19-3.13(m,5h),2.46(d,j=4.9hz,4h),2.34(s,3h),2.23(s,3h),1.75(dd,j=14.4,7.2hz,2h),1.01(t,j=7.3hz,3h);13cnmr(100mhz,dmso-d6)δ155.80,155.22,126.03,117.13,115.78,54.54,47.90,32.51,24.61,22.84,13.07;hrms(esi):m/zcalcdforc20h28n7s(m+h)+,398.2126;found,398.2094;因此,可以确定所述化合物c20的结构式如上所示。实施例21本实施例提供一种化合物c21,该化合物c21的结构式如下所示:该化合物c21的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c21为白色固体,且经检测计算其收率约为62%,熔点为1622℃-165℃;1hnmr(400mhz,dmso-d6)δ7.24(d,j=8.9hz,2h),7.02(d,j=9.0hz,2h),6.11(s,1h),6.08-5.97(m,1h),5.36(dd,j=16.9,1.5hz,1h),5.13(d,j=10.0hz,1h),3.94(d,j=6.9hz,2h),3.23-3.11(m,4h),2.49-2.43(m,4h),2.35(s,3h),2.23(s,3h);13cnmr(100mhz,dmso-d6)δ164.15,163.60,155.82,149.44,145.67,134.00,127.23,126.00,118.02,115.77,88.79,54.54,47.90,45.72,33.25,24.62;hrms(esi):m/zcalcdforc20h26n7s(m+h)+,396.1970;found,396.1935;因此,可以确定所述化合物c21的结构式如上所示。实施例22本实施例提供一种化合物c22,该化合物c22的结构式如下所示:该化合物c22的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c22为白色固体,且经检测计算其收率约为72%,熔点为202℃-205℃;1hnmr(400mhz,dmso-d6)δ7.31(d,j=8.8hz,2h),7.10(d,j=8.9hz,2h),6.16(s,1h),4.13(d,j=2.5hz,2h),3.23(t,j=2.5hz,1h),2.81(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ163.89,163.27,155.82,147.98,145.63,128.44,125.98,116.62,89.07,80.18,73.90,52.05,45.40,41.95,24.66,19.11,18.50;hrms(esi):m/zcalcdforc20h24n7s(m+h)+,394.1813;found,394.1777;因此,可以确定所述化合物c22的结构式如上所示。实施例23本实施例提供一种化合物c23,该化合物c23的结构式如下所示:该化合物c23的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c23为白色固体,且经检测计算其收率约为38%,熔点为158℃-165℃;1hnmr(400mhz,dmso-d6)δ6.99(d,j=8.7hz,2h),6.78(d,j=8.8hz,2h),5.81(s,1h),2.90(d,j=7.2hz,4h),2.20(s,1h),2.03(s,3h),0.92(m,1h),0.33-0.19(m,2h),0.02(d,j=4.9hz,2h);13cnmr(100mhz,dmso-d6)δ165.04,163.53,155.77,147.97,145.50,128.50,126.02,116.57,88.79,51.98,45.34,41.89,36.19,24.62,11.22,5.64;hrms(esi):m/zcalcdforc21h28n7s(m+h)+,410.2126;found,410.2093;因此,可以确定所述化合物c23的结构式如上所示。实施例24本实施例提供一种化合物c24,该化合物c24的结构式如下所示:该化合物c24的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c24为白色固体,且经检测计算其收率约为68%,熔点为198℃-204℃;1hnmr(400mhz,dmso-d6)δ7.27(d,j=8.8hz,2h),7.07(d,j=8.9hz,2h),6.11(s,1h),3.18(d,j=6.8hz,3h),2.98(d,j=4.9hz,5h),2.58(s,3h),2.35(s,3h),1.85(d,j=12.2hz,2h),1.65(dd,j=29.6,10.5hz,4h),1.28-0.95(m,7h);13cnmr(100mhz,dmso-d6)δ165.14,163.48,155.72,145.55,128.65,128.27,128.01,126.04,116.26,114.37,88.77,53.14,46.38,33.14,31.81,25.81,25.43,24.61;hrms(esi):m/zcalcdforc24h34n7s(m+h)+,452.2596;found,452.2554;因此,可以确定所述化合物c24的结构式如上所示。实施例25本实施例提供一种化合物c25,该化合物c25的结构式如下所示:该化合物c25的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c25为白色固体,且经检测计算其收率约为83%,熔点为168℃-172℃;1hnmr(400mhz,dmso-d6)δ7.77(dd,j=6.0,3.1hz,2h),7.50(dd,j=6.1,3.1hz,2h),7.36(d,j=8.7hz,2h),7.13(d,j=8.8hz,2h),6.17(s,1h),5.03(s,2h),3.87(s,2h),3.51(s,2h),3.19(s,4h),2.83(s,3h),2.34(s,3h);13cnmr(100mhz,dmso-d6)δ163.80,162.68,155.85,150.89,148.12,145.69,131.74,128.16,126.26,125.37,116.58,114.07,89.18,51.98,45.33,41.87,25.57,24.43;hrms(esi):m/zcalcdforc25h28n9s(m+h)+,486.2188;found,486.2148;因此,可以确定所述化合物c25的结构式如上所示。实施例26本实施例提供一种化合物c26,该化合物c26的结构式如下所示:该化合物c26的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2不同,本实施例中的基团r2为该化合物c26为白色固体,且经检测计算其收率约为78%,熔点为168℃-172℃;1hnmr(400mhz,dmso-d6)δ8.10(d,j=1.8hz,1h),8.03(d,j=8.6hz,1h),7.95(s,1h),7.42(dd,j=8.6,1.8hz,1h),7.31(d,j=8.8hz,2h),7.10(d,j=8.9hz,2h),6.15(s,1h),4.82(s,2h),3.47(s,8h),2.81(s,3h),2.36(s,3h);13cnmr(100mhz,dmso-d6)δ164.17,163.79,155.85,148.04,145.61,139.13,138.23,131.52,129.50,128.43,126.10,124.71,124.54,121.65,116.60,88.94,52.10,45.45,42.01,27.75,24.65;hrms(esi):m/zcalcdforc26h27cln7s2(m+h)+,536.1457;found,536.1411;因此,可以确定所述化合物c26的结构式如上所示。实施例27本实施例提供一种化合物c27,该化合物c27的结构式如下所示:该化合物c27的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2和r3不同,本实施例中的基团r2为基团r3为ch3-。该化合物c27为白色固体,且经检测计算其收率约为82%,熔点为210℃-215℃;1hnmr(400mhz,dmso-d6)δ7.42(d,j=8.4hz,2h),7.33(d,j=8.4hz,2h),6.98(d,j=8.9hz,2h),6.91(d,j=9.0hz,2h),4.41(s,2h),3.16-3.08(m,4h),2.49-2.44(m,4h),2.43(s,3h),2.22(s,3h),1.80(s,3h);13cnmr(100mhz,dmso-d6)δ163.85,163.33,154.22,148.12,142.47,137.44,131.71,130.76,130.64,128.24,124.09,115.31,101.08,54.47,48.14,45.59,33.52,23.83,13.67;hrms(esi):m/zcalcdforc25h29cln7s(m+h)+,494.1893;found,494.1849;因此,可以确定所述化合物c27的结构式如上所示。实施例28本实施例提供一种化合物c28,该化合物c28的结构式如下所示:该化合物c28的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:参加反应的化合物q1、a1及b1的结构式与实施例1中的不同,尤其是化合物q1、a1及b1的结构式中的基团r2和r3不同,本实施例中的基团r2为基团r3为戊烷基ch3(ch2)4-。该化合物c28为白色固体,且经检测计算其收率约为67%,熔点为169℃-172℃;1hnmr(400mhz,dmso-d6)δ7.33(dd,j=19.6,8.4hz,4h),7.02(d,j=8.7hz,2h),6.91(d,j=8.8hz,2h),4.33(s,2h),3.10(s,4h),2.46(s,6h),2.40-2.32(m,2h),2.22(s,3h),1.33-1.19(m,3h),1.13(m,2h),1.05-0.95(m,2h),0.76(t,j=7.2hz,3h).13cnmr(100mhz,dmso-d6)δ163.38,163.10,154.24,148.73,142.86,137.48,131.67,130.75,130.22,128.19,125.53,115.26,105.88,54.87,54.33,48.16,45.49,33.40,31.10,28.03,25.64,23.34,21.80,13.90.hrms(esi):m/zcalcdforc29h37cln7s(m+h)+,550.2519;found,550.2471;因此,可以确定所述化合物c28的结构式如上所示。实施例29本实施例提供一种化合物c29,该化合物c29的结构式为所述结构式ii,具体如下所示:该化合物c29的制备方法与实施例1提供的化合物c1的制备方法基本相同,不同之处主要在于:所述步骤(1)中以所述化合物q2:3-氨基-1,2,4-三氮唑和β-酮酸酯类化合物c4h7(co)2och3为反应物,制得所述化合物a2;所述步骤(2)中以所述化合物a2和三氯氧磷为反应物,制得所述化合物b2;在所述步骤(3)中以所述化合物b2和化合物4-(n-甲基哌嗪)苯胺为反应物,制得结构式为ii所示的化合物c29。其中,该化合物的制备路线如下所示:该化合物c29为白色固体,且经检测计算其收率约为65%,熔点为137℃-142℃;1hnmr(400mhz,dmso-d6)δ7.14(d,j=8.7hz,2h),6.95(d,j=8.8hz,2h),3.22-3.08(m,4h),2.80(t,j=7.7hz,2h),2.49-2.41(m,4h),2.23(s,3h),2.14(t,j=7.2hz,2h),1.98-1.80(m,2h);13cnmr(100mhz,dmso-d6)δ173.08,155.62,153.81,149.55,146.34,142.51,127.93,127.68,114.77,102.24,55.99,54.52,47.88,45.69,34.09,30.66,28.46,22.95,18.52;hrms(esi):m/zcalcdforc19h24n7(m+h)+,350.2093;found,350.2064;因此,可以确定所述化合物c29的结构式如上所示。lsd1抑制活性测定实验方法:样品为上述实施例所合成的化合物c1至c29;样品储备液:称取1-2mg样品于1.5mlep管中,用dmso溶剂配制成浓度为20mm的溶液,4℃保存,实验过程中,再用dmso溶剂稀释至所需浓度。将待测样品和lsd1蛋白在室温孵育后,加入lsd1底物h3k4me2并孵育反应,之后加入荧光染料amplex和辣根过氧化酶hrp室温孵育,在酶标仪上设定激发光530nm,发射光590nm来检测荧光数值。实验结果采用spss软件计算被测量的抑制剂的半抑制浓度ic50值,如下表1~5所示。表1化合物c1-c6的ic50值样品c1c2c3c4c5c6ic50(μm)12.39±1.0938.13±1.11>5031.35±1.2118.51±1.1222.86±1.35表2化合物c7-c12的ic50值样品c7c8c9c10c11c12ic50(μm)23.09±1.7120.85±1.1529.24±1.0332.56±1.63>5017.38±1.27表3化合物c13-c18的ic50值样品c13c14c15c16c17c18ic50(μm)21.20±1.7225.75±1.0719.85±1.0125.78±1.6514.25±1.0528.13±1.07表4化合物c19-c24的ic50值样品c19c20c21c22c23c24ic50(μm)>5028.43±1.4530.14±1.0914.84±1.17>5024.42±1.41表5化合物c25-c29的ic50值样品c25c26c27c28c29ic50(μm)1.72±0.2316.17±1.24>50>50>50肿瘤细胞毒的测定实验方法:称取1-2mg样品化合物c25置于1.5mlep管中,然后用dmso配制成浓度是10mm的溶液,4℃保存放置,实验所需浓度利用培养基稀释。筛选:取对数生长期的细胞,消化计数后,用培养基调整细胞密度,以4000-8000个cell/孔接种至96孔板中,每孔100μl,培养24h后,弃去培养基,加入用培养基稀释好的药物,每个浓度设3个复孔,另设空白对照组及阳性对照组。药物作用72h后,每孔加入20μlmtt溶液,继续培养4h后,吸去液体,加入150μl的dmso,振荡均匀,酶标仪490nm处检测吸光度值,计算抑制率,计算公式如下:抑制率(%)=(空白组吸光度值-给药组吸光度值/空白组吸光度值)×100%。实验结果:经检测计算得知化合物c25抑制肺癌细胞a549的ic50值为23.76±0.33μm;化合物c25对肺癌细胞a549的增殖抑制曲线如图1所示。从图1中可以看出:随着化合物c25浓度的增加,肺癌细胞a549的存活率呈递减趋势,尤其是当化合物c25的浓度超过23.76±0.33μm之后,肺癌细胞a549的存活率急剧降低,因此,化合物c25对肺癌细胞表现出较好的增殖抑制活性。最后应当说明的是:以上实施例仅用以说明本发明的技术方案而非对其限制;尽管参照较佳实施例对本发明进行了详细的说明,所属领域的普通技术人员应当理解:依然可以对本发明的具体实施方式进行修改或者对部分技术特征进行等同替换;而不脱离本发明技术方案的精神,其均应涵盖在本发明请求保护的技术方案范围当中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1