基于联二苯骨架的硼氮有机发光材料及其制备方法与流程
本发明涉及发光材料领域,特别涉及一种基于联二苯骨架的硼氮有机发光材料及其制备方法。
背景技术:
迄今为止,生物化学分析、分子传感器、发光元件等领域的快速发展,对新型高效的荧光材料的开发有了迫切的需要。这类新型功能性荧光团需要有杰出的光化学稳定性,对光有高的吸收效率和量子产率,在吸收带和发射带有很高的调谐性来满足应用的需要。荧光有机分子已成为科学家在化学传感、生物成像、医学诊断、光动力疗法(pdt)、染料敏化太阳能电池(dsscs)和有机发光二极管(oled)中的光敏剂等广泛技术中不可或缺的工具。
在各种荧光分子中,硼氮类有机发光材料bodipy(硼二吡咯甲烷配合物)由于其优异的光学性质、热稳定性和化学多功能性而引起了极大的关注。虽然bodipy具有强吸收和高发射量子产率,但较小的斯托克斯位移(~20nm)是其应用的主要障碍。为了克服这个缺点,一般采取的方法是在bodipy的4号位进行大位阻基团的修饰。除此之外,寻找替代这类荧光染料、开发新的硼氮类有机发光材料也成了化学家们追捧的对象。这主要根据其b-n类螯合物结构从两方面入手:一、改变螯合基团的性质;二、改变b(iii)尾的性质(如bf2,b(ar)2,b(arf5)2,b(oar)2)。配位饱和的(通常是四面体)硼螯合物已经被研究,根据与b(iii)配位所涉及的原子,这些螯合物可分为三大类:n-o、n-n和n-c螯合物。
在实现本发明的过程中,发明人发现现有技术中至少存在以下问题:需要寻找新的b-n类螯合物作为硼氮类有机发光材料,带隙较窄、发光效率高、热稳定性好。
技术实现要素:
鉴于此,本发明提供一种新的基于联二苯骨架的硼氮类有机发光材料及其制备方法,所得硼氮类有机发光材料带隙较窄、发光效率高、热稳定性好。
具体而言,根据本发明的第一方面,本发明实施例提供了一种基于联二苯骨架的硼氮有机发光材料,结构如式(i)所示
其中,x自:6-20个碳原子的单环或多环芳族基、1-20个碳原子的单环或多环杂环基,任选地,x基团被取代基取代,所述取代基为甲基、卤素或甲氧基。
优选的,x为6-20个碳原子的单环或多环芳族基,任选地,x基团被取代基取代,所述取代基为甲基、卤素或甲氧基。
进一步优选的,x为苯基,任选地,x基团被取代基取代,所述取代基为甲基、卤素或甲氧基。
根据本发明的第二方面,本发明实施例还提供了所述硼氮有机发光材料的制备方法,合成路线如下所示:
具体步骤如下:
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应得到化合物(2),
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持5-20分钟,加入过量的三苯基硼的四氢呋喃溶液后置于40-70℃反应、过夜;静置至室温,抽滤后用冷四氢呋喃洗后柱层析即得到所述硼氮有机发光材料。所述超干四氢呋喃水含量低于50ppm,为本领域公知公用物质,有市售,市售包装内含有分子筛。所述化合物(2)与加入的三苯基硼的摩尔比优选为1:(3-6),最优选为1:6。
优选的,步骤(ⅱ)中所述三苯基硼的四氢呋喃溶液的浓度为0.05-1m,优选为0.25m。
优选的,步骤(ⅱ)中所述柱层析固定相为al2o3,流动相为二氯甲烷(简称dcm)。
本发明实施例提供的技术方案的有益效果至少包括:
本发明实施例提供了一种新的b-n类螯合物作为硼氮有机发光材料,带隙较窄、发光效率高、热稳定性好。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
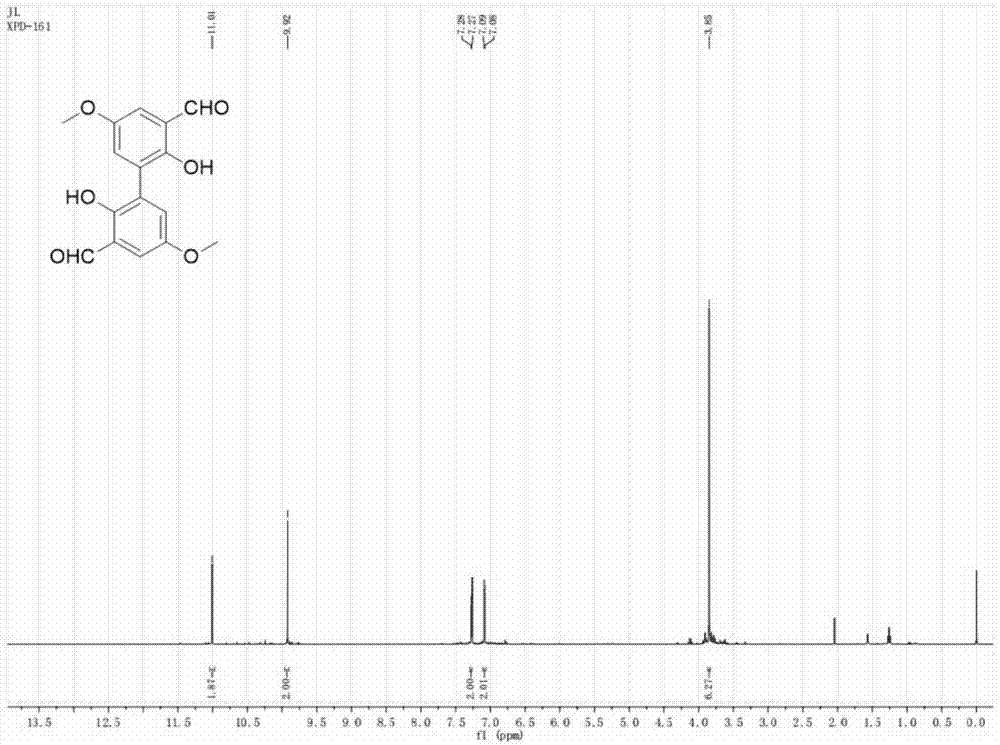
图1为实施例1中化合物(1)的1h-nmr谱图;
图2为实施例1中化合物(2)的1h-nmr谱图;
图3为实施例2中化合物(2)的1h-nmr谱图;
图4为实施例1所得硼氮类有机发光材料的1h-nmr谱图;
图5为实施例2所得硼氮类有机发光材料的1h-nmr谱图;
图6为实施例3中化合物(2)的1h-nmr谱图;
图7为实施例1所得硼氮类有机发光材料的热重分析图;
图8为实施例2所得硼氮类有机发光材料的热重分析图;
图9为实施例1所得硼氮类有机发光材料的吸收光谱图;
图10为实施例1所得硼氮类有机发光材料的荧光光谱图;
图11为实施例1所得硼氮类有机发光材料的循环伏安曲线图。
具体实施方式
为使本发明的技术方案和优点更加清楚,下面将结合附图对本发明实施方式作进一步地详细描述。
根据本发明的第一方面,本发明实施例提供了一种基于联二苯骨架的硼氮有机发光材料,结构如式(i)所示
其中,x自:6-20个碳原子的单环或多环芳族基、1-20个碳原子的单环或多环杂环基,任选地,x基团被取代基取代,所述取代基为甲基、卤素或甲氧基。
优选的,x为6-20个碳原子的单环或多环芳族基,任选地,x基团被取代基取代,所述取代基为甲基、卤素或甲氧基。
进一步优选的,x为苯基,任选地,x基团被取代基取代,所述取代基为甲基、卤素或甲氧基。
根据本发明的第二方面,本发明实施例还提供了所述硼氮有机发光材料的制备方法,合成路线如下所示:
具体步骤如下:
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应得到化合物(2),
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持5-20分钟,加入过量的三苯基硼的四氢呋喃溶液后置于40-70℃反应、过夜;静置至室温,抽滤后用冷四氢呋喃洗后柱层析即得到所述硼氮有机发光材料。所述超干四氢呋喃水含量低于50ppm,为本领域公知公用物质,有市售,市售包装内含有分子筛。所述化合物(2)与加入的三苯基硼的摩尔比优选为1:(3-6),最优选为1:6。
优选的,步骤(ⅱ)中所述三苯基硼的四氢呋喃溶液的浓度为0.05-1m,优选为0.25m。
优选的,步骤(ⅱ)中所述柱层析固定相为al2o3,流动相为dcm。
下述实施例中,所用试剂信息如下:
实验结果测试与表征方法如下:
nmr核磁测试:将0.5ml氘代溶剂加入到装有样品的核磁管中充分溶解,在室温下,用bruckerspectrometer400mhz型核磁共振分析仪进行测试。以四甲基硅烷的特征位移为内标峰。
热重分析测试:所合成的硼氮类有机发光材料是在德国耐驰tg209f3仪器上进行测定的,测试条件为程序升温,氮气保护氛围,室温-800℃;升温速率为10k/min,所测试的样品在测试前于60℃下真空干燥数小时。
紫外可见光近红外分光光度计分析测试:所合成的硼氮类有机光电材料的紫外光谱数据是在美析(中国)仪器有限公司uv-1500室温下测试,溶剂为无水氯苯,浓度约为10-4mol/l。
稳态瞬态荧光分析测试:所合成的硼氮类有机光电材料的荧光光谱数据是在edinburghinstrumentfls920上进行测定的,溶剂为无水氯苯,浓度约为10-4mol/l。
电化学测试:所合成的硼氮类有机光电材料的循环伏安曲线是在瑞士万通autolab上以50mv/s的扫速进行测定的,溶剂为无水二氯甲烷,电解质为四丁基六氟磷酸铵。
以下实施例中化合物(1)按下述步骤得到:
取2-羟基-5-甲氧基苯甲醛5g溶于50ml水中,加入4%的氢氧化钠水溶液20ml继续搅拌,十五分钟后,室温下缓慢滴加次氯酸钠约20ml,两小时后取其中析出的固体用乙酸乙酯洗涤即得到化合物(1)。
实施例1
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应,数小时后抽滤即得到化合物(2),x-nh2为对溴苯胺。图2为所得化合物2的1h-nmr谱图。
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持十分钟,按照1:6的摩尔比加入三苯基硼的四氢呋喃溶液(0.25m)后置于60℃反应,过夜。静置至室温,抽滤后用冷四氢呋喃洗后柱层析(al2o3,dcm)即得到所述硼氮有机发光材料,1h-nmr谱图如图4所示。
实施例2
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应,数小时后抽滤即得到化合物(2),x-nh2为苯胺。图3为所得化合物2的1h-nmr谱图。
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持十分钟,按照1:6的摩尔比加入三苯基硼的四氢呋喃溶液(0.25m)后置于60℃反应,过夜。静置至室温,抽滤后用冷四氢呋喃洗后柱层析(al2o3,dcm)即得到所述硼氮有机发光材料,1h-nmr谱图如图5所示。
实施例3
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应,数小时后抽滤即得到化合物(2),x-nh2为对甲氧基苯胺。图6为所得化合物2的1h-nmr谱图。
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持十分钟,按照1:6的摩尔比加入三苯基硼的四氢呋喃溶液(0.25m)后置于60℃反应,过夜。静置至室温,抽滤后用冷四氢呋喃洗后柱层析(al2o3,dcm)即得到所述硼氮有机发光材料。
实施例4
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应,数小时后抽滤即得到化合物(2),x-nh2为对溴苯胺。
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持十分钟,按照1:4的摩尔比加入三苯基硼的四氢呋喃溶液(0.5m)后置于50℃反应,过夜。静置至室温,抽滤后用冷四氢呋喃洗后柱层析(al2o3,dcm)即得到所述硼氮有机发光材料。
实施例5
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应,数小时后抽滤即得到化合物(2),x-nh2为苯胺。
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持十分钟,按照1:6的摩尔比加入三苯基硼的四氢呋喃溶液(1m)后置于60℃反应,过夜。静置至室温,抽滤后用冷四氢呋喃洗后柱层析(al2o3,dcm)即得到所述硼氮有机发光材料。
实施例6
(ⅰ)将化合物(1)2,2'-二羟基-5,5'-二甲氧基-[1,1'-联苯]-3,3'-二甲醛与x-nh2溶于乙醇中搅拌回流下反应,数小时后抽滤即得到化合物(2),x-nh2为对甲氧基苯胺。
(ⅱ)将化合物(2)溶于超干四氢呋喃中,充满氮气保持十分钟,按照1:3的摩尔比加入三苯基硼的四氢呋喃溶液(0.05m)后置于40℃反应,过夜。静置至室温,抽滤后用冷四氢呋喃洗后柱层析(al2o3,dcm)即得到所述硼氮有机发光材料。
在碳原子骨架的大π共轭体系中引入主族元素(如硼原子),是调节有机光电信息材料性质的重要手段。本发明实施例所述方法制备得到的硼氮有机红光材料带隙较窄、发光效率高(稳态瞬态荧光分析测试中测荧光光谱时测得实施例1所得硼氮类有机发光材料的量子产率约40%)、热稳定性好,同时合成方法简单易实现。图7-8表示本发明实施例所得的硼氮类有机发光材料实施例1和2在升温过程中,在320℃和390℃才出现明显的热分解,说明其热化学稳定性好;图9-10表示本发明实施例所得的硼氮类有机发光材料实施例1在氯苯中吸收波长为303nm、386nm和460nm,最佳激发波长为370nm和400nm,用420nm激发此时发射波长为632nm,斯托克斯位移较大;图11表示由循环伏安曲线计算得到起始电位eox==1.43ev,能级ehomo=-6.08ev,eg=1240/带边吸收=2.13ev,elumo=ehomo-eg=-3.95ev。
以上所述仅是为了便于本领域的技术人员理解本发明的技术方案,并不用以限制本发明。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!