正十六烷基磷酸胆碱的制备方法及其作为疫苗免疫佐剂的应用与流程
本发明属于生物医用材料领域,特别涉及一种正十六烷基磷酸胆碱的制备方法及其作为疫苗免疫佐剂的应用。
背景技术:
近几年,癌症免疫治疗作为一个新一代癌症治疗策略已经显示出巨大的潜力,并引起越来越多的关注。然而,如果单独使用肿瘤相关抗原,则不能诱导有效的免疫应答。因此,有效的肿瘤治疗需要免疫佐剂的帮助以引发强烈的抗肿瘤免疫应答。
众所周知,免疫在预防严重传染疾病方面发挥了关键性的作用。此外,随着当前和新出现的严重传染性疾病,免疫接种将继续成为最重要的疾病预防工具。采用免疫接种进行疾病治疗已经取得了很好的成绩,如对一些白血病的成功免疫治疗。在免疫过程中,抗原递送是至关重要的一步。然而,抗原不能单独免疫,因为裸抗原不能在疾病预防和治疗过程中诱导有效的免疫应答。因此,在实践中不同种的抗原总是需要免疫佐剂的协助,以诱导强烈的抗肿瘤细胞免疫。同时,佐剂能够有助于诱导强烈的免疫应答同时具有生物安全性。迄今为止,在实践中广泛使用的免疫佐剂包括弗氏佐剂和铝佐剂,并且只有后者具有良好的生物安全性才得以被批准用于临床。几十年来,铝佐剂已经被用于捍卫人类免疫的许多传染性疾病。然而,用铝佐剂免疫仍不能诱导足够强的细胞免疫来对抗病毒性感染疾病和肿瘤等严重疾病。因此,迫切需要开发新型的免疫佐剂以帮助抗原引发有效的细胞免疫。
近年来,已经进行了许多工作来开发新的免疫佐剂以辅助抗原递送。从广义上讲,这种免疫佐剂也可称为“疫苗递送系统”。针对整个抗原递送过程中的不同步骤设计和制备大量的新型疫苗递送系统。广泛采用的疫苗递送系统的设计策略包括抗原包封以防止过早降解,控制抗原释放,可持续抗原释放,靶向抗原递呈细胞(apcs),用于细胞质递送的溶酶体逃逸以促进抗原交叉递呈然后引起细胞免疫等。
技术实现要素:
本发明的首要目的在于克服现有技术的缺点与不足,提供一种正十六烷基磷酸胆碱。
本发明的另一目的在于提供所述正十六烷基磷酸胆碱的制备方法。
本发明的再一目的在于提供所述正十六烷基磷酸胆碱作为疫苗免疫佐剂的应用。
本发明的目的通过下述技术方案实现:一种正十六烷基磷酸胆碱,其结构式如式i所示:
所述的正十六烷基磷酸胆碱的制备方法,包括如下步骤:
(1)在保护性气体氛围下,将十六烷基二甲基叔胺和甲醇溶解到有机溶剂中,得到混合液ⅰ;
(2)将步骤(1)中得到的混合液ⅰ降温至-90℃~0℃,然后逐滴加入2-氯-2-氧代-1,3,2-二氧磷杂环戊烷进行反应,待反应结束后恢复至室温,放置,过滤,取沉淀,得到沉淀物ii;
(3)将步骤(2)中得到的沉淀物ii加热至25~90℃,搅拌反应,待反应结束后冷却至室温,洗涤,干燥,得到正十六烷基磷酸胆碱(c16-cp)。
步骤(1)中所述的保护性气体优选为氮气。
步骤(1)中所述的十六烷基二甲基叔胺和甲醇的摩尔比为1:10~10:1;优选为2:1。
步骤(1)中所述的有机溶剂优选为三乙胺。
步骤(1)中所述的有机溶剂的用量优选为每升有机溶剂配比0.12~3mol十六烷基二甲基叔胺计算。
步骤(2)中所述的降温为采用干冰-丙酮浴进行降温;优选为采用干冰-丙酮浴降温至-78℃。
步骤(2)中所述的2-氯-2-氧代-1,3,2-二氧磷杂环戊烷与所述十六烷基二甲基叔胺的摩尔比为1:5~5:1;优选为5:12。
步骤(2)和(3)中所述的反应优选为在保护性气体氛围下进行反应;更优选为在氮气氛围下进行反应。
步骤(2)中所述的反应的时间为1~10小时;优选为2小时。
步骤(2)中所述的恢复至室温优选为采用加热的方式恢复至室温。
步骤(2)中所述的放置的时间优选为1~10小时;优选为2小时。
步骤(3)中所述的反应的温度优选为65℃。
步骤(3)中所述的搅拌反应的时间为1~10小时(优选为搅拌过夜进行反应)。
步骤(3)中所述的洗涤为采用四氢呋喃(thf)进行洗涤;优选为用四氢呋喃(thf)洗涤3次以上。
所述的正十六烷基磷酸胆碱作为疫苗免疫佐剂的应用。
所述的正十六烷基磷酸胆碱作为免疫佐剂在制备疫苗中的应用。
所述的正十六烷基磷酸胆碱作为疫苗免疫佐剂在免疫治疗中的应用。
所述的免疫治疗包括癌症免疫治疗。
一种疫苗制剂,包括所述的正十六烷基磷酸胆碱和抗原。
所述的抗原优选为卵清蛋白。
所述的疫苗制剂中正十六烷基磷酸胆碱和抗原的质量比为5:1~1:5;优选为3:1。
所述的疫苗制剂的制备方法,包括如下步骤:将正十六烷基磷酸胆碱和抗原混合均匀后得到疫苗制剂。
所述的疫苗制剂还包括佐剂。
所述的佐剂优选为cpg寡聚脱氧核苷酸。
所述的疫苗制剂中正十六烷基磷酸胆碱,抗原与佐剂的质量比为1~20:1~20:1~20;优选为1~10:1:0.4~1;更优选为3:1:0.4。
所述的疫苗制剂的免疫接种方式优选为皮下注射。
所述的疫苗制剂的制备方法,包括如下步骤:将正十六烷基磷酸胆碱,抗原和佐剂混合均匀后得到疫苗制剂。
所述的正十六烷基磷酸胆碱在制备抗肿瘤药物中的应用。
发明相对于现有技术具有如下的优点及效果:
1、本发明提供了一种新型细胞膜粘附免疫佐剂,该新型细胞膜粘附免疫佐剂-正十六烷基磷酸胆碱通过采用磷酸胆碱基团用十六烷基链进行疏水改性,制备正十六烷基磷酸胆碱(c16-cp)作为疫苗递送系统,用于抗肿瘤免疫治疗。免疫结果表明,c16-cp纳米颗粒可以作为有效的疫苗递送系统,用于诱导有效的抗肿瘤免疫应答和抗癌症疾病。本研究提出的c16-cp递送的基于免疫的组合治疗方法可作为有效的疫苗递送系统,用于针对具有挑战性的癌症疾病进行有效的抗肿瘤免疫应答诱导。
2、本发明制备的c16-cp在中性ph环境中带正电荷。因此细胞膜粘附分子c16-cp可以通过静电吸引和疏水相互作用粘附到细胞膜上。因此,阳离子脂质正十六烷基胆碱磷酸盐可通过静电吸引和疏水相互作用与ova相互作用。
3、本发明制备的c16-cp分子可通过静电吸引吸附电负性抗原或佐剂,并通过疏水相互作用吸附抗原分子的疏水结构域,形成带正电荷的纳米制剂。然后通过皮下注射进行免疫接种,从而进一步检测其免疫应答的效果。结果显示,可以引发显着更高的抗原特异性体液和细胞免疫应答。包括显著升高的抗原特异性igg效价和细胞因子的分泌,且抑制了测试肿瘤模型中的e.g7-ova生长并延长了小鼠的存活时间。因此,正十六烷基胆碱磷酸盐纳米颗粒可以作为有效的疫苗递送系统,用于诱导有效的抗肿瘤免疫应答和抗癌症疾病。
4、本发明正十六烷基磷酸胆碱(c16-cp)结合了磷酸胆碱cp和十六烷基链反应的优点,是一种新型的生物医用高分子,具有细胞黏附性,疏水性,和生物安全性。
附图说明
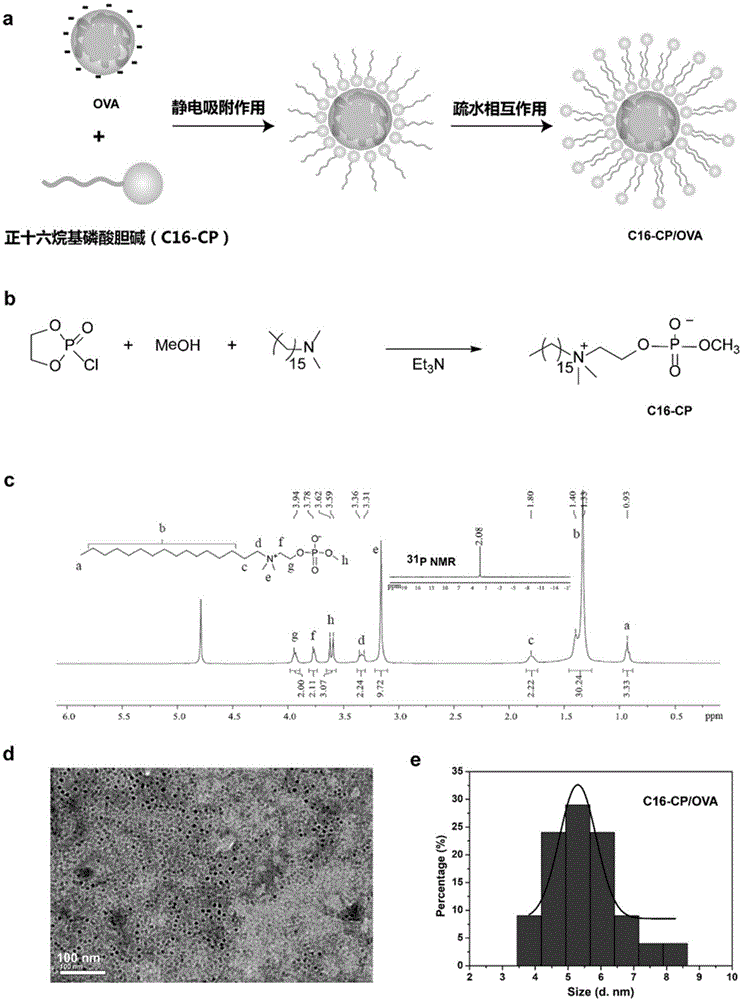
图1是由本发明中制备的c16-cp(细胞膜粘附两亲性分子)和蛋白质分子ova形成的c16-cp/ova纳米颗粒的示意图,c16-cp的合成途径及其在d2o溶剂中的1hnmr和31pnmr中的谱图,c16-cp/ova纳米颗粒的hrtem图像,以及通过imagej1.47v测量的c16-cp/ova纳米颗粒的相应直径分布直方图;其中,图a为c16-cp和蛋白质分子ova形成的c16-cp/ova纳米颗粒的示意图;图b为子c16-cp的合成途径;图c为c16-cp在d2o溶剂中的1hnmr和31pnmr中的谱图;图d为c16-cp/ova纳米颗粒的hrtem图像;图e为通过imagej1.47v测量的c16-cp/ova纳米颗粒的相应直径分布直方图。
图2是通过elisa测量的免疫小鼠血清中的ova特异性抗体分泌情况的统计图(数据表示为平均值±sem(n=5)(*p<0.05;**p<0.01;***p<0.001));其中,图a和b为指定时间点的ova特异性igg滴度(在第一次免疫后第14,21,28和35天);图c、d和e为第一次免疫后第35天小鼠血清中ova特异性igg亚型(igg1和igg2a)滴度和igg2a/igg1比例。
图3是免疫小鼠脾细胞中的细胞因子表达水平图(数据表示为平均值±sem(n=5)(*p<0.05;**p<0.01;***p<0.001));其中,图a为接种不同疫苗制剂后测定的细胞因子ifn-γ的水平;图b为接种不同疫苗制剂后测定的细胞因子tnf-α的水平;图c为接种不同疫苗制剂后测定的细胞因子il-12的水平;图d为接种不同疫苗制剂后测定的细胞因子il-6的水平。
图4是用pbs,ova,ova/cpg,c16-cp/ova和c16-cp/ova/cpg皮下免疫对携带e.g7-ova肿瘤的小鼠的抗肿瘤作用结果统计图(数据表示为平均值±sem(n=5)(*p<0.05;**p<0.01;***p<0.001));其中,图a为将e.g7-ova细胞接种到c57bl/6小鼠的右后方后,每只小鼠的肿瘤体积变化(在第7,14和21天对携带肿瘤的小鼠进行三次皮下免疫);图b为记录的每组存活曲线。
图5是c16-cp通过静电吸引和疏水相互作用粘附到细胞膜上的示意图。
具体实施方式
下面结合实施例对本发明作进一步详细的描述,但本发明的实施方式不限于此。除非特别说明,下列实施例中采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。下列实施例中未注明具体实验条件的试验方法,通常按照常规实验条件或按照制造厂所建议的实验条件。
实施例1
正十六烷基磷酸胆碱(c16-cp)的合成路线如图1(b)所示;其中,
正十六烷基磷酸胆碱(c16-cp)由以下步骤制得:
在氮气环境下,将甲醇(1.92g,0.06mol),三乙胺(100ml)和十六烷基二甲基叔胺(32.34g,0.12mol)加入到火焰干燥的250ml烧瓶中,并用干冰-丙酮浴冷却至-78℃。在2小时内向该冷混合物中滴加2-氯-2-氧代-1,3,2-二氧磷杂环戊烷(7.12g,0.05mol),继续反应2小时,然后再温热至室温2小时。在氮气环境下滤出沉淀物,将所得混合物在65℃下搅拌过夜,再将反应混合物冷却至室温,用thf(四氢呋喃)洗涤沉淀物3次。干燥后收集白色蜡状固体正十六烷基磷酸胆碱(c16-cp)。
c16-cp在d2o溶剂中的1hnmr和31pnmr中的谱图如图1c所示:1hnmr(400mhz,d2o):δ(ppm)3.94(m,2h,-ch2ch2o-),3.78(m,2h,-ch2ch2o-),3.62~3.59(d,3h,-och3),3.36~3.31(m,2h,-nch2ch2ch2-),3.14(s,6h,-n(ch3)2),1.80(br,2h,-nch2ch2ch2-),1.40-1.33(br,26h,-nch2ch2(ch2)13ch3-),0.93(t,3h,-ch2ch3);31pnmr(162mhz,d2o):δ(ppm)2.08(s)。
实施例2
正十六烷基磷酸胆碱(c16-cp)由以下步骤制得:
在氮气环境下,将甲醇(1.92g,0.06mol),三乙胺(100ml)和十六烷基二甲基叔胺(3.23g,0.012mol)加入到火焰干燥的250ml烧瓶中并用干冰-丙酮浴冷却至-78℃。在2小时内向该冷混合物中滴加2-氯-2-氧代-1,3,2-二氧磷杂环戊烷(3.56g,0.025mol),继续反应2小时,然后再温热至室温2小时。在氮气环境下滤出沉淀物,将所得混合物在65℃下搅拌过夜。后将反应混合物冷却至室温,用thf洗涤沉淀物3次。干燥后收集白色蜡状固体正十六烷基磷酸胆碱。
实施例3
正十六烷基磷酸胆碱(c16-cp)由以下步骤制得:
在氮气环境下,将甲醇(1.92g,0.06mol),三乙胺(100ml)和十六烷基二甲基叔胺(80.85g,0.3mol)加入到火焰干燥的250ml烧瓶中并用干冰-丙酮浴冷却至-78℃。在2小时内向该冷混合物中滴加2-氯-2-氧代-1,3,2-二氧磷杂环戊烷(14.25g,0.1mol),继续反应2小时,然后再温热至室温2小时。在氮气环境下滤出沉淀物,将所得混合物在65℃下搅拌过夜。后将反应混合物冷却至室温,用thf洗涤沉淀物3次。干燥后收集白色蜡状固体正十六烷基磷酸胆碱。
实施例4正十六烷基磷酸胆碱(c16-cp)作为疫苗免疫佐剂的应用:
(1)制备疫苗制剂
制备疫苗制剂ova(卵清蛋白),ova/cpg,c16-cp/ova,c16-cp/ova/cpg,脂多糖(lps)/ova纳米颗粒;其中,疫苗佐剂cpg寡聚脱氧核苷酸(简称cpg,购于广州润皓生物科技有限公司),c16-cp通过实施例1中的方法制备得到:选取磷酸盐缓冲盐水(pbs,ph7.4)作为溶剂;配置等体积的ova溶液(1mg/ml)与等体积的cpg溶液(0.4mg/ml)混合以制备ova/cpg混合物溶液;将上述ova/cpg混合物溶液加入等体积的c16-cp(3mg/ml)溶液或pbs溶液中以分别制备ova/cpg或c16-cp/ova/cpg纳米颗粒。此外,ova,c16-cp/ova和lps/ova纳米颗粒为通过将ova溶液(1mg/ml)与三倍体积的pbs,c16-cp(3mg/ml)或脂多糖(分别为lps,3mg/ml)混合得到的溶液。其中,
c16-cp(细胞膜粘附两亲性分子)和蛋白质分子ova形成的c16-cp/ova纳米颗粒的示意图如图1a所示;c16-cp/ova纳米颗粒的hrtem图像如图1d所示;通过imagej1.47v测量的c16-cp/ova纳米颗粒的相应直径分布直方图如图1e所示。
(2)小鼠免疫接种
将雌性c57bl/6小鼠(4~6周,北京维通利华实验动物技术有限公司)随机分成6组(n=5只小鼠/组)。然后在第0,14和28天通过皮下接种的方式,分别注射pbs,ova,ova/cpg,c16-cp/ova,c16-cp/ova/cpg或lps/ova制剂溶液各100μl(每组小鼠接种25μg的ova,除了单独的pbs组)。此外,在第三次免疫后7天,收集每组小鼠的脾脏和血清用于随后的免疫学分析。
(3)肿瘤治疗模型
将e.g7-ova细胞(0.5×106个细胞,上海慧颖生物科技有限公司)皮下接种到c57bl/6小鼠的右后背。然后在第7,14和21天在小鼠后腿部位通过皮下分别注射pbs,ova,ova/cpg,c16-cp/ova,c16-cp/ova/cpg或lps/ova疫苗制剂各100μl(每组小鼠接种25μg的ova,除了单独的pbs组)。在首次接种e.g7-ova细胞后监测小鼠的肿瘤大小。用以下公式计算肿瘤体积:肿瘤体积=0.5×w2×l(w:肿瘤宽度,l:肿瘤长度)。当肿瘤体积达到2000mm3时处死小鼠。
实施例5免疫应答指标的测定
(1)ova特异性抗体滴度的测定
通过酶联免疫吸附测定(elisa)测量从疫苗接种小鼠收集的血清(实施例4步骤(2))以检测ova特异性抗体的水平。简言之,将ova溶液(ova溶于0.1m碳酸盐缓冲液中,终浓度为10μg/ml),在4℃下于96孔微量培养板(costar,usa)上包被过夜。涂覆后,用pbs-tween20(pbs-t,其含有0.05%tween20)洗涤板3次以除去未涂覆的ova,然后在37℃下用2%(w/v)牛血清白蛋白(bsa)溶液封闭1小时。之后,将板用pbs-t洗涤4次,随后与血清样品(100μl/孔,用pbs-t稀释)在37℃温育2小时。孵育后,将板用pbs-t洗涤4次,然后与辣根过氧化物酶缀合的山羊抗小鼠igg,igg1或igg2a抗体(abcam,cambridge,usa)溶液(100μl/孔,用pbs-t稀释2000倍)在37℃下孵育1小时。孵育后,向每个孔中加入100μl显色液(bd,sandiego,usa)。在黑暗中温育10分钟后,向每个孔中加入100μl硫酸溶液(2m)以停止酶促反应。为了检测抗原-抗体复合物的水平,使用酶标仪(thermo,usa)读取每个孔在450nm的光学吸光度。
如图2a所示,一般趋势是在免疫后第14,21或28天,疫苗载体c16-cp或疫苗佐剂cpg的引入未引起ova特异性igg滴度的显着差异。相反,疫苗载体c16-cp或疫苗佐剂cpg的引入在免疫后第35天引起显着更高的ova特异性igg滴度。从图2b中,在免疫后的第14天至35天,每组中的igg滴度增加,并且在此期间引入疫苗载体c16-cp或疫苗佐剂cpg将引起更高程度的ova特异性igg滴度。此外,如图2c~2e所示,还测量了第一次免疫后第35天免疫小鼠血清中igg亚型igg1和igg2a的水平。与单独的ova制剂相比,c16-cp/ova制剂诱导显着更高的igg1滴度,igg2a滴度和igg2a/igg1比率。此外,c16-cp/ova/cpg制剂比ova/cpg制剂诱导显着更高的igg1滴度,igg2a滴度和igg2a/igg1比率。与c16-cp/ova制剂相比,c16-cp/ova/cpg制剂诱导显着更高的igg1滴度,igg2a滴度和igg2a/igg1比率。结果表明,引入疫苗载体c16-cp或疫苗佐剂cpg引起显着更高的ova特异性igg1滴度,igg2a滴度和th1极化。
(2)脾细胞分泌细胞因子的测定
将实施例4步骤(2)中获得的脾细胞(2.5×106个细胞/ml)接种在12孔板上,并用ova抗原溶液(25μg/ml,在rpmi1640培养基中)再刺激60小时。随后,通过离心收集上清液。通过使用相应的elisa试剂盒(biolegend,sandiego,ca,usa)测定ifn-γ,tnf-α,il-12和il-6的水平。
如图3所示,与单独的ova制剂相比,c16-cp/ova制剂诱导显着更高水平的细胞因子ifn-γ,tnf-α,il-12和il-6。此外,与ova/cpg制剂相比,c16-cp/ova/cpg制剂诱导显着更高水平的细胞因子ifn-γ,tnf-α,il-12和il-6。与c16-cp/ova制剂相比,c16-cp/ova/cpg制剂仅诱导显着更高水平的ifn-γ(但不诱导更高水平的tnf-α,il-12和il-6)。结果表明,疫苗载体c16-cp的引入可以引发显着更强的体液和细胞免疫应答,并且cpg的引入可以引发显著更强的细胞免疫应答。如上所述,通过引入疫苗载体c16-cp而改善的细胞免疫应该归因于在c16-cp存在下增加的抗原交叉呈递。
(3)抗肿瘤反应的分析
为了评估疫苗制剂的抗肿瘤功效,用不同的疫苗制剂免疫携带实体瘤的小鼠。首先,给雌性c57bl/6小鼠(4~6周)皮下注射表达ova的鼠t淋巴瘤e.g7-ova细胞(直接购买于上海慧颖生物科技有限公司)。在肿瘤细胞植入后,分别在第7,14和21天用不同的疫苗制剂(ova,ova/cpg,c16-cp/ova,c16-cp/ova/cpg,接种方式和接种量同实施例4步骤(2))免疫小鼠,并记录小鼠的肿瘤体积(4a)和存活时间(4b)。从图4a中可以看出,与pbs,ova或ova/cpg制剂相比,在第7天和第14天用c16-cp/ova或c16-cp/ova/cpg制剂接种引起明显的肿瘤生长迟缓。
综上,本发明开发了一种新颖而简单的策略来开发有效的基于纳米颗粒的亚单位疫苗。使用c16-cp纳米颗粒通过强静电相互作用吸附抗原蛋白ova和/或cpg。制备的c16-cp/ova和c16-cp/ova/cpg制剂可以引发显着更高的抗原特异性体液和细胞免疫应答。此外,利用c16-cp纳米颗粒作为疫苗递送系统抑制了肿瘤模型中的e.g7-ova生长并延长了小鼠的存活时间。这些结果表明,c16-cp纳米颗粒可以作为有效的疫苗递送系统,用于诱导有效的抗肿瘤免疫应答和抗癌症疾病。通过该项目的实施,基于c16-cp的疫苗佐剂具有快速抗原释放行为,可以交叉呈递抗原并提高免疫应答的质量和程度。
本发明正十六烷基磷酸胆碱(c16-cp)结合了磷酸胆碱cp和十六烷基链反应的优点,是一种新型的生物医用高分子,具有细胞黏附性,疏水性,和生物安全性。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!