核酸分子表达的调节的制作方法
本公开文本涉及调节靶核酸分子的表达的核酸分子、含有该核酸分子的组合物、使用了该核酸分子的调节靶核酸分子的表达的方法等。
背景技术:
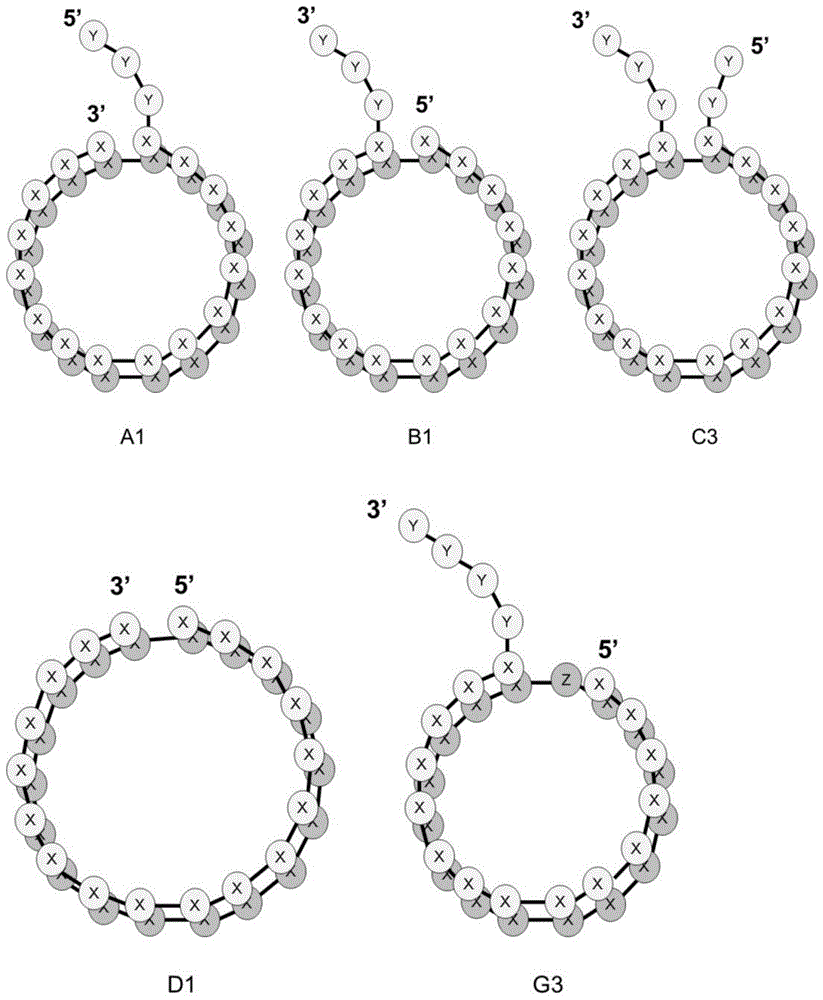
:自zamecnik及stephenson报道了寡核酸对基因表达的序列特异性抑制(反义法)以来(非专利文献1~2),已在开发使用核酸分子控制基因表达的核酸医药。核酸医药不仅包括前述反义法中使用的反义核酸,还包括rna干扰中使用的各种结构的核酸分子(非专利文献3、专利文献1~4)、以转录因子为靶标的诱饵核酸(非专利文献4)等。现有技术文献专利文献专利文献1:wo2009/029688专利文献2:wo2010/080129专利文献3:wo2011/103394专利文献4:wo2012/005368非专利文献非专利文献1:zamecnik和stephenson,procnatlacadsciusa.1978;75(1):280-4非专利文献2:stephenson和zamecnik,procnatlacadsciusa.1978;75(1):285-8非专利文献3:elbashir等,nature.2001;411(6836):494-8非专利文献4:yoshimura等,genether.2001;8(21):1635-42技术实现要素:发明所要解决的课题一直期望开发具有脱靶效应少、化学稳定性高、容易设计、制造等优点的核酸医药。用于解决课题的手段本公开文本的一些方式涉及以下内容。[1]核酸分子二聚体,其包含与靶核酸分子的至少一部分具有互补性的第一核酸分子、和与所述第一核酸分子具有互补性的第二核酸分子,所述第一核酸分子为直链状,所述第二核酸分子为环状,所述第一核酸分子与所述第二核酸分子至少局部地形成双链。[2]如[1]所述的核酸分子二聚体,其中,第一核酸分子比第二核酸分子长。[3]如[1]或[2]所述的核酸分子二聚体,其中,第一核酸分子的3’末端或5’末端形成突出。[4]如[1]~[3]中任一项所述的核酸分子二聚体,其中,第一核酸分子形成切口(nick)。[5]如[1]~[4]中任一项所述的核酸分子二聚体,其中,第一核酸分子的长度为16~30mer。[6]如[1]~[5]中任一项所述的核酸分子二聚体,其中,第二核酸分子的长度为9~30mer。[7]如[1]~[6]中任一项所述的核酸分子二聚体,其中,第一核酸分子及/或第二核酸分子进行了修饰。[8]组合物,其含有[1]~[7]中任一项所述的核酸分子二聚体。[9]医药组合物,其含有[1]~[7]中任一项所述的核酸分子二聚体、和1种或2种以上药学上可允许的添加物。[10]如[1]~[7]中任一项所述的核酸分子二聚体或者如[8]或[9]所述的组合物,其用于调节靶核酸分子的表达。[11]如[1]~[7]中任一项所述的核酸分子二聚体或者如[8]或[9]所述的组合物,其用于处置与靶核酸分子相关的疾病。[12]对与靶核酸分子相关的疾病进行处置的方法,其包括将有效量的[1]~[7]中任一项所述的核酸分子二聚体或者[8]或[9]所述的组合物施予至需要处置的对象的步骤。发明效果根据本公开文本的核酸分子具有以下的1种或2种以上效果。(1)能够调节作为靶标的核酸分子的表达。(2)因靶标非互补核酸分子导致的脱靶效应少。(3)能够避免诱导出由核酸分子导致的非序列特异性细胞应答。(4)能够避免诱导pkr的磷酸化。(5)能够避免tlr途径的激活。(6)血中的稳定性高。(7)核酸酶耐性高。(8)容易设计。(9)容易制造。附图说明[图1]图1为示意图,其示出了本公开文本的核酸分子二聚体的几种方式。位于上方的具有5’末端及3’末端的白色构建物表示tcna,位于下方的不具有5’末端及3’末端的灰色构建物表示tnna,标有x、y或z的粒子表示核苷酸,将粒子彼此连接的线表示核苷酸间的键合。[图2]图2示出了在制造本公开文本的核酸分子二聚体时设定的、tnna的连接位点的例子。[图3]图3示出了通过变性page确认tnna是否被环化的结果。泳道2及7表示5’磷酸化的直链状tnna(tn-2及tn-5),泳道1及6表示将5’磷酸化的直链状tnna用rnaser处理后的物质,泳道3及8表示将5’磷酸化的直链状tnna用t4rna连接酶1环化后的物质,泳道4及9表示将环化反应物用rnaser处理后的物质,泳道5表示分子量标记。另外,泳道1~4的tnna为16mer,泳道6~9的tnna为19mer。在泳道3及8中观察到的2根条带之中,上侧表示未环化的直链状tnna,下侧表示环化的tnna。[图4]图4示出了通过非变性page确认环状tnna(ctnna)与直链状tcna(ltcna)是否退火的结果。泳道1为对分子量标记进行退火的结果,泳道2为仅对环状tnna进行退火的结果,泳道3为仅对直链状tcna进行退火的结果,泳道4为对环状tnna与直链状tcna进行退火的结果。在泳道4中观察到的2根条带之中,上侧的条带表示环状tnna与直链状tcna退火得到的含有环状核酸分子的核酸分子二聚体(cna-nad)。[图5]图5示出了对各种核酸分子二聚体的kd效果进行评价的结果。[图6]图6示出了将含有环状tnna的核酸分子二聚体或对应的直链状核酸分子二聚体作用于细胞、通过western印迹法对细胞中的pkr磷酸化的程度进行评价的结果。p-pkr表示磷酸化pkr。[图7]图7示出了各种核酸分子所作用于的细胞中tlr3途径相关基因表达量。[图8]图8示出了各种核酸分子所作用于的细胞中tlr3途径相关蛋白质(tlr3、stat1)的磷酸化的图。[图9]图9示出了对ctnna及ltnna的核酸外切酶耐性进行评价的结果。[图10]图10示出了对各种核酸分子二聚体的kd效果进行评价的结果。纵轴表示基于内源性对照hprt归一化而得到的arhgap1的表达率。具体实施方式除非在本说明书中另有定义,本说明书中使用的所有技术用语及科学用语均具有与本领域技术人员通常理解的意思相同的含义。本说明书中提到的所有专利、申请及其他出版物(包括线上信息)的全部内容均通过引用并入本说明书中。另外,本说明书包含于2017年10月11日提出申请的、作为本申请主张优先权的基础的日本专利申请(日本特愿2017-197990号)的说明书及附图中记载的内容。本公开文本的一个方式中,涉及核酸分子二聚体(以下有时称为“本公开文本的核酸分子”、“含有环状tnna的核酸分子二聚体”等),其包含与靶核酸分子的至少一部分具有互补性的第一核酸分子(有时称为靶标互补核酸分子(target-complementarynucleicacid:tcna))、和与前述第一核酸分子具有互补性的第二核酸分子(有时称为靶标非互补核酸分子(target-non-complementarynucleicacid:tnna)),前述第一核酸分子为直链状,前述第二核酸分子为环状,前述第一核酸分子与前述第二核酸分子至少局部地形成双链(duplex)。本公开文本中,“靶核酸分子”是指作为利用本公开文本的核酸分子来调节表达的对象的核酸分子。作为靶核酸分子,例如但不限于存在于细胞内的rna及dna。靶核酸分子可以是内源性的,也可以是外源性的。作为rna,例如但不限于信使rna(mrna)、pre-mrna、微rna(mirna)、pre-mirna、piwi相互作用rna(pirna)、长链非编码rna(1ncrna)、核内非编码rna、线粒体非编码rna、反义转录物等rna转录物、病毒rna等。作为dna,可举出核dna、线粒体dna、病毒dna等。靶核酸分子可编码蛋白质等表达产物(例如,mrna、病毒rna等),也可不编码蛋白质等表达产物(例如,mirna、pirna、各种非编码rna、反义转录物等)。另外,靶核酸分子也可以是自身具有生理活性的核酸分子(例如,mirna、pirna等)。一些方式中,靶核酸分子所编码的表达产物与疾病相关。一些方式中,靶核酸分子是rna沉默的对象。作为rna沉默对象的靶核酸分子,例如但不限于存在于细胞质或核中的rna转录物、病毒rna等。另一方式中,靶核酸分子是rna激活(rnaa)的对象。作为rna激活对象的靶核酸分子,例如但不限于核dna、线粒体dna等dna、存在于dna附近的非编码rna等rna。rna沉默典型地指基于小分子rna的基因表达控制机制,包括rna干扰(rnai)、基于mirna的基因表达控制机制、基于pirna的基因表达控制机制等。rna干扰典型地指双链核酸分子所诱导的、靶rna被序列特异性地分解的现象。双链核酸分子进入细胞内后,根据其长度而被dicer切割,然后被包含argonaute(ago)蛋白的rna诱导沉默复合体(risc)摄入。risc被具有与靶rna互补的序列的反义链(向导链)引导,识别并切割靶rna。靶rna为mrna的情况下,不再表达mrna所编码的蛋白质等(基因沉默),靶rna为mirna、反义转录物的情况下,来自该mirna、反义转录物的作用消失。对于在基因表达抑制方面发挥作用的mirna、反义转录物,存在通过rna干扰使mirna、反义转录物分解而导致该基因的表达增加的情况。基于mirna的基因表达控制机制典型地指mirna所诱导的序列特异性的rna分解或翻译抑制。成熟mirna被摄入包含argonaute(ago)蛋白的mirna诱导沉默复合体(mirisc),将mirisc诱导至主要与种子序列(自5’末端起2~8位的序列)互补的mrna,抑制自mrna的翻译,同时分解并缩短存在于mrna的3’末端的多聚a尾,促进mrna的分解。基于pirna的基因表达控制机制典型地指pirna所诱导的序列特异性rna分解。pirna被摄入包含作为piwi亚家族蛋白的piwi蛋白的pirna诱导沉默复合体(pirisc)后迁移至核内,序列特异性地抑制靶基因的转录。rna激活典型地指利用将基因的启动子区域作为靶标的双链rna使该基因的表达增加的现象(li等,procnatlacadsciusa.2006;103(46):17337-42)。作为成为靶标的核酸分子,可以是dna(上述li),也可以是与启动子区域重复的转录物(例如,非编码转录物)(jiao和slack,epigenetics.2014;9(1):27-36)。迄今为止,已在e-钙粘蛋白、p21、vegf、孕酮受体(pr)、p53、nanog等多个基因中确认了rna激活(上述jiao和slack)。有时将实现rna激活的短链rna称为短链激活rna(sarna)。本公开文本中,用语“具有互补性”或“互补的”表示:某一核酸分子(第一核酸分子)与其他核酸分子(第二核酸分子)能够通过形成沃森-克里克型碱基对、形成非沃森-克里克型碱基对等方式来形成氢键。互补性可以是各种程度,互补性的程度可以由例如能与前述第二核酸分子的核酸残基形成氢键(例如,沃森-克里克碱基对)的前述第一核酸分子的连续核酸残基的百分率(percentage)(互补性百分比(percent))表示。例如,第一核酸分子及第二核酸分子由合计10个核苷酸构成并且构成第一核酸分子的10个核苷酸中的5个、6个、7个、8个、9个或10个核苷酸与具有10个核苷酸的第二核酸分子形成碱基对的情况下,互补性百分比分别为50%、60%、70%、80%、90%或100%。“具有完全的互补性”或“完全互补的”表示前述第一核酸分子的全部连续核酸残基与第二核酸分子中的相同数目的连续核酸残基以氢键键合。一个方式中,本公开文本的核酸分子二聚体中的第一核酸分子含有约15个~约30个或30个以上(例如,约15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30个或30个以上)的与1种或2种以上靶核酸分子或其一部分互补的核苷酸。本公开文本的核酸分子中的tcna是构成该核酸分子二聚体(有时也称为双链核酸分子)的核酸分子中的一方,且与靶核酸分子的至少一部分具有互补性。互补性的程度只要是tcna能在rna沉默、rna激活等中识别靶核酸分子的程度即可,并非一定需要100%的互补性。因此,tcna也可与靶核酸分子中的靶序列具有错配。错配的个数虽然也取决于tcna与靶核酸分子的靶位点的结合自由能,但可以是1个、2个、3个、4个、5个或6个以上。错配设置于tcna的任意位置均可,但从rna沉默的效率等的观点考虑,优选设置于5’末端。一些方式中,tcna与靶序列具有100%的互补性(即,错配的个数为0个)。另一方式中,tcna与靶序列具有至少约80%、至少约85%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%、至少约95%、至少约96%、至少约97%、至少约98%、或者、至少约99%等的互补性。特定的方式中,相对于靶序列而言,tcna含有1个、2个、3个、4个、5个或6个以上错配。tcna通过基于mirna的基因表达控制机制、或与其类似的基因表达控制机制来控制靶核酸分子的表达的情况下,tcna与靶核酸分子的互补性可以以mirna与其靶核酸分子的互补性作为基准。例如,就tcna而言,可以至少相当于mirna的种子区域的部分与靶核酸分子互补。即,该tcna包括仅在相当于mirna的种子区域的部分与靶核酸分子互补的方式。相当于mirna的种子区域的tcna的一部分可与靶核酸分子具有100%的互补性,也可具有数个、例如1个、2个、3个、4个或5个、优选1个错配。通过基于mirna的基因表达控制机制、或与其类似的基因表达控制机制来控制靶核酸分子的表达的tcna可具有例如包含种子区域的mirna(例如,成熟mirna)的核苷酸序列。包含该tcna的本公开文本的核酸分子的靶核酸分子可以与该mirna的靶核酸分子是同样的。一般已知mirna将多个不同的核酸分子作为靶标,因此,包含tcna的本公开文本的核酸分子也能够控制多个靶核酸分子的表达,所述tcna通过基于mirna的基因表达控制机制、或与其类似的基因表达控制机制来控制靶核酸分子的表达。就tcna的长度而言,只要本公开文本的核酸分子二聚体能够达成rna沉默、rna激活等中1种或2种以上的效果即可,没有特别限定,可以是约1~约49mer、更优选约15~约30mer。此处,“mer”表示构成tcna、tnna的单体(例如,核苷酸)的个数。一些方式中,tcna为适合摄入至risc的长度(例如,约15mer~约25mer)。另一方式中,tcna为适合作为dicer底物的长度(例如,约25~约30mer)。特定的方式中,tcna具有15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30mer的长度。tcna可具有适于诱导rna干扰的序列特征。作为该序列特征,可举出:(1)1位为a或u、(2)19位为g或c、(3)1~7位中a或u为4~7个、(4)连续的g或c小于10个、(5)gc含量为30%~52%、(6)1~5位中a或u为3个以上、(7)不存在内部重复序列、(8)1位为a、(9)17位为a、(10)10位为u、(11)7位不是g、(12)14位为a或u、(13)19位不是u、(14)1位不是g或c、(15)1位不是g、及它们的组合等。另外,对于tcna而言,出于抑制脱靶效应的目的,可对2位~8位的序列进行设计,使得在2位~8位的多核苷酸与具有互补序列的多核苷酸形成双链时、其熔解温度(tm)降低(成为例如约30℃以下、优选25℃以下、更优选约21.5℃以下)。可通过例如减少g/c碱基对的数目来使熔解温度降低。作为tcna的特定的非限定例子,可举出具有表2中记载的序列号25~31、33~35所表示的核苷酸序列的tcna。作为tcna的另一特定的非限定例子,可举出具有表12中记载的序列号38、表16中记载的序列号42~43所表示的核苷酸序列的tcna。作为tcna的其他特定的非限定例子,可举出具有包含种子区域的mirna(优选为成熟mirna)的核苷酸序列的tcna。需要说明的是,本说明书中,只要没有特别说明,则核苷酸序列上的位置以5’末端至3’末端的顺序记载。本公开文本的核酸分子二聚体中的tnna为构成该核酸分子二聚体的链中的一方,且与tcna具有互补性。互补性的程度只要是核酸分子二聚体能发挥rna沉默、rna激活等中1种或2种以上作用的程度即可,并非一定需要100%的互补性。因此,tnna也可与tcna具有错配。错配的个数虽然也取决于tnna与tcna的结合自由能,但可以是1个、2个、3个、4个、5个或6个以上。错配设置于tnna的任意位置均可。一些方式中,tnna与tcna具有100%的互补性(即,错配的个数为0个)。另一方式中,tnna与tcna具有至少约80%、至少约85%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%、至少约95%、至少约96%、至少约97%、至少约98%、或者、至少约99%等的互补性。特定的方式中,相对于tcna而言,tnna含有1个、2个、3个、4个、5个或6个以上错配。就tnna的长度而言,只要本公开文本的核酸分子二聚体能够达成rna沉默、rna激活等中1种或2种以上的效果即可,没有特别限定,可以是约2~约49mer、更优选约9~约30mer。一些方式中,tnna为适合tcna摄入至risc的长度(例如,约15~约25mer)。另一方式中,tnna为适合作为dicer底物的长度(例如,约25~约30mer)。特定的方式中,tnna具有9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30mer的长度。另外,通过使tnna的长度为16mer以下,从而即使在环状的tnna被核酸酶等切割、本公开文本的核酸分子二聚体成为直链状的情况下,仍然能够抑制因tnna导致的脱靶效应。就tnna的碱基序列而言,虽然为了与tcna形成双链而较大程度地依赖于tcna的碱基序列,但也可出于形成环状结构的目的而具有以下这样的序列特征。例如,可对tnna的碱基序列进行设计,以使得不会产生将tnna环化时能在环内导致形成双链的简单序列的重复、相同碱基的连续、回文结构等。简单序列的重复可设为例如3次以下、优选2次以下,相同碱基的连续可设为例如5个以下、优选4个以下。另外,在环内能形成碱基对的碱基数目可设为tnna的总碱基数的约80%以下、优选约75%以下、更优选约70%以下,在环内能形成g/c对的碱基数目可设为tnna的总碱基数的约40%以下、优选约35%以下、更优选约30%以下、进一步优选约25%以下。在环内能形成最长的连续碱基对的碱基数目可设为tnna的总碱基数的约60%以下、优选约55%以下、更优选约50%以下、进一步优选约45%以下。在环内能形成碱基对的碱基的数目可通过例如计数在将tnna的碱基序列于中央处折回时、相对的碱基之中彼此互补的碱基的数目等来确定。例如,将碱基数目为16的tnna的序列表示为:x01x02x03x04x05x06x07x08x09x10x11x12x13x14x15x16(式中,xn表示核苷酸,n表示核苷酸的编号)的情况下,将该序列于中央处(x08与x09之间)折回后,成为:x01x02x03x04x05x06x07x08x16x15x14x13x12x11x10x09。此处,例如,x02与x15、x04与x13、x05与x12、x06与x11这4对彼此互补的情况下,在环内能形成碱基对的碱基数目为8个,为tnna的总碱基数的50%,在环内能形成最长的连续碱基对的碱基数目为x04与x13、x05与x12、x06与x11这6个,为总碱基数的37.5%。环状tnna不具有特定的5’及3’末端,因此,在环内能形成碱基对的碱基数目等各数值的最大值可如下确定:每次将折回的位置错开1个碱基,同时针对全部可能的折回位置同样地确定能形成碱基对的碱基数目。例如,在上述的序列中将折回位置错开1个碱基后,成为:x02x03x04x05x06x07x08x09x01x16x15x14x13x12x11x10或x16x01x02x03x04x05x06x07x15x14x13x12x11x10x09x08,确定在上述状态下能形成碱基对的碱基数目。对于碱基数目为奇数的tnna而言,例如,以碱基数目为17的tnna为例时,可折回而成为:x01x02x03x04x05x06x07x08x09x17x16x15x14x13x12x11x10或x01x02x03x04x05x06x07x08x17x16x15x14x13x12x11x10x09,实施与碱基数目为偶数的情况同样的计数。作为tnna的特定的非限定例子,可举出具有表1中记载的序列号1~11所表示的核苷酸序列的tnna。作为tnna的另一特定的非限定例子,可举出具有表12中记载的序列号37、表15中记载的序列号41所表示的核苷酸序列的tnna。作为tnna的其他特定的非限定例子,可举出具有与包含种子区域的mirna(优选为成熟mirna)的核苷酸序列互补的核苷酸序列的tnna。本公开文本的核酸分子二聚体中,tcna为直链状。直链状是指:tcna具有经修饰或未经修饰的5’末端和3’末端,这些末端彼此不会经由共价键而键合。另外,本公开文本的核酸分子二聚体中,tnna为环状。环状是指:构成tnna的核苷酸等单体全部彼此键合,不具有5’末端和3’末端,并且,在成为环状后的tnna内未形成双链区。需要说明的是,虽然环状tnna实际上不具有5’末端及3’末端,但出于方便起见,有时将特定位置处单体间的键合被切断而形成了5’末端及3’末端的部位(例如,在环状tnna是将直链状tnna环化而得到的情况下,作为被环化前的直链状tnna中5’末端及3’末端的部位)称为环状tnna的5’末端及3’末端。环状tnna是将直链状tnna环化而得到的情况下,在直链状tnna中作为5’末端及3’末端的单体之间典型地经由磷酸二酯键而键合,但也可以通过其他形式键合。作为其他的键合形式,可举出例如硫代磷酸酯、3’-(或-5’)脱氧-3’-(或-5’)硫代-硫代磷酸酯、二硫代磷酸酯、硒代磷酸酯、3’-(或-5’)脱氧次膦酸酯、硼烷磷酸酯、3’-(或-5’)脱氧-3’-(或5’-)氨基磷酰胺酯、氢膦酸酯、硼烷基磷酸酯、磷酰胺酯、烷基或芳基膦酸酯、磷酸三酯、磷键、酰胺键、吗啉基、2’-5’键合等经修饰的核苷酸间的键合、二硫键、介由间隔物(spacer)的键合等。将直链状环状tnna的5’末端与3’末端介由间隔物而键合的情况下,优选设计为下述形式:将环化tnna与tcna退火时,tnna的间隔物将处于与被导入tcna的间隔物同样的位置、或处于不与tcna重复的位置。不与tcna重复的位置是下述这样的:例如,tcna不具有突出的情况下,为tcna的5’末端与3’末端之间;tcna具有5’突出的情况下,为tcna的3’末端与5’突出的基部之间;tcna具有3’突出的情况下,为tcna的5’末端与3’突出的基部之间;tcna在两端具有突出的情况下,为tcna的2个突出的基部之间;等等。作为间隔物,可举出无碱基核苷酸、聚醚(例如,聚乙二醇等)、多胺、聚酰胺、肽、甘油等。直链状tnna的两个末端的单体之间的键合的位置没有特别限定,可设定为环化后的tnna的任意的位置。需要说明的是,为了与构成环状tnna的其他单体之间的键合区分,有时将上述键合称为“末端间的键合”。末端间的键合的位置可通过例如设计直链状tnna的序列来调节。末端间的键合可与环状tnna中的其他单体间的键合相同或不同。可通过例如利用nmr、afm等的tnna的立体结构分析、利用核酸外切酶的耐性评价(与直链状核酸分子的比较)、利用电泳的条带位置分析(与直链状核酸分子的比较)、与tcna的退火的评价(若形成双链,则不会适当地退火)等来确认tnna为环状。本公开文本的核酸分子二聚体中,tcna与tnna至少局部地形成双链区(有时也称为互补键合区)。“双链区”是指互补或实质上互补的2个核酸分子的核酸残基通过形成沃森-克里克型碱基对而进行了氢键键合的区域,或者,互补或实质上互补的2个核酸分子通过能使它们之间形成双链的其他任意的方法而键合的区域。一些方式中,双链区在tcna及/或tnna的全长范围内形成。该方式中,例如,tcna和tnna的长度相同的情况下,在tcna和tnna这两者的全长范围内形成双链区,tcna比tnna长的情况下,在tnna的全长范围内形成双链区,tnna比tcna长的情况下,在tcna的全长范围内形成双链区。另一方式中,双链区形成于两个核酸分子的一部分。在双链区内不需要100%的互补性,可允许为实质上的互补性。实质上的互补性是指能在生物学条件下退火的核酸分子间的互补性。通过实验确定2个核酸分子是否能在生物学条件下退火的手段在该
技术领域:
中是公知的。或者,可以合成2个核酸分子,使其在生物学条件下反应,确定它们是否彼此退火。本公开文本的核酸分子二聚体中,双链区的长度虽然也取决于各核酸分子的长度,但可以是约1~约49mer、约1~约30mer、约15~约30mer等。特定的方式中,双链区的长度可以是9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30mer等。本公开文本的核酸分子二聚体典型地具有单一的双链区,但也可具有多个双链区。双链区中的核酸残基典型地全部通过形成沃森-克里克型碱基对而进行氢键键合,但并未氢键键合的核酸残基也可形成膨胀环、内环、分支环等。一些方式中,本公开文本的核酸分子二聚体中,tcna比tnna长,且形成切口。本公开文本的核酸分子二聚体中,tcna形成切口表示例如下述这样的情况:tcna通过形成双链而与tnna重叠、覆盖tnna,以该视角来观察时,tnna的连续2个单体之间的键合未被tcna覆盖。切口的非限定例子可举出例如图1的a1中的tcna的3’末端的核苷酸与5’突出的基部的核苷酸之间的间隙、图1的b1中的tcna的5’末端的核苷酸与3’突出的基部的核苷酸之间的间隙、图1的c3中的tcna的5’突出的基部的核苷酸与3’突出的基部的核苷酸之间的间隙、图1的d1中的tcna的5’末端的核苷酸与3’末端的核苷酸之间的间隙等。该方式中,优选的是,tcna的5’末端部分与3’末端部分不形成双链(茎)、tcna不形成膨胀环及/或分支环、tcna与tnna不形成内环、以及/或者、tcna不形成缺口(gap)。本公开文本的核酸分子二聚体中,tcna形成缺口是指:例如,tcna的2个核苷酸与tnna的位于由连续的3个以上核苷酸形成的区域的各端的核苷酸形成了碱基对时,该tcna的2个核苷酸彼此未相互键合;以及,tcna通过形成双链而与tnna重叠、覆盖tnna,以该视角来观察时,tnna的连续的3个以上单体之间的键合未被tcna覆盖。缺口的非限定例子可举出例如图1的g3中的tcna的3’突出的基部的核苷酸与5’末端的核苷酸之间的间隙等。一个方式中,tcna的5’末端部分及3’末端部分中的至少一方形成突出。突出的长度没有限定,可以是例如1~10mer、1~5mer、1~3mer等,更具体而言,可以是1、2、3、4、5、6、7、8、9、10mer等。突出可通过在tcna的5’及/或3’末端处设置与tnna错配的核苷酸等来形成。特定的方式中,tcna比tnna长的本公开文本的核酸分子二聚体包含:17mer的tcna和16mer的tnna、18mer的tcna和16mer的tnna、19mer的tcna和16mer的tnna、20mer的tcna和16mer的tnna、21mer的tcna和16mer的tnna、22mer的tcna和16mer的tnna、23mer的tcna和16mer的tnna、24mer的tcna和16mer的tnna、25mer的tcna和16mer的tnna、26mer的tcna和16mer的tnna、27mer的tcna和16mer的tnna、28mer的tcna和16mer的tnna、29mer的tcna和16mer的tnna、30mer的tcna和16mer的tnna、18mer的tcna和17mer的tnna、19mer的tcna和17mer的tnna、20mer的tcna和17mer的tnna、21mer的tcna和17mer的tnna、22mer的tcna和17mer的tnna、23mer的tcna和17mer的tnna、24mer的tcna和17mer的tnna、25mer的tcna和17mer的tnna、26mer的tcna和17mer的tnna、27mer的tcna和17mer的tnna、28mer的tcna和17mer的tnna、29mer的tcna和17mer的tnna、30mer的tcna和17mer的tnna、19mer的tcna和18mer的tnna、20mer的tcna和18mer的tnna、21mer的tcna和18mer的tnna、22mer的tcna和18mer的tnna、23mer的tcna和18mer的tnna、24mer的tcna和18mer的tnna、25mer的tcna和18mer的tnna、26mer的tcna和18mer的tnna、27mer的tcna和18mer的tnna、28mer的tcna和18mer的tnna、29mer的tcna和18mer的tnna、30mer的tcna和18mer的tnna、20mer的tcna和19mer的tnna、21mer的tcna和19mer的tnna、22mer的tcna和19mer的tnna、23mer的tcna和19mer的tnna、24mer的tcna和19mer的tnna、25mer的tcna和19mer的tnna、26mer的tcna和19mer的tnna、27mer的tcna和19mer的tnna、28mer的tcna和19mer的tnna、29mer的tcna和19mer的tnna、30mer的tcna和19mer的tnna、21mer的tcna和20mer的tnna、22mer的tcna和20mer的tnna、23mer的tcna和20mer的tnna、24mer的tcna和20mer的tnna、25mer的tcna和20mer的tnna、26mer的tcna和20mer的tnna、27mer的tcna和20mer的tnna、28mer的tcna和20mer的tnna、29mer的tcna和20mer的tnna、30mer的tcna和20mer的tnna、22mer的tcna和21mer的tnna、23mer的tcna和21mer的tnna、24mer的tcna和21mer的tnna、25mer的tcna和21mer的tnna、26mer的tcna和21mer的tnna、27mer的tcna和21mer的tnna、28mer的tcna和21mer的tnna、29mer的tcna和21mer的tnna、30mer的tcna和21mer的tnna、23mer的tcna和22mer的tnna、24mer的tcna和22mer的tnna、25mer的tcna和22mer的tnna、26mer的tcna和22mer的tnna、27mer的tcna和22mer的tnna、28mer的tcna和22mer的tnna、29mer的tcna和22mer的tnna、30mer的tcna和22mer的tnna、24mer的tcna和23mer的tnna、25mer的tcna和23mer的tnna、26mer的tcna和23mer的tnna、27mer的tcna和23mer的tnna、28mer的tcna和23mer的tnna、29mer的tcna和23mer的tnna、30mer的tcna和23mer的tnna、25mer的tcna和24mer的tnna、26mer的tcna和24mer的tnna、27mer的tcna和24mer的tnna、28mer的tcna和24mer的tnna、29mer的tcna和24mer的tnna、30mer的tcna和24mer的tnna、26mer的tcna和25mer的tnna、27mer的tcna和25mer的tnna、28mer的tcna和25mer的tnna、29mer的tcna和25mer的tnna、30mer的tcna和25mer的tnna、27mer的tcna和26mer的tnna、28mer的tcna和26mer的tnna、29mer的tcna和26mer的tnna、30mer的tcna和26mer的tnna、28mer的tcna和27mer的tnna、29mer的tcna和27mer的tnna、30mer的tcna和27mer的tnna、29mer的tcna和28mer的tnna、30mer的tcna和28mer的tnna、或者、30mer的tcna和29mer的tnna。本公开文本的核酸分子二聚体的、tcna比tnna长、且tcna的5’末端部分或3’末端部分中的任一者形成突出的方式中的tcna与tnna的关系在下文中由结构式表示。式中,y表示形成突出部的核苷酸(包括非修饰核苷酸及修饰核苷酸。以下相同),x表示形成双链区的核苷酸,数字表示核苷酸的数目。另外,m为1~10,优选为1~5,n为5~39,优选为14~29,o为1~10,优选为1~5,n’为5~38,优选为14~28,其中,m+n、n+o及m+n’+o各自独立地为15~49,优选为15~30。需要说明的是,环化tnna出于方便起见而以是否具有5’末端及3’末端的方式记载,但实际上,如上所述,5’末端与3’末端经由共价键而键合,不存在末端。这也适用于以下的同样的结构式中。(a)5’突出型5’ymxn3’(直链状tcna)3’xn5’(环状tnna)(b)3’突出型5’xnyo3’(直链状tcna)3’xn5’(环状tnna)(c)5’及3’突出型5’ymxn’yo3’(直链状tcna)3’xn’5’(环状tnna)本公开文本的核酸分子二聚体的一部分优选方式中的tcna与tnna的关系如下所示。需要说明的是,y表示形成突出部的核苷酸,x表示形成双链区的核苷酸,上段表示直链状tcna,下段表示环状tnna。另外,图1中示出a1、b1、c3的示意图。(a1)5’突出型,tcna为19mer,tnna为16mer5’yyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a2)5’突出型,tcna为20mer,tnna为16mer5’yyyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a3)5’突出型,tcna为21mer,tnna为16mer5’yyyyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a4)5’突出型,tcna为22mer,tnna为16mer5’yyyyyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a5)5’突出型,tcna为23mer,tnna为16mer5’yyyyyyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a6)5’突出型,tcna为24mer,tnna为16mer5’yyyyyyyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a7)5’突出型,tcna为25mer,tnna为16mer5’yyyyyyyyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxx5’(a8)5’突出型,tcna为20mer,tnna为19mer5’yxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(a9)5’突出型,tcna为21mer,tnna为19mer5’yyxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(a10)5’突出型,tcna为22mer,tnna为19mer5’yyyxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(a11)5’突出型,tcna为23mer,tnna为19mer5’yyyyxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(a12)5’突出型,tcna为24mer,tnna为19mer5’yyyyyxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(a13)5’突出型,tcna为25mer,tnna为19mer5’yyyyyyxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(b1)3’突出型,tcna为19mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxx5’(b2)3’突出型,tcna为20mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyyy3’3’xxxxxxxxxxxxxxxx5’(b3)3’突出型,tcna为21mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyyyy3’3’xxxxxxxxxxxxxxxx5’(b4)3’突出型,tcna为22mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyyyyy3’3’xxxxxxxxxxxxxxxx5’(b5)3’突出型,tcna为23mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyyyyyy3’3’xxxxxxxxxxxxxxxx5’(b6)3’突出型,tcna为24mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyyyyyyy3’3’xxxxxxxxxxxxxxxx5’(b7)3’突出型,tcna为25mer,tnna为16mer5’xxxxxxxxxxxxxxxxyyyyyyyyy3’3’xxxxxxxxxxxxxxxx5’(b8)3’突出型,tcna为20mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxxy3’3’xxxxxxxxxxxxxxxxxxx5’(b9)3’突出型,tcna为21mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxxxx5’(b10)3’突出型,tcna为22mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxxxx5’(b11)3’突出型,tcna为23mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxxyyyy3’3’xxxxxxxxxxxxxxxxxxx5’(b12)3’突出型,tcna为24mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxxyyyyy3’3’xxxxxxxxxxxxxxxxxxx5’(b13)3’突出型,tcna为25mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxxyyyyyy3’3’xxxxxxxxxxxxxxxxxxx5’(c1)5’及3’突出型,tcna为19mer,tnna为16mer5’yxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxx5’(c2)5’及3’突出型,tcna为20mer,tnna为16mer5’yyxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxx5’(c3)5’及3’突出型,tcna为21mer,tnna为16mer5’yyxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxx5’(c4)5’及3’突出型,tcna为22mer,tnna为16mer5’yyyxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxx5’(c5)5’及3’突出型,tcna为23mer,tnna为16mer5’yyyxxxxxxxxxxxxxxxxyyyy3’3’xxxxxxxxxxxxxxxx5’(c6)5’及3’突出型,tcna为24mer,tnna为16mer5’yyyyxxxxxxxxxxxxxxxxyyyy3’3’xxxxxxxxxxxxxxxx5’(c7)5’及3’突出型,tcna为25mer,tnna为16mer5’yyyyxxxxxxxxxxxxxxxxyyyyy3’3’xxxxxxxxxxxxxxxx5’(c8)5’及3’突出型,tcna为21mer,tnna为19mer5’yxxxxxxxxxxxxxxxxxxxy3’3’xxxxxxxxxxxxxxxxxxx5’(c9)5’及3’突出型,tcna为22mer,tnna为19mer5’yxxxxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxxxx5’(c10)5’及3’突出型,tcna为23mer,tnna为19mer5’yyxxxxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxxxx5’(c11)5’及3’突出型,tcna为24mer,tnna为19mer5’yyxxxxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxxxx5’(c12)5’及3’突出型,tcna为25mer,tnna为19mer5’yyyxxxxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxxxx5’虽然不希望受限于特定的理论,但可以认为,对于如上述那样tcna比tnna长的方式而言,即使在tnna被核酸酶等切割、核酸分子二聚体成为直链状的情况下,tcna向risc中的摄入也比tnna更占优势,可避免因tnna导致的脱靶效应。一些方式中,本公开文本的核酸分子二聚体中的tcna的长度与tnna相同,且tcna形成切口。因此,该方式中,tcna不形成突出、缺口、膨胀环及分支环中的任一种,tcna自身也不形成双链。优选tcna与tnna不形成内环。特定的方式中,tcna和tnna的长度相同的本公开文本的核酸分子二聚体包含:17mer的tcna和17mer的tnna、18mer的tcna和18mer的tnna、19mer的tcna和19mer的tnna、20mer的tcna和20mer的tnna、21mer的tcna和21mer的tnna、22mer的tcna和22mer的tnna、23mer的tcna和23mer的tnna、24mer的tcna和24mer的tnna、25mer的tcna和25mer的tnna、26mer的tcna和26mer的tnna、27mer的tcna和27mer的tnna、28mer的tcna和28mer的tnna、29mer的tcna和29mer的tnna、或者、30mer的tcna和30mer的tnna。tcna和tnna的长度相同、且形成切口的本公开文本的核酸分子二聚体的一部分优选方式中的tcna与tnna的关系如下所示。x表示形成双链区的核苷酸,上段表示直链状tcna,下段表示环状tnna。另外,图1示出d1的示意图。(d1)tcna为18mer,tnna为18mer5’xxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxx5’(d2)tcna为19mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxx5’(d3)tcna为20mer,tnna为20mer5’xxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxx5’(d4)tcna为21mer,tnna为21mer5’xxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxx5’(d5)tcna为22mer,tnna为22mer5’xxxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxxx5’(d6)tcna为23mer,tnna为23mer5’xxxxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxxxx5’(d7)tcna为24mer,tnna为24mer5’xxxxxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxxxxx5’(d8)tcna为25mer,tnna为25mer5’xxxxxxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxxxxxx5’一些方式中,本公开文本的核酸分子二聚体中的tcna形成缺口。缺口的长度没有限定,可以是例如1~10mer、1~5mer、1~3mer等,更具体而言,可以是1、2、3、4、5、6、7、8、9、10mer等。tcna的长度可以比tnna长,可以比tnna短,或者也可以与tnna相同。tcna的5’末端部分或3’末端部分中的任一者可形成突出。突出的长度没有限定,可以是例如1~10mer、1~5mer、1~3mer等,更具体而言,可以是1、2、3、4、5、6、7、8、9、10mer等。tcna的长度比tnna长、或与tnna相同的情况下,tcna的5’末端部分及/或3’末端部分通常形成突出。该方式中,优选tcna的5’末端部分与3’末端部分不形成双链,以及,tcna不形成膨胀环及/或分支环、tcna与tnna不形成内环。特定的方式中,tcna比tnna短的本公开文本的核酸分子二聚体包含:17mer的tnna和16mer的tcna、18mer的tnna和16mer的tcna、19mer的tnna和16mer的tcna、20mer的tnna和16mer的tcna、21mer的tnna和16mer的tcna、22mer的tnna和16mer的tcna、23mer的tnna和16mer的tcna、24mer的tnna和16mer的tcna、25mer的tnna和16mer的tcna、26mer的tnna和16mer的tcna、27mer的tnna和16mer的tcna、28mer的tnna和16mer的tcna、29mer的tnna和16mer的tcna、30mer的tnna和16mer的tcna、18mer的tnna和17mer的tcna、19mer的tnna和17mer的tcna、20mer的tnna和17mer的tcna、21mer的tnna和17mer的tcna、22mer的tnna和17mer的tcna、23mer的tnna和17mer的tcna、24mer的tnna和17mer的tcna、25mer的tnna和17mer的tcna、26mer的tnna和17mer的tcna、27mer的tnna和17mer的tcna、28mer的tnna和17mer的tcna、29mer的tnna和17mer的tcna、30mer的tnna和17mer的tcna、19mer的tnna和18mer的tcna、20mer的tnna和18mer的tcna、21mer的tnna和18mer的tcna、22mer的tnna和18mer的tcna、23mer的tnna和18mer的tcna、24mer的tnna和18mer的tcna、25mer的tnna和18mer的tcna、26mer的tnna和18mer的tcna、27mer的tnna和18mer的tcna、28mer的tnna和18mer的tcna、29mer的tnna和18mer的tcna、30mer的tnna和18mer的tcna、20mer的tnna和19mer的tcna、21mer的tnna和19mer的tcna、22mer的tnna和19mer的tcna、23mer的tnna和19mer的tcna、24mer的tnna和19mer的tcna、25mer的tnna和19mer的tcna、26mer的tnna和19mer的tcna、27mer的tnna和19mer的tcna、28mer的tnna和19mer的tcna、29mer的tnna和19mer的tcna、30mer的tnna和19mer的tcna、21mer的tnna和20mer的tcna、22mer的tnna和20mer的tcna、23mer的tnna和20mer的tcna、24mer的tnna和20mer的tcna、25mer的tnna和20mer的tcna、26mer的tnna和20mer的tcna、27mer的tnna和20mer的tcna、28mer的tnna和20mer的tcna、29mer的tnna和20mer的tcna、30mer的tnna和20mer的tcna、22mer的tnna和21mer的tcna、23mer的tnna和21mer的tcna、24mer的tnna和21mer的tcna、25mer的tnna和21mer的tcna、26mer的tnna和21mer的tcna、27mer的tnna和21mer的tcna、28mer的tnna和21mer的tcna、29mer的tnna和21mer的tcna、30mer的tnna和21mer的tcna、23mer的tnna和22mer的tcna、24mer的tnna和22mer的tcna、25mer的tnna和22mer的tcna、26mer的tnna和22mer的tcna、27mer的tnna和22mer的tcna、28mer的tnna和22mer的tcna、29mer的tnna和22mer的tcna、30mer的tnna和22mer的tcna、24mer的tnna和23mer的tcna、25mer的tnna和23mer的tcna、26mer的tnna和23mer的tcna、27mer的tnna和23mer的tcna、28mer的tnna和23mer的tcna、29mer的tnna和23mer的tcna、30mer的tnna和23mer的tcna、25mer的tnna和24mer的tcna、26mer的tnna和24mer的tcna、27mer的tnna和24mer的tcna、28mer的tnna和24mer的tcna、29mer的tnna和24mer的tcna、30mer的tnna和24mer的tcna、26mer的tnna和25mer的tcna、27mer的tnna和25mer的tcna、28mer的tnna和25mer的tcna、29mer的tnna和25mer的tcna、30mer的tnna和25mer的tcna、27mer的tnna和26mer的tcna、28mer的tnna和26mer的tcna、29mer的tnna和26mer的tcna、30mer的tnna和26mer的tcna、28mer的tnna和27mer的tcna、29mer的tnna和27mer的tcna、30mer的tnna和27mer的tcna、29mer的tnna和28mer的tcna、30mer的tnna和28mer的tcna、或者、30mer的tnna和29mer的tcna。关于tcna比tnna长的本公开文本的核酸分子二聚体及tcna和tnna的长度相同的本公开文本的核酸分子二聚体的特定的方式,如上文中所记载的那样。本公开文本的核酸分子二聚体的、tcna形成缺口的方式中的tcna与tnna的关系在下文中由结构式表示。式中,y表示形成突出部的核苷酸,x表示形成双链区的核苷酸,z表示由于tcna形成缺口而未与tcna的核苷酸形成碱基对的tnna的核苷酸,数字表示核苷酸的数目。另外,m为1~10,优选为1~5,n为5~39,优选为14~29,o为1~10,优选为1~5,n’为5~38,优选为14~28,p为1~10,优选为1~5,q为1~11,优选为1~6,其中,m+n、n+o、m+n’+o、n+p及n’+q各自独立地为15~49,优选为15~30。需要说明的是,虽然zp及zq出于方便起见而记载于tnna的5’侧,但如上文所述,在实际的环状tnna中既不存在5’末端也不存在3’末端,因此也可视作zp及zq位于3’末端。(e)缺口·非突出型5’xn3’(直链状tcna)3’xnzp5’(环状tnna)(f)缺口·5’突出型5’ymxn3’(直链状tcna)3’xnzp5’(环状tnna)(g)缺口·3’突出型5’xnyo3’(直链状tcna)3’xnzp5’(环状tnna)(h)缺口·5’及3’突出型5’ymxn,yo3’(直链状tcna)3’xn,zq5’(环状tnna)本公开文本的核酸分子二聚体的一部分优选方式中的tcna与tnna的关系如下所示。需要说明的是,y表示形成突出部的核苷酸,x表示形成双链区的核苷酸,z表示由于tcna形成缺口而未与tcna的核苷酸形成碱基对的tnna的核苷酸,上段表示直链状tcna,下段表示环状tnna。另外,图1示出g3的示意图。(e1)缺口·非突出型,tcna为19mer,tnna为21mer5’xxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxzz5’(e2)缺口·非突出型,tcna为19mer,tnna为23mer5’xxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxzzzz5’(e3)缺口·非突出型,tcna为19mer,tnna为25mer5’xxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxzzzzzz5’(e4)缺口·非突出型,tcna为21mer,tnna为23mer5’xxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxxzz5’(e5)缺口·非突出型,tcna为21mer,tnna为25mer5’xxxxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxxxxzzzz5’(f1)缺口·5’突出型,tcna为19mer,tnna为19mer5’yyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxzzz5’(f2)缺口·5’突出型,tcna为19mer,tnna为18mer5’yyyxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxzz5’(f3)缺口·5’突出型,tcna为19mer,tnna为16mer5’yyyyxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxz5’(f4)缺口·5’突出型,tcna为21mer,tnna为21mer5’yyyxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxzzz5’(f5)缺口·5’突出型,tcna为21mer,tnna为19mer5’yyyxxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxxz5’(f6)缺口·5’突出型,tcna为21mer,tnna为18mer5’yyyyxxxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxxxz5’(f7)缺口·5’突出型,tcna为21mer,tnna为16mer5’yyyyyyxxxxxxxxxxxxxxx3’3’xxxxxxxxxxxxxxxz5’(g1)缺口·3’突出型,tcna为19mer,tnna为19mer5’xxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxzzz5’(g2)缺口·3’突出型,tcna为19mer,tnna为18mer5’xxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxzz5’(g3)缺口·3’突出型,tcna为19mer,tnna为16mer5’xxxxxxxxxxxxxxxyyyy3’3’xxxxxxxxxxxxxxxz5’(g4)缺口·3’突出型,tcna为21mer,tnna为21mer5’xxxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxxxzzz5’(g5)缺口·3’突出型,tcna为21mer,tnna为19mer5’xxxxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxxxxz5’(g6)缺口·3’突出型,tcna为21mer,tnna为18mer5’xxxxxxxxxxxxxxxxxyyyy3’3’xxxxxxxxxxxxxxxxxz5’(g7)缺口·3’突出型,tcna为21mer,tnna为16mer5’xxxxxxxxxxxxxxxyyyyyy3’3’xxxxxxxxxxxxxxxz5’(h1)缺口·5’及3’突出型,tcna为19mer,tnna为19mer5’yxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxzzz5’(h2)缺口·5’及3’突出型,tcna为19mer,tnna为18mer5’yyxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxzzz5’(h3)缺口·5’及3’突出型,tcna为19mer,tnna为16mer5’yyxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxzz5’(h4)缺口·5’及3’突出型,tcna为21mer,tnna为21mer5’yxxxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxxxzzz5’(h5)缺口·5’及3’突出型,tcna为21mer,tnna为19mer5’yyxxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxxzz5’(h6)缺口·5’及3’突出型,tcna为21mer,tnna为18mer5’yyxxxxxxxxxxxxxxxxxyy3’3’xxxxxxxxxxxxxxxxxz5’(h7)缺口·5’及3’突出型,tcna为21mer,tnna为16mer5’yyyxxxxxxxxxxxxxxxyyy3’3’xxxxxxxxxxxxxxxz5’本公开文本的核酸分子二聚体的tcna及tnna可含有非修饰核苷酸及/或修饰核苷酸。本说明书中,有时将非修饰核苷酸及修饰核苷酸统一简称为“核苷酸”。非修饰核苷酸是指天然存在的构成dna、rna的核苷酸,即,由核酸碱基(腺嘌呤、鸟嘌呤、尿嘧啶、胸腺嘧啶、胞嘧啶)、糖(核糖、脱氧核糖)、和磷酸基构成的核苷酸。由非修饰核苷酸构成的非修饰核酸分子中,相邻的两个非修饰核苷酸之间通常经由磷酸二酯键而将一个非修饰核苷酸的3’位与另一个非修饰核苷酸的5’位连接。非修饰核苷酸可以是非修饰核糖核苷酸,也可以是非修饰脱氧核糖核苷酸,非修饰核酸分子可仅由非修饰核糖核苷酸构成,可仅由非修饰脱氧核糖核苷酸构成,或者也可由非修饰核糖核苷酸及非修饰脱氧核糖核苷酸这两者构成。修饰核苷酸是指含有对非修饰核苷酸的化学修饰的核苷酸。修饰核苷酸可以是人工合成的,也可以是天然存在的。修饰核苷酸包括对其核酸碱基、糖、骨架(核苷酸间的键合)、5’末端及/或3’末端进行修饰而得到的核苷酸。修饰核苷酸不仅包括对上述部位中的任一者进行修饰而得到的核苷酸,还包括对上述部位中的2处以上进行修饰而得到的核苷酸。作为针对核酸碱基的修饰,例如但不限于2,4-二氟甲苯甲酰基、2,6-二氨基、5-溴、5-碘、2-硫、二氢、5-丙炔基、及5-甲基修饰、脱碱基等。另外,作为修饰核酸碱基,例如但不限于黄嘌呤、次黄嘌呤、肌苷、2-氨基腺嘌呤、腺嘌呤及鸟嘌呤的6-甲基衍生物及其他烷基衍生物、通用碱基、腺嘌呤及鸟嘌呤的2-丙基衍生物及其他烷基衍生物、5-卤代尿嘧啶及5-卤代胞嘧啶、5-丙炔基尿嘧啶及5-丙炔基胞嘧啶、6-偶氮尿嘧啶、6-偶氮胞嘧啶及6-偶氮胸腺嘧啶、5-尿嘧啶(假尿嘧啶)、4-硫代尿嘧啶、8-卤代、氨基、硫醇、硫代烷基、羟基及其他的8-取代腺嘌呤及鸟嘌呤、5-三氟甲基及其他的5-取代尿嘧啶及5-取代胞嘧啶、7-甲基鸟嘌呤、无环核苷酸、去氮嘌呤、嘌呤及嘧啶的杂环取代类似物、例如氨基乙氧基吩噁嗪、嘌呤及嘧啶的衍生物(例如1-烷基衍生物、1-链烯基衍生物、杂芳环衍生物及1-炔基衍生物)及其互变异构体、8-氧代-n6-甲基腺嘌呤、7-二氮杂黄嘌呤、5-甲基胞嘧啶、5-甲基尿嘧啶、5-(1-丙炔基)尿嘧啶、5-(1-丙炔基)胞嘧啶、4,4-乙醇胞嘧啶、非嘌呤碱基及非嘧啶碱基、例如2-氨基吡啶及三嗪、无碱基核苷酸、脱氧无碱基核苷酸、倒位无碱基核苷酸、倒位脱氧无碱基核苷酸等。作为针对糖的修饰,例如但不限于:2’位的修饰,例如2’-o-烷基修饰(例如,2’-o-甲基修饰、2’-o-乙基修饰等)、2’-甲氧基乙氧基修饰、2’-甲氧基乙基修饰、2’-脱氧修饰、2’-卤代修饰(2’-氟修饰、2’-氯修饰、2’-溴修饰等)、2’-o-烯丙基修饰、2’-氨基修饰、2’-s-烷基修饰、2’-o-[2(甲基氨基)-2-氧代乙基]修饰、2’-烷氧基修饰、2’-o-2-甲氧基乙基、2’-烯丙氧基(-och2ch=ch2)、2’-炔丙基、2’-丙基、2’-o-(n-甲基氨基甲酸酯)修饰、2’-o-(2,4-二硝基苯基)修饰、2’-脱氧-2’-氟-β-d-阿拉伯糖修饰等;4’位的修饰,例如4’硫代修饰、4’-c-羟基甲基修饰等;以及,乙炔基、乙烯基、丙烯基、cf、氰基、咪唑、羧酸酯、硫代酸酯(thioate)、c1~c10低级烷基、取代低级烷基、烷芳基或芳烷基、ocf3、ocn、o-、s-或n-烷基、o-、s-或n-链烯基、soch3、so2ch3、ono2、no2、n3、杂环烷基、杂环烷芳基、氨基烷基氨基、聚烷基氨基或取代甲硅烷基等。作为上述以外的修饰糖,可举出例如锁核酸(lna)、氧杂环丁烷-lna(oxe)、非锁核酸(una)、亚乙基桥联核酸(ena)、阿卓糖醇核酸(ana)、己糖醇核酸(hna)等。本公开文本中,烷基包括饱和脂肪族基团,其包括直链烷基(例如,甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基等)、支链烷基(异丙基、叔丁基、异丁基等)、环烷(脂环式)基团(环丙基、环戊基、环己基、环庚基、环辛基)、烷基取代环烷基。一些方式中,直链或支链烷基在其骨架中具有6个或小于6个的碳原子(例如,就直链而言为c1~c6,就支链而言为c3~c6),更优选具有4个或小于4个的碳原子。同样地,优选的环烷基可在其环结构中具有3~8个碳原子,更优选可在环结构中具有5个或6个碳。用语c1~c6包括含有1~6个碳原子的烷基。烷基也可以是取代烷基、例如在烃骨架的1个或2个以上的碳上具有对氢进行取代的取代基的烷基部分。该取代基可包括例如链烯基、炔基、卤素、羟基、烷基羰基氧基、芳基羰基氧基、烷氧基羰基氧基、芳基氧基羰基氧基、羧酸酯基、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫代羰基、烷氧基、磷酸酯基、膦酸酯基、次膦酸酯基(phosphinate)、氰基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基及烷基芳基氨基)、酰基氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基及脲基)、脒基、亚氨基、巯基、烷基硫基、芳基硫基、硫代羧酸酯基、硫酸盐、烷基亚磺酰基、磺酸酯基、氨基磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基、或者芳香族部分或杂环式芳香族部分。本公开文本中,烷氧基包括与氧原子经共价键合连接而成的取代及非取代烷基、链烯基及炔基。烷氧基的例子包括甲氧基、乙氧基、异丙氧基、丙氧基、丁氧基及戊氧基。取代烷氧基的例子包括卤代烷氧基。烷氧基可被例如链烯基、炔基、卤素、羟基、烷基羰基氧基、芳基羰基氧基、烷氧基羰基氧基、芳基氧基羰基氧基、羧酸酯基、烷基羰基、芳基羰基、烷氧基羰基、氨基羰基、烷基氨基羰基、二烷基氨基羰基、烷基硫代羰基、烷氧基、磷酸酯基、膦酸酯基、次膦酸酯基、氰基、氨基(包括烷基氨基、二烷基氨基、芳基氨基、二芳基氨基及烷基芳基氨基)、酰基氨基(包括烷基羰基氨基、芳基羰基氨基、氨基甲酰基及脲基)、脒基、亚氨基、巯基、烷基硫基、芳基硫基、硫代羧酸酯基、硫酸盐、烷基亚磺酰基、磺酸酯基、氨基磺酰基、磺酰胺基、硝基、三氟甲基、氰基、叠氮基、杂环基、烷基芳基、或者芳香族部分或杂环式芳香族部分取代。卤代烷氧基的例子没有限定,包括氟甲氧基、二氟甲氧基、三氟甲氧基、氯甲氧基、二氯甲氧基、三氯甲氧基等。本公开文本中,卤素包括氟、溴、氯、碘。作为修饰骨架,例如但不限于硫代磷酸酯、硫代磷酸-d-核糖体、三酯、硫代酸酯、2’-5’键合(也称为5’-2’或2’5’核苷酸或者2’5’核糖核苷酸)、pace、pna、3’-(或-5’)脱氧-3’-(或-5’)硫代-硫代磷酸酯、二硫代磷酸酯、硒代磷酸酯、3’-(或-5’)脱氧次膦酸酯、硼烷磷酸酯、3’-(或-5’)脱氧-3’-(或5’-)氨基磷酰胺酯、氢膦酸酯、膦酸酯、硼烷基磷酸酯、磷酰胺酯、烷基或芳基膦酸酯及磷酸三酯修饰、烷基磷酸三酯、磷酸三酯基磷键、5’-乙氧基磷酸二酯、p-烷基氧基磷酸三酯、甲基膦酸酯等、及非含磷键、例如碳酸盐、氨基甲酸酯、甲硅烷基、硫、磺酸酯、磺酰胺基、甲基缩醛(formacetal)、硫代甲乙酰基、肟、亚甲基亚氨基、亚甲基甲基亚氨基、亚甲基亚肼基、亚甲基二甲基亚肼基及亚甲基氧基甲基亚氨基等。作为5’末端及/或3’末端修饰,可举出例如向5’末端及/或3’末端附加帽(capping)部分、5’末端及/或3’末端的磷酸基的修饰、例如[3~3’]-倒位脱氧核糖、脱氧核糖核苷酸、[5’-3’]-3’-脱氧核糖核苷酸、[5’-3’]-核糖核苷酸、[5’-3’]-3’-o-甲基核糖核苷酸、3’-甘油基、[3’-5’]-3’-脱氧核糖核苷酸、[3’-3’]-脱氧核糖核苷酸、[5’-2’]-脱氧核糖核苷酸及[5-3’]-二脱氧核糖核苷酸等。作为帽部分的非限定例子,可举出例如无碱基核苷酸、脱氧无碱基核苷酸、倒位(脱氧)无碱基核苷酸、烃(烷基)部分及其衍生物、镜像核苷酸(l-dna或l-rna)、lna及包括亚乙基桥联核酸的桥联核酸、键修饰核苷酸(例如,pace)及碱基修饰核苷酸、甘油基、二核苷酸、非环式核苷酸、氨基、氟、氯、溴、cn、cf、甲氧基、咪唑、羧酸酯、硫代酸酯、c1~c10低级烷基、取代低级烷基、烷芳基或芳烷基、ocf3、ocn、o-、s-或n-烷基、o-、s-或n-链烯基、soch3、so2ch3、ono2、no2、n3、杂环烷基、杂环烷芳基、氨基烷基氨基、聚烷基氨基或取代甲硅烷基等。帽部分也可作为非核苷酸突出来发挥功能。本公开文本中的修饰核苷酸中包括:2’-脱氧核糖核苷酸、2’-o-甲基核糖核苷酸、2’-脱氧-2’-氟核糖核苷酸、通用碱基核苷酸、非环式核苷酸、5-c-甲基核苷酸、含有生物素基、及末端甘油基及/或倒位脱氧无碱基残基的核苷酸、含有空间位阻分子、例如荧光分子等的核苷酸、含有3’-脱氧腺苷(虫草素)、3’-叠氮基-3’-脱氧胸苷(azt)、2’,3’-二脱氧肌苷(ddi)、2’,3’-二脱氧-3’-硫杂胞苷(3tc)、2’,3’-二脱氢-2’,3’-二脱氧胸苷(d4t)、及3’-叠氮基-3’-脱氧胸苷(azt)、2’,3’-二脱氧-3’-硫杂胞苷(3tc)或2’,3’-二脱氢-2’,3’-二脱氧胸苷(d4t)的核苷酸、具有northern构象的核苷酸、2’-甲基硫代乙基、2’-脱氧-2’-氟核苷酸、2’-脱氧-2’-氯核苷酸、2’-叠氮基核苷酸、及2’-o-甲基核苷酸、6元环核苷酸类似物(例如,wo2006/047842等中记载的含有己糖醇及阿卓糖醇核苷酸单体的核苷酸类似物)、镜像核苷酸(例如,l-dna(l-脱氧核糖腺苷-3’-磷酸酯(镜像da)、l-脱氧核糖胞苷-3’-磷酸酯(镜像dc)、l-脱氧核糖鸟苷-3’-磷酸酯(镜像dg)、l-脱氧核糖胸苷-3’-磷酸酯(镜像胸苷))及l-rna(l-核糖腺苷-3’-磷酸酯(镜像ra)、l-核糖胞苷-3’-磷酸酯(镜像rc)、l-核糖鸟苷-3’-磷酸酯(镜像rg)、l-核糖尿嘧啶-3’-磷酸酯(镜像du)等)。修饰核苷酸的非限定例子也记载于例如gaglione和messere,minirevmedchem.2010;10(7):578-95、deleavey和damha,chembiol.2012;19(8):937-54、bramsen和kjems,j.frontgenet.2012;3:154等中。一些方式中,本公开文本的核酸分子二聚体的tcna及/或tnna由非修饰核苷酸构成,不含修饰核苷酸。另一方式中,本公开文本的核酸分子二聚体的tcna及/或tnna含有非修饰核苷酸和修饰核苷酸这两者。另一方式中,本公开文本的核酸分子二聚体的tcna及/或tnna由修饰核苷酸构成,不含非修饰核苷酸。含有修饰核苷酸的本公开文本的核酸分子二聚体可具有上述修饰中的至少1种,也可具有上述中的2种以上修饰的组合。修饰可存在于本说明书中公开的核酸分子二聚体中的1个或2个以上核酸分子、例如tnna、tcna或这两者。一些方式中,tcna可含有修饰核苷酸,tnna可仅含有非修饰核苷酸。另一方式中,tcna可仅含有非修饰核苷酸,tnna可含有修饰核苷酸。本公开文本的核酸分子二聚体可含有相对于核酸分子中的总核苷酸而言为约5%~约100%的非修饰核苷酸(例如,约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%或约100%的非修饰核苷酸)。另外,本公开文本的核酸分子二聚体可含有相对于核酸分子中的总核苷酸而言为约5%~约100%的修饰核苷酸(例如,约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%或约100%的修饰核苷酸)。存在于核酸分子中的非修饰核苷酸或修饰核苷酸的实际的百分率依赖于存在于核酸分子中的核苷酸的总数。非修饰核苷酸或修饰核苷酸的百分率(非修饰百分比或修饰百分比)可基于存在于tnna、tcna或tnna及tcna这两者中的核苷酸的总数。一些方式中,可出于下述目的而使用修饰:为了使本公开文本的核酸分子的调节靶核酸分子表达的活性增加、及/或为了使核酸分子在体内的稳定性、尤其是血清中的稳定性增加、及/或为了使核酸分子的生物利用度增加。本公开文本的核酸分子二聚体的特定的非限定例子记载于表3中。本公开文本的核酸分子二聚体可进行或不进行标记。通过标记化,能够监测是否成功向靶位点递送、在生物体内的位置等,不仅可用于试验·研究,也可用于临床应用。标记可以选自本领域技术人员已知的任意的物质、例如任意的放射性同位素、磁性体、气体或在生理条件下产生气体的物质、发生核磁共振的元素(例如,氢、磷、钠、氟等)、对核磁共振元素的弛豫时间造成影响的物质(例如,金属原子或含有其的化合物)、与标记化物质结合的物质(例如,抗体等)、荧光物质、荧光团、化学发光物质、生物素或其衍生物、抗生物素蛋白或其衍生物、酶等。本公开文本的核酸分子二聚体能够序列特异性地调节靶核酸分子的表达。靶核酸分子的表达包括靶核酸分子的功能的表达。因此,对于靶核酸分子的表达而言,在例如靶核酸分子编码表达产物(例如,蛋白质及rna分子等核酸分子)的情况下,包括表达产物的生成,在靶核酸分子自身具有生理活性的情况下,包括其生理活性的表达。靶核酸分子的表达的调节包括调节靶核酸分子所编码的表达产物的生成、调节靶核酸分子所具有的生理活性。表达的调节包括表达的抑制及表达的增加。就调节的程度而言,在以不使本公开文本的核酸分子二聚体发挥作用的情况下的靶核酸分子的表达量为基准时,使本公开文本的核酸分子二聚体发挥作用的情况下的靶核酸分子的表达量可以是前述基准值的约±50%以上、优选约±60%以上、更优选约±65%以上、进一步优选约±70%以上、特别优选约±75%以上的程度。因此,本公开文本的核酸分子二聚体可用于调节靶核酸分子的表达。另外,在靶核酸分子的表达与疾病相关的情况下,本公开文本的核酸分子二聚体可用于处置与靶核酸分子的表达相关的疾病。一些方式中,本公开文本的核酸分子二聚体能够通过rna沉默来抑制靶核酸分子的表达。就抑制的程度而言,在将不使本公开文本的核酸分子二聚体发挥作用的情况下的靶核酸分子的表达量设为100%时,使本公开文本的核酸分子二聚体发挥作用的情况下的靶核酸分子的表达量可以是约50%以下、优选约40%以下、更优选约35%以下、进一步优选约30%以下、特别优选约25%以下的程度。该方式中的本公开文本的核酸分子二聚体可用于抑制靶核酸分子的表达。另外,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于处置与靶核酸分子的表达相关的疾病。另一方式中,本公开文本的核酸分子二聚体能够利用rnaa来使靶核酸分子的表达增加。就增加的程度而言,在将不使本公开文本的核酸分子二聚体发挥作用的情况下的靶核酸分子的表达量设为100%时,使本公开文本的核酸分子二聚体发挥作用的情况下的靶核酸分子的表达量可以是约120%以上、优选约130%以上、更优选约150%以上、进一步优选约180%以上、特别优选约200%以上的程度。该方式中的本公开文本的核酸分子二聚体可用于增加靶核酸分子的表达。另外,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于处置与靶核酸分子的表达相关的疾病。一些方式中,本公开文本的核酸分子二聚体的因tnna导致的脱靶效应少。更具体而言,与tnna呈非环状的同样的核酸分子二聚体、例如tnna呈直链状的同样的(例如,具有相同的碱基序列的)核酸分子二聚体相比,本公开文本的核酸分子二聚体的因tnna导致的脱靶效应更少。因此,对于本公开文本的核酸分子二聚体的tnna而言,为了避免脱靶效应而在序列设计上付出努力等的必要性低。该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应的同时调节靶核酸分子的表达,在靶核酸分子的表达与疾病相关的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够通过rna沉默等来抑制靶核酸分子的表达的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应的同时抑制靶核酸分子的表达,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够利用rnaa等使靶核酸分子的表达增加的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应的同时使靶核酸分子的表达增加,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应的同时、对与靶核酸分子的表达相关的疾病进行处置。一些方式中,本公开文本的核酸分子二聚体在施予至细胞的情况下,能够避免pkr(双链rna依赖性蛋白激酶)的磷酸化。即,即使将本公开文本的核酸分子二聚体施予至细胞,也不会诱导pkr的磷酸化,或者,即使诱导了pkr的磷酸化,其程度也低于tnna呈非环状的同样的核酸分子二聚体、例如tnna呈直链状的同样的(例如,具有相同的碱基序列的)核酸分子二聚体。该方式中的本公开文本的核酸分子二聚体可用于在避免pkr的磷酸化的同时调节靶核酸分子的表达,在靶核酸分子的表达与疾病相关的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免pkr的磷酸化的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够通过rna沉默等来抑制靶核酸分子的表达的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免pkr的磷酸化的同时抑制靶核酸分子的表达,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免pkr的磷酸化的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够利用rnaa等使靶核酸分子的表达增加的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免pkr的磷酸化的同时使靶核酸分子的表达增加,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免pkr的磷酸化的同时、对与靶核酸分子的表达相关的疾病进行处置。一些方式中,本公开文本的核酸分子二聚体在施予至细胞的情况下,能够避免tlr3途径的激活。即,即使将本公开文本的核酸分子二聚体施予至细胞,也不会诱导tlr3途径的激活,或者,即使诱导了tlr3途径的激活,其程度也低于tnna呈非环状的同样的核酸分子二聚体、例如tnna呈直链状的同样的(例如,具有相同的碱基序列的)核酸分子二聚体。该方式中的本公开文本的核酸分子二聚体可用于在避免激活tlr3途径的同时调节靶核酸分子的表达,在靶核酸分子的表达与疾病相关的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免激活tlr3途径的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够通过rna沉默等来抑制靶核酸分子的表达的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免激活tlr3途径的同时抑制靶核酸分子的表达,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免激活tlr3途径的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够利用rnaa等使靶核酸分子的表达增加的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免激活tlr3途径的同时使靶核酸分子的表达增加,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免激活tlr3途径的同时、对与靶核酸分子的表达相关的疾病进行处置。特定的方式中,本公开文本的核酸分子二聚体在施予至细胞的情况下,能够避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活。因此,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活的同时、调节靶核酸分子的表达,在靶核酸分子的表达与疾病相关的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够通过rna沉默等来抑制靶核酸分子的表达的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活的同时、抑制靶核酸分子的表达,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够利用rnaa等使靶核酸分子的表达增加的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活的同时、使靶核酸分子的表达增加;在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免因tnna导致的脱靶效应、pkr的磷酸化及tlr3途径的激活的同时、对与靶核酸分子的表达相关的疾病进行处置。pkr与双链rna非序列特异性地结合后发生自磷酸化而将nf-κb等底物磷酸化,引起干扰素等的产生。另外,tlr3与双链rna非序列特异性地结合后也发生自磷酸化而将nf-κb等底物磷酸化,引起干扰素等的产生。如此,认为pkr及tlr3在由核酸分子(尤其是双链rna分子)导致的非序列特异性细胞应答(例如,自然免疫)的诱导过程中起到作为位于最上游的感受器分子的作用,可避免pkr的磷酸化及tlr3途径的激活的本公开文本的核酸分子二聚体能够从该过程的最上游避免所述细胞应答的诱导。因此,一些方式中,本公开文本的核酸分子二聚体能够避免由核酸分子导致的非序列特异性细胞应答(例如,自然免疫)的诱导。另外,该方式中的本公开文本的核酸分子二聚体可用于在避免前述细胞应答的诱导的同时、调节靶核酸分子的表达,在靶核酸分子的表达与疾病相关的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免前述细胞应答的诱导的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够通过rna沉默等来抑制靶核酸分子的表达的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免前述细胞应答的诱导的同时、抑制靶核酸分子的表达,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免前述细胞应答的诱导的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够利用rnaa等使靶核酸分子的表达增加的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免前述细胞应答的诱导的同时、使靶核酸分子的表达增加,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免前述细胞应答的诱导的同时、对与靶核酸分子的表达相关的疾病进行处置。一些方式中,本公开文本的核酸分子二聚体在施予至细胞的情况下,能够避免选自ccl5、cxcl10、ifnβ1、il1β、il6、il10、il13、tnf及cxcr4中的至少1个基因的表达增强。也就是说,即使将本公开文本的核酸分子二聚体施予至细胞,也不会增强上述基因的表达,或者,即使增强了上述基因的表达,其程度也低于tnna呈非环状的同样的核酸分子二聚体、例如tnna呈直链状的同样的(例如,具有相同的碱基序列的)核酸分子二聚体。该方式中的本公开文本的核酸分子二聚体可用于在避免上述基因中的至少1个表达增强的同时、调节靶核酸分子的表达,在靶核酸分子的表达与疾病相关的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免上述基因中的至少1个表达增强的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够通过rna沉默等来抑制靶核酸分子的表达的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免上述基因中的至少1个表达增强的同时、抑制靶核酸分子的表达,在靶核酸分子的表达与疾病相关、靶核酸分子的表达的抑制对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免上述基因中的至少1个表达增强的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的核酸分子二聚体能够利用rnaa等使靶核酸分子的表达增加的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免上述基因中的至少1个表达增强的同时、使靶核酸分子的表达增加;在靶核酸分子的表达与疾病相关、靶核酸分子的表达的增加对于该疾病的改善有用的情况下,该方式中的本公开文本的核酸分子二聚体可用于在避免上述基因中的至少1个表达增强的同时、对与靶核酸分子的表达相关的疾病进行处置。本公开文本的核酸分子二聚体没有限定,可通过例如包括将直链状的tnna环化的步骤、和将环化的tnna与直链状的tcna退火的步骤的方法来制造。有时将包含将直链状的tnna环化而得到的环状tnna的、含有环状tnna的核酸分子二聚体称为“tnna环化核酸分子二聚体”。将直链状的tnna环化的步骤可通过将直链状的核酸分子环化的任意已知方法来达成。作为该方法,例如但不限于利用连接酶等的酶连接、及利用brcn、n-乙基-n’-(3-二甲基氨基丙基)碳二亚胺(有时简称为edc或edac等)、咪唑、n-羟基苯并三唑、1-均三甲苯基磺酰基-3-硝基-1,2,4-三唑(msnt)等的化学连接等。酶连接可通过例如使连接酶(根据进行连接的核苷酸的种类,为例如rna连接酶、dna连接酶等)作用于分别在5’末端具有磷酸基、在3’末端具有羟基的直链状的tnna来实施。反应温度优选为酶的最适温度或其附近的温度。反应时间没有特别限定,可以进行适当调整以达到所期望的程度的连接,可以是例如6小时~36小时、12小时~24小时等范围。连接反应有时会需要atp。各种连接酶皆有市售,反应条件优选遵循制造商的指示。在得到所期望的程度的连接后,可通过加热等使连接酶失活,使得连接酶不会对后续的反应造成影响。作为化学连接,已知各种方法。利用brcn的连接可通过向在5’末端或3’末端具有磷酸基的直链状的tnna添加brcn、咪唑及2价金属离子(例如,mn2+、co2+、ni2+、cu2+、zn2+、mg2+、fe2+等)、使其反应规定时间来实施(例如,dolinnaya等,nucleicacidsres.1993;21(23):5403-7、wang和kool,nucleicacidsres.1994;22(12):2326-33等)。利用edc的连接可通过将直链状的tnna在缓冲液(例如,含有2-吗啉基乙磺酸盐和mgcl2的缓冲液等)中与edc进行孵育来实施(例如,dolinnaya等,nucleicacidsres.1988;16(9):3721-38)。就利用edc的连接而言,通过使用在3’末端具有氨基或磷酸基的直链状的tnna,能够提高反应速度。利用msnt的连接记载于micura,chemeurj.1999;5(7):2077-82等中。环化的tnna可在从连接反应物纯化后用于与tcna的退火。纯化可使用透析等已知的任意的核酸纯化方法。连接反应物含有未反应的直链状tnna的情况下,可通过将反应物用核酸外切酶等选择性地分解直链状核酸分子的酶进行处理来分解直链状tnna、将环状tnna浓缩,或通过电泳(例如,变性page)等来分离反应物中的核酸分子、切出相当于环状tnna的条带,从而排除直链状tnna。环状tnna与直链状tcna的退火可使用已知的任意方法来实施。退火没有限定,可通过例如下述方法来实施:将已溶解于退火缓冲液的tnna及tcna于约70℃~约90℃加热约1分钟~约5分钟,然后,于约37℃孵育0.5~2小时。可通过例如电泳(例如,page)等来确认是否进行了退火。直链状的tnna可以设计为在保持原状(即,保持直链状)的情况下难以与tcna退火,但在环化后与tcna的退火变得容易(例如,使直链状tnna在环化时的连接位点(即,直链状的tnna的5’末端及3’末端)与将环化的tnna与tcna退火时由tcna形成的切口或缺口不一致)。通过这样设计直链状的tnna,从而在直链状tnna的环化反应后,即使反应物中混有未环化而残留的直链状tnna,由于直链状tnna的序列与tcna的互补序列大不相同,与tcna退火并形成直链状的核酸分子二聚体的可能性变低,因此,能够高纯度地得到本公开文本的含有环状tnna的核酸分子二聚体,并且能够避免因直链状tnna导致的脱靶效应,这是有利的。这种情况在利用核酸外切酶等酶学地除去非环化tnna时尤其有利。因此,本公开文本提供了高纯度的含有环状tnna的核酸分子二聚体的制造方法,其包括下述步骤:提供在保持直链状的情况下难以与tcna退火、但在环化后与tcna的退火变得容易的直链状tnna(例如,如下设计直链状tnna:使直链状tnna环化时的连接位点与将环化tnna与tcna退火时由tcna形成的切口或缺口不一致)。利用该制造方法得到的含有环状tnna的核酸分子二聚体的纯度,高于不使用上述的直链状tnna而制造的含有环状tnna的核酸分子二聚体的纯度。另外,本公开文本还涉及这样高纯度的含有环状tnna的核酸分子二聚体。上述的纯度是指含有环状tnna的核酸分子二聚体在含有环状tnna的核酸分子二聚体的制造步骤中的最终产物中所占的比例,可通过将最终产物中的含有环状tnna的核酸分子二聚体的摩尔数除以最终产物的总摩尔数、或将最终产物中的含有环状tnna的核酸分子二聚体的质量除以最终产物的总质量来计算。以质量为基准的纯度可基于例如将最终产物的色谱图(例如,使用高效液相色谱法(hplc)得到的色谱图)中的含有环状tnna的核酸分子二聚体的峰面积除以最终产物的总峰面积而得到的峰比等来计算。为了得到上述直链状的tnna,例如,可设计直链状tnna,使得在直链状的tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基的数目或比例(例如,相对于tnna或tcna中所含的全部核酸碱基而言的比例)成为规定值以下。相对于tnna中所含的总核酸碱基数而言,在直链状的tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基数的比例可以是例如约75%以下、约70%以下、约65%以下、约60%以下、约55%以下、约54%以下、约53%以下等。该设计方法的非限定例子如下所示。需要说明的是,以下的各序列中,xn表示tcna中所含的核酸碱基,yn表示tnna中所含的核酸碱基,n表示tcna中所含的核酸碱基的自5’末端起的位置。yn与n为相同数字的xn互补(例如,y1与x1互补)。(1)在直链状tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基对的比例的最大值为tnna中所含的全部核酸碱基的100%的情况:tcna:5’x1x2x3x4x5x6x7x8x9x10x11x12x13x14x15x16x17x18x193’tnna:3’y1y2y3y4y5y6y7y8y9y10y11y12y13y14y15y165’上述的例子中,tnna的16位~1位(5’至3’的顺序)的全部核酸碱基与tcna的对应部分(1位~16位)的全部核酸碱基互补,在直链状tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基数为16。因此,上述的核酸碱基数相对于tnna中所含的总核酸碱基数的比例(%)为16÷16×100=100(%)。(2)在直链状tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基对的比例的最大值为tnna中所含的全部核酸碱基的50%的情况:tcna:5’x1x2x3x4x5x6x7x8x9x10x11x12x13x14x15x16x17x18x193’tnna:3’y9y10y11y12y13y14y15y16y1y2y3y4y5y6y7y85’上述的例子中,tnna的8位~1位(y1y2y3y4y5y6y7y8)的全部核酸碱基与tcna的对应部分(1位~8位)的全部核酸碱基(x1x2x3x4x5x6x7x8)互补,tnna的16位~10位(y9y10y11y12y13y14y15y16)的全部核酸碱基与tcna的对应部分(10位~16位)的全部核酸碱基(x9x10x11x12x13x14x15x16)互补。因此,在直链状tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基数最大为8,上述的核酸碱基数相对于tnna中所含的总核酸碱基数的比例(%)为8÷16×100=50(%)。该比例为50%的tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基对的比例的最大值变得最低。(3)在直链状tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基对的比例的最大值为tnna中所含的全部核酸碱基的75%的情况:tcna:5’x1x2x3x4x5x6x7x8x9x10x11x12x13x14x15x16x17x18x193’tnna:3’y5y6y7y8y9y10y11y12y13y14y15y16y1y2y3y45’上述的例子中,tnna的4位~1位(y1y2y3y4)的全部核酸碱基与tcna的对应部分(1位~4位)的全部核酸碱基(x1x2x3x4)互补,tnna的16位~5位(y5y6y7y8y9y10y11y12y13y14y15y16)的全部核酸碱基与tcna的对应部分(5位~16位)的全部核酸碱基(x5x6x7x8x9x10x11x12x13x14x15x16)互补。因此,在直链状tnna与tcna的对应部分之间形成的连续互补区域中所含的核酸碱基数最大为12,上述的核酸碱基数相对于tnna中所含的总核酸碱基数而言的比例(%)为12÷16×100=75(%)。作为得到上述那样的直链状的tnna的其他手段,可举出如下设计直链状tnna:使直链状tnna环化时的连接位点(即,直链状tnna的5’末端及3’末端)成为和将环化tnna与tcna退火时由tcna形成的切口或缺口不同的位置。优选以连接位点成为远离切口或缺口的位置的方式进行设计,特别优选以连接位点成为切口或缺口的相反侧或相反侧的附近的方式进行设计。此处,相反侧是指:例如,将构成tnna的全部单体在圆周上均等地排列的情况下,在tnna上相对于圆的中心而与切口或缺口的中点呈点对称的位置。图2中示出了优选的连接位点的非限定例子。就图2所示的核酸分子二聚体而言,tcna具有切口及5’突出,成为切口相反侧的tnna中的位置为4。切口的相反侧的附近可以是例如1~3及5~7、2~3及5~6、3及5等。构成tnna的核苷酸的数目为奇数个的情况下,成为切口相反侧的tnna中的位置为位于正对切口的相反侧位置上的核苷酸的3’侧或5’侧。本公开文本的核酸分子二聚体可与已知的任意的递送担载体(其对于向作用部位的递送具有辅助、促进或简单化的作用)一同递送或施予,也可无需上述递送担载体而直接进行递送或施予。作为递送担载体,可使用病毒载体或非病毒载体。作为非病毒载体,例如但不限于聚合物粒子、脂质粒子、无机粒子等粒子状担载体。作为粒子,可使用大小为纳米水平的纳米粒子。作为聚合物粒子,例如但不限于含有阳离子性聚合物、聚酰胺胺(pamam)、脱乙酰壳多糖、环糊精、聚乳酸乙醇酸共聚物(plga)、聚乳酸己内酯共聚物(plca)、聚(β氨基酯)、去端胶原蛋白(atelocollagen)等聚合物的聚合物粒子。作为阳离子性聚合物,可举出例如聚赖氨酸(例如,聚l-赖氨酸(pll))、聚乙烯亚胺(pei)、它们的衍生物等。作为聚乙烯亚胺的衍生物,可举出例如聚乙烯亚胺-聚乙二醇共聚物(pei-peg)、聚乙烯亚胺-聚乙二醇-n-乙酰氨基半乳糖(pei-peg-gal)、聚乙烯亚胺-聚乙二醇-三(n-乙酰氨基半乳糖)(pei-peg-trigal)、接枝pei、例如半乳糖pei、胆固醇pei、抗体衍生物化pei等。含有胺的聚合物在被摄入核内体时,能发挥有利于脱离核内体的质子海绵效应。脂质粒子包括脂质体、非脂质体型脂质粒子等。脂质体是具有被脂质双层膜包围的内腔的小泡,非脂质体型脂质粒子是不具有这样的结构的脂质粒子。脂质粒子可含有阳离子性脂质、可离子化的(ionizable)脂质、辅助脂质等。对于将具有负电荷的核酸分子等导入细胞内而言,阳离子性脂质是特别有用的。作为阳离子性脂质的非限定例子,可举出n-(α-三甲基铵基乙酰基)-双十二烷基-d-谷氨酸酯氯化物(tmag)、n,n’,n”,n”’-四甲基-n,n’,n”,n”’-四棕榈基精胺(tmtps)、2,3-二油基氧基-n-[2(精胺羧基酰胺)乙基]-n,n-二甲基-1-丙基三氟乙酸铵(dospa)、n-[1-(2,3-二油基氧基)丙基]-n,n,n-三甲基氯化铵(dotma)、双十八烷基二甲基氯化铵(dodac)、双十二烷基溴化铵(ddab)、1,2-二油基氧基-3-三甲基铵基丙烷(dotap)、3β-[n-(n’,n’-二甲基氨基乙烷)氨基甲酰基]胆固醇(dc-chol)、1,2-二肉豆蔻酰基氧基丙基-3-二甲基羟基乙基溴化铵(dmrie)、o,o’-双十四碳酰基-n-(α-三甲基铵基乙酰基)二乙醇胺氯化物(dc-6-14)等。其他有用的阳离子性脂质的例子也记载于wo2012/170952等中。作为可离子化的脂质,可举出可离子化的阳离子性脂质。可离子化的阳离子性脂质具有在pka以上的ph下呈非离子性、但在低于pka的ph下呈阳离子性的性质。可离子化的脂质有时具有叔胺。通过含有胺,从而在被摄入核内体时能发挥有利于脱离核内体的质子海绵效应。一些方式中,可离子化的阳离子性脂质的pka可以是7.0以上、7.5以上、7.6以上、7.8以上、8.0以上等。作为可离子化的脂质的非限定例子,可举出dlindap、dlindma、dlinkdma、dlinkc2-dma等。其他有用的可离子化的阳离子性脂质的例子也记载于wo2013/185116等中。辅助脂质是有助于脂质粒子的稳定化等的脂质。辅助脂质在电荷方面可以是中性的。作为辅助脂质的非限定例子,可举出胆固醇、二油酰磷脂酰乙醇胺(dope)、棕榈酰油酰-磷脂酰乙醇胺(pope)、二植烷酰磷脂酰乙醇胺(dphpe)、二硬脂酰磷脂酰乙醇胺(dspe)、二棕榈酰磷脂酰乙醇胺(dppe)、二肉豆蔻酰磷脂酰乙醇胺(dmpe)、peg脂质等。作为无机粒子,可举出例如金纳米粒子、量子点、二氧化硅纳米粒子、氧化铁纳米粒子(例如,超顺磁氧化铁纳米粒子(spion))、纳米管(例如,碳纳米管(cnt))、纳米金刚石、富勒烯等。可对上述粒子担载体加以各种修饰。可举出例如利用peg的隐形化、利用靶向化配体的靶向化、利用细胞穿透肽(cpp)的修饰等。也可使上述的聚合物、靶向化配体、cpp等的功能部位与本公开文本的核酸分子二聚体结合而制成偶联物。由此,能够在不使用上述担载体的情况下将本公开文本的核酸分子二聚体制成制剂。可使上述功能部位与tcna及tnna中的任一者结合,优选使其与被认为不会直接作用于靶核酸分子的tnna结合。可使功能部位与tnna的任意部分结合。特定的方式中,使功能部位与tcna形成了切口或缺口的tnna的一部分结合。另一方式中,使功能部位与从tcna形成了切口或缺口的位置远离的tnna的一部分、例如切口或缺口的相反侧的tnna的一部分结合。本公开文本的核酸分子二聚体可介由皮肤施用、经皮施用或注射(静脉注射、皮内注射、皮下注射、肌肉注射、动脉注射、点滴注射等),进行全身施予、或者以离体(exvivo)或体内(invivo)的方式局部施予至相关的组织。本公开文本的核酸分子二聚体可通过肺递送、例如吸入气雾剂或喷雾干燥制剂等(其可利用能实现核酸分子向相关肺组织的迅速的局部导入的吸入装置或喷雾器来施予)来进行施予。本公开文本的核酸分子二聚体还可施予至中枢神经系统(cns)或末梢神经系统(pns)。核酸分子向cns的递送没有限定,可通过蛛网膜下及脑室内施予、导管及泵的移植、向损伤部位或病变部位的直接注射或灌注、向脑动脉系统的注射、或血脑屏障的化学开放或渗透压开放等来实施。本公开文本的核酸分子二聚体可利用适合目的的递送系统来递送。递送系统可包括例如水性及非水性的凝胶、霜、复合乳液、微乳液、脂质体、软膏、水性及非水性的溶液、洗剂、气雾剂、烃基剂及粉末等,并且可含有赋形剂、例如增溶剂、促渗透剂(例如,脂肪酸、脂肪酸酯、脂肪族醇及氨基酸等)及亲水性聚合物(例如,聚卡波非及聚乙烯吡咯烷酮等)。一个方式中,药学上可允许的担载体为脂质体或经皮促进剂。递送系统也可包括贴片、片剂、栓剂、阴道栓剂、凝胶及霜,并且可含有赋形剂、例如增溶剂及促进剂(例如丙二醇、胆汁酸盐及氨基酸等)、及其他媒介物(vehicle)(例如,聚乙二醇、脂肪酸酯及衍生物、及亲水性聚合物、例如羟丙基甲基纤维素及透明质酸等)。可用于递送本公开文本的核酸分子二聚体的方法、系统记载于例如rettig和behlke,molther.2012;20(3):483-512、kraft等,jpharmsci.2014;103(1):29-52、hong和nam,theranostics.2014;4(12):1211-32、kaczmarek等,genomemed.2017;9(1):60等中。本公开文本的一些方式涉及含有本公开文本的核酸分子二聚体的组合物(以下有时称为本公开文本的组合物)。本公开文本的组合物中所含的核酸分子二聚体可以是同一种,也可以是2种以上不同的核酸分子二聚体。本公开文本的组合物含有2种以上不同的核酸分子二聚体的情况下,核酸分子二聚体可以针对不同的靶核酸分子,也可以针对同一靶核酸分子的不同序列(区域)。本公开文本的组合物不仅可含有本公开文本的核酸分子二聚体,也可含有上述的任意的担载体、稀释剂、递送媒介物、递送系统等。本公开文本的组合物可用于处置与靶核酸分子相关的疾病。因此,本公开文本的组合物可以成为用于处置与靶核酸分子相关的疾病的医药组合物(以下,有时称为本公开文本的医药组合物)。本公开文本的医药组合物可含有1种或2种以上药学上可允许的添加物(例如,表面活性剂、担载体、稀释剂、赋形剂等)。药学上可允许的添加物在医药领域中是熟知的,记载于例如全部内容被本说明书引用的remington’spharmaceuticalsciences,18thed.,mackpublishingco.,easton,pa(1990)等中。一些方式中,与本公开文本的核酸分子二聚体同样地,本公开文本的医药组合物可用于处置与靶核酸分子的表达相关的疾病。特定的方式中,本公开文本的医药组合物可用于在避免因tnna导致的脱靶效应、pkr的磷酸化、tlr3途径的激活及由核酸分子导致的非序列特异性细胞应答(例如,自然免疫)的诱导中的至少一者的同时、对与靶核酸分子的表达相关的疾病进行处置。另外,本公开文本的医药组合物可用于在避免选自ccl5、cxcl10、ifnβ1、il1β、il6、il10、il13、tnf及cxcr4中的至少1个基因表达增强的同时、对与靶核酸分子的表达相关的疾病进行处置。本公开文本中,“处置”包括以疾病的治愈、暂时性缓解或预防等为目的的、医学上允许的所有种类的预防性及/或治疗性介入。例如,“处置”包括医学上允许的出于各种目的的介入,所述目的包括:与靶核酸分子相关的疾病发展的延迟或停止、病变的缩减或消失、该疾病发病的预防或复发的防止等。因此,前述核酸分子二聚体及医药组合物中包含用于治疗与靶核酸分子相关的疾病的医药组合物、及用于预防与靶核酸分子相关的疾病的医药组合物。本公开文本的核酸分子二聚体或医药组合物可通过包括口服及肠胃外这两者的各种途径(例如,口服、颊侧、口腔内、静脉内、肌肉内、皮下、皮内、局部、直肠、动脉内、门静脉内、心室内、经粘膜、经皮、鼻腔内、腹腔内、气管内、肺内及子宫内等途径,不受限定)进行施予,也可制备为适于各施予途径的剂型。所述剂型及制剂方法可适当采用任意的已知剂型及制剂方法(参见例如remington’spharmaceuticalsciences,18thed.,mackpublishingco.,easton,pa(1990)等)。例如,作为适于口服施予的剂型,例如但不限于散剂、颗粒剂、片剂、胶囊剂、液剂、悬浮剂、乳剂、凝胶剂、糖浆剂等,另外,作为适于肠胃外施予的剂型,可举出溶液性注射剂、悬浮性注射剂、乳浊性注射剂、使用前制备型注射剂等注射剂。肠胃外施予用制剂可以是水性或非水性的等渗性无菌溶液或悬浮液的形态。本公开文本涉及的组合物可通过任意形态来供给,从保存稳定性的观点考虑,可以以能够在使用前制备的形态提供,例如,可以以能够由医师及/或药剂师、护士或其他辅助医务人员等在医疗现场或其附近进行制备的形态提供。这种情况下,前述组合物以其必需构成要素中的至少1种包含在1个或2个以上的容器中的形式被提供,可在使用之前、例如24小时前以内、优选3小时前以内、并且更优选在即将使用之前进行制备。制备时,可适当使用在制备场所通常能够获得的试剂、溶剂、配药器具等。本公开文本的另一其他方式还涉及试剂盒或包(pack),其包含本公开文本涉及的组合物或其构成要素,用于制备前述组合物,并用于处置与靶核酸分子相关的疾病;以及,以所述试剂盒或包的形式提供的前述组合物、或其必要构成要素。所述试剂盒或包中所含的组合物的各构成要素如上文中关于前述组合物所述。本试剂盒除了上述以外还可包含关于组合物的制备方法、使用方法(例如,施予方法等)等的指示,例如使用说明书、记录有关于使用方法的信息的介质、例如软盘、cd、dvd、蓝光碟片、内存卡、u盘等。另外,所述试剂盒或包可包含用于完成组合物的全部构成要素,但并非必须包含全部构成要素。因此,前述试剂盒或包可以不包含在医疗现场、实验机构等通常能够获得的试剂、溶剂、例如无菌水、生理盐水、葡萄糖溶液等。本公开文本的另一方式涉及对与靶核酸分子相关的疾病进行处置的方法(以下有时称为“本公开文本的处置方法”),该方法包括将含有对前述疾病进行处置的药物的有效量的本公开文本涉及的核酸分子二聚体或医药组合物施予至需要处置的对象的步骤。此处,有效量是指例如预防该疾病的发病及复发、或治愈该疾病的量。前述处置方法中施予至对象的核酸分子二聚体或医药组合物的具体用量可考虑与需要施予的对象相关的下述各种条件而确定:例如,靶标的种类、方法的目的、治疗内容、疾病的种类、症状的严重程度、对象的一般健康状态、年龄、体重、对象的性别、膳食、施予的时期及频率、合用的医药、对于治疗的反应性、及对于治疗的依从性等。医药组合物的每天的总施予量没有限定,可以是例如以核酸分子二聚体的量计约1μg/kg~约1000mg/kg体重、约10μg/kg~约100mg/kg体重、约100μg/kg~约10mg/kg体重。或者,施予量可基于患者的表面积来计算。作为施予途径,包括包含口服及肠胃外这两者在内的各种途径,例如,口服、颊侧、口腔内、静脉内、肌肉内、皮下、皮内、局部、直肠、动脉内、门静脉内、心室内、经粘膜、经皮、鼻腔内、腹腔内、气管内、肺内及子宫内等。对于施予频率而言,根据使用的制剂或组合物的性状、如上所述的对象的条件的不同而不同,例如,可以是每天多次(即每天2、3、4次或5次以上)、每天1次、每数天(即每2、3、4、5、6、7天等)、每周数次(例如,每周2、3、4次等)、每周、每数周(即每2、3、4周等)。本公开文本中,用语“对象”表示任意的生物个体,优选为动物,更优选为哺乳动物,进一步优选为人类的个体。对象可以是健康的(例如,未患有特定或任意的疾病),也可患有某种疾病,但在谋求对与靶核酸分子相关的疾病的处置等时,典型地表示患有该疾病或具有罹患该疾病的风险的对象。本公开文本的另一方式涉及调节靶核酸分子的表达的方法(以下有时称为“本公开文本的表达调节方法”),该方法包括将有效量的本公开文本涉及的核酸分子二聚体或医药组合物施予至含有靶核酸分子的细胞的步骤。此处,有效量是指例如能够以可检测的程度调节该靶核酸分子表达的量。若靶核酸分子的表达与蛋白质的产生有关,则可利用已知的蛋白质检测方法来进行检测,例如但不限于,利用了抗体的免疫沉淀法、eia(酶免疫测定法,enzymeimmunoassay)(例如,elisa(酶联免疫吸附测定法,emzyme-linkedimmunosorbentassay)等)、ria(放射免疫分析法,radioimmunoassay)(例如,irma(免疫放射分析法,immunoradiometricassay)、rast(放射过敏原吸附试验,radioallergosorbenttest)、rist(放射免疫吸附试验,radioimmunosorbenttest)等)、western印迹法、免疫组织化学法、免疫细胞化学法、流式细胞术等。若靶核酸分子的表达与核酸分子的产生有关,则可利用已知的核酸分子检测方法来进行检测,例如但不限于,利用可与该核酸分子或其特有片段特异性地杂交的核酸的各种杂交法、northern印迹法、southern印迹法、各种pcr法等。另外,靶核酸分子的表达为表达生理活性的情况下,可利用该生理活性的已知的任意检测方法来进行检测。本公开文本的表达调节方法可以通过体外(invitro)、离体或体内的方式进行。核酸分子二聚体或医药组合物向细胞的施予可利用已知的任意方法来实施,例如,体内的情况下,可通过如上文中针对本公开文本的处置方法记载的包括口服及肠胃外这两者的各种途径来实施,体外或离体的情况下,可通过向含有细胞的介质(例如,培养基等)中添加核酸分子二聚体或医药组合物等来实施。实施例以下,通过实施例详细地说明本发明,但本发明的内容不限于此。例1:含有环状核酸分子的核酸分子二聚体(circularnucleicacidmolecule-containingnucleicacidmoleculedimer,cna-nad)的制造cna-nad是通过将直链状的靶标非互补核酸分子(targetnon-complementarynucleicacid,tnna)环化、并将其与直链状的靶标互补核酸分子(targetcomplementarynucleicacid,tcna)退火而制造的。(1)使用的序列tnna使用了以下的序列。[表1]表1tnna序列名称序列序列号tn-15’-p-gagcugcuccauuaac-3’1tn-25’-p-cugcuuaauuaacgag-3’2tn-35’-p-gaauaugaccaaaguc-3’3tn-45’-p-cugcuuaacauuaacgag-3’4tn-55’-p-cugcuuaaccauuaacgag-3’5tn-65’-p-gaauaugacaaccaaaguc-3’6tn-75’-p-cugcuuaaaaccauuaacgag-3’7tn-85’-p-cugcuuaaccaaccauuaacgag-3’8tn-95’-p-cugcuuaagcccaaccauuaacgag-3’9tn-105’-p-uucaaggaccaucuuc-3’10tn-115’-p-ucuucuucgcgcacca-3’11tn-125’-ccauuaacgagcugcu-3’12tn-135’-cugcuuaauuaacgag-3’13tn-145’-uuaacgagcugcuuaa-3’14tn-155’-ccaaagucgaauauga-3’15tn-165’-ccauuaacgagcugcuuaa-3’16tn-175’-cugcuuaaccauuaacgag-3’17tn-185’-caaccaaagucgaauauga-3’18tn-195’-ccauuaacgagcugcuuaadtdt-3’19tn-205’-caaccaaagucgaauaugadtdt-3’20tn-215’-ccaucuucuucaagga-3’21tn-225’-gcgcaccaucuucuuc-3’22tn-235’-gcaccaucuucuucaagga-3’23tn-245’-ggagcgcaccaucuucuuc-3’24tcna使用了以下的序列。[表2]表2tcna序列名称序列序列号tc-15’-uuaagcagcucguuaaugg-3’25tc-25’-ucauauucgacuuugguug-3’26tc-35’-uuaagcagcucguuaaugguu-3’27tc-45’-uuaagcagcucguuaauggdtdt-3’28tc-55’-ucauauucgacuuugguugdtdt-3’29tc-65’-uuaagc+agcucguuaaugg-3’30tc-75’-uuaagc+agcucguua+augg-3’31tc-85’-p-uuaagcagcucguuaaugg-3’32tc-95’-uccuugaagaagauggugc-3’33tc-105’-gaagaagauggugcgcucc-3’34tc-115’-uuaagcagcucguuaa-3’35表中,a、c、g及u表示rna,da、dc、dg及dt表示dna,p表示磷酸基,+表示lna。(2)tnna的环化按照制造商的指示,在atp的存在下,于37℃使rna连接酶(t4rna连接酶1,neb)与分别在5’末端具有磷酸基、在3’末端具有羟基的直链状的tnna反应16小时,将tnna的5’末端与3’末端连接。反应结束后,将反应物于65℃孵育15分钟,使rna连接酶失活。将反应物注入20%t变性聚丙烯酰胺/尿素凝胶,于250v电泳90分钟。将凝胶用0.5μg/ml的溴化乙锭染色15分钟,使用uv来检测条带。作为ladder标记,使用了dynamarker(r)smallrnaiieasyload(biodynamicslaboratory)。使用了tn-2及tn-5作为tnna的电泳的结果示于图3。需要说明的是,作为非环化对照,使用了连接前的tnna,作为环化对照,使用了将tn-2及tn-5如上所述地环化后、出于浓缩环化核酸分子的目的用rnaser(epicentre)处理而得到的物质。由图3可知,在5’末端具有磷酸基的tnna(tn-2及tn-5)被环化。切出环化核酸分子的条带,粉碎凝胶后,使其于37℃溶出至水中4小时以上,使用dr.gentle(r)precipitationcarrier(takarabio)共沉淀并纯化。将其溶解于不含rnase的水中,作为环状(circular)tnna(ctnna)用于之后的实验。(3)退火将上述(2)中得到的含有ctnna的核酸分子溶液6μl、和将与ctnna相同摩尔浓度的直链状(linear)tcna(ltcna)溶解于不含rnase的水中得到的核酸分子溶液各6μl、与作为退火缓冲液的tris-edta缓冲液(10mmtris-hcl,50mmnacl,1mmedta)3μl混合,于80℃反应5分钟,然后于37℃反应1小时。为了确认退火,通过非变性page对反应物进行分析。将反应物注入20%聚丙烯酰胺凝胶,于200v电泳70分钟。将凝胶用0.5μg/ml的溴化乙锭染色15分钟,使用uv来检测条带。作为ladder标记,使用了dynamarker(r)smallrnaiieasyload(biodynamicslaboratory)。使用tn-2作为tnna、使用tc-1作为tcna的电泳的结果示于图4。根据该图所示的结果,确认到ctnna与ltcna发生了退火。利用上述的方法,制造以下的cna-nad。需要说明的是,以下的表中的“长度(tn/tc)”表示“tnna的长度/tcna的长度”。[表3]表3含有环状tnna的核酸分子二聚体的制造例名称tnnatcna靶基因长度(tn/tc)结构cl-1tn-1tc-1plk116/19tcna具有5’末端突出cl-2tn-2tc-1plk116/19tcna具有3’末端突出cl-3tn-3tc-2plk116/19tcna具有3’末端突出cl-4tn-5tc-4plk119/21tcna具有3’末端突出cl-5tn-5tc-1plk119/19tcna具有切口cl-6tn-6tc-2plk119/19tcna具有切口cl-7tn-4tc-1plk118/19tcna具有3’末端突出cl-8tn-7tc-1plk121/19tcna具有缺口cl-9tn-8tc-1plk123/19tcna具有缺口cl-10tn-9tc-1plk125/19tcna具有缺口cl-11tn-2tc-4plk116/21tcna具有3’末端突出cl-12tn-4tc-4plk118/21tcna具有3’末端突出cl-13tn-7tc-4plk121/21tcna具有3’末端突出+缺口cl-14tn-8tc-4plk123/21tcna具有3’末端突出+缺口cl-15tn-9tc-4plk125/21tcna具有3’末端突出+缺口cl-16tn-2tc-3plk116/21tcna具有3’末端突出cl-17tn-4tc-3plk118/21tcna具有3’末端突出cl-18tn-5tc-3plk119/21tcna具有3’末端突出cl-19tn-7tc-3plk121/21tcna具有切口cl-20tn-8tc-3plk123/21tcna具有缺口cl-21tn-9tc-3plk125/21tcna具有缺口cl-22tn-2tc-6plk116/19tcna具有3’末端突出cl-23tn-2tc-7plk116/19tcna具有3’末端突出cl-24tn-10tc-9gfp16/19tcna具有3’末端突出cl-25tn-11tc-10gfp16/19tcna具有3’末端突出除了代替tnna而将tcna环化以外,与上述同样地操作,制造以下的cna-nad。[表4]表4含有环状tcna的核酸分子二聚体的制造例名称tnnatcna靶基因长度(tn/tc)结构lc-1tn-17tc-8plk119/19tnna具有切口另外,tnna和tcna均不进行环化,将直链状tnna与直链状tcna如上述(3)所述地进行退火,制造以下的核酸分子二聚体。[表5]表5tnna/tcna非环化核酸分子二聚体的制造例例2:含有环状tnna的核酸分子二聚体的敲低效果(1)将a549细胞以0.1×105个/孔的密度接种于24孔培养板,在含有10%fbs的杜氏改良eagle培养基(dulbecco’smodifiedeagle’smedium)(dmem,sigma-aldrich)中于37℃、5%co2下孵育。第二天,按照制造商的方案,将在opti-mem(sigma-aldrich)培养基中含有lipofectaminernaimax转染试剂(thermofisherscientific)和各核酸分子的试样以核酸分子的最终浓度成为10nm的方式添加至a549细胞培养物中,转染5小时。转染后,将培养基置换为含有10%fbs的dmem培养基。在自转染开始24小时后,使用rneasyminikit(qiagen)提取rna,使用superscriptvilomastermix(thermofisherscientific)进行逆转录反应后,使用sybrgreenpcrmastermix(thermofisherscientific)实施实时pcr,测定plk1的表达量。结果示于下表。表中,mrna残留率用将未处理组(nt)中的mrna的残留率作为100%的情况下的比率(%)来表示,将10nm的rna浓度下的mrna残留率为30%以下的情况判定为合格(○)。[表6]表6各种核酸分子二聚体的mrna残留率如上所述,可知利用含有环状tnna的核酸分子二聚体能够充分地得到敲低效果。例3:含有环状tnna的核酸分子二聚体的敲低效果(2)对具有各种结构(区别在于有无突出、缺口)的含有环状tnna的核酸分子二聚体的敲低效果进行了研究。简单而言,将a549细胞以2×103个/孔的密度接种于96孔培养板,将图5所示的各核酸分子二聚体的最终浓度设为20nm,除此以外,与例2同样地操作,基于mrna残留率对各核酸分子二聚体的敲低效果进行评价。由图5所示的结果可知,无论含有环状tnna的核酸分子二聚体有无突出,tcna是否具有切口、缺口,均可获得充分的敲低效果。例4:含有环状tnna的核酸分子二聚体的敲低效果(3)对在tcna中具有修饰的含有环状tnna的核酸分子二聚体的敲低效果进行了研究。简单而言,作为核酸分子二聚体,使用了表7中记载的核酸分子二聚体,除此以外,与例2同样地操作,对各核酸分子二聚体的敲低效果进行了评价。[表7]表7在tcna中具有修饰的核酸分子二聚体的mrna残留率试样名称平均%sdnt1009.6cl-2302.4cl-22244.8cl-23241.5ll-590.5ll-12130.7ll-13160.6由表7所示的结果可知,就含有环状tnna的核酸分子二聚体而言,即使tcna进行了修饰,也可获得充分的敲低效果。例5:含有环状tnna的核酸分子二聚体的敲低效果(4)对将其他核酸分子作为靶标的含有环状tnna的核酸分子二聚体的敲低效果进行了研究。简单而言,将a549细胞以2.5×104个/孔的密度接种于6孔培养板,将表8所示的各核酸分子二聚体的最终浓度设为20nm,除此以外,与例2同样地操作,基于mrna残留率对各核酸分子二聚体的敲低效果进行评价。结果示于表8。数值为将各测定值基于gapdh的测定值归一化、且将仅加入了转染试剂的试剂对照(mock)设为100的情况下的相对值。[表8]表8将gfp作为靶标的核酸分子二聚体的mrna残留率由上表所示的结果可知,含有环状tnna的核酸分子二聚体即使针对不同的靶核酸分子,也可获得充分的敲低效果。例6:利用含有环状tnna的核酸分子二聚体避免脱靶效应通过将含有环状tnna的核酸分子二聚体和与其对应的tcna环化核酸分子二聚体的敲低效果进行比较,对有无因tnna导致的脱靶效应进行评价。使用cl-4作为含有环状tnna的核酸分子二聚体,使用lc-1作为tcna环化核酸分子二聚体,与例2同样地测定mrna残留率。结果示于下表。mrna残留率的表示方式与例2同样。另外,将1nm的浓度下mrna残留率显示为40%以下的情况判定为合格(○)。[表9]表9由含有环状tnna的核酸分子二聚体导致的脱靶效应由上述结果可知,使诱导rna沉默的核酸分子(tcna)呈环状、使tnna呈直链状时,mrna残留率并未降低,反之,使tcna呈直链状、使tnna呈环状时,mrna残留率降低。由此暗示了在将tnna环化(tcna为直链状)的情况下,能够抑制源于tnna的脱靶效应。例7:利用含有环状tnna的核酸分子二聚体避免pkr磷酸化评价了利用含有环状tnna的核酸分子二聚体能否避免pkr的激活(磷酸化)。将a549细胞以0.25×105个/孔的密度接种于6孔培养板,在含有10%fbs的dmem培养基中于37℃、5%co2下孵育。第二天,按照制造商的方案,将在opti-mem(sigma)培养基中含有lipofectaminernaimax转染试剂(thermofisherscientific)和各核酸分子二聚体的试样以核酸分子二聚体的最终浓度成为20nm的方式添加至a549细胞培养物中,转染5小时。转染后,将培养基置换为含有10%fbs的dmem培养基。在自转染开始24小时后,使用一部分培养物,与例2同样地操作,测定plk1的mrna残留率。另外,在自转染开始72小时后,将培养物溶解于裂解缓冲液中提取蛋白质,出于检测磷酸化pkr的目的而供于western印迹法。裂解缓冲液的组成为在合计10ml中含有下述成分:1%np-40(np-40alternativeproteingradedetergent,10%溶液,过滤灭菌,calbiochem)100μl、1mtris-hcl(ph7.5)500μl、5mnacl300μl、0.5medta(ph8.0)20μl、透析水(dialyzedwater)9.08ml、complete,mini,edta-free(roche)1片、phosstop(roche)1片。将印迹膜用5%的phosphoblocker封闭试剂(cellbiolabs,akr-103)进行封闭,使其与一抗(抗p-pkr抗体(ab32036,1/1000稀释)、抗pkr抗体(ab32052,1/1000稀释)及抗gapdh抗体(ab8245,1/5000稀释))反应、并接着与二抗(ecl抗兔igg抗体,1/4000稀释)反应,使用amershameclprimewestern印迹法检测试剂(gehealthcare,rpn2232)检测条带。mrna残留率的结果示于表10,western印迹法的结果示于图6。需要说明的是,表中,mrna残留率用将未处理组(nt)中的mrna的残留率作为100%的情况下的比率(%)来表示,将20nm的rna浓度下mrna残留率kd效率显示为25%以下的情况判定为合格(○)。[表10]表10基于含有环状tnna的核酸分子二聚体的mrna残留率由图6的结果可知,使含有环状tnna的核酸分子二聚体发挥作用的细胞中的pkr的磷酸化的程度与对应的直链状核酸分子二聚体相比明显更小。例8:利用含有环状tnna的核酸分子二聚体避免tlr3途径激活通过各种方法,评价了利用含有环状tnna的核酸分子二聚体能否避免tlr3途径的激活(相关基因的表达诱导)。(1)基于定量pcr的评价将a549细胞以0.25×105个/孔的密度接种于6孔培养板,在含有10%fbs的dmem培养基中于37℃、5%co2下孵育。第二天,按照制造商的方案,将在opti-mem(sigma)培养基中含有lipofectaminernaimax转染试剂(thermofisherscientific)和各核酸分子的试样以核酸分子二聚体的最终浓度成为20nm的方式添加至a549细胞培养物中,转染6小时。转染后,将培养基置换为含有10%fbs的dmem培养基。在自转染开始24小时后,使用一部分培养物,与例2同样地操作,测定与tlr3途径相关的ccl5、cxcl10、ifnα1、ifnβ1、il6、il10及tnf的表达量。作为对照,使用了未处理对照(nt)及仅加入了转染试剂的试剂对照(mock)。由图7所示的结果可知,含有环状tnna的核酸分子二聚体与传统的sirna、非对称直链状核酸分子二聚体相比,tlr3途径相关基因的表达诱导更少。(2)基于pcr阵列的评价将a549细胞以0.25×105个/孔的密度接种于6孔培养板,在含有10%fbs的dmem培养基中于37℃、5%co2下孵育。第二天,按照制造商的方案,将在opti-mem(sigma)培养基中含有lipofectaminernaimax转染试剂(thermofisherscientific)和各核酸分子的试样以核酸分子二聚体的最终浓度成为20nm的方式添加至a549细胞培养物中,转染5小时。转染后,将培养基置换为含有10%fbs的dmem培养基。在自转染开始24小时后,使用rneasyminikit(qiagen)提取rna,使用rt2firststrandkit(qiagen)进行逆转录反应后,使用rt2profilerpcrarray(qiagen)实施实时pcr,测定与tlr3途径相关的基因的mrna表达量。下表示出了关于在nt与各核酸分子之间表达量存在2倍以上的差异的基因的结果。需要说明的是,数值为使用管家基因(actb/b2m/gapdh/hprt1)的平均值进行校正、且将未处理对照(nt)设为1而得到的倍率。[表11]表11tlr3途径相关基因的mrna表达量由该表所示的结果可知,在使含有环状tnna的核酸分子二聚体发挥作用的细胞中,在tlr3途径下游表达的基因(ccl2、ccl5、il1b)的表达与传统的sirna、非对称直链核酸分子二聚体相比没有被诱导。(3)基于western印迹的评价将a549细胞以0.25×105个/孔的密度接种于6孔培养板,在含有10%fbs的dmem培养基中于37℃、5%co2下孵育。第二天,按照制造商的方案,将在opti-mem(sigma)培养基中含有lipofectaminernaimax转染试剂(thermofisherscientific)和各核酸分子二聚体的试样以核酸分子二聚体的最终浓度成为20nm的方式添加至a549细胞培养物中,转染6小时。在自转染开始6小时后,与例7同样地将培养物溶解于裂解缓冲液中提取蛋白质,出于检测与tlr3途径相关的蛋白质的磷酸化的目的而供于western印迹法。将印迹膜用5%的phosphoblocker封闭试剂(cellbiolabs,akr-103)进行封闭,使其与一抗(抗p-tlr3抗体(nbp2-24904,1/1000稀释)、抗tlr3抗体(ab62566,1/1000稀释)、gapdh(ab8245,1/5000稀释)、抗p-stat1抗体(sc-8394,1/200稀释)、抗stat-1抗体(sc-464,1/200稀释))反应、并接着与二抗(ecl抗兔igg抗体、1/4000稀释,ecl抗小鼠igg抗体、1/2000稀释)反应,使用amershameclprimewestern印迹法检测试剂(gehealthcare,rpn2232)检测条带。由图8所示的结果可知,在使含有环状tnna的核酸分子二聚体发挥作用的细胞中,与tlr3途径相关的蛋白质(tlr3、stat1)的磷酸化与传统的sirna、非对称直链核酸分子二聚体相比没有被诱导,因此,本途径未被激活。例9:核酸外切酶耐性的评价评价了环化核酸分子对于核酸外切酶的稳定性。向核酸外切酶溶液(rnaser,epicentre,4.5u)中加入环状或直链状tnna,使其成为20μm,并使总量为100μl。将样品于37℃孵育,在经过0、5、10、20及40分钟后分别回收样品的一部分,于-80℃保存。回收全部样品后,将各样品注入20%变性聚丙烯酰胺凝胶,于200v电泳70分钟。将凝胶用0.5μg/ml的溴化乙锭染色15分钟,使用uv来评价条带量。由图9所示的结果可知,与直链状核酸分子相比,环状核酸分子对于核酸外切酶的耐性明显更高。例10:含有环状tnna的核酸分子二聚体的敲低效果(5)对将其他核酸分子作为靶标的tnna环化核酸分子二聚体的敲低效果进行了研究。作为核酸分子二聚体,使用了将mt1mmp作为靶标的表12~表13所示的核酸分子二聚体。各核酸分子二聚体使用与例1同样的方法制备。[表12]表12tnna及tcna的序列[表13]表13核酸分子二聚体的构成使用mda-mb231作为细胞,使用表12~表13所示的核酸分子二聚体作为核酸分子二聚体,将mt1mmp的表达量作为测定对象,除此以外,与例2同样地操作,对由前述核酸分子二聚体带来的mt1mmp的敲低效果进行了评价。结果示于表14。表中,mrna残留率用将未处理组(nt)中的mrna的残留率作为100%的情况下的比率(%)来表示,将10nm的rna浓度下的mrna残留率为30%以下的情况判定为合格(○)。[表14]表14各种核酸分子二聚体的mrna残留率试样名称mrna残留率(%,nt=100)评价cl-0125.7○ll-019.0○如上所述,可知由含有环状tnna的核酸分子二聚体带来的敲低效果不限于特定的基因。例11:包含mirna的序列的含有环状tnna的核酸分子二聚体的敲低效果对包含mirna的核苷酸序列的tnna环化核酸分子二聚体的敲低效果进行了研究。作为mirna的核苷酸序列,使用了hsa-mir-34a-5p的序列。各核酸分子二聚体使用与例1同样的方法制备。使用的序列示于表15,各核酸分子二聚体的构成示于表16。[表15]表15tnna及tcna的序列[表16]表16核酸分子二聚体的构成名称tnnatcna长度(tn/tc)结构ll-02tn-03tc-0319/22直链状,tcna具有3’末端突出cl-02tn-04tc-0319/22环状,tcna具有3’末端突出cl-03tn-04tc-0419/22环状,tcna具有3’末端突出使用hct116作为细胞,使用表15~表16所示的核酸分子二聚体作为核酸分子二聚体,将arhgap1的表达量作为测定对象,除此以外,与例3同样地操作,对由前述核酸分子二聚体带来的arhgap1的敲低效果进行了评价。已知arhgap1为mir-34a的靶基因,利用mir-34a可抑制其表达(matsui等,molther.2016;24(5):946-55)。如图10的结果所示,与未处理组(nt)相比,任一种含有环状tnna的核酸分子二聚体均显示出显著的敲低效果。本领域技术人员理解,可在不脱离本发明的精神的前提下施以多种多样的改变。因此,应理解,本说明书中记载的本发明的方式仅为示例,其并未意图对本发明范围加以限制。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1