一种核酸检测前处理自动化处理装置的制作方法
本发明属于核酸分子检测领域,具体涉及一种核酸检测前处理自动化处理装置。本发明实现了核酸检测前处理全自动,即自动实现核酸提取、扩增、纯化等前处理,处理完毕样本可经外部配套测序仪进行检测,本发明简化了试验流程,减少了出错机会,提高了整体检测的稳定性。
背景技术:
高通量测序技术是最近十年开始发展的新型分子检测技术。市场上主流的高通量测序仪主要由Illumina、ThermoFisher等提供,任何一种高通量测序平台在进行检测前都会首先要求从生物样本中抽提DNA或RNA,然后把待测DNA样本构建测序文库,即在待测DNA两端连接上测序仪通用的接头DNA序列,在整个构建文库的过程中添加了不少工具酶和缓冲体系,不利于后期的反应,所以需要进行一次DNA纯化操作去除各种酶和缓冲液,从而让该待测片段DNA可以在测序仪不同的芯片上进行测序反应。
常规的高通量测序检测前处理包括核酸提取,文库构建、纯化三个步骤。
核酸提取。核酸检测首先要进行样本核酸提取。常见的方法有乙醇沉淀法、硅胶柱结合法、玻璃珠法、磁性颗粒结合分离法。所有方法的基本原理就是裂解样本——结合——清洗——洗脱等四个步骤。单一样本整个过程约需40分钟。
文库构建。文库构建的基本概念是在待测DNA加上和后续测序仪器配套的DNA接头。基本流程是:1.末端补平;2.碱基最后增加一个A;3.连接接头;4.PCR扩增。由于每一步都有独立的酶和缓冲体系,所以在常规的高通量测序文库构建过程中,每一次反应中间都需要进行基于硅胶柱或磁性颗粒的DNA纯化。也就说常规的高通量测序文库构建流程有:1.末端补平;2.纯化;3.碱基最后增加一个A;4.纯化;5.连接接头;6.纯化;7.PCR扩增等7个步骤。
纯化。文库构建过程中加入了各种工具酶,DNA溶液和磁性颗粒、硅胶膜、玻璃珠等介质结合,清洗液清洗两次去除各种杂质,最终用洗脱液洗脱DNA。
自此完成一个从原始样本到最终测序文库的所有试验环节。整个试验流程需要5~8个小时,在每个实验环节都需要标记试管以免弄错样本,费时费力。
针对上述的复杂试验步骤,市场上有一些仪器代替人工操作。由于高通量测序为目前市场上全新的技术,有针对每个步骤的单一设备,比如核酸提取可以有多种类型的核酸提取仪,文库构建可以通过自动移液工作站完成,文库的纯化可以由手工完成,也可以通过自动移液工作站完成。核酸提取仪,一次可实现12-96个不等的核酸提取。操作者需要把样本放入仪器中,40分钟后,取出提取完的样本,标记后以待后续实验使用。核酸前处理,反应配置、温控、混匀可由移液工作站实现,开始前操作者把需要的配套试剂放置在工作站台面上,设置好程序,标记好投入产出的试验管位置,开始运行。由于移液工作站为开放平台,在整个多步试验操作过程中,操作者需要不定期进行96孔板封膜、开膜,或者不定期进行大量的管盖开闭工作,虽然一部分工作由工作站来完成,但整体仍然需要人工大量介入,无法实现整个过程的无人值守,多个步骤需要人工来标记、排序、设置。同时由于试验一旦开始,无法再临时增加或改变试验流程,一旦临时有样本需要处理,或者改变试验流程,将对整体参与试验的样本产生影响。
技术实现要素:
本发明的目的在于克服现有技术中存在的缺陷,提供一种核酸检测前处理自动化装置,可实现核酸检测前处理的全自动,包括提取、文库构建、产物纯化,最终产物可直接用于高通量测序,全程无人值守。
一种核酸检测前处理自动化装置,其特征在于,包括
用于放置样本和前处理试剂的试剂盘;
用于放置试剂盘的底座,底座上设有温控模块和混匀模块;
用于实现磁性颗粒分离、清洗和洗脱的磁力分选模块;
用于转移试剂盘内试剂的移液装置,移液装置设有移液模块和移液枪头;
用于支撑移液装置的移动导轨平台;和
用于控制温控模块、旋转模块、混匀模块、磁力分选模块和移液模块运行的主机。
本发明的核酸检测前处理自动化装置,在一个独立试剂盘内全自动运行核酸提取、建库、纯化等处理,每台装置作为一个单元独立封闭运行,可通过串联方式无限扩展数量,实现多个样品同时检测。
进一步地,铝箔封膜上设置管道支架,管道支架和盖板之间设有硅胶层。在进行核酸检测自动化前处理的时候,先移除试剂盘的盖板,装置的移液装置(例如移液枪头)可直接戳破硅胶和铝箔封膜,进入腔室进行移液操作,操作结束后,移液装置退出铝箔和硅胶。铝箔封膜会留有穿透孔,而硅胶回弹后,使试剂孔仍然处于密封状态,试剂孔内试剂不会挥发影响整体试验。
所述试剂盘为圆形、方形或长方形,也可以是其他不规则形状。试剂孔可根据试剂盘的形状作优化排布。多孔试剂盘优选采用一次性独立试剂盘,待检测样本加入试剂盘后在该试剂盘内完成从初始样本、核酸提取、核酸检测前处理的全部流程。
所述核酸测序前处理试剂包括核酸提取试剂、文库构建试剂和DNA纯化试剂,包括但不限于核酸末端补平、加A、连接、纯化等步骤试剂。
所述试剂孔包括裂解孔、磁珠孔、提取孔、文库构建孔、PCR反应孔、纯化孔、最终样本孔和废液孔。
所述底座上设有旋转模块。试剂盘可通过底座上的旋转模块进行转动、移动。
所述移液模块包括移液泵。
所述磁力分选模块包括设于底座和试剂盘旁边的活动磁铁。
本发明装置具有温控模块、移液模块、混匀模块和磁力分选模块,可实现温控、移液、混匀、磁力分选功能。混匀模块使装置内部可实现水平涡旋、上下垂直混匀样本。温控模块可以在一个或多个步骤,对试剂盘内试剂进行加热、低温、升变温处理。移液模块看实现在试剂盘不同试剂孔之间液体的转移,可由仪器内置或试剂盘内含一个或多个移液枪头实现。磁力分选模块可通过设置电磁铁或永磁铁实现磁性颗粒分离、清洗、洗脱。
在一个具体实施中,核酸检测前处理自动化装置采用一次性丢弃的试剂盘,试剂盘内含有提取试剂、文库构建试剂、DNA纯化试剂。样本加入试剂盘样本孔以后,仪器内部移液加入裂解液;利用仪器进行混匀10分钟;移液加入结合液和磁珠,混匀10分钟;利用磁力分选模块吸附磁珠,移液模块去除上清,加入500ul清洗液,混匀磁珠2分钟,磁力分选去除清洗液,重复三次;加入30ul洗脱液和磁珠混合,60度加热5分钟;移液模块移液上清去文库构建孔;移液加入末端补平酶,37度30分钟,75度灭活20分钟;移液加入DNA接头,DNA连接酶,20度30分钟,75度20分钟灭活;移液去纯化孔,加入磁珠和纯化结合液,混匀10分钟;加磁力分选,去除上清,500ul清洗液清洗两次磁珠;50ul洗脱液加入磁珠,60度加热5分钟,移液DNA到最终样本室,样本核酸前处理结束。
本发明实现了在一个封闭的独立试剂盘,全自动无人值守的核酸检测前处理的自动化,操作者把样本放入试剂盘后就可让仪器自动运行,产物可直接用于后期测序分析。大大简化了试验流程,避免了常规手工操作的繁琐,也避免了利用核酸提取仪、移液工作站等仪器配套使用时候,需要多次标记试管,人工来移动试管等环节,从试验流程上杜绝了样本混淆的可能。
本发明的核酸检测前处理自动化装置具有以下优点:
(1)全自动。仪器全自动实现了核酸检测前处理全自动,包括核酸提取、末端补平、加A、连接接头、产物纯化等步骤。全自动无人值守,整个过程手工操作不超过5分钟,把样本放入试剂盘,试剂盘放入仪器内即可全自动运行。
(2)封闭。试剂盘在一个封闭体系内运行,保证了样本不会混淆,也保证了样本之间不会互相污染。
(3)快速。由于通过仪器实现的不同试验步骤之间的直接连接,减少了多个环节需要的样本标记工作,大大加快了整体试验速度。
(4)可编程。由于仪器具有混匀、移液、温控、磁力分选等模块,因此设备可根据实际需要进行再次开发,扩展性大。
(5)通量高。仪器为单一样本一个操作单元,但可通过串联形式无限放大,从而灵活实现高通量操作。
附图说明
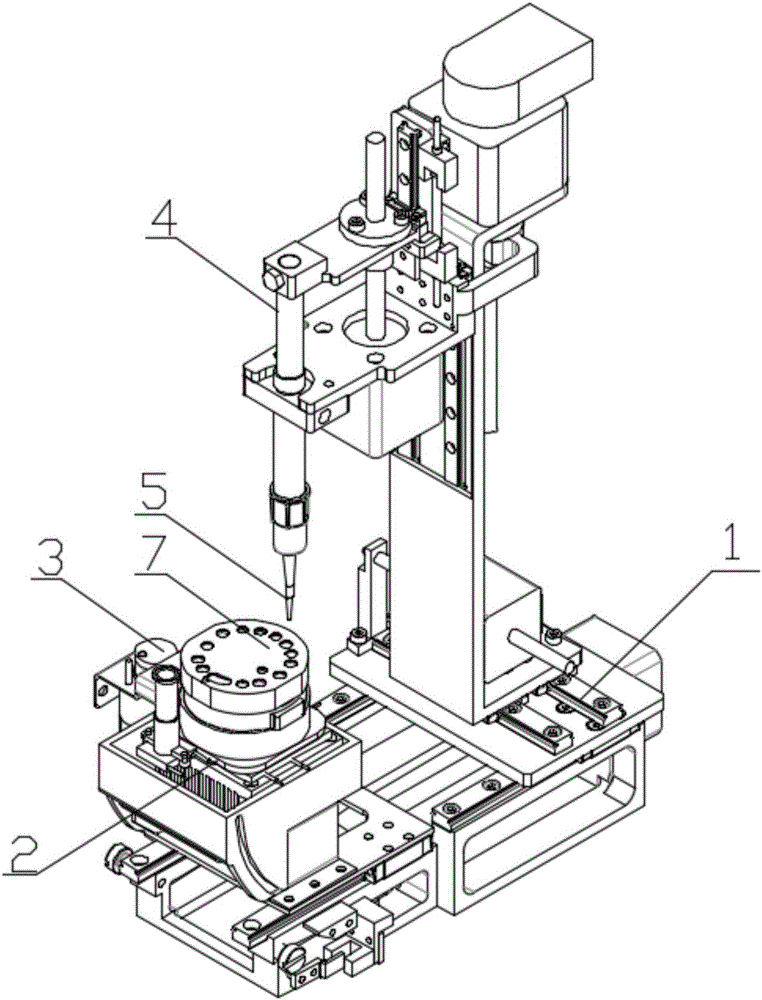
图1是核酸检测前处理自动化装置结构示意图。
图2是试剂盘示意图。
图3是试剂盘局部剖视图。
图4是多个核酸检测前处理自动化装置实现串联扩展示意图。
具体实施方式
实施例1
如图1所示的核酸检测前处理自动化装置,由移动导轨平台1、底座2、活动磁铁3、移液泵4和移液枪头5构成。移液枪头5设于移液泵4上,移液泵可沿移动导轨平台1移动,并通过旋转模块转动。移动导轨平台1通过移液泵和移液枪头在试剂盘上部移动和转动实现移液。底座2对应试剂盘位置具有温控模块。底座2和试剂盘贴合,提供温度控制。试剂盘可通过底座2上的旋转模块进行转动、移动。
如图2-3所示的试剂盘,包括盖板6和试剂托盘7,试剂托盘7上设有若干试剂孔8,试剂孔8内分装有核酸测序前处理试剂,试剂孔开口处设置铝箔封膜9。铝箔封膜9上设置管道支架10,管道支架和盖板之间设有硅胶层11。试剂孔包括:1—裂解孔(6M盐酸胍、20%异丙醇);2—磁珠孔(40ul硅烷化磁珠);3—清洗液(80%乙醇);4—结合液(60%异丙醇);5—洗脱液(纯水pH8.0);6—提取孔;7—文库构建孔;8—末端补平酶混合孔(Klenow DNA聚合酶I,T4多聚核苷酸激酶);9—连接反应混合孔(T4DNA连接酶);10—纯化孔(40ul硅烷化磁珠);11—预留孔;12—最终样本孔;13—废液孔;14—预留孔;15—预留孔。
如图4所示是4个核酸检测前处理自动化装置串联示意图,可根据需要任意串联,实现多个样品同时检测。
实施例2
血浆游离DNA为小片段、碎片化DNA,片段长度100~300bp之间,峰值在160bp左右。1997年,卢煜明教授发现在孕妇外周血浆中含有胎儿的游离DNA,从而开创以游离DNA为检测来源,分析孕妇所怀胎儿是否有染色体异常。血浆中也存在来源于肿瘤细胞的循环肿瘤DNA(ctDNA),ctDNA被广泛用来做肿瘤液态活检,可以无创伤性的早期诊断、伴随诊断、预后随访等。
常规的检测方法是首先由临床样本包括血浆中抽提DNA,进行核酸检测处理、检测三个步骤。完成整个样本检测需要6~13个小时。其中样本核酸提取和检测前处理环节工作繁琐。
采用本发明的核酸检测前处理自动化装置可实现在一个封闭的独立试剂盘,全自动无人值守的核酸检测前处理的自动化,操作者把样本放入试剂盘后就可让仪器自动运行,产物可直接用于后期测序分析。具体操作方法如下:
600ul血浆样本,放入核酸检测前处理自动化装置进行全自动高通量文库构建。
1. 600ul血浆加入试剂盘裂解孔,裂解孔含有1.2ml血浆裂解液(6M盐酸胍、20%异丙醇);
2.混匀模块进行混匀5分钟,移液模块,依次移液600ul至提取孔和磁珠(40ul硅烷化磁珠)结合;
3.活动磁铁实现磁力分选,上清移至废液孔;
4. 500ul清洗液(80%乙醇)清洗磁珠三次,上清移至废液孔;
5. 60ul洗脱液移至提取孔,56度10分钟洗脱DNA;
6. DNA移至建库孔,加入补平酶(DNA聚合酶I、T4多聚核苷酸激酶)混合10ul;
7. 37度30分钟,75度20分钟灭活;
8.加入DNA接头5ul,加入DNA连接酶(T4核苷酸连接酶)混合物20ul;
9.16度20分钟,75度20分钟灭活;
10.移液模块,移取所有的产物至纯化试剂孔,纯化孔含有纯化反应所需要的磁珠;
11.利用移液模块上下混匀样本和磁珠,静置5分钟,上活动磁铁静置5分钟,移液模块移上清至废液孔;
12. 500ul清洗液清洗磁珠两次,上活动磁铁,上清移至废液孔;
13. 40ul洗脱液去纯化孔,洗脱DNA,利用移液模块移液至最终样本孔;
14.产物可直接用于后续的高通量测序检测。
实施例3
转录组测序的研究对象为特定细胞在某一功能状态下所能转录出来的所有RNA的总和,主要包括mRNA和非编码RNA。转录组研究是基因功能及结构研究的基础和出发点,通过新一代高通量测序,能够全面快速地获得某一物种特定组织或器官在某一状态下的几乎所有转录本序列信息,已广泛应用于基础研究、临床诊断和药物研发等领域。
常规的检测方法是首先由临床样本包括全血、血浆中抽提RNA,进行核酸检测处理、检测三个步骤。完成整个样本检测需要6~30个小时。其中样本核酸提取和检测前处理环节工作繁琐。
采用本发明的核酸检测前处理自动化装置可实现在一个封闭的独立试剂盘,全自动无人值守的核酸检测前处理的自动化,操作者把样本放入试剂盘后就可让仪器自动运行,产物可直接用于后期测序分析。具体操作方法如下:
200ul全血样本,放入核酸检测前处理自动化装置实现转录组建库全自动处理。
1. 200ul样本加入试剂盘样本孔以后,移液加入300ul裂解液;
2.混匀模块进行混匀10分钟;
3.移液加入200ul结合液和10ul磁珠,混匀10分钟;
4.利用磁力分选模块吸附磁珠,移液模块去除上清;
5.加入500ul清洗液,混匀磁珠2分钟,磁力分选去除清洗液,重复三次;
6.加入30ul洗脱液和磁珠混合,60度加热5分钟;
7.移液模块移液上清至提取孔;
8.提取孔含有30ul oligo dT的磁珠,65度30分钟;
9.磁力分选,去除上清,500ul清洗液清洗,磁力分选去除上清;
10. 30ul洗脱液加入提取孔,60度加热5分钟,移液上清cDNA去文库构建孔;
11.移液加入末端补平酶和dATP,37度30分钟,65度灭火5分钟;
12.移液加入DNA接头,连接酶,20度30分钟,65度5分钟灭活;
13.加入10ul磁珠和200ul纯化结合液,混匀10分钟;
14.加磁力分选,去除上清,500ul清洗液清洗两次磁珠;
15. 50ul洗脱液加入磁珠,60度加热5分钟;
16.移液DNA到最终样本孔,本自动化处理装置试验结束;
17.最终DNA可以直接用于后续高通量测序检测。
- 还没有人留言评论。精彩留言会获得点赞!