一种Cu(I)配位聚合物及其制备方法与应用与流程
本发明属于多孔配位聚合物技术领域,尤其涉及一种cu(i)配位聚合物,并涉及该cu(i)配位聚合物的制备方法,还公开了该cu(i)配位聚合物的应用,以及一种光催化剂。
背景技术:
金属有机骨架材料是一类新型的有机无机杂化材料,由于其晶体结构有序,比表面积大,孔径可调节等诸多优点,已经在气体存储与分离、分子传感、光电材料、药物载体、催化剂等领域展现了重要的应用前景。
随着人们越来越关注能源危机和环境污染等问题,寻找可持续和清洁能源就成为了科学家们研究的必然趋势。特别是,近几年来,金属有机骨架材料已经被广泛用作光催化剂用于光解水制氢。相当多的一部分金属有机骨架材料表现出类半导体行为,其规则的孔结构有利于抑制光生电子和空穴的复合,因此显著提高光催化活性。
然而,现有的光催化剂在光解水制氢时,往往需要结合光敏剂和/或助催化剂一并使用,从而成本高昂,且现有的光催化剂本身的催化活性还不够理想。
技术实现要素:
本发明旨在克服现有技术中的上述技术缺陷,并提供一种新的多孔铜配位聚合物,用于光解水制氢,以达到降低催化成本,提高催化效率的目的。
具体地,本发明第一方面提供了一种cu(i)配位聚合物,其具有以下分子式:
{[cui(h2po4)(dpe)]5(dpe)0.5(h2o)7}n;
其中,n为大于1的整数,dpe为1,2-二(4-吡啶基)乙烯,其结构式如下所示:
并且,所述cu(i)配位聚合物以一价cu为中心,每个cu周围连接两个dpe有机配体和一个h2po4-;可见,其构成了三配位构型。
众所周知,磷酸配体的结构式如下:
优选地,所述cu(i)配位聚合物的框架结构的分解温度为220℃。
并且,本发明第二方面提供了一种第一方面所述的cu(i)配位聚合物的制备方法,其包括以下步骤:
s1:向反应容器中加入cuo,1,2-二(4-吡啶基)乙烯和去离子水,搅拌以混合均匀;
s2:接着,加入h3po4水溶液,继续搅拌,并密封该反应容器;
s3:在高温下进行水热反应;
s4:后处理,即得所述cu(i)配位聚合物的单晶产物。
其中,所述cu(i)配位聚合物的单晶产物的形貌为橙红色针状晶体,属于单斜晶系,c2/c空间群,晶胞参数
可见,发明人选择以低成本的过渡金属铜的氧化物为原料,并以具有多个配位点的1,2-二(4-吡啶基)乙烯(dpe)有机配体和微量的磷酸成功合成了所述cu(i)配位聚合物。因此,该cu(i)配位聚合物易于制备,同时,所述制备方法的反应条件温和,从而易于控制,并且所制得的产物的热稳定性较好。
优选地,在上述制备方法中,所述h3po4水溶液的质量浓度为85%。
优选地,在上述制备方法中,所述水热反应的温度为100至200℃。
优选地,在上述制备方法中,所述水热反应的持续时间为24~96小时。
优选地,在上述制备方法中,所述后处理包括以下:
自然冷却至室温,得到橙红色针状晶体,用去离子水反复洗涤,自然晾干。
优选地,在上述制备方法中,cuo,1,2-二(4-吡啶基)乙烯与h3po4的摩尔比为1:1:1。
此外,本发明第三方面提供了第一方面所述的cu(i)配位聚合物的应用,具体地,该{[cui(h2po4)(dpe)]5(dpe)0.5(h2o)7}n用于光催化分解水以制备氢气。
本发明第三方面还提供了一种光催化剂,所述光催化剂为第一方面所述的cu(i)配位聚合物。
总之,本发明所提供的技术方案至少具有以下有益效果:
本发明提供的cu(i)配位聚合物的制备方法的反应条件温和,易于控制,并且依据该制备方法制得的产物的热稳定性较好;并且,本发明提供的cu(i)配位聚合物可以作为一种光催化剂,其催化活性较高,特别是,其在无需任何光敏剂和助催化剂的条件下能够将水分解为氢气,可见,其制备和应用成本均较低;因此,本发明所述的cu(i)配位聚合物在光催化制氢方面具有广阔的应用前景。
附图说明
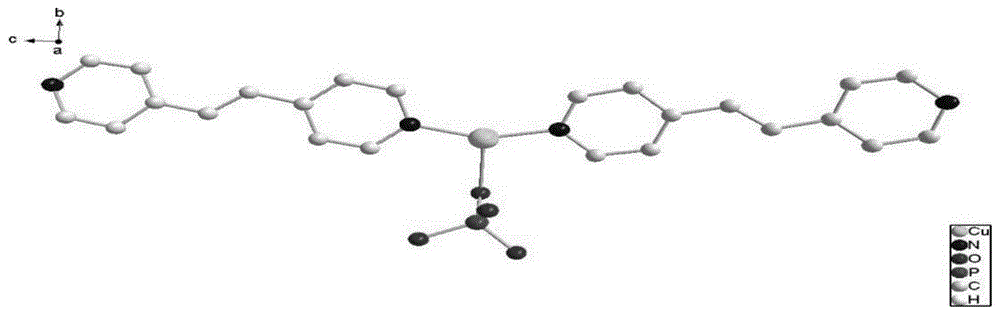
图1为本发明所述的cu(i)配位聚合物的金属中心铜的配位环境图;
图2为本发明所述的cu(i)配位聚合物的一维链状图;
图3为本发明所述的cu(i)配位聚合物由一维链状图所拓扑的三维结构图;
图4为依据实施例3制备的cu(i)配位聚合物的粉末的xrd图与模拟所述cu(i)配位聚合物的xrd图;
图5为依据实施例3制备的cu(i)配位聚合物的热重曲线图;
图6为依据实施例3制备的cu(i)配位聚合物的固体紫外光谱图;
图7为依据实施例1制备的cu(i)配位聚合物用作光催化剂进行光解水的产氢图;其中,横坐标为辐照时间,纵坐标为单位质量催化剂的产氢量。
具体实施方式
下面结合具体实施方式对本发明作进一步阐述,但本发明并不限于以下实施方式。下述实施例中的实验方法,如无特殊说明,均为常规方法;下述实施例中所用的原料、试剂等,如无特殊说明,均可从公开商业途径获得。
根据本发明所述的cu(i)配位聚合物,其具有以下分子式:
{[cui(h2po4)(dpe)]5(dpe)0.5(h2o)7}n;
其中,n为大于1的整数,dpe为1,2-二(4-吡啶基)乙烯;
并且,所述cu(i)配位聚合物以一价cu为中心,每个cu周围连接两个dpe有机配体和一个h2po4-。
在一个优选实施方式中,cu(i)配位聚合物的制备方法包括以下步骤:
s1:向耐高温玻璃瓶中加入cuo,1,2-二(4-吡啶基)乙烯和去离子水,搅拌以混合均匀;
s2:接着,加入85%h3po4水溶液,继续搅拌,并密封该耐高温玻璃瓶;
s3:在高温下进行水热反应;
s4:后处理,即得所述cu(i)配位聚合物的单晶产物。
在一个进一步优选的实施方式中,所述水热反应的温度为100至200℃。
在一个进一步优选的实施方式中,所述水热反应的持续时间为24~96小时。
在一个进一步优选的实施方式中,所述后处理包括以下步骤:
自然冷却至室温,得到橙红色针状晶体,用去离子水反复洗涤,自然晾干。
在一个进一步优选的实施方式中,cuo,1,2-二(4-吡啶基)乙烯与h3po4的摩尔比为1:1:1。
在一个优选实施方式中,将所述cu(i)配位聚合物用作光催化剂,以制备氢气,具体包括以下步骤:
p1:称取一定量的光催化剂并加入到玻璃反应瓶中;
p2:向该玻璃反应瓶中加入10%的乳酸水溶液,超声一段时间;
p3:将该玻璃反应瓶连接到连通气相色谱仪的多通道反应器,密闭抽真空,进行光照,以制备氢气。
实施例1
准确称量0.265gcuo,0.606g1,2-二(4-吡啶基)乙烯(dpe),放入耐高温玻璃瓶中,向玻璃瓶中加入10ml的去离子水,搅拌一段时间使其混合均匀;再向玻璃瓶中加入227μl85%h3po4溶液,继续搅拌一段时间。将其密封后在120℃进行水热反应,反应36h后,待玻璃瓶自然冷却至室温,得到橙红色针状晶体,用去离子水反复洗涤,自然晾干得到纯度较高的单晶样品。
实施例2
准确称量0.265gcuo,0.606g1,2-二(4-吡啶基)乙烯(dpe),放入耐高温玻璃瓶中,向玻璃瓶中加入20ml的去离子水,搅拌一段时间使其混合均匀;再向玻璃瓶中加入227μl85%h3po4溶液,继续搅拌一段时间。将其密封后在140℃进行水热反应,反应48h后,待玻璃瓶自然冷却至室温,得到橙红色针状晶体,用去离子水反复洗涤,自然晾干得到纯度较高的单晶样品。
实施例3
准确称量0.265gcuo,0.606g1,2-二(4-吡啶基)乙烯(dpe),放入耐高温玻璃瓶中,向玻璃瓶中加入30ml的去离子水,搅拌一段时间使其混合均匀;再向玻璃瓶中加入227μl85%h3po4溶液,继续搅拌一段时间。将其密封后在160℃进行水热反应,反应72h后,待玻璃瓶自然冷却至室温,得到橙红色针状晶体,用去离子水反复洗涤,自然晾干得到纯度较高的单晶样品。
实施例4
取实施例3制得的cu(i)配位聚合物进行表征,具体包括:
(1)cu(i)配位聚合物晶体结构测定
在显微镜下选取尺寸合适的单晶,在室温下用经石墨单色化的mokα射线
表1cu(i)配位聚合物晶体的主要参数
(2)cu(i)配位聚合物单晶纯度的表征
具体地,图4清楚地示出了依据实施例3制备的cu(i)配位聚合物的粉末的xrd图与模拟所述cu(i)配位聚合物的xrd图;可见,实测图谱与模拟图谱完美地匹配,从而表明所制备的cu(i)配位聚合物的纯度高。
(3)cu(i)配位聚合物的热稳定性表征
具体地,图5示出了依据实施例3制备的cu(i)配位聚合物的热重曲线,该图谱显示其在室温至150℃范围内失重6%(对应配位聚合物中客体水分子的缺失);220-300℃范围内失重26%(对应配位聚合物中部分dpe配体的缺失);320℃后该配位聚合物的结构完全分解掉。
(4)cu(i)配位聚合物的固体紫外表征
具体地,图6示出了依据实施例3制备的cu(i)配位聚合物的固体紫外光谱图,可见分别在300nm,450nm处出现较强的吸收峰,分别归属于有机配体吡啶环中的π→π*电子跃迁和金属-配体之间的d→π*电荷转移(mlct)。
应用实施例
此外,发明人还将依据实施例1制备的cu(i)配位聚合物用作光催化剂进行光解水,以制备氢气,具体包括以下步骤:
p1:称约20mg的光催化剂并加入到玻璃反应瓶中;
p2:向该玻璃反应瓶中加入30ml10%的乳酸水溶液,超声一段时间;
p3:将该玻璃反应瓶连接到连通气相色谱仪的多通道反应器,密闭抽真空,进行光照,以制备氢气;设定每一小时采一次样,取五个样,记录数据。
参见图7,可见,在使用该cu(i)配位聚合物作为光催化剂,且乳酸作为牺牲剂的条件下,5个小时的产氢量为3.5mmol/g,换算成光催化剂活性为0.71mmol·g-1·h-1。
此外,发明人还实施了一系列平行试验,以比较光催化剂活性的强弱,其中,第①~⑧行为近几年来一些典型的配位聚合物光催化产氢活性的实验数据,第⑨行则为上述应用实施例的数据,具体如下表2所示:
由此可见,本发明所述的cu(i)配位聚合物的光催化活性较高,而且其在无需任何光敏剂和助催化剂的条件下就能够将水分解为氢气。
以上对本发明的具体实施例进行了详细描述,但其只是作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行的等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明的精神和范围下所作的均等变换和修改,都应涵盖在本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!