一种冠醚类化合物及其应用的制作方法
本发明属于有机合成
技术领域:
,具体涉及一种冠醚类化合物及其应用,其作为胶粘接,应用于水下粘附玻璃、有机玻璃、金属、聚四氟乙烯板等一系列材质,是一种操作方便、粘附速度快、可防水、粘附能力强、可重复使用、无有机溶剂、绿色环保的胶粘剂。
背景技术:
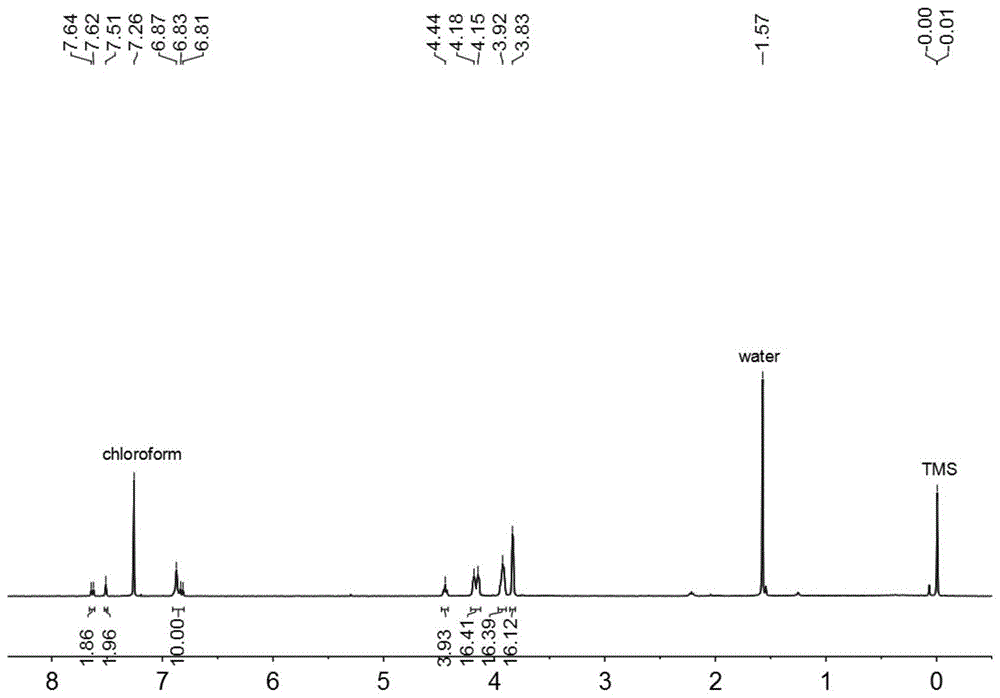
:胶粘剂是一种能将两种材料的表面粘合在一起,并能防止脱落的一类材料,多为高分子化合物和各类辅助材料组成。胶粘剂的粘合方式可以是化学粘合或物理粘合。常见的胶粘剂有瞬间胶、环氧树脂胶、厌氧胶、光固化胶、热熔胶、压敏胶、乳胶等,其被粘物包括木材、玻璃、纸、金属、有机玻璃、塑料、皮革、橡胶等。虽然这些常见的粘合剂具有使用广泛、粘合能力强的特点,但仍然存在许多缺点:1、胶粘剂成分复杂,除了起到粘附效果的高分子组分外,需要添加多种辅助组分;2、为获得良好的溶解性和较好的涂布性能,需要使用有毒有害的有机溶剂;3、通过高分子聚合反应产生粘附效果,硬化速度较慢且无法重复利用。超分子聚合物是一类有小分子化合物组装成的高分子量的自适应材料,通过非共价键连接。超分子聚合物由于其动态可逆性,具有刺激响应性和高粘度等特点,是目前材料科学的研究热点之一。法国科学家costantinocreton报道了一个双脲类超分子聚合物胶粘剂,该胶粘剂能有效粘合铁和pdms表面。然而在粘附过程中需要使用甲苯,同时制备过程复杂,需要在高温高真空条件下制备。技术实现要素:为了解决现有技术中存在的缺陷,本发明的目的是在于提供了一种冠醚类化合物,其结构式如式一所示:式一中,y为o或s,r1为h或r2为h或其中x为o,s或nh,rm为选自以下取代基中的一种:其中,a′和a″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或a′和a″均为h;b′和b″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或b′和b″均为h;c为h、卤素、no2、nh2、oh或och3;n为1、2、3、4、5或6。优选的,式一中,y为o或s,r1为r2为其中x为o、s或nh,rm为选自以下取代基中的一种:其中,a′和a″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或a′和a″均为h;b′和b″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或b′和b″均为h;c为h、卤素、no2、nh2、oh或och3;n为1、2、3、4、5或6。优选的,式一中,y为o,r1为r2为其中x为o,rm为选自以下取代基中的一种:其中,a′和a″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或a′和a″均为h;b′和b″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或b′和b″均为h;c为h、卤素、no2、nh2、oh或och3;n为1、2、3、4、5或6。优选的,rm为其中,a′和a″中的一个为h,另一个为卤素、no2、nh2、oh或och3;或a′和a″均为h;n为1、2、3、4、5或6。优选的,a′和a″均为h;n为2。本发明所述的冠醚类化合物,通过常规的酯化方法即可获得,其反应路线如下:本发明还提供了上述冠醚类化合物的应用,将其加热熔融,作为胶粘剂涂布于粘附表面进行粘结即可。本发明的化合物能够通过加热的方法,形成超分子聚合物。本发明的化合物具有可逆的粘附性能。本发明的冠醚类化合物作为胶粘剂时,其加热熔融的温度可根据实际使用的冠醚类化合物的熔点进行设置,一般加热温度高于熔点10℃左右。与现有技术相比,本发明的优势和有益效果:(1)本发明的冠醚类化合物作为胶粘剂,化学结构明确,成分单一,不需要添加各种辅助物质。(2)本发明的冠醚类化合物作为胶粘剂,粘附过程简单,无需有机溶剂参与,避免了因溶剂的存在,而使被粘物变形、错位和收缩等弊病。(3)本发明的冠醚类化合物作为胶粘剂,硬化速度快,具有防水性,可用于玻璃、金属、纸张、塑料、木头、大理石、瓷砖、聚四氟乙烯乃至各种生物组织(如猪皮)等材料的快速粘合。(4)本发明的冠醚类化合物作为胶粘剂,可以重复利用,粘附能力不变化,是一类绿色环保可循环利用的新型胶粘剂。附图说明图1为本发明实施例1制得的样品的核磁氢谱图;图2为本发明实施例1制得的样品的核磁碳谱图;图3为本发明实施例2制得的样品的核磁氢谱图;图4为本发明实施例2制得的样品的核磁碳谱图;图5为本发明实施例3制得的样品的核磁氢谱图;图6为本发明实施例3制得的样品的核磁碳谱图;图7为本发明实施例4制得的样品的核磁氢谱图;图8为本发明实施例4制得的样品的核磁碳谱图;图9为粘附后的材料的粘附强度测试实物图。具体实施方式下面结合具体实施例,进一步阐述本发明。值得说明,这些实施例仅用于说明本发明,而不用于限定本发明的保护范围。在实际应用中技术人员根据本发明做出的改进和调整,仍属于本发明的保护范围。实施例1双苯并24-冠-8-1,3-丙二酯,分子结构式如下所示:在100毫升的圆底烧瓶中,投入2.0克双苯并24-冠-8-羧酸,0.77克1,3-丙二醇和0.49克4-二甲氨基吡啶,用50毫升二氯甲烷溶解,冰浴搅拌十分钟后加入1.5克1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,室温反应24小时。加入2毫升10%盐酸搅拌5分钟后分液,下层有机层水洗旋干得粗产物,粗产物再通过硅胶柱分离纯化,得到0.68克产物,产率为65%。氢谱、碳谱数据分别如下:1hnmr(400mhz,cdcl3,roomtemperature):δ7.63(d,j=8.0hz,2h),7.51(s,2h),6.87-6.81(m,10h),4.44(s,4h),4.16(d,j=12hz,16h),3.92(s,16h),3.83(s,16h);熔点:118.3-120.2℃;13cnmr(125mhz,cdcl3,roomtemperature):δ166.20,152.99,148.93,148.28,123.95,122.78,121.44,121.42,114.41,114.08,112.03,71.45,71.34,71.26,69.94,69.77,69.62,69.52,69.41,69.35,69.29,61.61,61.53,59.14,31.99,28.35。实施例2双苯并24-冠-8-季戊四酯,分子结构式如下所示:在150毫升的圆底烧瓶中,投入2.0克双苯并24-冠-8-羧酸,0.14克季戊四醇和0.25克4-二甲氨基吡啶,用100毫升二氯甲烷溶解,冰浴搅拌十分钟后加入1.5克1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,室温反应24小时。待反应结束后,加入2毫升10%盐酸搅拌5分钟后分液,下层有机层水洗旋干得粗产物,粗产物再通过硅胶柱分离纯化,得到1.8克产物,产率为88%。氢谱、碳谱数据分别如下:1hnmr(400mhz,cdcl3,roomtemperature):δ7.59(d,j=4.0hz,2h),7.57(d,j=4.0hz,2h),7.47(s,4h),6.87(t,j=4.0hz,16h),6.80(s,2h),6.78(s,2h),4.59(s,8h),4.17-4.13(m,32h),3.94-3.90(m,32h),3.83-3.82(m,32h);熔点:50.4-52.5℃;13cnmr(125mhz,cdcl3,roomtemperature):δ165.71,153.23,148.93,148.37,124.05,122.06,121.44,114.36,114.10,112.06,71.43,71.32,71.25,69.94,69.74,69.58,69.49,69.40,69.34,69.30,63.15,43.21。实施例3双苯并24-冠-8-双季戊四酯,分子结构式如下所示:在100毫升的圆底烧瓶中,投入2.0克双苯并24-冠-8-羧酸,0.21克双季戊四醇和0.34克4-二甲氨基吡啶,用50毫升二氯甲烷溶解,冰浴搅拌十分钟后加入1.91克1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,室温反应24小时。待反应结束后,加入2毫升10%盐酸搅拌5分钟后分液,下层有机层水洗旋干得粗产物,粗产物再通过硅胶柱分离纯化,得到0.32克产物,产率为15%。氢谱、碳谱数据分别如下:1hnmr(400mhz,cdcl3,roomtemperature):δ7.49(d,j=8.0hz,5h),7.42(s,5h),6.87(s,27h),6.70(d,j=8.0hz,5h),4.50(s,11h),4.13(s,48h),3.91(s,48h),3.81(d,j=4.0hz,48h),3.67(s,4h);熔点:42.1-44.2℃;13cnmr(125mhz,cdcl3,roomtemperature):δ165.65,153.00,148.90,148.25,123.84,122.21,121.44,114.23,114.01,111.89,71.45,71.33,71.28,69.94,69.75,69.59,69.40,69.33,69.25。实施例4苯并21-冠-7-季戊四酯,分子结构式如下所示:在100毫升的圆底烧瓶中,投入2.0克苯并21-冠-7-羧酸,0.17克季戊四醇和0.35克4-二甲氨基吡啶,用50毫升二氯甲烷溶解,冰浴搅拌十分钟后加入1.9克1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,室温反应24小时。待反应结束后,加入2毫升10%盐酸搅拌5分钟后分液,下层有机层水洗旋干得粗产物,粗产物再通过硅胶柱分离纯化,得到0.7克产物,产率为35%。氢谱、碳谱数据分别如下:1hnmr(400mhz,cdcl3,roomtemperature)δ7.51(dd,j=8.0,4.0hz,4h),7.45(d,j=4.0hz,4h),6.73(d,j=8.0hz,4h),4.51(s,8h),4.17–4.13(m,16h),3.94–3.89(m,16h),3.81–3.77(m,16h),3.74–3.71(m,16h),3.67(s,32h);13cnmr(125mhz,cdcl3,roomtemperature)δ165.73,153.24,148.40,124.04,122.11,114.54,112.30,71.33,71.21,71.13,71.10,71.00,70.98,70.58,69.61,69.46,69.30,69.13,63.15,43.20。拉伸性能测试:采用熔融后的胶状物和市售pva胶粘剂均匀涂布于材料的粘附表面后,使用微机控制电子万能材料试验机(hy-0580,上海衡翼精密仪器有限公司)进行拉力测试(如图9所示)。取实施例1-4的样品,分别于高于其熔点10℃的条件下加热熔融,将熔融后的胶状物均匀涂布于玻璃的粘附表面,立刻进行粘接,再于室温下进行粘附强度测试,其结果如表1所示:表1不同样品对玻璃的拉伸试验测试结果样品玻璃(psi)实施例1139.2实施例2290.2实施例3244.5实施例4183.2市售pva胶粘剂55.3注:市售pva胶粘剂,购于英国bakerross公司。取实施例2的样品,于60℃的条件下加热熔融,将熔融后的胶状物均匀涂布于聚四氟乙烯的粘附表面,立刻进行粘接,再于室温下进行粘附强度测试,其结果如表2所示:表2不同样品对聚四氟乙烯的拉伸试验测试结果样品聚四氟乙烯(psi)实施例240.2市售pva胶粘剂0注:市售pva胶粘剂,购于英国bakerross公司。取实施例2的样品,于60℃的条件下加热熔融,将熔融后的胶状物均匀涂布于不同材料的粘附表面,立刻进行粘接,再于不同温度下进行粘附强度测试,其结果如表3所示:表3实施例2的样品对不同材料于不同温度下的拉伸试验测试结果当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1