杂交瘤细胞株1G8、抗体及其应用的制作方法
本发明属于生物技术领域,特别是涉及一种杂交瘤细胞株1g8、其产生的能特异性且高亲和力结合人糖化血红蛋白hba1c的单克隆抗体,其制备方法,其可变区序列,及其应用。
背景技术:
糖化血红蛋白a1c是评价糖尿病血糖控制水平的首选指标,并且与糖尿病慢性并发症的发生和发展密切相关。近年来,许多国家糖尿病学会和who推荐将其作为糖尿病的首选诊断标准,拓宽了hba1c的应用范围。hba1c是糖化血红蛋白的主要组成成分,占总糖化血红蛋白(glycatedhemoglobin,ghb)的60%,目前临床定量测定及应用的是hba1c结果。hba1c由葡萄糖的游离醛基与hba的β链n末端缬氨酸的氨基经非酶促结合反应,先形成不稳定的schiff碱(醛亚胺),然后经过amadori(葡糖胺)重排,最后形成稳定的酮胺化合物,其含量主要取决于血糖浓度及血糖与血红蛋白的接触时间,可以反映测定前120d的平均血糖水平,糖化血红蛋白的个体内生物学变异小于2%。目前临床实验室普遍采用的糖化血红蛋白测定方法有多种,按原理可分为两大类:一类是基于糖化与非糖化血红蛋白所带电荷不同,如离子交换层析法、电泳法;另一类是基于糖化与非糖化血红蛋白的结构不同,如免疫法、亲和层析法及酶法等。而在第二类的免疫法测定hba1c体外诊断试剂中则需要使用其单克隆抗体作为核心原料。
目前,这些免疫法检测中所使用的hba1c特异性抗体主要以进口小鼠单抗为主,而国内也有少数抗体公司已开发该抗体,不过市场占有率远不及国外品牌,究其原因主要是国内研发的该抗体特异性和灵敏度不够高,达不到该指标临床检测要求。
技术实现要素:
发明目的:针对上述现有技术,本发明提供了一种杂交瘤细胞株1g8、其产生的抗人hba1c单克隆抗体,其制备方法,其可变区氨基酸序列及核酸序列,以及其应用。
技术方案:本发明所述的杂交瘤细胞株1g8,保藏于中国典型培养物保藏中心,其保藏编号为cctccno:c2019256,地址:武汉市武汉大学,保藏时间:2019年10月29日。
本发明所述杂交瘤细胞株1g8产生的抗人hba1c单克隆抗体。
所述抗人hba1c单克隆抗体,其重链可变区的cdrh1为seqidno:4所示氨基酸序列,cdrh2为seqidno:6所示氨基酸序列,cdrh3为seqidno:8所示氨基酸序列;其轻链可变区的cdrl1为seqidno:12所示氨基酸序列,cdrl2为seqidno:14所示氨基酸序列,cdrl3为seqidno:16所示氨基酸序列。
进一步的,所述抗人hba1c单克隆抗体重链可变区为seqidno:2所示的氨基酸序列,其轻链可变区为seqidno:10所示的氨基酸序列。
所述的抗人hba1c单克隆抗体还包括选自igg1、igg2、igg3、igg4、igm或iga亚型的重链恒定区,以及选自kappa或lambda亚型的轻链恒定区。
进一步优选的,所述抗人hba1c单克隆抗体还包括选自igg2b亚型的重链恒定区,以及选自kappa亚型的轻链恒定区。
本发明还公开了一种编码上述抗人hba1c单克隆抗体的核酸,其重链可变区如seqidno:1所示,其轻链可变区如seqidno:9所示。
进一步的,包含上述抗人hba1c单克隆抗体的检测试剂或者试剂盒也在本发明的保护范围内。所述检测试剂或者试剂盒在体外检测糖化血红蛋白中的应用也在本发明的保护范围内。
本发明以化学合成的糖肽与klh偶联物作为免疫原,免疫balb/c小鼠,待其血清效价达到融合要求,取其脾细胞与sp2/0-ag14骨髓瘤细胞进行细胞融合,通过hat选择性培养基筛选得到能稳定分泌抗人hba1c特异性单克隆抗体的杂交瘤细胞株1g8,经亚克隆化及扩大培养后,在分子水平上进行抗体重、轻链可变区基因的调取。单克隆抗体可通过将杂交瘤细胞注射至小鼠腹腔,取腹水收集后经硫酸铵沉淀法和proteing亲和层析柱纯化获得,并对其抗体特性进行鉴定。
有益效果:本发明成功制备了杂交瘤细胞株1g8,并通过其产生了抗人hba1c单克隆抗体,该抗体亲和力高,特异性强,在免疫比浊平台上能高灵敏度的结合hba1c从而检测人血液中hba1c含量,该抗体可以作为核心试剂应用到其它免疫检测平台,满足临床上运用免疫检测方法检测hba1c的要求。
附图说明
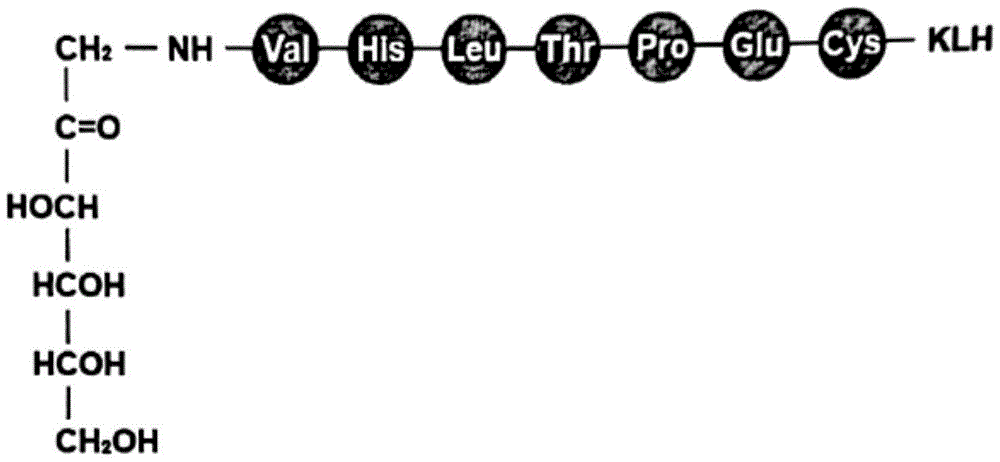
图1:用于动物免疫的合成糖肽与klh偶联物化学结构示意图,val-his-leu-thr-pro-glu六个氨基酸为hba1cn端本身所有的氨基酸,而cys是特意添加在c端用于偶联klh;
图2:3只免疫小鼠在第4次免疫后10天抗血清与hba1c间接elisa反应效价结果,横坐标为抗血清稀释倍数,单位为千,纵坐标为波长450nm下光密度值(od);
图3:3只免疫小鼠在第4次免疫后10天抗血清与hb间接elisa反应效价结果,横坐标为抗血清稀释倍数,单位为千,纵坐标为波长450nm下光密度值(od);
图4:纯化的抗人hba1c单克隆抗体变性还原sds-page电泳结果;
图5:抗人hba1c单克隆抗体亚型鉴定elisa检测结果;
图6:纯化的抗人hba1c单克隆抗体与hba1c和hb间接elisa反应结果,横坐标为纯化抗体浓度,单位为ng/ml,纵坐标为波长450nm下光密度值(od);
图7:两株抗人hba1c单克隆抗体与hba1c及hb的间接elisa反应比较结果,1g8为本发明中抗人hba1c单克隆抗体克隆号,bbi-f7c2为购自bbisolutions的一株抗人hba1c单克隆抗体,横坐标为抗体浓度,单位为ng/ml,纵坐标为波长450nm下光密度值(od)。
具体实施方式
下面结合具体实施例对本申请作出详细说明。
实施例1:免疫原制备
根据人糖化血红蛋白hba1c的结构及其与非糖化和其它形式糖化血红蛋白的结构区别,设计一条糖化多肽序列(如图1),并委托多肽合成公司(浙江昂拓莱斯)进行化学合成。合成的糖肽经质谱分析其分子量为960.07,经高效液相色谱分析其纯度大于95%。合成糖肽再进一步偶联klh以增强免疫原性,最终状态呈干粉,质量为5mg,将其溶解于2ml超纯水,并分装保存在-20℃。
实施例2:动物免疫及抗血清效价测定
选取3只6~8周龄balb/c小鼠(北京斯贝福)同笼饲养,分别编号#1、#2、#3。首次免疫时将实施例1中免疫原与等体积弗氏完全佐剂(sigma)充分混合,超声乳化完全,采取皮下两点和腹腔两点注射,免疫剂量为每只小鼠50μg免疫原,注射体积为0.2ml。间隔14天进行第二次免疫,此次免疫与首次免疫区别在于将弗氏完全佐剂改成弗氏不完全佐剂(sigma)。再间隔14天和28天分别进行第三、第四次免疫,此两次免疫与第二次免疫的区别在于将免疫剂量调整为25μg。第四次免疫后第10天,每只小鼠通过尾静脉采血约0.1ml,4℃放置半小时,然后10000rpm,4℃离心10min,分离血清检测抗血清效价。
检测抗血清效价时采用间接elisa方法,其中间接elisa方法如下:分别用hba1c(meridiana01273h-1)和血红蛋白(hb)(meridiana38192h-2)包被酶标板,2μg/ml,50μl/孔,4℃过夜。次日倾去包被液,用0.05%pbst人工洗板3次后,加入0.5%bsa(sigma)封闭,200μl/孔,37℃,1h。弃去封闭液,0.05%pbst人工洗板3次后,加入自1:1000开始倍比稀释的上述抗血清共7个稀释度,空白对照为pbs,50μl/孔,37℃,1h。0.05%pbst人工洗板3次后,加入1:20000稀释的辣根过氧化物酶标记的山羊抗小鼠igg(h+l)二抗(jacksonimmunoresearch115-035-072),50μl/孔,37℃,1h。0.05%pbst人工洗板5次后,加入显色底物tmb(湖州英创),50μl/孔,室温,10min,最后加入1m硫酸终止反应。在酶标仪上读取od450nm,结果显示与hba1c反应性中,#1小鼠的抗血清效价最高达到1:32000以上,而#2小鼠的抗血清效价达到1:16000以上,#3小鼠的抗血清效价最低为1:2000(如图2),同时3只小鼠的抗血清与hb的反应性均很小(如图3),说明使用实施例1中免疫原免疫小鼠产生的抗体主要为hba1c特异性抗体。
第四次免疫后间隔30天选取抗血清效价最高的#1小鼠进行第五次免疫,此次免疫不使用佐剂,采取尾静脉注射,免疫剂量为25μg免疫原,注射体积为0.2ml。此次免疫间隔4天后进行细胞融合。
实施例3杂交瘤单克隆细胞株的制备
1.细胞融合
细胞融合采用聚乙二醇法。具体操作如下:
1)融合前一周,复苏sp2/0-ag14骨髓瘤细胞(北京北纳)。在细胞融合前两天,扩大培养sp2/0-ag14,使其在融合当天处于对数生长期。
2)进行细胞融合前半小时,预先处理sp2/0-ag14细胞,重悬sp2/0-ag14细胞后计数,取2-3×107个细胞置于37℃水浴锅待用。
3)将待融合的小鼠进行心脏取血,同上操作收集血清,保存在-20℃,可做融合后筛选的阳性对照。断颈处死小鼠,浸泡于75%酒精中,转移到细胞房。取脾脏进行研磨,经70μm筛网过滤制成单细胞悬液。
4)将预先处理好的sp2/0-ag14细胞和脾细胞混合均匀,离心1000rpm×5min,弃上清。用无血清的rpmi1640基础培养基(gibco)洗涤混合细胞两次,最后一次将上清倾倒干净。取1ml37℃预温的peg1450(sigma),缓慢滴加到细胞沉淀上,作用90s,立即加入37℃预温的无血清rpmi1640基础培养基,5分钟内加完,混匀后离心800×5min,细胞沉淀重悬在含hat(sigma)的10%fbs(royacel)+杂交瘤补充物(roche)-rpmi1640培养基中,均匀铺至96孔板中,80μl/每孔,于37℃、5%co2的细胞培养箱中培养。
5)融合后定期观察细胞状态。在融合第5~7天,进行换液,即用新鲜含hat的10%fbs+杂交瘤补充物-rpmi1640培养基换出培养孔板中全部培养基,120μl/每孔,继续培养5~7天。
2.阳性融合细胞的筛选及亚克隆化
通过间接elisa检测各孔中细胞分泌抗体的情况。分别以hba1c和hb蛋白作为elisa筛选包被抗原,hrp标记的山羊抗小鼠igg(h+l)二抗作为检测抗体,选择与hba1c反应阳性但与hb反应阴性的孔,显微镜下观察若有成活的杂交瘤细胞或细胞团,进行标记,挑取hba1c阳性值较高的孔,采用有限稀释法将孔中的细胞进行克隆化,经过三次亚克隆后建立稳定分泌单克隆抗体的杂交瘤细胞株,并进行扩大培养。杂交瘤细胞株命名为1g8,保藏于中国典型培养物保藏中心,其保藏编号为cctccno:c2019256,地址:武汉市武汉大学,保藏时间:2019年10月29日。
实施例4抗hba1c单克隆抗体的制备及纯化
1.腹水制备
取3只10~16周龄balb/c雌鼠(北京斯贝福),每只小鼠提前12~18天腹腔左右各注射0.25ml腹水制备佐剂(北京博奥龙)。取生长对数期杂交瘤细胞计数,取6*106个细胞用10ml无菌pbs洗两次,离心时用1000rpm,5min,最终用无菌pbs调整细胞浓度至2*106个/ml,然后给上述小鼠腹腔左右各注射0.5ml细胞悬液并按摩腹部使细胞分布均匀。约10~14天后小鼠腹部明显隆起并开始收集腹水,一般隔天收集一次,共收集三次。每次收集好腹水,2000rpm离心5min后收集上清(用移液枪尽量吸走最上层油脂),短时间保存在4℃,长时间保存在-20℃。
2.抗体纯化
1)取上述保存腹水14000rpm离心10min,除去细胞碎片和颗粒杂质。
2)转移上清液并用滤纸过滤,收集滤出液并测量体积。
3)边搅拌边慢慢加入等体积的饱和硫酸铵到滤出液中,终浓度为1:1。
4)将溶液放在磁力搅拌器上室温温和搅拌2小时再分装至高速离心管4℃静置过夜,使蛋白质充分沉淀。
5)第二天取出直接10000rpm离心30min,弃上清保留沉淀晾干。
6)加入0.5倍滤出液体积的pbs溶解沉淀,然后超滤离心脱盐浓缩。
7)加入滤出液两倍体积的结合缓冲液稀释浓缩液,并用0.45μm滤膜过滤。
8)收集滤出液用proteing预装柱(常州天地人和)按照厂家说明书进行亲和纯化。
9)收集洗脱液用截留分子量为50kd的超滤离心管(millipore)进行脱盐浓缩。
3.抗体浓度及纯度测定
脱盐浓缩后的抗体采用bradford法测定抗体浓度,并用sds-page电泳初步鉴定抗体纯度(如图4)。
实施例5抗hba1c单克隆抗体的特性鉴定
1.抗体亚型的鉴定
采用mouse单克隆抗体亚型鉴定试剂盒(proteintech)鉴定得到的抗人hba1c单克隆抗体的亚型,酶标板上预包被了针对小鼠igg1、igg2a、igg2b、igg2c、igg3、igm、kappalightchain、lambdalightchain的特异性抗体,具体实验操作见试剂盒说明书。结果如图5,我们得到的抗人hba1c单克隆抗体的重链亚型为igg2a,轻链亚型为kappa。
本发明的抗体可以作为其他同型重组表达,例如igg1,igg3,igg4,igm和iga。
2.抗体反应性的测定
采用间接elisa方法检测纯化的抗体与hba1c和hb的反应性,具体步骤如下:分别用hba1c和hb包被酶标板,2μg/ml,50μl/孔,4℃过夜。次日倾去包被液,用0.05%pbst人工洗板3次后,加入0.5%bsa封闭,200μl/孔,37℃,1h。弃去封闭液,0.05%pbst人工洗板3次后,加入自1μg/ml开始两倍递比稀释的纯化抗体共8个稀释度,50μl/孔,37℃,1h。0.05%pbst人工洗板3次后,加入1:20000稀释的辣根过氧化物酶标记的山羊抗小鼠igg(h+l)二抗,50μl/孔,37℃,1h。0.05%pbst人工洗板5次后,加入显色底物tmb,50μl/孔,室温,10min,最后加入1m硫酸终止反应。在酶标仪上读取od450nm,结果显示该纯化抗体在一定浓度范围内与hba1c有较强反应,而与hb几乎不反应(如图6),说明该抗人hba1c单克隆抗体特异性非常高。
同时,我们购买了一株业界公认较好的抗人hba1c单克隆抗体,生产自英国bbisolutions(bm300-f7c2)公司,其可应用于elisa及侧向层析。我们比较了本发明中抗人hba1c单克隆抗体和bbisolutions这株抗体与hba1c和hb的反应性,结果如图7,本发明中抗人hba1c单克隆抗体以优于bbisolutions这株抗体的亲和力结合hba1c,且与hb结合能力更小,因此本发明中抗人hba1c单克隆抗体亲和力更高而特异性更强。
实施例6杂交瘤细胞株重轻链可变区基因的克隆
1.抗人hba1c单克隆抗体重轻链可变区基因提取、扩增及初步鉴定
实施例3中阳性杂交瘤细胞株扩大培养后,收集对数生长期的细胞,使用novagen鼠源抗体可变区基因克隆的整套试剂并按照其说明书对本发明中所述抗体的重轻链可变区基因进行克隆测序。具体方法路线为:使用straighta’stmmrnaisolationkits从收集杂交瘤细胞株中分离总rna,然后使用firststrandcdnasynthesiskit和ig-3'constantregionprimer合成第一条cdna链,接着使用ig-5'primers和novataqdnapolymerase以第一条cdna链为模板进行pcr扩增,得到的pcr扩增产物使用vectorcloningkit克隆到克隆载体中,并进行筛选,分离dna进行基因测序。
2.抗人hba1c单克隆抗体重轻链可变结构域的基因测序及分析
在genbank中,比对测序结果与小鼠抗体核酸序列,结果显示该抗体的轻链和重链的可变区序列与提交的小鼠igg可变区序列的同源性超过97%,确定测序得到的基因序列为小鼠抗体序列。利用imgt/v-quest与abysis软件分析得到抗体轻链和重链可变区的氨基酸序列及cdr区、fr区的划分。分析结果表明:杂交瘤细胞株抗体重链可变结构域vh的核苷酸序列和氨基酸序列如seqidno:1和seqidno:2所示;杂交瘤细胞株轻链可变结构域vl的核苷酸序列和氨基酸序列如seqidno:9和seqidno:10所示;重链可变结构域vh依次包含高变区cdrh1、cdrh2和cdrh3,所述的核苷酸序列依次为seqidno:3、5、7,氨基酸序列依次为seqidno:4、6、8;轻链可变结构域vl依次包含高变区cdrl1、cdrl2和cdrl3,所述的核苷酸序列依次为seqidno:11、13、15,氨基酸序列依次为seqidno:12、14、16。
抗体可变区核酸及氨基酸序列
seqidno1:
gatgtgcagctggtggagtctgggggaggcttagtgcagcctggagggtcccggaaactctcctgtgcagcctctggattcactttcagtaactttggaatgcactgggttcgtcaggttccagagaaggggctggagtgggtcgcatacattagtggtgacagaaccatgtactatgcagacacagtgaagggccgattcaccatctccagagacaatcccaagaacaccctgttcctgcaaatgaccagtctaaggtctgaggacacggccatgtattactgtgcagtttaccttgcctatgctatggactattggggtcaaggaacctcagtcaccgtctcctca
seqidno2:
dvqlvesggglvqpggsrklscaasgftfsnfgmhwvrqvpekglewvayisgdrtmyyadtvkgrftisrdnpkntlflqmtslrsedtamyycavylayamdywgqgtsvtvss
seqidno3:
aactttggaatgcac
seqidno4:
nfgmh
seqidno5:
tacattagtggtgacagaaccatgtactatgcagacacagtgaagggc
seqidno6:
yisgdrtmyyadtvkg
seqidno7:
taccttgcctatgctatggactat
seqidno8:
ylayamdy
seqidno9:
gatgttttgatgacccaaactccactctccctgcctgtcagtcttggagatcaagcctccatctcttgcagatctagtcagagtattgtacatagtaatggaaacacttatttagaatggtacctgcagaaaccaggccagtctccaaagctcctgatctacaaagtctccaaccgattttctggggtcccagacaggttcagtggcagtggatcagggacagatttcacactcaagatcaggagagtggaggctgaggatctgggagtttattactgccttcaaggttcacatgttccattcacgttcggctcggggacaaagttggaaataaaa
seqidno10:
dvlmtqtplslpvslgdqasiscrssqsivhsngntylewylqkpgqspklliykvsnrfsgvpdrfsgsgsgtdftlkirrveaedlgvyyclqgshvpftfgsgtkleik
seqidno11:
agatctagtcagagtattgtacatagtaatggaaacacttatttagaa
seqidno12:
rssqsivhsngntyle
seqidno13:
aaagtctccaaccgattttct
seqidno14:
kvsnrfs
seqidno15:
cttcaaggttcacatgttccattcacg
seqidno16:
lqgshvpft
序列表
<110>浙江蓝盾药业有限公司
<120>杂交瘤细胞株1g8、抗体及其应用
<160>16
<170>siposequencelisting1.0
<210>1
<211>348
<212>dna
<213>人工序列(artificialsequence)
<400>1
gatgtgcagctggtggagtctgggggaggcttagtgcagcctggagggtcccggaaactc60
tcctgtgcagcctctggattcactttcagtaactttggaatgcactgggttcgtcaggtt120
ccagagaaggggctggagtgggtcgcatacattagtggtgacagaaccatgtactatgca180
gacacagtgaagggccgattcaccatctccagagacaatcccaagaacaccctgttcctg240
caaatgaccagtctaaggtctgaggacacggccatgtattactgtgcagtttaccttgcc300
tatgctatggactattggggtcaaggaacctcagtcaccgtctcctca348
<210>2
<211>116
<212>prt
<213>人工序列(artificialsequence)
<400>2
aspvalglnleuvalgluserglyglyglyleuvalglnproglygly
151015
serarglysleusercysalaalaserglyphethrpheserasnphe
202530
glymethistrpvalargglnvalproglulysglyleuglutrpval
354045
alatyrileserglyaspargthrmettyrtyralaaspthrvallys
505560
glyargphethrileserargaspasnprolysasnthrleupheleu
65707580
glnmetthrserleuargsergluaspthralamettyrtyrcysala
859095
valtyrleualatyralametasptyrtrpglyglnglythrserval
100105110
thrvalserser
115
<210>3
<211>15
<212>dna
<213>人工序列(artificialsequence)
<400>3
aactttggaatgcac15
<210>4
<211>5
<212>prt
<213>人工序列(artificialsequence)
<400>4
asnpheglymethis
15
<210>5
<211>48
<212>dna
<213>人工序列(artificialsequence)
<400>5
tacattagtggtgacagaaccatgtactatgcagacacagtgaagggc48
<210>6
<211>16
<212>prt
<213>人工序列(artificialsequence)
<400>6
tyrileserglyaspargthrmettyrtyralaaspthrvallysgly
151015
<210>7
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>7
taccttgcctatgctatggactat24
<210>8
<211>8
<212>prt
<213>人工序列(artificialsequence)
<400>8
tyrleualatyralametasptyr
15
<210>9
<211>336
<212>dna
<213>人工序列(artificialsequence)
<400>9
gatgttttgatgacccaaactccactctccctgcctgtcagtcttggagatcaagcctcc60
atctcttgcagatctagtcagagtattgtacatagtaatggaaacacttatttagaatgg120
tacctgcagaaaccaggccagtctccaaagctcctgatctacaaagtctccaaccgattt180
tctggggtcccagacaggttcagtggcagtggatcagggacagatttcacactcaagatc240
aggagagtggaggctgaggatctgggagtttattactgccttcaaggttcacatgttcca300
ttcacgttcggctcggggacaaagttggaaataaaa336
<210>10
<211>112
<212>prt
<213>人工序列(artificialsequence)
<400>10
aspvalleumetthrglnthrproleuserleuprovalserleugly
151015
aspglnalaserilesercysargserserglnserilevalhisser
202530
asnglyasnthrtyrleuglutrptyrleuglnlysproglyglnser
354045
prolysleuleuiletyrlysvalserasnargpheserglyvalpro
505560
aspargpheserglyserglyserglythraspphethrleulysile
65707580
argargvalglualagluaspleuglyvaltyrtyrcysleuglngly
859095
serhisvalprophethrpheglyserglythrlysleugluilelys
100105110
<210>11
<211>48
<212>dna
<213>人工序列(artificialsequence)
<400>11
agatctagtcagagtattgtacatagtaatggaaacacttatttagaa48
<210>12
<211>16
<212>prt
<213>人工序列(artificialsequence)
<400>12
argserserglnserilevalhisserasnglyasnthrtyrleuglu
151015
<210>13
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>13
aaagtctccaaccgattttct21
<210>14
<211>7
<212>prt
<213>人工序列(artificialsequence)
<400>14
lysvalserasnargpheser
15
<210>15
<211>27
<212>dna
<213>人工序列(artificialsequence)
<400>15
cttcaaggttcacatgttccattcacg27
<210>16
<211>9
<212>prt
<213>人工序列(artificialsequence)
<400>16
leuglnglyserhisvalprophethr
15
- 还没有人留言评论。精彩留言会获得点赞!