一种硅量子点/环糊精铜荧光簇及其制备方法和在检测巯基化合物中应用与流程
本发明属于分析检测技术领域,具体涉及一种硅量子点/环糊精铜荧光簇的制备方法及采用该荧光簇检测巯基化合物。
背景技术:
半胱氨酸是人体中一种重要的巯基氨基酸,有能力形成二硫键,有助于蛋白质结构构建和蛋白质折叠。食品工业中,半胱氨酸是良好的水果保鲜剂和食品添加剂。半胱氨酸衍生物谷胱甘肽也是一种巯基化合物,能消除人体自由基,可以提高人体免疫力,维护健康,抗衰老。因此精确测定半胱氨酸类巯基活性物质的含量具有现实意义。
对于巯基化合物的检测常需要一些大型仪器,比如高效液相色谱、液质联用、气质联用等,测量昂贵耗时。而荧光检测方法操作方便,具有高灵敏度。目前已有使用荧光分析方法实现对半胱氨酸的检测,wang等制备了磷氮共掺杂的碳量子点(sensorsandactuatorsb-chemical,2018:1627-1634),与金纳米棒结合后发生荧光猝灭,fe3+和h2o2产生的羟基自由基可诱导金纳米棒腐蚀,导致碳量子点荧光恢复,加入半胱氨酸会抑制蚀刻进度,进而实现半胱氨酸的定量检测,但该方法过程较复杂,涉及贵金属,成本较高。borghei等(journaloffluorescence,2017,27(2):529-536)利用巯基和金属的强作用力形成的cys-cuncs团簇,团簇荧光强度与半胱氨酸浓度密切相关,从而实现定量检测半胱氨酸;但半胱氨酸在低浓度时量增荧光增强,但高浓度时量增荧光反而减弱,故不能连续检测,应用受限。“基于钙黄绿素-铜(ⅱ)荧光体系测定乙酰半胱氨酸”,杨晓红等利用二价铜离子能与钙黄绿素配位,使体系的荧光强度降低,巯基与cu2+的亲和力强,可从钙黄绿素-铜(ⅱ)的络合物中夺取铜离子而使钙黄绿素游离出来,使钙黄绿素游离出来荧光强度得以恢复,从而检测乙酰半胱氨酸的浓度。目前采用黄绿素-铜(ⅱ)的络合物或其它铜离子络合物方法检测巯基化合物时,铜离子会对测试结果直接干扰,另外铜离子还能与其它氨基酸形成络合物,其它氨基酸也会对巯基化合物检测结果产生干扰,限制其实际使用。
荧光分析方法中,荧光探针有着举足轻重的作用。常用的有机荧光探针亮度低或光稳定性差,降低了荧光传感器的灵敏度和稳定性,而半导体硅的量子点具有发光效率高、稳定性优越的特点,使得高性能的荧光传感器成为可能性。利用硅量子点/环糊精铜自组装形成荧光簇,荧光簇荧光强度随巯基化合物的含量增加而增强,从而实现高效便捷地定量测定巯基化合物的含量。
技术实现要素:
本发明所要解决的技术问题是提供一种硅量子点/环糊精铜荧光簇的制备方法及应用,利用表面有氨基修饰的硅量子点siqds-(nh2)n上氨基与β-环糊精铜cu2-β-cd桥上铜的配位作用,自组装形成siqds-(nh2)n/cu2-β-cd荧光簇,利用荧光簇的荧光强度变化定量测定水溶性巯基化合物。这种方法成本低、操作简单和环境友好,且具有较宽的检测限。
本发明的依据是硅量子点溶液中加入巯基化合物,和初始硅量子点的荧光强度一致;而siqds-(nh2)n和cu2-β-cd形成荧光簇后,加入巯基化合物,荧光强度增强,且荧光强度的增量与巯基化合物的含量成比例。
本发明提供的一种siqds-(nh2)n/cu2-β-cd荧光簇的制备方法,按照下述步骤进行:
(1)制备含多氨基的硅量子点siqds-(nh2)n
烧瓶中加入适量的kh-550和去离子水,磁力搅拌水解,加入抗坏血酸溶液,继续搅拌30min,再转移到聚四氟乙烯内衬的高压水热釜中,放入120-180℃的马弗炉中保温12-24h;
(2)制备β-环糊精铜cu2-β-cd
配制10ml氢氧化钠和β-环糊精的混合溶液,再向其中加入硫酸铜溶液15ml,迅速形成氢氧化铜蓝色沉淀,室温下搅拌12h后,过滤除去氢氧化铜沉淀,滤液中加入乙醇,溶液中逐渐出现蓝色沉淀,静置后将其过滤,固体用少量乙醇洗涤,在40℃条件下干燥,得到蓝色固体粉末即为产物;
(3)siqds-(nh2)n/cu2-β-cd荧光簇的制备
将浓度为20g/l的siqds-(nh2)n和1×10-3mol/l的cu2-β-cd按体积比为1:0.1-1:0.5充分混合进行自组装10-30min,在15~25℃室温条件下进行,自组装结束即得siqds-(nh2)n/cu2-β-cd荧光簇溶液。
作为优选,步骤(1)中950g/lkh550液体和去离子水的水解体积配比为2:18-4:16,混合总体积与抗坏血酸溶液体积比为4:1,抗坏血酸的浓度为0.05-0.1mol/l。
作为优选,步骤(2)混合液中氢氧化钠浓度为0.2-0.5mol/l,β-环糊精浓度为0.01-0.02mol/l;硫酸铜浓度为0.02-0.04mol/l。
上述的siqds-(nh2)n/cu2-β-cd荧光簇可用于巯基化合物的定量检测,优选合成的硅量子点的最大激发波长为360nm。
其应用按如下步骤进行:
在上述siqds-(nh2)n/cu2-β-cd荧光簇溶液中加入不同浓度巯基化合物溶液(0-240μm),溶液总体积保持一致且静置10-30min时间,然后测量体系的荧光发射光谱。以巯基化合物的浓度为横坐标,荧光增强率的103倍为纵坐标,拟合线性方程,计算检测限。
作为优选,上述巯基化合物为l-半胱氨酸(l-cys),d-半胱氨酸(d-cys)或谷胱甘肽(gsh)中的一种。
由上述技术方案可知:本发明首先采用kh-550为原料,通过水热法,制备氨基修饰的硅量子点siqds-(nh2)n;然后利用氨基氮上的孤对电子与β-环糊精铜桥上铜的配位作用,自组装形成siqds-(nh2)n/cu2-β-cd荧光簇。在荧光簇的应用过程中,由于巯基化合物上巯基与β-环糊精铜配位能力更强,在siqds-(nh2)n/cu2-β-cd荧光簇溶液中,加入巯基化合物后,其原有的硅量子点/环糊精铜荧光簇解体,释放出自由的siqds-(nh2)n,从而使得溶液荧光增强。荧光强度的增量与巯基化合物的添加量成比例,因而,可实现溶液中巯基化合物的荧光检测。
本发明的有益效果是:
(1)本发明提供了荧光法定量测定水溶性巯基化合物的方法,数据可靠稳定,方法操作简捷、制备容易、成本低,是一种环境友好型的测定方法。
(2)本发明提供的荧光法实现对巯基化合物特异性检测,其他常见离子和化合物几乎不产生干扰。
(3)本发明提供的测定巯基化合物的浓度范围在0-240μm,检测限为0.48μm。
附图说明
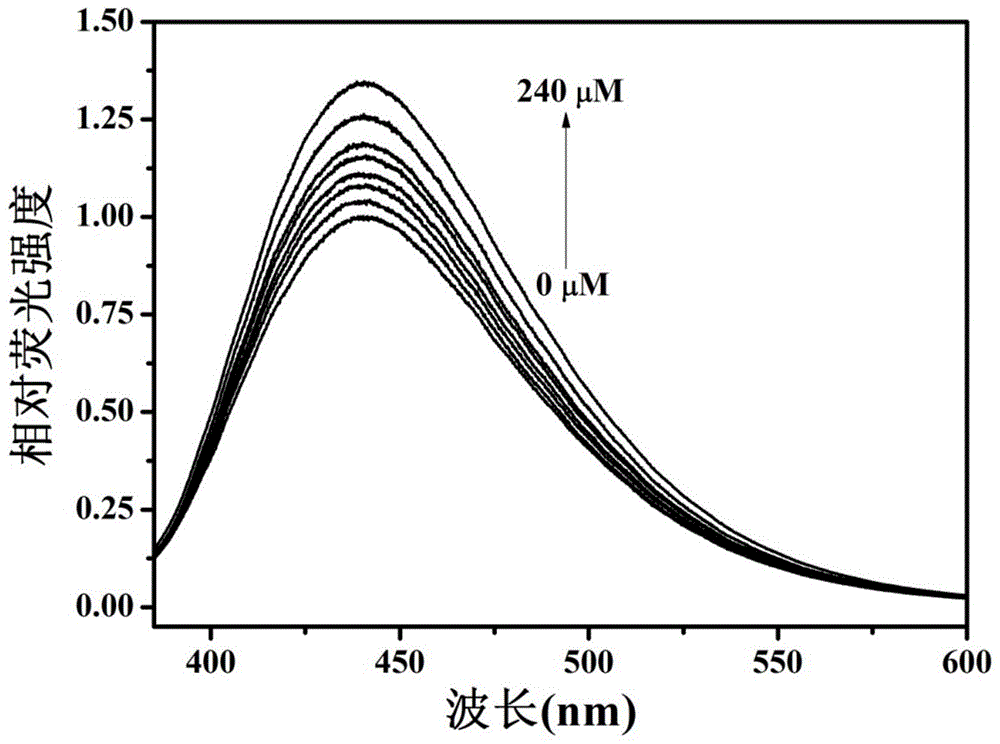
图1为不同浓度的l-半胱氨酸条件下荧光簇的相对荧光强度;
图2为不同浓度的l-半胱氨酸和荧光增强率的线性关系;
图3为不同浓度的d-半胱氨酸条件下荧光簇的相对荧光强度;
图4为不同浓度的d-半胱氨酸和荧光增强率的线性关系;
图5为不同浓度的谷胱甘肽条件下荧光簇的相对荧光强度;
图6为不同浓度的谷胱甘肽和荧光增强率的线性关系;
图7为共存物质(l-cys和未标明的干扰物均为300μm)的干扰测定图;
图8ph=6条件下,硅量子点以及cu2+、cu2+和l-cys存在下的荧光光谱;
图9ph=8条件下,硅量子点以及cu2+、cu2+和l-cys存在下的荧光光谱;
图10为siqds-(nh2)n/cu2-β-cd荧光簇的afm图;
图11为siqds-(nh2)n量子点的afm图。
具体实施方式
下面结合具体的实施例,进一步详细地描述本发明。应理解,这些实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。
实施例1
(1)制备含多氨基的硅量子点siqds-(nh2)n
烧瓶中加入950g/lkh-550和去离子水,体积比2:18,共20ml,磁力搅拌水解,加入浓度为0.05mol/l的抗坏血酸溶液5ml继续搅拌30min,再转移到聚四氟乙烯内衬的高压水热釜中,放入120℃的马弗炉中保温24h;
(2)制备β-环糊精铜cu2-β-cd
配制10ml氢氧化钠和β-环糊精的混合溶液,混合溶液中,氢氧化钠的浓度为0.2mol/l,β-环糊精的浓度为0.01mol/l;再向其中加入0.02mol/l硫酸铜溶液15ml,迅速形成氢氧化铜蓝色沉淀,室温下搅拌12h后,过滤除去氢氧化铜沉淀,滤液中加入乙醇,溶液中逐渐出现蓝色沉淀,静置后将其过滤,固体用少量乙醇洗涤,在40℃条件下干燥,得到蓝色固体粉末即为产物;
(3)siqds-(nh2)n/cu2-β-cd荧光簇的制备
将浓度为20g/l(si含量计)的siqds-(nh2)n和1×10-3mol/l的cu2-β-cd按体积比为1:0.1充分混合进行自组装10min,自组装结束即为siqds-(nh2)n/cu2-β-cd荧光簇溶液。
实施例2
(1)制备含多氨基的硅量子点siqds-(nh2)n
烧瓶中加入kh-550和去离子水,体积比3:17,共20ml,磁力搅拌水解,加入浓度为0.08mol/l的抗坏血酸溶液5ml继续搅拌30min,再转移到聚四氟乙烯内衬的高压水热釜中,放入150℃的马弗炉中保温18h;
(2)制备β-环糊精铜cu2-β-cd
配制10ml氢氧化钠和β-环糊精的混合溶液,其中,氢氧化钠的浓度为0.35mol/l,β-环糊精的浓度为0.015mol/l;再向其中加入0.03mol/l硫酸铜溶液15ml,迅速形成氢氧化铜蓝色沉淀,室温下搅拌12h后,过滤除去氢氧化铜沉淀,滤液中加入乙醇,溶液中逐渐出现蓝色沉淀,静置后将其过滤,固体用少量乙醇洗涤,在40℃条件下干燥,得到蓝色固体粉末即为产物;
(3)siqds-(nh2)n/cu2-β-cd荧光簇的制备
将浓度为20g/l的siqds-(nh2)n和1×10-3mol/l的cu2-β-cd按体积比为1:0.2充分混合进行自组装20min,自组装结束即为siqds-(nh2)n/cu2-β-cd荧光簇溶液。
实施例3
(1)制备含多氨基的硅量子点siqds-(nh2)n
烧瓶中加入kh-550和去离子水,体积比4:16,共20ml,磁力搅拌水解,加入浓度为0.1mol/l的抗坏血酸溶液5ml继续搅拌30min,再转移到聚四氟乙烯内衬的高压水热釜中,放入180℃的马弗炉中保温12h;
(2)制备β-环糊精铜cu2-β-cd
配制10ml氢氧化钠和β-环糊精的混合溶液,其中,氢氧化钠的浓度为0.5mol/l,β-环糊精的浓度为0.02mol/l;再向其中加入0.04mol/l硫酸铜溶液15ml,迅速形成氢氧化铜蓝色沉淀,室温下搅拌12h后,过滤除去氢氧化铜沉淀,滤液中加入乙醇,溶液中逐渐出现蓝色沉淀,静置后将其过滤,固体用少量乙醇洗涤,在40℃条件下干燥,得到蓝色固体粉末即为产物;
(3)siqds-(nh2)n/cu2-β-cd荧光簇的制备
将浓度为20g/l的siqds-(nh2)n和1×10-3mol/l的cu2-β-cd按体积比为1:0.5充分混合进行自组装30min,自组装结束即为siqds-(nh2)n/cu2-β-cd荧光簇溶液。
其中图10为siqds-(nh2)n/cu2-β-cd荧光簇的afm(原子力显微镜)图;图11为siqds-(nh2)n量子点的afm(原子力显微镜)图。从图中可以看出,荧光簇呈几百纳米不规则米粒状,siqds-(nh2)n量子点平均粒径为5.625nm。
实施例4
siqds-(nh2)n/cu2-β-cd荧光簇的应用
在实施例31.5ml浓度0.0067g/ml(si含量计)的siqds-(nh2)n/cu2-β-cd荧光簇溶液中分别加入0-240μm不同浓度l-cys,d-cys以及gsh的溶液1.5ml,溶液总体积保持一致且静置30min时间后,360nm激发,测定体系的荧光发射光谱,图1,3,5分别为l-cys,d-cys,gsh在荧光簇检测条件下的相对荧光光谱。以巯基化合物的浓度(0-240μmol/l)为横坐标,荧光增强率的103倍为纵坐标(荧光增强率=(aμm相对荧光强度-0μm相对荧光强度)/0μm相对荧光强度*100%),拟合线性方程,计算检测限,图2,4,6分别为l-cys,d-cys,gsh的浓度和荧光增强率的关系图,拟合的线性方程相似,有一致的检测限(0.48μmol/l),说明检测机理一样。另外,对比图2和图4发现,荧光簇中环糊精铜虽是手性主体材料,但巯基化合物手性对检测结果没干扰。
实施例5
siqds-(nh2)n/cu2-β-cd对l-cys的荧光测定
实施例3中的siqds-(nh2)n/cu2-β-cd荧光簇溶液360nm激发,最大荧光发射峰处的峰高设定为1。在上述荧光簇溶液中加入l-cys(浓度为0.24μμ),静置10min后,360nm激发,最大荧光发射峰的峰高相对于siqds-(nh2)n/cu2-β-cd为1.19。
由此可知,巯基化合物可使得siqds-(nh2)n/cu2-β-cd荧光簇溶液荧光增强。
对比例1
siqds-(nh2)n对l-cys的荧光测定
将浓度为0.02g/ml的siqds-(nh2)n,360nm激发,最大荧光发射峰处的峰高设为1.0;浓度为0.02g/ml的siqds-(nh2)n中加入l-cys(浓度0.24μm),360nm激发,最大荧光发射峰的峰高相对于siqds-(nh2)n体系也为1.0,说明l-cys的加入并未使得siqds-(nh2)n荧光增强,因此,siqds-(nh2)n不能用于l-cys的荧光测定。
对比例2
(1)制备含多氨基的硅量子点siqds-(nh2)n,同实施例1。
(2)siqds-(nh2)n-cu(ⅱ)的制备;
siqds-(nh2)n溶液的ph呈较强的碱性,将浓度20g/l的siqds-(nh2)n和0.002mol/l的cuso4按体积比2:1混合,得到的混合液的ph值在8~9之间,由于是弱碱性条件,cu2+可能以cu(oh)2的纳米粒子或胶束存在,cu(ii)能与量子点的氨基氮上的孤对电子配位,形成siqds-(nh2)n-cu(ⅱ);
如果将siqds-(nh2)n溶液用hcl溶液预调呈弱酸性,将浓度20g/l(si含量计)的siqds-(nh3+)n和0.002m的cuso4体积比2:1混合,混合液ph值在5~6之间,由于cu2+与siqds-(nh3+)n都是带正电荷,所以仅以siqds-(nh3+)n形态存在,量子点荧光不会发生淬灭。
(3)采用siqds-(nh2)n-cu(ⅱ)对l-cys的荧光测定
向siqds-(nh2)n-cu(ⅱ)溶液中加入l-cys,l-cys的浓度为0.24μm,360nm激发,测得siqds-(nh2)n-cu(ⅱ)的荧光谱图。
检测结果:
在弱酸条件下加入铜(ii),量子点荧光没淬灭,反而略有增加,加入l-cys后荧光恢复(如图8所示),无法用于l-cys的荧光测定。
在碱性条件下加入铜(ii),荧光猝灭,但加入l-cys后荧光无变化(如图9所示)。cu(oh)2的纳米粒子或胶束cu(ii)能与量子点的氨基氮上的孤对电子配位,发生能量转移,导致荧光淬灭。但加入l-cys荧光无变化,这是由于半胱氨酸l-cys的巯基与cu(ii)的结合能力低于氨基,所以不会有荧光响应。而cu2-β-cd的cu(ii)是以特有的铜桥键形式存在,它与巯基结合能力大于氨基,因而能对巯基化合物有荧光响应,且铜离子不会对测试结果直接干扰。
实施例6
巯基化合物的检测的干扰实验
在实施例3中的siqds-(nh2)n/cu2-β-cd荧光簇溶液中加入l-cys(浓度为300μm),静置40min后,360nm激发,最大荧光发射峰处的峰高设为1.0;在上述加有l-cys(浓度为300μm)的荧光簇溶液中,再分别加入k+,na+,mg2+,cu2+,so42-,co32-,cl-,trp,phe,asp,lys,ala,glu,thr,组成共存体系,各物质的浓度均为300μm,上述溶液体系静置40min后,360nm激发,最大荧光发射峰相对峰高值分别为0.9909,1.0100,1.0194,0.6133,0.9877,1.0074,1.0262,0.9931,1.0425,1.0295,1.0951,1.0750,1.0384,1.0503,1.0818;作图得到图7,等摩尔浓度的其他氨基酸会导致荧光强度稍增,误差在3.8-9.5%之间;等摩尔浓度的离子干扰在1.0%左右,但cu2+在300μm会对结果有很大干扰,但由于人体血液中游离cu2+的浓度和食物中cu2+的浓度极低,当以3μm的cu2+干扰检测时,检测误差<2%,因此,实际检测中cu2+对检测干扰很小。
实施例中未注明具体的条件,按照常规条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。本发明中所用方法,若无特别限定说明,均为本领域的常规方法。以上所述仅为本发明的较好实施方式,并不用以限制本发明,凡是依据本发明的技术实质对以上实施例作的修改,均包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!