用于由皮肤生物标记测量氧化应激反应和氧化损坏的非侵入性方法与流程
本发明涉及用于测量与皮肤样品的氧化应激反应和/或氧化损伤相关联的一种或多种生物标记的量、以及这些生物标记的量的关联与相关性的方法,因为它直接与哺乳动物皮肤健康的改善相关联。
背景技术:
头皮/皮肤是显著的器官系统,由起到对环境侵袭的第一道防线功能的多个特化组织构成。虽然早期的研究主要集中于皮肤的阻隔功能,已经变得清楚的一点是此器官是动态的:对甚至是环境中微小的变化感测并响应,从而帮助保持内稳态。环境影响诸如太阳辐、污染、或者甚至皮肤护理产品的施用导致复杂的级联事件,它们最终导致数百或者数千个基因表达的改变。基因表达的这些改变一般被翻译成催化化学反应的蛋白质生成的改变(或积聚、释放、改性等等),最终导致细胞响应。随着这些化学反应的进行,常常留下代谢副产物作为已经发生了何种化学过程的指示。分析与给定皮肤病症例如头皮屑相关联的这些所得蛋白质和小分子生物标记可提供有价值的信息,用于了解病症以及开发用于诊断和/或改善皮肤病症目的的产品。头皮屑是一种常见的慢性复发性头皮病症,具有片状剥落和瘙痒感。头皮屑的发病机理是复杂的,并且好像是头皮、微生物区系和宿主免疫系统之间相互作用的结果。对这种病症的许多之前的工作已经集中于检查一些表面水平的现象。传统的基于专家观察的评估及基于自我观察的评估与基于大型仪器的在生理水平上的表皮结构和功能的评估相结合。新的生物分子学能力达到了病理生理的理解深度,而非之前用传统研究方法达到的理解深度;然而,对导致这种病症的关键症状的分子事件的清晰了解仍未出现。为了解释这些关键分子事件,可通过皮肤表面的胶带剥除、随后通过化学或生物分析方法,来非侵入性地获得双分子取样。组胺最近被鉴定为头皮瘙痒的敏感生物标记。需要另外的生物标记以允许更详细的头皮屑病症的病理生理描述,以及用作指示头皮屑治疗方案程度和完成度的相关量度。受关注的一个此类区域是氧化应激反应。在文献中熟知的是氧化应激反应对皮肤造成损伤并且抗氧化剂能够提供对不同来源氧化损伤的保护作用。自由基的形成是导致皮肤老化和损伤的广泛接受的机制。自由基是高反应性的分子,具有未配对的电子,其能够直接损坏各种细胞结构膜、脂质、蛋白质、和DNA。这些反应性氧物质的损伤效应在正常代谢和免疫响应期间受到内部诱导,并且通过各种氧化应激反应源如暴露于阳光、一手烟或二手烟、环境毒素、饮食不良、应力等受到外部诱导。这些各种反应性氧物质必须不断从细胞中去除以保持健康代谢功能。人体有若干方法用以处理这一状况1)去除反应性氧物质,2)清除铁和其它金属,3)清除形成的自由基,以及4)修复分子损伤。当反应性氧物质的产生与对抗它们的抗氧化剂防御之间的平衡遭到破坏时,引发氧化应激反应。自由基也导致炎症,炎症被认为在皮肤老化中起到附加的作用并且对总体皮肤健康有害。自由基的产生加剧老化,而对抗它们的内源性防御机制的完整性和能力减轻老化。不平衡导致对细胞结构的渐进的和累积的损伤,引起老化并加速老化,其中环境老化与天然老化过程叠加。
氧化应激反应和由于氧化损伤而产生的所得分子(例如,氧化脂质)可通过非侵入性取样的生物标记进行评估,这使得它们可用于常规的临床评估。
为了评估头皮屑病症的氧化应激反应,使用基于抗体的分析来定量蛋白质绿过氧物酶(MPO)。MPO是一种促炎性酶,它作为抵抗广泛微生物病原体(例如,鳞斑霉属(Malassezia))的宿主防御机制的一部分由中性粒(PMNs)分泌。MPO能够将过氧化氢转化成杀菌剂次氯酸,以及一系列潜在损伤性的反应性氧物质(ROS)。此外,MPO能够行使抗微生物肽或蛋白质的功能。虽然未全面地理解该机制,但如下假设是合理的:由MPO生成的反应性氧物质当杀死病原体时可能引起对周围组织的连带损伤。为了评估由氧化应激反应引起的氧化损伤,使用高效液相色谱法与串联质谱法来定量若干氧化脂质。这些方法用于辨别在来自无头皮屑受试者、头皮屑受试者、和经头皮屑治疗的受试者的头皮胶带剥除提取物之间的差别。
非侵入性取样方法对皮肤/头皮护理中的生物标记应用是重要的。胶带剥除已经被成功地用于收集与来自皮肤/头皮的氧化应激反应和氧化损伤相关联的小分子和蛋白质用于后续的分析。
技术实现要素:
本发明的一个实施例涉及用于诊断受试者皮肤健康的非侵入性方法,该非侵入性方法包括:收集来自受试者的皮肤样品/上皮细胞样品;检测选自上皮细胞样品/皮肤细胞样品中的绿过氧物酶和氧化脂质的一种或多种生物标记的含量;基于检测到的生物标记的含量诊断受试者是否具有氧化应激反应和/或氧化损伤。
本发明的另一个实施例涉及用于诊断受试者的氧化应激反应和氧化损伤的非侵入性方法,该非侵入性方法包括:将粘合剂制品施用到哺乳动物的上皮;允许上皮细胞粘附到粘合剂制品;将粘合剂制品从哺乳动物的上皮移除;使用用于提取的标准实验室方法制备粘合剂制品;从粘附到所述粘合剂制品的上皮细胞中提取选自绿过氧物酶和氧化脂质的生物标记;测量来自粘附到所述粘合剂制品的上皮细胞的生物标记;测定治疗后相比于基线样品上皮细胞中的生物标记的量。
通过阅读本公开,本发明的这些和其它特征、方面和优点对本领域的技术人员将变得显而易见。
附图说明
图1是示出无头皮屑患者对头皮屑患者的绿过氧物酶含量的比较的图。
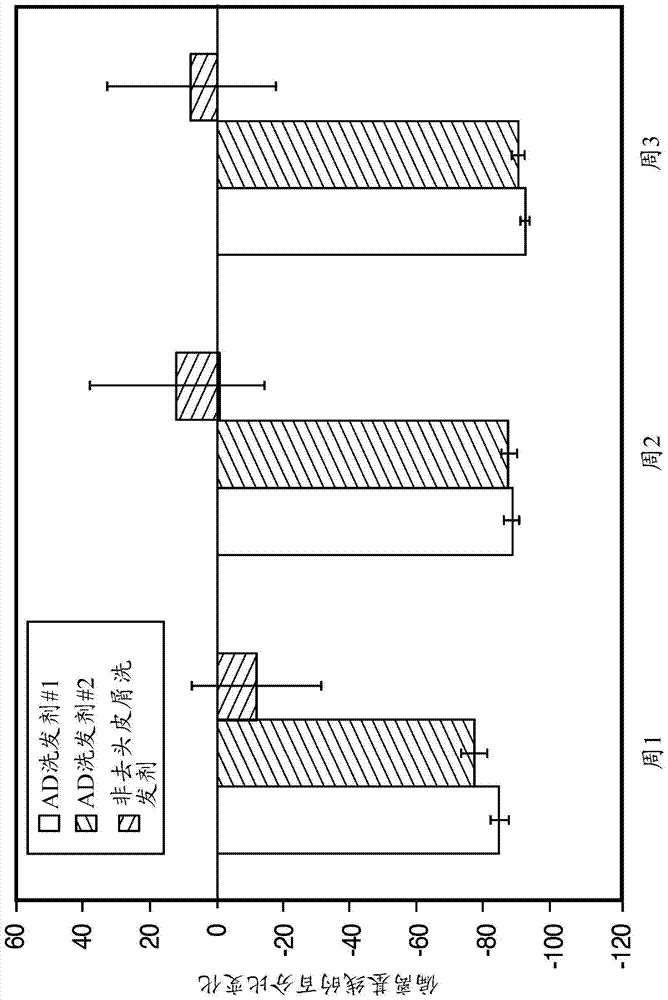
图2是示出头皮屑患者在用去头皮屑洗发剂或非去头皮屑洗发剂治疗后绿过氧物酶含量偏离基线的变化的图。
图3是示出头皮屑患者的绿过氧物酶基线含量和在用去头皮屑洗发剂治疗后的绿过氧物酶含量对无头皮屑群体的绿过氧物酶含量的归一化结果的图。
图4是示出在无头皮屑患者对头皮屑患者中的(±)-9-羟基-10E,12Z-十八碳二烯酸和(±)-13-羟基-10E,12Z-十八碳二烯酸(HODE)与角鲨烯氢过氧化物含量的比较的图。
图5是示出头皮屑患者在用去头皮屑洗发剂或非去头皮屑洗发剂治疗后的氧化脂质偏离基线的变化的图。
具体实施方式
尽管说明书通过特别指明并且清楚地要求保护本发明的权利要求作出结论,据信,本发明通过下列具体实施方式将更好地理解。
本发明可包含下列因素、由其组成、或基本上由其组成:本文所述的本发明的基本要素和限定条件、以及本文所述的或其它适用于旨在供哺乳动物消费的组合物的任何附加或任选成分、组分或限定条件。
除非另外指明,所有的百分比、份数和比率以本发明组合物的总重量计。与所列成分相关的所有此类重量均是基于活性物质含量计的;因此不包括可能包含于可商购获得的物质中的载体或副产物。
本发明的各个实施例中的组分和/或步骤,包括可任选加入的那些,详细描述于下文。
所有引用文献的相关部分均引入本文以供参考;任何文献的引用不可解释为是对其作为本发明的现有技术的认可。
除非另外特别说明,所有比率都是重量比率。
除非另外特别说明,所有温度是摄氏度。
除非另外指明,所有包括数量、百分比、分数和比例的量被理解为由词“约”所修饰,并且量不旨在显示有效数字。
除非另外指明,“一个”、“一种”和“所述”是指“一个或多个”。
本发明中“包括”指可加入其它不影响最终结果的成分。该术语包括术语“由…组成”和“基本上由…组成”。本发明的组合物和方法/过程可包括本文所述的本发明元素和限制,以及本文所述的任何附加或任选成分、组分、步骤或限制、由本文所述的本发明元素和限制,以及本文所述的任何附加或任选成分、组分、步骤或限制组成,和基本上由本文所述的本发明基本元素和限制,以及本文所述的任何附加或任选成分、组分、步骤或限制组成。
本文“有效的”是指一定量的受试品活性足够高以使待治疗病症发生显著积极的改善。受试品活性的有效量将随着待治疗的具体病症、病症的严重度、治疗持续时间、并发治疗的性质、以及类似因素而发生改变。
如本文所用,术语“差异含量”的生物分子可包括任何提高的或降低的含量。在一个实施例中,差异含量是指含量增加了:至少5%;至少10%;至少20%;至少30%;至少40%;至少50%;至少60%;至少70%;至少80%;至少90%;至少100%;至少110%;至少120%;至少130%;至少140%;至少150%;或更多。在另一个实施例中,差异含量是指含量降低了:至少5%;至少10%;至少20%;至少30%;至少40%;至少50%;至少60%;至少70%;至少80%;至少90%;至少100%。生物分子以统计学上显著的差异含量表达(即,使用Student T-test、Welch′s T-test或Matched Pair T-test测得的P值小于0.2(双侧))。
术语“皮肤”是指脊椎动物的外蒙皮,其由两层细胞组成,分别是厚的内层(真皮)和薄的外层(表皮)。表皮是皮肤外部的非血管层。它由从内到外的五层上皮构成:(1)基底层(表皮基底层);(2)棘层(表皮棘层);(3)颗粒层(表皮颗粒层);(4)透明层(表皮透明层);和(5)角质层(表皮角质层)。
术语“样品”指来自受试者皮肤或表皮的任何制备物。
术语“非侵入性”指不需要将器械或装置插入皮肤或身体孔口进行诊断或治疗的方法。
术语“粘合剂装置”指通过将粘合剂或粘附材料用于基底以移除皮肤的表皮层的装置。例如使用粘合带诸如(聚丙烯酸酯粘合剂;CuDerm;Dallas TX)、Durapor、SebutapeTM(丙烯酸类聚合物膜;CuDern;Dallas,TX)、TegadermTM、Duct胶带(333Duct Tape,Nashua胶带产品)、Tape(3M Scotch 810,St.Paul,Minn.)、DiamondTM(The Sellotape Company;Eindhoven,the Netherlands)、SentegaTM(聚丙烯胶带,Sentega Eiketten BV,Utrecht,The Netherlands)来对皮肤取样。所述粘合剂可为任何常用的压敏型粘合剂或那些在皮肤上快速固化的粘合剂(诸如氰基丙烯酸酯)。所述粘合剂可位于柔性的或固体的背衬上以使取样更容易。恒压装置(例如Desquame Pressure Instrument,CuDerm;Dallas,TX)可用于在取样期间向粘合剂装置施压。
来自组织的样品可通过本领域熟知的许多方法进行分离。用于分离样品的侵入性方法包括使用针(例如在血液取样期间)、以及不同组织的活组织检查、起泡和激光穿孔。由于这些技术的侵入性实质,存在提高的死亡率和发病率风险。此外,侵入性技术能够非故意地影响皮肤状态,这可能导致不精确的或错误的结果。此外,侵入性技术难以对大群体实施。侵入性技术可能导致受试者不适并可能导致感染或其它副作用的风险增大。本发明提供用于测量皮肤氧化应激反应和氧化损伤的生物标记的非侵入性方法。
术语“客观地”指无成见或偏见的。另选的,任何专家或自我评估本质上是“客观的”。
术语“归一化”和/或“归一的”指一组头皮屑患者接近正常群体状态的程度。
术语“标准化”和/或“标准化的”指就绿过氧物酶而言,相对于在对应的粘合剂或粘合剂制品上测得的蛋白质的量的生物标记值。就氧化脂质而言,标准化是指相对于对应的非氧化母体脂质的氧化脂质的值。一个非限制性示例将为ng氧化脂质/ng母体脂质或pg绿过氧物酶/μg可溶解蛋白质。
术语“基线”指在研究开始时收集的信息,从中测量研究中存在的变化。
在本发明的另一个实施例中,存在许多可使用的另选的“非侵入性”取样方法。
SebutapeTM:这是一种非侵入性方法,其中SebutapeTM(丙烯酸类聚合物膜;CuDerm;Dallas,TX)仅有非常轻微的粘性,并且可被施用并在不引起不适的情况下从甚至看得见红肿的皮肤移除。通过这种技术回收/测定的生物标记已经包括蛋白质(例如细胞因子)、肽(例如神经肽)、和小分子(脂质)。在历史上,制造并售卖这种胶带用于皮脂收集并且因此能够用于脂质分析。
胶带是聚丙烯酸酯粘合剂,也由CuDerm制造。其可用于回收与SebutapeTM相同的生物标记,但是也移除某些表皮结构蛋白(例如角质、包膜素)。其也已经被用于回收作为全身炎症标记的皮质醇和血清白蛋白、和小分子(组胺)以及角质层脂质。
杯擦洗(Cup Scrubs):杯擦洗(Cup Scrubs)通常在缓冲液、非离子表面活性剂或有机溶剂(例如乙醇)的存在下直接从皮肤表面提取蛋白质。杯擦洗(Cup Scrubs)主要用于回收可溶解的生物标记诸如细胞因子,但是也可用于回收小的有机分子。从杯擦洗中能够回收并定量比胶带剥除法多得多的细胞因子。这可能是由于若干原因。(a)由于存在洗涤剂并且它们是液体的,杯擦洗法最可能地取样与胶带剥除法不同的蛋白质组。(b)用杯擦洗法,不必在收集样品后进一步提取细胞因子,因为它们已经存在于溶液中。
毛发拔除:拔除毛发是通常使用镊子从拔除对象身上通过机械拔出去除人或动物毛发的方法。毛发拔除的毛囊区域通常在缓冲液和非离子表面活性剂存在的情况下进行提取以回收可溶解蛋白质生物标记诸如细胞因子,并且也能够用有机溶剂提取以回收小的有机分子如脂质。
动物(即,狗)收集方法:D-SquameTM胶带样品从狗皮肤上通过分开它们的毛皮(无剃刮)来收集。可从胶带中分析与皮肤炎症、分化和屏障完整性相关的多种生物标记,其包括总蛋白、可溶解蛋白、皮肤多个分析物特征(皮肤MAP)、皮肤细胞因子和角质层脂质(神经酰胺、胆固醇、脂肪酸)。
在本发明的一个实施例中,本发明提供非侵入性地获取用于分离绿过氧物酶和氧化脂质的样品的方法和分析。
在一个实施例中,使用粘合剂装置可用于实现此类取样。
在准备此类用于头皮屑取样的取样研究中,在基线随访中有资质的分级人员将完成各受试者的头皮附着鳞屑评分(ASFS)分级并且最高的片状剥落八分体将被鉴定用于胶带剥除取样。最高的片状剥落八分体将在基线和不同时间点进行取样。将在各时间点上从每个受试者中收集胶带剥除样品。
按需重复所述胶带剥除取样额外若干次,在之前的取样区域顶部的相同部位放置各胶带盘。在收集样品后将胶带置于标记板中进行适当标记的孔内。
在取样后进行提取和定量程序。在本发明的一个实施例中,来自胶带样品提取物的绿过氧物酶和氧化脂质的定量可经由基于抗体的免疫测定法或通过LC/MS/MS的分析进行。在本发明的这一实施例中,准备基于抗体的分析或LC/MS/MS分析时进行样品提取。
对于绿过氧物酶方法,将适当的标准提取缓冲液加入每个收集管中,并且随后在冰上超声处理提取30分钟。从胶带剥除物中分离各提取溶液并将每个样品的等分试样置于96孔聚丙烯板的指定位置。然后用常规试剂诸如白蛋白补充胶带样品的提取物等分试样以帮助防止分析物在实验室器具壁上的损失,将其转移到96孔聚丙烯深孔板上并冻存在-80℃用于绿过氧物酶分析。另一等分试样不补充试剂并且用BCATM Protein Assay Kit,Pierce catalog#23227分析可溶解的蛋白质。
在提取过程后,可通过常规方法制备绿过氧物酶标准品和对照物。绿过氧物酶用来自Mesoscale Discovery的绿过氧物酶免疫测定试剂盒进行定量。可将结果报告为绿过氧物酶的量/胶带剥除物的量,或者可通过用绿过氧物酶的量除以也存在于胶带剥除提取物中的蛋白质的量将结果标准化。已经单独描述了蛋白质方法。通过标准统计方法和计算进行数据分析。
在本发明的另一个实施例中,可使用反相梯度高效液相色谱法与串联质谱仪(HPLC/MS/MS)进行来自粘合剂制品、胶带剥除物的提取物的氧化脂质的定量。
将得自人类受试者的头皮的胶带剥除物(单个或多个胶带剥除物)置于单个聚丙烯琥珀色小瓶或玻璃琥珀色小瓶中,并且随后用提取溶剂(0.1%的丁基化羟基甲苯的甲醇溶液,w/v)涡旋10分钟来提取。使用反相梯度高效液相色谱法与串联质谱仪(HPLC/MS/MS)分析标准品和头皮胶带剥除物的提取物。表1中列出的分析物(氧化或非氧化脂质)和ISTD通过阳离子电喷(ESI)进行监控。通过给信号绘图构建标准曲线,本文将其定义为各标准品对对应于标准品的各分析物质量的峰面积比率(峰面积分析物/峰面积ISTD)或仅为峰面积分析物。然后使用生成的回归公式反推在校准基准和人头皮提取物样品中的每种分析物的质量。可将结果报告为氧化脂质的质量/胶带剥除物的质量,或者可通过用氧化脂质的量除以也存在于胶带剥除提取物中的对应母体非氧化脂质的量将结果标准化。此外,结果可通过用存在于胶带剥除提取物中的对应蛋白质的量来标准化氧化脂质的量进行报告。标准化也可通过收集去除的细胞、干燥细胞并称重细胞来完成。
表1-分析物
方法延伸
虽然上文描述了使用的确切方法,但在上述多个步骤中可使用许多替代方法,它们是逻辑延伸。用于从胶带剥除物中分离绿过氧物酶和氧化脂质的提取溶剂可为任何合适的含水的、有机物或有机物/含水的混合物,其提供合适的回收。由于LC/MS/MS和基于抗体的免疫测定法的高选择性和敏感度,一般认为它们是用于定量分析生物基质中有机分子的最先进方法。然而,可使用提供所需的敏感度和选择性的任何分析技术和/或其它方法。例如,已经使用了用于评估生物分子的其它方法,所述方法包括:毛细管电泳、超临界流体与其它色谱分离技术和/或它们的组合。类似地,也已经使用无分离技术的仪器方法,包括核磁共振光谱法、质谱法、电化学和荧光测定法。此外,也已经使用配体结合方法,诸如竞争性和非竞争性酶联免疫吸附测定法(ELISA)和放射性免疫测定(RIA)或者其它标记方案。在蛋白质分析中基于酶的测定法有长期的应用历史。使用基于细胞或组织的生物测定方法也可用作检测手段。在本发明的一个实施例中,毛发拔除引起的氧化应激反应和氧化损伤的生物标记的定量可利用与用于胶带剥除样品的方法相同的碱性提取和分析方法进行。
胶带剥除提取物的蛋白质测定:
用上述适合方法测得的皮肤胶带剥除样品上的绿过氧物酶含量可用胶带剥除提取物中存在的蛋白质的量进行标准化。通过用绿过氧物酶的量除以胶带剥除提取物中的蛋白质的量完成标准化。
胶带剥除提取物中的蛋白质的量或用于测定皮肤上绿过氧物酶含量的等同基质可使用文献中描述的多种蛋白质测定方法进行测定。此类方法的实例包括总氮测定、总氨基酸测定和基于任何比色、荧光、化学发光方法的蛋白质测定。这些方法可涉及或可不涉及在蛋白质测定前进一步制备胶带剥除提取物的样品。下文给出了胶带剥除提取物中用于蛋白质测定的特定方法的非限制性实例。对蛋白质测定方法、它们的适用性和限制的综述在Thermo Scientific Pierce Protein Assay Technical Handbook中进行了描述,其可从下文的链接中下载,以引用方式并入本文。www.piercenet.com/Files/1601669_PAssayFINAL_Intl.pdf.关于蛋白质测定的其它信息可见于Redinbaugh,M.G.和Turley,R.B.(1986),Adaptation of the bicinchoninic acid protein assay for use with microtiter plates and sucrose gradient fractions.Anal.Biochem.153,267-271,以引用方式并入本文。
用BCATM Protein Assay Kit(Pierce)提取并分析取样自人皮肤的粘合带的蛋白质含量。用常规的提取缓冲液提取取样自人皮肤的胶带剥除物。在提取后,将胶带提取物的等分试样转移到96-孔聚丙烯深孔板中并储存在2-8℃用于蛋白质测定。
BCATM Protein Assay Kit的作用机制为在碱性介质中由蛋白质将Cu2+还原成Cu1+并由二喹啉甲酸(BCA)敏感选择性比色检测Cu+1。通过一个Cu1+离子螯合2个BCA分子形成的紫色反应产物表现出在562nm波长处的强吸光度。使用酶标仪测量光密度(OD)。提高的牛血清白蛋白(BSA)的浓度(以微克每毫升(μg/mL)表示)在该测定法中用于生成校准曲线。从BSA原液中制备的合适测定QC将用于监控样品分析期间的测定法性能。
在本发明的一个另选的实施例中,可直接测量粘合剂或粘合剂制品上的蛋白质来完成蛋白质测定,诸如用850A(CuDerm Corporation,Dallas,Texas)测量蛋白质。
在本发明的另一个实施例中,另外的氧化应激反应标记物(除不饱和脂肪酸氢过氧化物/氢氧化物、胆固醇氢过氧化物/氢氧化物和角鲨烯氢过氧化物/氧化物/氢氧化物之外)可包括下列:
热激蛋白(Hsp)27
Hsp27的细胞保护特性来源于它调节反应性氧物质并提高谷胱甘肽含量的能力。
热激蛋白27(HSP27)属于小分子量热激蛋白(HSP)家族(12–43kDa)。HSP27和小分子量HSP家族的其它成员共有一个保守的c-末端结构域,α-晶状体蛋白结构域,它与脊椎动物眼α-晶状体蛋白[1]相同。HSP27初始响应于热休克而被表征为伴侣蛋白,其促进损伤蛋白质的正确重折叠。对HSP27的持续研究揭示该蛋白响应于非热休克的细胞应激情况;例如氧化应激反应和化学应激。在氧化应激反应期间,HSP27作为抗氧化剂起作用,通过提高细胞内谷胱甘肽的含量并降低细胞内铁含量来降低反应性氧物质(ROS)的含量。
蛋白质的氧化修饰
在生物学体系中的蛋白质氧化通过半胱氨酰硫醇的天然自氧化、蛋白质与反应性氧物质(ROS)的相互作用以及通过由氧化酶催化的精细受控的反应而进行。蛋白质与ROS的反应能够引起半胱氨酸、甲硫氨酸、酪氨酸、苯丙氨酸和色氨酸残基的氧化。甲硫氨酸氧化通过测定甲硫氨酸亚砜进行监控,酪氨酸氧化可通过形成的二酪氨酸的量进行监控,苯丙氨酸的氧化通过形成o-酪氨酸和m-酪氨酸进行监控,色氨酸残基的氧化通过监控N-甲酰犬尿氨酸、犬尿氨酸和/或喹啉酸进行监控。另外,白蛋白cys34残基的共价和氧化修饰已经被提出作为温和氧化应激反应的特定生物标记。这些蛋白质修饰加合物残基通常在酶水解完全或化学消化之后进行测定。
蛋白质可经由氧化途径进行修饰,氧化途径涉及形成蛋白质羰基,其主要由赖氨酸、脯氨酸和精氨酸残基形成。赖氨酸经由氧化脱氨基形成2-氨基己二酸半醛(AASA),并且谷氨酸半醛(GSA)通过氧化脯氨酸和精氨酸残基形成。AASA和GSA能够在分别还原成6-羟基-2-氨基己酸和5-羟基-2-氨基戊酸后进行检测。蛋白质羰基化也能够通过在用2,4-二硝基苯肼衍生化后基于ELISA的方法进行测定。
另外,蛋白质可通过氧化途径,通过与由多不饱和脂肪酸氧化形成的α,β-不饱和烯醛反应(参见不饱和烯醛与蛋白质的反应产物和硫醚氨酸途径)并且通过与糖形成早期糖化加合物(EGA)和高级糖化产物(AGE)(参见EGA和AGE)而被修饰。
DNA氧化和羟基化核苷酸1
DNA损伤一般是氧化应激反应的一种量度,主要原因是由于内源性反应性氧物质(ROS)引起的自由基损伤。对完整DNA的氧化损伤可使用COMET测定法进行测量。氧化损伤可通过监控多种羟基化核苷酸进行测量,包括也称为8-氧代脱氧鸟苷(8-oxodG)的8-羟基脱氧鸟苷(8OHdG)、4,6-二氨基-5-甲酰胺基嘧啶(FapyAde)和2,6-二氨基-4-羟基-5-甲酰胺基嘧啶(FapyGua)。
异构前列腺素1
异构前列腺素是由多不饱和脂肪酸(PUFA),诸如花生四烯酸(AA)和ω-3二十碳五烯酸(EPA)的自由基催化氧化形成的一系列前列腺素样异构体,通常PUFA氧化发生于磷脂形式。异构前列腺素来源于AA氧化,产生F-型前列腺环(称为F2-异构前列腺素)并产生5-F2-系列IsoP、8-F2-系列IsoP、12-F2-系列IsoP和15-F2-系列IsoPs8-系列。相似地,D/E-环和A/J-环异构前列腺素也由AA形成。F3家族的异构前列腺素相似地由EPA形成并产生5-F3-系列、8-F3-系列、11-F3-系列、12-F3-系列、15-F3-系列和18-F3-系列异构前列腺素。
α,β-不饱和醛1
多不饱和脂肪酸的氧化常响应于氧化应激反应而发生,产生由脂肪酸氢过氧化物形成引发的自由基,其能够发生进一步反应以提供生物学体系中的广泛多种α,β-不饱和烯醛,诸如丙二醛、丙烯醛、丁烯醛、4-羟基壬烯醛、4-羟基己烯醛和4-氧代-壬烯醛。这些α,β-不饱和烯醛已经作为氧化损伤的生物标记。
α,β-不饱和烯醛与蛋白质的反应产物和硫醚氨酸途径
α,β-不饱和烯醛是反应性亲电体并且与多种亲核化合物形成产物,这些亲核化合物包括共价蛋白质加合物,其称为高级脂肪氧化最终产物(ALE)诸如己酰基-赖氨酸、己酰基-组氨酸、Ne-(3-甲基吡啶)赖氨酸,并且与硫醚氨酸化合物(谷胱甘肽、半胱氨酸和硫醚氨酸)形成硫醚(例如1,4-二羟壬硫醚氨酸、3-羟丙基硫醚氨酸和羧乙基硫醚氨酸)。
早期糖化加合物(EGA)和高级糖化最终产物(AGE)
蛋白质的糖化是一系列非酶的、复杂的平行和依序发生的反应,统称为美拉德反应,并且发生在所有组织和体液中。糖化加合物可通过蛋白质与葡萄糖和反应性α-氧代醛诸如乙二醛、甲基乙二醛和3-脱氧葡糖醛酮及其它糖类衍生物的反应而形成。糖化中的早期反应导致形成果糖酰-赖氨酸和N-末端氨基酸残基衍生的果糖胺,并且称为早期糖化加合物(EGA)。晚期反应形成稳定的最终阶段加合物,称为高级糖化最终产物,诸如单赖氨酰加合物(羧甲基赖氨酸(CML)、羧乙基赖氨酸(CEL)和吡咯素)、单缬氨酰加合物(羧甲基缬氨酸(CMV)和羧乙基缬氨酸(CEV))、氢化咪唑酮、双(赖氨酰)咪唑交联物(GOLD、MOLD、DOLD)和来源于赖氨酸与精氨酸交联的戊糖素。当蛋白质通过蛋白质水解作用降解或者当蛋白质通过化学裂解降解时,释放EGA和AGE。AGE的形成和积聚已经涉及到了衰老相关疾病的进展。过去20年的研究已经使AGE涉及到与衰老相关的大多数疾病中。CML可为衰老、动脉粥样硬化、和糖尿病中的氧化应激反应和长期蛋白损伤的一般标记物。
作为氧化应激反应的生物标记的抗氧化剂1
内源性抗氧化剂在控制由自由基机制引起的氧化损伤中起到关键的防御作用。关键的内源性抗氧化剂包括抗坏血酸(AsA)、谷胱甘肽(GSH)、α-生育酚和辅酶Q 10(CoQ)。这些内源性氧化还原(氧化和还原形式)抗氧化剂的含量改变可用作氧化应激反应的量度。
(1)Biomarkers for Antioxidant Defense and Oxidative Damage:Principles and Practical Applications;G.Aldini,K-J Yeum,E.Niki和R.M.Russell,eds,Wiley-Blackwell,Iowa,2010,该文献以引用的方式并入本文。
实例
用于评估氧化应激反应和氧化损伤的基本过程
受试者由有资质的分级人员进行评估以确定他们的头皮状态。头皮屑受试者由有资质的分级人员确定他们的可见片状剥落水平。对无头皮屑的健康头皮受试者进行基线评估以确定每个生物标记的归一化水平。受试者通过由有资质的分级人员在两个单独的临床研究中进行鉴定;研究#1和研究#2。在研究#1中,有60个无头皮屑受试者,它们进行MPO含量的基线评估。有119个头皮屑患者用包含1%的ZPT的去头皮屑洗发剂治疗,115个头皮屑患者用包含1%的硫化硒的去头皮屑洗发剂治疗,并且60个头皮屑受试者用不含去头皮屑活性物质的非去头皮屑洗发剂治疗。评估他们的MPO基线含量,并且在使用产品1周、2周和3周后分别再次评估。在研究#2中,有30个无头皮屑受试者进行氧化脂质的基线评估。有60个头皮屑受试者用去头皮屑洗发剂治疗,并且有60个头皮屑受试者用不含去头皮屑活性物质的非去头皮屑洗发剂治疗。评估他们的基线氧化脂质,并且在使用产品3周后再次评估。
受试者在用去头皮屑洗发剂治疗前,用常规的无调理剂的非去头皮屑洗发剂洗两周。头皮屑受试者用去头皮屑洗发剂(包含吡啶硫酮锌、或硫化硒的洗发剂组合物)或无去头皮屑活性物质的非去头皮屑洗发剂治疗三周,从由有资质的分级人员在基线随访上测定的最高片状剥落八分体中收集胶带剥除样品。对于头皮屑受试者,在基线和产品治疗后获取头皮胶带剥除物。对于无头皮屑受试者,仅在基线获取头皮胶带剥除物。将胶带保存在-80℃直到进行提取。通过分开毛发进行含头皮屑部位的取样,所述取样通过施用胶带(CuDerm Corporation)并按需摩擦该胶带。对于无头皮屑受试者,对无片状剥落的部位取样。将胶带置于预先标记的12孔培养盘中进行贮藏。
将用常规的提取缓冲液和在冰上超声处理来提取样品。胶带样品提取物的等分试样随后被转移到预先标记的聚丙烯收集管中并冻存在-80℃下以分析MPO和氧化脂质。另一等分试样指定用BCATM Protein Assay Kit,Pierce catalog#23227进行MPO提取物的可溶解蛋白质分析。
在提取后,通过基于抗体的免疫测定法或LC/MS/MS分析样品的绿过氧物酶和氧化脂质。化合物的有关定量值随后通过上文列出的用于绿过氧物酶的BCA蛋白质测定法所测定的提取物中的可溶解蛋白质的量或通过氧化脂质所对应的母体非氧化脂质的量进行标准化。对来自去头皮屑洗发剂治疗组的样品进行基线分析和治疗后分析,并且对无头皮屑组的样品仅进行基线分析。配对T检验用于分析非头皮屑(健康的)、头皮屑基线和经头皮屑治疗的受试者的差异。对经头皮屑治疗的受试者与无头皮屑受试者进行比较以确定在用去头皮屑产品治疗后的归一化程度。
结果概述
数据的统计学分析:收集在基线和治疗后的头皮屑受试者和在基线的无头皮屑受试者的数据。假设在受试者之间以及受试者内部分析物含量变化较大(基线->治疗),在分析前将数据转化成log10标度是更有效的。对当量log10比值(例如log10(Week 3/基线))进行统计学分析。将最后报告的结果重新转化成它们的初始标度(或者基线值的%变化)以便于说明。使用SAS JMP(版本7.0.2)软件进行所有统计学分析。使用≤0.20(双侧)的P值测定统计学差异。
图1中的数据说明头皮屑MPO含量比非头皮屑含量显著更高(P值=0.0005)。用上述适用方法测得的人头皮胶带剥除样品上的MPO含量可用胶带剥除提取物中存在的蛋白质的量进行标准化。从独立的无头皮屑组中测定MPO含量以确定正常皮肤MPO含量。通过用MPO含量除以胶带剥除提取物中的蛋白量完成标准化。
图2中的数据说明用去头皮屑洗发剂治疗一周后的MPO含量与基线含量相比减少77%,治疗两周后与基线含量相比减少87%,并且经3周时间后与基线含量相比减少89%(P值<0.0001)。MPO的减少符合与无头皮屑群体的含量比较所显示的改善。去头皮屑洗发剂展示与非去头皮屑洗发剂相比在所有治疗时间点上的显著改善(P值<0.0001)。这些MPO含量已经通过胶带剥除提取物中的蛋白质的量进行了标准化。
图3中的数据说明去头皮屑治疗将MOP含量恢复到上文图1中讨论的无头皮屑组的MOP含量。这是一种有用的有益效果传达手段,头皮屑群体期望恢复到正常和/或健康状态。
图4中的数据说明头皮屑HODE含量比非头皮屑含量显著更高(P值<0.001)。图4中的数据说明头皮屑SQOOH含量比非头皮屑含量显著更高(P值=0.13)。用上述适用方法测得的人头皮胶带剥除样品上的氧化脂质可用胶带剥除提取物中的氧化脂质除以它对应的母体非氧化脂质进行标准化。HODE含量已经通过用HODE含量除以胶带提取物中的亚油酸的量进行标准化,并且SQOOH通过除以胶带剥除提取物中的角鲨烯量进行标准化。
图5中的数据展示在用去头皮屑洗发剂治疗3周后测得的标准化氧化亚油酸(HODE)与基线相比的显著减少(P值<0.01)。减少符合与无头皮屑群体的含量比较所显示的改善。去头皮屑洗发剂展示与非去头皮屑洗发剂相比的显著改善(P值=0.005)。图5中的数据展示在用去头皮屑洗发剂治疗3周后测得的标准化角鲨烯氢过氧化物与基线相比的显著减少(P值<0.01)。减少符合与无头皮屑群体的含量比较所显示的改善。去头皮屑洗发剂展示与非去头皮屑洗发剂相比的显著改善(P值=0.013)。
在特定实施例中,此类性能评估可对比较在用去头皮屑组合物治疗前后的受试者的皮肤健康状态有利。例如,如果受试者转换或保持某一去头皮屑组合物或治疗方案,一些去头皮屑组合物可发挥更快的见效速度,这将被受试者体会到。允许客观测量受试者的特定皮肤健康有益效果的评估可允许在用特定去头皮屑组合物或治疗方案治疗前以及在受试者转换到特定去头皮屑组合物或治疗方案后比较受试者的状态。另外,此种评估可用作一种支持认证工具,其支持特定治疗或治疗方案声称提供的特定皮肤健康有益效果。例如,如果一种特定组合物或治疗方案宣称其将减少瘙痒症状,如本文所公开的评估可用于支持声称的具体健康状态有益效果,示出受试者的瘙痒不适情况已经减少了。可得益于去头皮屑组合物和治疗方案的皮肤健康非限制性状况包括瘙痒、片状剥落、过敏、皮肤屏障完整性、干燥、氧化应激反应和氧化损伤、自身防御、天然保护。
也可将许多分析的结果作为营销或广告信息来使用,以促进特定产品、产品组合和技术的有效性。可放置在产品包装上的可由本发明证实的广告宣传语的实例包括但不限于确立宣传语(例如,“临床证明”或“测试显示”)、用前和用后宣传语(例如,“用后头皮屑减轻到50%以下”)、单体宣传语、比较宣传语、因数宣传语(例如,“3倍的头皮屑减少量”)、以及预防和治疗宣传语。例如,产品包装可提及分析并且可展示产品的经客观证明的有效性或比较信息。另外,还可将分析数据用于与不同的生活习惯相关的临床信息,所述生活习惯可与或可不与不同的产品或产品组结合使用。
另一个实施例包括其中标准化生物标记在施用吡啶硫酮锌洗发剂后,在与施用前的生物标记的基线含量进行比较时存在变化。在另一个实施例中,标准化分子生物标记在施用硫化硒洗发剂后,在与施用前的生物标记的基线含量进行比较时存在变化。在另一个实施例中,可测量生物标记,其确定与治疗后的正常群体相比皮肤健康发生至少5%的改善。在另一个实施例中,与治疗后的正常群体相比皮肤健康发生至少10%,至少20%,至少30%,至少40%,至少50%,至少60%,至少70%,至少80%,至少90%和更高达100%的改善。在另一个实施例中,在头皮屑和非头皮屑(无治疗)之间可存在至少5%的差值。另外,在头皮屑和非头皮屑之间可存在至少10%的差值,在头皮屑和非头皮屑之间可存在至少20%,至少30%,至少40%,至少50%,至少60%,至少70%,至少80%,至少90%,以及更高达100%或更高的差值。
本文所公开的量纲和值不应理解为严格限于所引用的精确值。相反,除非另外指明,每个这样的量纲旨在表示所述值以及该值附近的函数等效范围。例如,所公开的量纲“40mm”旨在表示“约40mm”。
具体实施方式中的所有引用文献的相关部分均以引用方式并入本文;任何文献的引用不可解释为是对其作为本发明的现有技术的认可。当本文献中术语的任何含义或定义与引入本文以供参考的文献中相同术语的任何含义或定义冲突时,将以赋予本文献中那个术语的含义或定义为准。
尽管已用具体实施例来说明和描述了本发明,但是对那些本领域的技术人员显而易见的是,在不背离本发明的实质和范围的情况下可作出许多其它的改变和变型。因此,所附权利要求中旨在包括属于本发明范围内的所有这些改变和变型。
- 还没有人留言评论。精彩留言会获得点赞!