一种基于聚合酶等温扩增技术检测重金属离子的方法与流程
本发明属于分析化学或环境监测技术领域,具体涉及一种基于磁性纳米粒子和聚合酶等温扩增反应信号放大技术检测重金属镍离子的电化学方法。
背景技术:
镍是维持机体新陈代谢过程所必需的微量元素,其生物学作用极为广泛,但镍及其化合物又是常见的环境污染因子。镍广泛应用于电镀、汽车、电解、农药、医药、油漆等行业。镍可以通过大气吸入和饮食等多种途径进入人体,当体内积蓄过量时会造成鼻腔、肺和心脏等一系列疾病,甚至诱发癌症。因此,镍是环境、食品等介质中需要监控的重金属之一。目前,镍的常用测定方法有分光光度法、原子光谱法、电感耦合等离子体质谱法和荧光法等。这些方法不仅需要高精密度的仪器,对操作技术要求高,且检测周期长、检测成本高。因此,需要发展简单、快速,且可实现痕量检测镍的新方法和新技术。
核酸等温扩增技术是近年发展起来的一种全新的核酸体外扩增技术,其反应过程始终维持在恒定的温度下,通过添加不同活性的酶和各自特异性引物(或不加)来达到快速核酸扩增的目的。与常规PCR技术相比,不需要模板的热变性、温度循环、电泳及紫外观察等过程。核酸等温扩增技术对仪器的要求大大简化,反应时间大大缩短,具有简单、快速、特异性强的特点,现已被广泛应用于各类核酸、病毒和微生物的检测。1994年,通过体外筛选技术得到脱氧核酶(DNAzyme)及其催化性能的发现,促进了核酸等温扩增技术的快速发展。脱氧核酶是利用体外分子进化技术获得的一类具有高效催化活性和结构识别能力的单链DNA分子。与RNA相似,脱氧核酶可以形成复杂多样的折叠结构并显示出催化功能,可以催化DNA或RNA切割、DNA连接、DNA水解等多类反应。与传统蛋白酶相比,脱氧核酶具有稳定性高,相对分子质量小,易化学合成、修饰与复制,受酸度等环境因素影响小等优势。脱氧核酶非常容易进行以核酸为识别模式或者信号表达模式的生物传感器构建。此外,脱氧核酶具有对DNA进行连接与断裂的催化能力,可以应用到基因调控与治疗。
磁性纳米粒子是近年来发展起来的一种新型纳米材料,由于磁性纳米粒子具有特殊的磁导向性、超顺磁性、易清洗、易分离,以及表面可连接生化活性功能基团等特性,使其在核酸分析、临床诊断、靶向药物、细胞分离和酶固定化等领域的应用得到了广泛的发展。磁性纳米粒子的这些特性可以显著地提高生物传感器检测的灵敏度,缩短生化反应时间,提高检测通量,为生物传感器领域的应用开辟了广阔的前景。
本发明基于磁性纳米粒子和聚合酶等温扩增反应作为信号放大技术,利用Ni2+对DNA酶的RNA位点特异性切割和电化学方法,实现对重金属Ni2+的超痕量检测。为了增加分析速率和稳定性,磁纳米粒子表面发生聚合酶等温扩增反应形成的长链DNA复合物采用金磁电极吸附固定,该方法具有简单、快速、灵敏度高等优点。
技术实现要素:
本发明的目的之一是设计不同序列的DNA,构建一种快速、灵敏的电化学传感器。
本发明的目的之二是提供一种基于磁性纳米粒子和聚合酶等温扩增反应放大技术联用构建电化学传感器的制备方法。
本发明的目的之三是将构建的电化学传感器用于重金属离子的高灵敏、快速检测。
本发明的具体技术方案如下:
1. 一种基于磁性纳米粒子和聚合酶等温扩增反应放大技术联用构建重金属离子电化学传感器
首先制备Fe3O4@Au核-壳磁性纳米粒子,将DNA核酸链S1通过Au-S键固定到Fe3O4@Au表面。Ni2+存在时,核酸链S1在rA位点被Ni2+切割为两段,导致其3′端核酸链成为单链,S1的3′端单链与另一条互补序列的DNA单链S2发生杂交结合。当加入聚合酶和底物dNTP后,在S2的诱导延伸作用下促使S1打开并发生等温扩增放大反应,最后将亚甲基蓝(MB)嵌入到双链DNA空隙。形成的长链DNA复合物通过磁性富集在金磁电极表面实现电化学响应信号的放大。根据电化学信号的增强实现对标准溶液或样品溶液中Ni2+浓度的定量测定。
2. 一种基于磁性纳米粒子和聚合酶等温扩增反应放大技术联用构建重金属离子电化学传感器的制备方法
(1)Fe3O4@Au核-壳磁性纳米粒子的制备
首先采用共沉淀法制备Fe3O4,将FeCl2、FeCl3和浓HCl溶于超纯水中,超声脱氧。将上述混合溶液滴加到NaOH溶液中,80℃搅拌下通N2气保护,得到Fe3O4磁性纳米粒子。在Fe3O4/乙醇溶液中加入3-氨丙基三乙氧基硅烷,对Fe3O4粒子表面进行氨基化。在上述溶液中加入HAuCl4水溶液,以柠檬酸钠为还原剂,得到Fe3O4@Au核-壳磁性纳米粒子。
(2)双链DNA标记Fe3O4@Au粒子的制备
将步骤(1)得到的Fe3O4@Au磁性纳米粒子与DNA核酸链S1在37℃下反应12 h,孵化,磁分离,得到S1标记的Fe3O4@Au。将Ni2+与S1标记的Fe3O4@Au在37℃下孵化1 h,核酸链S1在DNA酶位点被Ni2+切割为两段,核酸链S1的5′端的部分碱基缺失导致其3′端核酸链成为单链,之后于95℃加热5 min,引发S2可与S1 3′端互补单链在37℃杂交3 h形成双链DNA,得到双链DNA标记的Fe3O4@Au磁性纳米粒子。
(3)聚合酶等温扩增反应
在步骤(2)得到的双链DNA标记的Fe3O4@Au Tris-HCl缓冲液中加入聚合酶和底物dNTP,37℃下杂交反应2 h,得到长链DNA复合物。最后,DNA复合物与亚甲基蓝(MB)在37℃反应3 h,将MB嵌入到Fe3O4@Au表面的双链DNA中。
(4)Ni2+电化学传感器的制备
将工作电极(金磁电极)在piranha溶液中浸泡1 h,超纯水清洗。然后分别用0.3 mm和0.05 mm的Al2O3抛光粉打磨,依次在超纯水、无水乙醇、超纯水中超声清洗。最后在0.5 M H2SO4溶液中,以50 mV/s的扫速在-0.2~1.6 V之间进行循环伏安扫描30圈,活化电极。N2气吹干备用。步骤(3)得到的长链DNA复合物通过磁性富集作用修饰到活化的金磁电极表面,构建重金属Ni2+电化学传感器。
3. Ni2+离子的检测方法
(1)使用电化学工作站以三电极体系进行测试,饱和甘汞电极为参比电极,铂丝电极为对电极,修饰的金磁电极为工作电极,在10 mM pH 7.4的PBS缓冲溶液(包含20 mM NaCl和0.1 M NaClO4)中进行测试;
(2)用微分脉冲伏安法(DPV)对重金属离子进行检测,设置扫描电位范围为0~1.2 V,扫描速率为0.1 V/S,记录峰电流的大小,并保存数据;
(3)根据所得DPV峰电流的大小与Ni2+离子浓度的关系,绘制工作曲线;
(4)采用标准加入法,在水样溶液中加入不同浓度的Ni2+离子标准溶液,按照工作曲线的绘制方法对不同浓度的Ni2+离子进行检测。
与现有技术相比,本发明具有以下优点和有益成果:
(1)本发明利用磁性纳米粒子和聚合酶等温扩增反应双重信号放大技术联用构建重金属离子电化学传感器。
(2)本发明将Fe3O4@Au核-壳磁性纳米粒子引入到电化学传感器的构建中,采用金磁电极,从而增加了修饰电极的稳定性。
(3)本发明利用Ni2+对DNA酶特异性切割作用,设计特定序列的DNA,从而增强了电极对重金属离子的选择性,增加了传感器的特异性。
(4)本发明制备的电化学传感器用于重金属Ni2+离子的检测,具有较高的选择性和抗干扰能力,线性范围宽,检测限低,可用于实际水样中超痕量Ni2+离子的测定。
附图说明
图1是使用本发明的磁性纳米粒子和聚合酶等温扩增反应放大技术检测重金属Ni2+的示意图;
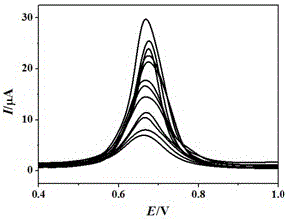
图2是使用本发明的磁性纳米粒子和聚合酶等温扩增技术检测不同浓度Ni2+的DPV曲线图;
图3是使用本发明的磁性纳米粒子和聚合酶等温扩增技术检测Ni2+的标准曲线图,其中横坐标是Ni2+的浓度,单位是mM或M,纵坐标是DPV峰电流,单位是mA。
具体实施方式
下面结合具体实施例进一步说明本发明,但不构成对发明的进一步限制。
实施例1 一种基于磁性纳米粒子和聚合酶等温扩增反应放大技术联用检测重金属Ni2+的方法
本发明基于磁性纳米粒子和聚合酶等温扩增反应放大技术联用检测重金属Ni2+的方法原理如图1所示。核酸链S1通过Au-S键固定到Fe3O4@Au磁性纳米粒子表面。Ni2+存在时,核酸链S1在DNA酶位点被Ni2+切割,核酸链S1的5′端的部分碱基缺失导致其3′端核酸链成为单链,进而与另一条互补序列的DNA单链S2发生杂交结合。当加入聚合酶和底物dNTP后,在S2的诱导延伸作用下促使S1打开并发生等温扩增放大反应。最后将MB嵌入到双链DNA空隙,形成的长链DNA复合物通过磁性富集在金磁电极表面实现电化学响应信号的放大。根据电化学信号的增强实现对标准溶液或样品溶液中Ni2+浓度的定量测定。
实施例2 寡核苷酸序列设计
本发明所设计的寡核苷酸序列由中国上海Sangon生工生物工程上海(股份)有限公司合成,并通过 HPLC纯化检验,冻干。本发明设计的寡核苷酸序列如下:
S1:5’- ACT CAC TAT︱RA︱GGA AGA GAT GGA CGT GAG TCG ACT AGA CAC GTC CAT CTC TGC AGT CGG GTA GTT AAA CCG ACC TTC AGA CAT AGT GAG TAG CA -3’-SH;
S2:5’- CTA CTC ACT ATG TCT -3’;
将寡核苷酸溶解在超纯灭菌水中,-18℃保存备用。
实施例3 Fe3O4@Au核-壳磁性纳米粒子的制备
取1 g FeCl2×4H2O、2.6 g FeCl3×6H2O和0.425 mL浓HCl溶于100 mL水中,超声脱氧。将上述混合液滴加到125 mL 0.75 M NaOH溶液中,N2保护下80℃搅拌,得到Fe3O4磁性纳米粒子。配制5 g/L的Fe3O4/乙醇溶液25 mL,超声分散,滴加0.4 mL 3-氨丙基三乙氧基硅烷,室温下搅拌7 h,稀释至1 g/L。分别加入14 mL 0.6 M HAuCl4×4H2O和0.3 mL 0.2 M柠檬酸钠溶液,室温下超声处理,溶液颜色由浅黄变为黑色,得到Fe3O4@Au核-壳磁性纳米粒子。
实施例4 寡核苷酸S1和S2标记Fe3O4@Au核-壳磁性纳米粒子
取1 mg Fe3O4@Au粒子分散于1 mL 0.6 mM的S1溶液中, 37℃恒温水浴混合12 h,PBS缓冲液清洗,制得S1标记的Fe3O4@Au粒子。取60 mL S1标记的Fe3O4@Au与60 mL不同浓度的Ni2+溶液在37℃恒温水浴中孵化1 h,Tris-HCl缓冲液清洗,95℃加热5 min。再取60 mL 1 mM S2与上述溶液杂交3 h,制得S1和S2双链DNA标记的Fe3O4@Au核-壳磁性纳米粒子。
实施例5聚合酶等温扩增反应
取60 mL实施例4制得的双链DNA标记Fe3O4@Au核-壳磁性纳米粒子,用20 mM pH 7.4 Tris-HCl(含60 mM KCl和10 mM MgCl)将上述溶液稀释至600 mL,然后与200 mM dNTP和25 U/mL 聚合酶于37℃下杂交反应2 h,Tris-HCl缓冲液清洗,制得长链DNA复合物修饰的Fe3O4@Au粒子。最后再与20 mM MB于37℃下杂交3 h,Tris-HCl缓冲液清洗。
实施例6 电化学传感器制备
将金磁电极在piranha溶液中浸泡1 h,超纯水清洗。然后分别用0.3 mm和0.05 mm的Al2O3抛光粉打磨,依次在超纯水、无水乙醇中超声清洗。在0.5 M H2SO4溶液中,以50 mV/s的扫速在-0.2~1.6 V之间进行循环伏安扫描30圈,活化电极。N2气吹干备用。将处理好的金磁电极浸入实施例5所制得的溶液中,利用磁性富集作用将其固定在金磁电极表面,制得Ni2+电化学传感器。
实施例7 重金属离子的检测
使用电化学工作站以三电极体系进行测试,饱和甘汞电极为参比电极,铂丝电极为对电极,金磁电极为工作电极。采用微分脉冲伏安法测定重金属Ni2+浓度,以10 mM pH 7.4 PBS (含20 mM NaCl和0.1 M NaClO4) 为缓冲液,电位范围为0~1.2V,电位增幅为4 mV,脉冲周期为0.5 s。微分脉冲曲线峰电流与不同Ni2+浓度的关系曲线如图2所示,DPV峰电流与Ni2+浓度在100 aM ~ 1 mM范围内呈现良好的线性关系(图3),相关系数R 为0.9962,线性方程为ipc (mA) = 2.01logc (M) + 37.56,检出限为10 aM。本发明提出的传感器相比较其他传感器,具有更宽的线性范围和更低的检出限,采用磁性纳米粒子和聚合酶等温扩增反应放大技术可实现Ni2+的超痕量检测。
实施例8 样品测定
将待测样品溶液代替Ni2+离子标准溶液,采用标准加入法,按照标准曲线方法对样品溶液中的Ni2+进行测定。测定结果表明,检测结果与加入的Ni2+标准溶液浓度一致,具有满意的回收率和相对标准偏差,本发明制备的电化学传感器能用于实际样品中Ni2+的测定。
上面结合附图对本发明实施例进行了说明,但本发明不限于上述实施例,还可以根据本发明的发明创造的目的做出多种变化,凡依据本发明技术方案的精神实质和原理下做的改变、修饰、替代、组合、简化,均应为等效的置换方式,只要符合本发明的发明目的,只要不背离本发明基于磁性纳米粒子和聚合酶等温扩增反应放大技术联用构建重金属离子电化学传感器的制备方法,超痕量重金属离子电化学测定方法及应用的技术原理和发明构思,都属于本发明的保护范围。
序列表
生工生物工程(上海)股份有限公司
DNA人工序列
S1:5'-ACT CAC TAT︱RA︱GGA AGA GAT GGA CGT GAG TCG ACT AGA CAC GTC CAT CTC TGC AGT CGG GTA GTT AAA CCG ACC TTC AGA CAT AGT GAG TAG CA -3'-SH;
S2:5'-CTA CTC ACT ATG TCT-3';
- 还没有人留言评论。精彩留言会获得点赞!
- 环介导等温扩增多重耐药基因oqxAB的检测引物、检测试剂盒及检测方法与制造工艺
- 一种气单胞菌的核酸等温扩增检测试剂盒及其检测方法与制造工艺
- 一种霍乱弧菌环介导等温扩增试剂盒及其应用的制造方法与工艺
- 用于检测番茄晚疫病菌的LAMP引物组合物和应用的制造方法与工艺
- 基于颜色判定的环介导等温扩增(LAMP)技术检测雪松疫霉根腐病菌的制造方法与工艺
- Sortase A介导的(S)‑羰基还原酶寡聚体高效催化(S)‑苯基乙二醇的合成的制造方法与工艺
- 用于旋转机器中的超导线圈的等温支承部和真空容器的制造方法与工艺
- 用于扩增细胞群的方法、试剂盒及装置与制造工艺
- 基于环介导等温扩增消光技术的转基因玉米MIR604检测方法与制造工艺
- 基于环介导等温扩增消光技术的玉米检测方法与制造工艺
- 一种霍乱弧菌环介导等温扩增试剂盒及其应用的制造方法与工艺
- 用于检测番茄晚疫病菌的LAMP引物组合物和应用的制造方法与工艺
- 基于颜色判定的环介导等温扩增(LAMP)技术检测雪松疫霉根腐病菌的制造方法与工艺
- Sortase A介导的(S)‑羰基还原酶寡聚体高效催化(S)‑苯基乙二醇的合成的制造方法与工艺
- 用于旋转机器中的超导线圈的等温支承部和真空容器的制造方法与工艺
- 基于环介导等温扩增消光技术的转基因玉米MIR604检测方法与制造工艺
- 基于环介导等温扩增消光技术的玉米检测方法与制造工艺
- 一套鉴定甘蔗上三种短体线虫的环介导等温扩增引物及其试剂盒的制造方法与工艺
- RNA扩增方法与制造工艺
- 用于扩增核酸样品的等温方法与制造工艺