环介导等温扩增多重耐药基因oqxAB的检测引物、检测试剂盒及检测方法与流程
本发明涉及细菌基因检测技术领域,特别涉及环介导等温扩增多重耐药基因oqxAB的引物,还涉及一种用环介导等温扩增方法检测多重耐药基因oqxAB的试剂盒,还涉及用环介导等温扩增方法检测多重耐药基因oqxAB的检测方法。
背景技术:
质粒编码的多重耐药外排泵oqxAB最早是在研究喹乙醇耐药机制时予以发现。2003年,丹麦科学家Sorensen等首次从猪的粪便样品分离的大肠杆菌中发现了介导喹乙醇耐药性的质粒pOLA52。2004年,Hansen等从pOLA52质粒上发现了对喹乙醇耐药的外排泵基因oqxAB。由于其耐药机制非常符合RND家族的主动外排泵特征,因此属于质粒介导的RND家族。
Strahilevitz等研究发现,外排泵oqxAB基因可降低细菌对喹诺酮类药物的敏感性,因此将其归入质粒介导的喹诺酮类耐药机制(plasmid-mediated quinolone resistance,PMQR)中。Lars等研究表明,oqxAB不仅可以介导喹乙醇、喹诺酮类、氯霉素的耐药,其作用底物还包括洗必泰、西曲溴铵、三氯生等清洁剂、洗涤剂和消毒剂。另外研究中还发现,氟甲喹、卡巴氧、甲氧苄啶、四环素等药物的耐药现象也可以随着oqxAB基因而转移,分析原因表明oqxAB可以与其他药物的耐药基因共同转移。
目前,oqxAB已经在世界各地广泛发现,如丹麦、韩国、瑞士、日本、美国等,并大多出现于肠杆菌科细菌中,如大肠杆菌、沙门氏菌和肺炎克雷伯菌中。在研究人源和动物源oqxAB基因时,有关研究结果已经证实,动物源和人源耐药菌株具有相同的耐药特征,并且来源于同一株克隆菌株。因此含有oqxAB的肠杆菌科细菌已威胁人类的健康,给临床治疗带来了巨大的挑战。
对于多重耐药基因oqxAB的检测,目前的实验室诊断主要是基于PCR技术进行确证。但是PCR方法容易出现假阳性,并且检测成本高,操作比较复杂,检测时间长(一般需要2-3小时),这些都影响了临床携带oqxAB基因的检测结果。
环介导等温扩增方法(LAMP)是近年来新兴的一种基因扩增方法,对仪器设备要求不高,只需要一个恒温水浴锅或金属浴就可以,成本低,且临床上容易做到,检测时间较短,不超过1个小时,为快速、准确诊断基因的一种新方法。环介导等温扩增方法已经广泛应用于检测细菌的领域,并有很多相关专利获得授权。目前国内外均未见使用LAMP方法检测多重耐药基因oqxAB的报道。
技术实现要素:
为了解决PCR扩增容易出现假阳性、检测成本高、操作复杂、检测时间长的问题,增补使用LAMP检测多重耐药基因oqxAB的空白,本发明提供了使用环介导等温扩增多重耐药基因oqxAB的引物。本发明建立了一种多重耐药基因oqxAB的LAMP检测方法,根据oqxAB基因保守区的6段序列提供了一对特异性内引物,一对特异性外引物和一对环引物。
本发明还提供了检测多重耐药基因oqxAB的试剂盒。
本发明还提供了检测多重耐药基因oqxAB的检测方法。
本发明是通过以下措施实现的:
一种环介导等温扩增多重耐药基因oqxAB的引物,由一对外引物、一对内引物和一对环引物组成,其核苷酸序列分别如下:
外引物F3:5'-TGCGCGCGGAGTATCC-3'
外引物B3:5'-GAACCTGCGCCTGATCC-3'
内引物FIP:5'-TGTTTTCAACGCCGTTGATCGC-GGCGCCAACCCGAAAG-3'
内引物BIP:5'-TACATGAAATCGGTCGCCGGC-TACCCGGGCGGAAGGT-3'
环引物LF:5'-TGTTTTCAACGCCGTTGATCGC-3'
环引物LB: 5'-TACATGAAATCGGTCGCCGGC-3'
其中,外引物与内引物的摩尔比为1:8,外引物与环引物的摩尔比为1:4。
一种检测多重耐药基因oqxAB的试剂盒,包括若干个装有反应液的LAMP反应管,其中每25 μl反应液中含有:12.5 μl 2×等温反应缓冲液、1.0 μl Bst DNA聚合酶、40 pmol内引物FIP、40 pmol内引物BIP、 5 pmol外引物F3、5 pmol外引物B3、20 pmol环引物LF、20 pmol环引物LB,余量为灭菌双蒸水;其中Bst DNA聚合酶的活性单位为8 U/μl。2×等温反应缓冲液中含有40 mM pH为8.8的Tris-HCl、20 mM KCl、16 mM MgSO4、20 mM (NH4)2SO4、0.2%wt% Tween20、1.6 M甜菜碱、2.8 mM dNTP。
所述的试剂盒,还包括1μl钙黄绿素。
一种检测多重耐药基因oqxAB的检测方法,包括以下步骤:
(1)提取待检测细菌基因组总DNA。
(2)使用所述的试剂盒进行检测,具体操作为:将待检细菌基因组DNA加入LAMP反应管的反应液中,混匀,同时设置阳性对照和阴性对照,阳性对照中加入反应液内的为含有oqxAB多重耐药基因的基因组DNA,阴性对照中加入反应液内的为灭菌双蒸水。将LAMP反应管置于水浴锅中进行扩增,扩增条件为:65 ℃水浴恒温反应45 min。
步骤(2)中待检细菌基因组DNA为含DNA的浓度为0.003-300 ng/μl的DNA溶液。
所述的检测方法,LAMP反应管中出现白色沉淀的为阳性结果,不出现白色沉淀的为阴性结果。
所述的检测方法,其特征是在扩增反应前的反应管中加入1μl的钙黄绿素,反应结束后扩增产物变为绿色的是阳性结果,橙色的是阴性结果。
步骤(1)中提取的待检细菌基因组DNA包括以下步骤:将待检的细菌菌株过夜培养后,取1ml的菌液12000 rpm离心2 min,彻底弃去上清。取沉淀用细菌基因组DNA提取试剂盒提取细菌基因组总DNA,最后溶于50 μl灭菌双蒸水中,测定细菌基因组DNA的浓度为52 ng/μl左右,-20 ℃保存备用。
本发明的有益效果:
1、采用LAMP技术,特异性强,比PCR检测方法灵敏度高,不需要昂贵的PCR仪器,只需要普通的金属浴或水浴锅即可,且结果不必用凝胶电泳方法来观察,通过肉眼观察白色沉淀或使用荧光染料显色肉眼直接观察即可判定结果,时间大大缩短,从普通PCR仪器的2-3h缩短至45min左右,简单而快速,可广泛应用于兽医及人医领域包括实验室及临床基层对多重耐药基因oqxAB的快速检测;
2、解决了现有技术时间长、工作量大、交叉污染、操作复杂等缺陷;
3、具有特异性强、灵敏度高、快速且成本低、操作方法更简单,适于现场快速检测的优点。
附图说明
图1为实施例3中普通PCR方法检测oqxAB基因灵敏度检测结果。其中1-7号管中加入的为倍比稀释的含有oqxAB的大肠杆菌基因组DNA,8号管为阴性对照。其中1-7号管的基因组DNA浓度分别为52 ng/μl、5.2 ng/μl、0.52 ng/μl、5.2*10-2 ng/μl、5.2*10-3 ng/μl、5.2*10-4 ng/μl、5.2*10-5 ng/μl。结果显示:1-4号能扩增到目的条带,为阳性;5-8号没有扩增到肉眼可见的目的条带,为阴性。
图2为实施例3中LAMP方法检测oqxAB基因灵敏度检测结果。1-7号管中加入的为倍比稀释的含有oqxAB的大肠杆菌基因组DNA,8号管为阴性对照。其中1-7号管的基因组DNA浓度分别为52 ng/μl、5.2 ng/μl、0.52 ng/μl、5.2*10-2 ng/μl、5.2*10-3 ng/μl、5.2*10-4ng/μl、5.2*10-5 ng/μl;M为5000 bp。结果显示,1-6号能扩增到目的条带,为阳性;7-8号没有扩增到肉眼可见的目的条带,为阴性。
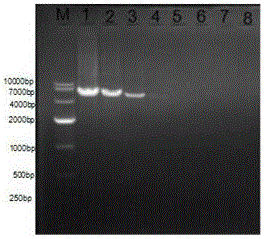
图3为实施例4中普通PCR方法检测oqxAB基因特异性检测结果。其中,1-7号管中加入的模板分别为阳性对照、阴性对照、大肠杆菌(ATCC 25922,oqxAB 阴性)、沙门氏菌(ATCC 50035,oqxAB 阴性)、金黄色葡萄球菌(ATCC 29213,oqxAB 阴性)、铜绿假单胞菌(ATCC 27853,oqxAB 阴性)和肺炎双球菌(ATCC 49619,oqxAB阴性);M为10000 bp。结果,只有阳性对照出现阳性条带,其他结果均为阴性。
图4为实施例4中LAMP方法方法检测oqxAB基因特异性检测结果。其中,1-6号管中加入的模板分别为大肠杆菌(ATCC 25922,oqxAB 阴性)、沙门氏菌(ATCC 50035,oqxAB 阴性)、金黄色葡萄球菌(ATCC 29213,oqxAB 阴性)、铜绿假单胞菌(ATCC 27853,oqxAB 阴性)、肺炎双球菌(ATCC 49619,oqxAB阴性)和阳性对照;M为5000 bp;7号管加入阴性对照。结果,只有阳性对照出现阳性条带,其他结果均为阴性。
具体实施方式:
为了更好的理解本发明,下面结合具体实例来进一步说明。
实施例1:制备检测多重耐药基因oqxAB的试剂盒
(1)检测引物的设计
由于在设计LAMP引物时,一般要求序列的长度为≤2000 bp,而目前已知的oqxAB的基因序列大多数为5140 bp。因此,首先根据NCBI上已知的oqxAB基因的序列,比较大肠杆菌、沙门氏菌和肺炎克雷伯三种菌株的oqxAB基因的序列,找出保守区域,分别设计一对特异性内引物FIP、BIP,一对特异性外引物F3、B3,以及环引物LF、LB,用以对多重耐药基因oqxAB进行检测。在试验过程中,每一对引物都设计了若干对,根据试验结果,挑选出效果最好的引物,碱基序列如下:
外引物F3:5'-TGCGCGCGGAGTATCC-3' (SEQ No.1)
外引物B3:5'-GAACCTGCGCCTGATCC-3' (SEQ No.2)
内引物FIP:5'-TGTTTTCAACGCCGTTGATCGC-GGCGCCAACCCGAAAG-3' (SEQ No.3)
内引物BIP:5'-TACATGAAATCGGTCGCCGGC-TACCCGGGCGGAAGGT-3' (SEQ No.4)
环引物LF:5'-TGTTTTCAACGCCGTTGATCGC-3' (SEQ No.5)
环引物LB: 5'-TACATGAAATCGGTCGCCGGC-3' (SEQ No.6)
(2)检测试剂盒
设置检测多重耐药基因oqxAB的试剂盒,该试剂盒包括装有反应液的LAMP反应管。
反应液以25 μl计,含有12.5 μl 2×等温反应缓冲液、1.0 μl Bst DNA聚合酶、40 pmol内引物FIP、40 pmol内引物BIP、 5 pmol外引物F3、5 pmol外引物B3、20 pmol环引物LF、20 pmol环引物LB,余量为灭菌双蒸水。
其中Bst DNA聚合酶的活性单位为8 U/μl。
2×等温反应缓冲液中含有40 mM pH为8.8的Tris-HCl、20 mM KCl、16 mM MgSO4、20 mM (NH4)2SO4、0.2%wt% Tween20、1.6 M甜菜碱、2.8 mM dNTP。
其中,外引物与内引物的摩尔比为1:8,外引物与环引物的摩尔比为1:4.
为了设置对照组,每个试剂盒最少设置三个LAMP反应管,此试剂盒设置六个LAMP反应管。
扩增产物的副产物焦磷酸离子与Mg2+反应会产生焦磷酸镁(白色沉淀)的衍生物,此衍生物与生成的扩增产物成正比,由于LAMP法能产生大量的扩增产物,衍生物产量也会大增,于是可以呈现出肉眼可见的白色沉淀,以此来验证是否有靶基因的存在。
为了更明显的观察扩增结果,试剂盒中设置有荧光染料钙黄绿素(螯合剂),与试剂中的锰离子(Mn2+)结合处于淬灭状态,扩增产物的副产物焦磷酸离子与Mn2+结合释放钙黄绿素,淬灭状态解除,发出黄绿色荧光。因此可以根据扩增产物的颜色变化来判断扩增结果。
实施例2:用环介导等温扩增方法检测多重耐药基因oqxAB的检测方法
(1)提取待检的临床菌株的基因组DNA
将待检的临床菌株过夜培养后,取1 mL的菌液12000 rpm离心2 min,彻底弃上清。取沉淀用细菌基因组DNA提取试剂盒提取细菌基因组总DNA,最后溶于50 μl灭菌双蒸水中, -20 ℃保存备用。
(2)LAMP扩增
使用实施例1中的试剂盒,设置一个检测管、一个阳性对照管和一个阴性对照管。在检测管内加入2 μl待检DNA样本,阳性对照管中加入2 μl 含oqxAB基因的大肠杆菌基因组DNA(DNA浓度为52 ng/μl),阴性对照管中加入2 μl灭菌双蒸水。加完后混匀,稍离心,使沾在管壁上的样品也溶解在反应液中。将反应管置水浴锅中进行扩增,扩增条件为:65℃水浴恒温反应45 min。
(3)结果分析:
观察反应后的混合液颜色。阳性对照管和检测管有沉淀,阴性对照管保持澄清。加入1 μl钙黄绿素后,阳性对照管和检测管变为绿色,阴性对照管保持橙色,说明待检细菌中含有oqxAB基因。
实施例3:oqxAB基因LAMP检测方法与普通PCR方法灵敏度比较
取含oqxAB基因的大肠杆菌基因组DNA(浓度为52 ng/μl),按10倍比稀释,分别为原液的10-1、10-2、10-3、10-4、10-5、10-6倍,分别取2 μl作为LAMP反应和PCR反应的模板。在LAMP反应管和PCR反应管中分别加入以上倍比稀释的含oqxAB基因的细菌基因组DNA 2 μl。
其中LAMP反应管置于65 ℃恒温水浴锅中反应45-60 min,反应结束后直接用肉眼观察颜色变化,用电泳验证结果。
PCR反应中所有引物为根据NCBI上已知的oqxAB基因的保守序列用Primer5.0软件设计,按以下碱基序列经DNA合成仪合成:
上游引物F:5'-CCCTGGACCGCACATAAAG-3'
下游引物R:5'-AAAGAACAAGATTCACCCGCAAC-3'
扩增目的片段大小为5140bp。PCR反应体系设置为:其中10×LA BufferⅡ (Mg2+plus)2.5μl、dNTP mixture 4.0 μl、10 μM上游引物F 0.5 μl、10 μM 下游引物R 0.5 μl、Takara LA Taq DNA聚合酶 0.25 μl、模板 2 μl、灭菌双蒸水补齐25μl。PCR产应条件为:95℃ 5 min,然后进行30 个循环,循环条件为95 ℃ 1 min,54 ℃ 30 s,72 ℃ 5 min,最后72℃ 延伸10 min。反应结束后取8μl PCR产物进行1.2%的琼脂糖凝胶电泳检测,根据是否扩增目的条带判定阳性和阴性。
PCR产物经电泳检测,结果如图1所示。反应管1-4均出现目的条带,且条带的颜色越来越淡,而5-8号未出现目的条带。说明原液稀释至10-3(5.2*10-2 ng/μl)还可以检测到oqxAB基因。
LAMP方法中,加入钙黄绿素后,1-6管的颜色为明显的绿色,7-8管颜色为橙色,说明原液稀释10-5(5.2*10-4 ng/μl)还可以检测到oqxAB基因。电泳检测结果如图2所示。颜色变化与电泳图谱结果一致。换算成拷贝数,普通PCR可实际检测的浓度为5.2*10-2 ng/μl,拷贝数为9.38*106 copys/ml,LAMP方法实际可检测浓度为5.2*10-4 ng/μl,拷贝数为9.38*104copys/ml,提高了2个数量级。
综合LAMP和PCR反应结果可以看出,LAMP反应灵敏度要比普通的PCR反应高出2个数量级(100倍),反应时间比PCR短,且不需要凝胶电泳检测,直接通过肉眼观察即可判定结果。
实施例4:oqxAB基因LAMP检测方法和普通PCR方法特异性比较
选择大肠杆菌(ATCC 25922)、沙门氏菌(ATCC 50035)、金黄色葡萄球菌(ATCC 29213)、铜绿假单胞菌(ATCC 27853)和肺炎双球菌(ATCC 49619)作为试验菌株,分别提取基因组DNA,按照实施例2中所建立的oqxAB基因环介导等温扩增检测方法进行检测;同时以以上基因组DNA为模板按照实施例3的PCR反应体系和检测程序进行PCR扩增;都以大肠杆菌(含oqxAB基因)基因组DNA作为阳性对照,灭菌双蒸水作为阴性对照,验证本发明所建立的LAMP方法的特异性。
PCR扩增结果电泳图谱见图3,LAMP结果只有阳性对照管变为绿色,电泳图谱如图4所示。由于LAMP方法更加直观简便,且耗时短,因此更加适合临床快速检测的需要。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受实施例的限制,其它任何未背离本发明的精神实质与原理下所做的改变、修饰、组合、替代、简化均应为等效替换方式,都包含在本发明的保护范围之内。
<110>山东省农业科学院畜牧兽医研究所
<120>环介导等温扩增多重耐药基因oqxAB的检测引物、检测试剂盒及检测方法
<160> 8
<210> 1
<211> 16
<212> DNA
<213>人工合成
<400> 1
TGCGCGCGGA GTATCC 16
<210> 2
<211> 17
<212> DNA
<213>人工合成
<400> 2
GAACCTGCGC CTGATCC 17
<210> 3
<211> 38
<212> DNA
<213>人工合成
<400> 3
TGTTTTCAAC GCCGTTGATC GCGGCGCCAA CCCGAAAG 38
<210> 4
<211> 37
<212> DNA
<213>人工合成
<400> 4
TACATGAAAT CGGTCGCCGG CTACCCGGGC GGAAGGT 37
<210> 5
<211> 22
<212> DNA
<213>人工合成
<400> 5
TGTTTTCAAC GCCGTTGATC GC 22
<210> 6
<211> 21
<212> DNA
<213>人工合成
<400> 6
TACATGAAAT CGGTCGCCGG C 21
<210> 7
<211> 19
<212> DNA
<213>人工合成
<400>7
CCCTGGACCG CACATAAAG 19
<210> 8
<211> 23
<212> DNA
<213>人工合成
<400> 8
AAAGAACAAG ATTCACCCGC AAC 23
- 还没有人留言评论。精彩留言会获得点赞!
- 一种霍乱弧菌环介导等温扩增试剂盒及其应用的制造方法与工艺
- 用于检测番茄晚疫病菌的LAMP引物组合物和应用的制造方法与工艺
- 基于颜色判定的环介导等温扩增(LAMP)技术检测雪松疫霉根腐病菌的制造方法与工艺
- Sortase A介导的(S)‑羰基还原酶寡聚体高效催化(S)‑苯基乙二醇的合成的制造方法与工艺
- 用于旋转机器中的超导线圈的等温支承部和真空容器的制造方法与工艺
- 基于环介导等温扩增消光技术的转基因玉米MIR604检测方法与制造工艺
- 基于环介导等温扩增消光技术的玉米检测方法与制造工艺
- 一套鉴定甘蔗上三种短体线虫的环介导等温扩增引物及其试剂盒的制造方法与工艺
- RNA扩增方法与制造工艺
- 用于扩增核酸样品的等温方法与制造工艺