一类席夫碱化合物作为氰根离子和铜离子荧光探针的应用的制作方法
一、技术领域:
本发明涉及生物分析领域,具体涉及一类席夫碱化合物作为氰根离子和铜离子荧光探针的应用。
二、
背景技术:
:
剧毒氰根离子在医药、杀虫剂和肥料的合成中是一种十分重要的原材料,其广泛应用于医学、冶金、电镀等领域(journalofmaterialsprocessingtechnology,2001,119(3):336-343.)。科学研究表明当氰根离子进入血液循环后,氰根离子与血液中的细胞色素氧化酶产生反应,抑制酶的级联反应,使其丧失电子传递能力,使得呼吸链中断,从而引起细胞内的缺氧导致中枢神经絮乱,严重时导致细胞窒息死亡(chemicalcommunications,2014(50):11583-11586)。因此,对于氰根离子的检测具有十分重要的意义。检测氰根的方法有伏安法、滴定法、电化学法和色谱法(hydrometallurgy,2011,106(4):135-140;chemistry-aeuropeanjournal,2014,20(41):13226-13233;biosensorsandbioelectronics,2005,20(12):2581-2593;societyreviews,2010,39(1):127-137.),但这些方法都需要昂贵的设备,且检测耗时长,很难实现及时分析等广泛应用。因此需要寻找简单、快速、经济地检测氰根的方法。
铜离子作为人体中一种微量元素在各种生理过程中起十分重要的调节作用。然而,铜离子的过量及缺乏都会导致机体的病变,铜缺乏会引起冠状动脉硬化从而形成冠心病;过量的铜离子可以造成中枢神经系统损伤,影响了人体的肾脏,肝脏,肺和其他部位,甚至导致严重的疾病,如帕金森病和阿尔茨海默氏病。在环境中过高浓度的铜离子会引起水体细菌、藻类的死亡,对于水环境造成严重的污染(journalofluminescence,2016,180,292–300;rscadvances,2016,6,102096-102101.)。因此,对铜离子的选择性检测在环境保护和人体健康方面具有十分重要的意义。目前,常用的铜离子检测方法有原子吸收法、离子色谱法、电化学检测等方法。相比于这些检测方法,荧光检测方法具有实时、快速、简便、选择性和灵敏度高等优点,被认为是检测阳离子和阴离子的有效方法。
荧光检测方法目前在很多领域有广泛的应用,如生物分子检测、医学病理研究、环境污染物检测等。
本发明采用一类席夫碱化合物作为荧光探针用于荧光检测氰根和铜离子。该类席夫碱化合物在氰根离子和铜离子存在下关环氧化。该类席夫碱化合物用于作为氰根和铜离子荧光探针的应用目前还没有报道。
三、
技术实现要素:
本发明的提供一类席夫碱化合物用于作为氰根和铜离子荧光探针的应用,该方法可以快速、简便、高效和特异性对氰根离子和铜离子进行检测。
为实现上述目的,本发明采用的技术方案为:
一类席夫碱化合物作为氰根离子和铜离子荧光探针的应用。
所述的该类席夫碱化合物在磷酸缓冲液和乙腈的混合体系中作为氰根离子和铜离子荧光探针的应用。
该类席夫碱其结构式为:
所述的磷酸缓冲液的ph=7.4,浓度为10mm,磷酸缓冲液与乙腈的体积比为1:2。
与现有技术相比,本发明具有如下优点和效果:
1.本发明克服了以往分析方法的缺陷,采用一类席夫碱作为荧光探针用于氰根离子和铜离子的检测,该方法可以快速、简便、高效和特异性对氰根离子和铜离子进行检测;
2.本发明提供了一类以双醛化合物为母体,通过醛基和芳香胺衍生物的氨基作用生成的具有对称结构的席夫碱化合物。该类席夫碱化合物在强亲核试剂氰根离子和氧化性铜离子的共同作用下关环氧化,生成能发出强蓝色荧光的关环产物;
3.本发明所用的席夫碱化合物制备简单、易于合成。该类席夫碱化学物对氰根离子和铜离子的检测具有高选择性和高灵敏度,能够准确、快速地检测氰根离子和铜离子,对于其它金属阳离子和阴离子没有任何响应;
4.、本发明所述席夫碱化合物可用于氰根离子和铜离子的荧光检测,为环境检测提供了有效的分析方法。
四、附图说明
图1是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱1,先加入20μm氰根离子,再加入20μm铜离子,1分钟后,2分钟后,3分钟后,4分钟后的荧光强度的变化图;
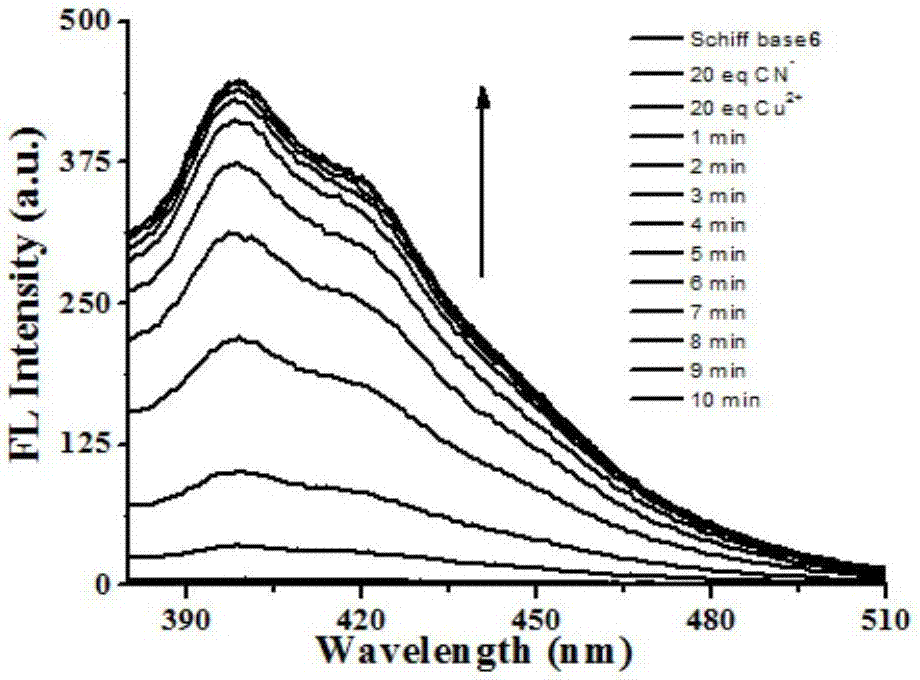
图2是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱6,先加入20μm氰根离子,再加入20μm铜离子,1分钟后,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后,9分钟后,10分钟后的荧光强度的变化图;
图3是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入20μmcn-后,再分别加入1μm,2μm,3μm,4μm,5μm,6μm,7μm,8μm,9μm,10μm的铜离子,其在最大发射波长439nm处荧光强度随时间的变化图;
图4是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入20μmcn-后,再分别加入不同浓度的铜离子(1μm,2μm,3μm,4μm,5μm,6μm)其在最大发射波长439nm处荧光强度随不同铜离子浓度线性关系图;
图5是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入20μmcn-后,再加入8μm铜离子或分别加入10μm其它金属阳离子(依次为al3+,ba2+,ca2+,cd2+,co2+,fe2+,fe3+,k+,mg2+,mn2+,ni2+,pb2+,zn2+,cr3+,li+,na+,hg2+)荧光强度变化图;
图6是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入20μmcn-后,再分别加入各种金属阳离子作用的荧光柱状图;黑色柱:席夫碱1加入10μm其它金属离子后在其最大发射波长439nm下的荧光的变化;灰色柱:席夫碱1加入10μm其它金属离子及5μm铜离子后在其最大发射波长439nm下的荧光的变化,从左到右依次为al3+,ba2+,ca2+,cd2+,co2+,fe2+,fe3+,k+,mg2+,mn2+,ni2+,pb2+,zn2+,cr3+,li+,na+,hg2+;
图7是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入8μmcu2+后,再分别加入1μm,5μm,10μm,20μm,25μm,30μm,40μm氰根离子,其在最大发射波长439nm处荧光强度随时间的变化图;
图8是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入8μmcu2+后,再分别加入不同浓度的氰根离子(1μm,5μm,10μm,20μm,25μm,30μm)其最在大发射波长439nm处荧光强度随不同氰根离子浓度线性关系;
图9是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入8μmcu2+后,再分别加入50μm氰根离子或分别加入50μm其它阴离子(依次为s2-,scn-,so32-,so42-,s2o32-,clo4-,p2o42-,co32-,hco32-,cl-,br-,i-,no2-,no3-,ch3coo-)荧光强度变化图;
图10是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱1,先加入8μmcu2+后,再与各种阴离子作用的荧光柱状图;黑色柱:席夫碱1加入50μm其它阴离子后在其最大发射波长439nm下的荧光的变化;灰色柱:席夫碱1加入50μm其它阴离子及50μm氰根离子后在其最大发射波长439nm下的荧光的变化,从左到右依次s2-,scn-,so32-,so42-,s2o32-,clo4-,p2o42-,co32-,hco32-,cl-,br-,i-,no2-,no3-,ch3coo-;
图11是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱6,先加入20μmcu2+后,再分别加入1μm,10μm,20μm,30μm,40μm氰根离子,其在最大发射波长在399nm处荧光强度随时间的变化图;
图12是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,浓度为1μm席夫碱6,先加入20μmcu2+后,在分别加入不同浓度的氰根离子(1μm,10μm,20μm,30μm,40μm)其在最大发射波长在399nm处荧光强度随不同氰根离子浓度线性关系;
图13是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱2,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后,9分钟后,10分钟后的荧光强度的变化图;
图14是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱7,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后,9分钟后,10分钟后,11分钟后,12分钟后的荧光强度的变化图;
图15是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱3,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后,9分钟后,10分钟后,11分钟后,12分钟后的荧光强度的变化图;
图16是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱8,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后的荧光强度的变化图;
图17是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱4,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后的荧光强度的变化图;
图18是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱9,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后,9分钟后,10分钟后的荧光强度的变化图;
图19是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱5,先加入20μm氰根离子后,再加入20μm铜离子,2分钟后,3分钟后,4分钟后,5分钟后,6分钟后,7分钟后,8分钟后,9分钟后,10分钟后,11分钟后,12分钟后,13分钟后,14分钟后,15分钟后,16分钟后的荧光强度的变化图;
图20是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中加入浓度为1μm席夫碱10,先加入20μm氰根离子后,再加入20μm铜离子,10分钟后,15分钟后,20分钟后,25分钟后,30分钟后,35分钟后,40分钟后,45分钟后,50分钟后的荧光强度的变化图。
五、具体实施方式:
一类席夫碱化合物,其特征在于该类席夫碱其结构式为:
所述的该类席夫碱化合物在磷酸缓冲液(10mm,ph=7.4)和乙腈(v:v=1:2)的混合体系中作为氰根离子和铜离子荧光探针的应用。
此类席夫碱化合物在低浓度下本身背景荧光较弱,氰根离子作为亲核性极强的亲核试剂可以进攻席夫碱的碳氮双键,同时在氧化性铜离子作用下生成能发出强荧光的关环产物。
此类席夫碱化合物只对氰根离子和铜离子有荧光响应,对于其它的阴离子和金属阳离子没有荧光响应。这类席夫碱化合物可以特异性地荧光检测溶液中的氰根离子和铜离子,如以下合成式:
将合成的席夫碱1-10溶解到无水乙腈溶液中配成1mm母液;氰化钾固体溶解到去离子水中配成10mm氰根离子溶液;五水合硫酸铜固体溶解到去离子水中配成10mm铜离子溶液。
以下给出9种实施例,具体以席夫碱1和席夫碱6这两组对照物对于氰根离子和铜离子检测进行详细阐述,其他的几组化合物根据实验结果证明,其效果完全相类似。
实施例一:席夫碱化合物1(x=oh;r1=och3;r2=t-bu)对氰根离子和铜离子响应时间分析
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,检测荧光强度,加入席夫碱1后溶液几乎没有荧光;再加入6μl配制的10mm氰根离子,检测荧光强度变化,荧光强度几乎不变;再加入6μl配制的10mm铜离子,检测荧光强度变化,荧光强度明显增强。且随着时间的变化荧光强度逐渐增强,当时间达到4分钟时荧光强度趋于稳定(见图1)。
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm氰根离子后,再分别加入浓度为1μm,2μm,3μm,4μm,5μm,6μm,7μm,8μm,9μm,10μm铜离子,检测在其最大发射波长439nm处荧光强度随时间的变化,当加入的铜离子浓度达到8μm时荧光强度基本上达到最大值,且4分钟后保持不变(见图3)。
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入2.4μl配制的10mm铜离子后,再分别加入浓度为1μm,5μm,10μm,20μm,25μm,30μm,40μm氰根离子,检测在其最大发射波长439nm处荧光强度随时间的变化,当加入的氰根离子浓度达到30μm时荧光强度基本上达到最大值,且6分钟后保持不变(见图7)。
实施例二:席夫碱化合物1(x=oh;r1=och3;r2=t-bu)对铜离子的定量检测应用
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm氰根离子后,再分别加入不同浓度的铜离子(1μm,2μm,3μm,4μm,5μm,6μm),检测在不同铜离子浓度下最大发射波长439nm处荧光强度,得到线性关系图(见图4)。铜离子的浓度为横轴(单位为μμ),439nm处荧光强度为纵轴。其中荧光强度(y)与铜离子浓度(x)满足一元线性方程:y=-113.79+113.5×x,相关系数r=0.966。席夫碱化合物1(x=oh;r1=och3;r2=t-bu)可用于对铜离子的定量检测应用。
实施例三:席夫碱化合物1(x=oh;r1=och3;r2=t-bu)对氰根离子的定量检测应用
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入2.4μl配制的10mm铜离子后,再分别加入不同浓度的氰根离子(1μm,5μm,10μm,20μm,25μm,30μm),检测在不同氰根离子浓度下最大发射波长439nm处荧光强度,得到线性关系图(见图8)。氰根离子的浓度为横轴(单位为μμ),439nm处荧光强度为纵轴。其中荧光强度(y)与氰根离子浓度(x)满足一元线性方程:y=-0.022+12.855×x,相关系数r=0.985。席夫碱化合物1(x=oh;r1=och3;r2=t-bu)可用于对氰根离子的定量检测应用。
实施例四:席夫碱化合物1(x=oh;r1=och3;r2=t-bu)对铜离子选择性检测应用
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm氰根离子,再加入2.4μl配制的10mm铜离子或分别加入3μl浓度为10mm其它金属阳离子(al3+,ba2+,ca2+,cd2+,co2+,fe2+,fe3+,k+,mg2+,mn2+,ni2+,pb2+,zn2+,cr3+,li+,na+,hg2+),检测荧光强度变化(见图5),只有加入铜离子荧光强度增强。取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm氰根离子,再分别加入3μl浓度为10mm除铜离子以外的其它金属阳离子(al3+,ba2+,ca2+,cd2+,co2+,fe2+,fe3+,k+,mg2+,mn2+,ni2+,pb2+,zn2+,cr3+,li+,na+,hg2+),检测荧光强度变化,黑色柱是加入其它金属阳离子在最大发射波长439nm处荧光强度值;取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm氰根离子,再分别加入3μl配制的10mm其它金属阳离子及1.5μl配制的10mm铜离子,检测荧光强度变化,灰色柱是加入其它金属阳离子及铜离子在最大发射波长439nm处荧光强度值(见图6)。在含有氰根离子的乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系中,席夫碱1(x=oh;r1=och3;r2=t-bu)可用于对铜离子选择性检测应用。
实施例五:席夫碱化合物1(x=oh;r1=och3;r2=t-bu)对氰根离子选择性检测应用
取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入2.4μl配制的10mm铜离子,再分别加入15μl配制的10mm氰根离子或分别加入15μl浓度为10mm其它阴离子(s2-,scn-,so32-,so42-,s2o32-,clo4-,p2o42-,co32-,hco32-,cl-,br-,i-,no2-,no3-,ch3coo-),检测荧光强度变化(见图9),只有加入氰根离子荧光强度增强。取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入2.4μl配制的10mm铜离子,再分别加入15μl浓度为10mm除氰根离子以外的其它阴离子(s2-,scn-,so32-,so42-,s2o32-,clo4-,p2o42-,co32-,hco32-,cl-,br-,i-,no2-,no3-,ch3coo-),检测荧光强度变化,黑色柱是加入其它阴离子在最大发射波长439nm处荧光强度值;取3μl席夫碱1母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入2.4μl配制的10mm铜离子,再分别加入15μl配制的10mm其它阴离子及15μl配制的10mm氰根离子,检测荧光强度变化,灰色柱是加入其它阴离子及氰根离子在最大发射波长439nm处荧光强度值(见图10)。在含有铜离子的乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系中,席夫碱1(x=oh;r1=och3;r2=t-bu)可用于对氰根离子选择性检测应用。
实施例六:席夫碱化合物6(x=oh;r1=h;r2=t-bu)对氰根离子和铜离子响应时间分析
取3μl席夫碱6母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,检测荧光强度,加入席夫碱6后溶液几乎没有荧光;再加入6μl配制的10mm氰根离子,检测荧光强度变化,荧光强度几乎不变;再加入6μl配制的10mm铜离子,检测荧光强度变化,荧光强度明显增强。且随着时间的变化荧光强度逐渐增强,当时间达到10分钟时荧光强度趋于稳定(见图2)。取3μl席夫碱6母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm铜离子后,再分别加入浓度为1μm,10μm,20μm,30μm,40μm氰根离子,检测在其最大发射波长399nm处荧光强度随时间的变化(见图11),随着氰根离子浓度增加荧光强度逐渐增强,当氰根离子浓度达到40μm荧光强度基本上达到最大值,且4分钟后保持不变。
实施例七:席夫碱化合物6(x=oh;r1=h;r2=t-bu)对氰根离子的定量检测应用
取3μl席夫碱6母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm铜离子,再分别加入不同浓度的氰根离子(1μm,10μm,20μm,30μm,40μm),检测在不同氰根离子浓度下最大发射波长399nm处荧光强度,得到线性关系图(见图12)。氰根离子的浓度为横轴(单位为μμ),399nm处荧光强度为纵轴。其中荧光强度(y)与氰根离子浓度(x)满足一元线性方程:y=-0.54+3.679×x,相关系数r=0.963。席夫碱化合物6(x=oh;r1=h;r2=t-bu)可用于对氰根离子的定量检测应用。
实施例八:其它席夫碱化合物对氰根离子和铜离子响应时间分析
其它席夫碱对于氰根离子和铜离子响应时间检测方法与实施例一的过程相同,分别取3μl其它席夫碱母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,检测荧光强度;再加入6μl配制的10mm氰根离子检测荧光强度变化;再加入6μl配制的10mm铜离子检测荧光强度变化,随着时间的增加分别检测不同时间下的荧光强度变化,直到荧光强度达到稳定(见图13-图20)。除了席夫碱5响应时间20分钟,席夫碱10响应时间50分钟外,席夫碱2,3,4,7,8和9响应都比较迅速,10分钟时荧光强度都趋于稳定。
实施例九:席夫碱化合物对氰根和铜离子响应性质研究
取3μl席夫碱母液加入到乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)3ml中,再加入6μl配制的10mm氰根离子,再加入6μl配制的10mm铜离子,通过检测荧光强度变化,得到该类席夫碱化合物的激发波长和最大发射波长,对应的最大发射波长下的荧光强度不再发生变化需要的最短时间和在对应的最大发射波长下的荧光强度增强倍数(见表1)。高效液相色谱(流动相:乙腈/水(v:v=8:2);检测器:365nm)分别检测席夫碱化合物1-10的保留时间和席夫碱化合物在测试体系中与50倍浓度的氰根离子和铜离子的作用关环产物的保留时间,计算不同保留时间下峰面积比值算出生成氧化关环产物转化率,除了席夫碱2和7转化率30%左右,其它席夫碱的转化率都达到70%以上(见表1)。
表1的前两列是对应席夫碱化合物1-10的最大激发和发射波长;中间一列是通过高效液相色谱(流动相:乙腈/水(v:v=8:2);检测器:365nm)对席夫碱化合物1-10(1μm)和席夫碱化合物在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中与50μm的氰根离子和50μm的铜离子作用后关环产物的分析,即根据计算不同保留时间下峰面积比值得到席夫碱生成相应的关环氧化产物转化率;最后两列是在乙腈和磷酸缓冲液(10mm,ph=7.4)的混合体系(v:v=2:1)中,席夫碱的浓度为1μm,在加入20μm氰根离子和20μm铜离子后在对应的最大发射波长下的荧光强度不再发生变化需要的最短时间和在对应的最大发射波长下的荧光强度增强倍数。
表1
综上所述,本发明的该类席夫碱化合物在测试体系中对于氰根离子和铜离子具有很好的响应灵敏性和选择性,可应用于体外对氰根离子和铜离子检测。应当理解,所附权利要求概括了本发明的范围,在本发明构思的引导下,本领域的技术人员应意识到,对本发明的各实施例方案所进行的一定的改变,都将被本发明的内容所覆盖。
- 还没有人留言评论。精彩留言会获得点赞!