多种抗体标记的SERS探针和基底及其制备方法和应用与流程
本发明属于分子生物学技术领域,具体涉及多种抗体标记的sers探针和基底及其制备方法和应用。
背景技术:
胰腺癌是预后最差的消化道恶性肿瘤之一,国家肿瘤中心对2015年全国肿瘤登记中心收集的全国各登记处上报的2012年恶性肿瘤登记资料进行分析估计,其中胰腺癌的发病例数为8.6万,发病率为6.35/105,在所有恶性肿瘤发生率中排第10位,其死亡例数达7.7万,死亡率为5.72/105,位居第6位。胰腺癌缺乏特异的临床表现和敏感的早期诊断指标,其诊断和随访常用的血清标志物是ca19-9,但诊断特异性差。目前胰腺癌术前的诊断和分期主要依赖于影像学包括螺旋ct增强扫描和磁共振成像(mri)的表现,进行原发肿瘤大小(t)、n-区域淋巴结(n)、m-远处转移(m)的分期(tnm)判断。ct扫描时间短,成像速度快,价格便宜,但是辐射量大,不能作为常规的检查方法。mri软组织分辨率高,能显示细节,无辐射,但是检查时间长,扫描范围的限制难以对远处转移进行评估,但最终确诊仍需病理学检查。所以目前急需开发一些快速、灵敏、特异性高、无创伤、价格适宜的胰腺癌早期诊断和分期判断的新方法和新技术。
随着对肿瘤研究的不断深入,研究者发现肿瘤患者血液中存在少量循环肿瘤细胞(ctc)以及由坏死癌细胞释放的少量循环肿瘤dna(ctdna)。通过检测血液中的ctc和ctdna对患者肿瘤进行诊断与监测的方法被称为液体活检(liquidbiopsy)。相对于传统的手术活检和穿刺活检方法,液体活检能够解决临床取样的难点,满足对患者高频检测的需求,并具有相比于穿刺活检副作用小、操作简单、能重复取样、成本低的优点。因此液体活检有望在肿瘤的早期筛查、肿瘤患者的动态监测和个体化用药等精准医疗方面将发挥越来越重要的作用。
外泌体(exosomes)作为人体内一类重要囊泡,也开始受到越来越多的关注。由于肿瘤衍生的外泌体含有肿瘤特异性蛋白质和mirna,在肿瘤的生长、转移中扮演者重要的角色,可以作为潜在的肿瘤诊断标志物。通过从体液,如血浆、血清和尿液中提取的外泌体,可包含肿瘤相关的信息,更易于实现对肿瘤的早期检测。研究者从胰腺癌病人血清中分离得到的外泌体中发现了一种磷脂酰肌醇聚糖-1(gpc1)糖蛋白,但是在其他良性胰腺疾病及正常人的血液中分离的外泌体中,gpc1的含量非常低。这项检测比传统的elisa检测糖抗原ca19-9更可靠。这种基于外泌体标志物所建立的非侵入性的胰腺癌诊断方法,可以非常精确地从良性胰腺疾病中诊断出早期癌变。此外,胰腺癌外泌体中microrna-10b的表达也升高。也有研究发现胰腺导管腺癌细胞产生的外泌体对肝转移有促进作用,且迁移抑制因子(mif)表达显著升高。循环外泌体中的mif可作为胰腺癌预后判断及肝转移预测的生物标志物。因此,外泌体是肿瘤研究的一个新兴领域,也是继循环肿瘤细胞ctc和ctdna后又一备受关注的液体活检的肿瘤标志物和治疗及预后的靶点。
目前对外泌体的定量表征方法主要有纳米粒子跟踪分析(nta),电镜观察形貌,流式细胞计数法,基于外泌体表面蛋白的elisa法或westernblot法,这些方法所需样本量大,灵敏度和特异性不高,样本处理复杂费时,处理通量小,无法在临床上实施,且仪器昂贵,不适合在临床推广。表面增加拉曼散射光谱(sers)是近年来发展起来的新型表征方法和信号标记手段,具有信号强,信号稳定没有淬灭现象,易于标记,光谱信号具有“指纹”特性等优点。sers探针的标记技术正在生物成像,疾病诊断,药物运输等生物医学领域发挥着越来越重要的作用。目前采用sers探针标记免疫法和外泌体相关迁移抑制因子(mif)检测胰腺癌外泌体并实现分期判断的研究还未见文献报道。
我们的研究发现,双功能多巴胺修饰及保护的玻璃片及sers探针能够高灵敏高特异性地检测到单个外泌体。因此,本发明设计了多种抗体(anti-mif,anti-gpc1,anti-egfr,anti-epcam)标记的sers探针,结合多巴胺修饰的玻璃片,实现了细胞系产生的外泌体的高灵敏检测。基于anti-mif的sers免疫方法具有最高的灵敏度,该体系用于临床胰腺癌血清样本的诊断,统计数据结果能够显著区分胰腺癌病人及健康人的血样,并且能对胰腺癌的不同tnm的肿瘤阶段进行分类(p1,2和p3,是否转移),与病理切片的结果吻合度高。该方法仅需要2ul血清样本,无需进行高速离心,单个样本的检测时间仅花15分钟。此外,该发明还结合sers成像技术,实现了高通量样本的同时成像,便于临床医生快速、准确地进行胰腺癌的临床诊断。
技术实现要素:
本发明的目的在于提出一种用于胰腺癌外泌体的高灵敏检测的多种抗体(anti-mif,anti-gpc1,anti-egfr,anti-epcam,anti-cd9,anti-cd63)标记的sers探针和基底及其制备方法,以及探针和基底在胰腺癌外泌体的高灵敏检测中的应用。
本发明把anti-mif的sers免疫方法用于临床胰腺癌血清样本的诊断,具有最高的灵敏度和特异性性,统计数据结果能够显著区分胰腺癌病人及健康人的血样,并且能对胰腺癌的不同tnm的肿瘤阶段进行分类(p1,2和p3,是否转移),与病理切片的结果吻合度高。
本发明提出的多种抗体标记的sers探针和基底的制备方法,具体步骤如下:
(1)在2~20mm核壳结构的金-银纳米颗粒溶液中,加入anti-mif、anti-gpc1、anti-egfr、anti-epcam、anti-cd9、anti-cd63六种抗体,每种抗体的浓度为5~40μg/ml,每种抗体的加入量为30~150μl;并加入浓度为1~20mg/ml的多巴胺溶液40~150μl;室温下反应0.5~4小时;反应后的溶液经过离心,再用去离子水进行分散;得到多种抗体标记的sers探针;
(2)取普通的玻璃载玻片泡于8~14m的naoh中4~7h,再往溶液中添加浓度为10~100mg/ml的多巴胺溶液6~10ml,将上述培养皿放在专用摇床上摇0.5~2h,之后用去离子水冲洗干净;
将修饰并清洗后的载玻片置于含有六种抗体anti-mif、anti-gpc1、anti-egfr、anti-epcam、anti-cd9、anti-cd63的体积浓度为0.2~2%的bsa(牛血清白蛋白)中,其中,每种抗体的浓度为1~10mg/ml,反应0.5~3h;用去离子水冲洗1~3次后,自然晾干,得到基片。
本发明制备的多种抗体标记的sers探针和基底,可用于胰腺癌外泌体的高灵敏检测,具体步骤如下。
(1)细胞培养以及外泌体的提取
把胰腺癌细胞系panc-01在rpmi1640培养基中培养,培养基在使用之前添加2~20%胎牛血清、50~150μg/ml苄青霉素和50~150μg/ml链霉素,细胞置于含2~10%co2孵箱内在25~45℃条件下培养至足够数量。
采用高速离心方法提取外泌体。首先,将细胞培养液置于离心机于500~2000g(这里的g是指离心力,有时用转速来表示,但涉及到高速离心都用离心力g来表示,下同)离心2~10min,再1000~3000g离心2~10min,去除细胞碎片,取上层清液经0.22μm滤膜过滤,将滤液置于超速离心机中在4℃、120000~200000g离心1~5h,取下层沉淀加入pbs(磷酸盐缓冲溶液)溶解,再置于超速离心机在4℃、120000~200000g离心1~5h,弃上清液,沉淀即为富集的外泌体,加入pbs溶解,置于-20℃冰箱中保存。
外泌体的表征采用马尔文公司的nanosightns300对外泌体的粒径分布进行分析,取2~20μl外泌体,用pbs稀释10~200倍。nanosightns300镜头选择scmos,激光选择blue488,实验温度在22.4~22.6℃,每个样品测量3~6次。采用场发射透射电子显微镜(tem)观察外泌体形貌。取5~20μl外泌体于400目碳膜图层网格上,用滤纸片将多余液体从网格边缘擦去,在室温下干燥。加入2~20μl3%磷钨酸溶液,室温负染1.5min,用滤纸片吸干染液后在65℃白炽灯下加热烘干2~5min。
(2)用多种抗体标记的sers探针检测胰腺癌外泌体
先将聚多巴胺修饰的玻璃片(即基片)用0.01~0.1%bsa溶液在25~40℃下浸泡20~80分钟,然后用pbs冲洗3~5遍;把外泌体溶液采用pbs稀释至不同浓度:5.44χ102--2.72χ1010个外泌体/ml;取2~10ul外泌体溶液滴到包被有特定抗体的聚多巴胺修饰的玻璃片上,在25~40℃下反应20~80分钟,然后用pbs冲洗3~5遍;再取1~10ul标记有特定抗体的sers探针滴到对应的玻璃片上,在25~40℃下反应30~90分钟,然后用去离子水冲洗;制备好的玻璃片在拉曼光谱仪(如horibajobinyvon公司,德国)上进行光谱扫描,激发光波长为785nm。
(3)结果分析。上述得到的多种抗体标记的sers探针,具有表面增强的拉曼信号,在1073.51cm-1处有最强且窄的拉曼信号分子patp的光谱信号峰。
为了数据显示方便,本发明采用sers光谱图中1073.51cm-1处的拉曼强度的对数值进行分析。对不同浓度(5.44χ102to2.72χ1010个外泌体/ml)的外泌体采用多种抗体标记的sers平台绘制标准工作曲线。结果显示anti-mif具有最大的灵敏度,anti-gpc1的灵敏度最低,anti-mif,anti-gpc1,anti-egfr,anti-epcam这四种抗体平台的检测限(lod)均达到了9x10-19mol/l。2ul5.44χ102个/ml浓度的样品中只含有1个外泌体,表明本发明的sers体系能够实现单个外泌体的检测。而商业用的mifelisa试剂盒最低只能检测到2.72χ108个/ml浓度的外泌体样本,且样本所需量达到100ul。因此,用本发明的多种抗体标记的sers探针免疫检测胰腺癌外泌体,比商业elisa试剂盒的检测胰腺癌外泌体,灵敏度提高6个数量级。
本发明提供的多种抗体标记的sers探针和基底可用于胰腺癌病人的血清样本分析,及胰腺癌的肿瘤分期和转移判断。
(1)血清样本的免离心多抗体检测的具体步骤如下:
血清样本在使用前采用pbs稀释2~5倍,然后用0.22um的滤膜过滤,最后取1~10ul稀释后的样本滴到聚多巴胺、抗体修饰的玻璃片上。玻璃片在25~40℃下反应20~80分钟,然后用pbs冲洗3~5遍;再取1~10ul分别标记有anti-mif、anti-gpc1、anti-egfr抗体的sers探针滴到对应的玻璃片上,在25~40℃下反应30~90分钟,然后用去离子水冲洗;制备好的玻璃片在拉曼光谱仪上进行光谱扫描,激发光波长为785nm。
(2)从上海某医院收集了从2012年12月到2016年8月期间的22例胰腺癌病人和20例健康人的血清样本。胰腺癌病人的平均年龄为60.45±9.81岁,9名女性和13名男性,健康人组的平均年龄为57.75±8.16岁,其中7名女性和13名男性。该研究是在该医院医学研究伦理委员会的批准下进行的,所有病人在收集样本前都签了知情同意书。对其血清样本进行免离心多抗体检测。统计数据分析如下:所得到的sers光谱图中采用1073.51cm-1处信号的对数值进行分析。数据采用graphprism6.0,统计解析软件spss21.0和作图软件origin7.5来进行作图和统计数据分析。
对于胰腺癌病人和健康人的血清样本的检测结果采用统计分析。shapiro-wilk检验显示胰腺癌病人组wexperiment=0.901,p=0.032<0.10,而健康人对照组的wcontrol=0.913,p=0.072<0.10,这说明这两组数据都不呈现正态分布。所以我们对这两组独立样本采用非参数mann-whitney检验,z=-5.541,p<0.0001,说明这两组样本具有统计学意义上的显著性差异。胰腺癌病人组和健康人对照组的平均值分别为3.79±0.11和2.08±0.218。以上结果说明本发明中采用基于抗体mif的sers探针标记的方法可以区别胰腺癌病人和健康人,并为临床诊断提供了参考范围,有望使用到实际的临床的液体活检诊断领域。
进一步,本发明根据sers信号强度的对数值对17例胰腺癌病人样本进行tnm分期(不包含5例没有tnm分期的胰腺癌样本),分成p1-2和p3两组。根据组织病理学报告,这些病人样本已经被分成正常、浸润未转移(浸润到胰腺旁组织如脂肪组织、神经、十二指肠黏膜、胆管)、转移(转移到肝、脾、肾上腺、淋巴结)。基于anti-mif的sers数据通过mann-whitney检验统计结果发现正常组、p1-2、转移和浸润未转移组之间都有统计学显著性差异(p<0.05),并且与组织病理学报告吻合。我们也惊讶地发现,anti-mif的sers数据也同时能将p3肿瘤分期与p1-2阶段区别开,这意味着本发明可以为肿瘤的进一步分期并实现精准的肿瘤诊断提供更多的参考价值。此外,本发明也采用商业用人mifelisa试剂盒对病人的血清样本进行了分析。测试结果发现在胰腺癌病人血样中有9名病人显示有阳性结果,而在正常人中也有8名健康人显示阳性结果。以上结果说明,本发明的anit-mifsers平台可以提供更多更精准的诊断和肿瘤分期信息,并且所需样本量少,仅需2ul,而elisa需要100ul样本。
此外,本发明也采用了anti-gpc1和anti-egfr修饰的sers体系对胰腺癌病人和健康人血清样本进行测试和统计数据结果分析。结果发现基于这两种抗体的sers体系也能区别健康人和胰腺癌,健康人和pt1~2期,健康人和胰腺癌浸润未转移,但不能区别胰腺癌的pt1~2和pt3期,也不能区别转移和浸润非转移的血样。
与现有报道相比,本发明的外泌体相关迁移抑制因子(mif)标记的sers探针标记方法简单方便,用于胰腺癌外泌体的检测,快速灵敏,特异性高,所需样本量少,无需高速离心的分离过程,实现了临床胰腺癌病人和健康人血清样本的检测,并且能够用于胰腺癌的转移和分期判断。该发明也适用于其他多种抗体sers平台的开发和应用。
(1)sers探针合成方法简便:玻璃片修饰和sers标记抗体的方法采用温和的包埋法进行,不需要复杂的仪器,不需要高温强酸强碱等苛刻条件,反应条件非常温和,且无需复杂的特殊的化学反应试剂。玻璃片修饰均匀,sers标记稳定性高,能放置数月不发生聚集。
(2)快速高效:加入细胞系或临床血清样本后均只需要反应1小时,就能达到有效的捕获。血清样本只需要用0.22um的膜过滤,无需复杂耗时的高速离心过程。sers信号收集快速。
(3)灵敏度高:外泌体的最低检测浓度是9x10-19mol/l,2ul样品中仅含有1个外泌体,所以可以实现单个外泌体的检测。
(4)特异性高:该体系用于临床复杂样本血清的检测,仅经过0.22um过滤膜的过滤,其他成分对检测没有干扰。用于临床血样的检测可以显著区分胰腺癌病人和健康人的血样,所以可以用于临床胰腺癌的早期诊断。
(5)可用于辅助诊断:mif抗体的sers探针法可用于区分胰腺癌病人的不同阶段,可辅助医生进行分期判断。血清检测没有对病人没有创伤,是一种无创的液体活检方法,所以特别适用于高频次的肿瘤的术后监测和疗效评估。
(6)可拓展性强:除了anti-mif,其他多种抗体标记的sers方法也能用于胰腺癌的诊断和分期,但由于抗体的结合力和特异性的差别,检测性能会有所变化。但我们可以选择灵敏度更高特异性更强的抗体,建立适用于其他疾病的sers标记方法,也可以多种抗体联合使用。
附图说明
图1为sers标记、外泌体的图示。其中,(a)胰腺癌细胞panc-01细胞系提取的外泌体的tem照片,(b)为胰腺癌细胞panc-01提取的外泌体的nta粒径分布图。
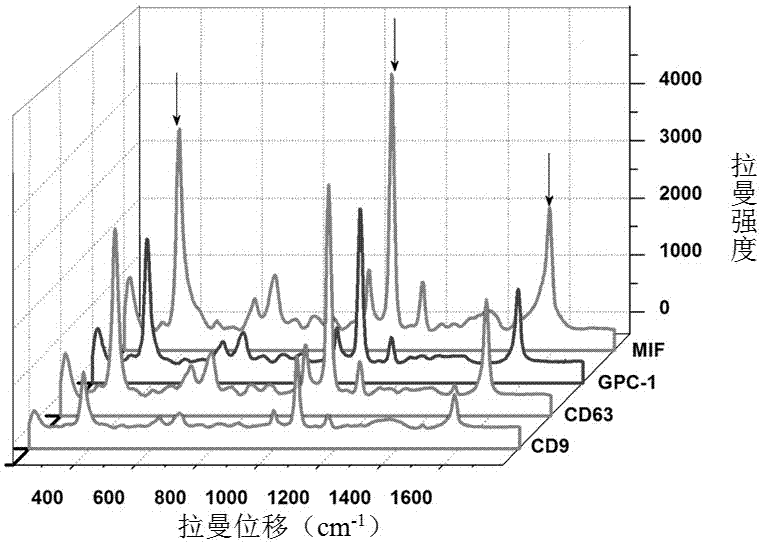
图2为anti-cd9/cd63/mif/gpc1构建的sers标记体系用于检测panc-01细胞系提取的外泌体的拉曼光谱图。
图3为sers标记的拉曼光谱图。其中,(a)为不同外泌体浓度下anti-mif构建的sers标记的拉曼光谱图,(b)为在1073.51cm-1处的拉曼信号强度随着外泌体浓度的变化曲线,(c)拉曼强度和外泌体浓度的线性标准工作曲线。
图4为sers标记的血清样本组的拉曼信号强度分布柱状图和检验统计数据分析图。其中,(a)为基于anti-mif的sers标记的胰腺癌病人血清样本组的拉曼信号强度分布柱状图,(b)为基于anti-mif的sers标记的健康人血清样本组的拉曼信号强度分布柱状图,(c)为血清样本组的shapiro-wilk检验统计数据分析图。
图5.胰腺癌病人血清样本的分期和转移判断的shapiro-wilk统计分析图。其中,(a)胰腺癌的分期判断,区别pt2-1和pt3,(b)胰腺癌的浸润或转移判断。
具体实施方式
下面通过具体实施例,进一步描述本发明。
实施例1:
(1)多种抗体标记的sers探针及基底的制备
于5mm的核壳结构的金-银纳米颗粒溶液中分别加入50μl10μg/ml的anti-mif,anti-gpc1,anti-egfr,anti-epcam,anti-cd9,anti-cd63六种抗体,与60μl的10mg/ml多巴胺溶液,室温下反应1小时。反应后的溶液经过离心,再用去离子水进行分散。另外,取普通的玻璃载玻片泡于12mnaoh中5h,再往溶液中添加20mg/ml的多巴胺溶液8ml,将上述培养皿放在专用摇床上摇1h,之后用去离子水冲洗干净。将修饰并清洗后的载玻片置于含有5mg/mlanti-mif,anti-gpc1,anti-egfr,anti-epcam,anti-cd9,anti-cd63的1%浓度bsa中反应2h,用去离子水冲洗3次后,自然晾干。
(2)细胞培养以及外泌体的提取
胰腺癌细胞系panc-01在rpmi1640培养基中培养,培养基在使用之前添加10%胎牛血清、60μg/ml苄青霉素和80μg/ml链霉素,细胞置于含6%co2孵箱内在35℃条件下培养至足够数量。
外泌体采用高速离心方法进行提取。首先,将培养液置于离心机于1200g离心5min,再2000g离心6min去除细胞碎片,取上层清液经0.22μm滤膜过滤,将滤液置于超速离心机中在4℃、140000g离心2h,取下层沉淀加入pbs溶解,再置于超速离心机在4℃、140000g离心2h,弃上清液,沉淀即为富集的外泌体,加入pbs溶解,置于-20℃冰箱中保存。
(3)外泌体的表征
采用马尔文公司的nanosightns300对外泌体的粒径分布进行分析,取5μl外泌体,用pbs稀释20倍。nanosightns300镜头选择scmos,激光选择blue488,实验温度在22.4~22.6℃,每个样品测量4次。采用场发射透射电子显微镜(tem)观察外泌体形貌。取10μl外泌体于400目碳膜图层网格上,用滤纸片将多余液体从网格边缘擦去,在室温下干燥。加入10μl3%磷钨酸溶液,室温负染2min,用滤纸片吸干染液后在65℃白炽灯下加热烘干4min。
(4)基于多种抗体标记的sers免疫检测胰腺癌外泌体
先将聚多巴胺修饰的玻璃片用0.05%bsa溶液30℃下浸泡50分钟,然后用pbs冲洗4遍。外泌体溶液采用pbs稀释到不同的浓度,取3ul外泌体溶液滴到包被有特定抗体的聚多巴胺修饰的玻璃片上,36℃下反应30分钟,然后用pbs冲洗3遍。再取3ul标记有特定抗体的sers探针滴到对应的玻璃片上,35℃下反应60分钟,然后后用去离子水冲洗。制备好的玻璃片在拉曼光谱(horibajobinyvon公司,德国)上进行光谱扫描,激发光波长为785nm。
(5)血清样本的免离心多抗体检测
从上海长海医院收集了从2012年12月到2016年8月期间的10例胰腺癌病人和11例健康人的血清样本。胰腺癌病人的平均年龄为60.45±9.81岁,4名女性和6名男性,健康人组的平均年龄为57.75±8.16岁,其中4名女性和7名男性。该研究是在长海医院医学研究伦理委员会的批准下进行的,所有病人在收集样本前都签了知情同意书。血清样本在使用前采用pbs稀释3倍,然后用0.22um的滤膜过滤,最后取2ul稀释后的样本滴到聚多巴胺、抗体修饰的玻璃片上。玻璃片在30℃下反应50分钟,然后用pbs冲洗3遍;再取2ul分别标记有anti-mif、anti-gpc1、anti-egfr抗体的sers探针滴到对应的玻璃片上,在30℃下反应50分钟,然后用去离子水冲洗;制备好的玻璃片在拉曼光谱仪上进行光谱扫描,激发光波长为785nm。
(6)统计数据分析所得到的sers光谱图中采用1073.51cm-1处信号的对数值进行分析。数据采用graphprism6.0,统计解析软件spss21.0和作图软件origin7.5来进行作图和统计数据分析。
实施例2:
(1)多种抗体标记的sers探针及基底的制备
于8mm的核壳结构的金-银纳米颗粒溶液中加入80μl20μg/ml的anti-mif,anti-gpc1,anti-egfr,anti-epcam,anti-cd9,anti-cd63等抗体与60μl的10mg/ml多巴胺溶液,室温下反应1小时。反应后的溶液经过离心,再用去离子水进行分散。另外,取普通的玻璃载玻片泡于12mnaoh中5h,再往溶液中添加20mg/ml的多巴胺溶液8ml,将上述培养皿放在专用摇床上摇1h,之后用去离子水冲洗干净。将修饰并清洗后的载玻片置于含有10mg/mlanti-mif,anti-gpc1,anti-egfr,anti-epcam,anti-cd9,anti-cd63的1%浓度bsa中反应2h,用去离子水冲洗3次后,自然晾干。
(2)细胞培养以及外泌体的提取
胰腺癌细胞系panc-01在rpmi1640培养基中培养,培养基在使用之前添加10%胎牛血清、60μg/ml苄青霉素和80μg/ml链霉素,细胞置于含6%co2孵箱内在35℃条件下培养至足够数量。
外泌体采用高速离心方法进行提取。首先,将培养液置于离心机于1200g离心5min,再2000g离心6min去除细胞碎片,取上层清液经0.22μm滤膜过滤,将滤液置于超速离心机中在4℃、140000g离心2h,取下层沉淀加入pbs溶解,再置于超速离心机在4℃、140000g离心2h,弃上清液,沉淀即为富集的外泌体,加入pbs溶解,置于-20℃冰箱中保存。
(3)外泌体的表征采用马尔文公司的nanosightns300对外泌体的粒径分布进行分析,取5μl外泌体,用pbs稀释20倍。nanosightns300镜头选择scmos,激光选择blue488,实验温度在22.4~22.6℃,每个样品测量4次。采用场发射透射电子显微镜(tem)观察外泌体形貌。取10μl外泌体于400目碳膜图层网格上,用滤纸片将多余液体从网格边缘擦去,在室温下干燥。加入10μl3%磷钨酸溶液,室温负染2min,用滤纸片吸干染液后在65℃白炽灯下加热烘干4min。
(4)基于多种抗体标记的sers免疫检测胰腺癌外泌体
先将聚多巴胺修饰的玻璃片用0.05%bsa溶液30℃下浸泡50分钟,然后用pbs冲洗4遍。外泌体溶液采用pbs稀释到不同的浓度,取3ul外泌体溶液滴到包被有特定抗体的聚多巴胺修饰的玻璃片上,36℃下反应30分钟,然后用pbs冲洗3遍。再取3ul标记有特定抗体的sers探针滴到对应的玻璃片上,35℃下反应60分钟,然后后用去离子水冲洗。制备好的玻璃片在拉曼光谱(horibajobinyvon公司,德国)上进行光谱扫描,激发光波长为785nm。
(5)血清样本的免离心多抗体检测
从上海长海医院收集了从2012年12月到2016年8月期间的12例胰腺癌病人和9例健康人的血清样本。胰腺癌病人的平均年龄为60.45±9.81岁,5名女性和7名男性,健康人组的平均年龄为57.75±8.16岁,其中3名女性和6名男性。该研究是在长海医院医学研究伦理委员会的批准下进行的,所有病人在收集样本前都签了知情同意书。血清样本在使用前采用pbs稀释5倍,然后用0.22um的滤膜过滤,最后取6ul稀释后的样本滴到聚多巴胺、抗体修饰的玻璃片上。玻璃片在37℃下反应70分钟,然后用pbs冲洗5遍;再取5ul分别标记有anti-mif、anti-gpc1、anti-egfr抗体的sers探针滴到对应的玻璃片上,在37℃下反应70分钟,然后用去离子水冲洗;制备好的玻璃片在拉曼光谱仪上进行光谱扫描,激发光波长为785nm。
(6)统计数据分析,所得到的sers数据采用graphprism6.0,统计解析软件spss21.0和作图软件origin7.5来进行作图和统计数据分析。
- 还没有人留言评论。精彩留言会获得点赞!