一种检测金刚烷胺类药物的试纸条、制备方法及其应用与流程
属于食品安全检测领域,具体涉及一种检测金刚烷胺类药物的试纸条、制备方法及其应用。
背景技术:
金刚烷胺是最早用于抑制流感病毒的抗病毒药,在抑制人流感病毒方面,金刚烷胺具有价格低廉,效果明显等特点。目前还未在兽医临床上用于动物病毒的预防和治疗,即尚未批准用作兽医。将人用抗病毒药物用于畜禽,不仅容易导致动物性食品中药物残留、动物病毒、动物机体产生免疫抑制和耐药性等问题,还可导致病毒发生变异,影响动物疫病控制及人用病毒药物的有效性。因此农业部在2005年发布第560号公告中,明确禁止在兽药领域生产和销售使用金刚烷胺。现今常规检测金刚烷胺的方法一般为液相色谱法或液质联用法。
目前,市面上还未发现有中药材、中药饮片及食品中,尤其是肉制品中金刚烷胺的快检试剂盒,若采用上述实验方法,操作过程都比较复杂,实验时间长、实验成本高,且并不适用于现场检测。
技术实现要素:
本发明的目的在于提供一种检测金刚烷胺类药物的试纸条、制备方法及其应用,本发明试纸条在检测步骤和检测成本上都有着明显的优势,适合于现场检测。
本发明解决其技术问题是采用以下技术方案来实现的。
本发明提出了一种检测金刚烷胺类药物的试纸条,试纸条包括衬底、滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜和吸水纸,其中,滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜和吸水纸依次首尾衔接并固定于衬底上;免疫胶体金纸片上设有胶体金标记的抗金刚烷胺单克隆抗体,免疫硝酸纤维素膜上设有包被金刚烷胺-牛血清白蛋白复合物的检测线和包被羊抗兔igg的质控线。
本发明还提出一种上述试纸条的制备方法,包括以下步骤:将滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜、吸水纸依次粘贴在衬底上,制得试纸条。
本发明还提出了一种快速检测金刚烷胺类药物的试剂盒,包括盒体和检测卡,该检测卡包括壳体和上述的试纸条。
本发明还提出了一种利用上述试剂盒快速检测金刚烷胺类药物的方法,包括以下步骤:
样品制备:称取样品适量,进行预处理;
标准品溶液制备:取金刚烷胺标准品适量,用二氯甲烷溶解;
待测液制备:向样品或标准品溶液中分别加入稀释液、提取液,充分振荡后离心,吸取离心后的上清液部分于试管中,吹干,再向吹干后的试管中加入复溶液,充分混匀;
检测:取待测液滴加入金标微孔中,分析检测结果。
本发明还提出了一种上述试剂盒在检测中药材、中药饮片及食品中残留的金刚烷胺类药物中的应用。
本发明的有益效果是:
本发明提供了一种检测金刚烷胺类药物的试纸条、制备方法及其应用,本发明中的试纸条通过免疫竞争抑制法来定性检测中药材、中药饮片及食品中出现的金刚烷胺成分,具有特异性强、灵敏性高、操作简单方便等优点。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
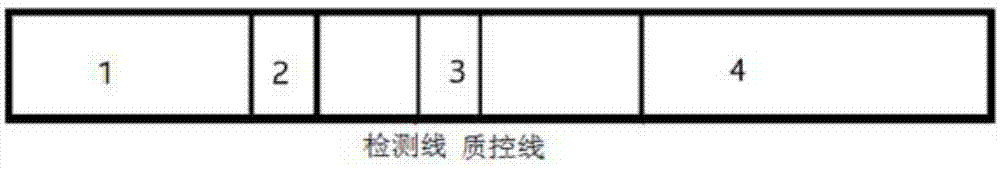
图1为金刚烷胺胶体金检测试纸条示意图。
附图标号:1-滤样纸;2-免疫胶体金纸片;3-免疫硝酸纤维素膜;4-吸水纸。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
下面对本发明实施例提供的一种检测金刚烷胺类药物的试纸条、制备方法及其应用进行具体说明。
本发明实施例提供一种检测金刚烷胺类药物的试纸条,该试纸条包括衬底、滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜和吸水纸,其中,滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜和吸水纸依次首尾衔接并固定于衬底上;免疫胶体金纸片上设有胶体金标记的抗金刚烷胺单克隆抗体,免疫硝酸纤维素膜上设有包被金刚烷胺-牛血清白蛋白复合物的检测线和包被羊抗兔igg的质控线。
本发明实施例提供一种检测金刚烷胺类药物的试纸条,该试纸条的检测原理:将待检样本滴加于微孔试剂中,混匀后,将试纸条插入孵育后的微孔试剂中,待检样品液与微孔中的金标抗体结合后一起向免疫硝酸纤维素膜扩散;若待检样品液中金刚烷胺类药物的含量高,则扩散过程中待检样品液中的金刚烷胺类药物可与金标抗体相结合,进而完全封闭金标抗体上金刚烷胺类药物的抗原结合点,阻止金标抗体与免疫硝酸纤维素膜上金刚烷胺-牛血清白蛋白复合结合,检测线不显色,而羊抗兔igg则可与金标抗体结合,质控线显色;若待检样品液中金刚烷胺类药物的含量低或无,则金标抗体上的抗原结合位点不能被封闭,进而金标抗体会与免疫硝酸纤维素膜上金刚烷胺-牛血清白蛋白结合,检测线显色,同时羊抗兔igg也可与金标抗体结合,质控线显色。如果质控线不显色,则试纸失效。
本发明实施例还提出一种上述试纸条的制备方法,包括以下步骤:将滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜、吸水纸依次粘贴在衬底上,制得试纸条。
在一些实施方式中,免疫胶体金纸片的制备包括以下步骤:
制备免疫胶体金溶液;用预处理液浸泡玻璃纤维纸,干燥,再用免疫胶体金溶液喷涂预处理后的玻璃纤维纸,干燥,制得免疫胶体金纸片。
在一些实施方式中,免疫胶体金溶液的制备包括以下步骤:用喷金缓冲液稀释胶体金标记的抗金刚烷胺单克隆抗体,获得od540值为1.6-1.8的免疫胶体金溶液,抗金刚烷胺单克隆抗体与胶体金结合的标记浓度为18-20μg/ml,胶体金的粒径为30-40nm,优选的,胶体金的粒径为35nm。
本发明实施例中的胶体金可以购自市售或者采用柠檬酸三钠还原法制备,胶体金的粒径为30-40nm,优选的,胶体金的粒径为35nm。采用本发明实施例中的柠檬酸三钠还原法,得到胶体金分子呈大小均一的30nm球形颗粒,由于胶体金颗粒大小适中、整体均一,使其与单克隆抗体的结合效率更高、效果更稳定。
在一些实施方式中,喷金缓冲液包括以下质量百分比的成分:10~15wt%1.0mtris液,0.2~0.5wt%聚乙二醇20000,0.1~0.2wt%牛血清白蛋白,0.1~0.3wt%脱脂牛奶,0.4~0.6wt%酪蛋白,0.02~0.08wt%叠氮化钠,余量为水,且喷金缓冲液ph为8.0±0.05;
预处理液包括以下质量百分比的成分:1~1.5wt%tween-20,3~5wt%双糖或多糖混合,余量为水。
本发明实施例中的免疫胶体金纸片的制备过程中:用预处理液浸泡玻璃纤维纸,干燥,再用免疫胶体金溶液喷涂预处理后的玻璃纤维纸,干燥,制得免疫胶体金纸片,每30-35ml预处理液浸泡玻璃纤维纸261mm×220mm×0.5mm,干燥后,再用免疫胶体金溶液喷涂玻璃纤维纸,每261mm×220mm×0.5mm玻璃纤维纸上喷涂20-25ml免疫胶体金溶液,干燥,制得免疫胶体金纸片。
在一些实施方式中,免疫硝酸纤维素膜的制备包括以下步骤:将0.4~0.6mg/ml金刚烷胺-牛血清白蛋白复合物和0.3~0.5mg/ml羊抗兔igg分别喷在硝酸纤维素膜检测线和质控线的位置上,烘干,制得免疫硝酸纤维素膜。
本发明实施例中制备的免疫硝酸纤维素膜:每1m长硝酸纤维素膜分别包被有1ml的羊抗兔igg和金刚烷胺-牛血清白蛋白复合物溶液,检测线和质控线的间距为5.0mm。
本发明实施例还提供一种快速检测金刚烷胺类药物的试剂盒,包括盒体和检测卡,检测卡包括壳体和上述试纸条。
本发明实施例还提供一种利用上述试剂盒快速检测金刚烷胺类药物的方法,包括以下步骤:
样品制备:称取样品适量,进行预处理;
标准品溶液制备:取金刚烷胺标准品适量,用二氯甲烷溶解;
待测液制备:向样品或标准品溶液中分别加入稀释液、提取液,充分振荡后离心,吸取离心后的上清液部分于试管中,吹干,再向吹干后的试管中加入复溶液,充分混匀;
检测:取待测液滴加入金标微孔中,分析检测结果。
在一些实施方式中,稀释液为乙腈,提取液为0.4%-0.6wt%的三氯乙酸水溶液、乙酸水溶液、甲酸水溶液中的一种或几种,复溶液为0.8-1.2m的pbs缓冲液,样品、稀释液、提取液的体积比为5:3:2,复溶液与待测液的体积比为5:2,检测时的反应时间为3-5min。
本发明实施例中的使用上述试剂盒进行检测的方法中,试剂盒样品处理方法是:称取均质后的待测样品于反应容器中,加入适量稀释液及提取液,充分震荡混匀,使金刚烷胺尽可能多的溶到溶剂中。该溶剂可以是三氯乙酸水溶液、乙酸水溶液、甲酸水溶液或其他溶剂中的一种或几种。其中优选为三氯乙酸水溶液,因为提取效果理想,溶剂的体积可优选所取食品量的0.8倍-1.5倍,优选1倍。这样可以将食品中的金刚烷胺充分提取,又不用因取样品液过多而造成吹干时间延长,从而导致检测周期过长。经过以上处理之后得到的待测液加入金标微孔中,等待3-5min,分析检测结果。
本发明实施例还提供一种上述试剂盒在检测中药材、中药饮片及食品中残留的金刚烷胺类药物中的应用,尤其是在检测肉制品中残留的金刚烷胺类药物中的应用。
本发明实施例所提供的检测金刚烷胺类药物的试纸条的工作原理为:利用高度特异的抗体-抗原特异性结合反应及免疫膜层析技术,通过免疫竞争抑制法来定性检测中药材、中药饮片及食品中出现的金刚烷胺成分,尤其是用于快速检测禽蛋类食品中是否非法残留金刚烷胺成分,具有特异性强、灵敏性高、操作简单方便等优点。
试剂盒内的检测试纸条是实现金刚烷胺检测的关键,在试纸条检测线(t线)包被了金刚烷胺-牛血清白蛋白复合物;在试纸条的免疫胶体金纸片上固定有胶体金标记的抗金刚烷胺单克隆抗体。当样品提取液从加样孔加入,渗透到试纸条的加样垫上,被检样本首先与玻璃纤维膜上的胶体金标记的金刚烷胺单克隆抗体结合,并通过毛细作用继续层析至免疫硝酸纤维素膜,顺序通过免疫硝酸纤维素膜上喷点了金刚烷胺-牛血清白蛋白复合物的检测线和喷点了羊抗兔igg的质控线。
如果样品提取液中含有金刚烷胺,它们将与金刚烷胺-牛血清白蛋白复合物竞争胶体金-抗金刚烷胺抗体上有限的抗原结合位点,当金刚烷胺浓度达到产品设计的阈值浓度以上时,它们将占据抗金刚烷胺单克隆抗体上的部分或全部的抗原结合位点,这样就阻止了胶体金标记的抗金刚烷胺单克隆抗体和检测线的金刚烷胺-牛血清白蛋白复合物结合,检测线不能捕获到足够的胶体金颗粒而出现较质控线浅的红色色带或无红色色带出现,检测结果呈阳性。如果样品提取液中没有金刚烷胺或金刚烷胺的浓度低于阈值浓度,则抗金刚烷胺单克隆抗体-胶体金随同样品提取液运行至检测线,检测线捕获到胶体金颗粒而呈现较质控线深或一样深的红色色带,检测结果呈阴性。
在试纸条上的质控线(c线)包被有羊抗兔igg,以指示试剂盒反应系统工作是否正常(免疫胶体金纸片上的羊抗兔蛋白,随样品在纸条上的运行已经到达质控线所在位置,羊抗兔蛋白与羊抗兔igg结合,即可出现红色色带)。质控线的出现与金刚烷胺的存在无关。质控线色带的出现表明:①样品加入量充足②样品在纸条上运行正常。
以下是本发明中的试纸条的使用方法:
1.将试剂盒放置在水平台面上。
2.用加样吸管吸取样品提取液,然后滴4滴(120ul)样品提取液到试剂盒的加样孔中。每检测一份不同的样品注意要使用不同的吸管。
3.观察结果:在滴加样品后3-5min判读结果。
检测结果的判断方法:
阴性:在结果观察窗口内出现两条色带,t线(检测线,靠近加样孔一端)显色比c线深或一样深,表示样品中无金刚烷胺存在。
阳性:在结果观察窗口,t线明显比c线浅或t线无显色,表示样品中有金刚烷胺存在。
无效:质控线(c线)不出现。任何情况下,c线均应形成,表示加样和操作正确。c线未出现表明测试结果是不确定的,可能是操作不当或试剂板已失效,应重做。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
一种金刚烷胺胶体金检测试剂盒的制备方法,包括以下步骤:
1.胶体金的制备
本发明实施例中所使用的胶体金可以购自市售或者采用下述的柠檬酸三钠还原法制备。
柠檬酸三钠还原法制备胶体金,包括以下步骤(配置各种水溶液均采用双蒸或三蒸去离子水):
制备浓度为0.01%的haucl4水溶液100ml,水浴或油浴至99℃,控制温度恒定,之后边搅拌边加入1%柠檬酸三钠(na3c6h5o7·2h2o)水溶液1.80ml,继续搅拌加热20min左右,超声振荡,频率为25khz,3min后冷却至4.0℃水浴中保持温度恒定,即制得30nm左右粒径的胶体金溶液。
2.免疫胶体金的制备
2.1将抗金刚烷胺单克隆抗体用0.1mph8.0的磷酸盐缓冲液稀释至浓度为1.0mg/ml的抗体溶液。
2.2取1000ml的胶体金溶液,往里加入100ml0.1mph8.0磷酸盐缓冲液混合3min。在快速搅拌下,再缓缓将稀释的抗金刚烷胺单克隆抗体溶液20ml加入其中。室温反应5min并不时缓缓搅拌。
2.3反应结束后,在上述反应液中快速加入20ml的10%的牛血清白蛋白(bsa)溶液,室温反应5min并不时缓缓搅拌。
2.4将制备好的免疫胶体金8000转/min离心20min,保留沉淀,并收集上清10000转/min离心30min,弃上清。收集两次离心沉淀用含有0.1%bsa的硼酸缓冲液复溶到od540在10。
3.免疫胶体金纸片的制备
3.1预处理液的制备:准确称取10mltween-20,70g可溶性淀粉,加纯化水定容至1000ml。
3.2喷金缓冲液的制备:取800ml纯化水,往里加入150ml1.0mtris液,用盐酸调节ph至8.0。准确称取3.0g聚乙二醇20000、2.0g牛血清白蛋白,2.0g脱脂牛奶,5.0g酪蛋白溶液和0.6g叠氮化钠加入溶液中,充分溶解,混合均匀,加纯化水至总体积1000ml。
3.3用喷金缓冲液稀释胶体金标记的抗金刚烷胺单克隆抗体,至溶液od540值为1.7,获得免疫胶体金溶液。
3.4用预处理液浸泡玻璃纤维纸,每30ml预处理液浸泡玻璃纤维纸261mm×220mm×0.5mm,浸泡30min后,37℃下干燥;再用免疫胶体金溶液喷涂玻璃纤维纸,每261mm×220mm×0.5mm玻璃纤维纸上喷涂25ml免疫胶体金溶液,干燥,制得免疫胶体金纸片。
4.免疫硝酸纤维素膜的制备
4.1将羊抗兔igg用磷酸盐缓冲液稀释成0.4mg/ml,制得质控线(c线)溶液。
4.2将金刚烷胺-牛血清白蛋白复合物用磷酸盐缓冲液稀释至蛋白浓度为0.5mg/ml,制得检测线(t线)溶液。
4.3用点膜机喷点c、t线溶液,制得免疫硝酸纤维素膜。每1m长硝酸纤维素膜分别包被有1ml的c线和t线溶液,检测线和质控线的间距为5.0mm。
5.将滤样纸、免疫胶体金纸片、免疫硝酸纤维素膜、吸水纸依次粘贴在胶板上,切裁成宽度为4mm的试纸条(如图1所示)。
6.将检测试纸条装入塑料盒内即得检测试剂盒。
本发明设计的金刚烷胺胶体金检测试剂盒的阈值为1μg/ml。
实施例2
一种快速检测肉制品中金刚烷胺残留的方法,包括以下步骤:
1.样品制备:称取5g经均质组织样本,装入15ml离心管中;
2.标准品制备:取用金刚烷胺兽药粉末(98%含量,取0.041g,有效成分记为0.04g,溶于10ml水中,混匀即可),制备浓度为5ppb、0.4ppm、40ppm、4000ppm共4份不同浓度的溶液;
3.向15ml离心管中加入3ml乙腈、2ml三氯乙酸水溶液,充分振荡混匀3min,4000转/min离心5min;
4.用0.5ml一次性吸管取分层后的上清液(切勿吸取下层)全部(约2.5ml)加入到配套5ml离心管中,65℃下空气(或氮气)吹干(离心管管底有部分颗粒状未吹干黄色油脂属正常现象);
5.向吹干的5ml离心管中加入0.3ml(竖直滴加6滴)1m的pbs缓冲液,充分振摇溶解离心管底部及内壁固体残留物,此溶解液即为待检液;
6:检测:取待测液滴加入金标微孔中,反应3-5min即可。
实施例3
金刚烷胺胶体金检测试剂盒的灵敏度实验
1.检测方法:
1.1取实施例1制备的金刚烷胺胶体金检测试剂盒,将试剂盒放置在水平台面上。
1.2用加样吸管吸取样品,然后滴4滴(约120ul)样品到试剂盒的加样孔中。每检测一份不同的样品使用不同的吸管。
1.3观察结果:在滴加样品后3-5min判读结果。
2.检测样品:
配置金刚烷胺浓度为0μg/ml,0.5μg/l,2μg/l,40μg/ml,4mg/ml,的质控参考品作为样品,每个浓度重复3次。
3.检测结果:
浓度为0μg/ml,0.5μg/ml,的样本均显示阴性,2μg/l,40μg/ml,4mg/ml,的样本均显示阳性。本发明试剂盒的检测灵敏度为2μg/l,该金刚烷胺胶体金检测试剂盒灵敏度符合检测要求。
实施例4
金刚烷胺胶体金检测试剂盒的特异性实验
1.检测方法:
1.1取实施例1制得的金刚烷胺胶体金检测试剂盒,将试剂盒放置在水平台面上。
1.2用加样吸管吸取用于检测交叉反应实验的检测样品,然后滴4滴(约120ul)样品到试剂盒的加样孔中。每检测一份不同的样品使用不同的吸管。
1.3观察结果:在滴加样品后3-5min判读结果。
2.检测样品:
用不同浓度的氟苯尼考、五氯酚钠、磺胺、金刚烷胺等对本发明的试剂盒进行检测,观察是否发生交叉反应。
3.检测结果:
结果证实,本发明实施例的试剂盒对金刚烷胺的检测不会受到氟苯尼考、五氯酚钠、磺胺、金刚烷胺等的干扰,即本发明实施例的金刚烷胺胶体金试剂盒在一定浓度下,不会与类似效果的染料产生交叉反应,特异性良好。
实施例5
金刚烷胺胶体金检测试剂盒的重复性和稳定性实验
1.试剂盒的批内和批间重复性实验
1.1实验方法:
将同批和不同批次的金刚烷胺胶体金检测试剂盒分别检测0.1、0.5、1、2μg/l标准品,每个浓度重复3次,观察试剂盒的重复性。
1.2实验结果:经验证,金刚烷胺胶体金检测试剂盒的批内和批间重复性为100%,假阳性率和假阴性率均为0。
2.试剂盒的稳定性实验
2.1实验目的:
将金刚烷胺胶体金检测试剂盒密封保存,并存放于4℃及室温(25℃左右)下,观察不同存放温度对试剂盒稳定性的影响。
2.2实验方法:
保存于4℃的试剂盒每20天取出4份次,分别检测0.1、0.5、1、2μg/l浓度的标准品;保存于室温(25℃)的试剂盒每10天取出4份次,分别检测0.1、0.5、1、2μg/l浓度的标准品。
3.实验结果:
经验证,试纸条在4℃下可保存24个月,在室温下可保存18个月,在可保存的期限内,试剂盒均可达到2μg/l的检测灵敏度。
以上所描述的实施例是本发明一部分实施例,而不是全部的实施例。本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!