一种甲型通用及H7N9亚型流感病毒胶体金联合检测试纸的制备方法与流程
本发明涉及生物医药领域,特别是一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸的制备方法。
背景技术:
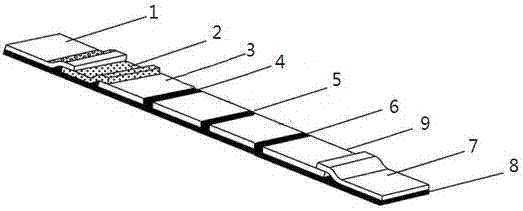
:流行性感冒病毒(influenzavirus),是正粘病毒科(orthomyxoviridae)的代表种,简称流感病毒,包括人类流感病毒、猪流感病毒、马流感病毒以及禽流感病毒等类群,其中人类流感病毒根据其核蛋白的抗原性可以分为:甲(a)、乙(b)、丙(c)三型,是流行性感冒(流感)的病原体。其中甲型流感病毒抗原性易发生变异,可以进一步分为h1n1、h3n2、h5n1、h7n9等亚型(h和n分别代表流感病毒血凝素和神经氨酸酶两种表面糖蛋白),多次引起世界性大流行。例如1918~1919年的大流行中,全世界至少有2000万~4000万人死于流感;乙型流感病毒对人类致病性也比较强,但是人们还没有发现乙型流感病毒引起过世界性大流行;丙型流感病毒只引起人类不明显的或轻微的上呼吸道感染,很少造成流行。甲型流感病毒于1933年分离成功,乙型流感病毒于1940年获得,丙型流感病毒直到1949年才成功分离。感染鸟类、猪等其他动物的流感病毒,其核蛋白的抗原性与人甲型流感病毒相同,但是由于甲型、乙型和丙型流感病毒的分类只是针对人流感病毒的,因此通常不将禽流感病毒等非人类宿主的流感病毒称作甲型流感病毒。流感病毒h7n9亚型是禽流感病毒的一个亚型,其传播会致人死亡,情况特殊,有基因突变的风险。人感染h7n9禽流感潜伏期一般为7天以内,患者一般表现为流感样症状,如发热,咳嗽,少痰,可伴有头痛、肌肉酸痛和全身不适。重症患者病情发展迅速,表现为重症肺炎,体温大多持续在39度以上,出现呼吸困难,可伴有咳血痰;可快速进展出现急性呼吸窘迫综合征、纵隔气肿、脓毒症、休克、意识障碍及急性肾损伤等,甚至死亡。由于流感病毒感染会降低呼吸道粘膜上皮细胞清除和黏附异物的能力,大大降低了人体抵御呼吸道感染的能力,因此流感经常会造成继发性感染,由流感造成的继发性肺炎是流感致死的主要死因之一。目前,流感的诊断主要是结合临床症状进行实验室检查,包括病毒分离培养鉴定和核酸检测方法。病毒分离培养常用的方法有动物接种、鸡胚接种和组织(细胞)培养等。根据病毒种类不同,敏感动物的选择,适宜接种的部位,或者培养细胞的来源都有不同。而且,病毒分离培养耗费时间长,环境要求高,操作者感染风险大,在临床诊断和流行病监测等方面的应用十分有限。核酸检测是直接检测病原体核酸的一系列技术的总称,也就是常说的基因检测,是通过血液、其他体液或细胞对病原体核酸进行检测的技术,可以诊断疾病,也可以用于疾病风险的预测,其基本步骤包括核酸提取、扩增和检测分析。由于核酸检测是直接检测病原体核酸,具有高敏感,高特异和短检测窗口期等优点,为疫病早诊断、早治疗、降低病死率以及控制疫情争取时间。但是,核酸检测需要掌握专业技术的专业人才在具备资质的专业实验室使用专业仪器设备才能进行,检测实验条件限制了该方法只能用于流感病毒的最终实验室确定性检测,并不能够适用于临床或流行病监测一线的快速检测。此外,虽然目前市场上有甲型流感病毒胶体金检测试纸,或者h7n9亚型流感病毒胶体金检测试纸,但是该类试纸并不能够特异、敏感、快速的检测h7n9流感病毒,而且不能同时对感染流感病毒的类型情况作出准确检测,尤其是对于致病性较强的h7n9亚型流感病毒不能作出快速检测。技术实现要素:针对上述情况,为解决现有技术之缺陷,本发明的目的就是提供一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸的制备方法,可有效解决现有甲型通用及h7n9流感病毒检测方法特异性低、敏感性差、费时、繁琐的问题。本发明解决的技术方案是,本发明一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸,包括试纸壳和试纸条,试纸条装在试纸壳内,试纸条包括样品垫、胶体金垫、反应膜、吸水垫和背衬,背衬上依次固定有样品垫、胶体金垫、反应膜和吸水垫,样品垫的后端扣压在胶体金垫的前端,胶体金垫的后端扣压在反应膜的前端,吸水垫的前端扣压在反应膜的后端,反应膜上依次包被有h7n9亚型流感病毒检测线、甲型流感病毒检测线和质控线;试纸壳上有样本孔和检测结果区,样本孔对应于试纸条上的样品垫,检测结果区上的t1、t2和c分别与试纸条上的h7n9亚型流感病毒检测线、甲型流感病毒检测线和质控线对应;其制备方法包括以下步骤:(1)制备样品垫所述样品垫包括样品处理液和玻纤膜;每1000ml样品处理液由18-22g牛血清白蛋白(bsa)、4-6g聚乙二醇辛基苯基醚(tritonx-100)和0.008-0.012m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;玻纤膜裁切成20-24mm宽,将100μl样品处理液喷涂在0.6-1.0cm长的玻纤膜上,37℃干燥过夜,得样品垫;(2)制备胶体金垫所述的胶体金垫包括玻纤膜和金标抗体液,玻纤膜裁切成5-9mm宽,将100μl金标抗体液喷涂在1.0-2.0cm长的玻纤膜上,干燥后密闭静置平衡10-14小时,即得胶体金垫;所述金标抗体液的制备包括:1)制备胶体金稀释液:每1000ml胶体金稀释液由8-12g牛血清白蛋白、23-27g蔗糖、0.4-0.6g吐温-20、0.8-1.2g叠氮钠和0.008-0.012m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;2)制备胶体金颗粒溶液:取质量浓度为0.01%的氯金酸水溶液40-60ml,加热至煮沸,加入质量浓度为1%的柠檬酸三钠水溶液550-650μl,加热至出现酒红色,再加入40-60ml、4℃预冷的电导率为18.20的纯净水,即得粒径为30nm的胶体金颗粒溶液;胶体金颗粒溶液吸收峰波长为530-535nm,吸光度值大于0.40;3)制备胶体金标记抗体:取步骤2)制备的胶体金颗粒溶液8-12ml,磁力搅拌条件下,加入体积浓度为30%的双氧水溶液30-35μl;室温磁力搅拌混合8-12min后,加入0.15-0.25m的碳酸钾水溶液280-320μl,室温磁力搅拌8-12min后,加入0.15-0.25mg纯化冻干的抗流感病毒单克隆抗体h1-13;抗流感病毒单克隆抗体h1-13冻干前缓冲液为0.01m,ph7.4的磷酸盐缓冲液;室温磁力搅拌60min后,加入0.08-0.12g牛血清白蛋白,室温磁力搅拌混合8-12min后,加入0.008-0.012g聚乙二醇6000,室温磁力搅拌混合25-35min,得金标抗体,将金标抗体移入离心管,在4℃,7000-9000rpm下离心8-12min,弃去上清,酒红色沉淀即为胶体金标记抗体;4)制备金标抗体液:用步骤1)制备的胶体金稀释液稀释步骤3)制备的胶体金标记抗体,至稀释后的金标抗体液在波长530-535nm下的吸光度值大于0.40,得金标抗体液;(3)制备检测线和对照线所述的检测线和对照线分别是按每厘米检测线用2μl点膜液,将检测抗体点膜液、对照抗体点膜液喷涂在反应膜上,室温晾干,即成:所述检测抗体点膜液和对照抗体点膜液的制备包括:1)制备点膜稀释液:所述点膜稀释液是由0.008-0.012m、ph为7.4的磷酸盐缓冲液,0.15mol/l氯化钠,10mol/l乙二胺四乙酸,1g/l叠氮钠,30g/l的甲醇,其余为超纯水制成;2)制备检测抗体点膜液:将纯化冻干的抗流感病毒单克隆抗体h7-50和a1-6,用点膜稀释液稀释至1.5-2.5mg/ml;所述抗流感病毒单克隆抗体h7-50和a1-6纯度均大于90%,效价大于1:105;3)制备对照抗体点膜液:将效价大于1:107的山羊抗小鼠多抗用点膜稀释液稀释至0.6-1.0mg/ml;(4)组装检测试纸首先将反应膜包被上h7n9亚型流感病毒检测线、甲型流感病毒检测线和质控线,再固定粘贴到背衬上,将胶体金垫的后端扣压在反应膜的前端,吸水垫的前端扣压在反应膜的后端,样品垫的后端扣压在胶体金垫的前端,将样品垫、胶体金垫、和吸水垫的其余部分固定在背衬上,得试纸条;再将试纸条装在试纸壳内,试纸壳上的样本孔对应于试纸条上的样品垫,检测结果区上的t1、t2和c分别与试纸条上的h7n9亚型流感病毒检测线、甲型流感病毒检测线和质控线对应;即得甲型通用及h7n9亚型流感病毒胶体金检测试纸。本发明利用甲型通用及h7n9亚型流感病毒单克隆抗体的特异性,制备出甲型通用及h7n9亚型流感病毒胶体金检测试纸,能够方便快捷的在临床和流行病监测一线特异性检测出甲型通用及h7n9亚型流感病毒,解决了目前只能够在实验室中利用核酸检测甲型通用及h7n9亚型流感病毒的缺陷,可以在一次检测中同时对甲型流感病毒和h7n9亚型流感病毒进行快速检测,便于在基层现场、疫病控制区、大中小医院和疾控单位场所等对人类或者禽类的流感传播情况和严重程度作出准确快速的监测,实现对甲型通用及h7n9亚型流感病毒简便、特异、灵敏的快速检测,结果稳定可靠,经济效益和社会效益十分显著。附图说明图1为本发明试纸条的结构主视图。图2为本发明试纸壳的结构主视图。图3为本发明的使用状态图。具体实施方式以下结合实施例和附图对本发明的具体实施方式作详细说明。本发明在具体实施中,是由以下实施例实现。本发明一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸,包括试纸壳10和试纸条9,试纸条9装在试纸壳10内,试纸条9包括样品垫1、胶体金垫2、反应膜3、吸水垫7和背衬8,背衬8上依次固定有样品垫1、胶体金垫2、反应膜3和吸水垫7,样品垫1的后端扣压在胶体金垫2的前端,胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,反应膜3上依次包被有h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6;试纸壳10上有样本孔11和检测结果区12,样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;其制备方法包括以下步骤:(1)制备样品垫所述样品垫1包括样品处理液和玻纤膜;每1000ml样品处理液由18-22g牛血清白蛋白(bsa)、4-6g聚乙二醇辛基苯基醚(tritonx-100)和0.008-0.012m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;玻纤膜裁切成20-24mm宽,将100μl样品处理液喷涂在0.6-1.0cm长的玻纤膜上,37℃干燥过夜,得样品垫1;(2)制备胶体金垫所述的胶体金垫2包括玻纤膜和金标抗体液,玻纤膜裁切成5-9mm宽,将100μl金标抗体液喷涂在1.0-2.0cm长的玻纤膜上,干燥后密闭静置平衡10-14小时,即得胶体金垫2;所述金标抗体液的制备包括:1)制备胶体金稀释液:每1000ml胶体金稀释液由8-12g牛血清白蛋白、23-27g蔗糖、0.4-0.6g吐温-20、0.8-1.2g叠氮钠和0.008-0.012m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;2)制备胶体金颗粒溶液:取质量浓度为0.01%的氯金酸水溶液40-60ml,加热至煮沸,加入质量浓度为1%的柠檬酸三钠水溶液550-650μl,加热至出现酒红色,再加入40-60ml、4℃预冷的电导率为18.20的纯净水,即得粒径为30nm的胶体金颗粒溶液;胶体金颗粒溶液吸收峰波长为530-535nm,吸光度值大于0.40;3)制备胶体金标记抗体:取步骤2)制备的胶体金颗粒溶液8-12ml,磁力搅拌条件下,加入体积浓度为30%的双氧水溶液30-35μl;室温磁力搅拌混合8-12min后,加入0.15-0.25m的碳酸钾水溶液280-320μl,室温磁力搅拌8-12min后,加入0.15-0.25mg纯化冻干的抗流感病毒单克隆抗体h1-13;抗流感病毒单克隆抗体h1-13冻干前缓冲液为0.01m,ph7.4的磷酸盐缓冲液;室温磁力搅拌60min后,加入0.08-0.12g牛血清白蛋白,室温磁力搅拌混合8-12min后,加入0.008-0.012g聚乙二醇6000,室温磁力搅拌混合25-35min,得金标抗体,将金标抗体移入离心管,在4℃,7000-9000rpm下离心8-12min,弃去上清,酒红色沉淀即为胶体金标记抗体;4)制备金标抗体液:用步骤1)制备的胶体金稀释液稀释步骤3)制备的胶体金标记抗体,至稀释后的金标抗体液在530-535nm下的吸光度值大于0.40,得金标抗体液;(3)制备检测线和对照线所述的检测线和对照线分别是按每厘米检测线用2μl点膜液,将检测抗体点膜液、对照抗体点膜液喷涂在反应膜上,室温晾干,即成:所述检测抗体点膜液和对照抗体点膜液的制备包括:1)制备点膜稀释液:所述点膜稀释液是由0.008-0.012m、ph为7.4的磷酸盐缓冲液,0.15mol/l氯化钠,10mol/l乙二胺四乙酸,1g/l叠氮钠,30g/l的甲醇,其余为超纯水制成;2)制备检测抗体点膜液:将纯化冻干的抗流感病毒单克隆抗体h7-50和a1-6,用点膜稀释液稀释至1.5-2.5mg/ml;所述抗流感病毒单克隆抗体h7-50和a1-6纯度均大于90%,效价大于1:105;3)制备对照抗体点膜液:将效价大于1:107的山羊抗小鼠多抗用点膜稀释液稀释至0.6-1.0mg/ml;(4)组装检测试纸首先将反应膜3包被上h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6,再固定粘贴到背衬8上,将胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,样品垫1的后端扣压在胶体金垫2的前端,将样品垫1、胶体金垫2、和吸水垫7的其余部分固定在背衬8上,得试纸条9;再将试纸条9装在试纸壳10内,试纸壳10上的样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;即得甲型通用及h7n9亚型流感病毒胶体金检测试纸。实施例1本发明一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸,包括试纸壳10和试纸条9,试纸条9装在试纸壳10内,试纸条9包括样品垫1、胶体金垫2、反应膜3、吸水垫7和背衬8,背衬8上依次固定有样品垫1、胶体金垫2、反应膜3和吸水垫7,样品垫1的后端扣压在胶体金垫2的前端,胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,反应膜3上依次包被有h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6;试纸壳10上有样本孔11和检测结果区12,样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;其制备方法包括以下步骤:(1)制备样品垫所述样品垫1包括样品处理液和玻纤膜;每1000ml样品处理液由18g牛血清白蛋白、4g聚乙二醇辛基苯基醚和0.008m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;玻纤膜裁切成20mm宽,将100μl样品处理液喷涂在1.0cm长的玻纤膜上,37℃干燥过夜,得样品垫1;(2)制备胶体金垫所述的胶体金垫2包括玻纤膜和金标抗体液,玻纤膜裁切成5mm宽,将100μl金标抗体液喷涂在2.0cm长的玻纤膜上,干燥后密闭静置平衡10小时,即得胶体金垫2;所述金标抗体液的制备包括:1)制备胶体金稀释液:每1000ml胶体金稀释液由8g牛血清白蛋白、23g蔗糖、0.4g吐温-20、0.8g叠氮钠和0.008m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;2)制备胶体金颗粒溶液:取质量浓度为0.01%的氯金酸水溶液40ml,加热至煮沸,加入质量浓度为1%的柠檬酸三钠水溶液550μl,加热至出现酒红色,再加入40ml、4℃预冷的电导率为18.20的纯净水,即得粒径为30nm的胶体金颗粒溶液;胶体金颗粒溶液吸收峰波长为530nm,吸光度值大于0.40;3)制备胶体金标记抗体:取步骤2)制备的胶体金颗粒溶液8ml,磁力搅拌条件下,加入体积浓度为30%的双氧水溶液30μl;室温磁力搅拌混合8min后,加入0.15m的碳酸钾水溶液280μl,室温磁力搅拌8min后,加入0.15mg纯化冻干的抗流感病毒单克隆抗体h1-13;抗流感病毒单克隆抗体h1-13冻干前缓冲液为0.01m,ph7.4的磷酸盐缓冲液;室温磁力搅拌60min后,加入0.08g牛血清白蛋白,室温磁力搅拌混合8min后,加入0.008g聚乙二醇6000,室温磁力搅拌混合25min,得金标抗体,将金标抗体移入离心管,在4℃,7000rpm下离心12min,弃去上清,酒红色沉淀即为胶体金标记抗体;4)制备金标抗体液:用步骤1)制备的胶体金稀释液稀释步骤3)制备的胶体金标记抗体,至稀释后的金标抗体液在530nm下的吸光度值大于0.40,得金标抗体液;(3)制备检测线和对照线所述的检测线和对照线分别是按每厘米检测线用2μl点膜液,将检测抗体点膜液、对照抗体点膜液喷涂在反应膜上,室温晾干,即成:所述检测抗体点膜液和对照抗体点膜液的制备包括:1)制备点膜稀释液:所述点膜稀释液是由0.008m、ph为7.4的磷酸盐缓冲液,0.13mol/l氯化钠,8mol/l乙二胺四乙酸,0.8g/l叠氮钠,28g/l的甲醇,其余为超纯水制成;2)制备检测抗体点膜液:将纯化冻干的抗流感病毒单克隆抗体h7-50和a1-6,用点膜稀释液稀释至1.5-2.5mg/ml;所述抗流感病毒单克隆抗体h7-50和a1-6纯度均大于90%,效价大于1:105;3)制备对照抗体点膜液:效价大于1:107的山羊抗小鼠多抗用点膜稀释液稀释至0.6-1.0mg/ml;(4)组装检测试纸首先将反应膜3包被上h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6,再固定粘贴到背衬8上,将胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,样品垫1的后端扣压在胶体金垫2的前端,将样品垫1、胶体金垫2、和吸水垫7的其余部分固定在背衬8上,得试纸条9;再将试纸条9装在试纸壳10内,试纸壳10上的样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;即得甲型通用及h7n9亚型流感病毒胶体金检测试纸。实施例2本发明一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸,包括试纸壳10和试纸条9,试纸条9装在试纸壳10内,试纸条9包括样品垫1、胶体金垫2、反应膜3、吸水垫7和背衬8,背衬8上依次固定有样品垫1、胶体金垫2、反应膜3和吸水垫7,样品垫1的后端扣压在胶体金垫2的前端,胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,反应膜3上依次包被有h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6;试纸壳10上有样本孔11和检测结果区12,样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;其制备方法包括以下步骤:(1)制备样品垫所述样品垫1包括样品处理液和玻纤膜;每1000ml样品处理液由20g牛血清白蛋白、5g聚乙二醇辛基苯基醚和0.01m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;玻纤膜裁切成22mm宽,将100μl样品处理液喷涂在0.8cm长的玻纤膜上,37℃干燥过夜,得样品垫1;(2)制备胶体金垫所述的胶体金垫2包括玻纤膜和金标抗体液,玻纤膜裁切成7mm宽,将100μl金标抗体液喷涂在1.6cm长的玻纤膜上,干燥后密闭静置平衡12小时,即得胶体金垫2;所述金标抗体液的制备包括:1)制备胶体金稀释液:每1000ml胶体金稀释液由10g牛血清白蛋白、25g蔗糖、0.5g吐温-20、1.0g叠氮钠和0.01m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;2)制备胶体金颗粒溶液:取质量浓度为0.01%的氯金酸水溶液50ml,加热至煮沸,加入质量浓度为1%的柠檬酸三钠水溶液600μl,加热至出现酒红色,再加入50ml、4℃预冷的电导率为18.20的纯净水,即得粒径为30nm的胶体金颗粒溶液;胶体金颗粒溶液吸收峰波长为533nm,吸光度值大于0.40;3)制备胶体金标记抗体:取步骤2)制备的胶体金颗粒溶液10ml,磁力搅拌条件下,加入体积浓度为30%的双氧水溶液32μl;室温磁力搅拌混合10min后,加入0.2m的碳酸钾水溶液300μl,室温磁力搅拌10min后,加入0.2mg纯化冻干的抗流感病毒单克隆抗体h1-13;抗流感病毒单克隆抗体h1-13冻干前缓冲液为0.01m,ph7.4的磷酸盐缓冲液;室温磁力搅拌60min后,加入0.1g牛血清白蛋白,室温磁力搅拌混合10min后,加入0.01g聚乙二醇6000,室温磁力搅拌混合30min,得金标抗体,将金标抗体移入离心管,在4℃,8000rpm下离心10min,弃去上清,酒红色沉淀即为胶体金标记抗体;4)制备金标抗体液:用步骤1)制备的胶体金稀释液稀释步骤3)制备的胶体金标记抗体,至稀释后的金标抗体液在533nm下的吸光度值大于0.40,得金标抗体液;(3)制备检测线和对照线所述的检测线和对照线分别是按每厘米检测线用2μl点膜液,将检测抗体点膜液、对照抗体点膜液喷涂在反应膜上,室温晾干,即成:所述检测抗体点膜液和对照抗体点膜液的制备包括:1)制备点膜稀释液:所述点膜稀释液是由0.01m、ph为7.4的磷酸盐缓冲液,0.15mol/l氯化钠,10mol/l乙二胺四乙酸,1.0g/l叠氮钠,30g/l的甲醇,其余为超纯水制成;2)制备检测抗体点膜液:将纯化冻干的抗流感病毒单克隆抗体h7-50和a1-6,用点膜稀释液稀释至2.0mg/ml;所述抗流感病毒单克隆抗体h7-50和a1-6纯度均大于90%,效价大于1:105;3)制备对照抗体点膜液:将效价大于1:107的山羊抗小鼠多抗用点膜稀释液稀释至0.8mg/ml;(4)组装检测试纸首先将反应膜3包被上h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6,再固定粘贴到背衬8上,将胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,样品垫1的后端扣压在胶体金垫2的前端,将样品垫1、胶体金垫2、和吸水垫7的其余部分固定在背衬8上,得试纸条9;再将试纸条9装在试纸壳10内,试纸壳10上的样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;即得甲型通用及h7n9亚型流感病毒胶体金检测试纸。实施例3本发明一种甲型通用及h7n9亚型流感病毒胶体金联合检测试纸,包括试纸壳10和试纸条9,试纸条9装在试纸壳10内,试纸条9包括样品垫1、胶体金垫2、反应膜3、吸水垫7和背衬8,背衬8上依次固定有样品垫1、胶体金垫2、反应膜3和吸水垫7,样品垫1的后端扣压在胶体金垫2的前端,胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,反应膜3上依次包被有h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6;试纸壳10上有样本孔11和检测结果区12,样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;其制备方法包括以下步骤:(1)制备样品垫所述样品垫1包括样品处理液和玻纤膜;每1000ml样品处理液由22g牛血清白蛋白、6g聚乙二醇辛基苯基醚和0.012m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;玻纤膜裁切成24mm宽,将100μl样品处理液喷涂在0.6cm长的玻纤膜上,37℃干燥过夜,得样品垫1;(2)制备胶体金垫所述的胶体金垫2包括玻纤膜和金标抗体液,玻纤膜裁切成9mm宽,将100μl金标抗体液喷涂在1.0cm长的玻纤膜上,干燥后密闭静置平衡14小时,即得胶体金垫2;所述金标抗体液的制备包括:1)制备胶体金稀释液:每1000ml胶体金稀释液由12g牛血清白蛋白、27g蔗糖、0.6g吐温-20、1.2g叠氮钠和0.012m、ph为7.4的磷酸盐缓冲液,余量为超纯水制成;2)制备胶体金颗粒溶液:取质量浓度为0.01%的氯金酸水溶液60ml,加热至煮沸,加入质量浓度为1%的柠檬酸三钠水溶液650μl,加热至出现酒红色,再加入60ml、4℃预冷的电导率为18.20的纯净水,即得粒径为30nm的胶体金颗粒溶液;胶体金颗粒溶液吸收峰波长为535nm,吸光度值大于0.40;3)制备胶体金标记抗体:取步骤2)制备的胶体金颗粒溶液12ml,磁力搅拌条件下,加入体积浓度为30%的双氧水溶液35μl;室温磁力搅拌混合12min后,加入0.25m的碳酸钾水溶液320μl,室温磁力搅拌12min后,加入0.25mg纯化冻干的抗流感病毒单克隆抗体h1-13;抗流感病毒单克隆抗体h1-13冻干前缓冲液为0.01m,ph7.4的磷酸盐缓冲液;室温磁力搅拌60min后,加入0.12g牛血清白蛋白,室温磁力搅拌混合12min后,加入0.012g聚乙二醇6000,室温磁力搅拌混合35min,得金标抗体,将金标抗体移入离心管,在4℃,9000rpm下离心8min,弃去上清,酒红色沉淀即为胶体金标记抗体;4)制备金标抗体液:用步骤1)制备的胶体金稀释液稀释步骤3)制备的胶体金标记抗体,至稀释后的金标抗体液在535nm下的吸光度值大于0.40,得金标抗体液;(3)制备检测线和对照线所述的检测线和对照线分别是按每厘米检测线用2μl点膜液,将检测抗体点膜液、对照抗体点膜液喷涂在反应膜上,室温晾干,即成:所述检测抗体点膜液和对照抗体点膜液的制备包括:1)制备点膜稀释液:所述点膜稀释液是由0.012m、ph为7.4的磷酸盐缓冲液,0.17mol/l氯化钠,12mol/l乙二胺四乙酸,1.2g/l叠氮钠,32g/l的甲醇,其余为超纯水制成;2)制备检测抗体点膜液:将纯化冻干的抗流感病毒单克隆抗体h7-50和a1-6,用点膜稀释液稀释至2.5mg/ml;所述抗流感病毒单克隆抗体h7-50和a1-6纯度均大于90%,效价大于1:105;3)制备对照抗体点膜液:将效价大于1:107的山羊抗小鼠多抗用点膜稀释液稀释至1.0mg/ml;(4)组装检测试纸首先将反应膜3包被上h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6,再固定粘贴到背衬8上,将胶体金垫2的后端扣压在反应膜3的前端,吸水垫7的前端扣压在反应膜3的后端,样品垫1的后端扣压在胶体金垫2的前端,将样品垫1、胶体金垫2、和吸水垫7的其余部分固定在背衬8上,得试纸条9;再将试纸条9装在试纸壳10内,试纸壳10上的样本孔11对应于试纸条9上的样品垫1,检测结果区12上的t1、t2和c分别与试纸条9上的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6对应;即得甲型通用及h7n9亚型流感病毒胶体金检测试纸。所述的反应膜3的材质是硝酸纤维素膜,型号为:millipore,m135,制备时将反应膜裁切成宽度为25mm的条;所述的吸水垫7的材质是加厚吸水纸,将加厚吸水纸裁切成宽度为26mm的条,然后将其粘贴到背衬相应位置上即可。所述的背衬8尺寸为77mm×4mm。所述的胶体金垫2尺寸为7mm×4mm。所述的反应膜3尺寸为25mm×4mm。所述的h7n9亚型流感病毒检测线4、甲型流感病毒检测线5和质控线6尺寸为1-2mm×4mm。所述的吸水垫7尺寸为26mm×4mm。所述的样品垫1尺寸为22mm×4mm。所述的样品垫1一端扣压住胶体金垫21mm,胶体金垫2一端扣压住反应膜41mm,吸水垫7一端扣压住反应膜41mm。样品垫上含有处理样品成分的化学试剂,当含有流感病毒的样品液滴到其上时,它会溶解样品垫中的化学试剂,对样品中的h7n9流感病毒进行裂解、调整反应体系的离子强度和ph值等,并对非特异杂质进行封闭,使其更符合抗原抗体反应条件,有利于样品中的h7n9流感病毒抗原与金垫上的抗体结合。金垫上含有胶体金标记的抗h7n9流感病毒特异性单克隆抗体及其相关化学试剂,显示酒红色。当这些胶体金标记的抗h7n9流感病毒特异性单克隆抗体在俘获到流感病毒抗原后,随着液体侧向流,h7n9流感病毒抗原又与相应的检测线处的另一特异性抗h7n9流感病毒单克隆抗体结合而大量聚集,肉眼就可见红色或粉红色条带。反应膜上划有检测线和对照线,是免疫显色反应线的形成处。检测线处固定有特异的抗流感病毒单克隆抗体,可以和随液体侧向流扩散过来的流感病毒抗原与胶体金标记的流感病毒单克隆抗体复合物结合,对流感病毒抗原形成双抗体夹心,通过胶体金显色,指示出检测阳性带。对照线处固定有羊抗鼠抗体,可以和未与检测带结合的胶体金标记的单克隆抗体结合(鼠源性单克隆抗体),以确定反应体系是正常的。吸收垫的作用是在反应完全后对反应体系多余液体进行吸收、存储。本发明甲型通用及h7n9亚型流感病毒胶体金检测试纸检测方法:1.样本收集1)人类鼻/咽拭子:采集咽拭子时,病人坐下,头后倾,张大嘴,由检查者用压舌板固定舌头。用棉签采集舌腭弓后,扁桃体隐窝至咽后壁,反复擦拭3~5次,收集粘膜细胞,避免触及舌、口腔粘膜和唾液。采集鼻拭子时,将鼻拭子插入鼻孔分泌物较多处,轻轻转动并推动鼻拭子,直至鼻甲(离鼻孔约2.5cm)受阻处,贴鼻壁旋转拭子三次,采好样品的拭子,置于预加有0.3ml标本提取液的离心管中,漩涡振荡混匀,置于4℃冰箱备用(样品最多保存8h)。2)禽类粪便:采集粪便标本一般取新鲜的自然排出的粪便3~5g,必要时可肛拭子采取,放入干燥、清洁、无吸水性的有盖容器内,贴好标识送检。盛粪便标本的容器必须有盖,有明显标记。要选取粪便的脓、血、粘液等异常成分进行检查。表面无异常时应从粪便表面、深处及粪端多处取材,采好样品的拭子,置于预加有1ml标本提取液的离心管中,漩涡振荡混匀,置于4℃冰箱备用。2.检验方法测试前请将所有试剂恢复至室温,测试应在室温下进行。1)样本处理a在离心管内垂直加入300μl样本提取液。b将采样后的鼻咽拭子插入样本提取管的溶液内,紧靠离心管内壁旋转约10次,使标本尽可能溶解在提取溶液中。c沿离心管内壁挤压鼻拭子的棉签头,使液体尽可能留在管内,取出并弃去鼻拭子。d用漩涡混合器混匀30秒,待用。2)检测程序a沿铝箔袋撕口处打开,将测试卡(即本发明试纸)取出平放。b向测试卡的样本孔中加入100μl处理后的标本提取物。c15~20分钟内观察显示的结果,在20分钟后显示的结果无效。3.检验结果的判读(如图3所示)阳性:三条红色/粉色反应线,即在检测区(t1和t2)及质控区(c)各出现一条红色/粉色/棕色反应线。证明h7n9亚型和甲型流感病毒均为阳性反应。阳性:二条红色/粉色反应线,即在检测区(t2)及质控区(c)各出现一条红色/粉色/棕色反应线。证明甲型流感病毒为阳性反应。阴性:一条红色/粉色反应线,即仅在质控区(c)出现一条红色/粉色反应线。无效:质控区(c)无红色/粉色/棕色反应线出现,检测无效,建议此时用新试卡重新检测。注:条带显色深浅与提取样本中所含的被测物质含量有关,不论颜色强度多少,都应按照条带是否显色判断结果。本发明内含质控过程,当c区出现红色条带,表明操作正确有效,否则测试无效。表1核酸检测/本发明胶体金检测结果对照检测方法h7n9流感病毒核酸检测符合率对照标本核酸检测符合率核酸检测98100198100胶体金检测98100198100综上,本发明对病人或者禽类无创取材、操作简便,快速,可在十分钟内出结果,无需仪器设备,检测成本低,检测过程无污染产生、对甲型流感病毒各亚型,尤其是h7n9亚型均可检测,适用于对流行病现场进行快速、大规模批量检测,具有良好的经济和社会效益。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1