一种检测人幽门螺旋杆菌抗体的荧光免疫层析试剂盒及其制备方法与流程
本发明属于体外诊断试剂免疫层析诊断
技术领域:
,具体涉及一种检测人幽门螺旋杆菌抗体的荧光免疫层析试剂盒及其制备方法。
背景技术:
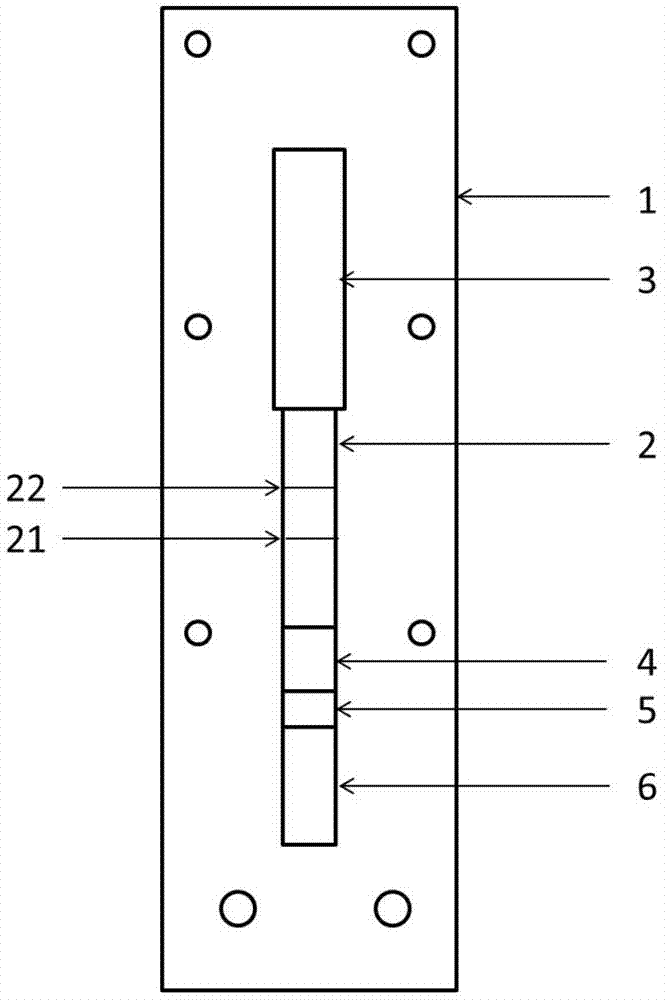
:幽门螺杆菌(helicobacterpylori,hp)是一种寄生在胃部和十二指肠的革兰氏阴性微量需氧细菌,其感染非常普遍,全球自然人群感染率超过50%。几乎所有的幽门螺杆菌感染者在组织学上均存在慢性活动性炎性反应,最新的专家共识将hp胃炎明确为“一种感染(传染)性疾病”,但其中约70%以上感染者无症状,其他可导致慢性胃炎、消化性溃疡等,常见症状包括胃上部不适感以及疼痛、胀气、厌食、恶心、呕吐以及深色或焦油色粪便等。研究表明幽门螺杆菌是胃炎、消化性溃疡的主要致病因素,并且与功能性消化不良、胃黏膜相关性淋巴组织(malt)淋巴瘤、胃癌的发生密切相关,世界卫生组织国际癌症研究机构已将其纳入一类致癌因子。有关幽门螺杆菌感染的国际指南中指出,根除幽门螺杆菌可显著减少胃和十二指肠疾病包括胃癌的发病率,并可在未来减少幽门螺杆菌感染的新发病例。幽门螺杆菌感染的诊断方法依据取材有无创伤性分为两大类:侵入性检测方法和非侵入性检测方法。前者是指依赖胃镜取材的检测方法,包括组织学检测(如he染色、warthin-starry银染、改良giemsa染色、甲苯胺蓝染色、丫啶橙染色、免疫组织化学染色等)、细菌培养和快速尿素酶试验(rut)等;后者则包括血清学(抗体)检测、粪便抗原检测和尿素呼气试验(ubt)等。不同的诊断方法有各自的优势和局限性。现有的幽门螺旋杆菌的检测试剂盒存在制备方法复杂、耗时长、价格昂贵等问题。技术实现要素:本发明的目的是解决上述现有技术的不足,提供一种检测人幽门螺旋杆菌抗体的荧光免疫层析试剂盒及其制备方法。本发明是通过以下技术方案实现的:一种检测人幽门螺旋杆菌抗体的荧光免疫层析试剂盒,包括支持物(1),固定在支持物(1)上的印迹膜(2),固定在印迹膜(2)一端的吸水垫(3)和另一端的结合垫(4),结合垫(4)的另一端固定有样本垫(5),样本垫(5)另一端固定有滤血膜(6);所述印迹膜(2)上设置有包被cagaa、尿素酶和细胞空泡毒素(vaca)重组抗原混合物的检测线(21),以及包被羊抗鼠igg的控制线(22);所述结合垫(4)喷制有偶联鼠抗人igg的荧光乳胶微球。优选地,所述支持物(1)为塑料板。优选地,所述印迹膜(2)为硝酸纤维素膜。优选地,所述检测线(21)上包被的cagaa、尿素酶和细胞空泡毒素重组抗原的质量比为(2-3):(0.5-1.5):(0.5-1.5)。优选地,所述荧光乳胶微球为结合荧光标记物探针的聚苯乙烯乳胶微球,可由光电倍增管直接检测激发荧光信号,具有较高温度信噪比、更高的信号检测量和检测灵敏度。一种所述的检测人幽门螺旋杆菌抗体的荧光免疫层析试剂盒的制备方法,包括以下步骤:(1)制备划有检测线(21)、控制线(22)的印迹膜(2),在37℃环境下干燥0.5-1.5小时;(2)制备喷制有偶联鼠抗人igg荧光乳胶微球的结合垫(4),在37℃环境下干燥2-4小时;(3)在支持物(1)上放置步骤(1)制备的印迹膜(2),在印迹膜(2)一端设置吸水垫,另一端设置步骤(2)制备的结合垫(4),在结合垫(4)另一端设置样本垫(5),在样本垫(5)另一端设置滤血膜(6)。优选地,步骤(1)所述的检测线(21)与控制线(22)需连续且粗细均匀。优选地,步骤(2)所述制备喷制有偶联鼠抗人igg荧光乳胶微球的结合垫具体包括以下顺序步骤:(21)取荧光乳胶微球加入初洗液超声混匀后转速10000-15000rpm,离心不少于15min,弃上清液;(22)依次加入活化液1和活化液2,活化10-30min,活化条件为35-40℃,100-150rpm;活化后转速10000-15000rpm,离心不少于15min,弃上清液;(23)加偶联缓冲液超声至清透后离心不少于15min,弃上清液,得偶联液;(24)加入鼠抗人igg与偶联液混匀,偶联,反应结束后离心不少于15min;(25)加封闭液封闭,封闭结束后离心不少于15min,弃上清液;(26)加终洗液超声至清透后离心不少于15min,弃上清液;(27)加微球稀释液稀释定容;(28)将定容后的微球用微球稀释液稀释后喷在玻璃纤维素膜上,喷涂体积为8-12μl/cm;其中,初洗液为1.95g/l的吗啉乙磺酸与0.5‰的tween-20,naoh调ph至5.5;活化液1为初洗液配制的n-羟基硫代琥珀酰亚胺钠盐,浓度20mg/ml;活化液2为初洗液配制的1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,浓度20mg/ml;偶联缓冲液为1.95g/l的吗啉乙磺酸与0.5‰的tween-20,naoh调ph至7.0;封闭液为5g/l的牛血清白蛋白,2‰的tween-20与0.2mol/l的硼酸缓冲液;终洗液为6g/l的trisbase、0.5‰的tween-20、0.3‰的proclin300与5g/l的牛血清白蛋白,调ph至8.0;微球稀释液为20%海藻糖、1%s9、0.5%牛血清白蛋白、0.5‰的tween-20与10mmtrisbase,调ph至8.0。优选地,步骤(22)所述荧光微球活化过程需避光进行。优选地,步骤(24)所述鼠抗人igg与偶联液的质量比为(0.5-1.0):(3-6),偶联方法为37℃、100-150rpm偶联不少于2小时。优选地,步骤(25)所述封闭方法为加封闭液37℃、150rpm封闭活性基团不少于30-45min。优选地,所述超声均使微球及其偶联抗体完全分散,离心管内溶液清澈透光。优选地,步骤(28)所述喷出来的微球应呈雾状分散在玻璃纤维素膜上。本发明的设计原理是:幽门螺旋杆菌检测试剂盒在使用时,将待测样本加入试剂盒的样品点样处(滤血膜),滤血膜可除去血清中的血液凝块,样本经过结合垫时,结合垫上的微球偶联抗体鼠抗人igg能无差别的吸附血清中人igg抗体,微球经过印迹膜的检测线时,其上吸附的人igg抗体中的hp抗体可被检测线上包被的特异性hp重组抗原抓住,之后通过控制线时,微球吸附的鼠抗人igg抗体被检测线包被的羊抗鼠igg抗体捕获,因此可定量检测样本中的幽门螺旋杆菌抗原。本发明的有益效果在于:本发明幽门螺旋杆菌检测用试剂盒,利用间接法原理结合荧光乳胶微球的荧光特性实现了采用荧光免疫层析的方法对幽门螺旋杆菌抗体进行快速、灵敏的定量检测。本发明幽门螺旋杆菌检测用试剂盒的制备方法,操作简单快捷,便于控制,成本较低。附图说明图1为本发明检测人幽门螺旋杆菌抗体的荧光免疫层析试剂盒的示意图;图2为本发明实施例3中检测线(t线)和控制线(c线)的发光值比值(t/c值)与相应标准品浓度的标准曲线。附图标记:1,支持物;2,印迹膜;3,吸水垫;4,结合垫;5,样本垫;6,滤血膜。具体实施方式为更好理解本发明,下面结合实施例及附图对本发明作进一步描述,以下实施例仅是对本发明进行说明而非对其加以限定。实施例1本实施例幽门螺旋杆菌检测用试剂盒,如图1所示,包括支持物1,设置在支持物1上的印迹膜2,设置在印迹膜2一端为吸水垫3,对应另一端为结合垫4,设置在结合垫4另一端为样本垫5,设置在样本垫5另一端为滤血膜6。其中,支持物1选用塑料板,印迹膜2选用硝酸纤维素膜。硝酸纤维膜上设置有检测线21和控制线22,检测线21包被有cagaa、尿素酶和细胞空泡毒素(vaca)重组抗原混合物;控制线22包被有羊抗鼠igg。结合垫4喷制有偶联鼠抗人igg的荧光乳胶微球。硝酸纤维膜检测线21上包被的cagaa、尿素酶和细胞空炮毒素基因(vaca)重组抗原的混合质量比为(2-3):(0.5-1.5):(0.5-1.5)。本实施例幽门螺旋杆菌检测用试剂盒的制备方法,具体步骤为:⑴硝酸纤维素膜制备:将cagaa、尿素酶和细胞空炮毒素(vaca)重组抗原用磷酸缓冲液稀释成浓度为2-3mg/ml、0.5-1.5mg/ml、0.5-1.5mg/ml的混合抗原。将羊抗鼠igg用磷酸缓冲液稀释成浓度为1mg/ml。采用喷膜划线仪将hp重组抗原(cagaa、尿素酶和vaca重组抗原混合物)与羊抗鼠igg分别划线在硝酸纤维素膜上,37℃干燥1小时,备用。⑵结合垫制备:①溶液配制a:初洗液为1.95g/l的吗啉乙磺酸与万分之五的tween-20,氢氧化钠调ph至5.5。b:活化液1为初洗液稀释的n-羟基硫代琥珀酰亚胺钠盐,浓度20mg/ml;活化液2为初洗液稀释的1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,浓度20mg/ml。c:偶联液为1.95g/l的吗啉乙磺酸与0.5‰的tween-20,氢氧化钠调ph至7.0。d:封闭液为5g/l的牛血清白蛋白,2‰的tween-20与0.2mol/l的硼酸缓冲液。e:终洗液为6g/l的trisbase、0.5‰的tween-20、0.3‰的proclin300与5g/l的牛血清白蛋白,调ph值8.0。f:微球稀释液为20%海藻糖、1%s9、0.5%牛血清白蛋白、0.5‰的tween-20与10mmtrisbase,调ph至8.0。②荧光乳胶微球偶联抗体a:取荧光乳胶微球加入初洗液超声混匀后15000rpm离心15min,弃上清液。b:依次加入活化液1和活化液2,于37℃150rpm活化15min;活化后15000rpm离心15min,弃上清液。c:加偶联液超声至清透后15000rpm离心15min,弃上清液。d:加入鼠抗人igg与偶联液混匀,于37℃150rpm摇床上偶联2小时,离心15min,弃上清液。e:加500ul封闭液封闭微球的活性基团,37℃150rpm摇床上封闭30min,15000rpm离心15min,弃上清液。f:加终洗液超声至清透后离心15min,弃上清液。g:加微球稀释液稀释定容至1毫升。③结合垫制备将定容后的微球用微球稀释液10倍稀释后在喷7毫米宽度的玻璃纤维素膜上,喷制体积为12μl/cm。37℃干燥3小时,备用。⑶试剂条组装在塑料板上放置步骤(1)制备的硝酸纤维素膜,在硝酸纤维素膜一端为吸水垫,对应另一端为结合垫,设置在结合垫另一端为样本垫,设置在样本垫另一端为滤血膜。实施例2本实施例幽门螺旋杆菌检测用试剂盒,与实施例1不同的是,在微球偶联抗体过程中,于37℃100-150rpm摇床上偶联1小时,偶联后不离心直接加500ul封闭液封闭微球的活性基团,37℃150rpm摇床上封闭30min。其他同实施例1。实施例1和实施例2检测相同的样本,数据见表1。表1实施例1和实施例2检测相同的样本时检测浓度的变异系数cv<15%,实施例1和实施例2两种试剂条检测结果无明显差别。实施例3将幽门螺旋杆菌抗体稀释成1.56ug/l、3.13ug/l、6.25ug/l、12.5ug/l、25ug/l、50ug/l共6个浓度梯度作为标准品溶液,同时配制空白溶液。分别取6个标准品及空白溶液各80微升加入到试剂条的加样区(样本垫),15min后插入hitfia-必欧瀚荧光免疫分析仪上(必欧瀚生物技术(合肥)有限公司)读数,每个标准品检测3次。读取检测线(t线)和控制线(c线)的发光值及t/c值,见表2。计算t/c值与相应标准品的浓度关系,绘制标准曲线,见图2。标准曲线回归方程见表3。检测限可达到0.5ug/l。表2表3四参数logistic曲线拟合实施例4取36例随机的临床样本,采用本发明实施例1制备的试剂盒对幽门螺旋杆菌的抗体进行检测。检测方法为:80微升待测样本滴入试剂条加样区(样本垫)上,15min后插入hitfia-必欧瀚荧光免疫分析仪上(必欧瀚生物技术(合肥)有限公司)读数,每个标准品检测2次。读取检测线(t线)和控制线(c线)的发光值、t/c值,将样本的t/c值代入标准曲线中,计算浓度值,结果见表4。本实施例试剂条的灵敏度和精密度见表5。表4临床样本t线c线t/c值浓度(ug/l)19061588268829200.33712.70569824994028235387120.21221.689066345583015195094032.336515.162556411802745218930440.53914.203843518458660237883260.7765.8319096100258949239065324.193825.008855718279147309514520.59064.56725785492716247922920.22151.768491991866619220313064.169824.8861841012072586247073890.48863.8411891151319854174779302.936318.4350571251220547161134733.178719.728712135222179190470030.27422.2059241418215609295742560.61594.7436421519353300176001831.09967.920355168156382248110350.32872.6401271714644277236675930.61874.7630811828539918220676881.29339.118542196764029275313610.24571.971845206605618213680350.30912.4857972121021202268879480.78185.8705332216358589207695790.78765.909105237193799325660380.22091.763389245533710209880910.26372.120312525105438201513981.24588.8276862648177466205176522.348115.2269552713881880221761750.6264.813686287040884319327160.22051.7599862918220062227789970.79995.9907413015222162229754040.66255.065139314861388195460910.24871.996745328000173279095580.28662.3061583315559180201746990.77125.799906345466543226216670.24171.938543357460661211022690.35352.8327933613380333269301250.49693.901256表5由此可见,本方法可直接定量测定幽门螺旋杆菌抗体浓度,操作简单快速,15min即可获得结果,且成本低廉,灵敏度高,特异性强。以上所述实施方式仅仅是对本发明的优选实施方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案作出的各种变形和改进,均应落入本发明的权利要求书确定的保护范围内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1