一种治疗多发性硬化症的药物组合物的制作方法
本发明涉及一种治疗多发性硬化综合症的鼻腔粘膜给药组合物。
背景技术:
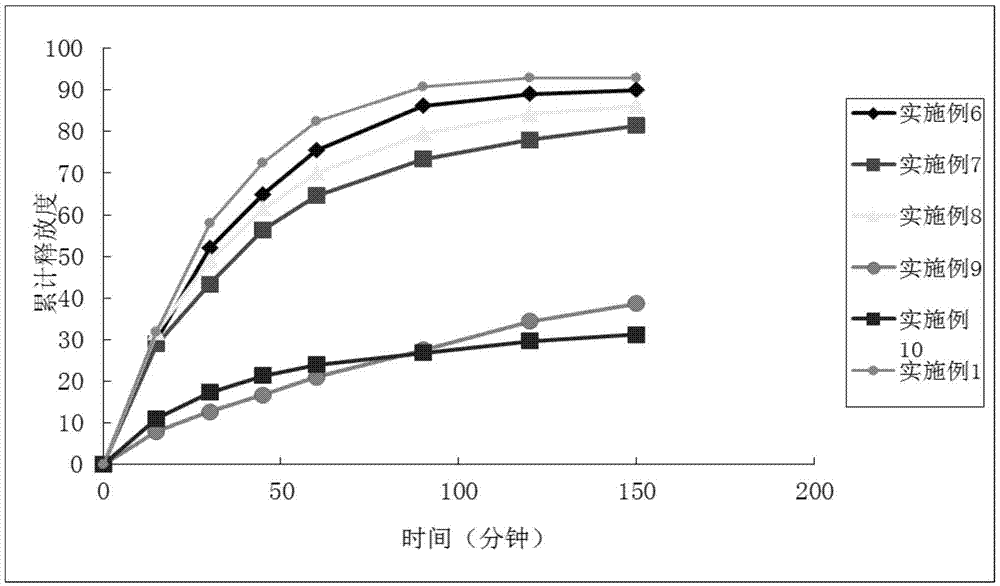
:多发性硬化综合症(multiplesclerosis,ms)在临床上是能够发生在人体的中枢神经系统中的一种的自身型的免疫性疾病,该类疾病的发生主要以人体生理自身反应性的免疫t细胞引起的,导致大脑及脊髓炎症及神经脱髓鞘变化为特征,其发病率不仅在欧美等国家属于高发性疾病,而且在我们果青壮年人群(尤其是三十岁人群中)中也是比较常见的一种疾病,该类疾病发病的原因一般与人体自身的免疫调节紊乱相关。目前公认ms临床分型:1.复发缓解型ms(rrms)ms的最常见病程类型,80%ms患者发病初期为本类型,表现为明显的复发和缓解过程,每次发作均基本恢复,不留或仅留下轻微后遗症。随着病程的进展多数在5~15年内最终转变为spms。2.继发进展型ms(spms)rrms后的一个病程类型,表现为在复发缓解阶段以后,疾病随着复发不能完全缓解并留下部分后遗症,疾病逐渐缓慢加重的过程。rrms患者中约50%在10年内/80%在20年内转变为本型。3.原发进展型ms(ppms)ms的少见病程类型,10%~15%ms患者最初即表现为本类型,临床没有缓解复发过程,疾病呈缓慢进行性加重,并且病程大于一年。4.进展复发型ms(prms)ms的少见病程类型,约5%~10%ms患者表现为本类型,疾病始终呈缓慢进行性加重,病程中有少数缓解复发过程。醋酸格拉替雷,市售商品名为是一种合成的多肽类化合物,由四种氨基酸组成:l-谷氨酸,l-丙氨酸,l-赖氨酸,l-络氨酸,用于治疗多发性硬化症。的疗效与耐受性皆获得十足的肯定,许多研究与临床经验证实其能大幅度地减低患者的复发率,改善失能的病况,减少脑部损伤之外。另外,相关研究亦显示较之干扰素更能显著地降低复发率,防止神经进一步的损伤与恶化,而且也具有更好的耐受性。在其它长期使用的疗效研究里(6年至最长12年不等),亦证实能持续地延缓患者其神经学上病程的恶化或者让患者维持稳定的病况,减少脑内损伤并防止神经元大量遭受破坏终至丧失功能的恶化情形。醋酸格拉替雷临床上以注射溶液使用,在所有的临床试验和用户使用反馈中,注射部位萎缩据观察为最常见的不良反应且大多数接受的患者均有此反应,另外其他最常见的副作用为注射部位的刺激反应,包括:红斑、疼痛、肿胀、搔痒、水肿、发炎与过敏反应。<美国专利6,214,791>公开的通过摄入或吸入来服用醋酸格拉替雷,缺点是无法避免胃肠液对药物的降解作用及肝脏的首过效应、酶代谢及酶降解。<美国专利申请公开第2001/0055568a1号>中的口服缺点同<美国专利6,214,791>,吸入方式虽可以避免高首过效应,但长时间吸入给药需要定期检查肺部生理情况。且醋酸格拉替雷属于长期服用药物,若连续给药易对肺部造成一定程度的损伤,药物剂量也不好控制,用法麻烦。<cn201380067117>公开一种口腔透黏膜给药的方式,但口腔内不自主的唾液分泌以及吞咽影响口腔黏膜途径的效能;药物的味觉刺激影响该途径的依从性。为了克服现有注射给药可能导致患者各种不良反应、依从性差或治疗暂停等负担,开发备选醋酸格拉默给药方案,使用所述的方案使醋酸格拉替雷能有效治疗一种形式的多发性硬化症症状。鼻腔给药系统指经由鼻腔给药,发挥局部或全身治疗或预防作用的一类制剂,尤其适用于除注射外其他途径给药困难而又需发挥全身作用的药物,如口服难以吸收的极性药物、在胃肠道中不稳定的药物、肝脏首过作用强的药物和蛋白及多肽类药物等。技术实现要素:醋酸格拉替雷的平均分子量在5000道尔顿~9000道尔顿之间,不宜透过鼻腔黏膜被吸收,实验者在实验过程中发现有些吸收促进剂有助于醋酸格拉替雷的吸收,但对鼻黏膜有一定的毒性作用,促进纤毛的清除作用,降低药物的生物利用度,发明人通过实验意外发现特定含量的特定生物粘附材料可以避免鼻腔中黏膜纤毛的清除作用,增加药物在黏膜上的停留时间,从而提高药物的生物利用度,同时能够减少对纤毛运动的毒性。为了克服上述技术缺陷,本发明一个方面提供了一种醋酸格拉替雷鼻用凝胶组合物,其由醋酸格拉替雷、凝胶基质和药学上可接受的其他辅料制成,所述可接受的其他辅料包括生物粘附材料1.15%~1.75%(1.15%、1.20%、1.25%、1.30%、1.35%、1.40%、1.45%、1.50%、1.55%、1.60%、1.65%、1.70%、1.75%),所述生物黏附材料选自淀粉、甲壳素、葡聚糖、黄原胶其中一种或多种的组合。进一步地,所述可接受的其他辅料包括吸收促进剂、生物粘附材料、渗透压调节剂、保湿剂、防腐剂、ph调节剂,其组分的占凝胶组合物的重量百分比为吸收促进剂2%~5%、渗透压调节剂4.5%~9.0%、保湿剂1%~5%、防腐剂0.1%~0.25、ph调节剂0.25%~0.35。进一步地,吸收促进剂选自十二烷基硫酸钠、去氧胆酸钠、胆酸钠、甘胆酸钠、牛磺胆酸钠、乙二胺四乙酸二钠、2-羟丙基-β-环糊精、卵磷脂其中一种或多种;渗透压调节剂选自氯化钠、甘露醇、葡萄糖、蔗糖其中一种或多种;保湿剂选自丙二醇、甘油、山梨醇、甘露醇其中一种或多种;防腐剂选自苯扎氯胺、苯甲醇、苯乙醇、edta其中一种或多种;ph调节剂选自醋酸、氢氧化钠其中一种或多种。进一步地,凝胶基质占凝胶组合物的重量百分比为5.25%~6.25%,选自聚乙烯醇、羟丙甲纤维素、卡波姆、甲基纤维素中的一种或多种。进一步地,醋酸格拉替雷1%占凝胶组合物的重量百分比为1%。本发明一个具体实施方案中,醋酸格拉替雷鼻用凝胶组合物包括醋酸格拉替雷1%,2-羟丙基-β-环糊精1%-5%,葡聚糖1.15%-1.75%,卡波姆5.25%-6.25%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂;优选包括醋酸格拉替雷1%,2-羟丙基-β-环糊精5%,葡聚糖1.15%,卡波姆6.25%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂。本发明一个具体实施方案中,醋酸格拉替雷鼻用凝胶组合物包括醋酸格拉替雷1%,卵磷脂1%-5%,甲壳素0.9%-1.75%,聚乙烯醇5.25%-6.25%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂;优选包括醋酸格拉替雷1%,卵磷脂1%,甲壳素1.75%,聚乙烯醇5.25%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂。本发明一个具体实施方案中,醋酸格拉替雷鼻用凝胶组合物包括醋酸格拉替雷1%,甘胆酸钠1%-5%,淀粉0.9%-1.75%,羟丙甲纤维素5.25%-6.25%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂;优选包括醋酸格拉替雷1%,甘胆酸3.75%,淀粉1.5%,羟丙甲纤维素5.5%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂。本发明一个具体实施方案中,醋酸格拉替雷鼻用凝胶组合物包括醋酸格拉替雷1%,甘胆酸钠1%-5%,黄原胶0.9%-1.75%,甲基纤维素5.25%-6.25%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂;优选包括醋酸格拉替雷1%,甘胆酸3.75%,黄原胶0.9%,甲基纤维素6%以及渗透压调节剂、保湿剂、防腐剂和ph调节剂。进一步地,所述凝胶组合物的制备方法为:将卡波姆加入水中,充分溶胀,用碱性的ph调节剂调节ph值得凝胶,然后将醋酸格拉替雷溶于水,加入其他组分混合,搅匀,得醋酸格拉替雷溶液,将此溶液加入到卡波姆溶胀物中,得醋酸格拉替雷鼻用凝胶剂;或将甲基纤维素或羟丙甲纤维素加入水中,充分溶胀,然后加入醋酸格拉替雷以及其他辅料混合,搅匀,得醋酸格拉替雷鼻用凝胶剂;或将聚乙烯醇加入水中,充分溶胀,用酸性ph调节剂调节ph值得凝胶,然后将醋酸格拉替雷溶于水,加入其他辅料混合,搅匀,得醋酸格拉替雷溶液,将此溶液加入到聚乙烯醇溶胀物中,得醋酸格拉替雷鼻用凝胶剂。本发明的另一方面涉及如前所述的醋酸格拉替雷鼻用凝胶组合物的制备方法,其包括如下步骤:将卡波姆加入水中,充分溶胀,用碱性的ph(7.0-8.0)调节剂调节ph值得凝胶,然后将醋酸格拉替雷溶于水,加入其他组分混合,搅匀,得醋酸格拉替雷溶液,将此溶液加入到卡波姆溶胀物中,得醋酸格拉替雷鼻用凝胶剂;或将甲基纤维素或羟丙甲纤维素加入水中,充分溶胀,然后加入醋酸格拉替雷以及其他辅料混合,搅匀,得醋酸格拉替雷鼻用凝胶剂;或将聚乙烯醇加入水中,充分溶胀,用酸性ph(5.0-6.0)调节剂调节ph值得凝胶,然后将醋酸格拉替雷溶于水,加入其他辅料混合,搅匀,得醋酸格拉替雷溶液,将此溶液加入到聚乙烯醇溶胀物中,得醋酸格拉替雷鼻用凝胶剂。本发明的再一个方面提供了醋酸格拉替雷鼻用凝胶组合物在制备治疗多发性硬化综合症的药物中的用途。本发明提供是一种治疗多发性硬化综合征的药物组合物,该组合物由醋酸格拉替雷、凝胶基质和药学上可接受的其他辅料吸收促进剂、生物粘附材料、渗透压调节剂、保湿剂、防腐剂、ph调节剂组成,其重量百分比为醋酸格拉替雷1%、凝胶基质5.25%~6.25%、吸收促进剂2%~5%、生物粘附材料1.15%~1.75%、渗透压调节剂4.5%~9.0%、保湿剂1%~5%、防腐剂0.1%~0.25、ph调节剂0.25%~0.35,其余为溶剂水。有益效果1、生物利用度高。与口服给药相比,鼻腔给药可避免药物在胃肠液中降解和肝脏首过效应,生物利用度高。小分子药物生物利用度接近静脉注射,大分子多肽类药物高于口服。2、速效,鼻黏膜面积大,黏膜下血管非常丰富,动脉、静脉和毛细血管交织成网状,药液可迅速吸收,从血管进人体循环。通过鼻腔给药可增加药物在脑组织中的分布,可用于治疗中枢神经系统疾病。3、胃肠道中容易破坏的药物,极性大而胃肠道难于吸收的药物,鼻黏膜都能很好的吸收,分子量大的多肽类、蛋白类药物,也能在吸收促进剂的存在下较好地吸收。4、使用方便,患者依从性好。与注射给药相比,鼻腔给药使用方便,易于被患者接受,便于自己用药。5、本发明的方法提高了大分子量的醋酸格拉替雷的皮肤粘膜透过率,能够增加醋酸格拉替雷的生物利用度,并降低清除作用。附图说明附图1为实施例13部分结果的释放结果曲线图。附图2为实施例13部分结果的释放结果曲线图。具体实施方式实施例1:醋酸格拉替雷鼻用凝胶剂组成:每200克的凝胶制剂的制备步骤为:(1)取处方量的凝胶基质卡波姆,加3~5重量倍的水,搅拌使其充分溶胀,滴加氢氧化钠调节ph值至7.0~8.0,搅拌得凝胶;(2)另取处方量醋酸格拉替雷加2~5重量倍的水溶解;(3)将葡聚糖、葡萄糖、甘油、edta加2~3重量倍水搅拌,使其溶解;(4)将步骤(2)和步骤(3)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂2-羟丙基-β-环糊精,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶。实施例2每200克的凝胶制剂的制备步骤为:(1)取处方量的凝胶基质聚乙烯醇,加4~7重量倍的水,滴加醋酸调节ph值至5.0~6.0,搅拌使其充分溶胀;(2)另取处方量醋酸格拉替雷加2~5重量倍的水溶解;(3)将甘露醇、苯扎氯胺、丙二醇、甲壳素加1~2重量倍水搅拌,使其溶解;(4)将步骤(2)和步骤(3)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂卵磷脂,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶。实施例3:醋酸格拉替雷鼻用凝胶剂组成:每200克的凝胶制剂的制备步骤为:(1)称取处方量的羟丙甲纤维素,加入4~7重量倍的水,边加边搅拌,使其充分溶胀;(2)另取处方量醋酸格拉替雷加2~5重量倍的水溶解;(3)将氯化钠、edta、甘油、淀粉加3~4重量倍水搅拌,使其溶解;(4)将步骤(2)和步骤(3)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂甘胆酸钠,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶。实施例4:每200克的凝胶制剂的制备步骤为:(1)称取处方量的甲基纤维素,加入4~7重量倍的水,边加边搅拌,使其充分溶胀;(2)另取处方量醋酸格拉替雷加2~5重量倍的水溶解;(3)将氯化钠、edta、甘油、黄原胶加3~4重量倍水搅拌,使其溶解;(4)将步骤(2)和步骤(3)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂甘胆酸钠,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶。实施例5每200克的凝胶制剂的制备步骤为:(1)称取处方量的甲基纤维素,加入4~7重量倍的水,边加边搅拌,使其充分溶胀;(2)另取处方量醋酸格拉替雷加2~5重量倍的水溶解;(3)将氯化钠、edta、甘油、聚维酮加3~4重量倍水搅拌,使其溶解;(4)将步骤(2)和步骤(3)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂2-羟丙基-β-环糊精,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶实施例6制备步骤同实施例1。实施例7制备步骤同实施例1。实施例8制备步骤同实施例1。实施例9制备步骤同实施例1。实施例10制备步骤同实施例1。实施例11空白凝胶基质对照组每200克的凝胶制剂的制备步骤为:(1)取处方量的凝胶基质卡波姆,加3~5重量倍的水,搅拌使其充分溶胀,滴加氢氧化钠调节ph值至7.0~8.0,搅拌得凝胶;(2)将葡聚糖、葡萄糖、甘油、edta加2~3重量倍水搅拌,使其溶解;(3)将步骤(2)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂2-羟丙基-β-环糊精,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶。实施例12无生物粘附材料对照组每200克的凝胶制剂的制备步骤为:(1)取处方量的凝胶基质卡波姆,加3~5重量倍的水,搅拌使其充分溶胀,滴加氢氧化钠调节ph值至7.0~8.0,搅拌得凝胶;(2)另取处方量醋酸格拉替雷加2~5重量倍的水溶解;(3)将葡萄糖、甘油、edta加2~3重量倍水搅拌,使其溶解;(4)将步骤(2)和步骤(3)的溶液加入到步骤(1)的凝胶基质溶液中,再加入促吸收剂2-羟丙基-β-环糊精,搅拌均匀,然后加水至200g,搅拌均匀,即制得成品凝胶。实施例13药物的鼻腔吸收模型:采用改良的franz扩散池测定醋酸格拉替雷凝胶的体外释放度,将半透膜(截留相对分子质量6500~9000)固定在扩散池两池问,扩散池两池内径为1.3cm,释药面积约为1.33cm2,向给药池中准确加入2ml醋酸格拉替雷凝胶,将扩散池放入16ml的37℃人工鼻液中,向接收池中加入已预热至37℃的人工鼻液10ml作为接收液,接收池中置一搅拌子以100r/min的转速转动,于15,30,45,60,90,120,180min分别取样,将介质全部取出并迅速补加等量预热的人工鼻液,样品液经适当稀释,0.45μm微孔滤膜过滤,并续滤液按色谱条件,测定醋酸格拉替雷的峰面积,计算累积释放度。色谱方法:照高效液相色谱法,采用kromasilnh2色谱柱,4.6×250mm,5μm,流动相为0.08mol/l磷酸盐缓冲液(磷酸调ph至4.0±0.1)-乙腈(35:65)为流动相,进行等度洗脱,检测波长275nm,柱温为30℃,流速1.0ml/min。醋酸格拉替雷拖尾因子应小于3.0。结果见下表(单位:%):从表中数据以及附图1的结果可知,一些生物粘附材料能极大的提高醋酸格拉替雷的释放,初始释放时间加快,释放速度稳定,释放量相比于不添加生物黏附材料的样品提高2倍,显著提高药物的生物利用度,而并非所有生物黏附材料均能达到良好的效果。这可能是由于不同的生物黏附材料与醋酸格拉替雷之间存在相互作用导致其效果也有很大差异。当选择聚维酮作为生物粘附材料时,其组合物的释放度在规定时间内无法达到治疗效果的要求。从表中数据以及附图2的结果可知,能够看出释放量与生物黏附材料的种类密切相关,非本发明的生物黏附材料效果较差,仅与不添加生物黏附材料的结果类似。实施例14药物对鼻腔上颚黏膜纤毛运动影响模型试验:选取中华大蟾蜍30只,随机分成6组,每组5只,即醋酸格拉替雷凝胶给药组;空白对照组,即0.9%氯化钠注射液;将蟾蜍仰卧固定,使口腔张开,分离并洗净上颚黏膜,于上颚黏膜处滴加试验样品溶液0.3ml,使浸没上颚黏膜,持续接触4h后用生理盐水洗净,将黏膜面向上平铺于载玻片上,滴加生理盐水,盖上盖玻片,于44×10倍光学显微镜下观察纤毛的运动情况,随后搁置于加有少量蒸馏水的层析缸中,密闭,使水蒸气近饱和状态,环境温度为20~25℃、以后每隔一段时间取出标本观察,记录从洗净试验样品至纤毛运动停止的时间,用生理盐水洗净黏膜上药液,继续观察纤毛运动是否恢复,记录恢复后持续运动的时间。以上实验中,取自蟾蜍上腭的黏膜先分成两小块,其中一块滴加受试液,另一块滴加生理盐水作为对照,用试验样品的纤毛持续运动时间除以对照组的时间得纤毛持续运动相对百分率,百分率越高,表示试验样品对纤毛的毒性影响越小。恢复后持续运动时间可以表明样品对纤毛毒性是否可逆。从表中数据可知,实施例1、2对纤毛的毒性影响最小,实施例3、4对纤毛有一定的毒性影响,实施例5对纤毛毒性影响较大,且通过恢复后运动时间可以产出,实施例5样品恢复后的持续运动时间急剧下降至1min以内,这证明实施例5样品中采用了聚维酮作为生物粘附材料对纤毛运动损伤大,其毒性作用不可逆,其余四个实施例的毒性作用均可逆。实施例15局部刺激性试验:取sd大鼠50只,随机分层5组,每组10只。设置醋酸格拉替雷凝胶给药组、空白对照组(给予生理盐水)、赋形剂组(空白凝胶基质)。每天给药1次,连续7天,在最后一次给药后24h处死大鼠,取出局部鼻腔黏膜,观察有无充血、红肿等现象,结果见下表:全身状况局部刺激症状局部黏膜组织状况空白对照组未见明显状况未见哮喘、咳嗽、呕吐、窒息无充血、红肿、溃破实施例11未见明显状况未见哮喘、咳嗽、呕吐、窒息无充血、红肿、溃破实施例1未见明显状况未见哮喘、咳嗽、呕吐、窒息无充血、红肿、溃破实施例2未见明显状况未见哮喘、咳嗽、呕吐、窒息无充血、红肿、溃破实施例3未见明显状况未见哮喘、咳嗽、呕吐、窒息无充血、红肿、溃破实施例4未见明显状况未见哮喘、咳嗽、呕吐、窒息无充血、红肿、溃破从表中数据可知,常规用药剂量下,实施例1~4鼻腔凝胶剂不会对用药者的局部组织产生明显的刺激作用。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1