辅酶Q10与二十八烷醇环糊精多元超分子包合物及其制备方法与流程
本发明涉及一种辅酶q10与二十八烷醇环糊精多元超分子包合物及制备方法,该包合物对高血脂等心血管疾病、高山缺氧、糖尿病、免疫力低下等疾病具有较好治疗和保健作用,它属于药品、保健品
技术领域:
。
背景技术:
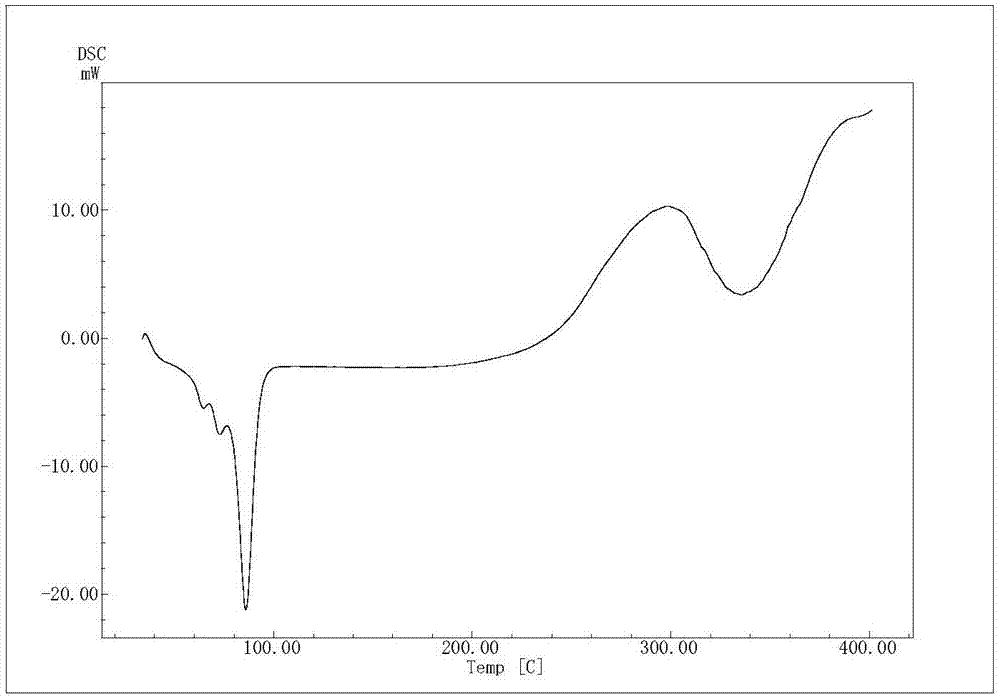
:辅酶q10(coenzymeq10)是一种由人体自行合成的化合物,因其母核六位上的侧链‐聚异戊二烯基的聚合度为10而得名,结构与维生素k类似。辅酶q10分为还原型辅酶q10(coq10h2,ubiquinol,泛醇)与氧化型辅酶q10(coq10,ubiquinone,泛醌)两种形态,coq10h2是coq10的二电子还原体。在体内,coq10h2与coq10作为一类递氢/递电子体共同参与线粒体内膜呼吸链等跨膜电子运输体系和细胞氧化磷酸化过程,在三磷酸腺苷(atp)的合成中起着重要作用,辅酶q10也是体内最强的抗氧化剂,具有清除细胞内自由基的作用。辅酶q10是人体中不可缺少的重要生理物质,其化学结构特点决定了它在人体中具有许多重要生理功能,它是生命活动中重要的能量传递物质,是线粒体呼吸链限速反应的关键性物质,在细胞能量生成、增强生物活力方面发挥重要作用。人体中含辅酶q10总量为500‐1500mg,20岁左右达到高峰,然后迅速减少,70岁以后比20岁年轻人减少57%。研究发现,在很多患病病人中,辅酶q10生理水平下降明显,如心衰病人(hf)中,病人心肌及血液中辅酶q10含量明显降低,从外源补充辅酶q10后,明显改善病人症状。研究发现,很多免疫力低下的病人,其辅酶q10生理水平较低,补充辅酶q10后,症状得到改善。因此,人体从外源补充辅酶q10,治疗各种辅酶q10生理水平低下成为一种公认的临床治疗方法。二十八烷醇俗名蒙旦醇,也称为普利醇,是一种直链高碳脂肪醇,是一种广泛存在于自然界的生物活性物质,由于其特殊的生理功效受到广泛的关注与研究。作为高级脂肪醇,二十八烷醇在自然界普遍存在于蔗蜡、糠蜡、蜂蜡及虫白蜡等天然物质中,在蔗蜡、米糠蜡和蜂蜡中含量较高,如蜂蜡中二十八烷醇在总脂肪醇中的含量为2.71%~15.78%,具有很高的利用价值。纯净的二十八烷醇外观为白色粉末或鳞片状晶体,溶点81~83℃,不溶于水,可溶于乙醇等有机溶剂中。二十八烷醇在酸、碱和较高温度条件下都具有较好的稳定性,不易吸潮,易于保存。从甘蔗、米糠、蜂蜡等植物中提取得到二十八烷醇产品往往是包括c22~c36一组高级脂肪醇混合物,其含量从10%‐99%。动物实验表明,二十八烷醇的白鼠急性经口ld50为18000mg/kg,其安全性高于食盐。因此,天然提取的二十八烷醇可以作为一种安全、绿色的添加剂。美国伊利诺斯大学cureton博士等研究人员证明其具有一系列独特的生理功能,包括提高机体耐久力、降低机体的应激反应、降低体内血脂和胆固醇、抗氧化以及其他生理功能。二十八烷醇还具有增强心脏功能、降低胆固醇,抗机体动脉粥样硬化、抑制胃溃疡、抗血小板聚集、保护肝脏等作用。随着对二十八烷醇的不断深入研究,开发二十八烷醇的相关产品逐渐成为国内外科研及应用的一个热点。辅酶q10与二十八烷醇均是脂溶性物质,难溶于水,均属于药剂学ⅱ类物质,口服给药吸收受限于溶解和释放,其绝对生物利用度均较低,提高溶解度和释放度将有利于提高生物利用度,另外辅酶q10对光、热、水不稳定。针对这种情况,近年来已经开发出多种提高口服给药生物利用度的方法,如包合技术、自乳化技术、脂质体等。包合技术是解决辅酶q10和二十八烷醇溶解度的其中一个较好方法,辅酶q10和二十八烷醇由于生物利用度的问题限制了应用,制备成超分子包合物以后,其生物利用度提高,作用更强,目前已有专利和文献报道辅酶q10和二十八烷醇单独环糊精包合物,其包合物虽然较其原料药提高了溶解度和释放,但仍然较低,溶解度普遍在20‐50ug/ml范围,在水中也很难分散,这也是目前一些环糊精包合物难以解决的缺点之一。另外一个问题是,如果同时使用辅酶q10环糊精包合物和二十八烷醇环糊精包合物制备制剂时,或临床同时服用两者的单独的包合物时,两者有可能在适宜的条件下发生分子重新识别和包合替换,即重新包合现象,致使部分化合物游离出来,导致产品不稳定和吸收下降。另一个方面两者分别制备包合物时,如要达到最佳包合效果,则需要更多的环糊精,尤其在两者同时复配使用时,复配药物载药量较低。目前未检索到对两者复配化合物进行包合的专利及文献研究报道。目前已公开发表的文献,经检索与本专利关联的有如下专利和文献:①在文献journalactapoloniaepharmaceutica(1995),vol.52,no.5,pp.379‐386和1996,vol.53,no.3,pp.193‐196.中描述了采用搅拌方法制备了辅酶q10的γ‐环糊精包合物。②美国专利6861447,该专利公开了制备γ‐环糊精包合物的方法。③世界专利wo2005/111224公开了一种新的辅酶q10的β‐环糊精包合物制备方法,采用搅拌法制备,生产时间需要20小时左右的时间才能完成。④中国专利cn200510048010.3公开了一种水溶性辅酶q10组合物的制备技术,是有关于γ‐环糊精与甘露醇固体分散体的技术。⑤中国专利cn200710079078.7公开了高级脂肪醇的包合物及其制备方法。⑥中国专利zl200610046307.0公开了一种水溶性辅酶q10羟丙基‐β‐环糊精包合物及制备方法,以上专利文献均是涉及到辅酶q10与二十八烷醇单独环糊精包合物,未涉及本发明技术。技术实现要素:本发明就是为了解决上述技术问题,而提供的一种辅酶q10与二十八烷醇环糊精多元超分子包合物及制备方法,本发明包合物可以在水中分散,它具有较大的溶解度、释放度和较好稳定性的特点,可以持续释放药物成分,本发明可以使包合物更容易在水中以纳米级在水中分散,扩大了溶解和吸收表面积,其生理活性超过了单独二元包合物。为了解决上述技术问题,本发明是通过下述技术方案实现的:辅酶q10与二十八烷醇环糊精多元超分子包合物,它主要是由下述原料按所述重量份数制备而成:辅酶q101份,二十八烷醇0.1‐1份,环糊精3‐15份。上述的辅酶q10与二十八烷醇复配的环糊精多元超分子包合物,它主要是由下述原料按所述重量份数制备而成:辅酶q101份,二十八烷醇0.1‐0.5份,环糊精5‐10份。上述的辅酶q10与二十八烷醇复配的环糊精多元超分子包合物,它是由下述原料按所述重量份数制备而成:辅酶q101份,二十八烷醇0.1‐0.5份,环糊精5‐10份,卵磷脂0.1‐0.3份。上述的辅酶q10是氧化型辅酶q10或还原型辅酶q10。上述的二十八烷醇是二十八烷醇单体成分或含二十八烷醇不少于50%的c22~c36高级脂肪烷醇混合物。上述的环糊精是γ‐环糊精、β‐环糊精或羟丙基‐β‐环糊精。上述的磷脂是大豆磷脂或蛋黄卵磷脂。辅酶q10与二十八烷醇复配的环糊精多元超分子包合物的制备方法,其工艺步骤如下:按所述重量份数取环糊精,与相当于环糊精3‐5倍重量份数的水混合,加热至60℃‐90℃,加入符合上述重量份数的辅酶q10和二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨15‐20次,放出研磨液,加水至固形物含量达到11‐13%,喷雾干燥得到辅酶q10与二十八烷醇复配的环糊精多元超分子包合物。辅酶q10与二十八烷醇复配的环糊精多元超分子包合物的制备方法,其工艺步骤如下:按所述重量份数取环糊精,与相当于环糊精3‐5倍重量的水混合,加热至60℃‐90℃,加入符合上述重量份数的辅酶q10和二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨15‐20次,放出研磨液,加水至固形物含量达到11‐13%,加入所述0.1‐0.3份重量的卵磷脂以15000转/分剪切均质0.5‐2分钟,喷雾干燥得到含有磷脂的辅酶q10与二十八烷醇复配的环糊精多元超分子包合物。上述的喷雾干燥可以使用冷冻干燥替代。本发明也可以加入胆固醇作为制备含有磷脂的包合物附加剂,增强形成的包合物脂质体磷脂膜效果。由于采用上述技术方案,使得本发明具有如下特点和效果:本发明与以往技术不同的是采用辅酶q10和二十八烷醇复配合用为一个制剂方案,目的是将起到很好的协同作用,辅酶q10和二十八烷醇都有良好的增强心脏功能和降血脂的作用,辅酶q10基于抗氧化应激、清除自由基和为心肌细胞提供能量机理治疗和改善心血管疾病,二十八烷醇具有保护心肌细胞线粒体完整性和调节心肌能量代谢作用,也具有抗氧化应激作用,二十八烷醇主要是通过调节胆固醇生物合成中的关键酶—羟甲基戊二酰辅酶a(hmg-coa)的活性来抑制胆固醇的合成,从而降低人体总胆固醇,由于该酶也是体内辅酶q10的合成酶,因此有可能对辅酶q10的生物合成构成影响,两者合用将消除这种影响,同时具有更强的协同生理活性作用,具有更强的抗氧化应激作用,效果更好。现有技术中辅酶q10与二十八烷醇存在低溶解度和生物利用度问题,一个可能的解决方案是,如能形成辅酶q10和二十八烷醇复配的环糊精多元包合物,将是解决这个问题的途径之一。辅酶q10和二十八烷醇两者化学结构有一定差异,但都具有较长碳链结构和较强脂溶性特点,按照其分子尺寸空间计算,环糊精空腔大小按理论计算有可能同时包容这两种分子部分长链,形成多元包合物,对于这种辅酶q10和二十八烷醇复配复合物的包合过程将完全不同于这两种化合物单独包合,包合形成的辅酶q10与二十八烷醇复配的环糊精包合物将是一种新的多元包合物物质。由于所形成的三元包合物其溶解度仍然较低且很难分散于水中,加入磷脂类化合物可以提高其分散性,磷脂分子具有双亲性以及脂肪酸长链特点,疏水的长链端具有插入已经形成辅酶q10和二十八烷醇复配三元包合物环糊精空腔形成部分包合的条件,可以与本发明包合物组装形成包合物脂质体,因此本发明在形成三元包合物基础上加入卵磷脂,成功形成了辅酶q10和二十八烷醇复配的环糊精磷脂多元包合物脂质体,该包合物具有磷脂包裹的前体纳米脂质体特点,可以以纳米级微粒分散于水中,进一步增大微粒表面积,将有利于目标客分子的吸收。本发明制得的辅酶q10与二十八烷醇复配的环糊精多元超分子包合物不是简单的物理混合物,它是一种由三种或四种成分组成的多元超分子包合物或包合物脂质体,具有不同于辅酶q10与二十八烷醇、环糊精或磷脂物理混合物的特征,也不同于辅酶q10环糊精包合物与二十八烷醇环糊精包合物以及它们的物理混合物,是一种新的包合物物质。它具有较大的溶解度、释放度和较好稳定性的特点,可以持续释放辅酶q10与二十八烷醇成分,本发明可以使包合物更容易在水中分散,扩大了溶解和吸收表面积,其生理活性超过了单独二元包合物。这主要通过如下方法来证明,将本发明的包合物、辅酶q10与二十八烷醇、环糊精以及它们的物理混合物、辅酶q10与环糊精包合物、二十八烷醇与环糊精包合物以及它们的物理混合物做热分析(dsc)和高效液相色谱和气相色谱以及红外光谱,结果表明,本发明的包合物物相dsc图谱不同于其他几种物质物相图谱,新的多元包合物dsc图谱中辅酶q10与二十八烷醇的熔点峰消失,证明本发明辅酶q10与二十八烷醇包合物形成了一种新的包合物物相,高效液相图谱证明经乙醚洗过的包合物中显示辅酶q10吸收峰,气相色谱图中证明显示二十八烷醇峰。红外光谱比较分析,采用红外光谱仪分别测定了辅酶q10、二十八烷醇与环糊精原料及三者物理混合物和包合物溴化钾压片在室温下的红外光谱,其中物理混合物图谱具有明显的辅酶q10和二十八烷醇及β‐环糊精的特征峰,而包合物图谱中辅酶q10和二十八烷醇特征峰消失或发生位移,证明已形成新的包合物。本发明加入卵磷脂形成的多元包合物脂质体的红外图谱也不同于四种成分特征图谱。本发明加入卵磷脂形成的多元包合物脂质体的dsc图谱也显著不同于辅酶q10与二十八烷醇及环糊精还有磷脂混合物图谱,经测定其溶解度和释放度显著高于不含有磷脂的多元包合物,将其分散在水溶液,可形成其粒径为200‐400nm的纳米磷脂脂质体溶液。经热分析dsc与高效液相色谱、气相色谱测定,其最佳包结重量比为辅酶q10:二十八烷醇:γ‐环糊精=1:0.2:5;辅酶q10:二十八烷醇:β‐环糊精=1:0.3:6;辅酶q10:二十八烷醇:羟丙基‐β‐环糊精=1:0.3:7。加入磷脂后形成包合物最佳包结重量比为,辅酶q10:二十八烷醇:γ‐环糊精:卵磷脂=1:0.2:5:0.2;辅酶q10:二十八烷醇:β‐环糊精:卵磷脂=1:0.3:6:0.2;辅酶q10:二十八烷醇:羟丙基‐β‐环糊精:卵磷脂=1:0.3:7:0.2。本发明研究了包合过程,经热分析dsc与高效液相色谱测定,包结重量比辅酶q10:γ‐环糊精=1:5;辅酶q10:β‐环糊精=1:6;辅酶q10:羟丙基‐β‐环糊精=1:7;二十八烷醇与环糊精包合物包结重量比,二十八烷醇:γ‐环糊精=1:18;二十八烷醇:β‐环糊精=1:17;二十八烷醇:羟丙基‐β‐环糊精=1:17。由于新形成的多元(三元)包合物辅酶q10与二十八烷醇、环糊精的最佳包结比所需的环糊精总量远远小于两个成分单独形成包合物的总量,推断辅酶q10与二十八烷醇与环糊精形成了单一的三元包合物,即环糊精分子空腔同时装入两个链状分子部分区段。本发明形成的多元(三元)包合物在同样环糊精用量情况下,包合辅酶q10与二十八烷醇的包封率和载药量显著超过两种成分单独包合物。证明其包合物化学结构主要是一个辅酶q10与一个二十八烷醇分子通过整体或部分装入超过多个以上环糊精分子的空腔,形成辅酶q10与二十八烷醇的环糊精多元复合超分子包合物。本发明超分子包合物同辅酶q10与二十八烷醇原型药以及它们的单独环糊精包合物相比,提高了两种成分的溶解度和释放度,其稳定性优于辅酶q10与二十八烷醇单体分子,也优于两者的包合物混合物稳定性。其中加入卵磷脂形成的多元包合物脂质体溶解度、释放度又显著高于其未加卵磷脂的三元包合物,它具有环糊精包合物和脂质体双重优点。清除dpph自由基抗氧化性试验表明,本发明的辅酶q10与二十八烷醇复配的β‐环糊精多元包合物清除自由基能力显著超过其辅酶q10与二十八烷醇单独二元包合物以及两种原料的混合物,而加入卵磷脂的β‐环糊精多元包合物脂质体具有更优的抗氧化性效果。红外光谱比较分析:采用红外光谱仪分别测定了辅酶q10、二十八烷醇与环糊精原料及卵磷脂及它们的物理混合物和包合物溴化钾压片在室温下的红外光谱,扫描范围为400~4000cm‐1。测定结果如图17、图18、图19、图20、图21、图22、图23所示。热分析(dsc)测定:取辅酶q10、二十八烷醇、环糊精、卵磷脂及它们的混合物、本发明辅酶q10与二十八烷醇复配的β‐环糊精多元包合物、辅酶q10与二十八烷醇复配的γ‐环糊精多元包合物、和辅酶q10与二十八烷醇复配的羟丙基‐β‐环糊精的多元包合物、辅酶q10与二十八烷醇复配的β‐环糊精磷脂多元包合物、辅酶q10与二十八烷醇复配的γ‐环糊精磷脂多元包合物、辅酶q10与二十八烷醇复配的羟丙基‐β‐环糊精磷脂的多元包合物各5mg(包合物经过乙醚洗后,干燥,再取样),压片、进行热分析(dsc)测定,结果见图1、图2、图3、图4、图5、图6、图7、图8、图9、图10、图11、图12、图13、图14、图15、图16,结果表明包合物不同于物理混合物dsc图谱,证明形成了新的物相。附图说明图1是q10原料dsc谱图。图2是二十八烷醇dsc谱图。图3是β‐环糊精dsc谱图。图4是γ‐环糊精dsc谱图。图5是羟丙基‐β‐环糊精dsc谱图。图6是磷脂dsc谱图。图7是β‐环糊精、辅酶q10、二十八烷醇‐物理混合物dsc谱图。图8是羟丙基‐β‐环糊精、辅酶q10、二十八烷醇物理混合物dsc谱图。图9是γ‐环糊精、辅酶q10、二十八烷醇‐物理混合物dsc谱图。图10是β‐环糊精、辅酶q10、二十八烷醇、磷脂物理混合物dsc谱图。图11是实施例5辅酶q10与二十八烷醇、β‐环糊精多元超分子包合物dsc谱图。图12是实施例10辅酶q10与二十八烷醇、羟丙基‐β‐环糊精多元超分子包合物dsc谱图。图13是实施例15辅酶q10与二十八烷醇、γ‐环糊精多元超分子包合物dsc谱图。图14是实施例18辅酶q10与二十八烷醇、磷脂、β‐环糊精多元超分子包合物dsc谱图15是实施例21辅酶q10与二十八烷醇含有卵磷脂羟丙基‐β‐环糊精多元超分子包合物dsc谱图。图16是实施例24辅酶q10与二十八烷醇含有卵磷脂γ‐环糊精多元超分子包合物dsc谱图。图17是辅酶q10原料红外光谱图。图18是二十八烷醇原料红外光谱图。图19是β‐环糊精原料红外光谱图。图20是大豆卵磷脂原料红外光谱图。图21是辅酶q10二十八烷醇β‐环糊精物理混合物红外光谱图。图22是实施例3辅酶q10二十八烷醇β‐环糊精多元包合物红外光谱图。图23是实施例18辅酶q10二十八烷醇β‐环糊精磷脂多元包合物红外光谱图。图24是实施例18辅酶q10二十八烷醇β‐环糊精磷脂多元包合物粒径分布图。图25是实施例3、13、16、22多元包合物辅酶q10累积释放曲线。图26是实施例3、13、16、22多元包合物二十八烷醇累积释放曲线。具体实施方式下面结合实施例对本发明进行进一步描述。以下实施例仅为本发明的几个具体实施例,但本发明的设计构思并不局限于此,凡利用此构思对本发明进行非实质性的改动,均应属于侵犯本发明保护范围的行为。下述实施例中的方法,如无特别说明,均为常规方法,所述的百分含量均为质量百分含量。实施例1本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,制备方法如下:取β‐环糊精30重量份,加入150重量份的水混合,加热至60℃,再加入10重量份氧化型辅酶q10及1重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨15次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为69.2%,二十八烷醇包封率为65.3%。实施例2本发明还原型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取β‐环糊精50重量份,加入250重量份的水混合,加热至65℃,再加入10重量份还原型辅酶q10及2重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到13%,进行冷冻干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为89.1%,二十八烷醇包封率为85.3%,计算包结比为1:0.33:6.06。实施例3本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取β‐环糊精100重量份,加入400重量份的水混合,加热至90℃,再加入10重量份氧化型辅酶q10及5重量份含量为50%二十八烷醇c22~c36高级脂肪烷醇混合物,搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到11%,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为85.3%,二十八烷醇包封率为81.4%。实施例4本发明还原型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取β‐环糊精120重量份,加入600重量份的水混合,加热至60℃,再加入10重量份还原型辅酶q10及10重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨17次,放料,加水至固形物含量达到12.5%,进行喷雾干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为87.8%,二十八烷醇包封率为74.8%。实施例5本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取β‐环糊精150重量份,加入450重量份的水混合,加热至75℃,再加入10重量份氧化型辅酶q10及7重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨17次,放料,加水至固形物含量达到12%,进行冷冻干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为88.5%,二十八烷醇包封率为80.2%。取该包合物5mg,进行热分析dsc测定。实施例6本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精30重量份,加入90重量份的水混合,加热至80℃,再加入10重量份氧化型辅酶q10及1重量份含量为60%二十八烷醇c22~c36高级脂肪烷醇混合物,搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到11.5%,进行冷冻干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为64.2%,二十八烷醇包封率为72.7%。实施例7本发明还原型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精50重量份,加入250重量份的水混合,加热至65℃,再加入10重量份还原型辅酶q10及2重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨17次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为88.4%,二十八烷醇包封率为86.2%,计算包结比为1:0.31:7.04。实施例8本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精100重量份,加入400重量份的水混合,加热至80℃,再加入10重量份氧化型辅酶q10及5重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为82.8%,二十八烷醇包封率为75.3%。实施例9本发明还原型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精120重量份,加入600重量份的水混合,加热至60℃,再加入10重量份还原型辅酶q10及10重量份含量为75%二十八烷醇c22~c36高级脂肪烷醇混合物搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到13%,进行冷冻干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为85.3%,二十八烷醇包封率为64.5%。实施例10本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精150重量份,加入750重量份的水混合,加热至90℃,再加入10重量份氧化型辅酶q10及7重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨15次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为86.7%,二十八烷醇包封率为81.4%。取该包合物5mg,进行热分析dsc测定。实施例11本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取γ‐环糊精30重量份,加入90重量份的水混合,加热至70℃,再加入10重量份氧化型辅酶q10及1重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨15次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为63.1%,二十八烷醇包封率为69.4%。实施例12本发明还原型辅酶q10与二十八烷醇环糊精三元超分子包合物,制备方法如下:取γ‐环糊精50重量份,加入250重量份的水混合,加热至65℃,再加入10重量份还原型辅酶q10及2重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为90.5%,二十八烷醇包封率为88.4%。计算包结比为1:0.22:4.98。实施例13本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,其制备方法如下:取γ‐环糊精100重量份,加入400重量份的水混合,加热至90℃,再加入10重量份氧化型辅酶q10及5重量份二十八烷醇,搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到13%,进行冷冻干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为82.3%,二十八烷醇包封率为75.9%。实施例14本发明还原型辅酶q10与二十八烷醇环糊精三元超分子包合物,制备方法如下:取γ‐环糊精140重量份,加入700重量份的水混合,加热至60℃,再加入10重量份还原型辅酶q10及10重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12.5%,进行喷雾干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为86.1%,二十八烷醇包封率为64.3%。实施例15本发明氧化型辅酶q10与二十八烷醇环糊精三元超分子包合物,制备方法如下:取γ‐环糊精150重量份,加入750重量份的水混合,加热至65℃,再加入10重量份氧化型辅酶q10及7重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨17次,放料,加水至固形物含量达到12%,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精三元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为87.9%,二十八烷醇包封率为80.6%。取该包合物5mg,进行热分析dsc测定。实施例16本发明氧化型辅酶q10、二十八烷醇及大豆卵磷脂复配的环糊精多元超分子包合物,制备方法如下:取β‐环糊精70重量份,加入210重量份的水混合,加热至75℃,再加入10重量份氧化型辅酶q10及1重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,加入1重量份大豆卵磷脂以15000转/分剪切1分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为79.9%,二十八烷醇包封率为74.7%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为210nm。实施例17本发明还原型辅酶q10、二十八烷醇及蛋黄卵磷脂复配的环糊精多元超分子包合物,制备方法如下:取β‐环糊精50重量份,加入250重量份的水混合,加热至60℃,再加入10重量份还原型辅酶q10及2重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨15次,放料,加水至固形物含量达到11%,加入2重量份蛋黄卵磷脂以15000转/分剪切1分钟,进行冷冻干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精含蛋黄卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为78.1%,二十八烷醇包封率为74.3%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为221nm。实施例18本发明氧化型辅酶q10、二十八烷醇及大豆卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取β‐环糊精100重量份,加入500重量份的水混合,加热至90℃,再加入10重量份氧化型辅酶q10及5重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,加入3重量份大豆卵磷脂以15000转/分剪切2分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为76.8%,二十八烷醇包封率为72.9%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为212nm。取包合物5mg,进行热分析dsc测定。实施例19本发明氧化型辅酶q10、二十八烷醇及蛋黄卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精70重量份,加入280重量份的水混合,加热至75℃,再加入10重量份氧化型辅酶q10及2重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,加入1重量份大豆卵磷脂以15000转/分剪切0.5分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为78.4%,二十八烷醇包封率为74.8%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为273nm。实施例20本发明还原型辅酶q10、二十八烷醇及大豆卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精50重量份,加入250重量份的水混合,加热至85℃,再加入10重量份还原型辅酶q10及2重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到11%,加入2重量份大豆卵磷脂以15000转/分剪切1分钟,进行喷雾干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为79.7%,二十八烷醇包封率为75.1%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为229nm。实施例21本发明氧化型辅酶q10、二十八烷醇及蛋黄卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取羟丙基‐β‐环糊精100重量份,加入500重量份的水混合,加热至65℃,再加入10重量份氧化型辅酶q10及5重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到13%,加入3重量份大豆卵磷脂以15000转/分剪切1分钟,进行冷冻干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为77.8%,二十八烷醇包封率为73.9%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为281nm。取包合物5mg,进行热分析dsc测定。实施例22其制备方法如下:取γ‐环糊精50重量份,加入250重量份的水混合,加热至75℃,再加入10重量份氧化型辅酶q10及3重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到13%,加入1重量份大豆卵磷脂以15000转/分剪切1分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为77.4%,二十八烷醇包封率为74.7%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为295nm。实施例23本发明还原型辅酶q10与二十八烷醇及蛋黄卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取γ‐环糊精70重量份,加入350重量份的水混合,加热至60℃,再加入10重量份还原型辅酶q10及2重量份二十八烷醇搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,加入2重量份大豆卵磷脂以15000转/分剪切1.3分钟,进行喷雾干燥,得到还原型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为79.1%,二十八烷醇包封率为74.6%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为289nm。实施例24本发明氧化型辅酶q10与二十八烷醇及大豆卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取γ‐环糊精100重量份,加入500重量份的水混合,加热至85℃,再加入10重量份氧化型辅酶q10及5重量份含量为75%二十八烷醇c22~c36高级脂肪烷醇混合物搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到11.5%,加入3重量份大豆卵磷脂以15000转/分剪切1分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为77.3%,二十八烷醇包封率为73.5%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为298nm。取包合物5mg,进行热分析dsc测定。实施例25本发明氧化型辅酶q10、二十八烷醇及大豆卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取β‐环糊精70重量份,加入350重量份的水混合,加热至85℃,再加入10重量份氧化型辅酶q10及1重量份60%二十八烷醇的c22~c36高级脂肪烷醇混合物搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,加入2重量份大豆卵磷脂以15000转/分剪切1分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为79.9%,二十八烷醇包封率为74.7%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为210nm。实施例26本发明氧化型辅酶q10、二十八烷醇及大豆卵磷脂复配的环糊精多元超分子包合物,其制备方法如下:取β‐环糊精80重量份,加入320重量份的水混合,加热至85℃,再加入10重量份氧化型辅酶q10及2重量份80%二十八烷醇的c22~c36高级脂肪烷醇混合物搅拌成糊状,放入胶体磨中,循环研磨20次,放料,加水至固形物含量达到12%,加入2重量份大豆卵磷脂以15000转/分剪切1分钟,进行喷雾干燥,得到氧化型辅酶q10与二十八烷醇复配的环糊精含大豆卵磷脂多元超分子包合物。分别用高效液相和气相色谱法测定包合物中辅酶q10和二十八烷醇的包封率,辅酶q10包封率为73%,二十八烷醇包封率为75%。取少量样品分散在水中,使溶液达到具有乳光的状态即可,通过马尔文粒度分析仪进行测定,测得该超分子包合物脂质体的粒径为236nm。实施例27高效液相色谱法测定包合物中辅酶q10取本发明相应实施例1‐26制备的辅酶q10与二十八烷醇复配的环糊精多元包合物适量,乙醚洗涤,挥散乙醚,加少量水溶散,用乙醇加热超声,放冷定容至规定浓度后,过滤,取续滤液作为供试品溶液,进样,色谱条件:辅酶q10:c18柱,流动相为乙腈∶四氢呋喃∶水=55∶40∶5(体积比),检测波长275nm,外标法定量,即得。实施例28气相色谱法测定包合物中二十八烷醇取本发明相应实施例1‐26制备的辅酶q10与二十八烷醇复配的环糊精多元包合物适量,乙醚洗涤,挥散乙醚。加少量水溶散,用乙醇加热超声,蒸干后用三氯甲烷溶解定容至规定浓度后,0.45um微孔滤膜过滤,待测。色谱条件依据国家标准gbt32947蜂蜡中二十八烷醇、三十烷醇的测定气相色谱法。实施例29溶解度测定:分别取本发明实施例1~26制备的辅酶q10与二十八烷醇环糊精包合物、辅酶q10与二十八烷醇及环糊精物理混合物适量,分别加入到100ml的纯水中,使成过饱和溶液,37℃水浴搅拌24小时,过滤。取滤液1ml,用无水乙醇定容至10ml,50℃超声20min,冷却至室温,用0.45um滤膜过滤,采用高效液相法测定辅酶q10含量;另取过滤的饱和溶液5ml,加无水乙醇20ml,50℃超声20min,挥干溶剂,用三氯甲烷溶解定容至10ml,用0.45um滤膜过滤,采用气相色谱法测定二十八烷醇含量,结果见表1、表2。结果表明,本发明实施例1~26制备的包合物中辅酶q10溶解度为49‐562μg/ml,二十八烷醇溶解度为21‐195μg/ml;辅酶q10与二十八烷醇物理混合物中辅酶q10原料未测出,二十八烷醇原料未测出。表1辅酶q10的溶解度表2二十八烷醇的溶解度表1、表2表明,本发明的辅酶q10与二十八烷醇复配的环糊精三元包合物与其原型药相比,加大幅度提高了溶解度,也高于其单独包合物的溶解度;本发明含有磷脂的多元包合物溶解度显著高于辅酶q10与二十八烷醇复配的环糊精三元包合物。实施例30释放度测定:采用透析袋法测定本发明实施例3、13、16、22制备的辅酶q10与二十八烷醇复配的环糊精多元包合物、辅酶q10与二十八烷醇物理混合物的体外释放度实验。选用醋酸纤维素半透膜(截留分子量10000)为渗透膜,于使用前在超纯水中煮沸半小时。药物释放介质为5%labrasol-20%乙醇-pbs溶液。取一定量的辅酶q10与二十八烷醇纳米结构脂质载体粉末、辅酶q10与二十八烷醇物理混合物加入透析袋中,用绳子扎紧两端,将透析袋置于装有250ml含5%labarsol-20%乙醇-pbs释放介质的锥形瓶中,(37±0.5)℃摇床振摇,速度为200r/min,于1h,2h,3h,5h,7h,9h,12h,24h取样10ml,再迅速补充10ml相同温度的空白释放介质,样品用hplc法和gc法分别测定q10和二十八烷醇的释放量,得到累积释放曲线如图25与图26。实施例31红外光谱法测定包合物采用红外光谱仪分别测定了原料、物理混合物和包合物实施例3及18溴化钾压片在室温下的红外光谱,扫描范围为400~4000cm‐1。图谱结果如图16‐23所示。其中物理混合物图谱具有明显的辅酶q10和二十八烷醇及β‐环糊精的特征峰,而包合物图谱中特征峰改变,证明已形成新的包合物。实施例32包合物稳定性测定本发明组合物的稳定性试验:取辅酶q10原料、二十八烷醇原料以及本发明实施例1‐26制备的包合物适量,进行影响因素试验考察。取上述物质在4000lx光下,温度40℃,相对湿度92.5%放置10天,分别于0天、5天、10天取样测定辅酶q10、二十八烷醇,结果见表3。表3影响试验结果表明本发明包合物稳定性优于两者原料稳定性以及它们单独包合物稳定性。实施例33清除dpph自由基法测抗氧化性试验:测试方法:分别取待测样品和空白样品(不含coq10和二十八烷醇的环糊精或环糊精及磷脂)150μl加入2.85ml超纯水中,即稀释20倍;样品为按照实施例3、7、13、18、21、24制备的辅酶q10与二十八烷醇复配的环糊精多元包合物、含有磷脂的辅酶q10与二十八烷醇复配的环糊精多元包合物、辅酶q10与二十八烷醇与环糊精单独包合物、辅酶q10与二十八烷醇原料混合物dpph(2,2‐diphenyl‐1‐picrylhydrazyl(freeradical))溶液的配制:准确称取8mgdpph粉末用无水乙醇定容到100ml容量瓶中,得2×10‐4mol/ldpph溶液,再稀释到5×10‐5mol/l待用;取试管编号,按表4进行加样,混合均匀,水浴37℃下反应60min后,在517nm波长处测定待测样品反应液吸光度值,以及空白样品的吸光度值。(调零参比为1ml空白样品与2ml超纯水混合)表4清除dpph自由基实验各成分所需量组别待测样品/ml空白样品/mldpph/ml超纯水/mla待测样.dpph2.004.00a待测样.水2.0004.0a空白样.dpph02.04.00利用下述公式计算抑制率:抑制率e(%)=(1‐(a待测样.dpph‐a待测样.水)/a空白样.dpph)×100%对辅酶q10与二十八烷醇复配的环糊精多元包合物、含有磷脂的辅酶q10与二十八烷醇复配的环糊精多元包合物、辅酶q10与二十八烷醇与环糊精单独包合物、辅酶q10与二十八烷醇原料混合物进行比较清除dpph自由基能力,结果如表5:表5不同浓度coq10-ln清除dpph自由基法实验结果结果表明本发明的辅酶q10与二十八烷醇复配的β‐环糊精多元包合物清除自由基能力显著超过其辅酶q10与二十八烷醇单独二元包合物以及两种原料的混合物,而加入卵磷脂的β‐环糊精多元包合物具有更优的效果。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1