抗NGLY-1抗体及使用方法与流程
相关申请
本申请根据35u.s.c.119(e)要求2018年5月23日提交的美国临时申请号62/675,715和2018年7月12日提交的美国临时申请号62/697,058的利益,上述两项申请各自通过引用整体纳入本申请。
背景技术:
ngly1r539x等位基因在小鼠n-聚糖酶1(ngly-1)基因中有一个(1)碱基对替换,其编码无义突变,从而导致过早终止密码子。该突变对应于在患者群体中确定为iv型先天性糖基化障碍(也称为alacrimia-choreoathesis-肝功能障碍综合征和ngly1缺陷)的致病变体的r524x突变。
技术实现要素:
在一些实施方案中,本文提供了一种与小鼠ngly-1和人ngly-1特异性地结合的抗体。在一些实施方案中,该抗体包含重链,该重链包含:(a)包含seqidno:3的序列的cdr1,(b)包含seqidno:4的序列的cdr2,和(c)包含seqidno:5的序列的cdr3。在一些实施方案中,抗ngly-1抗体包含轻链,该轻链包含:(a)包含seqidno:14的序列的cdr1,(b)包含seqidno:15的序列的cdr2,和(c)包含seqidno:16的序列的cdr3。
本文还提供了包含特异性地结合ngly-1和ngly-1的抗体的组合物和试剂盒。
本文进一步提供了包括使细胞与特异性地结合ngly-1和ngly-1的抗体接触的方法。这类方法可用于例如诊断具有ngly1缺陷的受试者。还提供了包含本文所述抗体的诊断试剂盒。
本发明还提供了使用与ngly-1和ngly-1特异性结合的抗体治疗癌症的方法。
本文提供的抗体可与人ngly-1蛋白或小鼠ngly-1蛋白特异性结合。为简单起见,应当理解,提及“特异性地结合ngly-1的抗体”或“抗ngly-1抗体”包括可特异性地结合小鼠ngly-1蛋白和可特异性地结合人ngly-1蛋白的抗体。
附图说明
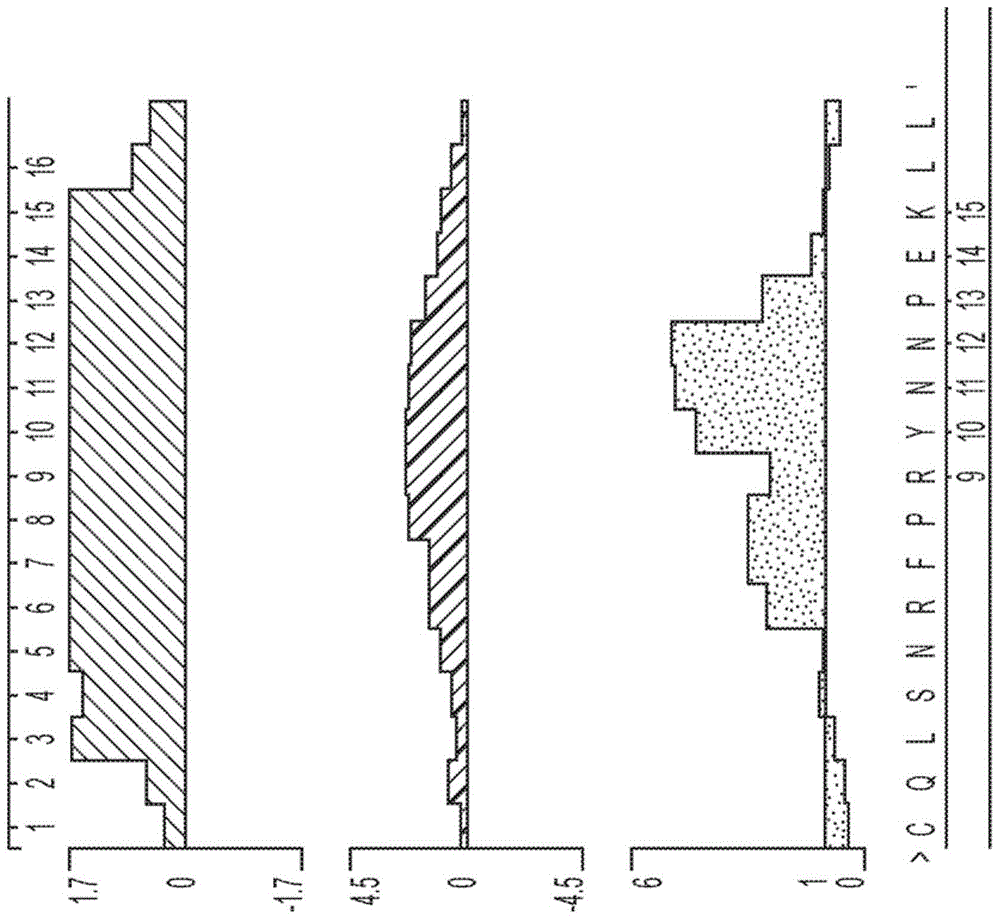
图1显示了ngly-1氨基酸序列283至299(seqidno:45)的抗原指数图(上)、亲水性图(中)和表面概率图(下)。
图2显示了ngly-1氨基酸序列442至460(seqidno:46)的抗原指数图(上)、亲水性图(中)和表面概率图(下)。
图3显示了全长nglyc-1与选择的两个候选肽的结构。
图4显示了证明本公开的单克隆抗体的抗ngly-1特异性的数据。组织使用c57bl/6j(wt)和jr27060ngly-1null纯合组织(hom)从胚胎16.5天脑和心脏收集。
图5显示了证明本公开的小鼠抗ngly-1单克隆抗体与人ngly-1交叉反应的数据。泳道1:f47e6小鼠c57bl/6j(wt);泳道2:f47e127060小鼠ngly-1null突变体;泳道3:人ipsc细胞:dgw-a1(ngly1双重突变体)-源自受影响的患者;泳道4:人ipsc细胞:39b9-1(校正的ngly-1双重突变体的一个等位基因);泳道5:人h9野生型es细胞。
图6显示了证明公开可得的抗ngly-1抗体之一检测与天然小鼠ngly-1蛋白大小非常相似的交叉反应蛋白的数据,表明该抗体对ngly-1不是特异性的。所使用的组织从b57bl/6j(jr00664)和纯合ngly1null(jr27060)胚胎(16.5天龄)分离。
图7显示了证明商业上可得的抗ngly-1抗体(sigma)对ngly-1不具有特异性的数据。预期大小的主要条带见图a的泳道2、6、9、10、13和图b的泳道1。图a-泳道1:jr00664心脏总提取物;泳道2:jr00664心脏线粒体部分;泳道3:jr00664心脏细胞溶质部分;泳道4:jr00664肾总提取物;泳道5:jr00664肾线粒体部分;泳道6:jr00664肾细胞溶质部分;泳道7:jr00664肝总提取物;泳道8:jr27962肝线粒体部分;泳道9:jr00664肝线粒体部分;泳道10:jr00664肝细胞溶质部分;泳道11:jr00664骨骼肌线粒体部分;泳道12:jr00664骨骼肌线粒体部分;泳道13:jr00664骨骼肌细胞溶质部分。图b-泳道1:c2c12小鼠肌细胞系;泳道2:2h11小鼠内皮细胞系;泳道3:mk4人胚胎肾细胞系;泳道4:nih3t3小鼠成纤维细胞系;泳道5:jr00664脑总提取物;泳道6:无裂解物对照。组织从jr00664c57bl/6j小鼠品系和jr27962c57bl/6j-ngly1em9lutzy/j(ngly缺陷的)小鼠品系获得。
图8a和8b显示了证明使用另一种商业上可得的抗ngly-1抗体(abcam)在小鼠c57bl/6j组织中检测62kda多肽的数据。这是比使用本公开的抗ngly-1单克隆抗体观察到的更小的蛋白质。此外,使用该商业上可得的抗ngly-1抗体检测到针对2-3kda的小多肽的强烈交叉反应性,并且在脑组织中未检测到62kda蛋白质的表达。这表明,利用这种商业上可得的抗体检测的蛋白质可能不是小鼠ngly-1。图8b:泳道1:jr00664脑总提取物;v2:jr00664脑线粒体部分;泳道3:jr00664脑细胞溶质部分;泳道4:jr00664肝总提取物;泳道5:jr27962(het)肝总提取物;泳道6:jr00664肝线粒体部分;泳道7:jr00664肝细胞溶质部分;泳道8:nih3t3细胞系(小鼠)。
图9显示了证明又一种商业上可得的抗nglyc-1抗体(encor)产生高背景,并且检测的主要蛋白质显著小于预期的数据。从针对来自已知ngly-1蛋白null品系的裂解物筛选抗体显示了多个条带保留。因此,这种商业上可得的抗体是非特异性的。该抗体针对人ngly-1的n末端300个氨基酸制备。泳道1:jr00664c57bl/6je16.5胚胎脑;泳道2:jr27060ngly1null小鼠e16.5胚胎脑;泳道3:jr28975ngly1null小鼠e16.5胚胎脑。
具体实施方式
ngly1缺陷是一种缺乏ngly1正常表达或功能的罕见的影响儿童的遗传性障碍。这些儿童表现出整体发育迟缓、肌肉张力的丧失、周围神经病变、癫痫发作、不良反射、语言障碍、泪液产生不足、角膜瘢痕、慢性便秘和/或肝功能障碍。ngly1的蛋白质产物编码一种称为n-聚糖酶1的酶,也称为pngase,其催化从糖蛋白的天冬酰胺侧链去除n-连接的寡糖。胞质pngase活性首先在酿酒酵母中报告(suzuki等,2000),随后发现其在许多物种(包括果蝇、秀丽隐杆线虫、小鼠和人)中是进化保守的。
本公开的一些方面提供了一种与ngly-1特异性结合并包含重链和轻链的抗体,其中该重链包含(a)包含seqidno:3的序列的cdr1,(b)包含seqidno:4的序列的cdr2,和(c)包含seqidno:5的序列的cdr3,和/或该轻链包含(a)包含seqidno:14的序列的cdr1,(b)包含seqidno:15的序列的cdr2,和(c)包含seqidno:16的序列的cdr3。
抗体(可互换地以复数形式使用)是能够通过位于免疫球蛋白分子的可变区中的至少一个抗原识别位点特异性地结合靶标如碳水化合物、多核苷酸、脂质、多肽等的免疫球蛋白分子。如本文所用,术语“抗体”不仅包括完整的(即,全长)单克隆抗体,还包括抗原结合片段(如fab、fab’、f(ab’)2、fv)、单链可变片段(scfv)、其突变体、包含抗体部分的融合蛋白、人源化抗体、嵌合抗体、双体抗体、线性抗体、单链抗体、单域抗体(例如,骆驼或美洲驼vhh抗体)、多特异性抗体(例如,双特异性抗体)及包含具有所需特异性的抗原识别位点的免疫球蛋白分子的任何其他修饰的结构,包括抗体的糖基化变体、抗体的氨基酸序列变体和共价修饰的抗体。抗体包括任何类别的抗体,如igd、ige、igg、iga或igm(或其亚类),并且抗体无需属于任何特定类别。根据其重链恒定区的抗体氨基酸序列,免疫球蛋白可分配到不同的类别。免疫球蛋白有五大类:iga、igd、ige、igg和igm,且其中几类可进一步分为亚类(同种型),例如igg1、igg2、igg3、igg4、iga1和iga2。对应于不同类别免疫球蛋白的重链恒定域分别称为α、δ、ε、γ和μ。不同类别的免疫球蛋白的亚基结构和三维构型是众所周知的。
本文所述方法中使用的抗体可以是鼠、大鼠、人或任何其他来源的(包括嵌合或人源化抗体)。在一些实例中,抗体包含修饰的恒定区,如免疫惰性的恒定区,例如不触发补体介导的裂解,或不刺激抗体依赖性细胞介导的细胞毒性(adcc)。可以使用美国专利no.5,500,362中公开的方法评价adcc活性。在其他实施方案中,恒定区如eur.j.immunol.(1999)29:2613-2624、pct申请号pct/gb99/01441;和/或uk专利申请号9809951.8中所述进行修饰。
在一些实施方案中,本公开的抗体是单克隆抗体。“单克隆抗体”指均质的抗体群体。
在一些实施方案中,本公开的抗体是人源化抗体。人源化抗体指非人(例如,鼠)抗体的形式,其为包含源自非人类免疫球蛋白的最小序列的特异性嵌合免疫球蛋白、免疫球蛋白链或其抗原结合片段。就大部分而言,人源化抗体是其中来自受体的互补决定区(cdr)的残基被来自具有所需特异性、亲和力和能力的非人类物种(供体抗体)如小鼠、大鼠或兔的cdr的残基所替代的人免疫球蛋白(受体抗体)。在一些情况下,人免疫球蛋白的fv框架区(fr)残基被相应的非人类残基替代。此外,人源化抗体可包含既不存在于受体抗体中也不存在于输入的cdr或框架序列中的残基,但其被包含以进一步改善和优化抗体性能。一般地,人源化抗体包含至少一个和通常两个可变域的基本上全部,其中全部或基本上全部cdr区对应于非人免疫球蛋白的cdr区,并且全部或基本全部fr区是人免疫球蛋白共有序列的fr区。人源化抗体最佳地还包含免疫球蛋白恒定区或结构域的至少一部分(fc),通常人免疫球蛋白的。抗体可以具有如wo99/58572中所述修饰的fc区。其他形式的人源化抗体具有一个或多个相对于原始抗体改变的cdr(一个、两个、三个、四个、五个、六个),其也称为“源自”原始抗体的一个或多个cdr的一个或多个cdr。人源化抗体也可以涉及亲和力成熟。
在其他实施方案中,本公开的抗体是嵌合抗体,其可包括人抗体的重链恒定区和轻链恒定区。嵌合抗体指具有来自第一物种的可变区或可变区的部分和来自第二物种的恒定区的抗体。典型地,在这些嵌合抗体中,轻链和重链的可变区模拟源自一个哺乳动物物种(例如,非人类哺乳动物,如小鼠、兔和大鼠)的抗体的可变区,而恒定部分与源自另一哺乳动物如人的抗体中的序列同源。在一些实施方案中,可以在可变区和/或恒定区中进行氨基酸修饰。
在一些实施方案中,本公开的抗体特异性地结合靶抗原,如(小鼠或人)ngly-1。与靶标或表位“特异性结合”(在本文中可互换使用)的抗体是本领域熟知的术语,并且确定这种特异性结合的方法在本领域中也是众所周知的。如果分子与特定靶抗原的反应或结合相比于其与替代靶标的反应或结合更频繁、更快速、持续时间更长和/或具有更高的亲和力,则称其表现出“特异性结合”。如果抗体与靶抗原的结合比与其他物质的结合具有更高的亲和力、亲合力、更容易和/或更长的持续时间,则该抗体与靶抗原“特异性结合”。例如,特异性(或优先)结合ngly-1表位的抗体是以比其结合其他ngly-1表位或非ngly-1表位更高的亲和力、亲合力、更容易和/或更长的持续时间结合该ngly-1表位的抗体。在一些实施方案中,ngly-1表位包含seqidno:45或46。在一些实施方案中,本公开提供了包含seqidno:45的氨基酸序列或由其组成的肽。通过阅读该定义还应理解,例如,特异性结合第一靶抗原的抗体可以或不可以特异性或优先结合第二靶抗原。因此,“特异性结合”或“优先结合”不一定要求(尽管可以包括)排他性结合。一般地,但不是必然,提及结合意味着优先结合。
在一些实施方案中,抗体和ngly-1之间的平衡解离常数(kd)为100pm至1000pm。例如,抗体和ngly-1之间的kd可以是100pm至900pm、100pm至800pm、100pm至700pm、100pm至600pm、100pm至500pm、100pm至400pm、100pm至300pm、150pm至1000pm、150pm至900pm、150pm至800pm、150pm至700pm、150pm至600pm、150pm至500pm、150pm至400pm、150pm至300pm、200pm至1000pm、200pm至900pm、200pm至800pm、200pm至700pm、200pm至600pm、200pm至500pm、200pm至400pm、200pm至300pm、250pm至1000pm、250pm至900pm、250pm至800pm、250pm至700pm、250pm至600pm、250pm至500pm、250pm至400pm或200pm至300pm。在一些实施方案中,抗体和ngly-1之间的平衡解离常数(kd)为100pm、150pm、200pm、210pm、220pm、230pm、240pm、250pm、260pm、270pm、280pm、290pm或300pm。在一些实施方案中,抗体和ngly-1之间的平衡解离常数(kd)小于500pm、小于400pm或小于300pm。在一些实施方案中,抗体和ngly-1之间的kd为1nm至100nm。
重链
重链是抗体的大多肽亚基。重链的大小和组成不同,但长度通常在450至550个氨基酸之间且由包含三个或四个免疫球蛋白结构域的恒定域(hc恒定)和包含单个免疫球蛋白结构域的可变域(hc可变)组成。重链的可变域对于结合抗原是重要的。免疫球蛋白结构域是通过β链三维排列成平行的β折叠片而形成的结构。哺乳动物中重链具有五种类型,其限定了抗体的类别,其中iga抗体包含alpha(α)重链,igd抗体包含delta(δ)重链,ige抗体包含epsilon(ε)重链,igm抗体包含mu(μ)重链,和igg抗体包含gamma(γ)重链。
在一些实施方案中,本公开的抗体的重链包含seqidno:1的序列。在一些实施方案中,本公开的抗体的重链包含与seqidno:1的序列具有至少95%、96%、97%、98%或99%同一性的序列。
轻链
轻链是抗体的小多肽。轻链大小不同,但长度通常在210至217个氨基酸之间且由包含单个免疫球蛋白结构域的恒定域(lc恒定)和包含单个免疫球蛋白结构域的可变域(lc可变)组成。哺乳动物中具有两种类型的轻链,其由恒定区的序列定义且分类为kappa(κ)或lambda(λ)。轻链的可变域对于结合抗原是重要的。抗体中通常仅存在一种类型的轻链,因此单一抗体中的两条轻链是相同的。
在一些实施方案中,本公开的抗体的轻链包含seqidno:13的序列。在一些实施方案中,本公开的抗体的轻链包含与seqidno:13的序列具有至少95%、96%、97%、98%或99%同一性的序列。
可变区
每个抗体具有由重链和轻链两者的可变域组成的独特的可变区,其包含抗原结合位点。可变区进一步细分为互补决定区(cdrs)和框架区(fr)。每个抗体上有两个可变域,其通常但不总是结合相同的抗原。
在一些实施方案中,重链包含与seqidno:10的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的可变区。在一些实施方案中,重链包含含有seqidno:10的序列的可变区。
在一些实施方案中,轻链包含与seqidno:21的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的可变区。在一些实施例中,轻链包含含有seqidno:21的序列的可变区。
cdr
可变区内的互补决定区(cdr)(也称为高变区,或hv)在给定位置中高比率具有相对于该位置最常见氨基酸不同的氨基酸。三个cdr(cdr1、cdr2、cdr3)存在于重链和轻链中,其形成直接接触抗原表面的一部分的柔性环。
在一些实施方案中,特异性地结合ngly-1的抗体包含重链,其包含(a)包含seqidno:3的序列的cdr1,(b)包含seqidno:4的序列的cdr2,和(c)包含seqidno:5的序列的cdr3。
在一些实施方案中,特异性地结合ngly-1的抗体包含轻链,其包含(a)包含seqidno:14的序列的cdr1,(b)包含seqidno:15的序列的cdr2,和(c)包含seqidno:16的序列的cdr3。
框架区
可变区内的框架区(fr)由分隔cdr序列的保守氨基酸序列组成。fr区形成β-折叠片结构,其用作为将cdr保持在适当位置以接触抗原表面的支架。每个重链和轻链内存在四个fr区。
在一些实施方案中,重链包含与seqidno:6的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的框架区;与seqidno:7的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的框架区;与seqidno:8的序列至少90%或至少95%相同的框架区;和/或与seqidno:9的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的框架区。
在一些实施方案中,轻链包含与seqidno:17的序列至少90%(例如,至少91%、92%、93%、94%、95%、96%、97%、98%或99%)相同的框架区;与seqidno:18的序列至少90%(例如,至少91%、92%、93%、94%、95%、96%、97%、98%或99%)相同的框架区;与seqidno:19的序列至少90%(例如,至少91%、92%、93%、94%、95%、96%、97%、98%或99%)相同的框架区;和/或与seqidno:20的序列至少90%(例如,至少91%、92%、93%、94%、95%、96%、97%、98%或99%)相同的框架区。
恒定区
抗体的恒定区被免疫细胞上的受体和蛋白质识别以启动和调节宿主防御机制。重链多肽的恒定区在免疫球蛋白类别的所有抗体中是相同的,但在免疫球蛋白类别之间不同。igγ、igα和igδ中的重链包含由三个免疫球蛋白结构域组成的恒定区和用于提高的柔性的铰链区。igμ和igε中的重链包含由四个免疫球蛋白结构域组成的恒定区。轻链多肽的恒定区由单个免疫球蛋白结构域组成。
在一些实施方案中,重链包含与seqidno:11的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的恒定区。在一些实施方案中,重链包含含有seqidno:11的序列的恒定区。
在一些实施方案,轻链包含与seqidno:22的序列至少90%或至少95%(例如,至少96%、97%、98%或99%)相同的恒定区。在一些实施方案中,轻链包含含有seqidno:22的序列的恒定区。
多核苷酸和抗体合成
本公开还提供了编码本文所述抗体的多核苷酸。本文中使用的“多核苷酸”包括单个核酸以及多个核酸,并且指分离的核酸分子或构建体,例如信使rna(mrna)或质粒dna(pdna)。多核苷酸可包含常规磷酸二酯键或非常规键(例如,酰胺键,如在肽核酸(pna)中发现的)。术语“核酸”指多核苷酸中存在的任何一个或多个核酸片段,例如,dna或rna片段。“分离的”多核苷酸是例如从其天然环境中移除的dna或rna。例如,为本公开的目的,载体中包含的编码抗体的重组多核苷酸被认为是分离的。分离的多核苷酸的进一步例子包括在异源宿主细胞中维持的重组多核苷酸或溶液中的纯化(部分或基本上)的多核苷酸。分离的rna分子包括本公开多核苷酸的体内或体外rna转录物。分离的多核苷酸或核酸可进一步包括合成产生的这类分子。另外,多核苷酸可包括调控元件,如启动子、核糖体结合位点或转录终止子。示例性多核苷酸序列提供于表2中(seqidno:23-44)。
在编码抗体的多核苷酸合成后,可将该多核苷酸插入表达载体中用于引入可用于产生所需抗体的宿主细胞中。本文描述了抗体或其片段(例如抗体的重链或轻链)的重组表达。一旦获得编码抗体分子或者抗体的重链或轻链或者其部分(优选包含重链或轻链可变域)的多核苷酸,可使用本领域可获得的技术通过重组dna技术产生用于产生抗体分子的载体。因此,本文描述了通过表达包含抗体编码核苷酸序列的多核苷酸制备蛋白质的方法。本领域技术人员可用的方法可以用于构建包含抗体编码序列和适当的转录和翻译控制信号的表达载体。这些方法包括例如体外重组dna技术、合成技术和体内基因重组。因此,本公开提供了可复制载体,其包含可操作地连接至启动子的编码本发明的抗体分子,或其重链或轻链,或重链或轻链可变域的核苷酸序列。这类载体可包括编码抗体分子恒定区的核苷酸序列,且抗体的可变域可被克隆到这种载体中用于表达整个重链或轻链。
术语“载体”或“表达载体”在本文中用于指引入宿主细胞中和在宿主细胞中表达所需基因的媒介。载体可选自质粒、噬菌体、病毒和反转录病毒。在一些实施方案中,载体包含选择标记、促进所需基因的克隆的适当限制性位点以及进入真核或原核细胞中和/或在其中复制的能力。根据本公开,可以使用多种表达载体系统。
一旦制备了编码抗体单体的亚体亚基的载体或dna序列,可将表达载体引入合适的宿主细胞中。质粒引入宿主细胞中可通过本领域技术人员可获得的各种技术来完成。这些技术包括但不限于转染(包括使用例如fugene或lipofectamine的脂转染)、原生质体融合、磷酸钙沉淀、与包膜的dna的细胞融合、显微注射和完整病毒的感染。在一些实施方案中,质粒引入宿主中是通过标准的磷酸钙共沉淀方法。携带表达构建体的宿主细胞在适合轻链和重链产生的条件下生长,并分析重链和/或轻链蛋白质合成。示例性分析技术包括酶联免疫吸附分析(elisa)、放射免疫分析(ria)或荧光激活细胞分选分析(facs)和免疫组织化学。
表达载体可通过任何可用的细胞转染技术转移至宿主细胞。然后可以通过可用的技术培养转染的细胞以产生本文所述的抗体。因此,本公开提供了包含编码本公开的抗体或其重链或轻链的多核苷酸(在一些实施方案中,其可操作地连接至异源启动子)的宿主细胞。
一旦本文所述的抗体分子被重组表达,可根据可用的纯化程序,包括例如通过色谱法(例如,离子交换、亲和,特别是通过在蛋白a后对特定抗原的亲和力,以及尺寸柱色谱(sizingcolumnchromatography))、离心、差异溶解(例如,硫酸铵沉淀)或通过任何其他标准的蛋白质纯化技术,对整个抗体、二聚体、单个轻链和/或重链或其他免疫球蛋白形式进行纯化;参见,例如scopes,"proteinpurification",springerverlag,n.y.(1982)。
n-聚糖酶1(ngly-1)的检测及ngly-1缺陷的诊断
本公开的另一方面提供了使用本文所述的抗体检测n-聚糖酶1(ngly-1)和诊断ngly-1缺陷的方法。这些方法也可用于监测ngly-1缺乏治疗的功效。由于本文所述的抗ngly-1抗体对ngly-1具有强的结合亲和力且可用于检测生物样品中ngly-1的存在,因此缺乏抗ngly-1抗体结合,或者抗ngly-1抗体的结合低于相对于对照的特定阈值,指示ngly-1缺陷。本文使用的术语“检测”指定量和/或定性检测。
在一些实施方案中,提供了用于诊断或检测方法中的抗ngly-1抗体。例如,提供了一种检测生物样品中ngly-1的存在(或不存在)的方法。在一些实施方案中,方法包括在允许抗ngly-1抗体与ngly-1结合的条件下使生物样品与本文所述的抗ngly-1抗体接触,和检测在抗ngly-1抗体与ngly-1之间是否形成复合物。例如,这种方法可以在体外进行。抗ngly-1抗体-ngly-1复合物的存在可以指示健康受试者(在不具有ngly-1缺陷的受试者中),而复合物形成的缺乏可以指示受试者具有ngly-1缺陷。
同样地,可以随时间监测ngly-1的水平,例如,以确定ngly-1缺陷治疗的功效。监测可以以均匀间隔的时间间隔进行,例如每天、每2天、每3天、每4天、每5天、每6天、每周、每两周、每3周、每月、每两月、每3个月、每4个月、每5个月、每6个月、每7个月、每8个月、每9个月、每10个月、每11个月或每年。在一些实施方案中,监测以不同间隔的时间间隔进行。例如,如果受试者的ngly-1水平在监测期内提高,则可能需要较低频率的监测。相反地,如果受试者的ngly-1水平在监测期内下降,则可能需要更频繁的监测。在一些实施方案中,受试者样品中存在的ngly-1水平可与参考样品的水平进行比较。本文中使用的“参考样品”是指来自不存在ngly-1缺陷的个体的样品或来自具有ngly-1缺陷的个体的样品。举例来说,当正在接受ngly-1缺陷治疗的受试者的ngly-1水平比来自具有ngly-1缺陷的受试者的参考样品的ngly-1水平更高可指示有效的治疗时,可以表明有效治疗。
可以使用本领域中可用的任何方法进行抗ngly-1抗体结合的检测,包括免疫测定,包括例如免疫组织化学(ihc)、免疫荧光(if)、免疫印迹(例如,蛋白质印迹)、流式细胞术(例如,facstm)和酶联免疫吸附测定(elisa)。在一些实施方案中,免疫印迹用于检测。
因此,在一些实施方案中,抗体与可检测标记物缀合(抗体-标记缀合物),例如酶、放射性同位素、荧光团、重金属(胶态金属)或发光分子。可检测标记的例子包括但不限于,荧光素酶、绿色荧光蛋白(gfp)、氯霉素乙酰转移酶(cat)、32p、33p、14c、125i、131i、35s、3h、荧光素、异硫氰酸荧光素(fitc)、dylight488、藻红蛋白(pe)、碘化丙啶(pi)、percp、pe-alexafluor700、cy5、别藻蓝蛋白、cy7、多种发光镧系元素(例如铕或铽)螯合物中的任何一种(例如,二亚乙基三胺五乙酸(dtpa)或四氮杂环十二烷-1,4,7,10-四乙酸(dota)的铕螯合物)、碱性磷酸酶、辣根过氧化物酶、金、铜、汞和镉。在一些实施方案中,可检测标记可以作为融合蛋白并入抗ngly-1抗体中。用于产生编码抗体-异源多肽融合蛋白的核酸的方法在抗体工程领域中是众所周知的,并在例如dakappagari等(2006)jimmunol176:426-440中描述。
本公开进一步提供了抗ngly-1抗体在诊断患有障碍(例如,ngly-1缺陷)的受试者的方法中的用途,该方法包括:通过将从受试者获得的样品与本文所述的抗ngly-1抗体接触并检测结合的抗体的存在来测定样品中ngly-1的存在或表达水平。生物样品指来自受试者的组织、细胞或组成部分的子集(例如,体液,包括但不限于血液、粘液、淋巴液、滑液、脑脊液、唾液、羊水、羊膜脐带血、尿液、阴道液和精液)。样品还可包括从受试者或其组织、细胞或组成部分的子集或者其分数或部分(包括但不限于,例如,血浆、血清、脊髓液、淋巴液、皮肤外段、呼吸道、肠道和泌尿生殖道、泪液、唾液、乳液、血细胞、肿瘤、器官)制备的匀浆、裂解物或提取物。
本公开还进一步提供了抗ngly-1抗体在制备用于诊断患有障碍(例如,ngly-1缺陷)的受试者的方法中的试剂的用途,该方法包括:通过将从受试者获得的样品与本公开的抗ngly-1抗体接触并检测结合的抗体的存在来测定样品中ngly-1的存在或表达水平。
本文提供了试剂盒,其包括本文所述的诊断性抗ngly-1抗体和使用说明。因此,在一些实施方案中,该试剂盒包括含有分别在seqidno:3-5和14-16中示出的重链和轻链可变区cdr序列、分别在seqidno:10和21中示出的重链和轻链可变区序列(其中该抗体或其抗原结合片段与人ngly-1特异性结合),或分别在seqidno:1和2中示出的全长重链和轻链序列的抗体。在某些实施方案中,抗体包含可检测的标记,例如,抗体-标记缀合物。这种试剂盒可包含至少一种额外的试剂。例如,在一些实施方案中,试剂盒包括缓冲剂、稳定剂、底物、至少一种免疫检测试剂(例如,用于免疫组织化学中的二级抗体)和/或分析所需的辅因子。在一些实施方案中,抗体和任选的试剂被适当地等分。在一些实施方案中,试剂盒包括用于从受试者获得生物样品的装置。这种装置可包括例如可用于从受试者获得流体或组织样品的试剂。
药物组合物
在一些方面,本公开提供了包含本文所述的抗体和药学上可接受的载体的药物组合物。“药学上可接受的载体”在对受试者(例如人)施用后或施用于受试者时不引起不希望的生理效应。药物组合物中的载体也必须在其与活性成分相容并能够稳定活性成分的意义上是“可接受的”。一种或多种增溶剂可用作用于递送活性剂的药用载体。药学上可接受的载体的实例包括但不限于生物相容性媒介、辅料、添加剂和稀释剂以获得可作为剂型使用的组合物。其他载体的例子包括胶体氧化硅、硬脂酸镁、纤维素和十二烷基硫酸钠。remington'spharmaceuticalsciences中描述了其他合适的药物载体和稀释剂,以及用于其使用的药剂辅料。
在一些实施方案中,组合物进一步包含用于治疗ngly-1缺陷的另外的药剂,例如酶替代疗法和/或质子泵抑制剂(engase抑制剂)(bi等,bioorgmedchemlett.2017;27:2962-6)。
在一些实施方案中,组合物是诊断组合物,并且进一步包含至少一种用于本文所述的基于免疫和/或基于核酸的诊断方法中的试剂。例如,试剂包括但不限于用于免疫测定中的那些试剂,免疫测定包括例如免疫组织化学(ihc)、免疫荧光(if)、免疫印迹(例如,蛋白质印迹)、流式细胞术(例如,facstm)和酶联免疫吸附测定(elisa)。这类试剂对于所使用的诊断方法的类型是特异性的,并且是本领域已知的。
治疗方法
在一些实施方案中,本公开提供了治疗患者的疾病或障碍的方法,包括向需要的患者施用治疗有效量的结合ngly-1蛋白的抗体。在一些实施方案中,疾病或障碍是癌症。癌症可以是癌瘤、肉瘤、淋巴瘤、白血病、黑色素瘤、间皮瘤、多发性骨髓瘤或精原细胞瘤,或者癌症可以是黑色素瘤、卵巢癌、乳腺癌、子宫颈癌、子宫内膜癌、结肠癌、胰腺癌、前列腺癌、肝癌、肾癌、肺癌、神经胶质瘤或淋巴瘤。在一些实施方案中,癌症为膀胱、血液、骨、脑、乳腺、中枢神经系统、子宫颈、结肠、子宫内膜、食道、胆囊、胃肠道、生殖器、泌尿生殖道、头、肾、喉、肝、肺、肌肉组织、颈、口腔或鼻粘膜、卵巢、胰腺、前列腺、皮肤、脾、小肠、大肠、胃、睾丸或甲状腺的癌症。在一些实施方案中,癌症为神经胶质瘤、肝癌或黑色素瘤。在一些实施方案中,癌症是黑色素瘤。
在一些实施方案中,该方法进一步包括施用第二药剂/癌症疗法,例如外科手术、第二化学治疗剂、放射治疗或免疫治疗。在一些实施方案中,第二化学治疗剂是烷化剂或烷化样药剂,如顺铂、达卡巴嗪或替莫唑胺。
在一些实施方案中,药物组合物配制用于以下施用:口服、脂肪内(intraadiposally)、动脉内、关节内、颅内、皮内、病灶内、肌内、鼻内、眼内、心包内、腹膜内、胸膜内、前列腺内、直肠内、鞘内、气管内、肿瘤内、脐内、阴道内、静脉内、膀胱内、玻璃体内、脂质体内、局部、粘膜、胃肠外、直肠、结膜下、皮下、舌下、局部地、经颊、经皮、阴道、乳液中(in
药物组合物可以有效量(即能够在治疗受试者中产生所需结果(例如,导致癌细胞的凋亡)的量)施用于哺乳动物(例如,啮齿动物、人、非人类灵长动物、狗、牛、羊、马、猫等)。本公开方法中使用的组合物的毒性和治疗效果可通过可用的药物学过程确定。任何一名受试者的剂量取决于多种因素,包括受试者的体型、体表面积、体重、年龄、待施用的特定组合物、施用时间和途径、一般健康状况、感染或癌症的临床症状以及同时施用的其他药物。本文所述的组合物通常以诱导癌细胞死亡(例如,诱导癌细胞的凋亡)的剂量施用,如通过鉴定血液学参数(全血细胞计数-cbc)的降低或者癌细胞的生长或增殖测定的。
实施例
实施例1
小鼠ngly1的蛋白质序列从string相互作用网络数据库(string-db.org)获得。使用editseq应用将序列加载到dnastar软件包中。editseq文件随后加载到protean应用中以生成特定物理化学特性的图:
1)使用jamesonwolf算法的抗原性指数
2)使用kyledoolittle算法的亲水性
3)使用emini算法的表面概率图。
基于代表氨基酸片段283-299(图1)和442-460(图2)的高抗原性指数、高亲水性和高表面概率,选择了两个候选肽用于在3-d模型中审查。
使用maxplanckinstitute的mpibionformatics工具包,特别是hhpred建模工具(toolkit.tuebingen.mpgde/#/tools/hhpred)生成3-d模型。由此产生的原子坐标被加载到macpymol3-d建模和渲染软件的本地副本中,并生成3-d模型。
肽1,一种源自鼠ngly1氨基酸283-299(含)的17聚体氨基酸肽cqlsnrfprynnpekll(seqidno:45),被选择并以洋红色突出显示;并且选择代表氨基酸442至460的肽2(seqidno:46)和以青色突出显示(图3)。
由于肽2是结构化的且相对难接近,其被拒绝作为候选肽。肽1显示出具有高度可及性的无序区域,且该肽的合成通过德国海德堡的peptidespecialtylabsgmbh订购。除了第三个氨基酸的单多态性外,该肽序列与人ngly1中的合成区相同。该氨基酸在小鼠中是亮氨酸,而在人中是苯丙氨酸。该肽的一部分与白喉类毒素载体蛋白缀合用于免疫。
缀合物以每小鼠10μg的剂量与明矾佐剂一起注射到雌性balb/cj小鼠中。小鼠通过间隔约两(2)周i.p注射三次进行免疫。第三次免疫后10天,分离脾细胞并与sp2骨髓瘤细胞融合以形成杂交瘤细胞系。杂交瘤在96孔平板中培养,且上清液在蛋白质阵列上和通过elisa筛选。阳性克隆通过蛋白质印迹使用从c57bl/6j和crispr/cas9产生的空白品系作为阳性和阴性对照制备的裂解物进一步验证。使用额外的免疫印迹来鉴定产生能够与人ngly1蛋白交叉反应的抗体的额外克隆。提供了同基因的人来源ngly1null和野生型ips细胞系,从而提供抗人ngly1交叉反应性的阳性和阴性对照评估。单个杂交瘤产生克隆5g8,其产生对鼠和人ngly1蛋白两者特异性的抗体并用于后续研究。
表1.抗ngly-1抗体氨基酸序列
*该序列可包括终止序列,如tga
前导序列加下划线。
表2.抗ngly-1抗体核酸序列
*该序列可包括终止序列,如tga
前导序列加下划线。
实施例2.
本实施例提供了本公开的抗ngly-1抗体与表3中列出的先前描述的和/或可商购的抗ngly-1抗体的比较。
图4-9描述了使用的条件和获得的结果。
表3.测试的抗体:ngly-1特异性
本文公开的所有参考文献、专利和专利申请相对于其各自引用的主题通过引用方式并入,其在某些情况下可包含文件的全部内容。
除非明确指出相反,说明书和权利要求书中使用的不定冠词“一”和“一个”应理解为指“至少一个”。
还应当理解,除非明确指出相反的情况,在本文要求保护的包括超过一个步骤或动作的任何方法中,该方法的步骤或动作的顺序不一定限于该方法的步骤或动作被陈述的顺序。
在权利要求以及上述说明书中,所有过渡短语如“包括”、“包含”、“携带”、“具有”、“含有”、“涉及”、“持有”、“由…构成”等应被理解为开放式的,即意味着包括但不限于。只有过渡短语“由…组成”和“基本上由…组成”根据unitedstatespatentofficemanualofpatentexaminingprocedures,section2111.03中所示应分别为封闭式或半封闭式过渡短语。
数值前的术语“约”和“基本上”指所陈述数值的±10%。
在提供数值范围的情况下,该范围的上限和下限之间的每一个值均在本文中被具体考虑和描述。
- 还没有人留言评论。精彩留言会获得点赞!