针对降钙素基因相关肽的拮抗剂抗体及其使用方法与流程
针对降钙素基因相关肽的拮抗剂抗体及其使用方法本申请是中国发明专利申请200680042443.0(PCT/IB2006/003181)的分案申请,母案申请日为2006年11月2日,题目为“针对降钙素基因相关肽的拮抗剂抗体及其使用方法”。本申请要求于2005年11月14日提交的美国专利申请No.60/736,623的优先权,其通过引用并入本文。技术领域本发明涉及抗CGRP拮抗剂抗体用于预防、改善或治疗血管运动症状如CGRP相关头痛(例如偏头痛)和热潮红的用途。
背景技术:
CGRP(降钙素基因相关肽)是37个氨基酸的神经肽,其属于肽家族,包括降钙素、肾上腺髓质素和淀粉不溶素。在人中,存在两种形式的CGRP(α-CGRP和β-CGRP),它们具有类似的活性。它们有三个氨基酸不同,并显示不同的分布。至少两种CGRP受体亚型也可解释有差异的活性。CGRP是中枢神经系统中的神经递质,并已显示是外周中有效的血管扩张药,含CGRP的神经元在外周与血管紧密结合。CGRP介导的血管扩张也与神经原性炎症相关(其作为导致原生质外渗和微脉管系统血管舒张的事件级联的一部分),其存在于偏头痛中。CGRP因其与血管运动症状的可能联系而被注意(Wyonetal.Scand.J.Urol.Nephrol.35:92-96(2001);Wyonetal.Menopause7(1):25-30(2000))。血管运动症状(VMS)如热潮红和寝汗是与绝经相关的最常见症状,发生在所有在天然或手术诱导后绝经女性的60%到80%中。热潮红很可能是中枢神经系统(CNS)对减退的性类固醇的适应性应答(FreedmanAm.J.HumanBiol.13:453-464(2001))。迄今为止,对于潮红的最有效的疗法是基于激素的治疗,所述激素包括雌激素和/或一些黄体酮。激素治疗能够有效缓和潮红,但是不适合所有女性。观察到的心理和情绪症状(如神经质、疲劳、易激惹、失眠、抑郁、失忆、头痛、焦虑、神经质或不能集中)被认为是由热潮红和寝汗后的睡眠缺乏引起的(Krameretal.,In:Murphyetal.,3.sup.rdInt′lSymposiumonRecentAdvancesinUrologicalCancerDiagnosisandTreatment-Proceedings,Paris,France:SCI:3-7(1992))。男性类固醇激素(雄激素)减少后也经历热潮红。在年龄相关的雄激素减退的情况下(Katovich,etal.,ProceedingsoftheSocietyforExperimentalBiology&Medicine,1990,193(2):129-35)以及与前列腺癌治疗相关的激素丧失的极端情况下(Berendsen,etal.,EuropeanJournalofPharmacology,2001,419(1):47-54)是这样的。三分之一的这类患者会经历足够严重到引起显著不适和不便的长期和频繁的症状。CGRP是与其它血管运动症状的病理学相关的有效的血管扩张剂,所述症状例如所有形式的血管性头痛,包括偏头痛(有先兆或无先兆)和丛集性头痛。Durham,N.Engl.J.Med.350:1073-1075,2004。患者偏头痛期间颈外静脉中的CGRP水平升高。Goadsbyetal.,Ann.Neurol.28:183-7,1990。静脉施用人α-CGRP在患有无先兆偏头痛的患者中诱导头痛和偏头痛,这提示CGRP在偏头痛中具有原因作用。Lassenetal.,Cephalalgia22:54-61,2002.CGRP与偏头痛的可能相关性是开发和测试大量下述化合物的基础,所述化合物抑制CGRP的释放(例如叔马曲坦)、拮抗CGRP受体(例如二肽衍生物BIBN4096BS(BoerhringerIngelheim);CGRP(8-37))或与一种或多种受体相关蛋白质相互作用,所述受体相关蛋白质例如受体活性膜蛋白(RAMP)或受体组件蛋白质(RCP)均影响CGRP对其受体的结合。Brain,S.etal.,TrendsinPharmacologicalSciences23:51-53,2002。A-2肾上腺素受体亚型和腺苷A1受体也调控(抑制)CGRP释放和三叉神经活化(Goadsbyetal.,Brain125:1392-401,2002)。针对GR79236(metrafadil)腺苷A1的受体(其已经显示在人中抑制神经原性血管舒张和三叉神经伤害感受)也可以具有抗偏头痛的活性(Arulmanietal.,Cephalalgia25:1082-1090,2005;Giffinetal.,Cephalalgia23:287-292,2003)。使得该理论混淆的是下述观察:用仅抑制神经原性炎症(例如速激肽NK1受体拮抗剂)或三叉神经活化(例如5HT1D受体激动剂)的化合物治疗显示作为偏头痛的急性治疗相对无效,引起一些研究人员质疑是否抑制CGRP释放是有效的抗偏头痛治疗的主要作用机制。Arulmanietal.,Eur.J.Pharmacol.500:315-330,2004。偏头痛是复杂的、常见的神经原性病症,其特征在于严重的、偶发的头痛和相关的特征,所述相关特征可包括恶心,呕吐,对光、声音或运动敏感。在一些患者中,头痛之前有前兆或伴随前兆。头痛可以是严重的,并在某些患者中也可以是单侧的。偏头痛发作对日常生活是破坏性的。在美国和西欧,偏头痛患者的总体患病率在一般人群中占11%(6%男性;15-18%女性)。另外,个体中发作的中位频率是1.5次/月。尽管能够获得大量治疗来缓和或减少症状,但是对每个月具有多于3-4次偏头痛发作的患者来说预防疗法是推荐的。Goadsbyetal.NewEngl.J.Med.346(4):257-275,2002。用于治疗偏头痛的药理学干涉的变化和患者间应答的多样性是该病症不同特性的证明。因此,显示5-羟色胺能以及肾上腺素能、去甲肾上腺素能、和多巴胺能活性的这类相对非选择性的药物,如麦角生物碱(例如麦角胺、二氢麦角胺、美西麦角),已经用于治疗偏头痛超过八十年。其它治疗包括阿片制剂(例如羟考酮)和β-肾上腺素能拮抗剂(例如普萘洛尔)。一些患者(通常是具有更温和症状的患者)能够用非处方药物控制它们的症状,所述非处方药例如一种或多种非甾体抗炎剂(NSAIDs),如阿司匹林、扑热息痛和咖啡因(例如Migraine)的组合。更近期地,已经用托吡酯治疗一些偏头痛患者,托吡酯是封闭电压依赖性钠通道和某些谷氨酸受体(AMPA红藻氨酸盐)、增强GABA-A受体活性和封闭碳酸酐酶的抗惊厥剂。相对而言更近期地,5-羟色胺5HT-1B/1D和/或5HT-1a受体激动剂(如叔马曲坦)在一些患者中的成功已经引起研究人员提出了该病症的5-羟色胺能病因学。不幸的是,尽管一些患者对该治疗反映良好,但是其它的患者对其作用相对有抵抗力。假定氨基酸能脑干细胞核中的离子通道功能障碍解释了该疾病,然而偏头痛的精确病理生理学仍未被充分理解。一种形式的偏头痛(家族性偏瘫偏头痛)已经显示与电压门控P/Q-型钙通道的α1亚基中的错义突变相关,人们认为很可能也在其它患者群体中发现其它的离子通道突变。尽管血管扩张与偏头痛相关并加重疼痛症状,但是这类神经血管事件目前被认为是该病症的结果而不是起因。总之,调节感觉输入的脑干途径的功能障碍被认为是偏头痛的统一特征。Goadsby,P.J.etal.,NewEngl.J.Med.346(4):257-275,2002。在本申请中引用了多种出版物(包括专利和专利申请)。这些出版物的公开内容通过引用整体并入本文。
技术实现要素:
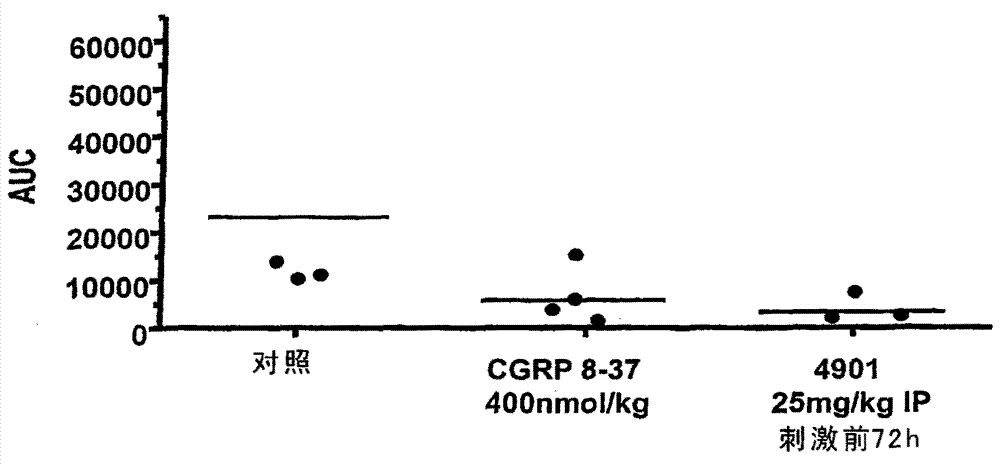
本文公开的发明涉及抗CGRP拮抗剂抗体和施用抗CGRP拮抗剂抗体用于治疗或预防血管运动症状的方法,所述血管运动症状例如头痛,如有先兆或无先兆的偏头痛、偏瘫性偏头痛、丛集性头痛、偏头痛神经痛、久头痛、紧张性头痛和由其它医疗条件(如由肿瘤引起的感染或颅内压升高)引起的头痛。其它血管运动症状包括热潮红。一方面,本发明提供了用于在个体中治疗或预防至少一种血管运动症状的方法,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体。一方面,本发明提供了用于在个体中治疗或预防头痛(例如偏头痛和丛集性头痛)的方法,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体。另一方面,本发明提供了用于在个体中改善、控制、减少头痛(例如偏头痛和丛集性头痛)发作或延迟头痛发生或发展的方法,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体。在另一实施方案中,本发明提供了用于在个体中改善、控制、减少头痛(例如偏头痛和丛集性头痛)发作或延迟头痛发生或发展的方法,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体与至少一种适用于治疗头痛的其它试剂的组合。这类其它试剂包括5-HT1-样激动剂(作用于其它5-HT1位点上的激动剂)和非甾体类抗炎药(NSAIDs)。可与抗CGRP抗体组合使用的5-HT1激动剂的例子包括已知为曲坦类(triptans)的一类化合物,如叔马曲坦、佐米曲坦、那拉曲坦、利扎曲坦、伊立曲坦、阿莫曲坦和夫罗曲坦。麦角生物碱和相关化合物也显示具有5-HT激动剂活性并被用于治疗头痛如偏头痛。这些化合物包括麦角胺、马来酸麦角新碱和甲磺酰麦角碱(例如二氢麦角柯宁碱、双氢麦角汀、双氢麦角隐亭和双氢麦角胺甲磺酸盐(DHE45))。可以与抗CGRP抗体组合使用的NSAIDs的例子包括萘普生、氟比洛芬、酮洛芬、奥沙普秦、依托度酸、吲哚美辛、酮咯酸、萘丁美酮、迈菲那密酸(mefanamicacid)和吡罗昔康。其它的NSAIDs包括环氧化酶2(COX-2)抑制剂。该组成员包括:塞来考昔;罗非考昔;美洛昔康;JTE-522;L-745,337;NS398及其可药用盐。另一方面,本发明提供了用于在个体中改善、控制、减少热潮红的发作或延迟其发生或发展的方法,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体。另一方面,本发明提供了用于在个体中改善、控制、减少热潮红的发作或延迟其发生或发展的方法,所述包括对个体施用有效量的抗CGRP拮抗剂抗体与至少一种适用于治疗热潮红的试剂的组合。这类其它试剂包括,但不限于基于激素(包括雌激素和/或黄体酮)的治疗。在一个实施方案中,在上述任何方法中使用的抗CGRP拮抗剂抗体是本文所述的任何抗体。在一些实施方案中,抗CGRP拮抗剂抗体能识别人CGRP。在一些实施方案中,抗CGRP拮抗剂抗体与人α-CGRP和β-CGRP均能结合。在一些实施方案中,抗CGRP拮抗剂抗体能与人和大鼠CGRP结合。在一些实施方案中,抗CGRP拮抗剂抗体结合具有CGRP的氨基酸25-37的C末端片段。在一些实施方案中,抗CGRP拮抗剂抗体结合CGRP的氨基酸25-37中的C末端表位。在一些实施方案中,抗CGRP拮抗剂抗体是单克隆抗体。在一些实施方案中,抗CGRP拮抗剂抗体是人源化的。在一些实施方案中,抗体是人的。在一些实施方案中,抗CGRP拮抗剂抗体是抗体G1(如本文所述)。在一些实施方案中,抗CGRP拮抗剂抗体包含表6所示抗体G1或G1变体的一个或多个CDR(例如一个、两个、三个、四个、五个或在一些实施方案中包含所有六个CDR)。还在其它实施方案中,抗CGRP拮抗剂抗体包含图5所示重链可变区的氨基酸序列(SEQIDNO:1)和图5所示轻链可变区的氨基酸序列(SEQIDNO:2)。在一些实施方案中,抗体包含下述经修饰的恒定区,所述恒定区例如是免疫惰性的(包括是部分免疫惰性的,其例如不引发补体介导的裂解、不刺激抗体依赖性细胞介导的细胞毒性(ADCC)、活化小胶质细胞),或具有降低的一种或多种这些活性。在一些实施方案中,恒定区被修饰,这如Eur.J.Immunol.(1999)29:2613-2624;PCT申请No.PCT/GB99/01441;和/或UK专利申请No.9809951.8中所述。在其它一些实施方案中,抗体包含人重链IgG2恒定区,所述恒定区包含以下突变:A330P331到S330S331(参考野生型IgG2序列的氨基酸排序)Eur.J.Immunol.(1999)29:2613-2624。在一些实施方案中,抗体的重链恒定区是具有任何以下突变的人重链IgG1:1)A327A330P331到G327S330S331;2)E233L234L235G236到P233V234A235,G236被删除;3)E233L234L235到P233V234A235;4)E233L234L235G236A327A330P331到P233V234A235G327S330S331,G236被删除;5)E233L234L235A327A330P331到P233V234A235G327S330S331和6)N297到A297或除N以外的任何其它氨基酸。在一些实施方案中,抗体的重链恒定区为带有任何以下突变的人重链IgG4:E233F234L235G236到P233V234A235,G236被删除;E233F234L235到P233V234A235;和S228L235到P228E235。还在其它一些实施方案中,恒定区N连接的糖基化不被糖基化(aglycosylated)。在一些实施方案中,通过突变寡糖附着残基(如Asn297)和/或侧翼残基(其为恒定区中N-糖基化识别序列的一部分),针对N连接的糖基化而言恒定区不被糖基化。在一些实施方案中,针对N连接的糖基化而言恒定区不被糖基化。可通过酶或通过在糖基化缺陷宿主细胞中表达使得针对N连接的糖基化而言恒定区不被糖基化。抗CGRP拮抗剂抗体对CGRP(例如在合适温度如25或37℃下通过表面等离振子共振测量的人α-CGRP)的亲合力(KD)可以是约0.02到约200nM。在一些实施方案中,亲合力为下述任何:约200nM、约100nM、约50nM、约10nM、约1nM、约500pM、约100pM、约60pM、约50pM、约20pM、约15pM、约10pM、约5pM或约2pM。在一些实施方案中,亲合力少于下述任何:约250nM、约200nM、约100nM、约50nM、约10nM、约1nM、约500pM、约100pM或约50pM。抗CGRP拮抗剂抗体可以在头痛之前、期间和/或之后被施用。在一些实施方案中,抗CGRP拮抗剂抗体在头痛(例如偏头痛和丛集性头痛)发作之前被施用。抗CGRP拮抗剂抗体的施用可以通过本领域已知的任何手段:口服、静脉内、皮下、动脉内、肌内、贲门内、椎管内、胸内、腹膜内、心室内、舌下、经皮和/或经过吸入。施用可以是全身的(例如静脉内)或局部的。在一些实施方案中,抗CGRP拮抗剂抗体可以与另一试剂(如用于治疗头痛的另一试剂)结合施用。另一方面,本发明提供了抗CGRP拮抗剂抗体用于制造本文所述任何方法中使用(例如用于治疗或预防头痛)的药物的用途。另一方面,本发明提供了用于预防或治疗头痛(例如偏头痛和丛集性头痛)的药物组合物,其包含有效量的抗CGRP拮抗剂抗体,所述抗体与一种或多种可药用赋形剂组合。另一方面,本发明提供了用于本文所述任何方法中的试剂盒。在一些实施方案中,所述试剂盒包含容器、包含本文所述抗CGRP拮抗剂抗体的组合物(其与可药用媒介组合)和在本文所述任何方法中使用该组合物的说明书。本发明还提供了抗CGRP拮抗剂抗体和来自表6所示的抗体G1或其变体的多肽。因此,一方面,本发明是由ATCC编号Nos.PTA-6866和PTA-6867的表达载体生产的抗体G1(可交换地称作”G1”)。例如,在一个实施方案中是包含重链的抗体,所述重链由ATCC编号为No.PTA-6867的表达载体生产。在再一个实施方案中为包含轻链的抗体,所述抗体由ATCC编号为No.PTA-6866的表达载体生产。G1的重链和轻链可变区的氨基酸序列在图5中显示。抗体G1的互补性决定区(CDR)部分(包括Chothia和KabatCDRs)也显示在图5中。应理解:涉及G1任何局部或整体区域包括由具有ATCC编号Nos.PTA-6866和PTA-6867的表达载体生产的序列和/或图5中所示的序列。本发明还提供了具有表6所示氨基酸序列的G1抗体变体。一方面,本发明是包含VH结构域的抗体,所述VH在氨基酸序列上与SEQIDNO:1至少85%、至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%相同。另一方面,本发明是包含VL的抗体,所述VL在氨基酸序列上与SEQIDNO:2至少85%、至少86%、至少87%、至少88%、至少89%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%相同。另一方面,本发明是包含表6所示抗体G1或其变体的片段或区域的抗体。在一个实施方案中,片段为抗体G1的轻链。在另一实施方案中,片段为抗体G1的重链。还在另一实施方案中,片段含有来自抗体G1轻链和/或重链的一个或多个可变区。还在另一实施方案中,片段含有来自图5所示轻链和/或重链的一个或多个可变区。还在另一实施方案中,片段含有来自抗体G1轻链和/或重链的一个或多个CDR。另一方面,本发明提供了多肽(其可以是或不是抗体),所述多肽含有SEQIDNO:5中公开的VHCDR3,或与SEQIDNO:5因1、2、3、4或5个氨基酸取代而不同的序列。在特别的实施方案中,这类氨基酸取代是保守的氨基酸取代。另一方面,本发明提供了多肽(其可以是或不是抗体),所述多肽含有SEQIDNO:8中公开的VLCDR3,或与SEQIDNO:8因1、2、3、4或5个氨基酸取代而不同的序列。在特别的实施方案中,这类氨基酸取代是保守的氨基酸取代。另一方面,本发明提供了多肽(其可以是或不是抗体),所述多肽包含以下任一种或多种:a)来自表6所示抗体G1或其变体的一个或多个(一个、两个、三个、四个、五个或六个)CDR;b)来自表6所示抗体G1重链的CDRH3的CDR;和/或c)来自抗体G1轻链的CDRL3的CDR。在一些实施方案中,CDR为图5所示的CDR。在一些实施方案中,来自表6所示抗体G1或其变体的一个或多个CDR与G1或其变体的至少一个、至少两个、至少三个、至少四个、至少五个或至少六个CDR至少约85%、至少约86%、至少约87%、至少约88%、至少约89%、至少约90%、至少约91%、至少约92%、至少约93%、至少约94%、至少约95%、至少约96%、至少约97%、至少约98%或至少约99%相同。在一些实施方案中,CDR为KabatCDR。在其它实施方案中,CDR为ChothiaCDR。在其它实施方案中,CDR为Kabat和ChothiaCDR的组合(也称作“组合的CDR”或“扩展的CDR”)。换言之,对于含有多于一个CDR的任何给定的实施方案而言,CDR可以是Kabat、Chothia和/或组合的中任一。在一些实施方案中,多肽(例如抗体)包含氨基酸序列KASKXaaVXaaTYVS,其中位置5上的Xaa为R、W、G、L或N;且其中位置7的Xaa为T、A、D、G、R、S、W或V。在一些实施方案中,氨基酸序列KASKXaaVXaaTYVS是抗体轻链的CDR1。在一些实施方案中,多肽(例如抗体)包含氨基酸序列XaaXaaSNRYXaa,其中位置1上的Xaa为G或A;其中位置2的Xaa为A或H;且其中位置7的Xaa为L、T、I或S。在一些实施方案中,氨基酸序列XaaXaaSNRYXaa是抗体轻链的CDR2。在一些实施方案中,多肽(例如抗体)包含氨基酸序列EIRSXaaSDXaaXaaATXaaYAXaaAVKG,其中位置5的Xaa为E、R、K、Q或N;其中位置8的Xaa为A、G、N、E、H、S、L、R、C、F、Y、V、D或P;其中位置9的Xaa为S、G、T、Y、C、E、L、A、P、I、N、R、V、D或M;其中位置12的Xaa为H或F;其中位置15的Xaa为E或D。在一些实施方案中,氨基酸序列EIRSXaaSDXaaXaaATXaaYAXaaAVKG是抗体重链的CDR2。在一些实施方案中,多肽(例如抗体)包含SEQIDNO:1的氨基酸序列,其中SEQIDNO:1位置99的氨基酸残基为L或被A、N、S、T、V或R取代;且其中SEQIDNO:1位置100的氨基酸残基为A或被L、R、S、V、Y、C、G、T、K或P取代。在一些实施方案中,本发明的抗体是人抗体。在其它实施方案中,本发明的抗体是人源化的抗体。在一些实施方案中,抗体是单克隆的。在一些实施方案中,抗体(或多肽)被分离。在一些实施方案中,抗体(或多肽)是基本纯的。抗体的重链恒定区可以来自任何类型的恒定区(例如IgG、IgM、IgD、IgA和IgE)和任何同种型(如IgG1、IgG2、IgG3和IgG4)。在一些实施方案中,抗体包含本文所述的经修饰的恒定区。另一方面,本发明提供了一种多核苷酸(其可以是被分离的),所述多核苷酸包含编码表6所示抗体G1或其变体的片段或区域的多核苷酸。在一个实施方案中,片段为抗体G1的轻链。在其它实施方案中,片段为抗体G1的重链。还在另一实施方案中,片段含有来自抗体G1轻链和/或重链的一个或多个可变区。还在另一实施方案中,片段含有来自抗体G1轻链和/或重链的一个或多个(即一个、两个、三个、四个、五个或六个)互补性决定区(CDRs)。另一方面,本发明是一种多核苷酸(其可以是被分离的),所述多核苷酸含有编码表6所示抗体G1或其变体的多核苷酸。在一些实施方案中,多核苷酸包含SEQIDNO:9和SEQIDNO:10所示的多核苷酸之一或二者。另一方面,本发明提供了编码本文所述任何抗体(包括抗体片段)或多肽的多核苷酸。另一方面,本发明提供了包含本文公开的任何多核苷酸的载体(包括表达载体和克隆载体)和宿主细胞。在一些实施方案中,载体为ATCCNo.PTA-6867的pDb.CGRP.hFcGI。在其它实施方案中,载体为ATCCNo.PTA-6866的pEb.CGRP.hKGI。另一方面,本发明是包含多核苷酸的宿主细胞,所述多核苷酸编码本文公开的任何抗体。另一方面,本发明是被本文所述任何抗体或多肽结合的CGRP复合物。在一些实施方案中,抗体是表6所示的抗体G1或其变体。另一方面,本发明是药物组合物,其包含有效量的本文所述任何多肽(包括抗体,如包含一个或多个抗体G1的CDR的抗体)或多核苷酸,和可药用的赋形剂。另一方面,本发明是产生抗体G1的方法,包括在允许生产抗体G1的条件下培养宿主细胞或其后代,其中所述宿主细胞包含编码抗体G1的表达载体;和在一些实施方案中纯化抗体G1。在一些实施方案中,表达载体包含SEQIDNO:9和SEQIDNO:10所示多核苷酸序列之一或二者。另一方面,本发明提供了通过在合适的细胞中表达一种或多种多核苷酸来生产本文所述任何抗体或多肽(通常随后回收和/或分离感兴趣的抗体或多肽)的方法,所述多核苷酸编码抗体(其可以被单独地表达为单个轻链或重链,或从一个载体表达轻链和重链二者)或多肽。抗CGRP拮抗剂抗体和多肽和编码本发明抗体和多肽的多核苷酸可以用于治疗、预防、改善、控制或减少CGRP异常功能相关疾病如头痛(例如偏头痛、丛集性头痛、久头痛和紧张性头痛)和其它病症(其可通过拮抗CGRP活性被治疗或预防)的发作。另一方面,本发明提供了包含本文所述任一种或多种组合物的试剂盒和组合物。这些试剂盒(其通常被适当地包装并与合适的说明书一起提供)适用于本文所述的任何方法。附图概述图1是显示12种鼠抗体对不同丙氨酸取代的人α-CGRP片段的亲合力的表格。在25℃,下使用Biacore,通过将Fab流过芯片上的CGRP测量亲合力。框内数值代表丙氨酸突变体相对于亲本片段25-37(斜体)的亲合力丧失,来自19-37亲本的K35A除外。″a″表示19-37和25-37片段的亲和力是在不同感受芯片上两个独立测量的平均值±标准偏差。″b″表示由于二相解离速率(offrate),这些相互作用与单一双分子相互作用模型有所偏差,从而使用构象改变模型测定它们的亲和力。灰标度键:白色(1.0)指示亲本亲和力;浅灰(小于0.5)指示比亲本更高的亲和力;深灰(多于2)指示比亲本更低的亲和力;黑色指示未检测到结合。图2A和2B显示了施用CGRP8-37(400nmol/kg)、抗体4901(25mg/kg)和抗体7D11(25mg/kg)对皮肤血流量的作用,这作为电脉冲刺激30秒后的血细胞通量来测量。在电脉冲刺激之前3-5分钟,静脉内(iv)施用CGRP8-37。电脉冲刺激前72小时,腹膜内(IP)施用抗体。图中每个点表示指定条件下处理的一只大鼠的AUC。图中每条线表示在指定条件下处理的大鼠的平均AUC。AUC(曲线下面积)等于Δ通量xΔ时间。″Δ通量″表示电脉冲刺激后通量单位的变化;″Δ时间″表示血细胞通量水平恢复为电脉冲刺激之前水平所需时间。图3显示了施用不同剂量的抗体4901(25mg/kg,5mg/kg,2.5mg/kg或1mg/kg)对皮肤血流量的作用,这作为电脉冲刺激30秒后的血细胞通量来测量。电脉冲刺激之前24小时静脉内(IV)施用抗体。图中每点表示在指定条件下处理的一只大鼠的AUC。图中线条表示在指定条件下处理的大鼠的平均AUC。图4A和4B显示了施用抗体4901(1mg/kgor10mg/kg,Lv.)、抗体7E9(10mg/kg,i.v.)和抗体8B6(10mg/kg,i.v.)对皮肤血流的作用,这作为电脉冲刺激30秒后的血细胞通量来测量。抗体被静脉内(i.v.)施用,然后在抗体施用后30分钟、60分钟、90分钟和120分钟进行电脉冲刺激。Y轴表示与未施用抗体时(时间0)的AUC水平相比的AUC百分比。X轴表示施用抗体和电脉冲刺激之间的时间(分钟)。与时间0相比,″*″表示P<0.05,″**″表示P<0.01。使用单向ANOVA用Dunnett′s多重比较检验分析数据。图5显示了抗体G1的重链可变区(SEQIDNO:1)和轻链可变区(SEQIDNO:2)的氨基酸序列。KabatCDR为黑体,ChothiaCDR加下划线。重链和轻链可变区的氨基酸残基被连续编号。图6显示了使用Biacore通过肽竞争对抗体G1的表位作图。N生物素化的人α-CGRP被捕获在SA感受芯片上。没有竞争肽时或与10μM竞争肽孵育1小时后,将G1Fab(50nM)倒在芯片上。测量芯片上G1Fab对人α-CGRP的结合。Y轴表示与不存在竞争肽时相比,竞争肽的存在封闭的结合百分比。图7显示了使用抗体G1(1mg/kg或10mg/kg,静脉内)或运载体(PBS,0.01%Tween20)对皮肤血流的作用,这作为电脉冲刺激30秒后的血细胞通量来测量。抗体G1或运载体被静脉内(i.v.)施用,然后在抗体施用后30分钟、60分钟、90分钟和120分钟进行神经电脉冲刺激。Y轴表示与未施用抗体或运载体时(时间0)的AUC水平(定义为100%)相比的AUC百分比。X轴表示施用抗体和电脉冲刺激之间的时间(分钟)。与运载体相比,″*″表示P<0.05,″**″表示P<0.01。施用双向ANOVA和Bonferroni后期检验分析数据。图8A显示了施用抗体G1(1mg/kg,3mg/kg或10mg/kg,静脉内)或运载体(PBS,0.01%Tween20)对皮肤血流的作用,这作为给药后24小时电脉冲刺激30秒后的血细胞通量来测量。抗体G1或运载体在神经电脉冲刺激前24小时被静脉内(i.v.)施用。Y轴表示曲线下的总面积(血细胞通量变化乘以刺激到通量恢复基线的时间差,AUC)。X轴表示抗体G1的不同剂量。与运载体相比,″*″表示P<0.05,″**″表示P<0.01。施用单向ANOVA和Dunn′s多重比较检验分析数据。图8B显示了施用抗体G1(0.3mg/kg,1mg/kg,3mg/kg或10mg/kg,静脉内)或运载体(PBS,0.01%Tween20)对皮肤血流的作用,这作为给药后7天电脉冲刺激30秒后的血细胞通量来测量。抗体G1或运载体在神经电脉冲刺激前7天被静脉内(i.v.)施用。Y轴表示总AUC。X轴表示抗体G1的不同剂量。与运载体相比,″**″表示P<0.01,″***″表示P<0.001。施用单向ANOVA和Dunn′s多重比较检验分析数据。图8C是对来自图8A和8B的数据的曲线拟合分析。抗体G1或运载体在神经电脉冲刺激前24小时或7天静脉(i.v.)施用。Y轴表示总AUC。X轴表示不同的G1剂量,以″mg/kg″为单位,用对数标度以测定EC5O。图9显示了电场刺激后抗体mu7E9(10mg/kg)、BIBN4096BS或运载体(PBS,0.01%Tween20)对脑膜中动脉直径改变的作用。在建立对电刺激的基线应答后0分钟的时间点静脉(i.v.)施用抗体mu7E9、BIBN4096BS或运载体。Y轴表示电场刺激后脑膜中动脉直径的改变。静止直径对应0%。X轴表示电脉冲刺激的时间(分钟)。与运载体相比,″*″指示P<0.05,″**″指示P<0.01。使用单向ANOVA和Dunett′s多重比较检验分析数据。图10显示了电场刺激后不同剂量的抗体G1(1mg/kg,3mg/kg或10mg/kg,静脉)或运载体(PBS,0.01%Tween20)对脑膜中动脉直径改变的作用。在电场刺激前7天静脉(i.v.)施用抗体G1或运载体。Y轴表示脑膜中动脉直径的改变。静止直径对应0%。X轴表示刺激电压。与运载体相比,″*″指示P<0.05,″**″指示P<0.01,″***″指示P<0.001。使用双向ANOVA和Bonferroniposttests分析数据。图11A显示了在吗啡上瘾的大鼠中皮下注射纳洛酮(1mg/kg)之前24小时静脉(i.v.)施用抗体mu4901(10mg/kg)或运载体(PBS,0.01%Tween20)对所述皮下注射诱导的体核温度降低的作用。Y轴表示与基线的温度差异。X轴表示从注射纳洛酮的点开始测量的时间。图11B显示了在吗啡上瘾的大鼠中皮下注射纳洛酮(1mg/kg)之前24小时静脉(i.v.)施用抗体mu4901(10mg/kg)或运载体(PBS,0.01%Tween20)对所述皮下注射诱导的尾表温度提高的作用。Y轴表示与基线的温度差异。X轴表示从注射纳洛酮的点开始测量的时间。发明详述本文公开的本发明提供了通过对个体施用治疗有效量的抗CGRP拮抗剂抗体,用于在个体中治疗和/或预防血管运动症状如头痛(例如偏头痛、丛集性头痛、久头痛和紧张性头痛)或热潮红的方法。本文公开的本发明还提供了来自表6所示G1或其变体的抗CGRP拮抗剂抗体和多肽。本发明还提供了这些抗体和多肽的制造和使用方法。一般技术除非另有说明,本发明的实践将使用分子生物学(包括重组技术)、微生物学、细胞生物学、生物化学和免疫学的常规技术,其在本领域技术的范围内。这类技术已在文献中被充分解释,所述文献例如MolecularCloning:ALaboratoryManual,secondedition(Sambrooketa1.,1989)CoIdSpringHarborPress;OligonucleotideSynthesis(MJ.Gait,ed.,1984);MethodsinMolecularBiology,HumanaPress;CellBiology:ALaboratoryNotebook(J.E.Cellis,ed.,1998)AcademicPress;AnimalCellCulture(R.I.Freshney,ed.,1987);IntroductiontoCellandTissueCulture(J.P.MatherandP.E.Roberts,1998)PlenumPress;CellandTissueCulture:LaboratoryProcedures(A.Doyle,J.B.Griffiths,andD.G.Newell,eds.,1993-1998)J.WileyandSons;MethodsinEnzymoiogy(AcademicPress,Inc.);HandbookofExperimentalImmunology(D.M.WeirandCC.Blackwell,eds.);GeneTransferVectorsforMammalianCells(J.M.MillerandM.P.Calos,eds.,1987);CurrentProtocolsinMolecularBiology(F.M.Ausubeletal.,eds.,1987);PCR:ThePolymeraseChainReaction,(Mullisetal.,eds.,1994);CurrentProtocolsinImmunology(J.E.Coliganetal.,eds.,1991);ShortProtocolsinMolecularBiology(WileyandSons,1999);lmmunobiology(CA.JanewayandP.Travers,1997);Antibodies(P.Finch,1997);Antibodies:apracticalapproach(D.Catty.,ed.,IRLPress,1988-1989);Monoclonalantibodies:apracticalapproach(P.ShepherdandCDean,eds.,OxfordUniversityPress,2000);Usingantibodies:alaboratorymanual(E.HarlowandD.Lane(ColdSpringHarborLaboratoryPress,1999);TheAntibodies(M.ZanettiandJ.D.Capra,eds.,HarwoodAcademicPublishers,1995)。定义“抗体”是能够通过位于免疫球蛋白分子可变区的至少一个抗原识别位点特异结合靶标(如碳水化合物、多核苷酸、脂质、多肽等)的免疫球蛋白分子。本文使用的该术语不仅包括完整的多克隆或单克隆抗体,而且包括其片段(如Fab,Fab′,F(ab′)2,Fv)、单链(ScFv)、突变体、包含抗体部分的融合蛋白(如结构域抗体)和免疫球蛋白分子的包含抗原识别位点的任何其它经修饰的构型。抗体包括任何种类的抗体,如IgG、IgA或IgM(或其亚家族),且抗体不必须是任何特别的种类。可以根据抗体重链恒定结构域的氨基酸序列,将免疫球蛋白指定为不同的种类。存在五种主要的免疫球蛋白:IgA、IgD、IgE、IgG和IgM,其中一些可以被进一步分为亚类(同种型),例如IgG1、IgG2、IgG3、IgG4、IgA1和IgA2。对应于不同免疫球蛋白家族的重链恒定结构域分别被称作α、δ、ε、γ和μ。不同家族免疫球蛋白的亚基结构和三维构型是公知的。本文使用的“单克隆抗体”是指从一群基本均质的抗体获得的抗体,即除了可少量存在的可能的天然存在的突变外,包含该种群的个体抗体是相同的。单克隆抗体是高度特异的,其针对单个抗原性位点。另外,与多克隆抗体制剂(其典型地包括针对不同决定簇(表位)的不同抗体)相反,每种单克隆抗体针对抗原上的单个决定簇。修饰词“单克隆的”指示抗体的特性是得自基本均质的抗体种群,并不应被理解为要求通过任何特定的方法生产抗体。例如,可以通过首先由KohlerandMilstein,1975,Nature,256:495描述的杂交瘤方法来制造,或可以通过U.S.Pat.No.4,816,567中所述的重组DNA方法来制造根据本发明待使用的单克隆抗体。单克隆抗体也可以分离自噬菌体文库,所述噬菌体文库使用例如McCaffertyetal.,1990,Nature,348:552-554中所述的技术产生。本文使用的“人源化的”抗体是指非人(例如鼠)抗体的下述形式,其为特异的嵌合体免疫球蛋白、免疫球蛋白链或其含有来自非人免疫球蛋白的最小序列的片段(例如Fv,Fab,Fab′,F(ab′)2或抗体的其它抗原结合亚序列)。对于大部分而言,人源化的抗体是下述人免疫球蛋白(受体抗体),所述人免疫球蛋白中来自受体的互补性决定区(CDR)被替换为来自非人物种的CDR(供体抗体)的残基,所述非人物种如小鼠、大鼠或兔,所述来自非人物种的CDR具有所需的特异性、亲和力和生物活性。在一些情况下,人免疫球蛋白的Fv框架区(FR)残基被替换为相应的非人残基。另外,人源化抗体可包含下述残基,所述残基既不存在于受体抗体中,也不存在于引入的CDR或框架区中,但是被包括在内以进一步精制和优化抗体表现。通常,人源化抗体基本包含所有的(至少一个,典型地两个)可变结构域,其中所有或几乎所有的CDR区对应于非人免疫球蛋白的CDR区,所有或几乎所有的FR区是人免疫球蛋白共有序列的FR区。人源化抗体最适当地也包含至少一部分免疫球蛋白恒定区或结构域(Fc),典型地为人免疫球蛋白的恒定区或结构域。抗体可具有如WO99/58572中所述被修饰的Fc区。其它形式的人源化抗体具有一个或多个CDR(一个、两个、三个、四个、五个、六个),其根据原始抗体被改变,也称作“来自”一个或多个原始抗体CDR的一个或多个CDR。本文使用的“人抗体”是指具有对应于下述抗体氨基酸序列的抗体,所述抗体由人生产和/或使用本领域已知或本文公开的用于制造人抗体的任何技术制造。人抗体的该定义包括包含至少一个人重链多肽或至少一个人轻链多肽的抗体。一个这样的例子是包含鼠轻链和人重链多肽的抗体。人抗体可以使用本领域已知的多种技术生产。在一个实施方案中,人抗体选自噬菌体文库,其中该噬菌体文库表达人抗体(Vaughanetal.,1996,NatureBiotechnology,14:309-314;Sheetsetal.,1998,PNAS,(USA)95:6157-6162;HoogenboomandWinter,1991,J.MoI.Biol.,227:381;Marksetal.,1991,J.MoI.Biol.,222:581)。也可以通过将人免疫球蛋白基因座引入转基因动物(例如小鼠,其中内源免疫球蛋白基因已经被部分或完全灭活)中制造人抗体。该途径描述于U.S.专利Nos.5,545,807;5,545,806;5,569,825;5,625,126;5,633,425和5,661,016。或者,可以通过使生产针对靶抗原的抗体的人B淋巴细胞(这类B淋巴细胞可从个体回收或可以在体外被免疫)永生来制备人抗体。参见例如Coleetal.,MonoclonalAntibodiesandCancerTherapy,AlanR.Liss,p.77(1985);Boemeretal.,1991,J.Immunol.,147(1):86-95和U.S.专利No.5,750,373。本文使用的术语“降钙素基因相关肽”和“CGRP”是指维持至少部分CGRP活性的任何形式的降钙素基因相关肽及其变体。例如,CGRP可以是α-CGRP或β-CGRP。本文使用CGRP包括所有哺乳动物种类的天然序列CGRP,例如人、犬、猫、马和牛。本文使用的“抗CGRP拮抗剂抗体”(可与“抗CGRP抗体”互换使用)是指下述抗体,所述抗体能够结合CGRP并抑制CGRP生物活性和/或CGRP信号转导介导的下游途径。抗CGRP拮抗剂抗体包括下述抗体,所述抗体能够(包括显著地)封闭、拮抗、抑制或降低CGRP生物活性,包括由CGRP信号转导的下游途径如受体结合和/或对CGRP细胞应答的激发。就本发明的目的而言,应明确地理解:术语“抗CGRP拮抗剂抗体”包括所有先前定义的术语、题目和功能状态和特征,由此,CGRP自身、CGRP生物活性(包括但不限于其介导任何方面头痛的能力)或生物活性的后果以任何有意义的程度上被实质上无效、降低或中和。在一些实施方案中,抗CGRP拮抗剂抗体结合CGRP并防止CGRP结合CGRP受体。在其它实施方案中,抗CGRP抗体结合CGRP并防止CGRP受体的激活。本文提供了抗CGRP拮抗剂抗体的例子。本文使用的术语“G1”和“抗体G1”可互换地使用,它们指由具有保藏号ATCCPTA-6867和ATCCPTA-6866的表达载体生产的抗体。图5显示了重链和轻链可变区的氨基酸序列。抗体G1的CDR部分(包括Chothia和KabatCDRs)图示于图5中。编码重链和轻链可变区的多核苷酸显示于SEQIDNO:9和SEQIDNO:10中。G1的表征描述于实施例中。术语“多肽”、“寡肽”、“肽”和“蛋白质”在本文可互换使用,来表示任何长度的氨基酸多聚体。该多聚体可以是线性的或分支的,其可含有经修饰的氨基酸,其可以被非氨基酸阻断。所述术语还包括已经被天然修饰或通过干涉被修饰的氨基酸多聚体;例如二硫键形成、糖基化、脂质化、乙酰化、磷酸化或任何其它加工或修饰,如与标签组分的缀合。还包括在定义中的是例如含有有一个或多个氨基酸类似物(包括例如非天然的氨基酸等)以及本领域已知的其它修饰的多肽。理解到因为本发明的多肽是以抗体为基础的,所以所述多肽能够作为单链或结合的链存在。本文可互换地使用的“多核苷酸”或“核酸”指任何长度的核苷酸多聚体,并包括DNA和RNA。核苷酸可以是脱氧核糖核苷酸、核糖核苷酸、经修饰的核苷酸或碱基,和/或它们的类似物,或可以由DNA或RNA聚合酶掺入多聚体中的任何底物。多核苷酸可包含经修饰的核苷酸,如甲基化的核苷酸和它们的类似物。如果存在对核苷酸结构的修饰,该修饰可以在多聚体装配之前或之后给予。核苷酸的序列可以被非核苷酸组件阻断。多核苷酸可在多聚化后被进一步修饰,例如通过与标签组件缀合来修饰。其它类型的修饰包括例如“帽子”、用类似物取代一个或多个天然存在的核苷酸、核苷酸间修饰,以及未修饰形式的多核苷酸,所述核苷酸间修饰例如为用不带电的键(例如甲基磷酸酯、磷酸三酯、磷酸酰胺、氨基甲酸酯等)修饰和用带电的键(硫代磷酸酯、二硫代磷酸酯等)修饰、含有悬挂部分如蛋白质(例如核酸酶、毒素、抗体、信号肽、ply-L-赖氨酸等)的修饰、用插入剂(例如吖啶、补骨脂素等)修饰、含有螯合剂(例如金属、放射性金属、硼、氧化金属等)的修饰、含有alkylator的修饰、用经修饰的键(例如α异头核酸)修饰。另外,任何通常存在于糖中的羟基基团可以被磷酸酯基团、磷酸基替换,被标准的保护基团保护,或被激活来制备与额外的核苷酸的额外键,或可以与固体支持物缀合。5’和3’端的OH可以被磷酸化或被胺或1到20个碳原子的有机加帽基团部分取代。其它羟基也可以被演化为标准的保护基团。多核苷酸还可以含有本领域一般已知的类似形式的核糖或脱氧核糖,包括例如2′-O-甲基-、2′-O-烯丙基、2′-氟-或2′-叠氮基-核糖,碳环糖类似物,D-异头糖,差向异构体糖如阿拉伯糖、木糖或来苏糖,吡喃糖,呋喃糖,景天庚酮糖,非环状类似物和非碱性核苷类似物如甲基核糖核苷。一个或多个磷酸二酯键可以被替换为备选的连接基团。这些备选的连接基团包括,但不限于其中磷酸盐被替换为P(O)S(″硫代酸盐″)、P(S)S(″二硫代酸盐″)、(O)NR2(″酰胺化物″)、P(O)R、P(O)OR′、CO或CH2(″formacetai″)的实施方案,其中每个R或R′独立地为H或被任选地含有(-O-)键、芳基、链烯基、环烷基、环链烯基或araldyl的烷基(1-20C)取代或未取代。多核苷酸中所有的键不必须是相同的。前文的叙述适用于本文所指的所有多核苷酸,包括RNA和DNA。抗体的“可变区”是指抗体轻链的可变区或抗体重链的可变区,其为单独的或组合的。重链和轻链的可变区各由四个框架区(FR)组成,所述四个框架区被三个互补性决定区(CDR)连接,所述互补性决定区也称作超变区。每个链中的CDR通过FR被紧密结合在一起,并与来自另一条链的CDR一起有助于形成抗体的抗原结合位点。存在至少两种用于确定CDR的技术:(1)以跨物种序列变异性为基础的途径(即Kabatetal.SequencesofProteinsofImmunologicalInterest,(5thed.,1991,NationalInstitutesofHealth,BethesdaMD));和(2)以抗原-抗体复合物的晶体学研究为基础的途径(Al-lazikanietal(1997)J.Molec.Biol.273:927-948)。本文使用的CDR可表示由任一途径或两个途径的组合定义的CDR。抗体的“恒定区”指抗体轻链的恒定区或抗体重链的恒定区,其为单独的或组合的。与抗体或多肽“优先结合”或“特异结合”(在本文可互换使用)的表位是本领域公知的术语,确定这类特异或优先结合的方法也是本领域公知的。如果一个分子与特定细胞或物质反应或结合比起它与其它细胞或物质的反应或结合而言更频繁、更快速、有更长持续时间和/或有更大亲和力,则称该分子显示“特异结合”或“优先结合”。如果抗体与靶标结合比起它与其它物质的结合具有更大亲和力、亲合力、更容易和/或具有更长持续时间,则该抗体“特异结合”或“优先结合”该靶标。例如,与CGRP特异或优先结合的抗体是下述抗体,所述抗体与该表位的结合比起它与其它CGRP表位或非CGRP表位的结合具有更大的亲和力、亲合力、更容易和/或具有更长的持续时间。通过阅读该定义还应理解到例如,与第一靶标特异或优先结合的抗体(或部分或表位)可与第二靶标特异或优先结合,或不特异或优先结合。同样,“特异结合”或“优先结合”不必须要求(尽管其可包括)专一结合。通常但不必须地,涉及结合时表示优先结合。本文使用的“基本纯”是指至少50%纯(即不含污染物)、更优选至少90%纯、更优选至少95%纯、更优选至少98%纯、更优选至少99%纯的材料。“宿主细胞”包括可以是或已经是载体受体的个体细胞或细胞培养物,所述载体用于掺入多核苷酸插入物。宿主细胞包括单个宿主细胞的后代,并且因为天然、偶然或故意的突变,所述后代不必须与原始的亲本细胞(在形态学或基因组DNA补体上)完全相同。宿主细胞包括用本发明的多核苷酸体内转染的细胞。术语“Fc区”用于定义免疫球蛋白重链C末端区域。“Fc区”可以是天然序列Fc区或变体Fc区。尽管免疫球蛋白重链的Fc区边界可变化,但是人IgG重链Fc区通常被定义为从位置Cys226的氨基酸残基或Pro230开始到其羧基端的一段。Fc区中残基的排序是如Kabat中的EU索引排序。Kabatetal.,SequencesofProteinsoflmunologicalInterest,5thEd.PublicHealthService,NationalInstitutesofHealth,Bethesda,Md.,1991。免疫球蛋白的Fc区通常含有两个恒定结构域CH2和CH3。本文使用“Fc受体”和“FcR”描述了结合抗体Fc区的受体。优选的FcR为天然序列人FcR。另外,优选的FcR是结合IgG抗体(γ受体)的FcR,并包括FcγRI、FcγRII和FcγRIII亚类的受体,包括这些受体的等位基因变体或者间接形式。FcγRII受体包括FcγRIIA(“激活受体”)和FcγRIIB(“抑制受体”),其具有主要在其胞浆区差异的类似的氨基酸序列。RavetchandKinet,1991,Ann.Rev.Immunol.,9:457-92;Capeletal.,1994,Immunomethods,4:25-34;和deHaasetal.,1995,J.Lab.Clin.Med.,126:330-41中综述了FcR。″FcR″也包括新生儿受体FcRn,其负责母体IgG到胎儿的转移(Guyeretal.,1976,J.Immunol.,117:587;andKimetal.,1994,J.Immunol.,24:249)。“补体依赖性细胞毒性”和″CDC″是指存在补体时靶标的溶解。补体系统的第一个组件(C1q)和与同种抗原复合的分子(例如抗体)的结合启动补体激活途径。为了评价补体活化,可进行例如Gazzano-Santoroetal.,J.Immunol.Methods,202:163(1996)中所述的CDC实验。“功能性Fc区”拥有天然序列Fc区的至少一个效应子作用。示范性的“效应子作用”包括C1q结合;补体依赖性细胞毒性(CDC);Fc受体结合;抗体依赖性细胞接到的细胞毒性(ADCC);吞噬作用;细胞表面受体(例如B细胞受体;BCR)的下调等。这类效应子作用通常要求Fc区与结合结构域(例如抗体可变结构域)组合并可使用本领域已知用于评估这类抗体效应子作用的多种实验评价。“天然序列Fc区”包含与天然存在的Fc区氨基酸序列相同的氨基酸序列。“变体Fc区”包含与天然序列Fc区通过至少一个氨基酸修饰而不同、但是维持天然序列Fc区至少一个效应子作用的氨基酸序列。优选地,与天然序列Fc区相比或与亲本多肽的Fc区相比,变体Fc区具有至少一个氨基酸取代,例如天然序列Fc区中或亲本多肽的Fc区中从约一个到约十个氨基酸取代,优选地从约一个到约五个氨基酸取代。本文的变体Fc区优选地与天然序列Fc区和/或与亲本多肽Fc区具有至少约80%的序列同一性,最优选与之有至少约90%的序列同一性,更优选与之有至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性。本文使用的“抗体依赖性细胞介导的细胞毒性”和“ADCC”是指细胞介导的反应,其中表达Fc受体(FcRs)的非特异性的细胞毒性细胞(例如天然杀伤(NK)细胞、中性粒细胞和巨噬细胞)识别靶细胞上的结合抗体,随后引起靶细胞裂解。感兴趣的分子的ADCC活性可以使用体外ADCC实验评估,例如描述于U.S.专利No.5,500,362或5,821,337中的实验。适用于这些实验的效应子细胞包括外周血单核细胞(PBMC)和NK细胞。或者或另外地,感兴趣的分子的ADCC活性可以体内评估,例如在如Clynesetal.,1998,PNAS(USA),95:652-656中公开的动物模型中评估。本文使用的“治疗”是用于获得有益的或所期望的临床结果的途径。就本发明的目的而言,有益的或所期望的临床结果包括,但不限于以下一种或多种:在头痛的任何方面改进,包括减轻严重性、缓和疼痛强度和其它相关症状、减少复发频率、提高患有头痛患者的生活质量和减少治疗头痛所需其它药物的剂量。对于偏头痛而言,其它相关症状包括,但不限于恶心、呕吐和对光、声音和/或运动敏感。对于丛集性头痛而言,其它相关症状包括,但不限于眼下方或周围肿胀、多泪、红眼、鼻漏或鼻充血和潮红的脸。“降低”头痛“发生率”表示任何降低的严重性(其可包括降低通常用于该病症的其它药物和/或治疗的需要和/或用量(例如暴露),所述其它药物包括例如用于偏头痛的麦角胺、双氢麦角胺或triptan)、持续时间和/或频率(包括例如在个体中延迟或提高到下次偶然发作的时间)。如本领域技术人员所理解的,个体可在它们对治疗的应答方面不同,同样,例如“减少个体中头痛发作的方法”表现了在合理期望(这类施用很可能在特定个体中导致这样的发病率降低)的基础上施用抗CGRP拮抗剂抗体。“改善”头痛或头痛的一种或多种症状表示与未施用抗CGRP拮抗剂抗体相比,头痛的一种或多种症状的减少或改进。“改善”也包括缩短或减少症状的持续时间。本文使用的“控制头痛”是指在个体中维持或降低头痛的一种或多种症状的严重性或持续时间或头痛发作的频率(与治疗前的水平相比)。例如,与治疗前水平相比,个体中头痛持续时间或严重性或发作频率被降低至少约10%、20%、30%、40%、50%、60%或70%之任一。本文使用的“延迟”头痛的发生是指延迟、妨碍、减缓、延缓、稳定和/或推迟疾病的进展。该延迟可以是不同长度的时间,取决于疾病史和、或被治疗的个体。如本领域技术人员所明白的,足够或显著的延迟可以有效地包括预防,因为个体不会发生头痛(例如偏头痛)。“延迟”症状发生的方法是与未使用该方法相比时,降低给定时间范围内发生症状的可能性和/或降低给定时间范围内症状程度的方法。这类比较典型地以临床研究为基础,使用统计学显著数量的受试者。头痛的“发生”或“发展”表示表示该病症的最初表现和/或随后的进展。头痛的发生是可检测的,并使用本领域公知的标准临床技术评价。然而,发生也表示不可检测的进展。就本发明的目的而言,发生或发展表示症状的生物学过程。“发生”包括发作、复发和发病。本文使用头痛的“发病”或“发作”包括初始发病和/或复发。本文使用的药物、化合物或药物组合物的“有效剂量”或“有效量”是足够产生有益的或期望的结果的量。对于预防性用途而言,有益的或期望的结果包括例如如消除或降低风险、减轻严重性或延迟疾病开始的结果,包括疾病的生物化学、组织学和/或行为症状,其并发症和在疾病发生时存在的中间病理学表型。对于治疗学用途而言,有益或期望的结果包括下述结果,例如降低疼痛强度、持续时间、或头痛发作频率和减少头痛引起的一种或多种(生物化学、组织学和/或行为)症状(包括其并发症和在疾病发生时存在的中间病理学表型)、提高该疾病患者的生活质量、减少治疗该疾病所需其它药物疗法的剂量、增强另一药物疗法的作用和/或延迟患者疾病的发展。有效剂量可以在一次或多次施用中被施用。就本发明的目的而言,有效的药物、化合物或药物组合物剂量是足够直接或间接完成预防性或治疗性治疗的用量。如临床语境中所理解的,有效的药物、化合物或药物组合物剂量可以与其它药物、化合物或药物组合物结合或不结合地达到。因此,在施用一种或多种治疗剂的语境中如果可以达到或达到了期望的结果,则可认为是“有效剂量”;单一剂量与一种或多种其它试剂组合时,如果可以达到或达到了期望的结果,则可认为是以有效的剂量提供的。“个体”或“受试者”是哺乳动物,更优选为人。哺乳动物还包括但不限于:农业动物、运动动物、宠物、灵长类、马、犬、猫、小鼠和大鼠。本文使用的“载体”表示一种构建体,其能够将一个或多个感兴趣的基因或序列递送进宿主细胞并优选在其中表达。载体的例子包括,但不限于病毒载体、裸DNA或RNA表达载体、质粒、粘粒或噬菌体载体、与阳离子冷凝剂结合的DNA或RNA表达载体、包裹在脂质体中的DNA或RNA表达载体,和某些真核生物细胞如生产者细胞。本文使用的“表达调控序列”是指指导核酸转录的核酸序列。表达调控序列可以是启动子(如组成型或诱导型启动子)或增强子。表达调控序列与待转录的核酸序列可操作地连接。本文使用的“可药用的运载体”或“可药用的赋形剂”包括任何下述材料,其与活性成分组合时允许该成分维持生物活性,并且对受试者的免疫体系是无反应性的。例子包括但不限于:任何标准的药物运载体,如磷酸盐缓冲的盐水溶液、水、乳剂(如油/水乳剂)和多种类型的湿润剂。用于气雾剂或肠胃外施用的优选稀释剂为磷酸盐缓冲的盐水或生理(0.9%)盐水。包含这类运载体的组合物通过公知的常规方法配制(参阅例如Remington′sPharmaceuticalSciences,18thedition,A.Gennaro,ed.,MackPublishingCo.,Easton,PA,1990;和Remington,TheScienceandPracticeofPharmacy20thEd.MackPublishing,2000)。本文使用术语“kon”旨在表示抗体与抗原的结合速率常数。本文使用术语“koff”旨在表示抗体从抗体/抗原复合物解离的速率常数。本文使用术语“KD”旨在表示抗体-抗原相互作用的平衡解离常数。本文使用术语“血管运动症状”旨在表示与血管舒张相关的病症,包括但不限于特别是由温度调节功能障碍导致的头痛(例如偏头痛、……其它)、热潮红、冷潮红(或瞬间热潮红(hotflashes))、失眠、睡眠紊乱、心境障碍、易激惹、大汗、寝汗、昼汗、疲劳等等。本文使用术语“面红”、“热潮红”和“瞬间热潮红”是本领域认可的术语,其表示体温偶发性紊乱,典型地由突发的皮肤潮红组成,通常伴随受试者的排汗。A.用于预防或治疗血管运动症状的方法一方面,本发明提供了用于在个体中治疗或预防至少一种血管运动症状如头痛(例如偏头痛)或热潮红的方法,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体或来自该抗体的多肽。另一方面,本发明提供了用于在个体中改善、控制、减少至少一种血管运动症状发作或延迟其发生或发展的方法,所述症状如头痛(例如偏头痛)或热潮红,所述方法包括对个体施用有效量的抗CGRP拮抗剂抗体。另一方面,本发明提供了用于在个体中改善、控制、减少头痛(例如偏头痛)发作或延迟其发生或发展的方法,包括对个体施用有效量的抗CGRP拮抗剂抗体与至少一种适用于治疗头痛的其它试剂的组合。这类其它试剂包括但不限于:5-HT激动剂和NSAID。例如,抗体和至少一种其它试剂可以伴随施用,即它们可以以足够接近的时间接近度施用从而允许它们个体的治疗作用重叠。例如,与抗CGRP抗体组合施用的5-HT激动剂或NSAID的量应当足以降低患者中头痛复发的频率,或产生与施用这些试剂中的一种而不存在其它时相比更长的持久作用。该步骤可用于治疗落入多种种类之任一中的头痛,包括:有先兆或无先兆的偏头痛;丛集性头痛;偏头痛性神经痛;久头痛;紧张性头痛;其它医学病症(例如感染或肿瘤引起的颅内压升高)导致的头痛;慢性发作性偏头痛;与结构损伤无关的多种头痛;与非血管性颅内病症相关的头痛;与物质施用及其停药相关的头痛;与非头感染相关的头痛;与代谢紊乱相关的头痛;与颅、颈、眼、耳、鼻、窦房结、牙、口或其它面部或颅结构病症相关的头痛;脑神经痛和神经干痛和去传入(deafferentiation)痛。本领域技术人员能够确定与抗CGRP抗体组合使用的特定试剂的合适剂量。例如,可以以从约0.01到约300mg的剂量施用舒马曲坦。当非肠胃外施用时,舒马曲坦的典型剂量为从约25到约100mg。通常优选约50mg,当肠胃外施用时,优选的剂量为约6mg。然而,这些剂量可以根据本领域的标准方法改变,从而将其针对特定患者或特定的组合治疗最优化。另外,例如塞来考昔可以以50和500mg之间的用量被施用。另一方面,本发明提供了用于在个体中改善、控制、减少热潮红发作或延迟其发生或发展的方法,包括对个体施用有效量的抗CGRP拮抗剂抗体与至少一种适用于治疗热潮红的其它试剂的组合。这类其它试剂包括,但不限于基于激素的治疗,所述激素包括雌激素和/或一些黄体酮。关于本文所述的所有方法,提及抗CGRP拮抗剂抗体时也包括包含一种或多种这些试剂的组合物。这些组合物可进一步包含本领域公知的合适赋形剂,如包括缓冲液的可药用赋形剂。本发明可单独使用或与其它常规治疗方法组合使用。抗CGRP拮抗剂抗体可以通过任何合适的途径施用给个体。本领域技术人员应当明白:本文所述的实施例不旨在限制,而是对可用技术的阐述。因此在一些实施方案中,抗CGRP拮抗剂抗体根据已知的方法施用给个体,例如静脉施用(例如作为推注施用或通过一段时间内的连续输注施用),通过肌内、腹膜内、脑脊髓内、皮下、关节内、舌下、滑膜内,通过吹入、椎观内、口内、吸入或局部途径。施用可以是全身性的(例如静脉施用)或局部的。可商业获得的用于液体制剂的喷雾器(包括喷射雾化器和超声喷雾器)适用于施用。液体制剂可直接喷雾,低压冻干粉末可以在重建后喷雾。或者,可以使用碳氟化合物制剂和压力定量气雾剂将抗CGRP拮抗剂抗体雾化,或作为低压冻干的和研细的粉末被吸入。在一个实施方案中,通过位点特异或靶向局部递送技术施用抗CGRP拮抗剂抗体。位点特异或靶向局部递送技术的例子包括抗CGRP拮抗剂抗体的多种可植入补给来源(depotsources)或局部递送导管,如输注导管、留置导管或套针、合成移植物、外膜覆膜(adventitialwraps)、分流器和支架或其它可植入的设备,位点特异的运载体、直接注射或直接应用。参阅例如PCT公开No.WO00/53211和U.S.专利No.5,981,568。抗CGRP拮抗剂抗体的多种制剂可用于施用。在一些实施方案中,抗CGRP拮抗剂抗体可以单独施用。在一些实施方案中,抗CGRP拮抗剂抗体和可药用的赋形剂可存在于多种制剂中。可药用的赋形剂是本领域已知的并是相对惰性的物质,其有助于药理学有效物质的施用。例如,赋形剂可以有形状或稠度,或作为稀释剂作用。合适的赋形剂包括但不限于稳定剂、湿润剂和乳化剂、不同渗量的盐、包胶剂、缓冲液和皮肤穿透促进剂。赋形剂以及用于肠胃外和非肠胃外药物递送的制剂公开于Remington,TheScienceandPracticeofPharmacy20thEd.MackPublishing(2000)中。在一些实施方案中,这些试剂被配制为用于通过(例如腹膜内、静脉内、皮下、肌内等)注射施用。因此,这些试剂可与可药用媒介如盐水、Ringer′s溶液、葡萄糖溶液等等组合。特定的给药方案(即剂量、时间和重复)将取决于特定的个体和该个体的医疗史。抗CGRP抗体可以使用任何合适的方法施用,所述方法包括注射(例如腹膜内、静脉内、皮下、肌内等)。抗CGRP抗体也可以如本文所述通过吸入施用。通常,对于抗CGRP抗体的施用而言,初始的候选剂量可以为约2mg/kg。就本发明的目的而言,典型的每日剂量可以从约3μg/kg到30μg/kg到300μg/kg到3mg/kg,到30mg/kg到100mg/kg或更多的范围内,取决于上述因素。例如可使用约1mg/kg、约2.5mg/kg、约5mg/kg、约10mg/kg和约25mg/kg的剂量。对于在若干天或更久的重复施用而言,根据病症持续治疗,直到发生期望的症状抑制或直到达到足够的治疗水平,例如降低疼痛。示范性的给药方案包括施用约2mg/kg的初始剂量,然后是约1mg/kg抗CGRP抗体的每周维持剂量,或然后是每隔一周约1mg/kg的维持剂量。然而,其它给药方法可以是有用的,取决于医生希望达到的药物代谢动力学衰变模式。例如,在一些实施方案中,考虑一周一到四次的给药。该疗法的过程容易地通过常规技术和实验检测。给药方案(包括使用的CGRP拮抗剂)可随时间变化。就本发明的目的而言,抗CGRP拮抗剂抗体的适当剂量取决于使用的抗CGRP拮抗剂抗体(或其组合物)、待治疗的头痛(例如偏头痛)类型和严重性、试剂是否就预防或治疗的目的被使用、先前疗法、患者的医疗史和对试剂的应答,以及主治医师的判断。典型地,临床医师会施用抗CGRP拮抗剂抗体,直到达到完成期望结果的剂量。剂量和/或频率可随治疗进程改变。经验性考虑(例如半衰期)通常有助于剂量的确定。例如,与人免疫系统相容的抗体(如人源化抗体或全人抗体)可用于延长抗体的半衰期和预防抗体被宿主的免疫系统攻击。施用频率可随着治疗进程确定和调整,并通常(但非必须)以头痛(例如偏头痛)的治疗和/或抑制和/或改善和/或延迟为基础。或者,抗CGRP拮抗剂抗体的持久连续释放制剂可以是适当的。用于达到持久释放的多种制剂和设备是本领域已知的。在一个实施方案中,可以按经验确定已经被给予一次或多次抗CGRP拮抗剂抗体施用的个体中抗CGRP拮抗剂抗体的剂量。个体被给予增加剂量的抗CGRP拮抗剂抗体。为了评估抗CGRP拮抗剂抗体的效力,可依照该疾病的指征来进行。根据本发明方法的抗CGRP拮抗剂抗体的施用可以是连续的或间断的,取决于例如受体的生理条件、施用目的是治疗性的还是预防性的,以及熟练医生已知的其它因素。抗CGRP拮抗剂抗体的施用可以在预选的时间段中基本上是连续的,或可以是一系列间隔的剂量,例如发生头痛(例如偏头痛)之前、期间或之后之任一;之前;期间;之前和之后;期间和之后;之前和期间;或发生头痛之前、期间和之后。施用可以在可能引起头痛的任何事件之前、期间和/或之后。在一些实施方案中,可存在多于一种抗CGRP拮抗剂抗体。可以存在至少一种、至少两种、至少三种、至少四种、至少物种不同的或更多的抗CGRP拮抗剂抗体。通常这些抗CGRP拮抗剂抗体可以具有彼此不会不利影响的互补活性。拮抗剂抗CGRP抗体也可以用于与其它CGRP拮抗剂或CGRP受体拮抗剂结合。例如,可使用一种或多种以下的CGRP拮抗剂:针对CGRP的抗反义分子(包括针对编码CGRP的核酸的抗反义分子)、CGRP抑制化合物、CGRP结构类似物、结合CGRP的CGRP受体的显性负相突变、抗CGRP受体抗体。抗CGRP拮抗剂抗体也可以与其它试剂结合使用,所述其它试剂起到增强和/或补充试剂有效性的作用。按下文所述,将根据本发明使用的抗CGRP拮抗剂抗体的治疗性制剂制备为低压冻干制剂或水性溶液的形式用于储存:将具有期望纯度的抗体与任选的可药用运载体、赋形剂或稳定剂混合(Remington,TheScienceandPracticeofPharmacy20thEd.MackPublishing(2000))。可接受的运载体、赋形剂或稳定剂在使用的剂量上对于受体是无毒的,并可包含缓冲液如磷酸、柠檬酸和其它有机酸;盐如氯化钠;抗氧化剂,包括抗坏血酸和甲硫氨酸;防腐剂(例如氯化十八烷基二甲基苄基铵;氯化六甲双铵;氯化苯甲烃铵、氯化苯乙铵;苯酚、丁醇或苯甲醇;对羟基苯甲酸烷基酯,如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯;儿茶酚;间苯二酚;环己醇;3-戊醇;和m-甲酚);低分子量(少于约10个残基)的多肽;蛋白质,如血清白蛋白、明胶或免疫球蛋白;亲水多聚体如聚乙烯吡咯酮;氨基酸如甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸或赖氨酸;单糖、二糖和其它碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂如EDTA;糖如蔗糖、甘露醇、海藻糖或山梨糖醇;成盐的反例子如钠;金属络合物(例如Zn-蛋白质络合物);和/或非离子型表面活性剂,如TWEENTM、PLURONICSTM或聚乙二醇(PEG)。通过本领域已知方法制备含有抗CGRP拮抗剂抗体的脂质体,所述方法例如描述于Epstein,etal.,Proc.Natl.Acad.Sci.USA82:3688(1985);Hwang,etal.,Proc.NatlAcad.Sci.USA77:4030(1980);和U.S.Pat.Nos.4,485,045和4,544,545中。具有增强的循环时间的脂质体公开于U.S.专利No.5,013,556中。尤其有用的脂质体可以通过反相蒸发法用脂质组合物产生,所述脂质组合物含有磷脂酰胆碱、胆固醇和PEG衍生的磷脂酰乙醇胺(PEG-PE)。通过将脂质体滤过确定孔径的滤器得到具有期望直径的脂质体。在胶体给药系统(例如脂质体、白蛋白微球、微乳剂、纳米颗粒和纳米胶囊)或大乳剂中,活性成分也可以被捕获在微胶囊中例如分别被捕获在羟甲基纤维素或明胶微胶囊和多聚(methylmethacylate)微胶囊中,所述微胶囊例如通过凝聚技术或通过界面聚合法制备。这类技术公开于Remington,TheScienceandPracticeofPharmacy20thEd.MackPublishing(2000)中。可制备缓释制剂。缓释制剂的合适例子包括含有抗体的固体疏水多聚体的半渗透性基质,所述基质是有形状物体(例如薄膜或微胶囊)的形式。缓释基质的例子包括聚酯、水凝胶(例如多聚(2-羟乙基-异丁烯酯)或多聚(乙烯醇))、多聚乳酸化合物(U.S.Pat.No.3,773,919)、L-谷氨酸共聚物和7乙基-L-谷氨酸盐、非降解性的乙烯-醋酸乙烯酯、降解性的乳酸-羟乙酸共聚物如LUPRONDEPOTTM(由乳酸-羟乙酸共聚物和醋酸亮丙瑞林组成的可注射微球)、乙酸异丁酸蔗糖酯和多聚-D-(-)-3-羟基丁酸。用于体内施用的配方必须是无菌的。这通过例如滤过无菌滤膜容易地实现。治疗性的抗CGRP拮抗剂抗体组合物通常被置于具有无菌接入口的容器(例如带有可被皮下注射针穿透的塞子的静脉注射溶液袋或瓶)中。根据本发明的组合物可以是用于口、肠胃外或直肠施用或通过吸入或吹入施用的单位剂型,如片剂、丸剂、胶囊、粉末、颗粒、溶液或悬浮液或栓剂。为了制备固体组合物如片剂,将主要的活性成分与药物运载体(例如常规的压片成分,如玉米淀粉、乳糖、蔗糖、山梨糖醇、滑石、硬脂酸、硬脂酸镁、磷酸二钙或树胶)和其它药物稀释剂(例如水)混合,形成含有本发明化合物或其无毒可药用盐的均相混合物的固体预配制组合物。当提到这些预配制组合物是均相的时,表示活性成分遍及组合物被均一地分散,从而组合物可以被容易地再分为等效的单位剂型,如片剂、丸剂和胶囊。然后将该固体预配制组合物再分为上述类型的单位剂型,其含有从0.1到约500mg的本发明活性成分。新组合物的片剂或丸剂可以被包被或者以其它方式复合,得到给予长效的优点的剂型。例如,片剂或丸剂可以包含内部剂量和外部剂量组分,后者是前者上外膜的形式。这两种组分可以被肠道层分开,所述肠溶层(entericlayer)作用在于抵抗胃中的崩解并允许内部组分完整地进入十二指肠或被延迟释放。多种材料可被用于这类肠溶层或包衣,这类材料包括大量多聚酸和多聚酸与如紫胶、鲸蜡醇和醋酸纤维素类材料的混合物。合适的表面活性剂尤其包括:非离子型试剂,例如聚氧乙烯山梨聚糖(例如TweenTM20、40、60、80或85)和其它山梨聚糖(例如SpanTM20、40、60、80或85)。含有表面活性剂的组合物应便利地包含0.05%和5%之间的表面活性剂,并可以在0.1%和2.5%之间。应当理解如果必需的话可添加其它成分,例如甘露醇或其它可药用的媒介。合适的乳剂可以使用可商业获得的脂肪乳剂来制备,所述脂肪乳剂例如IntralipidTM、LiposynTM、InfonutrolTM、LipofundinTM和LipiphysanTM。活性成分可被溶于预先混合的乳剂组合物中,或者其可溶于油(例如大豆油、红花油、棉籽油、芝麻油、玉米油或杏仁油)或通过将磷脂(例如卵磷脂、大豆磷脂或大豆卵磷脂)与水混合形成的乳剂中。应当理解可添加其它成分,例如甘油或葡萄糖,以调节乳剂的张力。合适的乳剂典型地含有多至20%的油,例如5%和20%之间。脂肪乳剂包含0.1和1.0Im之间、尤其是0.1和0.5Im之间的脂肪微滴,并具有5.5到8.0范围内的pH。乳剂组合物可以是通过将抗CGRP拮抗剂抗体与IntralipidTM或其组分(大豆油、卵磷脂、甘油和水)混合制备的组合物。用于吸入或吹入的组合物包括在可药用的、水性或有机溶剂或其混合物中的溶液和悬浮液和粉末。液体或固体组合物可含有上文公开的合适的可药用赋形剂。在一些实施方案中,通过口或鼻呼吸途径施用组合物用于局部或全身作用。优选地在无菌可药用溶剂中的组合物可以通过使用气体被喷洒。被喷洒的溶液可以从喷雾设备直接被呼吸,或喷雾设备可以与面罩、帷罩或间歇性正压呼吸机结合。溶液、悬浮液或粉末组合物可以从以适当方式递送配方的设备中(优选口或鼻地)被施用。头痛的诊断或评估是本领域充分确定的。评估可以根据受试者测量(例如症状的患者特征)来确定。例如,偏头痛可以基于以下标准诊断:1)头痛的偶发性发作持续4到72个小时;2)具有两种以下症状:单侧疼痛、博动、运动时加重,和中度或严重强度的疼痛;和3)以下症状之一:恶心或呕吐,和畏光或恐声(phonophobia)。Goadsbyetal.,N.Engl.J.Med.346:257-270,2002。治疗有效性可以通过本领域公知的方法评估。例如,可评估疼痛缓解。因此,在一些实施方案中,在施用抗CGRP抗体后1、2或几个小时后主观地观察到疼痛缓解。在一些实施方案中,在施用抗CGRP抗体后主观地观察头痛发作的频率。B.抗CGRP拮抗剂抗体本发明的方法使用抗CGRP拮抗剂抗体,所述CGRP拮抗剂抗体表示封闭、抑制或降低(包括显著地)CGRP生物活性的任何抗体分子,所述生物活性包括由CGRP信号转导介导的下游途径,例如受体结合和/或对CGRP的细胞应答的激发。抗CGRP拮抗剂抗体应显示以下特征中的任一种或多种:(a)结合CGRP;(b)封闭CGRP与其受体结合;(c)封闭或降低CGRP受体活化(包括cAMP活化);(d)抑制CGRP生物活性或下调由CGRP信号转导功能介导的下游途径;(e)预防、改善或治疗头痛(例如偏头痛)的任何方面;(f)提高CGRP的清除率;和(g)抑制(减少)CGRP合成、生产或释放。抗CGRP拮抗剂抗体是本领域已知的。参阅例如Tanetal.,Clin.Sci.(Lond).89:565-73,1995;Sigma(Missouri,US),产品编号C7113(clone#4901);Plourdeetal.,Peptides14:1225-1229,1993。就本发明的目的而言,抗体与CGRP以下述方式反应,所述方式抑制CGRP和/或CGRP信号转导功能介导的下游途径。在一些实施方案中,抗CGRP拮抗剂抗体识别人CGRP。在一些实施方案中,抗CGRP拮抗剂抗体与人α-CGRP和β-CGRP均结合。在一些实施方案中,抗CGRP拮抗剂抗体与人和大鼠CGRP结合。在一些实施方案中,抗CGRP拮抗剂抗体结合具有CGRP的氨基酸25-37的C末端片段。在一些实施方案中,抗CGRP拮抗剂抗体结合CGRP的氨基酸25-37中的C末端表位。适用于本发明的抗体可包括单克隆抗体、多克隆抗体、抗体片段(例如Fab、Fab′、F(ab′)2、Fv、Fc等)、嵌合抗体、双特异性抗体、杂缀合物抗体、单链(ScFv)、其突变体、包含抗体部分的融合蛋白(例如结构域抗体)、人源化抗体,和免疫球蛋白分子的包含所需特异性的抗原识别位点的任何其它经修饰的构型,包括抗体的糖基化变体、抗体的氨基酸序列变体和共价修饰的抗体。抗体可以是犬的、大鼠的、人的,或任何其它来源的(包括嵌合的或人源化的抗体)。在一些实施方案中,抗CGRP拮抗剂抗体是单克隆抗体。在一些实施方案中,抗CGRP拮抗剂抗体被人源化。在一些实施方案中,抗体是人的。在一些实施方案中,抗CGRP拮抗剂抗体是抗体G1(如本文所述)。在一些实施方案中,抗CGRP拮抗剂抗体包含表6所示抗体G1或G1变体的一个或多个CDR(例如一个、两个、三个、四个、五个或在一些实施方案中包含所有六个CDR)。还在其它实施方案中,抗CGRP拮抗剂抗体包含图5所示重链可变区的氨基酸序列(SEQIDNO:1)和图5所示轻链可变区的氨基酸序列(SEQIDNO:2)。在一些实施方案中,抗体包含经修饰的恒定区,例如本文所述是免疫惰性的恒定区。在一些实施方案中,恒定区如Eur.J.Immunol.(1999)29:2613-2624;PCT申请No.PCT/GB99/01441;和/或UK专利申请No.9809951.8中所述被修饰。在其它实施方案中,抗体包含人重链IgG2恒定区,所述恒定区包含以下突变:A330P331到S330S331(参考野生型IgG2序列的氨基酸排序)。Eur.J.Immunol.(1999)29:2613-2624。在一些实施方案中,抗体包含带有以下突变的IgG4恒定区:E233F234L235到P233V234A235。还在其它实施方案中,针对N连接的糖基化而言,恒定区不被糖基化(aglycosylated)。在一些实施方案中,通过突变寡糖附着残基(如Asn297)和/或侧翼残基(其为恒定区中N-糖基化识别序列的一部分),使得针对N连接的糖基化而言恒定区不被糖基化。在一些实施方案中,针对N连接的糖基化而言恒定区不被糖基化。可通过酶或通过在糖基化缺陷宿主细胞中表达使得针对N连接的糖基化而言恒定区不被糖基化。抗CGRP拮抗剂抗体对CGRP(例如人α-CGRP)的亲合力(KD)可以是约0.02到约200nM。在一些实施方案中,亲合力为下述任何:约200nM、约100nM、约50nM、约10nM、约1nM、约500pM、约100pM、约60pM、约50pM、约20pM、约15pM、约10pM、约5pM或约2pM。在一些实施方案中,亲合力少于下述任何:约250nM、约200nM、约100nM、约50nM、约10nM、约1nM、约500pM、约100pM或约50pM。测定抗体对CGRP的亲合力的一种方式是通过测量抗体的单功能Fab片段的亲合力。为了获得单功能的Fab片段,可以用木瓜蛋白酶切割抗体(例如IgG)或重组表达。可以通过装备有固定的链霉亲和素感受芯片(SA)的表面等离振子共振(Biacore3000TM表面等离振子共振(SPR)系统,Biacore,INC,PiscatawayNJ)使用HBS-EP电泳缓冲液(0.01MHEPES,pH7.4、0.15NaCl、3mMEDTA、0.005%v/v表面活性剂P20)测定抗体的抗CGRPFab片段的亲和力。可以在HBS-EP缓冲液中将生物素化的人CGRP(或任何其它CGRP)稀释为少于0.5ug/mL的浓度,并使用不同的接触时间将其注射越过个体芯片通道,以达到两种范围的抗原密度:用于详细动力学研究的50-200响应单位(RU)或用于筛选实验的800-1,000RU。再生研究显示25%v/v乙醇中25mMNaOH有效地去除了结合的Fab同时维持芯片上多于200个注射的CGRP活性。典型地,将纯化的Fab样品的连续稀释(针对0.1-10x评估的KD的浓度)以100μL/分钟注射1分钟,并允许至多2小时的解离时间。通过ELISA和/或SDS-PAGE电泳,使用已知浓度的Fab(通过氨基酸分析测定)作为标准测定Fab蛋白质的浓度。使用BlAevaluation程序,通过将数据整体与1∶1Langmuir结合模型(Karlsson,R.Roos,H.Fagerstam,L.Petersson,B.(1994).MethodsEnzymology6.99-110)拟合,同时获得动力学结合速率(kon)和解离速率(koff)。平衡解离常数(KD)值作为koff/kon计算。该方案适用于测定抗体对任何CGRP的亲合力,所述CGRP包括人CGRP、另一哺乳动物的CGRP(例如小鼠CGRP、大鼠CGRP、灵长类CGRP)以及不同形式的CGRP(例如α和β形式)。抗体的亲合力通常在25℃下测量,但是也可以在37℃测量。可以通过本领域已知的任何方法来制造抗CGRP拮抗剂抗体。免疫宿主动物的途径和时间表通常与如本文所进一步描述的、用于抗体刺激和生产的、确定的和常规的技术一致。用于生产人和小鼠抗体的一般技术是本领域已知的并在本文被描述了。本发明包括:任何哺乳动物受试者(包括人)或来自其中的生产抗体的细胞可以被加工,用作生产哺乳动物(包括人)杂交瘤细胞系的基础。典型地,用一定量的免疫原(包括本文所述的免疫原)腹膜内、肌内、口、皮下、脚掌内和/或皮内接种宿主细胞。可以使用Kohler,B.andMilstein,C.(1975)Nature256:495-497的或被Buck,D.W.,etal.,InVitro,18:377-381(1982)修饰的一般体细胞杂交技术,从淋巴细胞和无限增殖化骨髓瘤细胞制备杂交瘤。可以获得的骨髓瘤株系(包括但不限于X63-Ag8.653和来自SaIkInstitute,CellDistributionCenter,SanDiego,Calif.,美国的骨髓瘤株系)可用于杂交中。通常,该技术涉及使用本领域技术人员已知的促融剂(如聚乙二醇)或通过电手段融合骨髓瘤细胞和淋巴细胞。融合后将细胞从融合培养基中分离并在选择性生长培养基如次黄嘌呤-氨基蝶呤-胸腺嘧啶(HAT)培养基上培养,以消除未杂交的亲本细胞。可用本文所述的补充了血清或未补充血清的任何培养基lai培养分泌单克隆抗体的杂交瘤。作为细胞融合技术的另一选择,可以使用EBV无限增殖化B细胞生产本发明的抗CGRP单克隆抗体。如果需要,将杂交瘤扩展并亚克隆,并通过常规免疫测定步骤(例如放射免疫测定、酶免疫测定或荧光免疫测定)来测试上清液的抗免疫原活性。可用作抗体来源的杂交瘤包括生产对CGRP特异的单克隆抗体或其部分的亲本杂交瘤的所有衍生的后代细胞。可以使用已知步骤体外或体内培养生产这类抗体的杂交瘤。如果需要的化,可以通过常规免疫球蛋白纯化步骤(如硫酸铵沉淀、凝胶电泳、透析、色谱法和超滤)从培养基或体液中分离单克隆抗体。如果存在不期望的活性,可例如通过将制剂流过吸附剂并将期望的抗体从免疫原上洗脱或释放来去除,所述吸附剂由附着在固相上的免疫原组成。用人CGRP或含有靶氨基酸序列的片段免疫宿主动物能够得到一群抗体(例如单克隆抗体),所述靶氨基酸序列使用双功能试剂或衍生试剂与在要免疫的物种中是免疫原性的蛋白质缀合,所述蛋白质为例如钥孔虫戚血蓝素(keyholelimpethemocyanin)、血清白蛋白、牛甲状腺球蛋白或大豆胰蛋白酶抑制剂,所述双功能试剂或衍生试剂为例如马来酰亚胺苯甲酰硫代琥珀酰亚胺(maleimidobenzoylsulfosuccinimide)酯(通过半胱氨酸残基缀合)、N-羟基琥珀酰亚胺酯(通过赖氨酸残基)、丙烯醛、琥珀酸酐、SOCl2或R1N=C=NR,其中R或R1是不同的烷基。如果需要的话,可以对感兴趣的抗CGRP拮抗剂抗体(单克隆或多克隆)进行测序,随后可将多核苷酸序列克隆进载体中用于表达或繁殖。编码感兴趣的抗体的序列可以在宿主细胞中的载体中维持,然后可以将宿主细胞扩展或冷冻用于进一步的用途。或者,可将多核苷酸序列用于遗传操作,以“人源化”抗体或改善抗体的亲和力或其它特性。例如,恒定区可以被改造得更像人恒定区,从而如果抗体被用于临床试验和在人中治疗时避免免疫应答。可以期望遗传改造抗体序列,以获得对CGRP的更大亲和力和在抑制CGRP中的更强效力。本领域技术人员应当明白,可以对抗CGRP拮抗剂抗体进行一个或多个多核苷酸改变并仍然维持其对CGRP的结合能力。人源化单克隆抗体存在四个一般步骤。这些步骤为:(1)确定初始抗体轻和重可变结构域的核苷酸和预测的氨基酸序列(2)设计人源化抗体,即决定在人源化过程中使用何种抗体框架区(3)实际的人源化方法/技术和(4)人源化抗体的转染和表达。参阅例如U.S.专利Nos.4,816,567、5,807,715、5,866,692、6,331,415、5,530,101、5,693,761、5,693,762、5,585,089和6,180,370。包含来自于非人免疫球蛋白的抗原结合位点的大量“人源化”抗体分子已经被描述过,包括下述嵌合抗体,所述嵌合抗体具有与人恒定区融合的啮齿动物V区或经修饰的啮齿动物V区以及它们结合的互补性决定区(CDR)。参阅例如Winteretal.Nature349:293-299(1991),Lobuglioetal.Proc.Nat.Acad.Sci.USA86:4220-4224(1989),Shawetal.JImmunol.138:4534-4538(1987)和Brownetal.CancerRes.47:3577-3583(1987)。其它参考文献描述了在与适当的人抗体恒定区融合之前移植进人支持框架区(FR)的啮齿动物CDR。参阅例如Riechmannetal.Nature332:323-327(1988),Verhoeyenetal.Science239:1534-1536(1988)和Jonesetal.Nature321:522-525(1986)。另一参考文献描述了被重组修饰的啮齿动物框架区支持的啮齿动物CDR。参阅例如欧洲专利申请No.0519596。这些“人源化”分子被设计为最小化对啮齿动物抗人抗体分子的不期望的免疫应答,所述免疫应答限制了这些部分在人受体中治疗性应用的持续时间和有效性。例如,可以工程改造抗体恒定区,使得其为免疫惰性的(例如不引发补体裂解)。参阅例如PCT公开No.PCT/GB99/01441;UK专利申请No.9809951.8。还可以使用的人源化抗体的其它方法由Daughertyetal.,Nucl.AcidsRes.19:2471-2476(1991)和U.S.专利Nos.6,180,377;6,054,297;5,997,867;5,866,692;6,210,671和6,350,861和PCT公开No.WO01/27160中公开。再或者,可以通过使用可商业获得的小鼠获得完全的人抗体,所述小鼠已经被工程改造为表达特异的人免疫球蛋白蛋白质。被设计为生产更期望的(例如完全人抗体)或更有活力的免疫应答的转基因动物也可以用于产生人源化的抗体或人抗体。这类技术的例子为来自Abgenix,Inc.(Fremont,CA)的XenomouseTM和来自Medarex,Inc.(Princeton,NJ)的TCMouseTM。或者,可以使用本领域已知的任何方法重组制造和表达抗体。又或者,可以通过噬菌体展示技术重组制造抗体。参阅例如U.S.专利Nos.5,565,332;5,580,717;5,733,743;和6,265,150;和Winteretal.,Annu.Rev.Immunol.12:433-455(1994)。或可以使用噬菌体展示技术(McCaffertyetal.,Nature348:552-553(1990))从来自未免疫的供体的免疫球蛋白可变(V)结构域基因仓库中体外生产人抗体和抗体片段。根据该技术,将抗体V结构域在读码框内克隆进丝状噬菌体(如M13或fd)的主要或次要外壳蛋白中,并作为噬菌体颗粒表面上的功能性抗体片段展示。因为丝状颗粒含有噬菌体基因组的单链DNA拷贝,所以基于抗体功能特征的选择也导致选择编码显示这些特征的抗体的基因。因此,噬菌体模拟B细胞的一些特征。噬菌体展示可以以多种形式进行;综述参阅例如Johnson,KevinS.andChisweli,DavidJ.,CurrentOpinioninStructuralBiology3:564-571(1993)。可以使用若干种来源的V基因区段用于噬菌体展示。Clacksonetal.,Nature352:624-628(1991)从来自免疫小鼠脾中的V基因小量随机组合文库中分离的不同的抗噁唑酮抗体阵列。基本依照Marketal.,J.MoI.Biol.222:581-597(1991)或Griffithetal.,EMBOJ.12:725-734(1993)所述的技术可以构建来自未免疫的人供体的V基因仓库并分离针对不同抗原(包括自身抗原)阵列的抗体。天然免疫应答中,抗体基因以高速率累积突变(体细胞高度突变)。一些引入的改变会赋予更高的亲和力,并且在随后的抗原激发中优先地复制和分化展示高亲和力表面免疫球蛋白的B细胞。可以通过使用已知为“链改组(chainshuffling)”(Marks,etal.,Bio/Technol.10:779-783(1992))的技术模拟该天然过程。在该方法中,通过噬菌体展示获得的“原始”人抗体的亲和力可以如下被改进:用得自未免疫的供体的V结构域基因天然存在的变体仓库(仓库)连续地置换重链和轻链的V区域基因。该技术允许生产具有pM-nM范围内亲和力的抗体和抗体片段。制造非常大的噬菌体抗体仓库(也已知为“所有之母文库(themother-of-alllibraries)”)的策略已经由Waterhouseetal.,Nucl.AcidsRes.21:2265-2266(1993)描述。基因改组也可以用于从啮齿动物抗体中衍生人抗体,其中人抗体具有与初始的啮齿动物抗体相似的亲和力和特异性。根据该方法(其也被称作“表位印记”),通过噬菌体展示技术获得的啮齿动物抗体的重链或轻链V结构域基因被置换为人V结构域基因仓库,创建了啮齿动物-人嵌合体。在抗原上的选择导致能够重建功能性抗原结合位点(即表位支配(印记)配偶体的选择)的人可变区的分离。重复该过程从而置换剩余的啮齿动物V结构域时,获得人抗体(参阅1993年四月1日公开的PCT公开No.WO93/06213)。与通过CDR移植对啮齿动物抗体的常规人源化不同,该技术提供了完全的人抗体,其不具有啮齿动物来源的框架或CDR残基。显然,尽管上文的讨论仅涉及人源化的抗体,但是所讨论的一般性原则适用于定制用于例如犬、猫、灵长类、马和牛的抗体。还显而易见的是本文所述的人源化抗体的一个或多个方面(例如CDR移植、框架突变和CDR突变)可以组合。可按下文所述来重组制造抗体:首先将生产多种抗体或一种抗体的细胞从宿主动物中分离,获得基因序列,并使用该基因序列在宿主细胞(例如CHO细胞)中重组表达抗体。可使用的另一方法是在植物(例如烟草)或转基因乳中表达抗体序列。用于在植物或乳中重组表达抗体的方法已经被公开。参阅例如Peeters,etal.Vaccine19:2756(2001);Lonberg,N.andD.HuszarInt.Rev.Immunol13:65(1995);和Pollock,etal.,JImmunolMethods231:147(1999)。用于制造抗体衍生物(例如人源化的、单链的等)的方法是本领域已知的。免疫测定和流式细胞分选技术如荧光激活细胞分选术(FACS)也可以用于分离对CGRP特异的抗体。抗体可以结合与许多不同的运载体结合。运载体可以是活性的和/或惰性的。公知的运载体的例子包括聚丙烯、聚苯乙烯、聚乙烯、葡聚糖、尼龙、淀粉酶、玻璃、天然和经修饰的纤维素、聚丙烯酰胺、琼脂糖和磁石。就本发明的目的而言,运载体的特性可以是可溶的或不溶的。本领域技术人员会直到用于结合抗体的其它合适运载体,或应该能够使用常规实验确定。在一些实施方案中,运载体包括靶向心肌膜的部分。容易使用常规步骤(例如通过使用能够特异结合下属基因的寡核苷酸探针,所述基因编码单克隆抗体的重链和轻链)对编码单克隆抗体的DNA进行分离和测序。杂交瘤细胞左右这类DNA优选的来源作用。一旦被分离,可以将DNA置于表达载体(例如PCT公开No.WO87/04462中公开的表达载体)中,然后将其转染进宿主细胞中获得重组宿主细胞中单克隆抗体的合成,所述宿主细胞例如以其它方式不生产免疫球蛋白蛋白质的大肠杆菌细胞、猿猴COS细胞、中国仓鼠卵巢(CHO)细胞或骨髓瘤细胞。参阅例如PCT公开No.WO87/04462。DNA也可以被修饰,例如通过将同源鼠序列位置替换为人重链和轻链恒定结构域的编码序列(Morrisonetal.,Proc.Nat.Acad.Sci.81:6851(1984)),或通过将编码非免疫球蛋白多肽的序列的全部或部分与免疫球蛋白编码序列共价接合。以该方式制备“嵌合的”或“杂交的”抗体,其具有本文的抗CGRP单克隆抗体的结合特异性。可以使用本领域已知的方法鉴定或表征来自抗体的抗CGRP拮抗剂抗体和多肽,从而探测和/或测量CGRP生物活性的降低、缓和或中和。例如,也可以通过将候选试剂与CGRP孵育并监测任一种或多种以下特性来鉴定抗CGRP拮抗剂抗体:(a)结合CGRP;(b)封闭CGRP与其受体结合;(c)封闭或降低CGRP受体活化(包括cAMP活化);(d)抑制CGRP生物活性或由CGRP信号转导功能介导的下游途径;(e)预防、改善或治疗头痛(例如偏头痛)的任何方面;(f)提高CGRP的清除率;和(g)抑制(减少)CGRP合成、生产或释放。在一些实施方案中,通过将候选试剂与CGRP孵育并监测CGRP的结合和/或伴随的生物活性降低或中和来鉴定抗CGRP拮抗剂抗体或多肽。可以用经纯化的CGRP多肽,或用天然表达CGRP多肽或被转染以表达CGRP多肽的细胞进行结合测定。在一个实施方案中,结合测定是竞争性的结合测定,其中评价候选抗体与已知抗CGRP拮抗剂竞争结合CGRP的能力。该测试可以以多种形式进行,包括ELISA形式。在其它实施方案中,通过将候选试剂与CGRP孵育,并监测结合和伴随的对细胞表面上表达的CGRP受体活化抑制来鉴定抗CGRP拮抗剂抗体。在最初的鉴定后,可以通过生物测定进一步证实和精制候选抗CGRP拮抗剂抗体的活性,所述生物测定已知用于检验靶向的生物活性。或者,可以使用生物测定直接筛选候选者。例如,CGRP促进响应细胞中大量可测量的改变。这些改变包括但不限于:细胞(例如SK-N-MC细胞)中cAMP的刺激。也可以使用动物模型测量拮抗剂活性,例如测量由刺激大鼠隐神经诱导的皮肤血管扩张。Escottetal.,Br.J.Pharmacol.110:772-776,1993。可进一步使用头痛(例如偏头痛)的动物模型检验拮抗剂抗体或多肽的效力。Reuter,etal.,FunctionalNeurology(15)Suppl.3,2000。用于鉴定和表征抗CGRP拮抗剂抗体的方法中的一些在实施例中详细描述。可以使用本领域公知的方法表征抗CGRP拮抗剂抗体。例如,一种方法是鉴定其结合的表位,或“表位作图”。存在本领域已知的用于对蛋白质上的表位位置作图和表征的许多方法,包括解答抗体-抗原复合物的晶体结构、竞争测定、基因片段表达测定,和基于合成肽的测定,例如描述于Chapter11ofHarlowandLane,UsingAntibodies,aLaboratoryManual,ColdSpringHarborLaboratoryPress,ColdSpringHarbor,NewYork,1999中。在额外的例子中,可使用表位作图确定抗CGRP拮抗剂抗体结合的序列。表位作图可以从多种来源商业获得,例如PepscanSystems(Edelhertweg15,8219PHLelystad,荷兰)。表位可以是线性表位(即包含在单链氨基酸中)或通过氨基酸的三维相互作用形成的构型表位(其不必须包含在单链中)。多种长度(例如至少4-6个氨基酸长)的肽可以被分离或(例如重组地)合成,并用于与抗CGRP拮抗剂抗体的结合测定中。在另一例子中,抗CGRP拮抗剂抗体结合的表位可以通过使用来自CGRP序列的重叠肽并测定抗CGRP拮抗剂抗体的结合而在系统性筛选中确定。根据基因片段表达测定,随机地或通过特异的遗传构建使编码CGRP的开放读码框成为片段,并测定待所表达的CGRP片段与待检验的抗体的反应性。例如可以通过PCR生产基因片段,随后在存在放射性氨基酸的情况下体外转录和翻译为蛋白质。然后通过免疫沉淀和凝胶电泳测定抗体与放射性标记的CGRP片段的结合。也可以通过使用在噬菌体颗粒表面上展示的随机肽序列大文库(噬菌体文库)鉴定某些表位。或者,可以在简单的结合测定中测试确定的重叠肽片段文库对测试抗体的结合。在一个额外的例子中,可以进行抗原结合结构域诱变、结构域切换实验和丙氨酸扫描诱变,来鉴定表位结合所需的、充分的和/或必要的残基。例如,可以使用突变体CGRP进行结构域切换实验,其中CGRP多肽的多个片段已经被置换(切换)为来自密切相关的、但是抗原性不同的蛋白质(例如神经营养因子蛋白质家族的另一成员)的序列。可以通过评估抗体与突变体CGRP的结合,来评估特定CGRP片段对抗体结合的重要性。可用于表征抗CGRP拮抗剂抗体的又一方法是使用竞争测定法(其使用已知结合相同抗原的其它抗体,即CGRP上的多个片段)来确定抗CGRP拮抗剂抗体是否与其它抗体结合相同的表位。竞争测定法是本领域技术人员公知的。可以使用表达载体来指导抗CGRP拮抗剂抗体的表达。本领域技术人员熟悉使用表达载体体内获得外源蛋白质的表达。参阅例如U.S.专利Nos.6,436,908;6,413,942;和6,376,471。表达载体的施用包括局部或全身施用,包括注射、口施用、基因枪或插入导管施用和局部施用。在另一实施方案中,表达载体被直接施用至交感干或神经节,或施用进冠状动脉、心房、脑室或心包中。也可以使用含有表达载体或亚基因组多核苷酸的治疗性组合物的定向递送。受体介导的DNA递送技术描述于例如Findeisetal.,TrendsBiotechnol.(1993)11:202;Chiouetal.,GeneTherapeutics:MethodsAndApplicationsOfDirectGeneTransfer(J.A.Wolff,ed.)(1994);Wuetal.,J.Biol.Chem.(1988)263:621;Wuetal.,J.Biol.Chem.(1994)269:542;Zenkeetal.,Proc.Natl.Acad.Sci.USA(1990)87:3655;Wuetal.,J.Biol.Chem.(1991)266:338中。在基因治疗方案中,对局部施用而言,含有多核苷酸的治疗性组合物在约100mg到约200mgDNA的范围内被施用。在基因治疗方案中也可以使用约500ng到约50mg、约1μg到约2mg、约5μg到约500μg和约20μg到约100μgDNA范围内的浓度。可以使用基因递送媒介递送治疗性多...
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1