环境响应型多价态异喹啉-3-羧酸偶联物及其制备方法和应用与流程
本发明涉及异喹啉-3-羧酸偶联物,尤其涉及环境响应型多价态异喹啉-3-羧酸偶联物及其制备方法,本发明还涉及该环境响应型多价态异喹啉-3-羧酸偶联物在抗肿瘤中的应用,属于异喹啉-3-羧酸偶联物领域。
背景技术:
恶性肿瘤是多发性疾病,对人类健康造成了严重危害。发展恶性肿瘤的临床化疗药物一直是肿瘤研究的热点之一。异喹啉类生物碱广泛存在于自然界并具广谱的生物活性。自从1974年,kluepfel等从streptomyceslusitanus中分离到第一个具有抗肿瘤活性的四氢异喹啉天然产物naphthriydinomycin以来,异喹啉生物碱作为抗肿瘤剂的应用得到广泛关注(scott,j.d.;williams.r.m.chem.rev.2002,102,1669.)。其中ecteinascidin743于2007年被批准在欧洲上市用于治疗晚期软组织肉瘤(molinski,t.f.;dalisay,d.s.;lievens,s.l.;saludes,j.p.natrevdrugdiscov.2009,8,69.)。因此异喹啉类生物碱的研究成为抗肿瘤药物研发的热点之一,特别是在新药及其新药先导化合物发现中起着不可替代的作用。尽管异喹啉-3-羧酸表现出一定的抗肿瘤活性,但由于存在溶解度差、生物利用度低等缺陷,使得其无法很好地发挥抗肿瘤功能。现有的技术,如公布号为cn104211767a的中国发明专利申请公开了用寡肽agdv修饰异喹啉-3-羧酸,但是这样制得的异喹啉-3-羧酸衍生物在相对高的剂量下(1μm/kg)体内抗肿瘤的抑制率并不高。因此,有必要用新的技术进一步改善异喹啉-3-羧酸的抗肿瘤活性。
生物体内糖配体与蛋白之间可以通过多价效应的协同作用增强它们之间的亲和性、特异性,产生所谓的“多价效应”(multivalenteffect)或“簇 集效应”(clustereffect)。研究发现在细胞与细胞之间、细胞与毒素之间、细胞与病毒之间、细胞与细胞间质之间的吸附等生物过程中普遍存在这种多价态结合。生物系统中多价作用的强度可能比一个低分子量的配体与一个蛋白的单一作用或是他们几个单一作用的加和都高得多。公布号为cn101876658a(申请号:200910310366.8)的中国发明专利公开了多价性质使得细胞表面受体介导纳米载体内吞的效率显著提高。多价效应这一概念为设计新型药物分子提出了新方案。
肿瘤临床的化学治疗通常不容易获得满意疗效。在众多影响因素中,抗肿瘤药物的毒副作用至关重要。抗肿瘤药物在体内运输过程中会受到氧化还原物质等内源性刺激。氧化还原响应型药物就是人体内氧化还原反应作为刺激,来达到药物的智能释放。谷胱甘肽(gsh)是一种还原剂,能特异性地还原二硫键。其中最具有代表性的二硫键和巯基体系,二硫键在人体内广泛存在,对人体没有生理毒性,可以稳定存在于人体的血液环境中,但是在外界环境中含有一定量的具有还原性的巯基时,二硫键就会发生断裂。肿瘤组织细胞由于生长代谢比正常组织细胞快,消耗氧的量就高于正常细胞,因而肿瘤组织细胞含有的还原型谷胱甘肽的浓度就远高于正常组织细胞,当以二硫键键合在载体上的药物被运送肿瘤细胞时,就很容易被肿瘤细胞内大量的还原型谷胱甘肽还原,二硫键发生断裂而生成巯基,从而达到药物的靶向智能释放。
申请号为201410255238.9的中国专利公开了以β-环糊精为药物载体与七个有抗肿瘤活性的异喹啉-3-羧酸偶联得到优秀的抗肿瘤剂。但目前尚未见多个异喹啉这类具有抗肿瘤活性的生物碱通过二硫键偶联得到氧化还原响应的多价态化合物的合成及作为抗肿瘤剂的应用。
技术实现要素:
本发明的目的之一是提供一种具有抗肿瘤活性的氧化还原响应的多 价态异喹啉-3-羧酸偶联物;
本发明的目的之二是提供一种制备所述氧化还原响应的多价态异喹啉-3-羧酸偶联物的方法;
本发明的目的之三是提将所述的氧化还原响应的多价态异喹啉-3-羧酸偶联物应用于制备抗肿瘤药物。
为实现上述目的,本发明所采取的技术方案是:
一种具有良好抗肿瘤活性的氧化还原响应的多价态异喹啉-3-羧酸偶联物,其为式ⅰ所示的结构:
本发明进一步提供了一种制备所述式ⅰ所示结构的多价态异喹啉-3-羧酸偶联物的方法,包括:
(1)将异喹啉-3-羧酸与n-叔丁氧羰基三氨乙基胺进行缩合反应,得到下述式ⅱ所示的化合物:
(2)将式ⅱ所示的化合物脱去保护基得到式ⅲ所示的化合物:
(3)将式ⅲ所示的化合物与3,3’-二硫代丙二酸通过接肽的方式进行偶联,得到式ⅰ所示结构的多价态异喹啉-3-羧酸偶联物。
优选的,步骤(1)中在n,n-二甲基甲酰胺(dmf)溶液中,采用1-羟基苯并三唑(hobt),n,n'-二环己基碳二亚胺(dcc)将异喹啉-3-羧酸与n-叔丁氧羰基三氨乙基胺(tren)脱水缩合。
通过体外细胞毒实验,本发明分别评价了异喹啉-3-羧酸(4)、化合物(8)以及阳性药阿霉素三个化合物对于a2780、hela、hepg2、kb、mcf-7五株肿瘤细胞的细胞活性。实验结果显示,本发明的化合物8较母核异喹啉-3-羧酸(4)对肿瘤细胞的细胞毒作用有明显提高。
在体内小鼠移植性肿瘤模型中,本发明分别对母核异喹啉-3-羧酸(4)、本发明化合物(8)、阿霉素(dox)进行抗肿瘤评价。根据实验结果可见,本发明化合物(8)在2μmol/kg给药剂量下,抑瘤率为53.40%;与生理盐水组瘤重相比p<0.05,具有显著性差异;与母核异喹啉-3-羧酸(4)相比p<0.05,说明本发明化合物(8)在与母核(4)相同剂量下表现出优于母核的抗肿瘤活性。化合物(8)的剂量依赖性研究表明,在不同剂量下,各组瘤重之间相比,p值均小于0.05,并且化合物(8)在0.02μmol/kg给药剂量下的抗肿瘤活性与母核异喹啉-3-羧酸(4)在8μmol/kg的剂量下相当,p>0.05。这一结果表明,本发明的化合物(8)在低于母核异喹啉-3-羧酸400倍的剂量下达到与母核相当的抗肿瘤能力,表明化合物(8)是个优秀的抗肿瘤化合物。
本发明化合物(8)的化学结构中含有二硫键(s-s),其在还原环境中则会被还原剂(如还原型谷胱甘肽gsh)断裂,生成含有巯基(-sh)的还原产物,分子量为化合物(8)的一半,且极性发生改变。因此利用lc-ms 可以检测到当化合物(8)处于还原环境中化合物(8)的峰消失,在另一处则出现还原产物的新峰,并检测出相应的分子量。本发明化合物的体外还原响应释放实验结果说明本发明化合物(8)对gsh有良好的还原敏感响应性,药物对肿瘤环境具有刺激响应释放的能力。
本发明选用3,3’-二硫代丙二酸为连接臂,将四个异喹啉3-羧酸与通过三(2-氨基乙基)胺之偶联,形成异喹啉衍生物,不仅可以通过药物载体上多个药效团对病变位点的多价协同作用显著提高了抗肿瘤活性,而且可以通过二硫键对肿瘤环境氧化还原的响应,对药物进行智能靶向释放降低对正常组织的毒性。
附图说明
图1为本发明化合物(8)的合成路线。
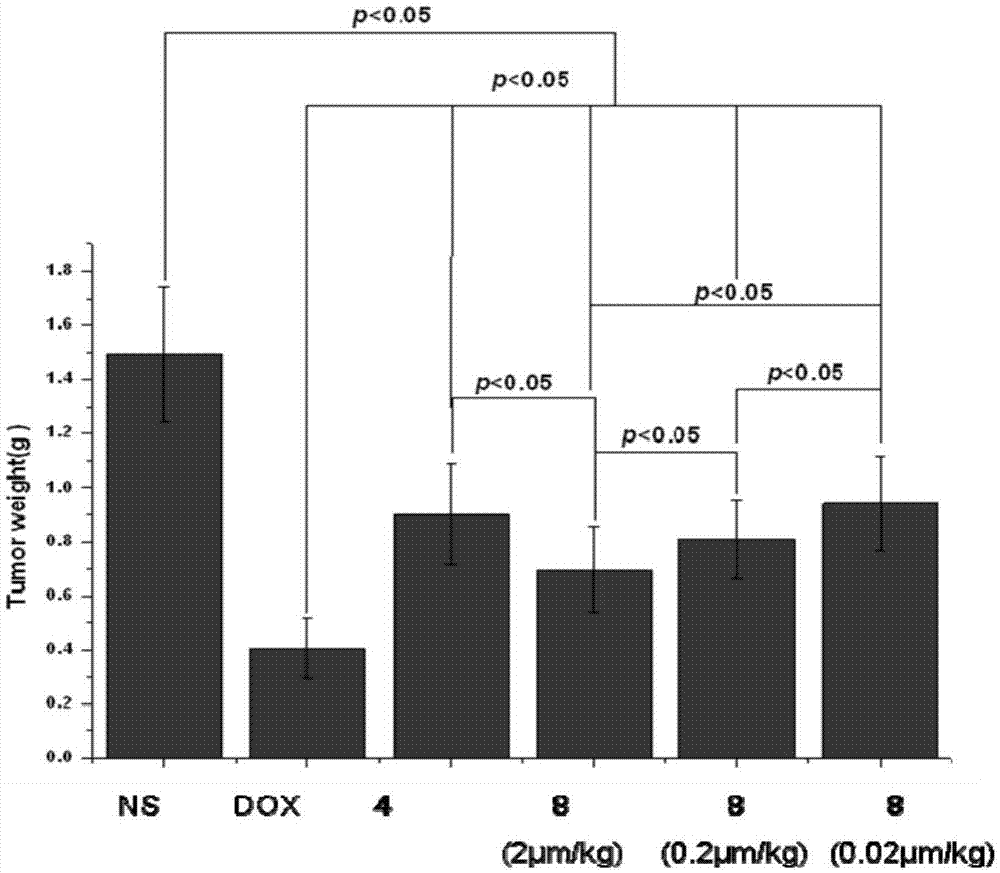
图2为本发明化合物(8)的体内肿瘤量效关系。
图3为本发明化合物(8)在体外还原响应的lc-ms图。
具体实施方式
下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随着描述而更为清楚。但是应理解所述实施例仅是范例性的,不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改或替换均落入本发明的保护范围。
实施例1制备(3s)-1,2,3,4-四氢异喹啉-3-羧酸(化合物1)
将hcl(320ml)和hcho(160ml)置于500ml茄瓶中,混合后加入l-phe(30.10g,182.45mmol),于油浴95℃反应24h后终止反应,冷却至室温。冰浴下用饱和naoh调节ph至6~7,有大量白色固体析出。过滤得白色固体(21.80g,67.54%)。esi-ms(m/z):178.1[m+h]+。
实施例2制备(3s)-1,2,3,4-四氢异喹啉-3-羧酸甲酯(化合物2)
在250ml茄瓶中加入甲醇(100ml),冰盐浴下逐滴滴加二氯亚砜(15ml),搅拌30min后,缓慢加入(3s)-1,2,3,4-四氢异喹啉-3-羧酸(1)(10.00g,56.50mmol),反应9-10h,将反应液抽干,得到白色固体(8.46g,78.40%)。esi-ms(m/z):192.0[m+h]+。
实施例3制备异喹啉-3-羧酸甲酯(化合物3)
在250ml茄瓶中加入(3s)-1,2,3,4-四氢异喹啉-3-羧酸甲酯(2)(4.23g,22.15mmol),冰盐浴下加入n,n-二甲基甲酰胺(50ml)将其溶解,加入高锰酸钾2.97g(18.79mmol),反应6h后加入乙醇(50ml)搅拌30min,移除溶剂,加入甲醇(30ml)复溶。柱层析分离纯化得到无色固体(858mg,24.56%)。esi-ms(m/z):188.0[m+h]+。
实施例4制备异喹啉-3-羧酸(化合物4)
在100ml茄瓶中加入异喹啉-3-羧酸甲酯(3)(858mg,4.59mmol),用少量甲醇溶解,冰盐浴下用2nnaoh调节ph=12,出现白色沉淀;待反应结束后,冰盐浴下用饱和khso4调节ph=7,旋除所有溶剂。用二氯甲烷和甲醇的混合溶液溶解,过滤,收集滤液。将滤液旋除后,得白色固体(481.7mg,60.69%)。esi-ms(m/z):171.9[m-h]-。
实施例5制备n-叔丁氧羰基三氨乙基胺(化合物5)
在100ml的双颈瓶中,滴加三氨乙基胺(5.1ml,34.23mmol)溶于30ml的二氧六环中,称取二碳酸二叔丁酯(1.2g,5.5mmol)溶于30ml的二氧六环中,然后缓慢滴加于反应液中,在n2保护下,反应17h。反应结束后,旋干反应液,旋干后得到的粗产物用柱层析分离纯化,得到透明油状物(940mg,69%)。esi-ms(m/z):246.2[m+h]+。
实施例6制备化合物(6)
在250ml茄瓶中加入异喹啉-3-羧酸(4)(415.2mg,2.4mmol),用dmf30ml溶解,n-叔丁氧羰基三氨乙基胺(5)(246.2mg,1mmol)溶于5mldmf后逐滴滴入茄瓶中,然后在油浴恒温50℃下加入dmtmm(664.1mg,2.4mmol),反应12h后,移除溶剂,然后柱层析分离纯化得到白色固体(353.6mg,63.6%)。esi-ms(m/z):557.2[m+h]+。1h-nmr(300mhz,dmso-d6):δ=9.097(s,2h),8.813(t,2h),8.448(s,2h),8.039(dd,j1=12.8hz,j2=4.5hz,4h),7.804(t,j=7.1hz,2h),7.710(t,j=7.2hz,2h),3.457(q,6h),2.752(t,j=6.2hz,6h),1.303(s,9h).13cnmr(75mhz,dmso-d6)δ/ppm=164.39,156.03,151.69,144.21,135.71,131.64,129.42,129.34,128.27,128.04,119.82,77.95,53.39,38.78,37.55,28.60。
实施例7制备化合物(7)
在100ml的茄瓶中加入化合物(6)(353.6mg,0.64mmol),滴加约2mltfa溶解,搅拌反应8h,待反应结束后,旋干溶剂,旋干后得到的粗产物用柱层析分离纯化得到白色固体(196.1mg,67.2%)。esi-ms(m/z):457.5[m+h]+。1h-nmr(300mhz,dmso-d6):δ=9.19(s,2h),8.92(t,2h),8.38(s,2h),8.06(dd,j1=18.0hz,j2=9.0hz,4h),7.77(t,j=7.5hz,2h),7.71(t,j=7.5hz,2h),3.45(q,4h),2.90(t,j=6.0hz,2h),2.75(t,j=6.0hz,6h).13cnmr(75mhz,dmso-d6)δ/ppm=164.71,151.76,144.07,135.63,131.60,129.45,129.36,128.22,128.08,119.89,54.08,40.82,40.55。
实施例8制备化合物(8)
在50ml的茄瓶中加入3,3’-二硫丙二酸(46.2mg,0.22mmol),hobt(58.1mg,0.43mmol),dcc(106.6mg,0.52mmol),用3mldmf溶解,置于冰浴下搅拌1h,撤去冰浴室温下搅拌1h,用2mldmf溶解化合物(7)(196.1mg,0.43mmol),然后逐滴滴入茄瓶中,反应12h。待反应结束后,过滤除去固体,旋干液体,旋干后得到的粗产物用柱层析分离纯化,得到白色固体(65.3mg,27.3%)。esi-ms(m/z):1086.4[m+h]+。1h-nmr(300mhz,dmso-d6):δ/ppm:=9.013(s,4h),8.777(t,j=5.4hz,4h),8.376(s,4h),7.983(d,j=8.4hz,4h), 7.953(d,j=9hz,4h),7.876(t,j=4.5,2h),7.728(td,j1=7.5hz,j2=1.2hz,4h),7.643(td,j1=8.1hz,j2=0.9hz,4h),3.500(q,j=5.4hz,8h),3.200(q,j=5.4hz,4h),2.876(t,j=7.2hz,4h),2.708(t,j=6hz,8h),2.649(t,j=6.6hz,4h),2.565(t,j=7.2hz,4h).13cnmr(75mhz,dmso-d6):δ/ppm:=170.50,164.53,151.57,144.00,135.54,131.52,129.31,129.26,128.17,127.96,119.83,53.44,53.33,37.48,37.42,35.47,34.28。
实验例1本发明化合物的体外细胞毒实验
本发明的化合物均用含0.5%dmso的培养基配制。共使用了a2780(人卵巢癌细胞)、hela(人宫颈癌细胞)、hepg2(人肝癌细胞)、mcf-7(人乳腺癌细胞)、kb(人口腔表皮癌细胞),五株肿瘤细胞。分别将生长状态良好、处于对数生长期的hela、a2780、hepg2、mcf-7、kb细胞按照4×105个/ml的密度接种于96孔板,每孔100μl。在37℃、5%co2条件下继续培养48小时,然后加入mtt溶液(5mg/ml)进行染色,每孔25μl。然后继续培养4小时,小心移除上清液,并加入100μl的dmso溶液。在摇床上震摇15分钟,使沉淀完全溶解。然后用酶联免疫检测仪检测各孔吸光度值,检测波长为490nm。计算抑瘤率及ic50。结果列入表1。
表1体外细胞毒活性(ic50±sdμm)a
a阿霉素用dox表示,n=6
在体外细胞毒实验中,分别评价了异喹啉-3-羧酸(化合物(4))、化合物(8)以及阳性药阿霉素三个化合物对于a2780、hela、hepg2、kb、mcf-7五株肿瘤细胞的细胞活性。实验结果显示,化合物(8)对a2780、hela、hepg2、kb、mcf-7五株肿瘤细胞的ic50值分别为17.17±1.19 μmol/l、22.30±3.33μmol/l、14.62±2.13μmol/l、11.54±0.92μmol/l、5.27±1.21μmol/l,母核异喹啉-3-羧酸(4)对a2780、hela、hepg2、kb、mcf-7五株肿瘤细胞的ic50值均大于100μmol/l。结果表明,本发明的化合物8较母核异喹啉-3-羧酸(4)对肿瘤细胞的细胞毒作用有明显提高。
实验例2荷s180小鼠移植性肿瘤模型评价化合物(8)体内抗肿瘤活性实验
无菌条件下取接种于icr小鼠7-10天的s180肉瘤细胞,加入适量生理盐水配制成瘤细胞悬液,细胞数为1.2×107个/ml,接种于健康雄性icr小鼠前肢腋皮下,每只小鼠注射0.2ml瘤液。健康icr雄性小鼠静息一天后,第二天在每只小鼠腋下接种s180细胞液0.2ml,并在接种后随机分为5组。肿瘤接种24h后,即第三天起,每组分别连续9天给药,实验组小鼠每日灌胃给药0.2ml本发明化合物的水溶液(2μmol/kg)。空白组小鼠每日灌胃给药0.2ml生理盐水。对照组小鼠每日腹腔注射0.2ml阿霉素水溶液(2μmol/kg)。第12天对各组小鼠脱椎处死,分别取出每只小鼠的肿瘤、心、肝、脾、肾、脑,并称重,最后统计化合物的抑瘤率。化合物的疗效以瘤重抑制百分率表示,计算如下:瘤重抑制率%=(1-给药组瘤重/空白组瘤重)×100%。实验结果见表2。
表2不同剂量化合物(8)对icr雄性小鼠肿瘤形成的影响的抗肿瘤活性
瘤重用mean±sdg表示,n=12;阿霉素用dox表示;a)与ns组相比,p<0.05;b)与dox组相比,p<0.05;c)与异喹啉-3-羧酸(4)相比,p<0.05;d)与化合物8(2μmol/kg)剂量相比,p<0.05;e)与化合物8(0.2μmol/kg)剂量相比,p<0.05;f)与异喹啉-3-羧酸(4)相比,p>0.05。
抑瘤率按公式计算:抑瘤率=(生理盐水组平均瘤重-实验组平均瘤重) /生理盐水组平均瘤重;统计方法采用独立样本t检验。
在体内小鼠移植性肿瘤模型中,分别对母核异喹啉-3-羧酸(4)、本发明化合物(8)、阿霉素(dox)进行抗肿瘤评价。得出以下结果:(1)阿霉素(dox)在2μmol/kg给药剂量下,抑瘤率为72.81%,与生理盐水组瘤重相比p<0.01,具有极显著性差异,说明小鼠s180移植性肿瘤模型建立成功。(2)异喹啉-3-羧酸(4)在8μmol/kg给药剂量下,抑瘤率为39.61%,与生理盐水组瘤重p<0.05,说明化合物异喹啉-3-羧酸(4)母核抗肿瘤活性。(3)本发明化合物(8)在2μmol/kg给药剂量下,抑瘤率为53.40%;与生理盐水组瘤重相比p<0.05,具有显著性差异;与母核异喹啉-3-羧酸(4)相比p<0.05,说明本发明化合物(8)在与母核(4)相同剂量下表现出优于母核的抗肿瘤活性。化合物(8)的剂量依赖性研究表明,在不同剂量下,各组瘤重之间相比,p值均小于0.05,并且化合物(8)在0.02μmol/kg给药剂量下的抗肿瘤活性与母核异喹啉-3-羧酸(4)在8μmol/kg的剂量下相当,p>0.05。这一结果表明,本发明的化合物(8)在低于母核异喹啉-3-羧酸400倍的剂量下达到与母核相当的抗肿瘤能力,表明化合物(8)是个优秀的抗肿瘤化合物。
实验例3本发明化合物的体外还原响应释放实验
化合物(8)的化学结构中含有二硫键(s-s),其在还原环境中则会被还原剂(如还原型谷胱甘肽gsh)断裂,生成含有巯基(-sh)的还原产物,分子量为化合物(8)的一半,且极性发生改变。因此利用lc-ms可以检测到当化合物(8)处于还原环境中化合物(8)的峰消失,在另一处则出现还原产物的新峰,并检测出相应的分子量。实验结果如图3所示,化合物(8)(m+na=1109.4173)在加入gsh后,二硫键断裂,化合物(8)的峰消失,生成还原产物(m+na=567.2136),说明化合物(8)对gsh有良好的还原敏感响应性,药物对肿瘤环境具有刺激响应释放的能力。
- 还没有人留言评论。精彩留言会获得点赞!