一种双二肽结构超分子凝胶因子及其制备方法与流程
本发明属于超分子自组装凝胶智能软材料技术领域,具体涉及一种双二肽结构超分子凝胶因子及其制备方法。
背景技术:
超分子凝胶是小分子化合物通过分子间氢键、范德华力、π-π堆砌以及配位键等非共价键作用,自组装形成线型、纤维状或带状微观结构,继而形成三维网络结构,将大量溶剂分子束缚在其网络空间中形成的宏观可视材料。超分子凝胶与聚合物凝胶相比,其凝胶因子间通过非共价键作用组装在一起,结合力较弱,对外界的刺激反应非常敏感且迅速,同时具有可逆性特点,因而在智能传感材料方面具有特殊应用价值。氨基酸具有丰富的官能团体系,易于进行设计、修饰和连接可响应或智能官能团,分子手性能够诱导凝胶因子自组装形成具有二级结构的螺旋纤维,作为凝胶构筑基团,能为超分子凝胶体系带来特殊的应用价值。
随着有机合成和超分子凝胶制备技术的不断进步,大批具有特殊响应功能的超分子凝胶材料应运而生,合成新型超分子凝胶因子并研究其凝胶性能是当今非常活跃的研究领域。中国专利201110310768.5公开了一种基于主客体作用的温敏性超分子凝胶,该凝胶态在40℃~70℃下受热,1min~30min可转化为溶胶态,具有可逆的温度敏感性特点,然而对金属离子、有机小分子等刺激不具有响应性,功能较为单一。中国专利201310208511.8公开了一种能够选择性识别氟离子的凝胶,DMSO凝胶体系遇到氟离子能够特异性变色,然而该凝胶因子在其它溶剂中不能发生自组装形成凝胶。Wang等人研究了基于4-吡啶甲醛与色氨酸反应制备得到的凝胶因子,该凝胶只能与单一金属离子形成凝胶,应用范围具有较大的局限性(Wang XJ,et al.Nanoscale,2016,8(12):6479-6483.)。
以上可知,开发多功能的超分子凝胶材料对于拓宽其应用范围,促进超分子凝胶材料在智能传感领域的应用,具有十分重要的意义。
技术实现要素:
针对现有的超分子凝胶材料只能对个别刺激进行响应,功能较为单一,应用范围受限的不足,本发明提供了一种双二肽结构超分子凝胶因子及其制备方法,该凝胶因子将长链疏水作用、π-π堆砌和氢键作用相结合,同时引入氨基酸作为手性诱导元素,能够在乙酸乙酯、四氢呋喃、DMF(二甲基甲酰胺)、DMSO(二甲基亚砜)等高极性溶剂中自组装形成凝胶软物质,吡啶、咪唑基团的引入又能为该凝胶因子与金属离子发生自组装提供条件,对温度、pH、应力刺激均具有良好的响应性,可用于传感器、缓释、吸附等多个领域。
本发明的技术解决方案是:
一种双二肽结构超分子凝胶因子,由双缬氨酸二胺衍生物与手性氨基酸芳烃衍生物通过缩合偶联反应得到,其结构通式为:
其中,R1选自中的一种,m为8~20;
R2选自中的一种;
R3选自中的一种。
一种双二肽结构超分子凝胶因子的制备方法,通过双缬氨酸二胺衍生物与手性氨基酸芳烃衍生物进行缩合偶联反应,反应方程式如下:
具体步骤如下:
步骤1,手性氨基酸芳烃衍生物的制备:将氨基酸与Na2CO3溶于蒸馏水中,室温搅拌溶解,缓慢滴加芳香族甲醛的甲醇溶液,室温搅拌3~6h,冷却至0~-5℃,缓慢加入NaBH4,搅拌反应8~12h,用乙酸调节pH至5~6,升至室温后继续搅拌1~3h,旋蒸后加入乙醇,50~80℃下加热溶解,过滤,旋蒸得到手性氨基酸芳烃衍生物;
步骤2,双二肽结构超分子凝胶因子的制备:配制手性氨基酸芳烃衍生物的四氢呋喃溶液,加入EDC.HCL(1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐)和HOBt(1-羟基苯并三唑),冷却至0~-5℃,加入双缬氨酸二胺衍生物,升温至25~50℃反应10~24h,在蒸馏水中沉淀,过滤,乙酸乙酯重结晶,得到双二肽结构超分子凝胶因子。
所述的双缬氨酸二胺衍生物为其中,R1选自中的一种,m为8~20。
步骤1中,所述的芳香族甲醛为4-吡啶甲醛、4-咪唑甲醛、苯甲醛中的一种,所述的氨基酸为选自缬氨酸、亮氨酸、色氨酸、丙氨酸、甘氨酸、苯丙氨酸中的一种。
步骤1中,所述的氨基酸与Na2CO3的摩尔比为1:0.4~1:0.6,蒸馏水与氨基酸的摩尔比为1:10~1:25,芳香族甲醛与氨基酸的摩尔比为1:1~1:3,NaBH4与氨基酸的摩尔比为1:3~1:5,乙醇与氨基酸的摩尔比为1:60~1:100。
步骤2中,所述的EDC.HCL与手性氨基酸芳烃衍生物的摩尔比为1:1.1~1:1.3,HOBt与手性氨基酸芳烃衍生物的摩尔比为1:1.1~1:1.3,蒸馏水与反应体系的体积比为1:30~1:50。
步骤2中,所述的手性氨基酸芳烃衍生物的四氢呋喃溶液的浓度为0.02~0.05mol/L。
本发明的双二肽结构超分子凝胶因子通过两种途径自组装形成凝胶:1)室温下一定浓度(10-50mg/mL)的凝胶因子混合溶液在超声作用下形成凝胶;2)一定浓度(10-50mg/mL)的凝胶因子在混合溶剂中经加热-冷却循环,形成凝胶。
与现有技术相比,本发明具有以下优点:
(1)通过长链二胺的疏水作用、芳烃的π-π堆砌和酰胺氢键作用的协同构筑,本发明的双二肽结构超分子凝胶因子在多数溶剂中都具有良好的凝胶形成能力,形成的凝胶热力学可逆,稳定性较好,对温度、pH、应力刺激均具有良好的响应性;
(2)手性氨基酸作为凝胶因子构筑基团,诱导凝胶因子在多种有机溶剂中自组装形成一维尺度的纤维结构,进而堆积形成多孔三维网状体系,因此本发明的双二肽结构超分子凝胶因子形成的凝胶具有较低的临界凝胶浓度和临界凝胶转变温度;
(3)凝胶因子中含有吡啶和咪唑官能团,具有良好的金属配位能力,可制成具有优异力学性能和光学性能的金属凝胶,在缓释、吸附金属离子等方面具有应用潜力。
附图说明
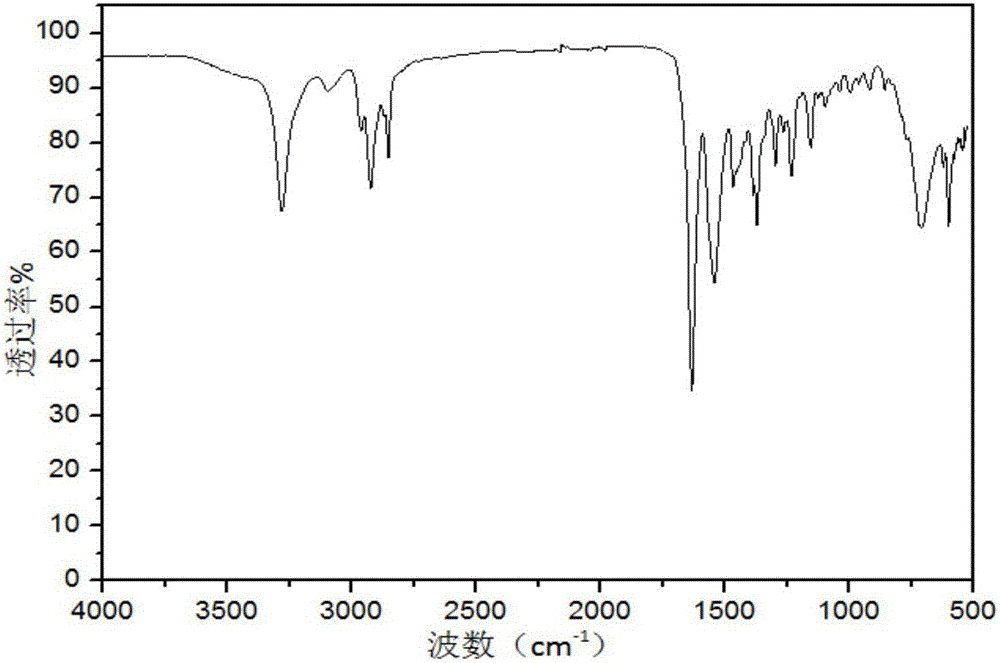
图1为实施例3制得的超分子凝胶因子的红外光谱图。
图2为实施例3制得的得超分子凝胶因子的核磁共振谱图。
图3为实施例3制得的超分子凝胶因子在乙醇/水为1:2时自组装冻干样品的扫描电镜图。
图4为实施例3制得的超分子凝胶因子在乙醇/水为1:2时自组装冻干样品的透射电镜图。
图5为实施例3制得的超分子凝胶因子在乙醇/水为1:2时自组装样品的刺激响应性转变图。
具体实施方式
下面结合实施例和附图对本发明作进一步详述。
本发明所述的双缬氨酸二胺衍生物参考美国专利【Bindl M,Herrmann R,KnaupG.U.S.Patent 9,126,896[P].2015-9-8.】制备得到,具体方法为:按缬氨酸:KOH:乙酰乙酸乙酯摩尔比为1:1:1.1加入装有分水器的四口烧瓶中,加入与缬氨酸摩尔比为1:8~1:10的乙酸异丙酯,加热回流反应至分水器中产生与缬氨酸摩尔比为1:1.5~1:1.8的水,得到烯胺化缬氨酸钾,补加与缬氨酸摩尔比为1:15~1:20的乙酸异丙酯,冷却,加入与缬氨酸摩尔比为1:1的特戊酰氯,室温搅拌0.5~1h,再冷却到5~10℃,加入与缬氨酸摩尔比为1:0.45~1:0.48的脂肪族长链二胺或芳香族二胺,与缬氨酸摩尔比为1:1.1~1:1.2的三乙胺和与缬氨酸摩尔比为1:12~1:15的乙酸异丙酯,10~15℃反应0.5~2h,加入与缬氨酸摩尔比为1:70~1:80的蒸馏水,并用盐酸酸化至pH为1-2,分液,弃去有机相,水相用NaOH调整pH至10-11,加入乙酸异丙酯萃取,分离有机相,水洗,重结晶得到双缬氨酸二胺衍生物。
所述的脂肪族长链二胺为碳原子数介于8~20的直链端基二胺中的一种,芳香族二胺为对苯二甲胺,间苯二甲胺中的一种。
实施例1:(R1为m=12,R2为R3为)
取5.860g(0.05mol)L-缬氨酸、3.300g(0.05mol)KOH、7.0ml(0.055mol)乙酰乙酸乙酯加入到装有搅拌器、温度计及分水器的500mL四口烧瓶中,继续加入50.0ml的乙酸异丙酯将其溶解,加热回流,直到分水器中生成大约1.6ml的水,得到烯胺化的缬氨酸钾。在上述烯胺化的缬氨酸钾体系中补加88.5ml乙酸异丙酯,将反应物冷却到10℃,加入6.029g特戊酰氯,再将温度升至17℃,搅拌45min,然后再冷却至10℃。将4.555g1,12-二氨基十二烷,5.768g三乙胺加入78.5ml乙酸异丙酯中,加入到上述反应体系中,室温下搅拌30min。将68.0ml水加入反应物,用约25.5ml浓盐酸将pH调至1-2,用分液漏斗分离出水相,用乙酸异丙酯洗涤,弃去有机相。用NaOH溶液将水相的pH调至10-11,加入适量乙酸异丙酯萃取,分离有机相,水洗,重结晶得十二亚甲基-1,12-双(N-L-缬氨酸),产率为60%。熔点:96~97℃。
FT-IR:ν(N–H),3281cm-1;ν(C–H),3092cm-1;ν(C=O),1632cm-1;ν(N–H),1540cm-1.
1H-NMR(500MHz,DMSO):δ=7.75(t,J=6Hz,2H),3.10-2.99(m,4H),2.88(d,J=6Hz,2H),1.85-1.80(m,2H),1.58(brs,4H),1.23(s,16H),0.85(d,J=6Hz,6H),0.78(d,J=6Hz,6H)ppm。
8.5mmol L-丙氨酸、4.25mmol Na2CO3两种原料加入三口烧瓶,加入15.0mL的蒸馏水,室温搅拌溶解,缓慢滴加含有8.5mmol4-吡啶甲醛的甲醇溶液,甲醇5mL,室温搅拌3h,冷却至0℃,缓慢加入10.2mmol NaBH4,搅拌反应12h,用乙酸调节反应混合物的pH至5~6,升至室温继续搅拌2h,旋蒸至无水,用40mL乙醇在50℃条件下加热溶解过滤,滤液旋蒸得到N-(4-吡啶甲基)-L-丙氨酸,产率为70%。
FT-IR:ν(NH),3375cm-1;ν(OH),3225cm-1;ν(CH),3019cm-1;ν(CH),2917cm-1;ν(C=O),1720cm-1;ν(C=N),1650cm-1.
1H-NMR(500MHz,DMSO):δ8.597~8.606(d,J=4.5Hz,2H),8.529~8.541(d,J=6Hz,2H),4.295~4.300(d,J=2.5Hz,2H),3.735~3.778(q,1H),1.525~1.539(d,J=7Hz,3H)。
取N-(4-吡啶甲基)-L-丙氨酸0.01mol溶解于200mL四氢呋喃中,加入0.013mol的EDC.HCL和0.013mol的HOBt,冷却至0℃,加入0.005mol的步骤a)中得到的双缬氨酸二胺衍生物,升温至50℃反应14h,倒入2000mL的蒸馏水中沉淀,过滤,乙酸乙酯重结晶双二肽结构超分子凝胶因子,产率为50%。
FT-IR:ν(NH),3215cm-1;ν(CH),3012cm-1;ν(CH),2987cm-1;ν(C=N),1683cm-1;ν(C=O),1690cm-1;ν(N-H),1580cm-1;ν(C=N),1430cm-1;ν(C-N),1292cm-1.
1H-NMR(500MHz,DMSO):δ8.568~8.580(d,J=6Hz,4H),7.927~8.068(m,4H),7.316~7.327(d,J=5.5Hz,4H),4.122~4.155(t,2H),3.556~3.828(dd,4H),2.981~3.088(m,4H),2.778~2.790(d,J=6Hz,2H),1.750~1.934(m,2H)1.350~1.361(brs,4H),1.193~1.233(s,16H),1.130~1.112(dd,J1=7,J2=15.5Hz,6H),0.830~0.912(dd,J1=7,J2=15.5Hz,12H)ppm.
反应方程式:
实施例2:(R1为m=12,R2为R3为)
十二亚甲基-1,12-双(N-L-缬氨酸)的制备方法同实施例1。
8.5mmolL-缬氨酸、4.25mmol Na2CO3两种原料加入三口烧瓶,加入8.0mL的蒸馏水,室温搅拌溶解,缓慢滴加含有8.5mmol苯甲醛的甲醇溶液,甲醇5mL,室温搅拌3h,冷却至0℃,缓慢加入10.2mmol NaBH4,搅拌反应12h,用乙酸调节反应混合物的pH至5~6,升至室温继续搅拌2h,旋蒸至无水,用40mL乙醇在50℃条件下加热溶解过滤,滤液旋蒸得到N-(苯甲基)-L-缬氨酸,产率为77%。
FT-IR:ν(NH),3575cm-1;ν(O-H),3400cm-1;-cm-1ν(-C=N-),1650cm-1;ν(-C=C-),1600cm-1;.
1H-NMR(500MHz,DMSO):δ7.2746~7.3243(q,4H),7.2011~7.2284(d,J=13.6Hz 1H),3.456~3.728(dd,4H),2.768~2.780(d,J=6Hz,1H),1.766~1.940(m,1H),0.910~0.933(d,J=11.5Hz,6H)ppm.
取N-(苯甲基)-L-缬氨酸0.01mol溶解于200mL四氢呋喃中,加入0.013mol的EDC.HCL和0.013mol的HOBt,冷却至0℃,加入0.005mol的步骤a)中得到的双缬氨酸二胺衍生物,升温至50℃反应14h,倒入2000mL的蒸馏水中沉淀,过滤,乙酸乙酯重结晶双二肽结构超分子凝胶因子,产率为58%。
FT-IR:ν(NH),3282cm-1;ν(CH),3012cm-1;ν(CH),2987cm-1;ν(C=C),1723cm-1;ν(C=O),1690cm-1;ν(N-H),1580cm-1;ν(C-N),1292cm-1.
1H-NMR(500MHz,DMSO):δ7.917~8.048(m,4H),7.2746~7.3243(q,8H),7.2011~7.2284(d,J=13.6Hz 2H),4.142~4.175(t,2H),3.456~3.728(dd,4H),2.982~3.089(m,4H),2.768~2.780(d,J=6Hz,2H),1.766~1.940(m,4H)1.350~1.361(brs,4H),1.193~1.233(s,16H),0.830~0.912(dd,J1=7,J2=15.5Hz,24H)ppm.
反应方程式:
实施例3:(R1为m=12,R2为R3为)
十二亚甲基-1,12-双(N-L-缬氨酸)的制备方法同实施例1。
8.5mmolL-缬氨酸、4.25mmol Na2CO3两种原料加入三口烧瓶,加入8.0mL的蒸馏水,室温搅拌溶解,缓慢滴加含有8.5mmol 4-吡啶甲醛的甲醇溶液,甲醇5mL,室温搅拌3h,冷却至0℃,缓慢加入10.2mmol NaBH4,搅拌反应12h,用乙酸调节反应混合物的pH至5~6,升至室温继续搅拌2h,旋蒸至无水,用40mL乙醇在50℃条件下加热溶解过滤,滤液旋蒸得到N-(4-吡啶甲基)-L-缬氨酸,产率为67%。
FT-IR:ν(NH),3385cm-1;ν(OH),3255cm-1;ν(CH),3069cm-1;ν(CH),2987cm-1;ν(C=O),1690cm-1;ν(C=C),1667;cm-1ν(C=N),1430cm-1.
1H-NMR(500MHz,DMSO):δ8.492~8.504(d,J=6Hz,2H),7.362~7.372(d,J=5Hz,2H),3.582~3.903(dd,2H),2.828~2.839(d,J=5.5,1H),1.879~1.944(m,1H),0.910~0.933(t,6H)ppm。
取N-(4-吡啶甲基)-L-缬氨酸0.01mol溶解于200mL四氢呋喃中,加入0.013mol的EDC.HCL和0.013mol的HOBt,冷却至0℃,加入0.005mol的步骤a)中得到的双缬氨酸二胺衍生物,升温至50℃反应14h,倒入2000mL的蒸馏水中沉淀,过滤,乙酸乙酯重结晶双二肽结构超分子凝胶因子,产率为58%。
IR(KBr,cm-1):ν(NH),3215cm-1;ν(C=C),1723cm-1;ν(C=O),1690cm-1;ν(N-H),1580cm-1;ν(C=N),1430cm-1;ν(C-N),1292cm-1,如图1所示。
1H-NMR(500MHz,DMSO):δ8.468~8.480(d,J=6Hz,4H),7.917~8.048(m,4H),7.319~7.330(d,J=5.5Hz,4H),4.142~4.175(t,2H),3.456~3.728(dd,4H),2.982~3.089(m,4H),2.768~2.780(d,J=6Hz,2H),1.766~1.940(m,4H)1.350~1.361(brs,4H),1.193~1.233(s,16H),0.830~0.912(dd,J1=7,J2=15.5Hz,24H)ppm,如图2所示。
反应方程式:
实施例4:(R1为m=12,R2为R3为)
十二亚甲基-1,12-双(N-L-缬氨酸)的制备方法同实施例1。
8.5mmolL-色氨酸、4.25mmol Na2CO3两种原料加入三口烧瓶,加入8.0mL的蒸馏水,室温搅拌溶解,缓慢滴加含有8.5mmol 4-咪唑甲醛的甲醇溶液,甲醇5mL,室温搅拌3h,冷却至0℃,缓慢加入10.2mmol NaBH4,搅拌反应12h,用乙酸调节反应混合物的pH至4~5,升至室温继续搅拌2h,旋蒸至无水,用40mL乙醇在50℃条件下加热溶解过滤,滤液旋蒸得到N-(4-咪唑甲基)-L-色氨酸,产率为61%。
取N-(4-咪唑甲基)-L-色氨酸0.01mol溶解于200mL四氢呋喃中,加入0.013mol的EDC.HCL和0.013mol的HOBt,冷却至0℃,加入0.005mol的步骤a)中得到的双缬氨酸二胺衍生物,升温至50℃反应14h,倒入2000mL的蒸馏水中沉淀,过滤,乙酸乙酯重结晶双二肽结构超分子凝胶因子,产率为55%。
反应方程式:
实施例5
凝胶因子在有机溶剂与水混合溶剂中自组装凝胶的性能测定。
取0.01g实施例3制得的凝胶因子加入凝胶管中,用移液枪向其中加入0.2mL的有机溶剂将凝胶因子溶解,随后向其中加入不同体积的水,混合均匀,用倒置试管法观察凝胶的形成。
表1为实例3制得的凝胶因子在有机溶剂与水混合溶剂中的凝胶性能
注:G表示凝胶,S表示溶解。
实施例6
凝胶因子室温下的最小凝胶浓度的测定。
取适量实例3制得的凝胶因子及一定比例的1mL混合溶剂,置于密封试管中,水浴加热使其完全溶解,将所得到的溶液置于室温下冷却至刚好形成凝胶时,此时的凝胶浓度,即为该室温下的最小凝胶浓度,结果如表2所示。
表2最小凝胶浓度
图3为凝胶因子在混合溶剂中通过自组装形成超分子凝胶的SEM图,从图中可以看出凝胶因子在混合溶剂中通过自组装形成纤维状结构,纤维结构进一步组装形成三维网状体系。图4为凝胶因子在混合溶剂中通过自组装形成超分子凝胶的TEM图,从图中可以看出凝胶因子在混合溶剂中通过自组装形成纤维网络体系,纤维直径在10nm左右。图5为凝胶因子在乙醇:水为1:2时组装形成的超分子凝胶的刺激响应性转变图,凝胶在加热、超声震荡、酸碱刺激下都会转变成溶胶,并具有可逆性。
- 还没有人留言评论。精彩留言会获得点赞!