一种关于银的有机‑无机杂化超分子聚合物、其制备方法及应用与流程
本发明属于光催化材料技术领域,具体涉及一种关于银的有机-无机杂化超分子聚合物、其制备方法及应用。
背景技术:
21世纪随着全球工业化进程的快速推进,环境污染问题日益严重,逐渐成为影响人类生存与发展的重要问题。光催化以其室温深度反应和可直接利用太阳能作为光源来驱动反应等独特性能,成为一种理想的环境污染治理技术和洁净能源生产技术。光催化反应是利用光能进行物质转化的一种方式,是光和物质之间相互作用的多种方式之一,是物质在光和催化剂同时作用下所进行的化学反应。光催化降解处理废水技术被认为是解决环境污染问题的最有应用前景的技术之一,已成为环境领域的研究热点。
目前,超分子作为一种新型分子功能材料不仅具有丰富的拓扑结构和多样的堆积方式,而且在有机废水的处理、光催化性能领域具有巨大的应用潜力。晶体工程涉及分子或化学基团在晶体中的行为、晶体的设计、结构与性能的控制以及晶体结构预测,它是实现从分子到功能材料的一条重要途径。而设计与合成结构新颖且在环境领域内具有潜在应用价值的超分子和无机-有机杂化材料是晶体工程学研究的两个重要的方面。
技术实现要素:
本发明的目的在于提供一种关于银的有机-无机杂化超分子聚合物,在用于降解亚甲基蓝染料中具有很好的光催化活性,该超分子聚合物以多络合点的N-杂环阳离子作为有机模板剂分别与硫氰酸银和碘化银进行分子组装得到,结构新颖,稳定性好。
本发明采用如下技术方案:
一种关于银的有机-无机杂化超分子聚合物,所述超分子聚合物的分子式为{[M-AP][Ag2Br3(SCN)]}n 或{[M-AP]2[Ag4I8]}n,其中,[M-AP]的结构式如下:
。
上述的关于银的有机-无机杂化超分子聚合物,所述{[M-AP][Ag2Br3(SCN)]}n的晶体属于单斜晶系,空间群为C2/c,晶胞参数为:a/Å=24.660(2),b/Å=12.8283(7),c/Å=15.5185(10),α=90.00°,β=104.995°(8),γ=90.00°;
所述{[M-AP]2[Ag4I8]}n的晶体属于正交晶系,空间群为Cmc21,晶胞参数为:a/Å=19.6895(4),b/Å=14.9590(4),c/Å=17.9275(3),α= 90.00°,β=90°,γ=90.00°。
上述的关于银的有机-无机杂化超分子聚合物,所述{[M-AP][Ag2Br3(SCN)]}n的重复单元[M-AP][Ag2Br3(SCN)]的结构式如式Ⅰ所示:
所述{[M-AP]2[Ag4I8]}n的重复单元[M-AP]2[Ag4I8]的结构式如式Ⅱ所示:
上述的关于银的有机-无机杂化超分子聚合物,所述{[M-AP][Ag2Br3(SCN)]}n由有机阳离子部分[M-AP]和无机阴离子部分[Ag2Br3(SCN)]构成,所述无机阴离子部分[Ag2Br3(SCN)]在构成超分子聚合物时的键接结构式如式Ⅰ(a)所示:
上述的关于银的有机-无机杂化超分子聚合物的制备方法,所述{[M-AP][Ag2Br3(SCN)]}n的制备方法包括以下步骤:
(1) 取硫氰酸银溶解后得溶液A1;
(2)取[M-AP] Br2溶解后得溶液B1;
(3)将溶液A1与溶液B1以滴加的方式进行混合,过滤取滤液,室温反应3-5天,洗涤,干燥,即得;
所述{[M-AP]2[Ag4I8]}n的制备方法包括以下步骤:
(i)取碘化银溶解后得溶液A2;
(ii)取[M-AP] Br2溶解后得溶液B2;
(iii)将溶液A2与溶液B2以滴加的方式进行混合,过滤取滤液,室温反应3-5天,洗涤,干燥,即得。
上述的关于银的有机-无机杂化超分子聚合物的制备方法,所用[M-AP] Br2通过以下方法合成得到:
取1,3-二(溴甲基)苯和4-氨基吡啶分别溶解后,混合,于80℃~100℃搅拌并回流9h~11h,冷却至室温,真空抽滤即得;
所用1,3-二(溴甲基)苯与4-氨基吡啶的摩尔比为1:2。
上述的关于银的有机-无机杂化超分子聚合物的制备方法,硫氰酸银与[M-AP] Br2的摩尔比为1:1;碘化银与[M-AP] Br2的摩尔比均为1:1。
上述的关于银的有机-无机杂化超分子聚合物的制备方法,步骤(1)中,在溶液A1中加入适量硫氰酸钾;步骤(i)中,在溶液A2中加入适量碘化钾。
上述的关于银的有机-无机杂化超分子聚合物的制备方法,步骤(3)中,溶液A1与溶液B1滴加的方式为:溶液B1滴加到溶液A1中,或者,溶液A1滴加到溶液B1中,优选方式为溶液B1滴加到溶液A1中;步骤(iii)中,溶液A2与溶液B2滴加的方式为:溶液B2滴加到溶液A2中,或者,溶液A2滴加到溶液B2中,优选方式为溶液B2滴加到溶液A2中;优选方式能够获得较高的产率。
上述的关于银的有机-无机杂化超分子聚合物的应用,所述超分子聚合物作为光催化剂用于光降解亚甲基蓝染料。
以下内容中,将{[M-AP][Ag2Br3(SCN)]}n记为超分子聚合物Ⅰ,将{[M-AP]2[Ag4I8]}n记为超分子聚合物Ⅱ。
本发明的有益效果如下:
本发明的制备原理为:以多络合点的N-杂环阳离子[M-AP]2+为模板剂与过渡金属Ag的卤化物或拟卤化物在适当的条件下进行自组装,从而得到超分子聚合物Ⅰ和Ⅱ。
1、本发明所述超分子聚合物,制备方法简单,易行,为催化降解废水中的有机染料提供了新的选择,同时拓展了超分子聚合物的应用价值。
2、本发明所述超分子聚合物的热稳定性比较好,耐热温度高达250℃以上,而且不溶于常见的有机溶剂,如乙腈,甲醇,乙醇,四氢呋喃等,有利于保持超分子聚合物结构的稳定性,适用的环境更为广泛,拓宽了该超分子聚合物的应用范围,同时本发明所述超分子聚合物在亚甲基蓝的光催化降解中,也表现出很好的催化作用。
附图说明
图1为超分子聚合物Ⅰ重复单元的结构图;
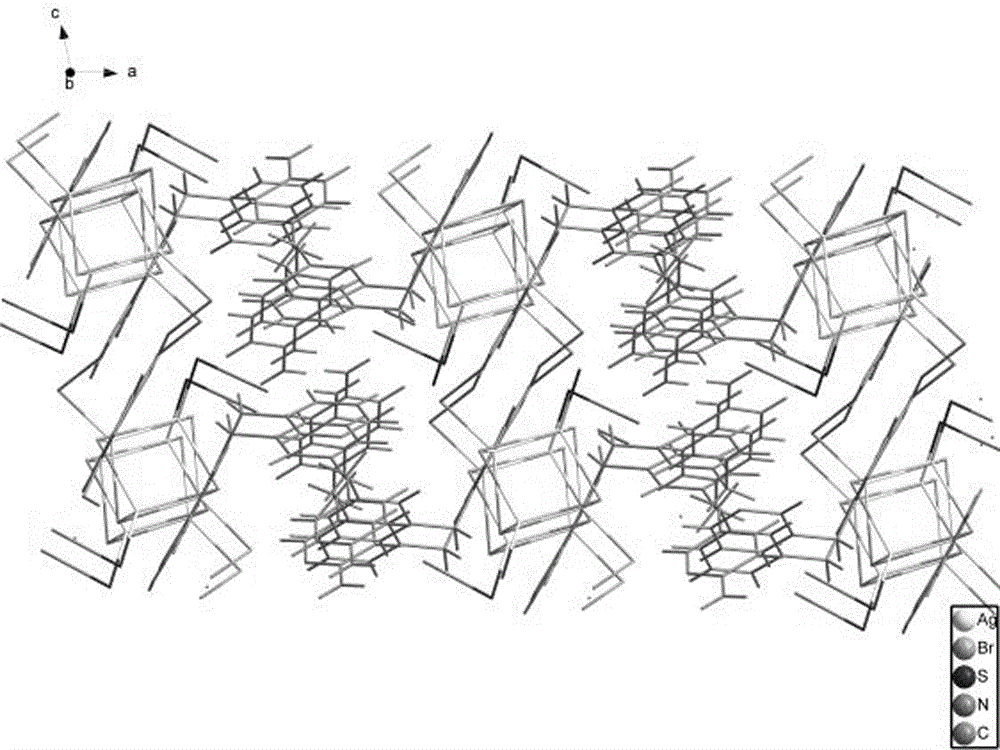
图2为超分子聚合物Ⅰ的堆积结构图;
图3为超分子聚合物Ⅱ重复单元的结构图;
图4为超分子聚合物Ⅱ的堆积结构图;
图5为超分子聚合物Ⅰ的紫外漫反射图;
图6为超分子聚合物Ⅱ的紫外漫反射图;
图7为超分子聚合物Ⅰ的PXRD(X-射线粉末衍射图);
图8为超分子聚合物Ⅱ的PXRD(X-射线粉末衍射图);
图9为超分子聚合物Ⅰ和Ⅱ的热稳定图;
图10为空白对照实验亚甲基蓝的吸光度变化图;
图11为超分子聚合物Ⅰ光催化降解亚甲基蓝的吸光度变化图;
图12为超分子聚合物Ⅱ光催化降解亚甲基蓝的吸光度变化图;
图13为超分子聚合物Ⅰ和Ⅱ光催化降解亚甲基蓝的浓度变化图。
具体实施方式
为了使本发明的技术目的、技术方案和有益效果更加清楚,下面结合附图和具体实施例对本发明的技术方案作出进一步的说明,但所述实施例旨在解释本发明,而不能理解为对本发明的限制,实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行,所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
本发明所述超分子聚合物Ⅰ和Ⅱ的制备方法中所用[M-AP] Br2,即1,3-二[(4-氨基吡啶基)-N-亚甲基]苯二溴盐,通过以下方法合成得到:
[M-AP] Br2的制备过程如下:
(1)取1,3-二(溴甲基)苯2.64g ( 0.01mol )于100mL圆底烧瓶内,加入30mL乙腈溶解;
(2)取4-氨基吡啶1.9g ( 0.02mol )于100mL小烧杯内,加入30mL乙腈,加热,磁力搅拌溶解;
(3)将上述4-氨基吡啶溶液加入1,3-二(溴甲基)苯溶液内,90℃条件下,磁力搅拌并回流10h;
(4)冷却至室温,真空抽滤,得高纯度的白色粉末状[M-AP] Br24.2 g。
[M-AP] Br2的产率为92%,反应式如式(1)所示:
(1)
以下制备超分子聚合物Ⅰ和Ⅱ的实施例所用[M-AP] Br2均通过上述合成方法得到。
实施例1:
超分子聚合物Ⅰ的制备过程如下:
(1)取硫氰酸银AgSCN 8.3 mg (0.05 mmol)放入玻璃瓶中,滴入蒸馏水0.25 mL ~0.50 mL(约5到10滴)后置于磁力搅拌器上搅拌,搅拌过程中加入3 mL乙腈和适量硫氰酸钾KSCN(摩尔比AgSCN:KSCN=1:4),乙腈和KSCN起到助溶作用以促进AgSCN溶解,至AgSCN完全溶解,得澄清溶液A1;
(2)取 [M-AP] Br2 22.6mg (0.05mmol)放入玻璃瓶中,加入蒸馏水0.25 mL ~0.50mL(约5到10滴),加热,震荡使其溶解,得溶液B1,溶液B1冷却至室温;
(3)将溶液B1滴加到溶液A1中,过滤取滤液,室温下静置3天后,得到白色菱形状晶体,干燥,得到超分子聚合物Ⅰ。
所得超分子聚合物Ⅰ的产率为75%(基于Ag计算得到)。
超分子聚合物Ⅰ的分子式为{[M-AP][Ag2Br3(SCN)]}n,结构式如图1所示,超分子聚合物Ⅰ{[M-AP][Ag2Br3(SCN)]}n 的晶体属于单斜晶系,空间群为C2/c,不对称重复单元包含一个[M-AP]2+有机阳离子和一个[Ag2Br3(SCN)]2-无机阴离子,如图1中的Ⅰ所示,图1中的Ⅰ(a)所示为无机阴离子部分的最小重复单元,呈类立方烷结构:在无机阴离子部分的骨架结构中,Ag有两种配位模式:Ag1分别与Br1、μ3-Br2、两个μ3-Br3配位,Ag2分别与SCN-、μ3-Br3、两个μ3-Br2配位;其中Br2和Br3均为三配位模式,同时与Ag1和Ag2配位形成类立方烷结构,而Br1和SCN-均为单配位模式,Br1与Ag1配位,SCN-与Ag2配位,Br1和SCN-均位于类立方烷的外部;Ag1-Br2和Ag1-Br3的键长分别为2.778 Å和2.824 Å, Ag2-Br2和Ag2-Br3的键长分别为2.793 Å和2.788 Å,Br2-Ag1-Br3和Br2-Ag2-Br3的键角分别是112.83°和113.48°,Ag1-Br2-Ag2和Ag1-Br3-Ag2的键角分别是67.09°和66.53°。由图1可知Ag1、Ag2、Br2、Br3形成类立方烷结构,Br1和SCN-位于类立方烷的外部。
图2所示为超分子聚合物Ⅰ的堆积结构图,展示出超分子聚合物Ⅰ的空间排布,重复单元间基本上依靠分子间相互作用结合在一起构成超分子聚合物Ⅰ,其中重复单元中的无机阴离子部分两两键接成一体。
对所得超分子聚合物Ⅰ进行元素及结构表征,结果如下:
元素分析(%)的理论值为:H: 2.69 ,C: 28.17, N: 8.94,实际测量值为:H:2.54,C:28.25,N:8.71 ;
红外主要吸收谱峰:3309(m), 3122(m), 2074(s), 1688(s), 1642(s), 1503(s), 1170(w), 849(m), 661(w), 589(w) cm-1;
紫外漫反射图,如图5所示,由图示信息可以计算出超分子聚合物Ⅰ的光学带隙Eg=1.62ev。
X-射线粉末衍射图如图7所示,其各项晶体学参数见表1:
表1 超分子聚合物Ⅰ的晶体学参数
超分子聚合物Ⅱ的制备过程如下:
(i)取碘化银AgI 11.8mg (0.05mmol)放入玻璃瓶中,滴入蒸馏水0.25 mL ~0.50mL(约5到10滴)后置于磁力搅拌器上搅拌,搅拌过程中加入3mL乙腈和适量碘化钾KI(摩尔比AgI:KI=1:4),乙腈和KI起到助溶作用以促进AgI溶解,至AgI完全溶解,得澄清溶液A2;
(ii)取 [M-AP] Br2 22.6mg (0.05mmol)放入玻璃瓶中,加入蒸馏水0.25 mL ~0.50mL(月5到10滴),加热,震荡使其溶解,得溶液B2,溶液B2冷却至室温;
(iii)将溶液B2滴加到溶液A2中,过滤取滤液,室温下静置3天后,得到黄色块状晶体,干燥,得到超分子聚合物Ⅱ。
所得超分子聚合物Ⅱ的产率为70%(基于Ag计算得到)。
分子式为:{[M-AP]2[Ag4I8]}n ,结构式如图3所示,超分子聚合物Ⅱ的不对称的重复单元由两个[M-AP]2+有机阳离子和一个[Ag4I8]4-无机阴离子构成,如图2所示。在无机阴离子骨架中,Ag有两种配位模式:Ag1分别与μ3-I1、两个μ3-I3、I2配位,Ag2分别与 μ3-I5,两个μ3-I3、I4配位,Ag3分别与μ3-I1、μ3-I3、μ3-I5、I6配位;其中,I1 、I3和I5均为三配位模式,与Ag1、Ag2和Ag3配位形成类立方烷结构,I2、I4和I6为单配位模式,I2与Ag1配位,I4与Ag2配位,I6与Ag3配位,I2、I4和I6均位于立方烷的外侧;此外,Ag1-Ag2的键长为3.083Å,Ag1-Ag3的键长为3.213Å,Ag3-Ag3的键长为3.173Å,Ag1-I1的键长为3.041 Å,Ag1-I2的键长为2.746 Å,Ag1-I3的键长为2.8795 Å,Ag2-I3的键长为2.9336 Å,Ag2-I4的键长为2.744Å,Ag2-I5的键长为2.935 Å,Ag3-I1的键长为2.8780Å,Ag3-I3的键长为2.8780 Å, Ag3-I5的键长为2.9787Å,Ag3-I6的键长为2.7801Å。在超分子聚合物Ⅱ重复单元的无机阴离子部分中,由四个Ag和八个I配位形成了类立方烷结构。
图4为超分子聚合物Ⅱ的堆积结构图,展示出超分子聚合物Ⅱ的空间排布,重复单元间依靠分子间相互作用力结合在一起构成超分子聚合物Ⅱ。
对所得超分子聚合物Ⅱ进行元素及结构表征,结果如下:
元素分析(%)的理论值为:H: 2.29 ,C: 22.17, N:6.01 ,实际测量值为:H:2.08,C:22.01,N:6.08
红外主要吸收谱峰:3409(w), 3282(w), 3074(w), 2218(w), 1642(s), 1503(s), 1449(m), 849(m), 761(m), 489(s) cm-1
紫外漫反射图,如图6所示,由图示信息可以计算出超分子聚合物Ⅱ的光学带隙Eg = 1.6 ev。
X-射线粉末衍射图,如图8所示,其各项晶体学参数见表2:
表2 超分子聚合物Ⅱ的晶体学参数
图9所示为实施例1所制备的超分子聚合物Ⅰ和Ⅱ的热稳定图,可以看出,超分子聚合物Ⅰ的耐热温度高达250℃,超分子聚合物Ⅱ的耐热温度高达300℃,两者的热稳定性较好,在实际的光降解应用中,适用范围更广。
实施例2:
超分子聚合物Ⅰ的制备过程如下:
(1)取AgSCN 8.3mg (0.05mmol)放入玻璃瓶中,滴入蒸馏水0.25 mL ~0.50mL(约5到10滴)后置于磁力搅拌器上搅拌,搅拌过程中加入3 mL乙腈和适量硫氰酸钾KSCN(摩尔比AgSCN:KSCN=1:4),乙腈和KSCN起到助溶作用以促进AgSCN溶解,至AgSCN完全溶解,得澄清溶液A1;
(2)取 [M-AP] Br2 22.6mg (0.05mmol)放入玻璃瓶中,加入蒸馏水0.25 mL ~0.50mL(约5到10滴),加热,震荡使其溶解,得溶液B1,溶液B1冷却至室温;
(3)将溶液A1滴加到溶液B1中,过滤取滤液,室温下静置3天后,得到白色菱形状晶体,干燥,得到超分子聚合物Ⅰ。
所得超分子聚合物Ⅰ的产率为63%(基于Ag计算得到)。
分子式为:{[M-AP][Ag2Br3(SCN)]}n, 红外主要吸收谱峰:3319(m), 3128(m), 2074(s), 1685(s), 1647(s), 1503(s), 1170(w), 849(m), 661(w), 589(w) cm-1。
超分子聚合物Ⅱ的制备过程如下:
(i)取AgI 11.8mg (0.05mmol)放入玻璃瓶中,滴入蒸馏水0.25 mL ~0.50mL(约5到10滴)后置于磁力搅拌器上搅拌,搅拌过程中加入3mL乙腈和适量碘化钾KI(摩尔比AgI:KI=1:4),乙腈和KI起到助溶作用以促进AgI溶解,得澄清溶液A2;
(ii)取 [M-AP] Br2 22.6mg (0.05mmol)放入玻璃瓶中,加入蒸馏水0.25 mL ~0.50mL(约5到10滴),加热,震荡使其溶解,得溶液B2,溶液B2冷却至室温;
(iii)将溶液A2滴加到溶液B2中,过滤取滤液,室温下静置3天后,得到黄色块状晶体,干燥,得到超分子聚合物Ⅱ。
所得超分子聚合物Ⅱ的产率为60%(基于Ag计算得到)。
分子式:{[M-AP]2[Ag4I8]}n ,红外主要吸收谱峰:3409(w), 3252(w), 3094(w), 2208(w), 1642(s), 1503(s), 1449(m), 849(m), 761(m), 489(s) cm-1
实施例3:
超分子聚合物Ⅰ的制备过程如下:
(1)取AgSCN 8.3mg (0.05mmol)放入玻璃瓶中,滴入蒸馏水0.25 mL ~0.50mL(约5到10滴)后置于磁力搅拌器上搅拌,搅拌过程中加入3 mL乙腈,乙腈起到助溶作用以促进AgSCN溶解,至AgSCN完全溶解,得澄清溶液A1;
(2)取 [M-AP] Br2 22.6mg (0.05mmol)放入玻璃瓶中,加入蒸馏水0.25 mL ~0.50mL(约5到10滴),加热,震荡使其溶解,得溶液B1,溶液B1冷却至室温;
(3)将溶液B1滴加到溶液A1中,过滤取滤液,室温下静置3天后,得到白色菱形状晶体,用蒸馏水、无水乙醇洗涤,干燥,得到超分子聚合物Ⅰ。
所得超分子聚合物Ⅰ的产率为54%(基于Ag计算得到)。
分子式:{[M-AP][Ag2Br3(SCN)]}n,红外主要吸收谱峰:3319(m), 3128(m), 2074(s), 1685(s), 1647(s), 1503(s), 1170(w), 859(m), 661(w), 589(w) cm-1。
超分子聚合物Ⅱ的制备过程如下:
(i)取AgI 11.8mg (0.05mmol)放入玻璃瓶中,滴入蒸馏水0.25 mL ~0.50mL(约5到10滴)后置于磁力搅拌器上搅拌,搅拌过程中加入3mL乙腈,乙腈起到助溶作用以促进AgI溶解,至AgI完全溶解,得澄清溶液A2;
(ii)取 [M-AP] Br2 22.6mg (0.05mmol)放入玻璃瓶中,加入蒸馏水0.25 mL ~0.50mL(约5到10滴),加热,震荡使其溶解,得溶液B2,溶液B2冷却至室温;
(iii)将溶液B2滴加到溶液A2中,过滤取滤液,室温下静置3天后,得到黄色块状晶体,干燥,得到超分子聚合物Ⅱ。
所得超分子聚合物Ⅱ的产率为47%(基于Ag计算得到)。
分子式:{[M-AP]2[Ag4I8]}n,红外主要吸收谱峰:3409(w), 3252(w), 3094(w), 2208(w), 1642(s), 1503(s), 1449(m), 849(m), 761(m), 489(s) cm-1。
应用试验1
将本发明实施例1所得超分子聚合物Ⅰ和Ⅱ作为光催化剂在紫外光条件下用于降解亚甲基蓝染料。
试验方法
(1)首先配制100 mL、浓度为1.0×10-5 mol L-1的亚甲基蓝溶液三份;
(2)称取实施例1所得超分子聚合物Ⅰ和Ⅱ各50 mg作为光催化剂分别加入到其中两份亚甲基蓝溶液中,另外一份亚甲基蓝溶液不加任何催化剂,做空白对照试验;
(3)为了确保吸附平衡,在暗处磁力搅拌30 min;
(4)然后用500 W高压汞灯照射,每间隔15 min,取3mL样品溶液进行分析,做样品溶液的紫外吸收光谱图;
(5)所得三份亚甲基蓝溶液的紫外吸收光谱图如图10,11,12所示,然后进行数据处理,得到如图13所示的浓度比值C/C0对时间t的曲线(C0为亚甲基蓝的初始浓度,C是时间为t时亚甲基蓝的浓度)。
从图10至13所示信息可以看出:
分别加入超分子聚合物Ⅰ和超分子聚合物Ⅱ的两份亚甲基蓝溶液随着光照时间的延长,最大吸收峰逐渐降低;
超分子聚合物Ⅰ作为光催化剂的亚甲基蓝溶液,在汞灯照射30 min后,超分子聚合物Ⅰ对亚甲基蓝的降解率为44% ,继续增加照射时间至80 min降解率为72%,90 min后降解率无明显增加;
超分子聚合物Ⅱ作为光催化剂的亚甲基蓝溶液,在汞灯照射30 min后,超分子聚合物Ⅱ对亚甲基蓝的降解率为33% ,继续增加照射时间至80 min降解率为60%,90 min后降解率无明显增加。
对比空白对照试验,超分子聚合物Ⅰ和Ⅱ在促进亚甲基蓝的降解方面发挥了积极作用,能够有效地促进亚甲基蓝的降解,其中,超分子聚合物Ⅰ对亚甲基蓝的降解效果优于超分子聚合物Ⅱ。
最后所应说明的是:上述实施例仅用于说明而非限制本发明的技术方案,任何对本发明进行的等同替换及不脱离本发明精神和范围的修改或局部替换,其均应涵盖在本发明权利要求保护的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!