用于分化的细胞重编程的小分子化合物组合、试剂盒及应用的制作方法
本发明涉及细胞生物学,药学,组织工程,再生医学等多个基础医学或临床医学领域,尤其涉及一种用于分化的细胞重编程的小分子化合物组合、试剂盒及应用。
背景技术:
:
间充质干细胞是一类具有多向分化潜能的成体干细胞,广泛存在于人体骨髓、脂肪、外周血液中,与胚胎干细胞或ips细胞相比,间充质干细胞具有更高的安全性、稳定性与低免疫原性,在骨与关节损伤、肿瘤、肝硬化、糖尿病、退行性疾病、神经损伤、老年痴呆及红斑狼疮等疾病的临床研究或临床治疗中已有较成熟的应用,具有巨大的产业价值,但存在数量稀少、来源有限、难以富集、获取过程复杂、受供体健康状态限制、细胞易老化、无法大量传代扩增等局限,因而未能广泛应用。胚胎干细胞与ips细胞可经过诱导获得间充质干细胞,但由于胚胎干细胞与ips细胞本身均存在伦理问题或安全隐患,因此未能广泛应用。
目前利用细胞转分化技术已经可以通过诱导分化的细胞如皮肤成纤维细胞获得其它类型的功能体细胞,如肌细胞、神经元、干细胞等。其中,采用小分子化合物及其组合诱导的直接转分化技术具备以下特点:①不导入外源性转录因子,不改变源细胞的基因结构,具有良好的安全性与稳定性,无免疫原性;②诱导系统较为稳定,易于质控,成本低廉;③诱导过程短,效率高,便于规模化生产。因此有望成为再生医学种子细胞研发及生产的基础技术。
传统的细胞转分化需要通过导入特定的外源性基因实现,有时还需要相应的小分子化合物或信号分子协同作用。文献已有较多采用特定外源性基因把某一分化的细胞诱导为另一功能性分化的细胞的报道。如文献已有采用bmp-2,bmp-7,lmp3单独或协同作用使皮肤成纤维细胞转分化为在体外、体内都具有骨形成作用的成骨细胞的报道。但导入外源性基因存在致瘤风险,并可能使目标细胞产生免疫原性,因而难以推广应用。2013年,邓宏魁报道仅采用小分子化合物或其组合可以实现鼠皮肤成纤维细胞重编程为神经细胞的转分化过程,并证实该细胞转分化技术具有诱导过程短、诱导系统稳定、易于质控、成本低、无外源性基因插入导致的致瘤风险、获得的目标细胞具有良好的安全性与稳定性且无免疫原性,具有潜在的临床应用价值与产业化前景。此后,申请号为201410075246.5的中国专利申请提供了一种把分化的细胞诱导转分化为神经干细胞的方法及其应用。具体地,该申请涉及采用组蛋白去乙酰化酶(hdacs)抑制剂、糖原合成酶激酶(gsk-3)抑制剂和转化生长因子β(tgf-β)信号通路抑制剂的组合,在正常生理低氧环境下诱导成纤维细胞、上皮细胞等分化的细胞转分化为具有良好多能性及传代稳定性的神经干细胞。申请号为201610213644.8的中国专利申请提供了一种诱导成纤维细胞转分化为心肌细胞的诱导培养基、方法及其应用,所述诱导培养基包含基础培养基和诱导小分子组合,所述诱导小分子组合为6tcfow或scfov,其中6为e61541、t为苯环丙胺、c为chir99021、f为毛喉素、o为dorsomorphin、w为iwr-1、s为sb431542、v为丙戊酸。该申请诱导培养基能够将成纤维细胞诱导转分化为心肌细胞。目前,通过采用单纯小分子化合物或其组合诱导人类分化的细胞如皮肤成纤维细胞获得施旺细胞(thomaec,etal,2014)、神经细胞(huw,etal,2015)、胰岛细胞(shengding,etal,2015)的成果已陆续见诸报道。
由于人类与小鼠存在约25%的基因差异,而将上述在小鼠细胞实验中获得成功的专利申请技术方案应用于人类细胞同类重编程的可行性不高;另一方面,由于采用同类细胞通过转分化获得不同目标细胞的具体理论基础与技术手段并不相同,采用上述技术方案并不能获得未见报道的其它类型分化的细胞。申请人采用上述报道的技术方案分别重复试验,既未能把应用于小鼠细胞的重编程技术方案成功应用于人的同类细胞重编程,也未能把人类分化的细胞诱导重编程为间充质干细胞。多种分化的细胞如皮肤成纤维细胞具有来源丰富、易于获取并易于在体外长期大量扩增培养的优点。目前利用细胞转分化技术已经可以把分化的细胞如皮肤成纤维细胞直接诱导为成肌细胞、神经元、肝细胞、成骨细胞等多种不同类型的功能细胞;或先诱导为多能干细胞后,再进一步定向诱导为相应的功能细胞。上述采用细胞转分化技术从某种特定分化的细胞如皮肤成纤维细胞直接或间接诱导获得的功能细胞已经不再保持源细胞的分子特征与功能,但获得了相应目标细胞的典型分子特征与细胞功能。目前,上述诱导性功能细胞已逐渐应用于疾病模型研究、临床治疗研究与组织工程研究。
传统的细胞转分化需要通过导入特定的外源性基因实现,有时还需要相应的小分子化合物、细胞因子或重组蛋白协同作用。文献已有较多采用特定外源性基因把某一分化的细胞诱导为另一功能性分化的细胞的报道。如文献已有采用bmp-2,bmp-7,lmp3单独或协同作用使皮肤成纤维细胞转分化为在体外、体内都具有骨形成作用的成骨细胞的报道。但导入外源性基因存在致瘤风险,并可能使目标细胞产生免疫原性,难以推广应用。2013年,邓宏魁报道仅采用小分子化合物或其组合可以实现鼠皮肤成纤维细胞重编程为神经细胞的转分化过程,并证实该细胞转分化技术具有诱导过程短、诱导系统稳定、易于质控、成本低、无外源性基因插入导致的致瘤风险、获得的目标细胞具有良好的安全性与稳定性且无免疫原性,具有潜在的临床应用价值与产业化前景。此后,申请号为201410075246.5的中国专利申请提供了一种把分化的细胞诱导转分化为神经干细胞的方法及其应用。具体地,该申请涉及采用组蛋白去乙酰化酶(hdacs)抑制剂、糖原合成酶激酶(gsk-3)抑制剂和转化生长因子β(tgf-β)信号通路抑制剂的组合,在正常生理低氧环境下诱导成纤维细胞、上皮细胞等分化的细胞转分化为具有良好多能性及传代稳定性的神经干细胞。申请号为201610213644.8的中国专利申请提供了一种诱导成纤维细胞转分化为心肌细胞的诱导培养基、方法及其应用,所述诱导培养基包含基础培养基和诱导小分子组合,所述诱导小分子组合为6tcfow或scfov,其中6为e61541、t为苯环丙胺、c为chir99021、f为毛喉素、o为dorsomorphin、w为iwr-1、s为sb431542、v为丙戊酸。该申请诱导培养基能够将成纤维细胞诱导转分化为心肌细胞。目前,通过采用单纯小分子化合物或其组合诱导人类分化的细胞如皮肤成纤维细胞获得施旺细胞(thomaec,etal,2014)、神经细胞(huw,etal,2015)、胰岛细胞(shengding,etal,2015)的成果已陆续见诸报道。
由于人类与小鼠存在约25%的基因差异,而将上述在小鼠细胞实验中获得成功的专利申请技术方案应用于人的同类细胞转分化可行性不高;另一方面,由于诱导同类细胞转分化获得不同目标细胞的具体理论基础与技术手段并不相同,申请人采用上述报道的技术方案分别重复试验,既未能把应用于小鼠细胞的转分化技术方案成功应用于人的同类细胞转分化,也未能把人类分化的细胞诱导转分化为间充质干细胞。
技术实现要素:
本发明提供了一种用于分化的细胞重编程的小分子化合物组合、试剂盒及应用。本发明通过利用小分子化合物组合按时序分阶段处理分化的细胞快速稳定程序化地获得大量间充质干细胞及其前体细胞、msc衍生细胞,及上述细胞的产物。
本发明首先提供一种小分子化合物组合,所述小分子化合物组合包括以下组分:tgf-β抑制剂,wnt/β-catenin激动剂,camp激动剂和pkc抑制剂。
进一步地,所述小分子化合物组合还包括rar激动剂,dnmt抑制剂,hmt抑制剂,组蛋白去甲基化酶抑制剂,ascorbate(抗坏血酸),jnk抑制剂,rock抑制剂和赖氨酸脱乙酰基酶抑制剂中的至少一种。
作为优选,所述小分子化合物组合包括按时序分阶段使用的第一阶段化合物和第二阶段化合物,所述第一阶段化合物为tgf-β受体抑制剂,wnt/β-catenin激动剂和camp激动剂;或所述第一阶段化合物为赖氨酸脱乙酰基酶抑制剂(lysinedeacetylasesinhibitors,kdacis),tgf-β受体抑制剂,wnt/β-catenin激动剂和camp激动剂;
所述第二阶段化合物包括tgf-β抑制剂,wnt/β-catenin激动剂,camp激动剂和pkc抑制剂。
进一步地,所述第二阶段化合物还包括rar激动剂,dnmt抑制剂,hmt抑制剂,组蛋白去甲基化酶抑制剂,ascorbate(抗坏血酸),jnk抑制剂,rock抑制剂和赖氨酸脱乙酰基酶抑制剂中的至少一种。
进一步地,所述tgf-β受体抑制剂为i型tgf-β受体抑制剂,所述camp激动剂为epac/rap1激动剂。
更进一步地,所述赖氨酸脱乙酰基酶抑制剂包括sodiumphenylbutyrate,butyrate,sodiumbutyrate,mc1568,ci994(tacedinaline),chidamide,cay10683(santacruzamatea),cudc-907,m344(histonedeacetylaseinhibitoriii),laq824(nvp-laq824,dacinostat),pracinostat(sb939),vpa,scriptaid,apicidin,lbh-589(panobinostat),ms-275,saha(vorinostat),trichostatin(tsa),psammaplina,pci-24781(abexinostat),rocilinostat(acy-1215),mocetinostat(mgcd0103),4-phenylbutyrate(4pb),splitomicin,srt1720,resveratrol,sirtinol,apha,ci-994,depudecin,fk-228,hc-toxin,itf-2357(givinostat),chidamide,rgfp966,phob,bg45,nexturastata,tmp269,cay10603,mgcd-0103,niltubacin,pxd-101(belinostat),pyroxamide,tubacin,ex-527,batcp,cambinol,mocpac,ptach,mc1568,nch51和tc-h106中的至少一种;
所述tgf-β受体抑制剂包括616452,ly2109761,pirfenidone,repsox(e-616452),sb431542,a77-01,tranilast,galunisertib(ly2157299),a8301,gw788388,itd-1,sd208,sb525334,ly364947,asp3029,d4476和sb505124中的至少一种;
所述pkc抑制剂包括go6983,ro31-8220mesylate,go6976和bisindolylmaleimidei(gf109203x)的至少一种;
所述wnt/β-catenin激动剂包括may-262611,chir98014,chir99021,licl,li2co3,td114-2,azd2858,azd1080,bio,kenpaullone,tws119,ly2090314,cbm1078,sb216763和ar-a014418中的至少一种;
所述camp激动剂包括epac/rap1激动剂,8-bromo-camp,dibutyryl-camp和sp-8-br-camps中的至少一种;
所述epac/rap1激动剂包括forskolin,ibmx,prostaglandine2(pge2),nkh477,8-pcpt-2′-o-me-camp,gsk256066,apremilast(cc-10004),roflumilast,cilomilast,rolipram和milrinone中的至少一种;
所述rar激动剂包括ttnpb,bexarotene,ch55,tamibarotene,retinol,am580,atra,13-cisra,vitamina及vitamina衍生物中的至少一种;
rock抑制剂包括:y-27632,y-276322hcl,thiazovivin,ripasudil(k-115),fasudil,fasudil(ha-1077)hcl,gsk429286a,rki-1447和pki-1313中的至少一种;
所述jnk抑制剂包括sp600125,jnkinhibitorix,as601245,as602801和jnk-in-8中的至少一种;
所述dnmt抑制剂包括rg108,thioguanine,5-aza-2'-deoxycytidine(decitabine),sgi-1027,zebularine,和5-azacytidine(aza)中的至少一种;
所述hmt抑制剂包括epz004777,epz5676,gsk503,bix01294和sgc0946中的至少一种;
所述组蛋白去甲基化酶抑制剂包括parnate(tranylcypromine),tranylcypromine(2-pcpa)hclsp2509,4sc-202,ory-1001(rg-6016),gskj1和gsk-lsd1中的至少一种。
作为优选,所述小分子化合物组合采用下列任一项:
vpa+chir99021+repsox+forskolin+go6983;
vpa+chir99021+sb431542+forskolin+go6983;
bio+sb431542+forskolin+go6983;
chir99021+repsox+forskolin+go6983+rolipram;
chir99021+repsox+forskolin+go6983+rolipram+sb431542;
chir99021+sb431542+forskolin+go6983+rolipram;
bio+sb431542+forskolin+go6983+rolipram;
vpa+chir99021+repsox+forskolin+go6983+nab;
chir99021+repsox+forskolin+go6983+nab;
vpa+bio+sb431542+rolipram+go6983;
bio+sb431542+rolipram+sp600125+go6983;
vpa+bio+sb431542+forskolin+go6983;
vpa+chir99021+sb431542+rolipram+go6983;
vpa+chir99021+repsox+forskolin+go6983+sp600125;
vpa+chir99021+repsox+forskolin+go6983+8-pcpt-2′-o-me-camp;
vpa+chir99021+repsox+forskolin+go6983+sb431542;
vpa+chir99021+sb431542+forskolin+go6983+tranilast;
vpa+chir99021+repsox+forskolin+go6983+sb431542+a8301;
vpa+chir99021+repsox+forskolin+go6983+rolipram+sb431542+a8301;
vpa+chir99021+repsox+forskolin+go6983+rolipram+sb431542;
vpa+chir99021+repsox+forskolin+go6983+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+rolipram;
vpa+chir99021+repsox+forskolin+go6983+rolipram+sb431542;
vpa+chir99021+repsox+rolipram+go6983;
vpa+chir99021+repsox+forskolin+go6983+parnate;
vpa+bio+repsox+forskolin+go6983;
chir99021+repsox+forskolin+go6983;
chir99021+repsox+rolipram+go6983;
chir99021+sb431542+forskolin+go6983;
chir99021+sb431542+rolipram+go6983;
chir99021+repsox+forskolin+sp600125+go6983;
chir99021+repsox+forskolin+sp600125+parnate+go6983;
bio+repsox+forskolin+go6983+rolipram;
bio+repsox+forskolin+go6983;
bio+repsox+forskolin+go6983+sp600125;
bio+sb431542+rolipram+go6983;
bio+sb431542+rolipram+go6983+sp600125;
bio+sb431542+rolipram+go6983+sp600125+parnate;
vpa+bio+sb431542+rolipram+go6983+sp600125;
vpa+chir99021+repsox+forskolin+go6983+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+sp600125+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125+am580;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+sp600125;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine+ascorbate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+ascorbate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+5-aza-2'-deoxycytidine+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125+am580+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine+ascorbate+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+ascorbate+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate+5-aza-2'-deoxycytidine+parnate。
所述小分子化合物组合为选自下述第一阶段化合物任意一项和第二阶段化合物任意一项的时序性小分子化合物组合,所述时序性小分子化合物组合所属的小分子化合物必须按一定的时序与相应的细胞或细胞产物接触;
作为进一步优选,第一阶段化合物可采用下列中的任一项:
chir99021+repsox;
bio+repsox;
bio+sb431542;
chir99021+sb431542;
bio+sb431542;
vpa+sb431542;
vpa+repsox;
vpa+chir99021+repsox;
vpa+chir99021+sb431542;
vpa+bio+repsox;
vpa+bio+sb431542;
chir99021+repsox+forskolin;
chir99021+repsox+rolipram;
bio+repsox+rolipram;
bio+sb431542+rolipram;
bio+sb431542+forskolin;
bio+repsox+forskolin;
chir99021+sb431542+rolipram;
chir99021+sb431542+forskolin;
vpa+chir99021+repsox+forskolin;
vpa+bio+repsox+forskolin;
vpa+chir99021+repsox+rolipram;
vpa+chir99021+sb431542+forskolin;
vpa+sb431542+rolipram;
vpa+repsox+rolipram;
vpa+sb431542+forskolin;
vpa+repsox+forskolin;
chir99021+repsox+forskolin+parnate;
vpa+chir99021+repsox+forskolin+parnate;
vpa+chir99021+repsox+parnate;
chir99021+repsox+parnate;
bio+repsox+parnate;
bio+sb431542+parnate;
chir99021+sb431542+parnate;
vpa+sb431542+parnate;
vpa+repsox+parnate;
vpa+repsox+forskolin+parnate;
chir99021+repsox+parnate;
vpa+repsox+parnate;
vpa+chir99021+repsox+forskolin+parnate;
第二阶段化合物可采用下列中的任一项:
vpa+chir99021+repsox+forskolin+go6983;
vpa+chir99021+sb431542+forskolin+go6983;
bio+sb431542+forskolin+go6983;
chir99021+repsox+forskolin+go6983+rolipram;
chir99021+repsox+forskolin+go6983+rolipram+sb431542;
chir99021+sb431542+forskolin+go6983+rolipram;
bio+sb431542+forskolin+go6983+rolipram;
vpa+chir99021+repsox+forskolin+go6983+nab;
chir99021+repsox+forskolin+go6983+nab;
vpa+bio+sb431542+rolipram+go6983;
bio+sb431542+rolipram+sp600125+go6983;
vpa+bio+sb431542+forskolin+go6983;
vpa+chir99021+sb431542+rolipram+go6983;
vpa+chir99021+repsox+forskolin+go6983+sp600125;
vpa+chir99021+repsox+forskolin+go6983+8-pcpt-2′-o-me-camp;
vpa+chir99021+repsox+forskolin+go6983+sb431542;
vpa+chir99021+sb431542+forskolin+go6983+tranilast;
vpa+chir99021+repsox+forskolin+go6983+sb431542+a8301;
vpa+chir99021+repsox+forskolin+go6983+rolipram+sb431542+a8301;
vpa+chir99021+repsox+forskolin+go6983+rolipram+sb431542;
vpa+chir99021+repsox+forskolin+go6983+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+rolipram;
vpa+chir99021+repsox+forskolin+go6983+rolipram+sb431542;
vpa+chir99021+repsox+rolipram+go6983;
vpa+chir99021+repsox+forskolin+go6983+parnate;
vpa+bio+repsox+forskolin+go6983;
chir99021+repsox+forskolin+go6983;
chir99021+repsox+rolipram+go6983;
chir99021+sb431542+forskolin+go6983;
chir99021+sb431542+rolipram+go6983;
chir99021+repsox+forskolin+sp600125+go6983;
chir99021+repsox+forskolin+sp600125+parnate+go6983;
bio+repsox+forskolin+go6983+rolipram;
bio+repsox+forskolin+go6983;
bio+repsox+forskolin+go6983+sp600125;
bio+sb431542+rolipram+go6983;
bio+sb431542+rolipram+go6983+sp600125;
bio+sb431542+rolipram+go6983+sp600125+parnate;
vpa+bio+sb431542+rolipram+go6983+sp600125;
vpa+chir99021+repsox+forskolin+go6983+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+sp600125+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125+am580;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+sp600125;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine+ascorbate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+ascorbate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate++5-aza-2'-deoxycytidine;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+5-aza-2'-deoxycytidine+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+5-aza-2'-deoxycytidine+sp600125+am580+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+5-aza-2'-deoxycytidine+ascorbate+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+sp600125+y27632+ascorbate++parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate+parnate;
vpa+chir99021+repsox+forskolin+go6983+ttnpb+epz004777+am580+y27632+ascorbate++5-aza-2'-deoxycytidine+parnate。
本发明还提供一种包含所述的小分子化合物组合的试剂盒或培养液/培养基,利用所述小分子化合物组合、试剂盒或培养液等能够用于在体内动员诱导或体外诱导制备间充质干细胞或以间充质干细胞为源细胞的再生医学种子细胞、组织工程种子细胞(如肝细胞、成骨细胞、软骨细胞等)及其产物,该小分子化合物组合可用于基础研究、临床治疗及组织工程产品研发与生产。
本发明还提供所述小分子化合物组合在诱导分化的细胞重编程中的应用,可应用本发明提供的小分子化合物组合诱导分化的细胞制备充质干细胞及其前体细胞、msc衍生细胞(由msc分化的细胞,如成骨细胞、软骨细胞、血管平滑肌细胞等),及上述细胞的产物。
本发明还提供所述小分子化合物组合在制备msc(间充质干细胞)及由msc分化的细胞中的应用。
msc及由msc分化的细胞与msc和/或由msc分化的细胞两种说法在意思上、范围上等同。
本发明还提供所述小分子化合物组合制备msc及由msc分化的细胞的方法。
本发明还提供通过所述小分子化合物组合制备得到的msc及由msc分化的细胞,本发明获得的间充质干细胞具有标准间充质干细胞的分子特性。所述间充质干细胞能够进行上万亿次的扩增,可大量生产,纯度高,具有良好的产业化前景,由msc分化的细胞也具有上述相同或相似优点。
本发明最后还提供所述小分子化合物组合制备的msc及由msc分化的细胞及细胞产物的应用,可用于基础研究、临床治疗、组织工程产品研发与生产,还可用于制备上述细胞的小分子化合物组合。
所述制备msc和/或由msc分化的细胞的方法如下:将分化的细胞与tgf-β受体的抑制剂,pkc的抑制剂,wnt/β-catenin的激动剂和camp的激动剂接触,经诱导处理,所述分化的细胞重编程为msc或msc分化的细胞(成骨细胞或软骨细胞或脂肪细胞)。
进一步地,将分化的细胞与tgf-β受体的抑制剂,pkc的抑制剂,wnt/β-catenin的激动剂和camp的激动剂,以及赖氨酸脱乙酰基酶抑制剂,rar激动剂,dna甲基转移酶(dnamethyltransferas,dnmt)抑制剂,组蛋白甲基转移酶(histonemethyltransferase,hmt)抑制剂,组蛋白去甲基化酶的抑制剂,ascorbate(抗坏血酸),jnk抑制剂和rock(rho-associatedproteinkinase)抑制剂中的至少一种接触。
更进一步地,所述分化的细胞首先进行活化预处理,所述活化预处理包括使分化的细胞与赖氨酸脱乙酰基酶抑制剂,tgf-β受体抑制剂,wnt/β-catenin激动剂和camp激动剂接触,该步骤中可省去赖氨酸脱乙酰基酶抑制剂;
更进一步地,所述接触诱导处理后将获得的细胞产物与细胞生长因子bmp4,pdgf-ab和b-fgf蛋白接触,采用细胞生长因子,有助于提高msc的得率。
所述分化的细胞来源于哺乳动物如人,其中所述分化的细胞包括成纤维细胞,上皮细胞,脂肪细胞或血液细胞,优选地所述分化细胞是成纤维细胞。
采用本发明提供的小分子化合物组合获得的间充质干细胞具有良好的多胚层多向分化潜能,传代稳定,扩增效率高。其工艺按时序分阶段流程化操作,便于精准操作与系统质控,易于标准化规模化生产。本发明能够不受供体来源限制地特异性或个体化获得大量间充质干细胞,有望开发成可用于骨与关节损伤、肿瘤、肝硬化、糖尿病、退行性疾病、神经损伤、老年痴呆及红斑狼疮等疾病基础研究或临床治疗的模型、技术或药物。
本发明的一些实施方案,具体小分子化合物的有效浓度如下,以下给出的浓度范围只是参考,可在此基础上做适应性修改,如果其他小分子替代以下小分子,浓度也可以做适应性调整。
forskolin浓度为2μm~20μm;repsox浓度为2~15um;chir99021浓度为1μm~10μm;vpa浓度为0.5mm~1.5mm;ttnpb浓度为3μm~8μm;am580浓度为0.03~0.08μm;epz004777浓度为3~8μm;go6983浓度为1~15μm;y27362浓度为3~15μm,l-ascorbinacid2-phosphate浓度为0.15~0.25mm;sp600125浓度为1~15μm;5-aza-2'-deoxycytidine浓度为0.5~15μm;tsa浓度为10nm~1μm。
本发明提供的小分子化合物组合,通过调整其组分,浓度,和作用时序获得的其他分化的细胞或干细胞,也属于所述小分子化合物组合的应用范围。
本发明的机理如下:本发明提供了能够提高细胞制备效率的小分子化合物组合,更进一步地提供按时序分阶段使用的小分子化合物组合,所述小分子化合物组合先对分化的细胞进行组蛋白乙酰化和甲基化处理,激活进入重编程的内源性启动子的转录,再进行诱导处理,使其最终重编程为间充质干细胞、成骨细胞、软骨细胞等。
与现有技术相比,本发明具有以下技术效果:本发明通过利用小分子化合物组合按时序分阶段处理分化的细胞快速稳定程序化地获得大量间充质干细胞及其前体细胞、msc衍生细胞,及上述细胞的产物,易于精准质控,标准化操作;所需样本量少,便于采集,来源广泛;便于规模化生产或个性化制备间充质干细胞及相关产品,可广泛应用于基础医学研究、临床治疗及组织工程产品研发,具有产业化前景。
附图说明
图1为通过小分子化合物诱导人源皮肤成纤维细胞向间充质干细胞重编程的细胞形态图;
图2为对重编程获得的间充质干细胞,进行标准的间充质干细胞表面标志物的流式方法检测结果图;
图3为对重编程的间充质干细胞分化多能性的检测结果图;
图4为检测重编程的间充质干细胞对t细胞的免疫抑制能力图;
图5为在免疫缺陷小鼠体内移植重编程的间充质干细胞,治疗小鼠股骨缺损的结果图;
图6为重编程获得的间充质干细胞的长期传代的细胞增值能力和干性的检测结果图。
图7为对重编程的间充质干细胞的成瘤性检测结果图;
图8为小分子化合物诱导人源皮肤成纤维细胞向成骨细胞转分化的细胞形态图;
图9为对获得成骨细胞的转分化效率和细胞纯度的鉴定结果图;
图10为在免疫缺陷小鼠体内移植转分化的成骨细胞治疗小鼠股骨缺损结果图。
具体实施方式
下面结合附图和具体实施例对本发明的技术方案做进一步说明,但本发明并不局限于以下方案。
实施例1
1、皮肤成纤维细胞的分离
1.1从供者身上获取直径约1cm的皮肤组织块,贴壁法分离皮肤成纤维细胞,分离的细胞培养于基础培养液里,所述基础培养液:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm。
1.2细胞传代大量扩增,细胞代数在第6代和第12代间,用于进行向间充质干细胞的转分化诱导。启动分化的前一天(day-1),接种细胞密度1~2.5x104/cm2培养于37℃,5%co2的培养箱中。
2、皮肤成纤维细胞的活化
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4~6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的定向诱导
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间6~10天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm~8μm)+am580(0.03-0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、第三阶段——提高向间充质干细胞转分化的效率
随后更换为第三阶段培养液,作用时间3-8天,在37℃,5%co2环境下培养细胞。第三阶段培养液是指,bmp4(10~20ng/ml)+pdgf-ab(100~250ng/ml)+b-fgf(10~50ng/ml)+10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。。
5、诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
实施例2
1、皮肤成纤维细胞的分离,同实施例1。
2、启动转分化时(day0),完全更换基础培养液为如下培养液,培养细胞4-6天,培养时间6——12天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm~8μm)+am580(0.03~0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
3、随后更换为如下培养液,作用时间3~8天,在37℃,5%co2环境下培养细胞。给阶段培养液为:bmp4(10~20ng/ml)+pdgf-ab(100~250ng/ml)+b-fgf(10-50ng/ml)+10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
实施例3
1、皮肤成纤维细胞的分离,同实施例1。
2、皮肤成纤维细胞的活化
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4~6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%~20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的定向诱导
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间6-10天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm~8μm)+am580(0.03~0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%~20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
实施例4
1、皮肤成纤维细胞的分离,同实施例1。
2、皮肤成纤维细胞的活化
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4-6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+chir99021(1μm~10μm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%~20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的定向诱导
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间6~10天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm-8μm)+am580(0.03-0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3-15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm)+sp600125(1~15μm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、第三阶段提高向间充质干细胞转分化的效率
随后更换为第三阶段培养液,作用时间3~8天,在37℃,5%co2环境下培养细胞。第三阶段培养液是指,bmp4(10~20ng/ml)+pdgf-ab(100~250ng/ml)+b-fgf(10-50ng/ml)+10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
5、诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
实施例5
1、皮肤成纤维细胞的分离,同实施例1。
2、皮肤成纤维细胞的活化
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4-6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%~20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的定向诱导
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间6~10天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm-8μm)+am580(0.03-0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm)+sp600125(8~12μm)+5-aza-2'-deoxycytidine(1μm~15μm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、第三阶段提高向间充质干细胞转分化的效率
随后更换为第三阶段培养液,作用时间3~8天,在37℃,5%co2环境下培养细胞。第三阶段培养液是指,bmp4(10~20ng/ml)+pdgf-ab(100~250ng/ml)+b-fgf(10~50ng/ml)+10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
5、诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
实施例6
1、皮肤成纤维细胞的分离,同实施例1。
2、皮肤成纤维细胞的活化
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4-6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的定向诱导
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间6~10天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm~8μm)+am580(0.03~0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm)+sp600125(8~12μm)+5-aza-2'-deoxycytidine(1μm~15μm)+parnate((1μm~10μm)),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、第三阶段——提高向间充质干细胞转分化的效率
随后更换为第三阶段培养液,作用时间3-8天,在37℃,5%co2环境下培养细胞。第三阶段培养液是指,bmp4(10~20ng/ml)+pdgf-ab(100~250ng/ml)+b-fgf(10~50ng/ml)+10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
5,诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
实施例7
1、皮肤成纤维细胞的分离,同实施例1。
2、皮肤成纤维细胞的活化
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4-6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+bio(1μm~10μm)+vpa(0.5mm~1.5mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的定向诱导
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间6~10天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm~8μm)+am580(0.03~0.08μm)+epz004777(3~8μm)+g06983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25mm)+sp600125(8~12μm)+5-aza-2'-deoxycytidine(1μm~15μm)+parnate((1μm~10μm)),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、第三阶段——提高向间充质干细胞转分化的效率
随后更换为第三阶段培养液,作用时间3~8天,在37℃,5%co2环境下培养细胞。第三阶段培养液是指,bmp4(10~20ng/ml)+pdgf-ab(100~250ng/ml)+b-fgf(10~50ng/ml)+10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
5、诱导的间充质干细胞的维持培养和扩增
随后更换为常规的间充质干细胞培养液或者市售商业化间充质干细胞培养液(赛业),对诱导的细胞进行维持培养和传代扩增。所述的常规的间充质干细胞培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)。
上述实施例诱导人皮肤成纤维细胞制备(重编程为)间充质干细胞,人源皮肤成纤维细胞向间充质干细胞转分化的细胞形态图见图1,获得的间充质干细胞的检测结果见表1、图2~图7;
图1中a图为皮肤成纤维细胞;b图为实施例1中的方法重编程获得的间充质干细胞;c图为重编程的间充质干细胞的生长曲线,重编程的间充质干细胞分别来源于两个成年人个体,细胞在培养皿中贴壁培养,生长到90%的汇合度的时候进行传代或者3天进行一次传代,重编程的细胞具备快速的增值能力;d图为细胞的克隆形成率,克隆形成率越高说明细胞增值活力越好,其中hufib代表未经处理的皮肤成纤维细胞,humsc代表体内分离的间充质干细胞,huimsc代表重编程的间充质干细胞;
表1
表1中检测了三株不同成年人个体来源的未经处理的皮肤成纤维细胞,分别是hufib01,hufib02和hufib03,以及重编程的间充质干细胞huimsc01和huimsc02,标准的间充质干细胞表面标志物的鉴定中cd29,cd90,cd73和cd105为阳性表达,cd24,cd45和cd34为阴性表达,重编程的间充质干细胞满足此细胞鉴定的要求,未经处理的皮肤成纤维细胞也具备同样的表达标志物的特征;
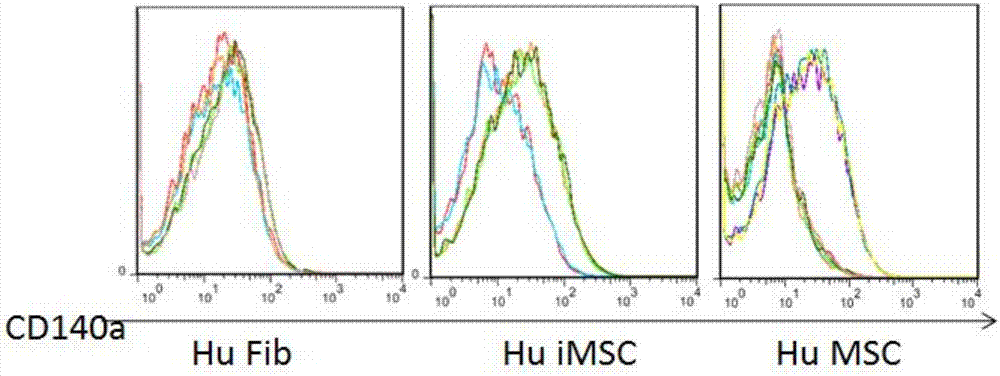
图2为鉴定间充质干细胞的另一表面标志物cd140a图,与未经处理的成纤维细胞hufib相比,huimsc和humsc的流式图有表达的偏移;
图3为对重编程的间充质干细胞分化多能性的检测结果图,使用标准的三系方法对来自于实施例1(a图)和实施例6(b图)中的huimsc和作为阴性对照的hufib进行成骨,成软骨和成脂肪的诱导,第21天,进行对应的染色检测,成骨分化使用茜素红染色,成软骨分化使用阿尔辛蓝染色,脂肪分化使用油红o染色;
图4为检测重编程的间充质干细胞对t细胞的免疫抑制作用,与hufib相比,huimsc与humsc有相似的免疫抑制能力;
图5为在免疫缺陷小鼠体内移植重编程的间充质干细胞,治疗小鼠股骨缺损的结果图。细胞移植28天后,使用microct检测移植部位的缺损修复情况,a图为空白对照组;b图为msc阳性对照组,c图为重编程的间充质干细胞组。与空白对照相比,间充质干细胞组对股骨缺损有明显的修复作用。
图6为对重编程获得的间充质干细胞的长期传代的细胞增值能力和干性的检测结果图,a图为对huimsc传代7代的生长曲线,生长到90%的汇合度的时候进行传代或者3天进行一次传代;c图为对p7代的huimsc进行3系诱导,21天后进行检测;b图为从成年人体内分离的皮肤成纤维细胞(在含10%血清的高糖培养液培养条件下,连续10代内的生长曲线,以此为原料,结合huimsc的扩增能力,可以大量生产和制备间充质干细胞。
图7为对重编程的间充质干细胞的成瘤性检测结果图;以0.6~1×105/只的细胞数量在nod-scid小鼠皮下移植huimsc,移植30只小鼠,一个月后未见成瘤。
实施例8重编程为成骨细胞
1、皮肤成纤维细胞的分离
1.1从供者身上获取直径约1cm的皮肤组织块,贴壁法分离皮肤成纤维细胞,分离的细胞培养于基础培养液里,所述基础培养液:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm。
1.2细胞传代大量扩增,细胞代数在第6代和第12代间,用于进行向成骨细胞的转分化诱导。启动分化的前一天(day-1),接种细胞密度1~2.5x104/cm2培养于37℃,5%co2的培养箱中。
2、皮肤成纤维细胞的激活
2.1启动转分化时(day0),完全更换基础培养液为第一阶段培养液,培养细胞4~6天,第一阶段培养液是指:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~25μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%~20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。在37℃,5%co2环境下培养细胞。
3、皮肤成纤维细胞的重编程
通过上述第2步骤的处理后,完全更换为第二阶段培养液进行细胞培养,培养时间5~18天,在37℃,5%co2环境下培养细胞。所述的第二阶段培养液是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+forskolin(2μm~20μm)+repsox(2~15um)+chir99021(1μm~10μm)+vpa(0.5mm~1.5mm)+ttnpb(3μm~8μm)+epz004777(3~8μm)+go6983(1~15μm)+y27362(3~15μm)+l-ascorbinacid2-phosphate(0.15~0.25m)+5-aza-2'-deoxycytidine(1μm~15μm),该培养系统中10%胎牛血清也可以被血清替代品(invitrogen)以10%-20%的浓度替代;100u/ml青霉素(sigma)和100μg/ml链霉素(sigma)可以不使用。
4、重编程细胞的定向诱导
随后更换为常规的成骨分化培养液或者市售商业化的成骨诱导液(赛业),培养12——30天后,获得成骨细胞。所述的成骨分化液具体是:10%胎牛血清(hyclone)+100u/ml青霉素(sigma)+100μg/ml链霉素(sigma)+高糖dmdm培养基(gibco)+10mmol/lβ-gly(β-甘氨酸)+100nmdexamethasone(地塞米松)+0.2mmascorbate-2-phosphate(维生素c磷酸酯);
5、诱导的成骨细胞的检测,检测基因runx2alp,bspii,ocn;茜素红染色标记细胞分泌的矿化结节;
诱导人皮肤成纤维细胞制备成骨细胞,人源皮肤成纤维细胞向成骨细胞转分化的细胞形态图见图8,获得的间充质干细胞的检测结果图9~图10;
图8为通过小分子化合物诱导人源皮肤成纤维细胞向成骨细胞转分化的细胞形态图,其中a图为皮肤成纤维细胞;b为实施例1中的方法转分化获得的成骨细胞,并进行了茜素红的染色;c为实施例5中的方法转分化获得的成骨细胞,并进行了茜素红的染色;d为对转分化的成骨细胞,进行成骨细胞分子标志物的定量鉴定,其中hufib代表未经处理的皮肤成纤维细胞(阴性对照),hu-ios代表转分化的成骨细胞,hu-os代表由体内msc体外诱导获得的成骨细胞(阳性对照);
图9为对获得成骨细胞的转分化效率和细胞纯度的鉴定结果图。经过小分子化合物组合处理后,使用传统的成骨诱导液分化14天,a图为镜下成骨细胞分泌的矿化结节的茜素红染色,镜下观察大部分细胞分泌了矿化结节;b图为runx2的免疫荧光染色;c图为以runx2标记为阳性的细胞与总细胞数相比,进行分化效率的统计,结果为90%以上的细胞高表达runx2,向成骨方向分化;d图为从成年人体内分离的皮肤成纤维细胞(hufib)在含10%血清的高糖培养液培养条件下,连续10代内的生长曲线,以此为原料制备的成骨细胞可以大量生产。
图10为在免疫缺陷小鼠体内移植转分化的成骨细胞治疗小鼠股骨缺损结果图;细胞移植28天后,使用microct检测移植部位的缺损修复情况,a图为空白对照组;b图为msc阳性对照组,c图为转分化的成骨细胞组。
应理解,在本发明范围内中,本发明的上述各技术特征在和下文(如实施例)中具体描述的各种技术特征之间可以互相结合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!
- 能够与配体偶联的单甲基缬氨酸化合物的制造方法与工艺
- 烟梗纤维微波降解制备烟用料液方法及应用与流程
- 利用特异性挥发物筛选昆虫相关嗅觉蛋白的方法与制造工艺
- 小分子共价抑制剂的计算机筛选方法及其在筛选S-腺苷甲硫氨酸脱羧酶的共价抑制剂的应用与制造工艺
- 一种合成抗原的分子量检测方法及应用与制造工艺
- 一种用于MALDI‑TOF‑MS分析小分子的氧化锌沸石复合材料及其制备方法与制造工艺
- 用于原位收集根系挥发物的试验装置及方法与制造工艺
- 一种核壳型纳米香精胶囊的制备方法与制造工艺
- 小分子共价抑制剂在制备抑制S-腺苷甲硫氨酸脱羧酶的药物上的应用及其筛选方法与制造工艺
- Linderolide H在制备治疗鼻炎药物中的应用的制造方法与工艺