用于鉴定受试者所感染的HEV基因型的方法和试剂盒与流程
本发明属于分子生物学、免疫学以及疾病诊断领域。具体而言,本发明涉及一种hev抗原表位多肽,所述抗原表位多肽可用于鉴定受试者所感染的hev基因型。本发明还涉及一种用于鉴定受试者所感染的hev基因型的试剂盒。本发明还涉及一种新的鉴定受试者所感染的hev基因型的方法。
背景技术:
戊型肝炎病毒(hepatitisevirus,hev)是引起戊型肝炎的病原体。戊型肝炎病毒(hev)所导致的戊型肝炎(he)已成为危害人类健康的严重公共卫生问题。who报道全球每年大约有2000万人感染、300多万急性肝炎病例和7万多死亡病例。其中孕妇感染hev后的病死率更高,可达20%。目前越来越多的研究发现,器官移植后的患者和hiv感染等免疫功能低下的患者感染hev后,可迁延为慢性肝炎。自2004年来,我国人群中戊型肝炎的发病率逐年上升,且也发现存在多例慢性肝炎。目前,国际公认的可感染人类的hev基因型有1型、2型、3型和4型。hev基因1型和2型仅感染人,基因3型和4型能感染人、猪和其它动物。其中,基因2型主要在非洲、中美洲流行,目前尚未在我国发现,其他基因型均已在我国发现。
由于不同基因型hev具有较明显的流行病学差异,因此明确hev的基因型对于戊型肝炎的诊断、预防及流行病学具有重要意义。目前常用的基因分型方法主要包括特异性引物扩增后直接测序分析、限制性片段长度酶切多肽性(rflp)分析、特异性探针pcr法和基因芯片法等,尽管这些方法的特异性和灵敏度很高,但由于这些基因分型方法都需要rna提取等过程,操作复杂,技术要求高,一般实验室难以开展;而且当样品中rna阴性或由于保存不当或处理过程中rna遭到破坏时,则不能进行基因分型。
因此,本领域需要开发不依赖于基因测序的hev基因分型方法,以实现更加经济、有效、快速、准确地鉴定受试者所感染的hev基因型。
技术实现要素:
在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员所通常理解的含义。并且,本文中所用的细胞培养、生物化学、细胞生物学等操作步骤均为相应领域内广泛使用的常规步骤。同时,为了更好地理解本发明,下面提供相关术语的定义和解释。
如本文中所使用的,术语“hevorf3蛋白”是指,天然存在于戊型肝炎病毒中的蛋白orf3,其由hev基因组的开放读码框架3(orf3)所编码。不同基因型hev病毒的orf3蛋白的序列均是本领域公知的,例如,1型hev病毒的orf3蛋白的序列可参见各种公共数据库(例如,genbank数据库登录号d11092、jq655734、m73218或x98292),3型hev病毒的orf3蛋白的序列可参见各种公共数据库(例如,例如genbank数据库登录号af060668、ap003430、ab073912或ay115488),4型hev病毒的orf3蛋白的序列可参见各种公共数据库(例如,genbank数据库登录号ab197673、ab097811、ay723745或jq655736)。
在本发明中,当提及1型hev病毒的orf3蛋白的氨基酸序列时,参照seqidno:1所示的序列来进行描述。例如,表述“1型hev病毒的orf3蛋白的第66-87位氨基酸残基”是指,seqidno:1所示的多肽的第66-87位氨基酸残基。然而,本领域技术人员理解,1型hev病毒可包括多种分离株,并且各种分离株的orf3蛋白的氨基酸序列之间可能存在着差异。进一步,本领域技术人员理解,尽管可能存在着序列差异,但是1型hev病毒的不同分离株的orf3蛋白在氨基酸序列上具有极高的同一性,并且具有实质上相同的生物学功能。因此,在本发明中,表述“1型hev病毒的orf3蛋白”不仅包括seqidno:1所示的蛋白,而且应包括各种1型hev病毒分离株的orf3蛋白(例如,genbank数据库登录号jq655734所示的orf3蛋白)。并且,当描述1型hev病毒的orf3蛋白的序列片段时,其不仅包括seqidno:1的序列片段,还包括各种1型hev病毒分离株的orf3蛋白中的相应序列片段。例如,表述“1型hev病毒的orf3蛋白的第66-87位氨基酸残基”包括,seqidno:1的第66-87位氨基酸残基,以及各种1型hev病毒分离株的orf3蛋白中的相应片段。
在本发明中,当提及3型hev病毒的orf3蛋白的氨基酸序列时,参照seqidno:2所示的序列来进行描述。例如,表述“3型hev病毒的orf3蛋白的第66-87位氨基酸残基”是指,seqidno:2所示的多肽的第66-87位氨基酸残基。然而,本领域技术人员理解,3型hev病毒可包括多种分离株,并且各种分离株的orf3蛋白的氨基酸序列之间可能存在着差异。进一步,本领域技术人员理解,尽管可能存在着序列差异,但是3型hev病毒的不同分离株的orf3蛋白在氨基酸序列上具有极高的同一性,并且具有实质上相同的生物学功能。因此,在本发明中,表述“3型hev病毒的orf3蛋白”不仅包括seqidno:2所示的蛋白,而且应包括各种3型hev病毒分离株的orf3蛋白(例如,genbank数据库登录号af060668所示的orf3蛋白)。并且,当描述3型hev病毒的orf3蛋白的序列片段时,其不仅包括seqidno:2的序列片段,还包括各种3型hev病毒分离株的orf3蛋白中的相应序列片段。例如,表述“3型hev病毒的orf3蛋白的第66-87位氨基酸残基”包括,seqidno:2的第66-87位氨基酸残基,以及各种3型hev病毒分离株的orf3蛋白中的相应片段。
在本发明中,当提及4型hev病毒的orf3蛋白的氨基酸序列时,参照seqidno:3所示的序列来进行描述。例如,表述“4型hev病毒的orf3蛋白的第66-87位氨基酸残基”是指,seqidno:3所示的多肽的第66-87位氨基酸残基。然而,本领域技术人员理解,4型hev病毒可包括多种分离株,并且各种分离株的orf3蛋白的氨基酸序列之间可能存在着差异。进一步,本领域技术人员理解,尽管可能存在着序列差异,但是4型hev病毒的不同分离株的orf3蛋白在氨基酸序列上具有极高的同一性,并且具有实质上相同的生物学功能。因此,在本发明中,表述“4型hev病毒的orf3蛋白”不仅包括seqidno:3所示的蛋白,而且应包括各种4型hev病毒分离株的orf3蛋白(例如,genbank数据库登录号jq655733所示的orf3蛋白)。并且,当描述4型hev病毒的orf3蛋白的序列片段时,其不仅包括seqidno:3的序列片段,还包括各种4型hev病毒分离株的orf3蛋白中的相应序列片段。例如,表述“4型hev病毒的orf3蛋白的第66-87位氨基酸残基”包括,seqidno:3的第66-87位氨基酸残基,以及各种4型hev病毒分离株的orf3蛋白中的相应片段。
在本发明中,表述“相应片段”是指,当对序列进行最优比对时,即当序列进行比对以获得最高百分数同一性时,进行比较的序列中位于等同位置的片段。
如本文中所使用的,术语“表位多肽”是指,抗原蛋白中能够被特异性抗体所识别的多肽片段。
如本文中所使用的,表述“分别具有如seqidno:4-6所示的氨基酸序列的表位多肽”是指,具有seqidno:4所示的氨基酸序列的表位多肽、具有seqidno:5所示的氨基酸序列的表位多肽、和具有seqidno:6所示的氨基酸序列的表位多肽的组合。
如本文中所使用的,术语“载体(vector)”是指,可将多核苷酸插入其中的一种核酸运载工具。当载体能使插入的多核苷酸所编码的蛋白获得表达时,载体称为表达载体。载体可以通过转化,转导或者转染导入宿主细胞,使其携带的遗传物质元件在宿主细胞中获得表达。载体是本领域技术人员公知的,包括但不限于:质粒;噬菌体;柯斯质粒等等。
如本文中所使用的,术语“可检测的标记”是指,可通过荧光、光谱、光化学、生物化学、免疫学、电学、光学或化学手段检测的任何组合物。在本发明中,特别优选的是,此类标记能够适用于免疫学检测(例如,酶联免疫测定法、放射免疫测定法、荧光免疫测定法、化学发光免疫测定法等)。这类标记是本领域熟知的,包括但不限于,酶(例如,辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、脲酶、葡萄糖氧化酶,等)、放射性核素(例如,3h、125i、35s、14c或32p)、荧光染料(例如,异硫氰酸荧光素(fitc)、荧光素、异硫氰酸四甲基罗丹明(tritc)、藻红蛋白(pe)、德克萨斯红、罗丹明、量子点或花菁染料衍生物(例如cy7、alexa750))、吖啶酯类化合物、磁珠(例如,
如本文中所使用的,术语“载体蛋白”是指,可通过与抗原或半抗原连接而诱导机体产生针对该抗原或半抗原的免疫应答的蛋白,其中所述免疫应答包括产生可以特异性结合该抗原或半抗原的抗体的反应。这类蛋白是本领域公知的,包括但不限于牛血清白蛋白(bsa)、钥孔血蓝蛋白(klh)、卵清蛋白(ova)、牛甲状腺球蛋白(btg)等。
如本文中所使用的,表述“能够识别并结合抗hev抗体的检测试剂”是指,能够和抗hev抗体特异性结合的物质。这类物质是本领域所公知的,或者可以利用本领域公知的方法制备得到,例如为抗体(即,二级抗体)、靶向多肽或核酸适体等。通常而言,特别优选的是,此类试剂能够通过免疫学检测来确定样品中抗hev抗体的量。免疫学检测的使用是特别有利的,因为其利用了抗原-抗体之间的特异性相互作用/结合亲和力。因此,只要试剂保留了与抗hev抗体特异性结合的反应性,那么该试剂即可以通过免疫学检测来确定样品中抗hev抗体的量(也即,该试剂即可用作能够识别并结合抗hev抗体的检测试剂)。保留与抗hev抗体特异性结合的反应性的各种试剂是本领域技术人员容易想到并且可容易获得的,其包括但不限于,抗抗hev抗体的抗体或其抗原结合片段,例如抗抗hev抗体的多克隆抗体或单克隆抗体,例如抗受试者种属来源的抗体。
如本文中所使用的,术语“特异性结合”是指,两分子(即结合分子与靶分子)之间的非随机的结合反应,如抗体和其所针对的抗原之间的反应。两分子之间的结合亲和力可用kd值描述。kd值是指由kd(特定的结合分子-靶分子相互作用的解离速率;亦称为koff)与ka(特定结合分子-靶分子相互作用的缔合速率;亦称为kon)之比得到的解离常数,或者指表示为摩尔浓度(m)的kd/ka。kd值越小,两分子结合越紧密,亲和力越高。在某些实施方式中,特异性结合某抗原的抗体(或对某抗原具有特异性的抗体)是指,抗体以小于大约10-5m,例如小于大约10-6m、10-7m、10-8m、10-9m或10-10m或更小的亲和力(kd)结合该抗原。kd值可通过本领域熟知的方法确定,例如使用表面等离子体共振术(spr)在biacore仪中测定。
如本文中所使用的,术语“免疫学检测”是指,利用抗原-抗体之间的特异性相互作用/结合亲和力来进行的测定,其一般可用于检测特定抗原或者抗体在样品中的存在或水平。此类免疫学检测是本领域技术人员公知的,包括但不限于,酶免疫测定法(eia)、化学发光免疫分析法(clia)、放射免疫测定法(ria)、荧光免疫测定法(fia)、western印迹法、免疫比浊法、表面等离子共振法等。在某些实施方式中,所述免疫学检测为酶免疫测定法(eia),例如elisa检测法、elispot检测法或cleia检测法。关于免疫学检测的详细描述,可参见例如,fundamentalimmunology,ch.7paul,w.,ed.,第2版,ravenpress,n.y.(1989)。
如本文中所使用的,术语“抗体”是指,通常由两对多肽链(每对具有一条“轻”(l)链和一条“重”(h)链)组成的免疫球蛋白分子。抗体轻链可分类为κ和λ轻链。重链可分类为μ、δ、γ、α或ε,并且分别将抗体的同种型定义为igm、igd、igg、iga和ige。在轻链和重链内,可变区和恒定区通过大约12或更多个氨基酸的“j”区连接,重链还包含大约3个或更多个氨基酸的“d”区。各重链由重链可变区(vh)和重链恒定区(ch)组成。重链恒定区由3个结构域(ch1、ch2和ch3)组成。各轻链由轻链可变区(vl)和轻链恒定区(cl)组成。轻链恒定区由一个结构域cl组成。抗体的恒定区可介导免疫球蛋白与宿主组织或因子,包括免疫系统的各种细胞(例如,效应细胞)和经典补体系统的第一组分(c1q)的结合。vh和vl区还可被细分为具有高变性的区域(称为互补决定区(cdr)),其间散布有较保守的称为构架区(fr)的区域。各vh和vl由按下列顺序:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4从氨基末端至羧基末端排列的3个cdr和4个fr组成。各重链/轻链对的可变区(vh和vl)分别形成抗体结合部位。氨基酸至各区域或结构域的分配遵循kabatsequencesofproteinsofimmunologicalinterest(nationalinstitutesofhealth,bethesda,md.(1987and1991)),或chothia&lesk(1987)j.mol.biol.196:901-917;chothia等人(1989)nature342:878-883的定义。术语“抗体”不受任何特定的产生抗体的方法限制。例如,其包括,特别地,重组抗体、单克隆抗体和多克隆抗体。抗体可以是不同同种型的抗体,例如,igg(例如,igg1,igg2,igg3或igg4亚型),iga1,iga2,igd,ige或igm抗体。
如本文中所使用的,抗体的“抗原结合片段”是指,全长抗体的一个或多个部分,所述部分保持结合抗体所结合的相同抗原(例如,抗hev抗体)的能力,与完整抗体竞争对抗原的特异性结合。通常参见,fundamentalimmunology,ch.7paul,w.,ed.,第2版,ravenpress,n.y.(1989),其以其全文通过引用合并入本文,用于所有目的。可通过重组dna技术或通过完整抗体的酶促或化学断裂产生抗原结合片段。在一些情况下,抗原结合片段包括fab、fab'、f(ab')2、fd、fv、dab和互补决定区(cdr)片段、单链抗体(例如,scfv)、嵌合抗体、双抗体(diabody)和这样的多肽,其包含足以赋予多肽特异性结合抗原能力的抗体的至少一部分。
如本文中所使用的,术语“核酸适体(aptamer)”是指,能够高亲和性和高特异性地结合目的靶蛋白(例如抗hev抗体)或其它生物靶分子的单链寡核苷酸,其可折叠形成例如茎环(stem-loop)、发夹(hairpin)、假结(pseudoknot)或g-四聚体(g-tetramer)的热力学稳定的三维空间结构,通过例如结构互补、碱基堆积力、范德华力、氢键或静电作用与目的靶蛋白或其它生物靶分子特异性结合。核酸适体可以为dna或rna,也可以包含核酸类似物(例如锁核酸(lna)、肽核酸(pna)、二醇核酸(gna)或苏糖核酸(tna))。获得结合特定靶蛋白的核酸适体的方法是本领域公知的,例如selex(systematicevolutionofligandsbyexponentialenrichment)筛选技术。
如本文中所使用的,术语“靶向多肽”是指,可以特异性结合目的靶蛋白(例如抗hev抗体)的多肽分子。在本发明中,该靶向多肽可包含天然氨基酸、合成的氨基酸或采用与天然存在的氨基酸类似的方式起作用的氨基酸模拟物(mimetics)。天然存在的氨基酸为通过遗传密码来编码的那些以及后来修饰的那些氨基酸,例如,羟基脯氨酸、γ-羟基谷氨酸盐、o-磷酸丝氨酸、磷酸苏氨酸或磷酸酪氨酸。在本发明中,可基于亲和力来确定靶向多肽与其目的靶蛋白之间的“特异性”,该亲和力可用靶向多肽与其所结合的目的靶蛋白的解离平衡常数(即,kd值)进行描述。kd值越低,靶向多肽与其所结合的目的靶蛋白之间的结合强度越强。在本领域中通常已知,大于约10-3m的kd值通常被认为表示非结合或非特异性结合。取决于具体的目的靶蛋白,可以通过本领域技术人员已知的方法获得特异性结合该靶蛋白的靶向多肽,例如通过噬菌体展示技术或蛋白质微阵列技术进行筛选。
如本文中所使用的,术语“二级抗体(secondaryantibody)”是指,可以与抗体特异性结合的抗体。通常而言,在免疫学检测中,一级抗体(primaryantibody)(例如,抗hev抗体)的fab结构域与抗原结合,导致其fc结构域暴露,因此二级抗体通常与一级抗体的fc结构域结合。由于fc结构域在相同动物类别中是恒定的,因此一种类型的二级抗体即可结合许多类型的来自同一动物类别的一级抗体。本领域技术人员熟知,如何根据一级抗体的物种来源选择相应的二级抗体。
如本文中所使用的,术语“捕获试剂”是指,在免疫学检测中,用于固定在固相载体上的一种物质,其可特异性结合待测抗体或待测抗原。在本发明中,所述捕获试剂为本发明的抗原表位多肽或复合物,其可特异性结合待测样品中的抗特定基因型hev抗体,再通过测定被捕获的抗hev抗体的量,以完成整个免疫学检测。
如本文中所使用的,术语“阳性对照样品”是指,含有已知量的抗特定基因型hev的抗体的样品,例如含有已知量的抗1型hev抗体的样品、含有已知量的抗3型hev抗体的样品或含有已知量的抗4型hev抗体的样品。在某些实施方式中,待测样品中待测抗体的量可以通过将待测样品的检测结果与所述阳性对照样品的检测结果进行比较来计算,这类方法是本领域熟知的,例如通过检测不同浓度的阳性对照样品而构建标准曲线来进行。在本发明中,术语“阴性对照样品”是指,不含有抗hev抗体或不含有抗特定基因型hev抗体的样品,例如不含有抗1型hev抗体的样品、不含有抗3型hev抗体的样品或不含有抗4型hev抗体的样品。
如本文中所使用的,术语“受试者”包括但不限于各种动物,特别是哺乳动物,例如牛科动物、马科动物、羊科动物、猪科动物、犬科动物、猫科动物、兔科动物、啮齿类动物(例如,小鼠或大鼠)、非人灵长类动物(例如,猕猴或食蟹猴)或人。
本发明至少部分基于发明人的下述出人意料的发现:hevorf3蛋白的第66-87位氨基酸残基具有明显的基因型特异性,来源于不同基因型hev(例如,基因1型、基因3型或基因4型)的由上述氨基酸残基组成的抗原表位多肽对通过用同基因型hevorf3全长蛋白免疫哺乳动物而产生的同型抗血清或自然感染同基因型hev的动物所产生的同型抗血清的结合反应强度显著高于非同型抗血清。基于这一发现,本发明人开发了新的鉴定受试者所感染的hev基因型的方法。
因此,在一个方面,本发明提供了一种分离的表位多肽,其包含hevorf3蛋白的第66-87位氨基酸残基。
在某些优选的实施方案中,所述表位多肽由hevorf3蛋白的第66-87位氨基酸残基组成。
在某些优选的实施方案中,所述hevorf3蛋白为1型hev病毒的orf3蛋白、3型hev病毒的orf3蛋白或4型hev病毒的orf3蛋白。
在某些优选的实施方案中,所述1型hev病毒的orf3蛋白具有如seqidno:1所示的氨基酸序列。
在某些优选的实施方案中,所述3型hev病毒的orf3蛋白具有如seqidno:2所示的氨基酸序列。
在某些优选的实施方案中,所述4型hev病毒的orf3蛋白具有如seqidno:3所示的氨基酸序列。
在某些优选的实施方案中,所述表位多肽具有选自下列的氨基酸序列:seqidno:4-6。
在本发明中,本发明的表位多肽不受任何特定的合成多肽的方法限制,可通过本领域技术人员已知的常规技术产生,例如dna重组技术或化学合成技术。在某些实施方式中,本发明的表位多肽通过dna重组技术获得,例如通过使用无细胞表达系统从编码这些蛋白或多肽的多核苷酸获得(无细胞表达系统包括例如基于网织红细胞裂解物的表达系统、基于麦胚提取物的表达系统以及基于大肠杆菌提取物的表达系统);或通过使用体内表达系统(例如,大肠杆菌原核表达系统、酵母真核表达系统)从编码这些蛋白或多肽的多核苷酸获得。作为另外一种选择,本发明的表位多肽可以通过化学合成产生。蛋白或多肽化学全合成的方法在本领域内是熟知的(参见,例如,raibautl,etal.,topcurrchem.2015;363:103-54;thapap,etal.molecules.2014;19(9):14461-83;dawsonpe,etal.,science,1994;266(5186):776-9;和wangp,etal.,tetrahedronlett,1998,39(47):88711-14;其通过引用并入本文),并且包括但不限于:固相肽合成技术(solidphasepeptidesynthesis,spps)或液相分段合成技术(例如,天然化学连接法(nativechemicalligation,ncl)、叠氮法(azidemethod)、转移活化酯法(transferactiveestercondensation,taec))。
在另一个方面,本发明提供了一种分离的核酸,其编码如上所述的表位多肽。
在另一个方面,本发明提供了一种载体,其包含如上所述的分离的核酸。可用于插入目的多核苷酸的载体是本领域公知的,包括但不限于克隆载体和表达载体。在某些实施方式中,所述载体是例如质粒,粘粒,噬菌体等。
在另一个方面,本发明还涉及包含如上所述的分离的核酸或载体的宿主细胞。此类宿主细胞包括但不限于,原核细胞例如大肠杆菌细胞,以及真核细胞例如酵母细胞,昆虫细胞,植物细胞和动物细胞(如哺乳动物细胞,例如灵长类动物细胞、人类细胞等)。本发明的宿主细胞还可以是细胞系,例如293t细胞。
在另一个方面,本发明提供了一种复合物,其包含本发明的表位多肽和修饰基团,其中所述修饰基团为载体蛋白或可检测的标记,并且所述表位多肽与所述修饰基团通过偶联、缀合或融合得到所述复合物。
在某些优选的实施方案中,所述修饰基团选自生物素、亲和素、链霉亲和素或去糖基化亲和素(例如,
在某些优选的实施方案中,所述修饰基团通过所述表位多肽的氨基酸残基连接至所述表位多肽的n端或c端。在某些优选的实施方案中,所述修饰基团通过接头基团连接至所述表位多肽的n端或c端。这类接头基团是本领域熟知的,包括但不限于氨基乙酸(ahx)、β-丙氨酸(β-ala)、4-氨基丁酸(gaba)、5-氨基戊酸(ava)或聚乙二醇(peg)。可使用本领域熟知的连接方法将修饰基团连接至本发明的表位多肽上,包括但不限于酶促方法、氧化取代法或共价偶联法,例如碳二亚胺法、活性酯法、戊二醛法、琥珀酸酐法或重氮化法;其可参见例如gregt.hermanson,生物偶联技术,第3版,academicpress,2013,以及c.m.niemeyer,生物偶联实验方法——策略与方法,huamanapress,2004,其全部通过引用并入本文。
在另一个方面,本发明提供了一种试剂盒,其包含本发明的表位多肽或如上所述的复合物。
在某些优选的实施方案中,所述试剂盒包含一种、二种或三种本发明的表位多肽。
在某些优选的实施方案中,所述试剂盒包含:
第一表位多肽,其包含1型hevorf3蛋白的第66-87位氨基酸残基;
第二表位多肽,其包含3型hevorf3蛋白的第66-87位氨基酸残基;和
第三表位多肽,其包含4型hevorf3蛋白的第66-87位氨基酸残基。
在某些优选的实施方案中,所述试剂盒包含一种、二种或三种本发明的复合物。
在某些优选的实施方案中,所述试剂盒包含:
第一复合物,其包含具有1型hevorf3蛋白的第66-87位氨基酸残基的表位多肽;
第二复合物,其包含具有3型hevorf3蛋白的第66-87位氨基酸残基的表位多肽;和
第三复合物,其包含具有4型hevorf3蛋白的第66-87位氨基酸残基的表位多肽。
在本发明中,包含如上所述的第一表位多肽、第二表位多肽和第三表位多肽的试剂盒或包含如上所述的第一复合物、第二复合物和第三复合物的试剂盒是特别有利的,其可一次性鉴定出受试者所感染的hev是否为1型、3型或4型。
在一个具体的实施方式中,所述试剂盒包含分别具有如seqidno:4-6所示的氨基酸序列的表位多肽。
在另一个具体的实施方式中,所述试剂盒包含:
第一复合物,其包含具有如seqidno:4所示的氨基酸序列的表位多肽;
第二复合物,其包含具有如seqidno:5所示的氨基酸序列的表位多肽;和
第三复合物,其包含具有如seqidno:6所示的氨基酸序列的表位多肽。在某些优选的实施方案中,所述试剂盒还包含能够识别并结合抗hev抗体的检测试剂。这类检测试剂是本领域熟知的,包括但不限于能够和抗hev抗体特异性结合的抗体、靶向多肽或核酸适体。在某些优选的实施方案中,所述检测试剂为二级抗体。
在某些优选的实施方案中,所述检测试剂带有可检测的标记,例如酶(例如辣根过氧化物酶或碱性磷酸酶)、化学发光试剂(例如吖啶酯类化合物)或荧光染料。在某些实施方式中,当所述可检测的标记为酶时,所述试剂盒还可以包含显色液,例如用于辣根过氧化物酶的邻苯二胺(opd)、四甲基联苯胺(tmb)、abts或鲁米诺类化合物,或用于碱性磷酸酶的对硝基苯磷酸酯(p-npp)或amppd。
在某些优选的实施方案中,所述试剂盒还包含固相载体,任选地还包含用于将所述表位多肽或所述复合物包被于所述固相载体上的包被试剂,例如包被缓冲液(例如,碳酸盐缓冲液、磷酸盐缓冲液、tris-hcl缓冲液或硼酸盐缓冲液)。在某些优选的实施方案中,所述固相载体包括由聚合物材料(例如聚氯乙烯、聚苯乙烯、聚丙酰胺或纤维素)制成或包被的凹孔平板、试管、珠粒(例如乳胶颗粒)或薄膜(例如硝酸纤维素膜),或由功能基团(例如氨基、羧基、生物素或亲和素)预包被的磁珠。在某些实施方式中,所述固相载体为微量滴定板,例如微孔板或酶标板。将蛋白或多肽包被于固相载体上的方法是本领域熟知的,例如物理吸附、通过氨基化或羧基化表面实现的共价偶联或通过亲和素-生物素系统、聚赖氨酸预包被表面、蛋白a或蛋白g预包被表面实现的介导结合。
在某些优选的实施方案中,所述试剂盒包含表面包被有所述表位多肽或所述复合物的固相载体。
在某些优选的实施方案中,所述试剂盒还包含一种或多种选自下列的试剂或装置:用于稀释样品的稀释液(例如,磷酸盐缓冲液或含有非离子型表面活性剂的磷酸盐缓冲液);阳性对照样品(例如,含有已知量的抗特定基因型hev的抗体的样品);阴性对照样品(例如,不含有抗hev抗体的样品或确定不含有抗特定基因型hev抗体的样品);用于终止酶催化底物显色反应的终止液(例如,硫酸、盐酸或氢氧化钠溶液);用于去除未参与反应的试剂的洗涤液(例如,磷酸盐缓冲液或含有非离子型表面活性剂的磷酸盐缓冲液);用于抑制非特异性结合的封闭液;和,采血装置(例如,无热原真空采血管)。
在某些优选的实施方案中,为了抑制样品中的蛋白之间的非特异性相互作用或蛋白与固相载体之间的非特异性吸附,通常可以在所述稀释液、洗涤液或封闭液中加入非离子型表面活性剂,例如吐温-20、吐温-40、吐温-60、吐温-80、tritonx-20、tritonx-100或tritonx-300;或惰性蛋白,例如白蛋白(如bsa)、血清(如小牛血清)、脱脂奶粉或酪蛋白。在某些优选的实施方案中,所述稀释液、洗涤液或封闭液的ph值维持在7.0至10.0之间。
在某些优选的实施方案中,所述阳性对照样品选自含有已知量的抗1型hev抗体的样品、含有已知量的抗3型hev抗体的样品或含有已知量的抗4型hev抗体的样品。在某些优选的实施方案中,所述阴性对照样品选自不含有抗1型hev抗体的样品、不含有抗3型hev抗体的样品或不含有抗4型hev抗体的样品。
在另一个方面,本发明还涉及如上所述的表位多肽或复合物在制备试剂盒中的用途,所述试剂盒用于鉴定受试者所感染的hev基因型。
在某些优选的实施方案中,所述hev基因型选自1型、3型和4型。
在某些优选的实施方案中,所述试剂盒包含一种、二种或三种本发明的表位多肽或复合物。
在某些优选的实施方案中,所述试剂盒包含:
第一表位多肽,其包含1型hevorf3蛋白的第66-87位氨基酸残基;
第二表位多肽,其包含3型hevorf3蛋白的第66-87位氨基酸残基;和
第三表位多肽,其包含4型hevorf3蛋白的第66-87位氨基酸残基。
在某些优选的实施方案中,所述试剂盒包含:
第一复合物,其包含具有1型hevorf3蛋白的第66-87位氨基酸残基的表位多肽;
第二复合物,其包含具有3型hevorf3蛋白的第66-87位氨基酸残基的表位多肽;和
第三复合物,其包含具有4型hevorf3蛋白的第66-87位氨基酸残基的表位多肽。
在本发明中,包含如上所述的第一表位多肽、第二表位多肽和第三表位多肽的试剂盒或包含如上所述的第一复合物、第二复合物和第三复合物的试剂盒是特别有利的,其可一次性鉴定出受试者所感染的hev是否为1型、3型或4型。
在一个具体的实施方式中,所述试剂盒包含分别具有如seqidno:4-6所示的氨基酸序列的表位多肽。
在另一个具体的实施方式中,所述试剂盒包含:
第一复合物,其包含具有如seqidno:4所示的氨基酸序列的表位多肽;
第二复合物,其包含具有如seqidno:5所示的氨基酸序列的表位多肽;和
第三复合物,其包含具有如seqidno:6所示的氨基酸序列的表位多肽。
在某些优选的实施方案中,所述试剂盒还包含能够识别并结合抗hev抗体的检测试剂。这类检测试剂是本领域熟知的,包括但不限于能够和抗hev抗体特异性结合的抗体、靶向多肽或核酸适体。在某些优选的实施方案中,所述检测试剂为二级抗体。在某些实施方式中,所述检测试剂为抗所述受试者种属来源的多克隆抗体或单克隆抗体。
在某些优选的实施方案中,所述检测试剂带有可检测的标记,例如酶(例如辣根过氧化物酶或碱性磷酸酶)、化学发光试剂(例如吖啶酯类化合物)或荧光染料。在某些实施方式中,当所述可检测的标记为酶时,所述试剂盒还可以包含显色液,例如用于辣根过氧化物酶的邻苯二胺(opd)、四甲基联苯胺(tmb)、abts或鲁米诺类化合物,或用于碱性磷酸酶的对硝基苯磷酸酯(p-npp)或amppd。
在某些优选的实施方案中,所述试剂盒还包含固相载体,任选地还包含用于将所述表位多肽或所述复合物包被于所述固相载体上的包被试剂,例如包被缓冲液(例如,碳酸盐缓冲液、磷酸盐缓冲液、tris-hcl缓冲液或硼酸盐缓冲液)。在某些优选的实施方案中,所述固相载体包括由聚合物材料(例如聚氯乙烯、聚苯乙烯、聚丙酰胺或纤维素)制成或包被的凹孔平板、试管、珠粒(例如乳胶颗粒)或薄膜(例如硝酸纤维素膜),或由功能基团(例如氨基、羧基、生物素或亲和素)预包被的磁珠。在某些实施方式中,所述固相载体为微量滴定板,例如微孔板或酶标板。将蛋白或多肽包被于固相载体上的方法是本领域熟知的,例如物理吸附、通过氨基化或羧基化表面实现的共价偶联或通过亲和素-生物素系统、聚赖氨酸预包被表面、蛋白a或蛋白g预包被表面实现的介导结合。
在某些优选的实施方案中,所述表位多肽或所述复合物包被在所述固相载体的表面。
在某些优选的实施方案中,所述试剂盒还包含一种或多种选自下列的试剂或装置:用于稀释样品的稀释液(例如,磷酸盐缓冲液或含有非离子型表面活性剂的磷酸盐缓冲液);阳性对照样品(例如,含有已知量的抗特定基因型hev的抗体的样品);阴性对照样品(例如,不含有抗hev抗体的样品或确定不含有抗特定基因型hev抗体的样品);用于终止酶催化底物显色反应的终止液(例如,硫酸、盐酸或氢氧化钠溶液);用于去除未参与反应的试剂的洗涤液(例如,磷酸盐缓冲液或含有非离子型表面活性剂的磷酸盐缓冲液);用于抑制非特异性结合的封闭液;和,采血装置(例如,无热原真空采血管)。
在某些优选的实施方案中,所述阳性对照样品选自含有已知量的抗1型hev抗体的样品、含有已知量的抗3型hev抗体的样品或含有已知量的抗4型hev抗体的样品。在某些优选的实施方案中,所述阴性对照样品选自不含有抗1型hev抗体的样品、不含有抗3型hev抗体的样品或不含有抗4型hev抗体的样品。
在某些优选的实施方案中,所述试剂盒通过包括下述步骤的方法来鉴定受试者所感染的hev基因型:
(1)将来自所述受试者的待测样品与一种捕获试剂接触,其中所述捕获试剂选自本发明的表位多肽或复合物,所述待测样品含有抗hev抗体;
(2)测定被所述捕获试剂所捕获的抗hev抗体的存在或其量;和
(3)根据步骤(2)中所述的抗hev抗体的存在或其量,判断所述受试者所感染的hev基因型。
在某些优选的实施方案中,所述待测样品选自全血、血清、血浆、淋巴液、组织液或外分泌液。
在本发明中,用于在步骤(2)中测定所述抗hev抗体的存在或其量的方法是本领域熟知的,例如免疫学检测,其包括但不限于酶免疫测定法(eia)、化学发光免疫分析法(clia)、放射免疫测定法(ria)、荧光免疫测定法(fia)、western印迹法、免疫比浊法或表面等离子共振法。在某些实施方式中,用于在步骤(2)中测定所述抗hev抗体的存在或其量的方法为酶免疫测定法(eia),例如elisa检测法、elispot检测法或cleia检测法。在某些实施方式中,在步骤(2)中,使用带有可检测的标记的二级抗体来测定所述抗hev抗体的存在或其量。
在另一个方面,本发明提供了用于鉴定受试者所感染的hev基因型的方法,其包括下述步骤:将来自所述受试者的待测样品与一种捕获试剂接触,其中所述捕获试剂选自本发明的表位多肽或复合物,所述待测样品含有抗hev抗体。
在某些优选的实施方案中,所述hev基因型选自1型、3型和4型。
在某些优选的实施方案中,所述用于鉴定受试者所感染的hev基因型的方法包括下述步骤:
(1)提供来自所述受试者的待测样品,其中所述待测样品含有抗hev抗体;
(2)将所述待测样品与一种捕获试剂接触,其中所述捕获试剂选自本发明的表位多肽或复合物;
(3)测定被所述捕获试剂所捕获的抗hev抗体的存在或其量;和
(4)根据步骤(3)中所述的抗hev抗体的存在或其量,判断所述受试者所感染的hev基因型。
在某些优选的实施方案中,所述待测样品选自全血、血清、血浆、淋巴液、组织液或外分泌液。
在本发明中,用于在步骤(3)中测定所述抗hev抗体的存在或其量的方法是本领域熟知的,例如免疫学检测,其包括但不限于酶免疫测定法(eia)、化学发光免疫分析法(clia)、放射免疫测定法(ria)、荧光免疫测定法(fia)、western印迹法、免疫比浊法或表面等离子共振法。在某些实施方式中,用于在步骤(3)中测定所述抗hev抗体的存在或其量的方法为酶免疫测定法(eia),例如elisa检测法、elispot检测法或cleia检测法。在某些实施方式中,在步骤(3)中,使用带有可检测的标记的二级抗体来测定所述抗hev抗体的存在或其量。
在某些优选的实施方案中,所述受试者为哺乳动物,例如啮齿类动物(如小鼠或大鼠)、非人灵长类动物(如猕猴或食蟹猴)或人。
发明的有益效果
目前hev基因分型方法主要依赖于基因测序,而rna提取等过程操作复杂、技术要求高,一般实验室难以开展,因此也难以满足大规模临床检测的需要。
本发明提供了一种分离的hev表位多肽、包含该多肽的复合物以及基于该多肽或复合物建立的用于鉴定受试者所感染的hev基因型的方法,与现有技术相比,本发明的技术方案至少具有以下有益效果:
(1)首次发现由hevorf3蛋白的第66-87位氨基酸残基所组成的多肽序列可用于hev基因分型,至少可用于区分基因1型、基因3型或基因4型;
(2)所涉及的操作简单、方便:例如,通过采集全血、分离血清,将其加入包被有本发明的表位多肽或复合物的酶标板中,洗涤后加入hrp标记二抗,然后加入酶显色底物即可完成对受试者所感染的hev基因型的检测;
(3)对实验条件、人员的技术能力、设备和环境的要求不高;
(4)对hev基因分型的检测结果准确率高;
(5)成本不高,易于推广,使用范围广。
下面将结合附图和实施例对本发明的实施方案进行详细描述,但是本领域技术人员将理解,下列附图和实施例仅用于说明本发明,而不是对本发明的范围的限定。根据附图和优选实施方案的下列详细描述,本发明的各种目的和有利方面对于本领域技术人员来说将变得显然。
附图说明
图1显示了实施例2中,使用1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂分别检测不同基因型orf3蛋白所免疫的小鼠的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,1型hevorf3蛋白(图1a)、3型hevorf3蛋白(图1b)和4型hevorf3蛋白(图1c)所分别免疫的小鼠的抗血清均与相应基因型的捕获试剂有明显的结合,而与其他基因型捕获试剂无交叉反应。
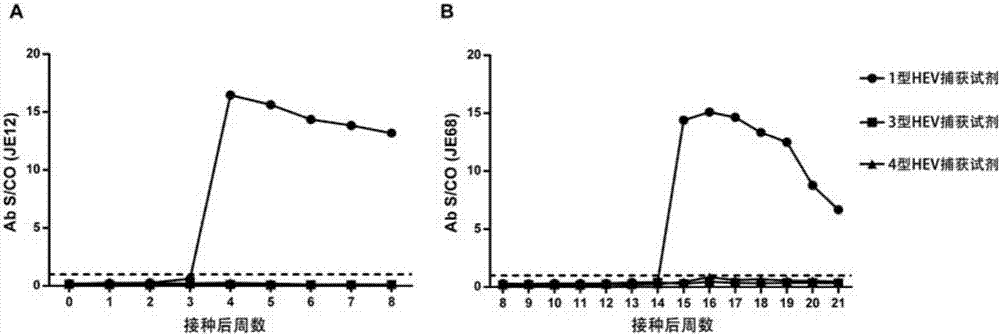
图2显示了实施例3中,使用1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂分别检测1型orf3蛋白所免疫的猕猴的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,1型hev捕获试剂对感染hev1型的两只猴子(je12和je68)的系列血清具有很强的结合反应,而3型和4型hev捕获试剂对上述系列血清均无阳性反应。
图3显示了实施例3中,使用1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂分别检测4型orf3蛋白所免疫的猕猴的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,4型hev捕获试剂对感染hev4型的三只猴子(je13、je53和je54)的系列血清具有强阳性反应,而1型和3型hev捕获试剂对上述系列血清无明显阳性反应。
图4显示了实施例4中,使用1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂分别检测自然感染hev3型的人的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,3型hev捕获试剂对3个自然感染hev3型的人(007b、002b和001b)的系列血清具有明显阳性反应,而其他基因型捕获试剂均无阳性反应。
图5显示了实施例4中,使用1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂分别检测自然感染hev4型的人的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,4型hev捕获试剂对3个自然感染hev4型的人(ya701、ya866和ya827)的系列血清具有明显阳性反应,而其他基因型捕获试剂均无阳性反应。
图6显示了实施例5中,使用1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂分别检测hev感染临床血清样本的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,商业化hev抗体检测试剂盒所测定的19例hev抗体阳性血清中有16例对4型hev捕获试剂的反应呈阳性,而1型和3型hev捕获试剂的检测均为阴性。
图7显示了实施例6中,使用1型hev捕获试剂、4型hev捕获试剂以及商业化hevigm抗体检测试剂、hevigg抗体检测试剂分别检测实验感染1型(je68)和4型(je54)hev的猕猴的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,在实验感染1型hev的猕猴(je68)系列血清中,1型hev捕获试剂对抗hev抗体检出时间晚于商业化hevigm抗体试剂,早于商业化igg抗体试剂;在实验感染4型hev的猕猴(je54)系列血清中,4型hev捕获试剂具有明显阳性反应,且对抗hevigg抗体的检出时间早于商业化igg抗体试剂。
图8显示了实施例7中,使用hevorf3蛋白的其它多肽片段作为捕获试剂检测实验感染不同基因型hev的动物的抗血清的分型结果,其中,图中虚线表示s/co值=1,当s/co值大于1时,判断为阳性。结果显示,refhev-3对3型hev抗血清呈阴性反应,refhev-1、refhev-4对同型抗血清呈阳性反应,但反应强度显著低于1型hev捕获试剂和4型hev捕获试剂。
序列信息
本发明涉及的部分序列的信息提供于下面的表1中。
表1:序列的描述
序列1(seqidno:1):
mgtrpcalglfcccsscfclccprhrpvsrlaavvggaaavpavvsgvtglilspsqspifiqptpsppmsplrpgldlvfanppdhsaplgvtrpsapplphvvdlpqlgprr
序列2(seqidno:2):
mnnmsfaspmgspcalglfcccsscfclccprhrpvsrlavavggaaavpavvsgvtglilspspspifiqptpsppmsfhnpglelaldsrpapsvplgvtspsapplppvvdlpqlglrr
序列3(seqidno:3):
mamppcalglfcfcsscfclccprhrpvsrlavvvggaaavpavvsgvtglilspspspifiqptpshltfqpppglelaldsrpahsaplgvtnpsapplppvvdlpqpglrr
序列4(seqidno:4):
psppmsplrpgldlvfanppdh
序列5(seqidno:5):
psppmsfhnpglelaldsrpap
序列6(seqidno:6):
pshltfqpppglelaldsrpah
序列7(seqidno:7):
psppmsplrp
序列8(seqidno:8):
psppisfhnp
序列9(seqidno:9):
pshltfqpqp
引物(5’-3’)(seqidno:10~13)
seeo1:cccttatcctgctgagcattctc(seqidno:10)
sebo1:aaytatgcwcagtaccgggttg(seqidno:11)
sebi1:gtyatgytytgcatacatggct(seqidno:12)
seei1:agccgacgaaatyaattctgtc(seqidno:13)
具体实施方式
现参照下列意在举例说明本发明(而非限定本发明)的实施例来描述本发明。
除非特别指明,本发明中所使用的分子生物学实验方法和免疫检测法,基本上参照j.sambrook等人,分子克隆:实验室手册,第2版,冷泉港实验室出版社,1989,以及f.m.ausubel等人,精编分子生物学实验指南,第3版,johnwiley&sons,inc.,1995中所述的方法进行;限制性内切酶的使用依照产品制造商推荐的条件。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。本领域技术人员知晓,实施例以举例方式描述本发明,且不意欲限制本发明所要求保护的范围。本文中提及的全部公开案和其他参考资料以其全文通过引用合并入本文。
实施例1.hev基因分型间接elisa检测法的建立
1.1hev抗原表位多肽的合成及纯化
从genbank数据库中下载hev各基因型orf3蛋白的氨基酸序列,其中各基因型orf3蛋白的第66-87位氨基酸残基如表2所示。由北京中科亚光生物科技有限公司分别合成基因1型、3型和4型的上述抗原表位多肽,并在n端偶联生物素,hplc纯化。基因1型、3型和4型的上述生物素标记的抗原表位多肽分别命名为1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂。
表2.hev各基因型orf3蛋白的第66-87位氨基酸残基序列
1.2亲和素包被板的制备
使用生物素包被微孔板,然后与合适浓度的链霉亲和素孵育,封闭后,4度保存备用。
首先使用生物素(购自thermo)包被微孔板,每孔加入100μl生物素稀释比例为1:1000的包被缓冲液,2-8℃过夜。然后使用亲和素(购自罗氏)进行第二次包被,每孔加入100μl亲和素稀释比例为1:2000的包被缓冲液,2-8℃过夜。最后,每孔加入200μl含1%酪蛋白的封闭液在37℃进行孵育,之后甩掉孔内封闭液,拍干,4度保存备用。
1.3基于hev表位多肽的hev基因分型间接elisa检测法
首先使用梯度稀释法优化各基因型表位多肽的包被浓度,即将各基因型表位多肽使用pbs进行梯度稀释后分别包被实施例1.2中获得的亲和素包被板,37℃预孵育后,4℃过夜。以确证hev抗体阴性的正常献血员的血清作为阴性对照,将其吸光值设为n;选择实验感染各基因型hev后的抗体阳转的猴血清作为阳性对照,将其吸光值设为p,计算p/n值。随着多肽包被浓度逐渐降低,其p/n值越来越大,最后达到平台期,取此时对应的多肽浓度为最佳包被浓度(1型、3型和4型表位多肽的最佳包被浓度分别是0.5μg/ml、1μg/ml和1.5μg/ml)。然后将每种基因型表位多肽以各自最佳包被浓度包被亲和素包被板,每孔加入100μl上述包被液,37℃孵育30min,使用ph7.4的pbst(含0.05%的tween-20)洗涤5遍,以获得不同基因型表位多肽包被的微孔板。对待测样品进行检测时,首先使用含5%牛血清的pbst将待测样品1:100稀释,然后取100μl/孔加入包被有多肽的微孔板中,37℃孵育30min;pbst洗涤5遍;除空白孔外,每孔加入100μlhrp标记的抗待测抗体的种属来源的igg的抗体(购自北京中杉金桥生物技术有限公司),在37℃孵育30min;去除液体,并用pbst洗涤5遍;然后加入tmb底物(购自美国bd公司),37℃显色15min;然后加入2mh2so4终止液,使用美国md-spectramaxm5多功能酶标仪在波长450nm和630nm处读取各孔吸光值a。以s/co值作为待测样品的最终检测值,其为样品的吸光值a除以cutoff值,cutoff值为各板阴性对照的吸光值的均值加3倍标准差。待测样品的s/co值大于1时,判定为阳性。
实施例2.hev基因分型间接elisa检测法在鼠抗血清中的分型效果评价
分别使用1型、3型和4型hevorf3全长蛋白(1型genbankno.jq655734;3型genbankno.af060668;4型genbankno.jq655733;由深圳菲鹏生物股份有限公司制备)皮下注射免疫9周龄的balb/c小鼠(购自中国食品药品检定研究院),以制备获得1型、3型和4型共3组抗血清。初次免疫采用与完全弗氏佐剂1:1混合乳化后的抗原,剂量为100μg/只,2周后进行加强免疫,采用与不完全弗氏佐剂1:1混合乳化后的抗原,剂量为50μg/只。2周后眼内眦取血获得抗血清。
使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,按照实施例1.2和1.3的方法,分别检测上述免疫后鼠抗血清。结果如图1所示,图1a显示了3种捕获试剂对由1型orf3全长蛋白所免疫的16只小鼠的抗血清的结合情况,其中13只小鼠的抗血清对1型hev捕获试剂的检测呈阳性,而其全部对其他基因型捕获试剂的检测呈阴性;图1b显示了3种捕获试剂对由3型orf3全长蛋白所免疫的9只小鼠的抗血清的结合情况,其中3只小鼠的抗血清对3型hev捕获试剂的检测呈阳性,而其全部对其他基因型捕获试剂的检测呈阴性;图1c显示了3种捕获试剂对由4型orf3全长蛋白所免疫的12只小鼠的抗血清的结合情况,其中5只小鼠的抗血清对4型hev捕获试剂的检测呈阳性,而其全部对其他基因型捕获试剂的检测呈阴性。
上述结果表明,分别由1型orf3全长蛋白、3型orf3全长蛋白和4型orf3全长蛋白所免疫的鼠血清仅与相应型别的捕获试剂有明显的结合,而跟其它型别捕获试剂均无交叉,初步显示了基于hevorf3蛋白第66-87位氨基酸残基的捕获试剂(1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂)良好的分型效果。
实施例3.hev基因分型间接elisa检测法在猕猴抗血清中的分型效果评价
使用1型hev病毒株(genbankno.jq655734)并采用静脉注射的途径分别攻击分别免疫2只猕猴(je12和je68),接种后每周采集一次血清,所有的血清以及粪便样品均保存于-60℃以下,避免反复冻融。使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,按照实施例1.2和1.3的方法,分别检测上述系列猴抗血清。图2a和图2b分别显示了3种捕获试剂对2只猕猴(je12和je68)的系列抗血清的检测结果。其中,je12在感染1型hev的3周后,其抗血清开始显现出对1型hev捕获试剂的强阳性反应;je68在感染1型hev的14周后,其抗血清开始显现出对1型hev捕获试剂的强阳性反应;同时,je12和je68在各个接种后时间点的抗血清对3型和4型捕获试剂的检测均无阳性反应。
使用4型hev病毒株(genbankno.jq655733)采用静脉注射的途径分别攻击3只猕猴(je13、je53和je54),接种后每周采集一次血清,所有的血清以及粪便样品均保存于-60℃以下,避免反复冻融。然后使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,按照实施例1.2和1.3的方法,分别检测上述系列猴抗血清。图3a、图3b和图3c分别显示了3种捕获试剂对3只猕猴(je13、je53和je54)的系列抗血清的检测结果。其中,4型捕获试剂对je13、je53和je544三只猕猴的抗血清均呈现有强阳性反应,而1型和3型捕获试剂则无明显反应,其中仅je54的感染4型hev的第7周的抗血清与3型捕获试剂表现出较弱的反应性,然后采用竞争eia方法对该抗血清样本进行了进一步分析,使用hev1、3、4型和兔型表位多肽混合物(每一种多肽用量均为0.1μg)包被的微孔板,用hev混合表位多肽包被的微孔板对待确定的样品进行抗体滴度测定,选择a450/630约为1的稀释度样品用于血清型的分析。对每份样品,需5孔(分别标记为非抑制对照、1型、3型、4型和兔型)每孔加入50μl已经稀释好的样品,然后在1型、3型、4型和兔型孔中分别加入50μl一定浓度的1型、3型、4型和兔型表位多肽(非抑制对照孔中加入50μl样品稀释液),混匀,37℃孵育30min,pbst洗涤5遍,加入100μl抗人igg抗体或抗兔igg抗体,37℃孵育30min,洗涤5遍,加入100μltmb,37℃孵育15min,最后终止反应,在波长450nm和630nm处读取各孔吸光值a。分别计算1型、3型、4型和兔型多肽的抑制率。若某一表位多肽的抑制率大于50%,则该表位多肽代表的型别为该样品的血清型。计算公式:肽抑制率=(未加肽的样品孔a450/630-加肽的样品孔a450/630)/未加肽的样品孔a450/630×100%。结果发现,仅4型捕获试剂对该抗血清样本能产生明显的抑制效果(抑制率为78.16%)。
上述结果表明,基于hevorf3蛋白第66-87位氨基酸残基的捕获试剂(1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂)对猕猴血清有良好的分型效果,且与不同基因型的抗血清无明显的交叉反应。
实施例4.hev基因分型间接elisa检测法在人抗血清中的分型效果评价
获得3位自然感染3型hev的患者(007b、002b和001b)在感染后不同时间点的人系列抗血清,上述血清盘购自德国biomex公司,货号:scp-hev-007a、scp-hev-002a、scp-hev-001a,患者型别、年龄、感染病毒基因型等信息详见说明书。然后使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,按照实施例1.3的方法,分别检测上述人系列抗血清。图4a、图4b和图4c分别显示了3种捕获试剂对3位患者(007b、002b和001b)的系列抗血清的检测结果。其中,3型捕获试剂对007b、002b和001b三只患者的系列抗血清均呈现有强阳性反应;同时,007b、002b和001b在各个感染后时间点的抗血清对1型和4型捕获试剂的检测均无阳性反应。
获得3位自然感染4型hev的患者(ya701、ya866和ya827)在感染后不同时间点的人系列抗血清,上述血清来自北京佑安医院,经测序证实为hev基因4型。然后使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,按照实施例1.3的方法,分别检测上述人系列抗血清。图5a、图5b和图5c分别显示了3种捕获试剂对3位患者(ya701、ya866和ya827)的系列抗血清的检测结果。其中,3型捕获试剂对ya701、ya866和ya827三只患者的系列抗血清均呈现有强阳性反应;而1型和4型捕获试剂则均无阳性反应。
上述结果表明,基于hevorf3蛋白第66-87位氨基酸残基的捕获试剂对自然感染hev的人血清也具有良好的分型效果。
实施例5.hev基因分型间接elisa检测法在临床血清样本中的分型效果评价
本实施例所述hev基因分型间接elisa检测法,使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,并按照实施例1.2和1.3的方法对待测血清进行检测。
首先使用商业化的hev抗体检测试剂盒(北京万泰公司,国械注准20153401411)检测59例临床肝炎患者的血清样品,其中有19例的抗hev抗体检测呈现阳性。然后再使用3种hev捕获试剂分别对这19例的抗血清进行检测,结果如图6所示,其中有16例对4型捕获试剂的检测呈阳性,而这19例的抗血清对1型和3型捕获试剂的检测均呈阴性。
为了验证捕获试剂的准确性,进一步对上述由捕获试剂鉴定为感染4型hev的16例患者的血清样品进行了基因测序。采用qiaampviralrnaminikit(货号:52904)进行rna的提取,然后使用superscripttmiiifirst-strandsynthesissystem试剂(货号:18080-051)进行逆转录,得到的pcr产物进行套式pcr反应,pcr引物序列见表3。pcr反应条件为94℃预变性5分钟;94℃变性1分钟,50℃退火45秒,72℃延伸1分钟,共35个循环;最后72℃延长10分钟。pcr产物由北京天润奥科生物科技有限公司进行序列测定。利用mega5.2软件进行序列的分析比对:全长基因分型标准株及其genebank登录号分别为:1型:sar-55(m80581,subtype1b),2型:mexico(m74506,subtype2a),3型:prototypeswinehev(af082843,subtype3a),4型:mo(jq655733,subtype4a),swgx40(eu676172,subtype4b),he-jf5(ab220973,subtype4b),w2-5(jq655736,subtype4d),w3(jq655735,subtype4h)。
表3.套式rt-pcr引物
*referencestrain:aj272108(y=torc,w=aort)
结果显示,有11例套式rt-pcr方法检测阳性,经测序证实为基因4型。
上述结果充分表明,结果显示基于hevorf3蛋白第66-87位氨基酸残基的捕获试剂能够用于区分临床血清样品所感染的hev的基因型。
实施例6.hev基因分型间接elisa检测法与商业化hev抗体检测试剂的比较
本实施例所述hev基因分型间接elisa检测法,使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,并按照实施例1.2和1.3的方法对待测血清进行检测。
使用各基因型捕获试剂、商业化的hevigm抗体检测试剂(北京万泰公司,国食药监械(准)字213第3400240号)和hevigg抗体检测试剂(北京万泰公司,国械注准20153401411),分别检测实施例3中所获得的1份实验感染hev1型的猕猴系列血清(je68)和1份实验感染hev4型的猕猴系列血清(je54)。图7a显示了在接种病毒后的不同时间点,1型捕获试剂和商业化试剂分别对1型猕猴抗血清的检测结果,结果显示1型捕获试剂比商业化的hevigm抗体试剂检出时间晚一周,但比商业化的igg抗体试剂要早,且检测的s/co值明显高于商业化的两种试剂。图7b显示了在接种病毒后的不同时间点,4型捕获试剂和商业化试剂分别对4型猕猴抗血清的检测结果,结果显示4型捕获试剂对抗hevigg抗体的检出时间比商业化的igg抗体试剂早一周左右,且检测的s/co值要明显高于后者。上述结果提示,基于hevorf3蛋白第66-87位氨基酸残基的捕获试剂不仅能用于区分受试者所感染的hev的基因型,而且也能用于hev感染的早期诊断。
实施例7.hevorf3蛋白的其它多肽片段用于hev基因分型的效果评价
在本实施例中,对hevorf3蛋白的其它多肽片段的基因分型效果进行了检测。
首先根据hevorf3蛋白的第66-75位氨基酸残基合成了各个基因型的对比多肽,其中各基因型orf3蛋白的第66-75位氨基酸残基如表3所示。由北京中科亚光生物科技有限公司分别合成基因1型、3型和4型的上述对比多肽,并在n端偶联生物素,hplc纯化。基因1型、3型和4型的上述生物素标记的对比多肽分别命名为1型hev对比多肽、3型hev对比多肽和4型hev对比多肽。
表4.
在本实施例中,使用实施例1.1中所获得的1型hev捕获试剂、3型hev捕获试剂和4型hev捕获试剂,以及上述1型hev对比多肽、3型hev对比多肽和4型hev对比多肽,并按照实施例1.2和1.3的方法对待测血清进行检测,其中1型hev对比多肽、3型hev对比多肽和4型hev对比多肽的包被浓度均为10μg/ml。
获得hev1型、3型和4型来源的血清样本,其中hev1型和4型血清样本来自实施例3中实验感染猕猴不同时间段的血清,3型来自biomex公司血清盘,每种基因型各6份。使用各基因型捕获试剂、各基因型对比多肽,分别检测同基因型的血清样本。图8显示了1型捕获试剂和对比多肽对6份1型hev感染样本的检测结果、3型捕获试剂和对比多肽对6份3型hev感染样本的检测结果和4型捕获试剂和对比多肽对6份4型hev感染样本的检测结果,结果显示本发明的1型捕获试剂、3型捕获试剂和4型捕获试剂对同基因型的hev感染抗血清均具有强阳性反应,1型捕获试剂的结合强度(s/co值)甚至高达20以上。相比之下,3型对比多肽对6份3型hev感染样本均无阳性反应,表明其无法用于鉴定受试者是否感染了3型hev;同时,虽然1型对比多肽和4型对比多肽对同基因型的hev感染抗血清呈现阳性反应,但其结合强度显著低于1型捕获试剂和4型捕获试剂(p<0.001)。
上述结果充分表明,基于hevorf3蛋白第66-87位氨基酸残基的捕获试剂可准确、高效地区分和鉴定受试者所感染的hev基因型,但基于hevorf3蛋白其他氨基酸残基的多肽片段(例如,第66-75位氨基酸残基)无法将1型hev、3型hev和4型hev全部区分出来,因此无法用于鉴定受试者所感染的hev基因型。
尽管本发明的具体实施方式已经得到详细的描述,但本领域技术人员将理解:根据已经公布的所有教导,可以对细节进行各种修改和变动,并且这些改变均在本发明的保护范围之内。本发明的全部分为由所附权利要求及其任何等同物给出。
序列表
<110>中国食品药品检定研究院
<120>用于鉴定受试者所感染的hev基因型的方法和试剂盒
<130>idc160164
<160>13
<170>patentinversion3.5
<210>1
<211>114
<212>prt
<213>戊型肝炎病毒(hepatitisevirus)
<400>1
metglythrargprocysalaleuglyleuphecyscyscysserser
151015
cysphecysleucyscysproarghisargprovalserargleuala
202530
alavalvalglyglyalaalaalavalproalavalvalserglyval
354045
thrglyleuileleuserproserglnserproilepheileglnpro
505560
thrproserproprometserproleuargproglyleuaspleuval
65707580
phealaasnproproasphisseralaproleuglyvalthrargpro
859095
seralaproproleuprohisvalvalaspleuproglnleuglypro
100105110
argarg
<210>2
<211>122
<212>prt
<213>戊型肝炎病毒(hepatitisevirus)
<400>2
metasnasnmetserphealaserprometglyserprocysalaleu
151015
glyleuphecyscyscyssersercysphecysleucyscysproarg
202530
hisargprovalserargleualavalalavalglyglyalaalaala
354045
valproalavalvalserglyvalthrglyleuileleuserproser
505560
proserproilepheileglnprothrproserproprometserphe
65707580
hisasnproglyleugluleualaleuaspserargproalaproser
859095
valproleuglyvalthrserproseralaproproleuproproval
100105110
valaspleuproglnleuglyleuargarg
115120
<210>3
<211>114
<212>prt
<213>戊型肝炎病毒(hepatitisevirus)
<400>3
metalametproprocysalaleuglyleuphecysphecysserser
151015
cysphecysleucyscysproarghisargprovalserargleuala
202530
valvalvalglyglyalaalaalavalproalavalvalserglyval
354045
thrglyleuileleuserproserproserproilepheileglnpro
505560
thrproserhisleuthrpheglnproproproglyleugluleuala
65707580
leuaspserargproalahisseralaproleuglyvalthrasnpro
859095
seralaproproleuproprovalvalaspleuproglnproglyleu
100105110
argarg
<210>4
<211>22
<212>prt
<213>人工序列
<220>
<223>1型hev捕获试剂/g1
<400>4
proserproprometserproleuargproglyleuaspleuvalphe
151015
alaasnproproasphis
20
<210>5
<211>22
<212>prt
<213>人工序列
<220>
<223>3型hev捕获试剂/g3
<400>5
proserproprometserphehisasnproglyleugluleualaleu
151015
aspserargproalapro
20
<210>6
<211>22
<212>prt
<213>人工序列
<220>
<223>4型hev捕获试剂/g4
<400>6
proserhisleuthrpheglnproproproglyleugluleualaleu
151015
aspserargproalahis
20
<210>7
<211>10
<212>prt
<213>人工序列
<220>
<223>1型hev对比多肽/refhev-1
<400>7
proserproprometserproleuargpro
1510
<210>8
<211>10
<212>prt
<213>人工序列
<220>
<223>3型hev对比多肽/refhev-3
<400>8
proserproproileserphehisasnpro
1510
<210>9
<211>10
<212>prt
<213>人工序列
<220>
<223>4型hev对比多肽/refhev-4
<400>9
proserhisleuthrpheglnproglnpro
1510
<210>10
<211>23
<212>dna
<213>人工序列
<220>
<223>引物
<400>10
cccttatcctgctgagcattctc23
<210>11
<211>22
<212>dna
<213>人工序列
<220>
<223>引物
<400>11
aaytatgcwcagtaccgggttg22
<210>12
<211>22
<212>dna
<213>人工序列
<220>
<223>引物
<400>12
gtyatgytytgcatacatggct22
<210>13
<211>22
<212>dna
<213>人工序列
<220>
<223>引物
<400>13
agccgacgaaatyaattctgtc22
- 还没有人留言评论。精彩留言会获得点赞!