一种利用生物酶降低含糖饮料甜度的方法与流程
本发明属于低糖食品的制备领域,特别涉及一种利用生物酶降低含糖饮料甜度的方法。
背景技术:
糖类是由碳、氧、氢等元素组成的人类各种生命活动所需能量的主要来源,其中葡萄糖是生物体内新陈代谢必不可少的营养物质。随着人们生活水平的提高,加上不良的饮食习惯造成摄入过多的糖类,导致龋齿、糖尿病和肥胖等多种疾病发生。一般通过控制糖的加入量或者寻找糖的替代品来减少食品中的糖含量,但对于直接由原料发酵而来的饮品,特别是含酒精饮料不能通过此类方法控制食品中的糖含量,因此,亟需开发新的方法降低糖含量。
技术实现要素:
本发明所要解决的技术问题是提供一种利用生物酶降低含糖饮料甜度的方法,本发明方法适用范围广,安全、无毒副作用,降解率可控,能耐受一定浓度的酒精,使用成本低,具有良好的应用前景。
本发明的一种利用生物酶降低含糖饮料甜度的方法,包括:
(1)分别配置葡萄糖氧化酶溶液、过氧化氢酶溶液;
(2)将葡萄糖氧化酶溶液和过氧化氢酶溶液混合,然后共固化,得到共固定化葡萄糖氧化酶-过氧化氢酶;
(3)将葡萄糖氧化酶溶液和/或过氧化氢酶溶液或共固定化葡萄糖氧化酶-过氧化氢酶加入葡萄糖溶液或含糖饮料中在ph为3.0-10.0,温度为30-60℃条件下振荡反应。
所述步骤(1)中葡萄糖氧化酶溶液、过氧化氢酶溶液的溶剂均为缓冲溶液。
所述缓冲溶液的ph值为3.0-10.0,浓度为50-200mm。
所述缓冲溶液由磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠中的一种或几种配制得到。
葡萄糖氧化酶和过氧化氢酶的混合比例,以测定的葡萄糖降解率最高时的酶活比例确定葡萄糖氧化酶和过氧化氢酶各自的最佳单酶添加量。
步骤(2)中葡萄糖氧化酶和过氧化氢酶的比例为0.5:1-150:1。
所述步骤(2)中共固定化为采用细菌纤维素进行共固化,细菌纤维素由木葡糖酸醋杆菌发酵得来。即采用木醋杆菌为菌种,在无菌条件下以接种环或者膜接的方法接种,然后将种子培养液置于30℃,160rpm的摇床中培养12-24h。以5-10%(v/v)的接种量接种于静态发酵培养基中,在30℃恒温培养箱中静置培养5-12d,得细菌纤维素薄膜。
所述共固化方法为吸附法、包埋法、交联法、结合法中的一种或几种。
所述步骤(3)中葡萄糖溶液的浓度为0-400g/l;含糖饮料为乙醇浓度为0-40v/v%的含糖饮料。
所述步骤(3)中可以通过控制氧气的通入量来控制反应进行的程度。
所述步骤(3)中振荡反应为:恒温振荡条件下进行,转速100-200rpm。
步骤(3)中固定化葡萄糖氧化酶-过氧化氢酶,可以重复多次用于含糖饮料的催化降解,每次使用结束后可用缓冲溶液冲洗1-5遍。
步骤(3)中的共固定化葡萄糖氧化酶-过氧化氢酶可重复使用1-8次。
有益效果
本发明适用范围较广,用于食品中不仅安全、无毒副作用,而且反应条件温和、绿色环保;酶降解时将酶固定化可以降低生产成本,可以通过控制氧气的通入量来控制反应的进行,从而可自行控制降解率;能耐受一定浓度的酒精,从而可用于发酵型甜酒等产品的降糖加工,具有良好的大规模应用前景。
附图说明
图1:游离葡萄糖氧化酶在不同温度下对100g/l葡萄糖溶液的降解率;
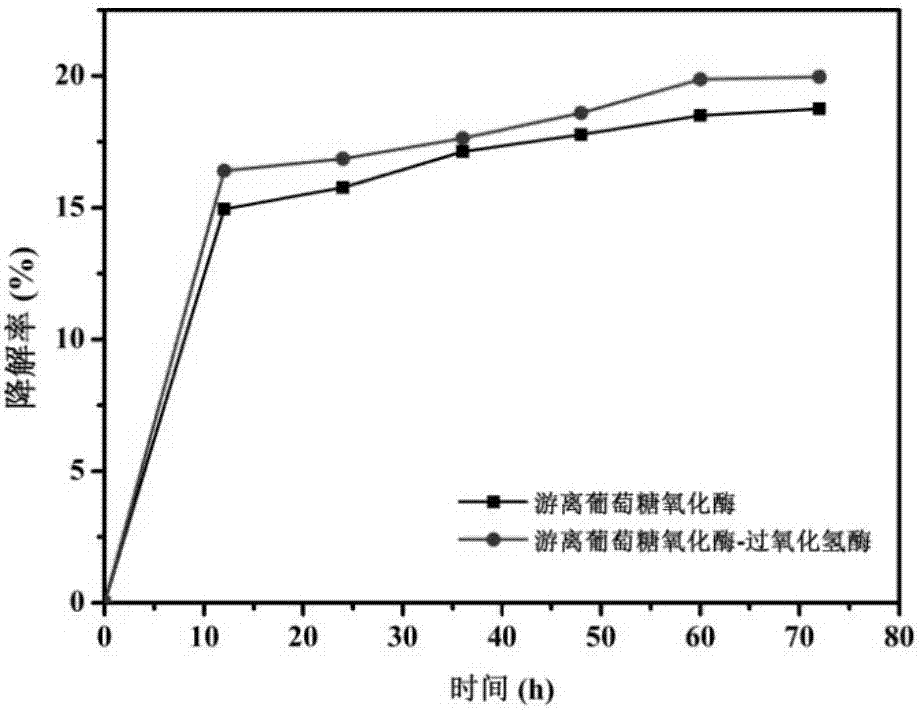
图2:游离葡萄糖氧化酶-过氧化氢酶对葡萄糖溶液的降解率;
图3:游离酶和固定化酶不同温度下的相对酶活力;
图4:游离葡萄糖氧化酶对不同浓度葡萄糖溶液的降解率;
图5:游离葡萄糖氧化酶对不同乙醇含量的葡萄糖溶液的降解率;
图6:游离、固定化葡萄糖氧化酶-过氧化氢酶对含乙醇的葡萄糖溶液的降解率;
图7:固定化酶不同加酶量对甜酒样品的降解;
图8:固定化酶的重复使用次数。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1
(1)稀释葡萄糖氧化酶
用磷酸二氢钠、磷酸氢二钠或磷酸二氢钾、磷酸氢二钾或乙酸、乙酸钠或柠檬酸、柠檬酸钠配制成ph5.0的50-200mm缓冲溶液,将葡萄糖氧化酶固体粉末溶解、稀释,制备成葡萄糖氧化酶溶液。
(2)游离酶液对葡萄糖溶液的降解
配制10mlph5.0的50g/l、100g/l、200g/l、400g/l葡萄糖溶液后,加入200μl游离葡萄糖氧化酶液,分别放置于30-60℃的恒温振荡水浴锅中100-200rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果发现在温度为40℃的条件下对葡萄糖溶液的降解率最高,葡萄糖浓度为100g/l时降解率约为19%,如图1所示。
实施例2
(1)稀释葡萄糖氧化酶、过氧化氢酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,分别将葡萄糖氧化酶、过氧化氢酶固体粉末溶解、稀释,按照过氧化氢酶与葡萄糖氧化酶酶活比例为0.5:1、2.5:1、5:1、25:1、50:1、100:1、150:1将两种酶液混合,成为混合酶液。
(2)游离葡萄糖氧化酶-过氧化氢酶酶液对葡萄糖溶液的降解
分别配制10ml,浓度为50g/l、100g/l、200g/l、400g/l的底物葡萄糖溶液,ph5.0加入200μl酶液,放置于37℃的恒温振荡水浴锅中100-200rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量,从而计算降解率。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果显示,游离葡萄糖氧化酶-过氧化氢酶降解率高于游离葡萄糖氧化酶,如图2所示。
实施例3
(1)稀释葡萄糖氧化酶、过氧化氢酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,分别将葡萄糖氧化酶、过氧化氢酶固体粉末溶解、稀释,按照一定比例将两种酶液混合,成为混合酶液。
(2)固定化葡萄糖氧化酶-过氧化氢酶的制备
固定葡萄糖氧化酶的加入量,变化过氧化氢酶的加入量,使两者的酶活力之比分别为0:1、0.5:1、2.5:1、5:1、25:1、50:1、100:1、150:1,测试产物生成量,在酶活比为25:1时葡萄糖降解率最大,此时的过氧化氢酶与葡萄糖氧化酶的酶活比为最佳的酶活添加比例。
采用吸附法、包埋法、交联法或共价键结合法中的一种方法,以过氧化氢酶与葡萄糖氧化酶的酶活比25:1制备固定化酶,然后取出用ph6.0pbs缓冲溶液冲洗1-5遍,用滤纸吸干表面水分,置于4℃冰箱保存备用;
(3)固定化酶对葡萄糖溶液的降解
配制10mlph5.0的100g/l葡萄糖溶液,加入200μl游离葡萄糖氧化酶液,分别放置于30℃、35℃、40℃、45℃、50℃、55℃、60℃的恒温振荡水浴锅中100rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果如图3所示固定化酶在温度为40℃时的酶活力最高,其中过氧化氢酶与葡萄糖氧化酶的酶活比为25:1。
实施例4
(1)稀释葡萄糖氧化酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,将葡萄糖氧化酶固体粉末溶解、稀释,制备成葡萄糖氧化酶溶液。
(2)游离酶液对葡萄糖溶液的降解
分别配制ph值为3.0-7.0的10ml,50g/l、100g/l、200g/l、400g/l葡萄糖溶液,加入200μl游离葡萄糖氧化酶液,放置于37℃的恒温振荡水浴锅中100rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果显示游离葡萄糖氧化酶在ph值为5.0时降解率最大。
实施例5
(1)稀释葡萄糖氧化酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,将葡萄糖氧化酶固体粉末溶解、稀释,制备成葡萄糖氧化酶溶液。
(2)游离酶液对葡萄糖溶液的降解
分别配制10ml,浓度为50g/l、100g/l、200g/l、400g/l的底物葡萄糖溶液,ph5.0加入200μl酶液,放置于37℃的恒温振荡水浴锅中100rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果显示游离葡萄糖氧化酶在底物浓度为50g/l时,降解率最大约为36%,如图4所示。
实施例6
(1)稀释葡萄糖氧化酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,将葡萄糖氧化酶固体粉末溶解、稀释,制备成葡萄糖氧化酶溶液。
(2)游离葡萄糖氧化酶液对葡萄糖溶液的降解
配制乙醇浓度(v/v%)分别为0-40%的200g/l的葡萄糖溶液,加入200μl葡萄糖氧化酶液、在37℃、ph5.0、100r/min的搅拌条件下反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果显示游离葡萄糖氧化酶降解含有乙醇的葡萄糖溶液时,醇浓为0-40%(v/v%)的降解率均约为4.5%,如图5。
实施例7
(1)稀释葡萄糖氧化酶、过氧化氢酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,分别将葡萄糖氧化酶、过氧化氢酶固体粉末溶解、稀释,按照过氧化氢酶与葡萄糖氧化酶酶活比例为0.5:1、2.5:1、5:1、25:1、50:1、100:1、150:1将两种酶液混合,成为混合酶液。
(2)固定化葡萄糖氧化酶-过氧化氢酶的制备
以葡萄糖降解率最大时的酶活比为最佳的酶活添加比例,采用吸附法、包埋法、交联法和结合法以过氧化氢酶与葡萄糖氧化酶的酶活比25:1制备固定化酶,然后取出用ph6.0pbs缓冲溶液冲洗1-5遍,用滤纸吸干表面水分,置于4℃冰箱保存备用;
(3)游离双酶、固定化双酶对葡萄糖溶液的降解
配制10mlph5.0的0-400g/l,含有乙醇0-40(v/v%)葡萄糖溶液,加入200μl游离葡萄糖氧化酶液,分别放置于40℃的恒温振荡水浴锅中100-200rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果如图6所示固定化双酶降解率高于游离双酶的降解率,且固定化双酶的降解率结晶不含乙醇。
实施例8
(1)稀释葡萄糖氧化酶、过氧化氢酶
用磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、乙酸、乙酸钠、柠檬酸、柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,分别将葡萄糖氧化酶、过氧化氢酶固体粉末溶解、稀释,按照过氧化氢酶与葡萄糖氧化酶酶活比例为0.5:1、2.5:1、5:1、25:1、50:1、100:1、150:1将两种酶液混合,成为混合酶液。
(2)固定化葡萄糖氧化酶-过氧化氢酶的制备
采用过氧化氢酶与葡萄糖氧化酶的最佳酶活比25:1,静置吸附24h,制备固定化酶,然后去除用ph6.0pbs缓冲溶液冲洗,用滤纸吸干表面水分,置于4℃冰箱保存备用;
(3)固定化酶对含糖饮料的降解
在含糖饮料中加入以上固定化酶,在37℃、200r/min的摇床中反应1h,重复使用多次,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果如图8所示,固定化酶重复使用少于4次时酶活降低较少。在使用7至8次之后,相对酶活力急剧下降,最终相对酶活仅剩22.5%。
实施例9
(1)稀释葡萄糖氧化酶
用磷酸二氢钠和磷酸氢二钠配制ph5.0的pbs缓冲溶液,将葡萄糖氧化酶固体粉末溶解、稀释,成为葡萄糖氧化酶溶液。
(2)游离酶液对葡萄糖溶液的降解
配制10mlph5.0的100g/l葡萄糖葡萄糖溶液,加入200μl游离葡萄糖氧化酶液,连续泵入氧气,分别放置于30-60℃的恒温振荡水浴锅中100-200rpm条件下振荡反应。每隔一段时间取样测试,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果发现在葡萄糖转化为糖酸的转化率可达100%,甜度降为0。并且可以通过调节氧气通入量来控制降糖率。
实施例10
(1)稀释葡萄糖氧化酶、过氧化氢酶
用乙酸和乙酸钠,或者柠檬酸和柠檬酸钠等药品配制成ph5.0的50-200mm缓冲溶液,分别将葡萄糖氧化酶、过氧化氢酶固体粉末溶解、稀释,按照过氧化氢酶与葡萄糖氧化酶酶活比为0.5:1、2.5:1、5:1、25:1、50:1、100:1、150:1将两种酶液混合,成为混合酶液。
(2)固定化葡萄糖氧化酶-过氧化氢酶的制备
采用过氧化氢酶与葡萄糖氧化酶的最佳酶活比25:1,静置吸附24h,制备固定化酶,然后用ph6.0pbs缓冲溶液冲洗,用滤纸吸干表面水分,置于4℃冰箱保存备用;
(3)固定化酶不同加酶量对含糖酒精饮料的降解
以过氧化氢酶和葡萄糖氧化酶的酶活比例为25:1制备固定化酶,其中god含量为701.25u/l、1402.5u/l、2805u/l、5610u/l、11220u/l。
在含糖酒精饮料(乙醇浓度10-40v/v%)中)分别加入上述固定化酶,在37℃、200r/min的摇床中反应1h,重复使用多次,用高效液相色谱(hplc)检测溶液中生成的葡萄糖酸的量以及葡萄糖减少的量。
hplc(aminexhpx-87hionexclusioncolumn,蒸发光散射检测器和紫外检测器同时使用)的检测方法,流动相:0.0015mol/l稀硫酸;流动相流速:0.6ml/min;柱温:50℃;检测波长:235nm;进样量:20μl。
结果显示制备固定化酶时加酶量越大,固定化酶对酒样品中含糖量的降解率越大。
- 还没有人留言评论。精彩留言会获得点赞!