化合物及其有机电子装置的制作方法
本发明是关于一种新颖化合物以及一种使用其的有机电子装置,尤指一种用于电子传输层的新颖化合物以及使用其的有机电子装置。
背景技术:
随着科技的进步,各种使用有机材料制成的有机电子装置蓬勃发展,常见的有机电子装置如有机发光二极管(organiclightemittingdevice,oled)、有机光敏晶体管(organicphototransistor)、有机光伏打电池(organicphotovoltaiccell)和有机光检测器(organicphotodetector)。
oled最初是由伊士曼柯达公司(eastmankodak)所发明并提出,伊士曼柯达公司的邓青云博士和stevenvanslyke以真空蒸镀法(vacuumevaporationmethod)于形成有有机芳香二元胺电洞传输层的透明氧化铟锡(indiumtinoxide,ito)玻璃上沉积电子传输材料{例如三(8-羟基喹啉)铝[tris(8-hydroxyquinoline)aluminum(iii),简称为alq3]};再于电子传输层上沉积金属电极,即可完成oled的制作。oled因兼具反应速率快、质轻、薄形化、广视角、亮度高、对比高、无需设置背光源以及低耗能的优点,因此备受关注,但oled仍具有低效率和寿命短的问题。
为了克服低效率的问题,其中一种改善方式为于阴极和阳极间设置中间层,请参阅图1所示,改良的oled依序设置有基板11、阳极12、电洞注入层13(holeinjectionlayer,hil)、电洞传输层14(holetransportlayer,htl)、发光层15(anemittinglayer,el)、电子传输层16(electrontransportlayer,etl)、电子注入层17(electroninjectionlayer,eil)和阴极18。当于阳极12和阴极18施加电压时,由阳极12射出的电洞会穿过hil和htl并移动至el,而由阴极18射出的电子会穿过eil和etl移动至el,使电洞和电子在el层重组成激子(exciton),当激子由激发态衰退返回基态时即可产生光线。
另一改善方式为改良oled中etl的材料,使电子传输材料展现出电洞阻挡能力,传统的电子传输材料包括3,3′-[5′-[3-(3-吡啶基)苯基][1,1′:3′,1″-三联苯]-3,3″-二基]联吡啶{(3,3′-[5′-[3-(3-pyridinyl)phenyl][1,1′:3′,1″-terphenyl]-3,3″-diyl]bispyridine,tmpypb}、3-(4-联苯基)-5-(4-叔丁基苯基)-4-苯基-4h-1,2,4-三嗪(3-(biphenyl-4-yl)-5-(4-tert-butylphenyl)-4-phenyl-4h-1,2,4-triazole,taz)、1,3,5-三(1-苯基-1h-苯并咪唑-2-基)苯[1,3,5-tris(1-phenyl-1h-benzimidazol-2-yl)benzene,tpbi]、三(2,4,6-三甲基-3-(3-吡啶基)苯基)硼烷[tris(2,4,6-trimethyl-3-(pyridin-3-yl)phenyl)borane,3tpymb]、1,3-联(3,5-二吡啶-3-基-苯基)苯[1,3-bis(3,5-dipyrid-3-yl-phenyl)benzene,bmpypb]和9,10-二(3-(3-吡啶基)苯基)蒽[9,10-bis(3-(pyridin-3-yl)phenyl)anthracene,dpypa]。
然而,即使使用了所述电子传输材料,oled的电流效率仍具有可改善的空间,因此,本发明提供了一种新颖的化合物以克服传统低电流效率的问题。
技术实现要素:
本发明的目的为提供一种新颖化合物,其可用于有机电子装置。
本发明的另一目的为提供一种使用该新颖化合物的有机电子装置,藉此降低有机电子装置的驱动电压,并提升有机电子装置的效率。
为达上述目的,本发明的新颖化合物可以式(i)表示:
于式(i)中,x1和x2各自独立为c(ra),且该二ra彼此相同或不同,该二ra连接构成芳香环;
于式(i)中,x3和x4各自独立为c(rb),且该二rb彼此相同或不同,该二rb连接构成多芳香环;
于式(i)中,z1至z10各自独立选自于由下列所构成的群组:氢原子、氘原子、三氟甲基、卤基、氰基、硝基、碳数为1至40的烷基、碳数为2至40的烯基、碳数为2至40的炔基、环上碳数为3至60的环烷基、环上碳数为3至60的杂环烷基、环上碳数为6至60的芳香基、环上碳数为3至60的杂芳基、碳数为1至40的烷氧基、环上碳数为6至60的芳氧基、碳数为1至40的硅烷基(alkylsilylgroup)、环上碳数为6至60的芳硅基(arylsilylgroup)、碳数为1至40的硼烷基(alkylboron)、环上碳数为6至60的芳硼基(arylborongroup)、碳数为1至40的膦基(phosphinegroup)和碳数为1至40的氧膦基(phosphineoxidegroup)。
根据本发明,式(i)中自x3和x4延伸形成的该多芳香环包含至少二环状芳香环彼此连接或并合,且该二环状芳香环的环状主结构是由碳原子所组成,即该二环状芳香环不是杂芳环且不包含任何氮、氧或硫等原子,然而,该二环状芳香环可连接有任何取代基,该取代基可包含任何原子并不仅限于碳原子。
根据本发明,式(i)中x1和x2包含的双键和该二c(ra)连接形成的双键互为共轭双键(conjugateddoublebond),并构成前述的该芳香环;相同的,式(i)中x3和x4包含的双键和该二c(rb)连接形成的双键互为共轭双键,并构成前述的该多芳香环;根据本发明,自x1和x2延伸形成的该芳香环和自x3和x4延伸形成的该多芳香环彼此连接并合而成包含至少六共轭双键的芳香基,更佳的,自x1和x2延伸形成的该芳香环和自x3和x4延伸形成的该多芳香环彼此连接并合而成包含至少八共轭双键的芳香基。
式(i)中自x1和x2延伸形成的该芳香环可以是经取代或未经取代且环上碳数为6至60的碳环,更佳的,自x1和x2延伸形成的该芳香环可以是经取代或未经取代且环上碳数为6至20的碳环。举例而言,该经取代或未经取代且环上碳数为6至60的碳环可以是经取代或未经取代的苯环(benzenering)、经取代或未经取代的萘环(naphthalenering)、经取代或未经取代的蒽环(anthracenering)、经取代或未经取代的菲环(phenanthrenering)、经取代或未经取代的芴环(fluorenering)、经取代或未经取代的芘环(pyrenering)、经取代或未经取代的苯并菲(benzophenanthrenering)、经取代或未经取代的苯并芘(benzopyrenering)、经取代或未经取代的荧蒽环(fluoranthenering)或经取代或未经取代的苯并荧蒽环(benzofluoranthenering),但不限于此。更佳的,该经取代或未经取代且碳数为6至60的碳环为经取代或未经取代的苯环结构。前述环上碳数为6至60的碳环上的取代基可以是但不限于:氘原子、卤基、氰基、硝基、碳数为1至12的烷基、碳数为2至12的烯基或碳数为2至12的炔基。
式(i)中自x3和x4延伸形成的该多芳香环可以是经取代或未经取代的萘环、经取代或未经取代的蒽环、经取代或未经取代的菲环、经取代或未经取代的芴环、经取代或未经取代的芘环、经取代或未经取代的苯并菲、经取代或未经取代的苯并芘、经取代或未经取代的荧蒽环或经取代或未经取代的苯并荧蒽环,但不限于此。前述多芳香环至少具有一取代基,该取代基可以是但不限于:氘原子、碳数为1至12的烷基、碳数为2至12的烯基、碳数为2至12的炔基或碳数为6至12的芳香基。例如,该经取代的芴环可以是经一甲基、二甲基或二甲苯基取代的芴环,即该经取代的芴环可以是9-甲基芴环(9-methylfluorenering)、9,9-二甲基芴环(9,9-dimethylfluorenering)或9,9-二甲苯基芴环(9,9-diphenylfluorenering)。
举例来说,该化合物可以下列式(i-i)至(i-xii)表示:
在上式(i-i)至(i-xii)中,n1是0至4的正整数,t可以是但不限于:氢原子、氘原子、甲基、乙基、丙基、丁基、戊基、己基或苯基。
较佳的,式(i)中z1至z8中至少一个是选自于由下列所构成的群组:具有至少一官能基且碳数为1至40的烷基、具有至少一官能基且碳数为2至40的烯基、具有至少一官能基且碳数为2至40的炔基、具有至少一官能基且环上碳数为3至60的环烷基、具有至少一官能基且环上碳数为3至60的杂环烷基、具有至少一官能基且环上碳数为6至60的芳香基、具有至少一官能基且环上碳数为3至60的杂芳基、具有至少一官能基且碳数为1至40的烷氧基、具有至少一官能基且环上碳数为6至60的芳氧基、具有至少一官能基且碳数为1至40的硅烷基、具有至少一官能基且环上碳数为6至60的芳硅基、具有至少一官能基且碳数为1至40的硼烷基、具有至少一官能基且环上碳数为6至60的芳硼基、具有至少一官能基且碳数为1至40的膦基和具有至少一官能基且碳数为1至40的氧膦基。所述该至少一官能基是选自于由下列所构成的群组:氰基、硝基、三氟甲基、氟基和氯基。而式(i)中z1至z8中的其他者可以是氢原子、氘原子或其他前述的取代基,该官能基选自于由氰基、硝基、三氟甲基、氟基和氯基所构成的群组。
更佳的,式(i)中z1至z8中至少一个是特定的芳香取代基,该芳香取代基是选自于由下列所构成的群组:
其中,r1至r7各自独立选自于由下列所构成的群组:氢原子、氘原子、三氟甲基、卤基、氰基、硝基、碳数为1至12的烷基、碳数为2至12的烯基、碳数为2至12的炔基、环上碳数为3至30的环烷基、环上碳数为3至30的杂环烷基、环上碳数为6至30的芳香基、环上碳数为3至20的杂芳基、碳数为1至40的烷氧基、环上碳数为6至30的芳氧基、碳数为1至40的硅烷基、环上碳数为6至30的芳硅基、碳数为1至40的硼烷基、环上碳数为6至30的芳硼基、碳数为1至30的膦基和碳数为1至30的氧膦基;
其中n为0至4的正整数;m为0至3的正整数;o是0至3的正整数;m和o的总和小于或等于5。
较佳的,r1至r3各自独立为苯基、吡啶基、嘧啶基、吡嗪基、哒嗪基、苯并吡啶基、苯并嘧啶基、苯并吡嗪基或苯并哒嗪基,但不限于此。
较佳的,式(i)中z1、z2、z3、z6、z7和z8中至少一个是前述特定芳香取代基;z4和z5各自独立选自于由下列构成的群组:氢原子、氘原子、碳数为1至12的烷基、碳数为2至12的烯基和碳数为2至12的炔基。或者,式(i)中z2、z3、z6和z7中至少一个是前述特定芳香取代基,且z1、z4、z5、z8各自独立选自于由下列构成的群组:氢原子、氘原子、碳数为1至12的烷基、碳数为2至12的烯基和碳数为2至12的炔基。
更佳的,式(i)中z2、z3、z6和z7中至少一个是选自于由下列构成的群组:
更佳的,式(i)中z1、z2、z3、z6、z7和z8中至少一个是经二苯基、二吡啶基、二嘧啶基、二吡嗪基、二哒嗪基、二苯并吡啶基、二苯并嘧啶基、二苯并吡嗪基或二苯并哒嗪基取代的三嗪基(triazinegroup)。
根据本发明,式(i)中的z1和z8可以是相同或是不同,z2和z7可以是相同或是不同,z3和z6可以是相同或是不同;于其中一实施例,z1、z2、z3、z6、z7和z8中的任其中二者可以是上述相同的取代基,而z1、z2、z3、z6、z7和z8中其他者可以选自于由下列所构成的群组:氢原子、氘原子、卤基、氰基、硝基、三氟甲基、碳数为1至12的烷基、碳数为2至12的烯基和碳数为2至12的炔基。
例如,z1、z4至z8各自独立为氢原子或氘原子,z2和/或z3是前述特定芳香取代基;或者,z1、z2、z4、z5、z7和z8各自独立为氢原子或氘原子,z3和z6皆为前述特定芳香取代基。
于式(i)中,z9和z10可以是相同或是不同,较佳的,z9和z10各自独立选自于由下列所构成的群组:氢原子、氘原子、三氟甲基、卤基、氰基、硝基、碳数为1至40的烷基、碳数为2至40的烯基、碳数为2至40的炔基、环上碳数为3至60的环烷基、环上碳数为3至60的杂环烷基、环上碳数为6至60的芳香基和环上碳数为3至60的杂芳基。更佳的,z9和z10各自独立选自于由下列所构成的群组:氢原子、氘原子、三氟甲基、氟基、溴基、氰基、硝基、碳数为1至40的烷基、碳数为2至40的烯基、碳数为2至40的炔基、环上碳数为6至60的芳香基和环上碳数为3至60的杂芳基。
具体而言,化合物可以选自于由下列所构成的群组:
化合物clxxxiii;化合物clxxxiv;化合物clxxxv;和化合物clxxxvi。
本发明提供了一种有机电子装置,该有机电子装置包括第一电极、第二电极和设置于该第一电极和该第二电极间的有机层,该有机层具有前述化合物。
较佳的,该有机电子装置为有机发光二极管。更佳的,本发明的新颖化合物可被用于形成电子传输层或电洞阻挡层的材料。
具体而言,该有机发光二极管包括:电洞注入层、电洞传输层、发光层、电子传输层和电子注入层;该电洞注入层形成于该第一电极上;该电洞传输层形成于该电洞注入层上;该发光层形成于该电洞传输层上;该电子传输层形成于该发光层上;该电子注入层形成于该电子传输层和该第二电极之间。
于其中一实施例,该有机层可以为电子传输层,即该电子传输层包含前述的新颖化合物。
较佳的,该电洞注入层可以为双层结构,即该oled于第一电极和电洞传输层之间具有第一电洞注入层和第二电洞注入层。
较佳的,该电洞传输层亦可以为双层结构,即该oled于电洞注入层的双层结构与发光层之间具有第一电洞注入层和第二电洞注入层。
较佳的,该电子传输层可以由新颖化合物(如所述化合物i至xviii)所制成,本发明的oled相较于商业上的oled具有较佳的电流效率。其中,商业上oled中使用的已知传输层材料如2-{4-[9,10-二(2-萘基)-2-蒽基]苯基}-1-苯基-1h-苯并[d]咪唑(2-[4-(9,10-di(naphthalen-2-yl)anthracen-2-yl)phenyl]-1-phenyl-1h-benzo[d]imidazole)、联(2-甲基-8-羟基喹啉)(p-苯基苯酚)铝(bis(2-methyl-8-quinolinolato)(p-phenylphenolato)aluminum)或2-(4-联苯基)-5-(4-叔丁基苯基)-1,3,4-恶二唑(2-(4-biphenylyl)-5-(4-tert-butylphenyl)-1,3,4-oxadiazole),pbd)。
较佳的,该oled包括电洞阻挡层,该电洞阻挡层形成于电子传输层和发光层之间,可防止电洞由发光层移动至电子传输层,所述电洞阻挡层可由上述新颖化合物、2,9-二甲基-4,7-联苯基-1,10-邻二氮杂菲(2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline,bcp)或2,3,5,6-四甲基-1-苯基-1,4-邻苯二甲酰亚胺(2,3,5,6-tetramethyl-phenyl-1,4-(bis-phthalimide),tmpp)所形成,但并不仅限于此。
较佳的,该oled包括电子阻挡层,该电子阻挡层形成于电洞传输层和发光层之间,可防止电子由发光层移动至电洞传输层,所述电子阻挡层可由9,9’-(1,1’-联苯基)-4,4’-二基二-9h-咔唑(9,9'-(1,1'-biphenyl)-4,4'-diylbis-9h-carbazole,cbp)或4,4',4”-三(n-咔唑基)三苯胺(4,4',4”-tri(n-carbazolyl)-triphenylamine,tcta)所形成,但并不仅限于此。
当oled设置有电洞阻挡层和/或电子阻挡层时,本发明的oled相较于传统的oled具有较高的发光效率。
所述第一和第二电洞传输层可以由n1,n1’-(联苯-4,4’-二基)二(n1-(1-萘基))-n4,n4'-二苯基苯-1,4-二胺(n1,n1’-(biphenyl-4,4'-diyl)bis(n1-(naphthalen-1-yl)-n4,n4’-diphenylbenzene-1,4-diamine))或n4,n4'-二(萘-1-基)-n4,n4’-二苯联苯基-4,4'-二胺(n4,n4'-di(naphthalen-1-yl)-n4,n4’-diphenylbiphenyl-4,4'-diamine,npb)所制成。
所述电洞注入层可由聚苯胺或聚乙烯基二氧噻吩(polyethylenedioxythiophene)所制成,但并不仅限于此。
所述发光层可由发光材料制成,该发光材料包括主发光体(host)和掺杂物(dopant),其中发光材料中的主发光体可以是但不限于9-[4-(1-萘基)苯基]-10-(2-萘基)蒽(9-(4-(naphthalen-1-yl)phenyl)-10-(naphthalen-2-yl)anthracene)。
针对红光oled,发光层中的掺杂物(dopant)可以为具有苝配位基(peryleneligands)、荧蒽配位基(fluorantheneligands)或二茚并配位基(periflantheneligands)的二价铱有机金属化合物,但不限于此。针对绿光oled,发光层中的掺杂物可以为二氨基芴(diaminofluorenes)、蒽二胺(diaminoanthracenes)或具有苯基吡啶配位基(phenylpyridineligands)的二价铱有机金属化合物,但不限于此。针对蓝光oled,发光层中的掺杂物可以为二氨基芴、蒽二胺、芘二胺(diaminopyrenes)或具有苯基吡啶配位基的二价铱有机金属化合物,但不限于此。通过不同的主发光体材料,oled可发出红光、绿光或蓝光。
所述电子注入层可以电子注入材料制成,例如8-氧代萘-1-基锂[(8-oxidonaphthalen-1-yl)lithium(ii)],但不限于此。
所述第一电极可以为氧化铟锡电极(indium-dopedtinoxideelectrode),但并不仅限于此。
所述第二电极的功函数(workfunction)低于第一电极的功函数。因此,第二电极可以是但不局限于铝电极、铟电极或镁电极。
本发明的其他目的、功效和技术特征,会以图、实施例和比较例进行更详细的说明。
附图说明
图1为oled的侧视剖面图。
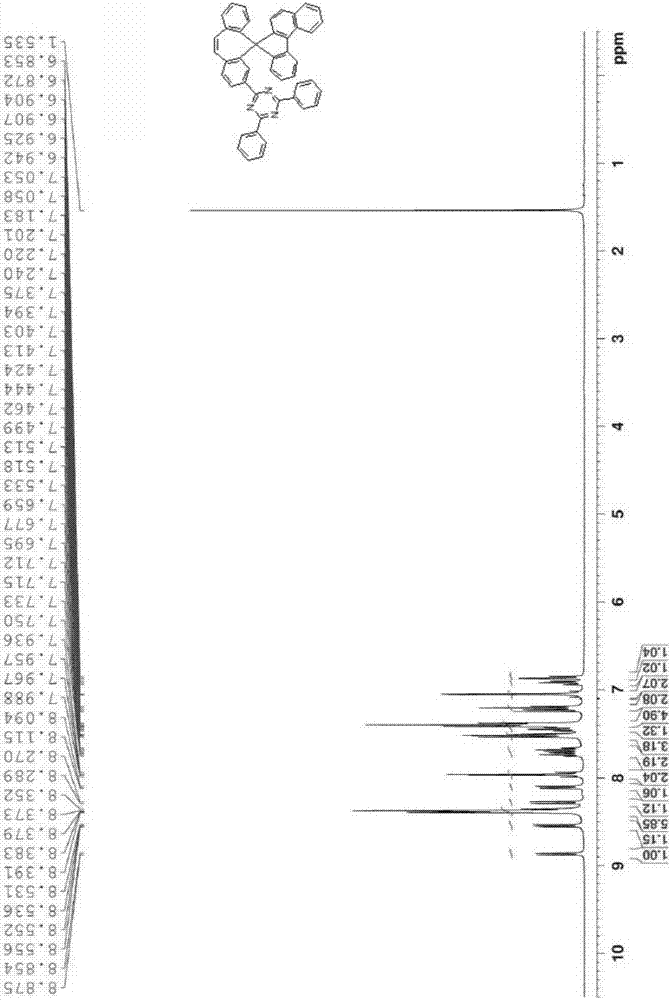
图2至图19分别为化合物1至18的氢核磁共振光谱图。
具体实施方式
以下列举数种实施例作为例示说明本发明的化合物及其有机电子装置的实施方式,以突显本发明相较于现有技术的差异;本领域技术人员可通过本说明书的内容轻易了解本发明所能达成的优点与功效,并且于不背离本发明的精神下进行各种修饰与变更,以施行或应用本发明的内容。
中间物a1的合成
中间物a1(intermediatea1)用于制备一种新颖化合物,中间物a1可通过下述合成机制a1中的步骤进行合成。
步骤1:合成中间物a1-1
混合86克(1.0当量)的3-溴二苯并[a,d]环庚烯-5-酮(3-bromodibenzo[a,d]cyclohepten-5-one)、106克(2.0当量)的n-溴代丁二酰亚胺(n-bromosuccinimide,nbs)和0.7克(0.01当量)的过氧化苯甲酰(benzylperoxide)于430毫升的四氯化碳(carbontetrachloride,ccl4)中,并加热至85℃进行反应,在反应的过程中以高效液相层析仪(highperformanceliquidchromatography,hplc)进行监测;当反应完成后,过滤分离反应所产生的沉淀物,使沉淀物以甲醇冲洗并再结晶纯化,再经浓缩和干燥后可获得123克的白色固体产物,产率为92.3%。经场脱附质谱(fielddesorptionmassspectroscopy,fd-ms)分析确定,白色固体产物即为中间物a1-1。fd-ms分析结果:c15h9br3o,理论值444.94,检测值444.94。
步骤2:合成中间物a1
使中间物a1-1(1.0当量)溶于二甲基亚砜(dimethylsulfoxide,dmso)(相对于反应物w/v=1/3)中并加热至70℃,反应过程中以hplc监测,在反应完成后,以冰水急速冷却并将沉淀物过滤再以硅胶管柱层析纯化,可获得淡黄色固体产物中间物a1,产率为93%。经fd-ms分析确定,fd-ms分析的结果:c15h9bro,理论值285.14,检测值为285.14。
中间物a2的合成
中间物a2用于制备一种新颖化合物,中间物a2是以类似于合成中间物a1的步骤1和步骤2,其差异在于:起始物3-溴二苯并[a,d]环庚烯-5-酮以2-溴二苯并[a,d]环庚烯-5-酮(casno.198707-82-3)代替,中间物a2的合成路径统整于合成机制a2中,在合成机制a2中所有中间物的分析方法皆同前述,分析结果列于下表1。
合成机制a2
中间物a3的合成
中间物a3用于制备一种新颖化合物,中间物a3是以类似于合成中间物a1的步骤1和步骤2所合成,其差异在于起始物3-溴二苯并[a,d]环庚烯-5-酮以3,7-二溴二苯并[a,d]环庚烯-5-酮(3,7-dibromodibenzo[a,d]cyclohepten-5-one)(casno.226946-20-9)代替,中间物a3的合成路径统整于合成机制a3中,在合成机制a3中所有中间物的分析方法皆同前述,分析结果列于下表1。
表1:各中间物的化学结构式和产率以及以fd-ms分析所得分子式和质量。
中间物a1至a3的修饰
除了中间物a1至a3之外,本领域技术人员可更替合成机制a1至a3中的起始物,并以类似于合成机制a1至a3的合成路径合成出其他中间物,例如以下列出的中间物a4至a15:
中间物b1和b3至b6的合成
中间物b1和b3至b6是将1-溴-2-碘苯(1-bromo-2-iodobenzene)与芳基硼酸反应而得,以下将芳基硼酸称为“反应物an(reactantan)”,中间物bn的合成路径如合成机制b-1所示。在合成机制b-1中,“反应物an”选自下表2中的反应物a1至a5;“中间物bn(intermediatebn)”选自下表2中的中间物b1和b3至b6。
根据合成机制b1,中间物b1和b3至b6是根据以下步骤进行合成。
1当量的1-溴-2碘苯、1.2当量的反应物an、3.0当量的碳酸钾、200毫升的甲苯、0.06当量的三苯基膦(triphenylphosphine,pph3)和0.015当量的乙酸钯于70℃下混合,当反应完成后,使混合液冷却至室温后,通过饱和食盐水和ea萃取获得有机层并以硫酸镁除水,接着以硅胶过滤,再将滤物以己烷洗涤并过滤获得中间物bn。在合成机制b中所有中间物bn的分析方法皆同前述,分析结果列于下表2。
表2:用于制备中间物b1和b3至b6的反应物an的化学结构式,中间物b1和b3至b6的化学结构式和产率以fd-ms分析所得分子式和质量。
中间物b2的合成
除了合成机制b-1之外,中间物b2可另以合成机制b-2合成。
步骤1:中间物b2-1的合成
混合0.05当量的双三苯基磷二氯化钯[dichlorobis-(triphenylphosphine)palladium),pd(pph3)2cl2]、1当量的2-溴苯甲醛、四氢呋喃(tetrahydrofuran,thf)(0.13至0.15m)和3当量的三乙基甲胺,在室温搅拌10分钟后将1.5当量的苯乙炔和0.05当量的碘化铜加入混合溶液中,并使之在室温下搅拌24小时,接着以饱和氯化铵水溶液急速冷却反应溶液,并以醋酸乙酯萃取有机相、以硫酸镁干燥、过滤再于低压环境下浓缩产物,将浓缩后的粗产物以硅胶管柱层析纯化获得中间物b2-1,产率为92.4%,产物经fd-ms分析结果为:c15h10o,理论分子量为206.64,测量分子量为206.64。
步骤2:中间物b2的合成
将1.0当量的中间物b2-1、0.05当量的三氟甲烷磺酸铜(copper(ii)trifluoromethanesulfonate,cu(otf)2)、反应物的五倍体积的1,2-二氯乙烷在室温、氩气的环境中依序加入1.2当量的1-(2-溴乙炔基)苯和1.0当量的三氟乙酸中,接着加热至100℃搅拌15分钟再静置冷却至室温,加入饱和的碳酸氢钠水溶液并以乙醚萃取三次,合并萃取而得的有机相后以盐水洗涤、以硫酸镁干燥再使溶剂挥发获得粗产物,将粗产物以己烷作为洗提液并以硅胶管柱层析纯化获得中间物b2,产率为80%,产物经fd-ms分析结果为:c16h11br,理论分子量为283.16,测量分子量为283.16。
中间物b1至b6的修饰
除了前述中间物b1至b6,本领域技术人员可通过采用有别于反应物a1至a5的芳基硼酸与1-溴-2碘苯反应,以类似于合成机制b-1的合成步骤成功合成其他中间物bn;同样的,本领域技术人员亦可使用类似于合成机制b-2的方式合成出其他中间物bn。例如下列中间物b7至b14:
中间物c的合成
前述中间物b1至b14(尤其指中间物b1至b6)可另用于合成中间物cn,中间物cn的合成路径如合成机制c-1所示。在合成机制c-1中,“中间物an”选自于包括中间物a1至a15及其相似物的群组;“中间物bn”选自于包括中间物b1至b14及其相似物的群组;“中间物cn”选自于表3-1中包括中间物c1至c9的群组;中间物c1至c9分别以下述步骤所合成。
步骤1:醇中间物(中间物cn-1)的合成
1.0当量的中间物bn溶于120毫升、0.4m的thf中,降温至-78℃后缓慢加入1.0当量、2.5m的正丁基锂(n-butyllithium,n-buli)并搅拌1小时,接着将0.7当量的中间物an加入反应溶液中并于室温下再搅拌3小时,反应完成后,以饱和氯化铵水溶液冷却反应溶液并萃取有机相,分离有机相后以石油醚再结晶产物获得白色产物,经fd-ms分析后确定为中间物cn-1,各中间物cn-1的化学结构式及fd-ms的测量结果列于表3-1中。
步骤2:中间物cn的合成
将1.0当量的中间物cn-1、醋酸(相较于反应物w/v=1/3)和五滴硫酸混合并于110℃下搅拌6小时,再以旋转蒸发器去除溶剂,并通过管柱层析纯化,再以甲苯使残余物在结晶获得中间物cn,中间物cn以fd-ms分析确定,并将分析结果列于表3-1中。
表3-1:合成中间物c1至c9使用的中间物an和bn;醇中间物的化学结构式;中间物c1至c9的化学结构式和产率以fd-ms侧得的分子式和质量。
中间物c1至c9的修饰
除了前述中间物c1至c9,本领域技术人员可通过置换除了中间物a1至a3外的其他中间物an,或是置换除了中间物b1至b6的其他中间物bn,使用类似于反应机制c-1的合成路径合成出其他中间物cn,例如下列的中间物c10至c21:
中间物cn-b的合成
前述中间物cn可再通过miyaura硼基化反应(miyauraborylationreaction)进一步修饰为中间物cn-b,“中间物cn-b”是将中间物cn的溴基取代为频那醇硼基[(pinacolato)borongroup],中间物cn-b可通过下述合成机制c1-b中的合成路径合成。
1.2当量的联硼酸频那醇酯[bis(pinacolato)diboron]、1.0当量的中间物cn、0.015当量的[1,1-双(二苯基膦基)二茂铁]二氯化钯[1,1-bis(diphenylphosphino)-ferrocenedichloropalladium(ii),pdcl2(dppf)]和3.0当量的醋酸钾于在0.3m的无水1,4-二恶烷(1,4-dioxane)中形成的混合溶液,并在110℃的氮气环境下搅拌8小时,待冷却至室温后,于低压环境下去除溶剂,并将残余物以管柱层析纯化获得白黄色产物。该白黄色产物的化学结构式和产率以及fd-ms分析的分子式和质量结果列于表3-2中。
表3-2:合成中间物cn-b使用的中间物cn以及中间物cn-b的化学结构式和产率以fd-ms分析而得的分子式和质量。
中间物cn-b的修饰
除了上述中间物cn和cn-b之外,本领域技术人员可任选自前述中间物cn所构成的群组,并以类似于合成机制c1-b的方式对任一中间物cn进行miyaura硼基化反应以合成中间物cn-b。
新颖化合物的合成
前述中间物cn和cn-b可通过合成机制i来合成新颖化合物,于合成机制i中,“反应物bn”选自于表4中包括反应物b1至b25的群组;“中间物c”包含前述中间物cn、cn-b及其相似物。
表4:反应物b1至b25的化学结构式和cas编号。
1.0当量的中间物cn、2.1当量的反应物bn、0.01当量的醋酸钯、0.04当量的2-(二环己基磷基)联苯[dicyclohexylphosphine(2-biphenyl),p(cy)2(2-biph)]、甲苯/乙醇(0.5m、v/v=10/1)和3.0m的碳酸钾水溶液混合,于氮气环境下以100℃的温度下回流12小时,反应完全后,将水和甲苯加入反应物溶液中,接着,使用溶剂将有机相萃取出来并以硫酸钠干燥,于低压环境下使溶剂挥发后利用硅胶管柱层析纯化剩余物,并以甲苯再结晶获得新颖化合物。
用以合成化合物i至xviii的反应物bn和中间物cn列于表5中,各化合物i至xviii分别以氢核磁共振光谱仪(h1-nmr)和fd-ms分析确定,化合物i至xviii的氢核磁共振光谱图如依序为图2至图19,且化合物i至xviii的化学结构式、产率、分子式和质量列于表5中。
表5:合成化合物i至xviii使用的反应物bn和中间物cn以及化合物i至xviii的化学结构式和产率以fd-ms分析而得的分子式和质量。
化合物i至xviii的修饰
除了前述化合物i至xviii之外,本领域技术人员可更替不同的中间物c(即中间物cn或cn-b)和反应物bn,并以类似于合成机制i的合成路径合成出其他新颖化合物。
oled装置的制备
将涂布有
之后,将真空蒸镀机的真空度维持在1x10-6torr至3x10-7torr,并于ito基板上依序沉积各种有机材料和金属材料,并获得实施例1至40的oled装置。于此,该ito基板上依序沉积有第一电洞注入层(hil-1)、第二电洞注入层(hil-2)、第一电洞传输层(htl-1)、第二电洞传输层(htl-2)、蓝/绿/红发光层(bel/gel/rel)、电子传输层(etl)、电子注入层(eil)和阴极(cthd)。
在上述oled装置的各层中,hat是用于形成hil-1和hil-2;hi-2是用于形成hil-1、hil-2和htl-1;hi-d是用于形成hil-1、ht-1和ht-2;ht-1和ht-2分别是用于形成htl-1和htl-2;本发明的新颖化合物和传统et材料(bcp和taz)是用于形成etl;liq是用于形成etd和eil;rh-1或rh-2/gh-1或gh-2/bh分别为形成rel/gel/bel的主要材料;rd/gd/bd-1或bd-2可作为rel/gel/bel的掺杂物。实施例的oled装置和比较例的oled装置的主要差异为:比较例的oled装置中etl是以bcp或taz制成,实施例的oeld装置中etl是以列于表5的新颖化合物所制成。上述各传统材料的详细化学结构式列于表6。
表6:使用于oled装置中商业材料的化学结构式
红光oled装置的制备
红光oled装置包括复数个有机层,各有机层依序沉积于ito基板上,用以制备第一红光oled和第二红光oled的各有机层的材料和厚度分别列于表7中,第一红光oled和第二红光oled的差异在于hil-1、hil-2、htl-1和rel使用的材料。
表7:第一红光oled和第二红光oled装置中各有机层的涂布顺序、名称、材料和厚度。
绿光oled装置的制备
绿光oled装置包括复数个有机层,各有机层依序沉积于ito基板上,用以制备第一绿光oled和第二绿光oled的各有机层的材料和厚度分别列于表8中,第一绿光oled和第二绿光oled的差异在于hil-1、hil-2、htl-1和gel使用的材料。
表8:第一绿光oled和第二绿光oled装置中各有机层的涂布顺序、名称、材料和厚度。
蓝光oled装置的制备
蓝光oled装置包括复数个有机层,各有机层依序沉积于ito基板上,用以制备第一蓝光oled和第二蓝光oled的各有机层的材料和厚度分别列于表9中,第一蓝光oled和第二蓝光oled的差异在于hil-1、hil-2、htl-1和bel使用的材料。
表9:第一蓝光oled和第二蓝光oled装置中各有机层的涂布顺序、名称、材料和厚度。
oled装置的效能
为了评估oled装置的效能,分别将红光、绿光和蓝光oled装置连接于电源供应器(厂牌:keithley;型号:2400),并以pr650的亮度计检测,所测得的色度以为国际照明委员会(commissioninternationaledel’eclairage1931,cie)制定的色度坐标[colorcoordinate(x,y)]示之,检测结果列于下表10中。其中,蓝光和红光的oled装置是在1000尼特(1nit=1cd/m2)的亮度下检测;绿光的oled装置是在3000尼特的亮度下检测。
实施例1至40和比较例1至6环上中oled装置的etl材料、cie颜色、驱动电压和电流效率列于表10中;于表10中,第一蓝光oled命名为b1,第二蓝光oled命名为b2,同样的,第一和第二红光oled以及第一和第二绿光oled依序命名为r1、r2、g1和g2。
表10:实施例1至40和比较例1至6中oled装置的etl材料、颜色、cie、驱动电压和电流效率。
根据表10的结果,相较于用于商业上电子传输材料(bcp或taz),本发明通过添加化合物i至xviii于电子传输层中,可降低红光、绿光或蓝光oled装置的驱动电压并改善电流效率,证实本发明的新颖化合物适用添加于各色oled装置中,并可达到降低驱动电压和改善电流效率的功效。
上述实施例仅为说明本发明的例示,并非于任何方面限制本发明所主张的范围,本领域技术人员能根据本发明的精神针对例如取代基的数量、位置或排列加以调整。本发明所主张的范围自应以申请范围所述为准,而非仅限于上述具体实施例。
- 还没有人留言评论。精彩留言会获得点赞!