一种基因工程菌及其制备方法和用途与流程
本发明涉及生物工程领域,具体涉及一种基因工程菌及其制备方法和用途。
背景技术:
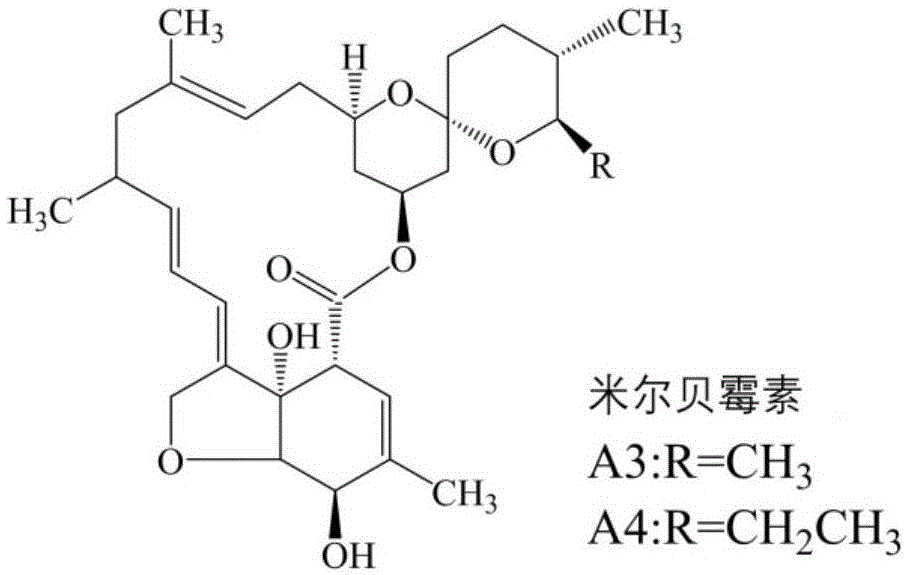
米尔贝霉素a3/a4属于十六元环大环内酯的聚酮类化合物,分子式为c31h44o7/c32h46o7,其化学结构式如图1所示。米尔贝霉素对昆虫类和寄生虫类具有高效的杀虫活性而对哺乳动物低毒,与其他农药无交互作用,在土壤、水和空气中降解较快,对周围环境友好,因此在农业上主要被用于防治螨虫、蚜虫和粉虱等害虫,且当米尔贝霉素a3和a4的比例为30%∶70%时,杀虫活性最高(张宝新,王相晶,向文胜.米尔贝霉素毒理学研究进展[j].世界农药,2009,4:11-2)。米尔贝霉素是目前最有前途的广谱、高效、新型、抗虫、无交叉抗性并且环保的生物杀虫剂。有专家预测,它可以替代目前使用于作物保护的有机磷、氨基甲酸酯、拟除虫菊酯类及有机氯类化合物。
5-酮-米尔贝霉素a3/a4是合成米尔贝霉素a3/a4的前体化合物,其分子式为c31h42o7/c32h44o7,化学结构式如图2中a所示。米尔贝肟(5-oximilbemycin)a3/a4是5-酮-米尔贝霉素a3/a4与羟胺发生肟化反应后的衍生物(反应式如图2所示),其活性比例为20%∶80%(徐倩倩,李继昌,向文胜等.米尔贝肟的研究进展[j].中国兽药杂志,2009,07:33-6),分子式为c31h43no7/c32h45no7,化学结构式如图2中b所示。米尔贝肟主要用于防治宠物猫犬的体内寄生虫(钩虫、恶丝虫、鞭虫和眼线虫等)和体外寄生虫(疥螨、脂螨、鼻螨和姬螯螨等),杀虫活性高、毒性低。米尔贝霉素和米尔贝肟已在日本、美国、荷兰以及中国台湾等多个国家和地区注册,但还没有在中国内地注册,其市场前景不可估量。
目前,米尔贝霉素主要是通过微生物发酵,然后再从发酵液中分离提取得到,但是其效价比较低,因此该抗生素的市场价格偏高,不利于其大规模应用。虽然传统的诱变筛选方法可以在一定程度上提高其效价,但是其机理并不清楚,不能为下一步的菌种改造提供理性化的思路。米尔贝肟的合成主要依靠两步化学合成法(图3),先用cro3将米尔贝霉素a3/a4氧化为5-酮-米尔贝霉素a3/a4,然后再与盐酸羟胺反应生成米尔贝肟。该合成过程不仅转化效率低,而且对环境不友好(重金属污染)。因此,5-酮-米尔贝霉素a3/a4作为化学中间体,提高其效价意义重大。
技术实现要素:
本发明所要解决的技术问题是为了克服现有技术当中米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的生产菌产生米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4产量较低的缺陷,提供了一种基因工程菌及其制备方法和应用。利用本发明所述基因工程菌,可有效提高米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的生产菌产生米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的产量,成本较低,适于工业化生产。
发明人前期通过对米尔贝霉素a3/a4的生产菌的多个调控基因进行大量筛选后,发现敲除milr2基因可以导致其米尔贝霉素a3/a4的产量下降,同时将milr2基因在该菌株中过表达后,可以使其米尔贝霉素a3/a4的产量提高,使用同样的策略在5-酮-米尔贝霉素a3/a4的生产菌中同样可以使5-酮-米尔贝霉素a3/a4的产量提高。
为解决上述技术问题,本发明采用的技术方案之一为,一种基因工程菌,所述基因工程菌是米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的生产菌中过表达milr2基因的工程菌。
本发明中,过表达是指将目的基因的序列与骨架质粒构建成质粒载体,通过转化,获得该基因产物大量积累的生物体。基因过表达的作用主要与基因本身编码蛋白的功能有关。一般来讲,过表达会导致该蛋白的含量增高,如果在细菌中过表达,有利于批量生产。
较佳地,所述米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的生产菌为吸水链霉菌(streptomyceshygroscopicus);更佳地,所述米尔贝霉素a3/a4的生产菌为吸水链霉菌nrrl5739,所述5-酮-米尔贝霉素a3/a4的生产菌为对吸水链霉菌nrrl5739的milf基因进行敲除后的菌株;其中,milf基因的敲除阻断了将5-酮-米尔贝霉素a3/a4还原为米尔贝霉素a3/a4,5-酮-米尔贝霉素a3/a4是米尔贝霉素a3/a4的上游产物,敲除这个基因中断了所述还原的过程。
较佳地,所述基因工程菌携带含有milr2基因的重组表达载体;更佳地,所述重组表达载体的骨架为含有强启动子的质粒;进一步更佳地,所述重组表达载体的骨架为含有红霉素启动子、kasop*或tipap的质粒,进一步更佳地,所述重组表达载体的骨架为含有红霉素启动子ermep*的质粒,优选质粒pib139。
本发明中,所述强启动子是指对rna聚合酶有很高亲和力的启动子,它能指导合成大量的mrna。本发明所述强启动子可以为本发明常规的强启动子,包括红霉素启动子和其它链霉菌强启动子例如kasop*或tipap等。
本发明中,所述红霉素启动子包括本领域常规的红霉素启动子,包括ermep*、ermep、ermep1、ermep2或ermep1*等。
较佳地,所述milr2基因编码的氨基酸序列的ncbi登录号为wp_014173392.1(序列如seqidno.2所示);更佳地,所述milr2基因的核苷酸序列的genbank号为cp002047.1(序列如seqidno.1所示)。
为解决上述技术问题,本发明采用的技术方案之一为,一种制备所述基因工程菌的方法,所述方法包括下列步骤:
1)构建milr2基因过表达的重组表达载体;
2)将构建的重组表达载体转化到中间宿主菌;
3)将带有重组表达载体的中间宿主菌与米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的生产菌进行接合培养。
较佳地,所述的中间宿主菌为大肠杆菌s17-1;和/或,所述的接合培养为在m-isp4培养基培养,培养温度为28℃。
所述m-isp4培养基为本领域常规培养基,较佳地,所述m-isp4培养基包括以下组分:0.5%黄豆饼粉、0.5%甘露醇、0.5%淀粉、0.2%蛋白胨、0.1%酵母粉、0.1%nacl、0.2%(nh4)2so4、0.1%k2hpo3、0.2%caco3、2%琼脂粉、0.1%无机盐微量元素溶液;除无机盐微量元素溶液所述百分比为体积比,其余所述百分比为各组分占培养基的质量体积百分比(克/毫升);更佳地,所述m-isp4培养基的ph值为7.0。
为解决上述技术问题,本发明采用的技术方案之一为,一种制备米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的方法,其包括将所述基因工程菌在发酵培养基中进行发酵培养。
较佳地,所述发酵培养基包括以下组分:12%蔗糖、1%脱脂奶粉、1%棉籽饼粉、0.1%k2hpo4、0.01%feso4·7h2o、0.3%caco3;所述百分比为各组分占培养基的质量体积百分比(克/毫升);
更佳地,所述发酵培养基的ph值为7.2,和/或,所述发酵的温度为25~30℃,优选28℃;和/或,所述发酵的培养时间为10~16天,优选14天;和/或,所述发酵的培养转速为180~250rpm,优选240rpm。
较佳地,所述制备米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的方法还包括先将所述基因工程菌接种于种子培养基中进行种子培养,然后将所得培养物转接至发酵培养基;
更佳地,所述种子培养基的培养温度为25~30℃,优选28℃;种子培养时间为1~2天,优选1天;种子培养转速为180~250rpm,优选240rpm;
和/或,所述转接的接种量为1~8%,优选4%。
为解决上述技术问题,本发明采用的技术方案之一为,所述基因工程菌在制备米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4中的用途。
为解决上述技术问题,本发明采用的技术方案之一为,milr2基因在调控米尔贝霉素a3/a4和/或5-酮-米尔贝霉素a3/a4的产量中的应用。
较佳地,所述调控米尔贝霉素a3/a4和/或5-酮-米尔贝霉素a3/a4的产量为提高米尔贝霉素a3/a4和/或5-酮-米尔贝霉素a3/a4的产量。
为解决上述技术问题,本发明采用的技术方案之一为,一种用于制备米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的发酵培养基,所述发酵培养基包括以下组分:12%蔗糖、1%脱脂奶粉、1%棉籽饼粉、0.1%k2hpo4、0.01%feso4·7h2o、0.3%caco3;所述百分比为各组分占培养基的质量体积百分比(克/毫升);
较佳地,所述发酵培养基的ph值为7.2;
和/或,所述发酵的温度为25~30℃,优选28℃;和/或,所述发酵的培养时间为10~16天,优选14天;和/或,所述发酵的培养转速为180~250rpm,优选240rpm。
在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
本发明所用试剂和原料均市售可得。
本发明的积极进步效果在于:
本发明通过在米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4的生产菌中过表达tetr类调控基因milr2,实现了米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4产量的提高。在本发明某一较佳实施例中,构建的一株米尔贝霉素a3/a4高产菌株中,米尔贝霉素a3/a4的产量比出发菌株提高约37.4%;构建的一株5-酮-米尔贝霉素a3/a4高产菌株中,5-酮-米尔贝霉素a3/a4的产量比出发菌株提高约46.5%。利用本发明所述基因工程菌生产米尔贝霉素a3/a4或5-酮-米尔贝霉素a3/a4,成本较低,适于工业化生产。
附图说明
图1为米尔贝霉素a3/a4的化学结构式。
图2为5-酮-米尔贝霉素a3/a4肟化反应。
图3为两步化学合成法合成米尔贝肟。
图4为milr2基因敲除菌株的凝胶电泳鉴定结果,泳道的样品从左向右依次为sipi-δr2、nrrl5739和标记(marker)。
具体实施方式
本发明所用的菌株、质粒、试剂和仪器
本发明涉及的吸水链霉菌(streptomyceshygroscopicus)nrrl-5739购于nrrl(美国农业研究菌种保藏中心),吸水链霉菌sipi-δf(产生5-酮-米尔贝霉素a3/a4的菌株)为本申请人通过对吸水链霉菌nrrl5739的milf基因进行敲除后得到的,其构建方法参考文献applmicrobiolbiotechnol(2014)98:9703–9712。用于接合转移的大肠杆菌(escherichiacoli)s17-1购于gibco-brl公司。
本发明中用于基因敲除的质粒pkc1139和用于基因过表达的质粒pib139为本实验室保存,两者的构建方法参考文献kiesert.practicalstreptomycesgenetics[j].2000,3(2000)。
本发明中使用的dna胶回收纯化以及质粒提取试剂盒购自axygen公司,所有限制性内切酶都购自thermofisherscientific公司,重组连接试剂盒购自vazyme公司,色谱纯的乙腈购自amethystchemicals公司,其他常规试剂均为国产分析纯或进口分装。
本发明中使用的恒温发酵摇床购自上海世平实验设备有限公司,1200型高效液相色谱仪购自agilenttechnologies公司。
本发明所用的培养基
1.液体lb培养基(1l)
蛋白胨10g,酵母提取物5g,nacl10g,蒸馏水1l;121℃灭菌20分钟。
2.固体lb培养基(1l)
蛋白胨10g,酵母提取物5g,nacl10g,琼脂粉20g;121℃灭菌20分钟。
3.固体m-isp4培养基配方(1l)
黄豆饼粉5g,甘露醇5g,淀粉5g,蛋白胨2g,酵母粉1g,nacl1g,(nh4)2so42g,k2hpo31g,caco32g,琼脂粉20g,无机盐微量元素溶液1ml,ph调至7.0;121℃灭菌20分钟。
4.液体2×yt培养基配方(1l)
蛋白胨16g,酵母粉10g,nacl5g;121℃灭菌20分钟。
5.mb固体培养基配方(1l)
蔗糖4g,酵母浸粉2g,脱脂奶粉1g,琼脂粉20g,ph调至7.2;121℃灭菌20分钟。
6.种子培养基配方(1l)
蔗糖20g,酵母浸粉5g,脱脂奶粉1g,k2hpo41g,ph调至7.2;121℃灭菌20分钟。
7.发酵培养基配方(1l)
蔗糖120g,脱脂奶粉10g,棉籽饼粉10g,k2hpo41g,feso4·7h2o0.1g,caco33g,ph调至7.2;121℃灭菌20分钟。
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
实施例1milr2基因敲除菌株的构建
milr2基因属于tetr类调控因子,其核苷酸序列的genbank号为cp002047.1(序列如seqidno.1所示),其氨基酸序列的ncbi登录号为wp_014173392.1(序列如seqidno.2所示),其n-端编码的结构域为hth-型的dna-binding结构域,c-端编码的结构域为信号感应结构域。
本发明利用常规的同源重组方法对milr2基因进行同框缺失,从而构建milr2基因敲除菌株,具体操作如下:以吸水链霉菌nrrl5739的基因组为模板,利用dmilr2-up-fw/dmilr2-up-rv和dmilr2-down-fw/dmilr2-down-rv两对引物分别进行pcr,扩增出up(1017bp)和down(1066bp)两条同源臂,然后再以up和down为模板,利用dmilr2-up-fw和dmilr2-down-rv两条引物进行overlappcr将up和down连接起来,最后将overlappcr产物与hindiii/ecori酶切的pkc1139进行重组连接得到pkc1139-δmilr2。将pkc1139-δmilr2转化到s17-1,然后通过常规的接合转移的方式将其转入吸水链霉菌nrrl5739菌株中得到接合子。将接合子接种于添加了萘啶酮酸和安普霉素的mb平板上,放在37℃培养,使其发生单交换。再将单交换菌株接种于种子培养基中,于28℃摇床培养4轮,使其发生双交换。最后利用dmilr2-v-fw/dmilr2-v-rv引物对丢掉质粒的双交换菌株进行常规的pcr和测序(测序公司为上海杰李生物技术有限公司)验证,pcr后的凝胶电泳结果如图4所示,验证结果显示本发明所得菌株为正确的milr2基因敲除菌株吸水链霉菌sipi-δr2。以上所述引物序列详见表1。
此外,为了确认吸水链霉菌sipi-δr2菌株的米尔贝霉素a3/a4生产能力,将其接种于25ml种子培养基中,于28℃、240rpm培养1-2天,按4%接种量接种到25ml发酵培养基中,28℃,240rpm,培养14天。取发酵样品于ep管中,同时加入三倍体积的无水乙醇,超声萃取30min,12000rpm离心5min,取上清液用hplc来测定米尔贝霉素a3/a4的含量。hplc条件如下:色谱柱为hypersil-c18柱(4.6mm×150mm,5μm),流动相为乙腈/水(体积比73:27),流速1.2ml/min,柱温30℃,紫外检测波长240nm,进样量10μl。结果显示:吸水链霉菌sipi-δr2菌株(产量为313mg/l)的米尔贝霉素a3/a4产量比吸水链霉菌nrrl5739(产量为456mg/l)降低了约31.2%。
实施例2在吸水链霉菌nrrl5739中构建milr2基因过表达菌株
本发明利用含有红霉素启动子ermep*的质粒pib139来构建milr2基因过表达质粒,进而构建milr2基因过表达菌株。具体操作过程如下:以吸水链霉菌nrrl5739的基因组为模板,利用milr2-oe-fw/milr2-oe-rv引物(序列详见表1)进行pcr扩增出milr2基因,然后利用ndei/ecori对pcr产物进行酶切后与ndei/ecori酶切过的pib139连接后得到质粒pib139-milr2。将pib139-milr2转化到s17-1,然后通过常规的接合转移的方式将其转入吸水链霉菌nrrl5739菌株中,在m-isp4培养基、温度为28℃的条件下进行培养,得到接合子。将所得接合子接种于添加了萘啶酮酸和安普霉素的mb平板上,于28℃传代培养,得到milr2基因过表达菌株吸水链霉菌sipi-r2。
为了确认吸水链霉菌sipi-r2菌株的米尔贝霉素a3/a4生产能力,利用和实施例1中相同的发酵和hplc检测方法来进行检测。结果显示:吸水链霉菌sipi-r2菌株(产量为627mg/l)的米尔贝霉素a3/a4产量比吸水链霉菌nrrl5739(产量为456mg/l)提高了约37.4%。
实施例3在吸水链霉菌sipi-δf中构建milr2基因过表达菌株
利用与实施例2中同样的方法将pib139-milr2质粒通过常规的接合转移的方式转入吸水链霉菌sipi-δf菌株中,得到milr2基因过表达菌株吸水链霉菌sipi-δf-r2,最后用与实施例1中相同的发酵和hplc检测方法来进行检测。结果显示:吸水链霉菌sipi-δf-r2菌株(产量为822mg/l)的5-酮-米尔贝霉素a3/a4产量比吸水链霉菌sipi-δf(产量为561mg/l)提高了约46.5%。
表1.构建milr2基因敲除菌株时使用的引物
本发明人利用pkc1139质粒来构建milr2基因敲除质粒,然后将该敲除质粒通过接合转移的方法转入吸水链霉菌nrrl5739菌株中,通过单交换和双交换后得到milr2基因缺失的菌株吸水链霉菌sipi-δr2,其产生米尔贝霉素a3/a4的产量明显降低。而利用含有红霉素启动子ermep*的质粒pib139来构建milr2基因过表达质粒,然后将该过表达质粒通过接合转移的方法转入吸水链霉菌nrrl5739和吸水链霉菌sipi-δf菌株中,通过安普霉素抗性筛选后得到milr2基因过表达菌株吸水链霉菌sipi-r2和吸水链霉菌sipi-δf-r2,两者分别产生米尔贝霉素a3/a4和5-酮-米尔贝霉素a3/a4的产量均显著提高。以上结果表明了milr2基因对米尔贝霉素a3/a4和5-酮-米尔贝霉素a3/a4的产量起着正调控的作用。
应理解,在阅读了本发明的上述内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求数所限定的范围。
sequencelisting
<110>上海医药工业研究院;中国科学院上海生命科学研究院
<120>一种基因工程菌及其制备方法和用途
<130>p180115120c
<160>10
<170>patentinversion3.5
<210>1
<211>609
<212>dna
<213>streptomyceshygroscopicus
<400>1
gtgagccagggaaaggcgcgtggtccgtacgccaggacaccggcccgcagagcggagatc60
gtacgggcggcgcgcgacagtttcgccgagaacggctacaccaaagcctccctgcgcgat120
atcgcggaacgggccggcatcacccacgccggcctcctccaccacttccgcaacaaggac180
gagctccttgccgaggtgcttgccgaacgggactcccaggagtggcagcacggcctcaca240
caggtcgacagcctcgaccagctcacgccctacctcggcgagctcatccgccaccaccag300
aaggcgcccgagctgatgcgcctgtggatcgaactcgccgccgcggcctcacgcacggac360
caccccgcccacgactacttcgtcgagcgctacgagcgcgggcgggcgcagttcgccgag420
gggttgcaggacgaagcggcccgcggcaggctgcgcgaggacctgagccccgagagcgcc480
gcgatcctcttccacgccgtgctcaacgggctccaactgcagtgggtactcgaccaggat540
ctcgatatcgtcggccccgtcaccgacttcgtacggctgctcttcggccacgatcaggcc600
gacgagtga609
<210>2
<211>202
<212>prt
<213>streptomyceshygroscopicus
<400>2
metserglnglylysalaargglyprotyralaargthrproalaarg
151015
argalagluilevalargalaalaargaspserphealagluasngly
202530
tyrthrlysalaserleuargaspilealagluargalaglyilethr
354045
hisalaglyleuleuhishispheargasnlysaspgluleuleuala
505560
gluvalleualagluargaspserglnglutrpglnhisglyleuthr
65707580
glnvalaspserleuaspglnleuthrprotyrleuglygluleuile
859095
arghishisglnlysalaprogluleumetargleutrpilegluleu
100105110
alaalaalaalaserargthrasphisproalahisasptyrpheval
115120125
gluargtyrgluargglyargalaglnphealagluglyleuglnasp
130135140
glualaalaargglyargleuarggluaspleuserprogluserala
145150155160
alaileleuphehisalavalleuasnglyleuglnleuglntrpval
165170175
leuaspglnaspleuaspilevalglyprovalthraspphevalarg
180185190
leuleupheglyhisaspglnalaaspglu
195200
<210>3
<211>57
<212>dna
<213>artificialsequence
<220>
<223>引物dmilr2-up-fw
<400>3
tcacgacgttgtaaaacgacggccagtgccaagcttctctgcgggtcgtagaagtcg57
<210>4
<211>22
<212>dna
<213>artificialsequence
<220>
<223>引物dmilr2-up-rv
<400>4
ggctttggtgtagccgttctcg22
<210>5
<211>48
<212>dna
<213>artificialsequence
<220>
<223>引物dmilr2-down-fw
<400>5
agtttcgccgagaacggctacaccaaagccgtgctcaacgggctccaa48
<210>6
<211>55
<212>dna
<213>artificialsequence
<220>
<223>引物dmilr2-down-rv
<400>6
tcacacaggaaacagctatgacatgattacgaattcatcgtgttccgcaatcagc55
<210>7
<211>20
<212>dna
<213>artificialsequence
<220>
<223>引物dmilr2-v-fw
<400>7
tgaggtcggcggagaagtcg20
<210>8
<211>19
<212>dna
<213>artificialsequence
<220>
<223>引物dmilr2-v-rv
<400>8
gcatcacgctggtttccct19
<210>9
<211>34
<212>dna
<213>artificialsequence
<220>
<223>引物milr2-oe-fw
<400>9
ggaattccatatggtgagccagggaaaggcgcgt34
<210>10
<211>26
<212>dna
<213>artificialsequence
<220>
<223>引物milr2-oe-rv
<400>10
ggaattctggagcggctggagaaccc26
- 还没有人留言评论。精彩留言会获得点赞!