一种基于5-醛基-1,10-菲咯啉制备的金属铱配合物及其应用的制作方法
本发明属于生物分析领域,具体涉及一种基于5-醛基-1,10-菲咯啉制备的金属铱配合物及其应用。
背景技术
氨基酸是组成多肽和蛋白质的基本单位,对人类和动物的健康起着十分重要的作用,所以对于氨基酸的特异性识别吸引着越来越多研究人员的关注。目前检测氨基酸的方法有核磁法、高效液相色谱法、毛细管电泳法、圆二色谱法、荧光法等。其中荧光法具有特异性好、检测范围广、检测时间短、灵敏度好等优点,被广泛应用到氨基酸的检测。高半胱氨酸(hcy)也称为高同型半胱氨酸,是氨基酸半胱氨酸(cys)的异种,在旁链部份硫醇基(-sh)前包含一个额外的亚甲基(-ch2-)。研究发现,hcy可以直接或间接导致血管内皮细胞损伤、促进血管平滑肌细胞增殖、影响低密度脂蛋白的氧化、增强血小板功能、促进血栓形成。因此,特异性识别hcy,特别是与类似半胱氨酸的区分识别,在临床医学中具有重要的意义。
技术实现要素:
本发明的目的在于提供一种基于5-醛基-1,10-菲咯啉制备的金属铱配合物及其应用,该金属铱配合物与高半胱氨酸结合后因形成六元噻嗪环而引起发光强度的变化,故可作为特异性识别高半胱氨酸的试剂。
为实现上述目的,本发明采用如下技术方案:
一种基于5-醛基-1,10-菲咯啉(
所述金属铱配合物可以和高半胱氨酸(hcy)形成六元噻嗪环,而使金属铱配合物的发光强度发生明显变化,故可将其制成发光探针,用于分子生物学、生物技术和医学中hcy的特异性识别。
本发明的显著优点在于:本发明金属铱配合物具有活泼的醛基,其对hcy表现出特异性识别的特点,并且可以实现高效的识别,具有较好应用前景。
附图说明
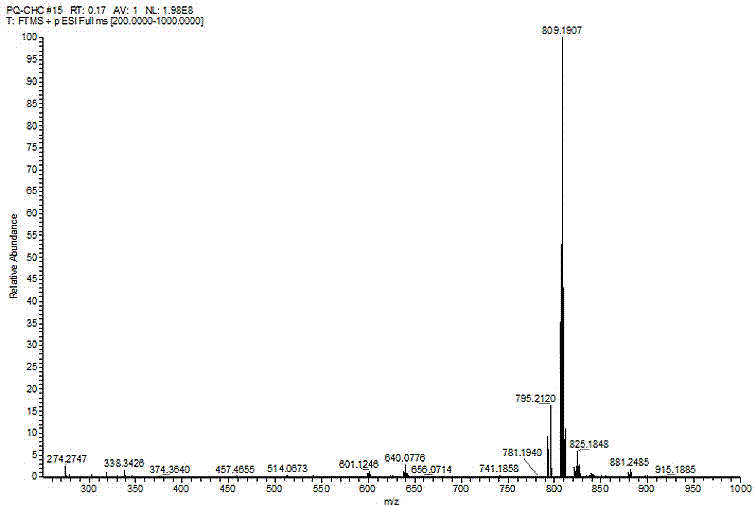
图1为金属铱配合物i的质谱图;
图2为金属铱配合物ii的质谱图;
图3为金属铱配合物i和不同浓度hcy作用后的紫外可见光吸收图谱;
图4为金属铱配合物i和不同浓度hcy作用后的荧光光谱图;
图5为以hcy浓度为横坐标、发光强度差值为纵坐标的金属铱配合物i的标准曲线图;
图6为金属铱配合物ii和不同浓度hcy作用后的紫外可见光吸收图谱;
图7为金属铱配合物ii和不同浓度hcy作用后的荧光光谱图;
图8为以hcy浓度为横坐标、发光强度差值为纵坐标金属铱配合物ii的标准曲线图;
图9为金属铱配合物i及其与hcy、csy作用60min内的荧光强度变化图;
图10为金属铱配合物ii及其与hcy、csy作用60min内的荧光强度变化图;
图11为金属铱配合物i及其加入hcy后的核磁共振对照图;
图12为金属铱配合物i加入hcy后的质谱图;
图13为金属铱配合物ii及其加入hcy后的核磁共振对照图;
图14为金属铱配合物ii加入hcy后的质谱图;
图15为金属铱配合物i与不同氨基酸作用的荧光光谱图;
图16为金属铱配合物ii与不同氨基酸作用的荧光光谱图。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
1.氯桥二聚体的制备
1)[(pq)2ircl]2(
2)[(bzq)2ircl]2(
2.金属铱配合物的制备
1)[(pq)2ir(phen-cho)]cl(配合物i)的合成:在50ml双口瓶中依次加入[(pq)2ircl]225mg(0.2mmol)、5-醛基-1,10-菲咯啉9mg(0.42mmol)、6ml二氯甲烷-甲醇混合液(1:1,v:v),在氮气保护下40℃冷凝回流12h,冷却至室温,减压旋转,所得固体用二氯甲烷与甲醇做为洗脱剂(100:1,v/v),过硅胶层析柱,得到橙红色固体,产率为56%。
1hnmr(400hz,dmso)δ(ppm):10.34(s,1h),9.63(d,1h),8.96(d,1h),8.85(s,1h),8.60(dd,4h),8.51(d,2h),8.37(d,2h),8.16(m,2h),7.83(d,2h),7.25(m,4h),7.10(d,2h),6.89(t,4h),6.53(d,2h).esi-ms:m/z(%)809.19(100){m-cl}+.calcdforc43h28irn4o,exactmass:809.1907。质谱图参见图1。
2)[(bzq)2ir(phen-cho)]cl(配合物ii)的合成:在50ml双口瓶中依次加入[(bzq)2ircl]223mg(0.2mmol)、5-醛基-1,10-菲咯啉9mg(0.42mmol)、6ml二氯甲烷-甲醇混合液(1:1,v:v),在氮气保护下40℃冷凝回流12h,冷却至室温,减压旋转,所得固体用二氯甲烷与甲醇做为洗脱剂(100:1,v/v),过硅胶层析柱,得到橙红色固体,产率为50%。
1hnmr(400hz,cdcl3)δ(ppm):10.66(s,1h),9.98(d,1h),9.79(m,2h),8.30(d,4h),7.94(d,3h),7.85(s,1h),7.74(t,4h),7.57(d,2h),7.41(s,1h),7.34(s,1h),7.25(d,2h),6.45(d,2h).esi-ms:m/z(%)757.16(100){m-cl}+.calcdforc39h24irn4o,exactmass:757.1591。质谱图参见图2。
3.具体应用
采用所制备的金属铱配合物作为荧光探针对高半胱氨酸(hcy)进行检测,具体检测方法由下述步骤实现:
1)配制ph为7.2、浓度为10mmol/l的tris-hcl缓冲液,再分别配制浓度为1.0mmol/l的[(pq)2ir(phen-cho)]cl或[(bzq)2ir(phen-cho)]cl的乙腈溶液和浓度为10mmol/l的hcy的tris-hcl溶液。取30μl10mmol/l的hcy的tris-hcl溶液加入到2970μltris-hcl缓冲液(ph=7.2c=10mm)中,制成浓度为1.0×10-4mol/l的hcy稀释液备用。
2)于5ml离心管中依次加入2370μl乙腈,30μl、1.0mmol/l[(pq)2ir(phen-cho)]cl或[(bzq)2ir(phen-cho)]cl的乙腈溶液,然后向其中加入0、30、150、300、600μl浓度为1.0×10-4mol/l的hcy稀释液,再加入一定体积的tris-hcl缓冲液(ph=7.2,c=10mm)定容至3ml,混合均匀;另于5ml离心管中依次加入2370μl乙腈,30μl、1.0mmol/l金属铱配合物的乙腈溶液,然后向其中加入15、30、60、120、150、180、240、270、300、360、420、480、540、600μl浓度为10mmol/l的hcy的tris-hcl溶液,再加入一定体积的tris-hcl缓冲液(ph=7.2,c=10mm)定容至3ml,混合均匀;从而获得hcy浓度分别为0、5、10、20、50、100、200、500、600、800、900μmol及1、1.2、1.4、1.6、1.8、2mmol的混合液;
3)移取含[(pq)2ir(phen-cho)]cl的混合液于比色皿中,分别测定其吸光度,然后以波长为横坐标、吸光度为纵坐标绘制不同hcy浓度的紫外图(参见图3)。
另移取混合液于比色皿中,设定激发波长为436nm,狭缝宽度为3.5nm/3.5nm,用荧光分光光度仪测定其在波长为564nm处对应的发光强度,然后以hcy浓度为横坐标,以其所对应的发光强度为纵坐标,绘制配合物与不同浓度hcy作用后的荧光光谱曲线(参见图4)。由图4可见,随着hcy浓度的增大,发光强度逐渐增强。
再以hcy的浓度为横坐标,以其所对应的发光强度差值为纵坐标绘制工作曲线(参见图5),显示有良好的线性关系。
4)移取含[(bzq)2ir(phen-cho)]cl的混合液于比色皿中,分别测定其吸光度,然后以波长为横坐标、吸光度为纵坐标绘制不同hcy浓度的紫外图(参见图6)。
另移取混合液于比色皿中,设定激发波长为396nm,狭缝宽度为4.5nm/4.5nm,用荧光分光光度仪测定其在波长为580nm处对应的发光强度,然后以hcy浓度为横坐标,以其所对应的发光强度为纵坐标,绘制配合物与不同浓度hcy作用后的荧光光谱曲线(参见图7)。由图7可见,随着hcy浓度的增大,发光强度逐渐增强。
再以hcy的浓度为横坐标,以其所对应的发光强度差值为纵坐标绘制工作曲线(参见图8),显示有良好的线性关系。
4.响应时间的研究
为了验证本发明的铱配合物[(pq)2ir(phen-cho)]cl和[(bzq)2ir(phen-cho)]cl对hcy检测的效果,现以下述实验为例进行说明:
1)于5ml离心管中,加入600μltris-hcl(ph=7.2,c=10mmol/l)的缓冲溶液和30μl1.0mmol/l的[(pq)2ir(phen-cho)]cl或[(bzq)2ir(phen-cho)]cl的乙腈溶液,然后加入一定体积的乙腈定容至3ml,混合均匀。移取混合溶液于比色皿中,设定激发波长为436nm,狭缝宽度为3.5nm/3.5nm,用荧光分光光度仪每隔10min测定一次,共测定60min,记录其在波长为564nm或580nm处对应的发光强度。
2)于5ml离心管中,加入300μltris-hcl(ph=7.2,c=10mmol/l)的缓冲溶液和30μl1.0mmol/l的[(pq)2ir(phen-cho)]cl或[(bzq)2ir(phen-cho)]cl的乙腈溶液,然后向其中加入300μlhcy的tris-hcl(ph=7.2,c=10mmol/l)溶液,最后加入一定体积的乙腈定容至3ml(即hcy的浓度为1.0×10-3mol/l),混合均匀。移取混合溶液于比色皿中,设定激发波长为436nm,狭缝宽度为3.5nm/3.5nm,用荧光分光光度仪每隔10min测定一次,共测定60min,记录其在波长为564或580nm处对应的发光强度。
3)于5ml离心管中,加入300μltris-hcl(ph=7.2,c=10mmol/l)的缓冲溶液和30μl1mmol/l的[(pq)2ir(phen-cho)]cl或[(bzq)2ir(phen-cho)]cl的乙腈溶液,然后向其中加入300μlcys的tris-hcl(ph=7.2,c=10mmol/l)溶液,最后加入一定体积的乙腈定容至3ml(即cys的浓度为1.0×10-3mol/l),混合均匀。移取混合溶液于比色皿中,设定激发波长为436nm,狭缝宽度为3.5nm/3.5nm,用荧光分光光度仪每隔10min测定一次,共测定60min,记录其在波长为564nm或580nm处对应的发光强度。
如图9所示,[(pq)2ir-(phen-cho)]cl在加入hcy(1.0×10-3mol/l)20min后,其564nm处的发光强度明显增强,约40min后达到平衡,发光强度增强约1.2倍。而加入cys后发光强度明显减小,直至与单纯配合物的发光强度相当。
如图10所示,[(bzq)2ir-(phen-cho)]cl在加入hcy(1.0×10-3mol/l)后,其580nm处的发光强度明显增强,约40min后达到平衡,发光强度增强约1.13倍。而加入cys后发光强度基本不变。
由此说明,hcy加入后和醛基发生了加成反应,使得金属铱配合物的发光强度逐渐增强,本发明制备的[(pq)2ir(phen-cho)]cl和[(bzq)2ir-(phen-cho)]cl可以很好地识别hcy。
图11-图14分别为金属铱配合物i、ii及其与hcy作用后的核磁共振对照图和质谱图,由图中进一步说明了配合物与hcy形成了新的六元噻嗪环。
5.不同氨基酸的研究
于5ml离心管中加入300μltris-hcl(ph=7.2,c=10mmol/l)的缓冲溶液和30μl1.0mmol/l的[(pq)2ir(phen-cho)]cl或[(bzq)2ir(phen-cho)]cl的乙腈溶液,然后向其中依次加入300μl的d-色氨酸(d-trp)、谷胱甘肽(gsh)、半胱氨酸(cys)、l-精氨酸(l-arg)、l-组氨酸(l-his)、l-异亮氨酸(l-ile)、l-赖氨酸(l-lys)、l-亮氨酸(l-leu)、l-蛋氨酸(l-met)、l-苯丙氨酸(l-phe)、l-色氨酸(l-trp)、l-苏氨酸(l-thr)、l-缬氨酸(l-val)及hcy的tris-hcl(ph=7.2,c=10mmol/l)溶液,各氨基酸的浓度均为1.0×10-2mol/l,最后加入一定体积的乙腈定容至3ml(即氨基酸的浓度为1.0×10-3mol/l,金属铱配合物的浓度均为10μm),混合均匀。
移取混合溶液于比色皿中,设定激发波长为436nm,狭缝宽度为3.5nm/3.5nm,用荧光分光光度仪测定其在波长为564nm([(pq)2ir(phen-cho)]cl)或580nm([(bzq)2ir(phen-cho)]cl)处对应的发光强度。
从图15、16中可以看出,[(pq)2ir(phen-cho)]cl及[(bzq)2ir(phen-cho)]cl与高半胱氨酸有很强的发光明显增强,其他氨基酸基本没变化或只有较弱的发光减弱的变化,证明所得金属铱配合物可对高半胱氨酸进行特异性识别,特别是可以从类似含巯基的半胱氨酸及谷胱甘肽中将其区分开来,这对临床医学检测具有非常重要的意义。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!