一种新型瑞格非尼抗肿瘤铂(II)配合物及其制备方法与应用与流程
本发明涉及瑞格非尼类抗肿瘤药物及其制备领域,尤其是一种新型瑞格非尼抗肿瘤铂(ii)配合物及其制备方法与应用。
背景技术
自1969年,美国化学家bosenbergb.等人首次发现顺式-二氯·二氨合铂(ii),具有强抗动物肿瘤活性后,无机金属配合物成为新一类抗癌药物,该领域的研究引起了化学工作者的极大重视。虽然目前临床广泛使用的金属配合物抗癌药物只有顺铂、卡铂、奈达铂和奥沙利铂等金属药物,但对该领域的研究表明,更多具有高抗癌活性,低毒副作用的金属配合物抗癌药物有望进人临床试验,使癌症的化学药物治疗有更大的选择范围。由于顺铂类药物在临床治疗中,产生严重的毒副作用和耐药性,研发新型高效、低毒、选择性高的铂类抗肿瘤化疗药物迫在眉睫。
另一方面,肺癌居恶性肿瘤发病率及死亡率均排第一位,肺癌已经连续2年成为人体健康头号杀手。其中肺腺癌约占肺原发肿瘤的40%,是肺癌的主要形式,目前主要采取以化疗为主的综合治疗方案,但对于晚期非手术肺癌患者的疗效仍维持在较低的水平,有效率仅20%~40%,5年生存率只有15%。其原因之一即肿瘤多药耐药(a549/ddp)的产生。因此,研发新型高效、低毒、靶向于人肺癌耐药细胞的铂类抗肿瘤化疗药物迫在眉睫。
此外,瑞格非尼(regorafenib)都是由德国拜耳和美国onyx公司共同研发的一个多激酶抑制剂类抗癌药物,它主要用于治疗转移性结直肠癌和不能手术切除或转移性胃肠道间质瘤。从目前的研究来看,尚未发现有以它们为活性配体的配合物及抗肿瘤活性研究的相关报道为了拓展这种药物在临床上的应用,本研究以瑞格非尼(regorafenib)为活性配体合成靶向于人肺癌耐药细胞(a549/ddp)抗肿瘤铂配合物,并对其抗肿瘤活性及其应用进行研究。
技术实现要素:
本发明的目的之一在于提供一种新型瑞格非尼抗肿瘤铂(ii)配合物。
为了实现上述目的,本发明提供的第一技术方案是这样的:一种新型瑞格非尼抗肿瘤铂(ii)配合物,其化学结构式如下式所示:
为了实现上述目的,本发明提供的第二技术方案是这样的:一种如上所述新型瑞格非尼抗肿瘤铂(ii)配合物的制备方法,其特征在于,包括以下步骤:
步骤1:按物质的量之比为1~5:1~5称取索拉非尼和二氯·二(二甲基亚砜)合铂(ii),溶于极性溶剂中,得到混合溶液;
步骤2:将所得混合溶液在回流下进行配位反应,过滤,收集沉淀物,洗涤,干燥,即得。
优选地,所述步骤1中的极性溶剂为体积浓度为1%~99%的甲醇、乙腈和/或乙醇溶液,用量为每1mmol的瑞格非尼用5~45ml极性溶剂。
优选地,所述步骤2中配位反应的温度为45~80℃,反应时间为8~48h,产率为80.0%~95.0%。
优选地,所述步骤2中洗涤所用溶剂为甲醇、丙酮和/或乙醚;所述步骤2中干燥的条件为:45℃条件下的真空干燥。
本发明的目的之三在于提供上述配合物的应用。
为了实现上述目的,本发明提供的第三技术方案是这样的:一种如上所述新型瑞格非尼抗肿瘤铂(ii)配合物应用于制备抗肿瘤药物。
本发明与现有技术相比,具有以下优点:
本发明以瑞格非尼(rfb)为活性配体,与二氯·二(二甲基亚砜)合铂(ii)配位反应合成了一种具有抗肿瘤活性的配合物1,并考察了它对nci-h460、sk-ov-3、t-24、hela、sk-o-v-3/ddp、a549/ddp肿瘤细胞和正常hl-7702细胞的活性和毒性实验,实验结果发现配合物1对人肺癌nci-h460细胞和人肺癌顺铂耐药a549/ddp肿瘤细胞的抑制作用较好,其ic50值分别为10.81±0.36μm和0.08±0.03μm,尤其是对a549/ddp肿瘤细胞的抑制作用最好,其体外抗肿瘤活性远远大于临床药物配体rfb(37.46±1.11μm)和经典的金属基抗癌药物顺铂(97.63±1.06μm);此外,配合物1对正常细胞hl-7702的毒性很小(ic50=85.06±2.01μm),其毒性远远小于其配体瑞格非尼(35.11±1.09μm)和顺铂(18.12±0.54μm)的毒性,体现出很好的靶向抑制人肺癌顺铂耐药a549/ddp肿瘤细胞的生长。总之,配合物1表现出优越的体外抗肿瘤活性,具有潜在的药用价值,有望用于各种抗肿瘤药物的制备。
附图说明
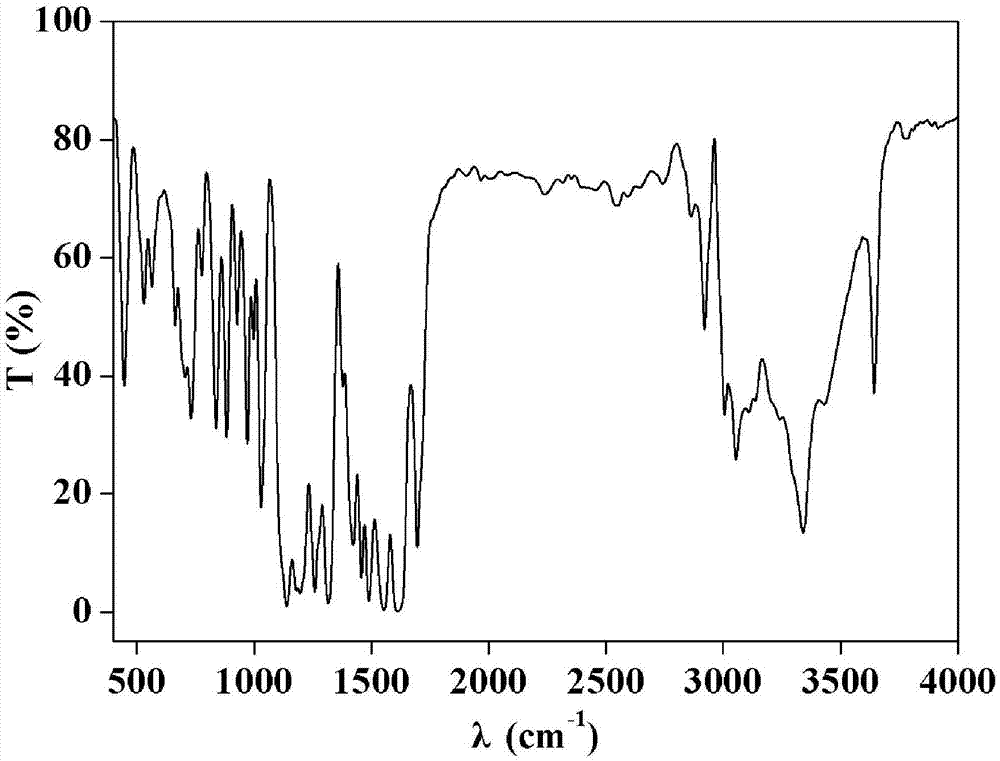
图1为本发明实施例1制得的配合物1的红外谱图;
图2为本发明实施例1制得的配合物1的电喷雾质谱图;
图3为本发明实施例1制得的配合物1的核磁共振氢谱图;
图4为本发明实施例1制得的配合物1的核磁共振碳谱图。
具体实施方式
下面结合具体实施方式,对本发明的权利要求做进一步的详细说明,但不构成对本发明的任何限制,任何在本发明权利要求保护范围内所做的有限次修改,仍在本发明的权利要求保护范围内。
下述实施例中涉及的瑞格非尼可参考现有文献(gong,p.;etal.res.chem.intermed.,2016,42:3209–3218.)进行制备;涉及的二氯·二(二甲基亚砜)合铂(ii)可参考现有文献(al-allaf,t.a.k.;etal.transit.met.chem.,1998,23:403-406.)进行制备。
下述实施例中,将“瑞格非尼”简写为“rfb”,将“二氯·二(二甲基亚砜)合铂(ii)”简写为“cis-ptcl2(dmso)2”。
实施例1
在50ml的高压反应釜中加入1.0mmol配体rfb和1.0mmolcis-ptcl2(dmso)2,加入25.0ml的无水甲醇和1.0ml的蒸馏水,在55℃条件下加热36小时,冷切至室温后,析出大量黄色的产物,抽滤,黄色产品依次用甲醇、丙酮和乙醚洗涤,45℃下真空干燥,最后得到黄色产物,产率为95.0%。
对所得黄色产物进行鉴定:
(1)红外光谱,其谱图如图1所示。
ir(kbr):3644,3341,3054,3006,2921,1696,1614,1490,1458,1423,1317,1197,1159,1140,1031,971,884,838,732,701,663,565,531,446cm-1.
(2)电喷雾质谱,其谱图如图2所示。
esi-msm/z:902.1[m-h+dmso]-,其中m为其分子量。
(3)核磁共振氢谱图,如图3所示。
1hnmr(400mhz,dmso-d6)δ9.56(s,1h),9.43(d,j=6.7hz,1h),8.79(s,1h),8.21(t,j=9.1hz,1h),8.13(s,1h),7.63(s,2h),7.43(dt,j=9.8,2.9hz,2h),7.15(dd,j=8.0,2.4hz,2h),3.56(s,5h),2.83(s,3h),2.55(s,1h)。
(4)核磁共振碳谱图,如图4所示。
13cnmr(101mhz,dmso-d6)δ171.21,167.43,156.15,154.30,152.59,151.85,150.03,147.70,147.60,139.42,132.60,127.43,127.13,126.17,126.06,124.60,123.49,123.15,122.90,121.89,117.66,117.15,115.25,112.49,109.78,109.55,44.82,40.89,32.67。
(5)元素分析结果,如表1所示。
表1元素分析结果
因此,可以确定所得黄色目标产物为铂配合物1,其结构式如下:
实施例2
在50ml的高压反应釜中加入配体1.0mmolrfb和5.0mmolcis-ptcl2(dmso)2,加入35.0ml的无水乙醇和10.0ml的蒸馏水,在80℃条件下加热48小时,冷切至室温后,析出大量黄色的产物,抽滤,黄色产品依次用甲醇、丙酮和乙醚洗涤,45℃下真空干燥,最后得到配合物1,产率为80.0%。
实施例3
在50ml的高压反应釜中加入配体5.0mmolrfb和1.0mmolcis-ptcl2(dmso)2,加入5.0ml的乙腈和30.0ml的蒸馏水,在45℃条件下加热8小时,冷切至室温后,析出大量黄色的产物,抽滤,黄色产品依次用甲醇、丙酮和乙醚洗涤,45℃下真空干燥,最后得到配合物1,产率为85.0%。
实施例4
在50ml的高压反应釜中加入配体1.0mmolrfb和1.0mmolcis-ptcl2(dmso)2,加入10.0ml的无水甲醇、10.0ml乙腈和10.0ml的蒸馏水,在60℃条件下加热24小时,冷切至室温后,析出大量黄色的产物,抽滤,黄色产品依次用甲醇、丙酮和乙醚洗涤,45℃下真空干燥,最后得到配合物1,产率为90.0%。
为了充分说明本发明所述的一种高活性的新型瑞格非尼抗肿瘤铂(ii)配合物1在制药中的用途,对配合物1进行了抗肿瘤活性实验和毒性实验研究。
1.细胞株与细胞培养
本实验选用人肺癌nci-h460细胞、人卵巢癌sk-ov-3细胞、耐顺铂sk-ov-3/ddp细胞、人膀胱癌a549细胞、人宫颈癌细胞hela和人正常肝细胞hl-77026种人类细胞株。
所有人源细胞株均培养在含100u/ml青霉素、10wt%小牛血、100u/ml链霉素的rpmi-1640培养液内,置37℃含体积浓度5%co2孵箱中培养。
2.待测化合物的配制
所用的配体rfb和配合物1的纯度均需≥95%,将它们的dmso储液用生理缓冲液稀释成20μmol/l终浓度≤1%的终溶液,测试该浓度下配体rfb和配合物1对正常细胞或所选的肿瘤细胞生长的抑制程度。
3.mtt法测定细胞生长抑制实验
(1)取对数生长期的正常细胞或肿瘤细胞,经胰蛋白酶消化后,用含10%小牛血清的培养液配制成浓度为5000个/ml的细胞悬液,以每孔190μl接种于96孔培养板中,使待测细胞密度至1000~10000孔,边缘孔用无菌pbs填充;
(2)5%co2,37℃孵育24h,至细胞单层铺满孔底,每孔加入一定浓度梯度的药物10μl,每个浓度梯度设4个复孔;
(3)5%co2,37℃孵育48小时,倒置显微镜下观察;
(4)每孔加入10μl5mg/ml的pbs溶液,继续培养4h;
(5)终止培养,小心吸去孔内培养液,每孔加入150μl的dmso充分溶解甲瓒沉淀,振荡器混匀后,在酶标仪用波长为570nm,参比波长为450nm测定各孔的光密度值;
(6)同时在调零孔加培养基、mtt和dmso,对照孔加细胞、培养液、mtt、相同浓度的药物溶解介质个dmso。
(7)根据测得的光密度值,即od值,来判断活细胞数量,od值越大,细胞活性越强。利用公式:
计算配体rfb和配合物1对所选细胞生长的抑制率,再以bliss法分别计算各受试化合物对所选的各个细胞株的ic50值。其结果如以下表2所示。
表2对各种细胞株的ic50值(μm)
实验结果发现配合物1对人肺癌nci-h460细胞和人肺癌顺铂耐药a549/ddp肿瘤细胞的抑制作用较好,其ic50值分别为10.81±0.36μm和0.08±0.03μm,尤其是对a549/ddp肿瘤细胞的抑制作用最好,其体外抗肿瘤活性远远大于临床药物配体rfb(37.46±1.11μm)和经典的金属基抗癌药物顺铂(97.63±1.06μm);此外,配合物1对正常细胞hl-7702的毒性很小(ic50=85.06±2.01μm),其毒性远远小于其配体瑞格非尼(35.11±1.09μm)和顺铂(18.12±0.54μm)的毒性,体现出很好的靶向抑制人肺癌顺铂耐药a549/ddp肿瘤细胞的生长。
综上,配合物1表现出优越的体外抗肿瘤活性,具有潜在的药用价值,有望用于各种抗肿瘤药物的制备。
- 还没有人留言评论。精彩留言会获得点赞!