用于封装和分割试剂的流体装置、系统和方法及其应用与流程
本申请要求于2014年4月10日提交的美国临时专利申请号61/977,804的优先权,该申请的全部公开内容通过引用而整体并入本文用于所有目的。
背景
在过去的二十年,生命科学领域经历了巨大的进步。从来源于重组脱氧核糖核酸(DNA)技术的产品的广泛商业化,到通过关键的研究工具(如聚合酶链反应、核酸阵列技术、稳健的核酸测序技术以及最近高通量下一代测序技术)的发展和商业化所实现的研究、开发和诊断的简单化。所有这些改善结合起来推动了生物研究、医学、诊断学、农业生物技术领域以及各种其他相关领域的飞速发展。
这些技术通常都不是单独存在的,相反,它们都被整合在包括样品采集和制备的上游部分,到数据采集、去卷积、解释和最终利用的下游部分的更广泛的工作流程中。而且,这些进步中的每一种,在标志着其领域大步前进的同时,也往往暴露出该工作流程中必须自身发展以适应该领域需求的关键瓶颈。例如,仅为了能够从样品材料开始对核酸进行测序,基因组测序就在两端受到了关键工作流程问题(在许多情况下,包括复杂和劳动密集型样品制备过程)的束缚。类似地,一旦获得了序列数据,则需要复杂的后端信息学以便将序列数据去卷积成为碱基判定,然后将确定的碱基序列组装成连续的序列数据,并最终将该序列数据与给定生物体的全基因组进行比对。
这些技术中的许多技术的一个关键瓶颈并非在于其生成大量数据的能力,而是在于其将该数据更具体地划归于复杂样品的一部分或许多多路(multiplexed)样品中的给定样品的能力。
技术实现要素:
本公开内容的装置、方法和系统为包括上述挑战在内的多个领域中的挑战提供了解决方案。本公开内容提供了用于生成封装的试剂以及包含这些封装的试剂的多路分区(multiplexed partitions)以用于多种应用的装置、系统和方法。
本公开内容的装置、系统和方法采用微流体系统来生成微胶囊或珠子的单分散群体,该微胶囊或珠子可具有与其缔合的试剂如生物试剂。还提供了用于选择性地且可控地将这些微胶囊或珠子分割(partition)至乳液中的液滴中以用于进行进一步反应和/或分析的装置、系统和方法。还提供了所述装置和系统的各种组件部分以及用于促进这些组件之间相互作用的接口组件。
本公开内容的一个方面提供了用于分割微胶囊的方法。所述方法可包括提供包含微胶囊悬浮液的水性流体,以及使所述水性流体流入包含分割流体的液滴生成交叉部(droplet generation junction)以在所述分割流体中形成所述水性流体的液滴群体(population of droplets)。所述水性流体的流速可以使得所述液滴群体中的不多于50%的液滴未被来自所述微胶囊悬浮液的微胶囊占据。
在一些实施方案中,所述流速使得所述液滴群体中的不多于25%的液滴未被微胶囊占据。在一些实施方案中,所述流速使得所述液滴群体中的不多于10%的液滴未被微胶囊占据。在一些实施方案中,所述流速使得液滴群体的不多于50%、45%、40%、35%、30%、25%、20%、15%、10%、5%、2%或1%未被微胶囊占据。
在一些实施方案中,所述液滴群体中的少于25%的液滴包含多于一个微胶囊。在一些实施方案中,所述液滴群体中的少于20%的液滴包含多于一个微胶囊。在一些实施方案中,所述液滴群体中的少于15%的液滴包含多于一个微胶囊。在一些实施方案中,所述液滴群体中的少于10%的液滴包含多于一个微胶囊。在一些实施方案中,所述液滴群体中的少于5%的液滴包含多于一个微胶囊。
在一些实施方案中,所述液滴群体中的至少80%的液滴包含单个微胶囊。在一些实施方案中,所述液滴群体中的至少90%的液滴包含单个微胶囊。在一些实施方案中,所述液滴群体中的至少95%的液滴包含单个微胶囊。在一些实施方案中,所述液滴群体中的至少70%、75%、80%、85%、90%、95%、98%或99%的液滴包含单个微胶囊。
在一些实施方案中,所述液滴生成交叉部可在微流体装置的微流体通道网络中。在一些实施方案中,所述微流体通道网络可包含将微胶囊的来源与所述液滴生成交叉部流体连接的第一通道区段。所述微流体通道网络还可包含将分割流体的来源与所述液滴生成交叉部连接的第二通道区段,以及与所述液滴生成交叉部流体连接、为所述液滴生成交叉部提供出口的第三通道区段。
在一些实施方案中,可通过提供横跨所述第一和第二通道区段的一个或多个压差来提供所述流速。在一些实施方案中,所述第一和/或第二通道区段可具有提供所述流速的截面尺寸,所述流速使得所述液滴群体中的不多于50%的液滴未被来自所述微胶囊悬浮液的微胶囊占据。在一些实施方案中,所述微流体通道网络可进一步包含在所述第一通道区段内的提供所述流速的一个或多个流动控制结构。
在一些实施方案中,所述微胶囊悬浮液的微胶囊具有平均截面尺寸和不大于10%的截面尺寸变异系数。在一些实施方案中,所述微胶囊悬浮液的微胶囊具有平均截面尺寸和不大于10%、8%、6%、4%、2%或1%的截面尺寸变异系数。
本公开内容的其他方面提供了用于分割微胶囊的方法。所述方法可包括使包含微胶囊悬浮液的水性流体流入包含分割流体的液滴生成交叉部。在液滴生成窗口期,所述微胶囊可以以变化小于30%的频率流入所述液滴生成交叉部。所述方法还可包括在所述液滴生成窗口期在所述分割流体中分割所述微胶囊。在一些实施方案中,所述频率大于50Hz。在一些实施方案中,所述频率大于500Hz。在一些实施方案中,所述频率大于1000Hz。在一些实施方案中,所述频率大于50Hz、100Hz、250Hz、500Hz、750Hz、1000Hz、1250Hz、1500Hz、1750Hz或2000Hz。
在一些实施方案中,在所述液滴生成窗口期,所述微胶囊以变化小于20%的频率流入所述液滴生成交叉部。在一些实施方案中,在所述液滴生成窗口期,所述微胶囊以变化小于10%的频率流入所述液滴生成交叉部。在一些实施方案中,在所述液滴生成窗口期,所述微胶囊以变化小于5%的频率流入所述液滴生成交叉部。在一些实施方案中,在所述液滴生成窗口期,所述微胶囊以变化小于30%、25%、20%、15%、10%、5%、2%或1%的频率流入所述液滴生成交叉部。
在一些实施方案中,使包含所述微胶囊悬浮液的水性流体流入包含分割流体的液滴生成交叉部可包括使所述水性流体流动通过与所述液滴生成交叉部流体连接的微流体通道。所述微流体通道可包含调节所述微胶囊的流动(例如,流速)的区域。
本公开内容的其他方面提供了用于产生微胶囊的方法。所述方法可包括提供在水性流体中的凝胶前体,以及使具有所述凝胶前体的水性流体流动通过与包含分割流体的液滴生成交叉部流体连接的流体导管。所述分割流体可包含凝胶活化剂。所述方法还可包括在所述分割流体中形成所述水性流体的液滴,其中在所述液滴内,所述凝胶活化剂与所述凝胶前体接触以形成凝胶微胶囊。在一些实施方案中,所述水性流体还可包含生物分子,其中例如所述生物分子可变得夹杂在所述凝胶微胶囊中。
本公开内容的其他方面提供了用于分割微胶囊的方法。所述方法可包括使包含单分散微胶囊群体的悬浮液的水性流体流入液滴生成交叉部。所述单分散群体可具有平均截面尺寸和不大于10%的截面尺寸变异系数。所述方法还可包括将分割流体引入到所述液滴生成交叉部中,以及将所述水性流体分离成在所述分割流体内的液滴,其中该液滴含有一个或多个微胶囊。
本公开内容的其他方面提供了一种微流体系统。所述微流体系统可包含含有与液滴生成交叉部流体连通的至少第一、第二和第三通道区段的微流体通道网络。所述第一通道区段可与包含含有水性流体的第一流体的第一流体来源流体连接。所述水性流体可包含安置在其中的多个微胶囊。此外,所述第二通道区段可与包含与所述水性流体不互溶的第二流体的第二流体来源流体连接。所述微流体系统还可包含与所述微流体通道网络连接的流动控制系统。所述流动控制系统可使所述第一流体和第二流体流入所述液滴生成交叉部以生成包含微胶囊的液滴;并且可使所述液滴流入所述第三通道区段,使得至少75%的液滴包含至少一个微胶囊并且少于25%的液滴包含多于一个微胶囊。
本公开内容的其他方面提供了一种微流体系统。所述微流体系统可包含微流体通道网络。所述微流体通道网络可包含与包含微胶囊悬浮液的第一水性流体的来源耦合的第一通道区段;与第二水性流体的来源耦合的至少一个第二通道区段,所述第一和第二通道区段在使所述第一水性流体与所述第二水性流体相接触的第一交叉部流体连通;以及与所述第一交叉部耦合并与至少一个第四通道区段在第二交叉部相交的第三通道区段。所述至少一个第四通道区段可与和所述第一和第二水性流体不互溶的流体的来源耦合。此外,所述第二交叉部可将所述第一和第二水性流体分割成在所述流体内的液滴。所述微流体系统还可包含与所述微流体通道网络可操作地耦合的流动控制系统。所述流动控制系统可使所述第一、第二和第三流体流动通过所述微流体通道网络,从而以至少50Hz并且变化小于20%的频率在所述流体中形成包含所述第一和第二水性流体的液滴。
基于其中仅示出和描述了本公开内容的说明性实施方案的以下详述,本公开内容的其他方面和优势将变得对本领域技术人员显而易见。应当理解,本公开内容能够具有其他不同的实施方案,并且其若干个细节能够在各个明显的方面进行修改,所有这些都不背离本公开内容。因此,附图和描述将被视为本质上是说明性的而非限制性的。
援引并入
本说明书中提到的所有出版物、专利和专利申请均通过引用并入本文,其程度如同特别地且单独地指出每个单独的出版物、专利或专利申请通过引用而并入。在通过引用而并入的出版物和专利或专利申请与本说明书包含的公开内容相矛盾的情况下,本说明书旨在取代和/或优先于任何这样的矛盾材料。
附图说明
图1A、1B和1C提供了示例性分割或液滴生成流体通道交叉部的示意图。
图2示意性地图示了简单示例性流体通道架构,用于将微胶囊及其他流体分割至油包水乳液中的液滴中。
图3A和3B示意性地图示了用于将封装的试剂分割至乳液中的液滴中的示例性流体通道架构。
图4示意性地图示了对分割封装的试剂有用的示例性通道网络和微流体装置。
图5示意性地图示了用于增强对流体装置内的微胶囊组合物的操控的示例性储室结构的侧视图。
图6A和6B图示了示例性微胶囊流动调节结构。
图7A和7B示意性地图示了将含流体的容器与装置上的流体储室相接合的示例。
具体实施方式
I.概述
本公开内容提供了对处理复杂样品以供采用高通量分析系统进行分析特别有用的装置、系统和方法,该高通量分析系统包括例如高通量核酸分析系统,如核酸阵列、核酸测序系统、核酸扩增和定量系统等。特别地,本文所述的装置、系统和方法对于提供封装的试剂或试剂系统,以及将这些试剂与样品组分共分割以供进一步反应和/或分析是特别有用的。试剂和样品组分的这种共分割可用于例如通过将样品的部分分隔至不同的分区而降低样品材料的复杂性。此外,还可通过分隔试剂,使每个样品部分经历不同的反应,包括例如,将独特标识符施加于不同的样品组分,例如,将离散的条形码或标记试剂附接至离散的样品组分。
这些共分割方法的特别优良的实例在公开的国际专利申请号WO2014/028537和美国专利申请号14/104,650(于2013年12月12日提交)、14/175,935(于2014年2月7日提交)、14/175,973(于2014年2月7日提交)以及61/937,344(于2014年2月7日提交)中进行了描述,各个文献的全部公开内容均通过引用而整体并入本文以用于所有目的。
举例而言,一种特别优良的方法提供了包含与微胶囊结合的核酸条形码序列(Barcode sequence)的聚合物微胶囊组合物,其中与给定微胶囊缔合的条形码具有基本相同的核苷酸序列,但其中不同的离散微胶囊将具有与这样的微胶囊缔合的不同的条形码序列。然后,使这些微胶囊中的每一个与样品流体(如包含来自样品材料的模板核酸的样品流体)的一部分接触。然后,将包含该模板核酸和微胶囊的样品材料混合物分割为小体积(如油包水乳液的液滴),使得该微胶囊和该样品材料的一部分被包含在相同的液滴内。除了控制液滴生成过程从而在给定分区中提供所需数目的微胶囊之外,还可以控制样品材料和乳化过程,从而在每个分区内提供所需量的样品材料(例如样品核酸材料),以例如在给定分区内提供单个模板分子或所需水平的基因组覆盖或其他所需水平的样品材料。
在分区内,使条形码序列与样品材料(例如模板核酸)反应,以有效地标记该样品材料或其一部分。例如,通过经由例如使用条形码序列作为延伸引物的模板序列扩增使该条形码序列与模板反应,可将条形码序列有效地“附接”至复制的或扩增的模板。类似地,延伸引物的复制产生了模板的互补链以及条形码的互补序列,同样,有效地将该条形码附接至模板。然后,条形码序列或其互补序列在扩增的模板分子或其互补链上的存在,或条形码序列或其互补序列与该扩增的模板分子或其互补链的附接,允许包含该条形码的序列读序(sequence read)以一定水平归属于最初分配至该分区的样品材料的相同部分,例如,相同模板分子或相同样品组分。
在许多情况下,包含一种或多种条形码序列的分子还可包含用于后续处理经扩增的模板序列的功能元件。这些功能序列包括例如引物序列(例如,靶向引物序列或通用引物序列)、引物识别序列、在序列内或序列复制时能形成二级结构的序列、富集序列(例如,用作亲和纯化序列的序列)、固定化序列、探针序列、反向互补或发夹序列,或多种其他功能序列中的任一种。
这样的分割过程和条形码化或标记过程存在很多种其他高价值的应用。本公开内容有利地提供了可极大地促进生成这样的分割的组合物或其组分的装置、系统和方法。
II.用于产生封装的试剂和分割的反应的流体系统
本公开内容提供了改进的流体系统,特别是改进的微流体系统,该改进的流体系统对于封装的试剂的生成以及将这些封装的试剂分割以用于后续反应和/或分析是有用的。如本文所用的,微流体系统通常是指采用一种或多种流体导管、通道、腔室等(它们包括一个或多个内部截面尺寸,例如,小于1000微米、小于200微米、小于100微米,以及在一些情况下小于约50微米或甚至小于约20微米的深度、长度或宽度)的流体系统。在一些情况下,一个或多个截面尺寸可以为约20微米或更小,或10微米或更小。通常,这些微流体通道或腔室将具有至少一个在约1微米至约100微米之间的截面尺寸。
应当理解,对封装的试剂的提及并非旨在将这样的试剂的范围限制于完全封闭的胶囊,而是旨在反映将试剂与给定颗粒、珠子或其他固体或半固体颗粒相缔合的多种方法中的任一种。特别地,封装通常是指特定物质与固体或半固体颗粒、珠子、封闭体(enclosure)、分区或液滴的夹带或其他附接、偶联或缔合,并且不限于其中物质被完全或部分地封闭在较大结构内的组合物。
在一些方面,封装的试剂与形状通常为球形的微胶囊相缔合,但是该微胶囊可以是细长的、塞形的或在其特定的形状方面以其他方式变化。在一些情况下,微胶囊将具有一个或多个小于200微米、小于150微米或小于约100微米的截面尺寸。在一些情况下,本公开内容的微胶囊具有一个或多个约10至约200微米、约20至150微米、约30至125微米,在许多情况下约40至约100微米,且在其他情况下约50至约75微米的截面尺寸。
虽然微胶囊的尺寸可能是重要的考虑因素,但在许多应用中,这些尺寸的可变性也是重要的考虑因素。特别地,例如,微胶囊通过微流体系统的输送可能显著地受到该微胶囊大小的影响。例如,相比于较小的微胶囊,大得多的微胶囊的简单流动阻力可能更大。类似地,相比于较小的微胶囊,较大微胶囊的堵塞倾向可能更大。在任一种情况下,微胶囊通过微流体系统的流速可能极大地受到微胶囊大小的影响。因此,在某些方面,将以具有基本上单分散的截面尺寸的微胶囊群体提供本文所述的微胶囊。就截面尺寸而言,短语“基本上单分散”是指偏离于(例如,以变异系数表示并显示为百分比)平均截面尺寸不多于50%、不多于40%、不多于30%、不多于20%或在一些情况下不多于10%的群体。
无论是在生成用于试剂的夹带或封装的微胶囊的情况下,还是在在非水性液滴内分割水性流体的情况下,本公开内容的装置和系统均可采用类似的架构。在简化的实例中,该架构可包括与第一交叉部流体连接的第一通道区段,该第一交叉部将该第一通道区段与第二通道区段和第三通道区段流体连接。该第二通道区段向该交叉部递送与第一水性流体不互溶的第二流体(例如油),从而允许在不互溶流体流内形成水性液滴。在本文中,该第二流体可以指分散流体、分割流体等。第一和第二流体通过该交叉部并进入第三通道区段的流动是受控制的,使得第一流体的液滴被分配至第三通道区段内的第二流体的流动流中。多种针对该基本结构的修改可用于更好地控制液滴形成并带来额外的流体流。如本文所用的,流体流动的控制包括通过施加更大或更小的用于引起该流体流动的驱动力来主动地控制流体流动。此外,可通过控制一种或多种流体和/或导管(流图流动通过该导管)的流动特征,来整体地或部分地控制流动。例如,可通过在导管内提供更高的流动阻力(例如,通过提供更高的粘度、更窄的导管尺寸),或在流体流内提供更大或更小的微胶囊,或上述的任意组合,来控制流体流动。在一些情况下,通过受控制的驱动力、受控制的导管尺寸和受控制的流体性质(例如粘度或颗粒组成)中的几种来给予控制。
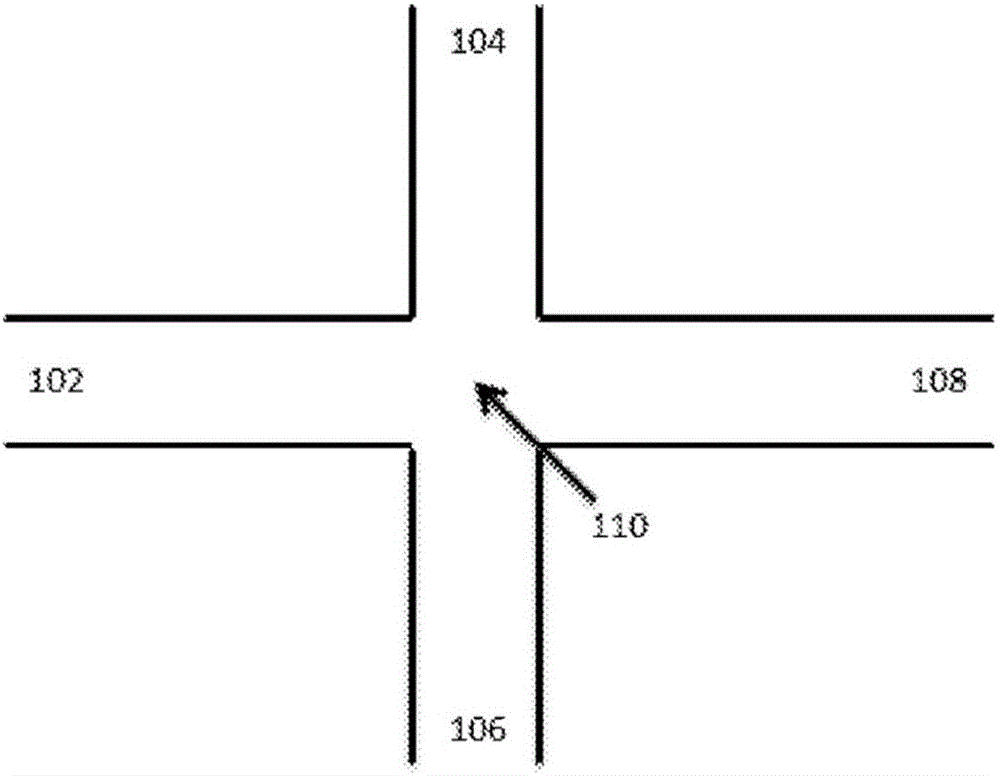
图1A提供了用于在通道中生成液滴的示例性基本通道架构的示意图。如图所示,第一通道区段102、第二通道区段104、第三通道区段106和第四通道区段108全部在第一交叉部110处流体连通。图1B示意性地图示了液滴在图1A的通道架构内的形成。
如图所示,第一水性流体112通过通道区段102流向交叉部110。与第一流体112不互溶的第二流体114经由通道区段104和106中的每一个流入交叉部110中,并进入第四通道区段108中。当第一水性流体112到达交叉部110时,其受到来自通道区段104和106的第二流体114流动的挤压,并使得第一水性流体112的单个液滴116被分配至第四通道区段108中。在一些情况下,邻近交叉部110的第四通道区段108的一部分可设置有与交叉部和/或通道区段102、104和106相比减小的截面(未示出),以促进第四通道区段108内的液滴形成。
如下文更详细讨论的,可在通道区段102、104、106或108的任一个中提供在交叉部110的上游、下游或这二者处的额外的通道区段,以允许向区段102中的第一水性流体流、区段104和/或106中的分割流体或者通道区段108中的含液滴流递送其他流体,例如,其他试剂、缓冲液等。
应当理解,该基本通道架构在用于试剂封装的微胶囊的生成中,以及这些封装的试剂与其他材料的最终分割中,被广泛使用。
在一个特定实例中并参考上述图1A和1B,可将聚合物前体材料的第一水溶液作为水性流体112而沿着通道区段102输送至交叉部110,同时将与该聚合物前体不互溶的第二流体114从通道区段104和106递送至交叉部110,以产生流入通道区段108中的聚合物前体材料的离散液滴。在一些方面,该第二流体114包含含有用于稳定所产生的液滴(例如,抑制所产生的液滴的后续聚结)的氟表面活性剂的油,如氟化油。特别有用的分割流体和氟表面活性剂的实例在例如美国专利申请号2010-0105112中进行了描述,该专利申请的全部公开内容通过引用以其全文并入本文而用于所有目的。聚合物前体材料可包含一种或多种可聚合的单体、线性聚合物或其他材料。
在制备凝胶微胶囊时,还可将活化剂与来自通道102的水性流112合并。在一些方面,将该活化剂安置在通道104和106的一个或多个中的第二流体流114内,从而允许液滴形成和反应发生同时进行,以产生所需的微胶囊116。例如,在聚合物前体材料包含线性聚合物材料例如线性聚丙烯酰胺、PEG或其他线性聚合物材料的情况下,活化剂可包含交联剂,或激活第一流内的交联剂的化学品。同样地,对于包含可聚合单体的聚合物前体,该活化剂可包含聚合引发剂。例如,在某些情况下,当聚合物前体包含丙烯酰胺单体与N,N’-双-(丙烯酰)胱胺(BAC)共聚单体的混合物时,可在通道区段104和106中的第二流体流内提供试剂如四乙基甲二胺(TEMED),该试剂引发丙烯酰胺和BAC共聚为交联聚合物网络或水凝胶。
在液滴形成中第二流体流114与第一流体流112在交叉部110接触后,TEMED可从第二流体114扩散至包含线性聚丙烯酰胺的第一水性流体112中,这将激活液滴内聚丙烯酰胺的交联,导致作为固体或半固体珠子或颗粒的凝胶例如水凝胶微胶囊116的形成。
虽然就聚丙烯酰胺封装进行了描述,但在本公开内容的上下文中也可采用其他“可激活的”封装组合物。例如,可使用藻酸盐液滴形成及随后暴露于二价金属离子例如Ca2+作为所述过程的封装过程。同样地,还可通过基于温度的胶凝,例如,在冷却后等,将琼脂糖液滴转化成胶囊。
根据本公开内容的一些方面,可在微胶囊形成时将一种或多种试剂与该微胶囊缔合。特别地,可将一种或多种试剂与组成微胶囊的聚合物基体(例如,线性聚合物)的前体试剂相缔合,使得该试剂将被夹杂在所形成的微胶囊内或以其他方式与所形成的微胶囊相缔合。例如,可将试剂与采用本文所述的过程交联成微胶囊的线性聚合物材料相偶联,导致该试剂与所形成且交联的凝胶微胶囊相偶联。或者,可将试剂与包含与该试剂相互作用的活性结合位点的聚合物前体在前体流中或形成后的微胶囊中合并。在其他方面,对于本文其他各处描述的交联活化剂,还可使活化剂与聚合物前体或形成的微胶囊接触,该活化剂激活可能与该试剂组分共价或非共价缔合的微胶囊的聚合物基体上的位点。
待并入至微胶囊中的试剂可包括多种不同试剂或对微胶囊的最终用途(例如,分析反应)有用的其他组分中的任一种。这样的试剂可包括标记基团(例如,荧光染料分子、FRET对、荧光纳米颗粒、荧光蛋白质、质量标签、电化学标签等)。这些试剂可包括生物或生化试剂,如核酸、核酸类似物、核酸模拟物、多核苷酸或类似物、寡核苷酸或类似物、酶、底物、抗体或抗体片段、抗原、表位、受体和受体结合组分、蛋白质、多肽、氨基酸、多糖,或在很多种分析的任一种中有用的几乎任何类型的生化试剂。同样地,还预想作用于生物或生化系统的化合物例如小分子药学活性化合物、放射性化合物、生物或生化化合物的抑制剂和或引发剂、化学库化合物等包含在这样的微胶囊中。在某些实例中,这些试剂可包括适用于在最终创建的分区内进行的所需反应的很多种不同试剂中的任一种,如核酸复制试剂(例如,引物、聚合酶、核苷酸或核苷酸类似物、缓冲液、辅因子等),特定的结合基团(例如,受体、抗体或抗体片段、结合肽),或任何其他试剂(例如,酶、底物、催化剂/引发剂、底物、抑制剂等)。
在一个实例中,在水性流体中提供了具有acrydite部分(Acryditemoiety)的多核苷酸,其中该多核苷酸在其交联至如本文所述的珠子之前与聚合物前体偶联。该多核苷酸可包括一种或多种功能核酸序列,如引物序列、附接序列、连接序列或条形码序列。参见,例如,美国专利申请号61/937,344,该专利申请通过引用整体并入本文。
微胶囊一旦被创建,则可从例如储室或在通道区段108末端处的其他出口收集微胶囊。然后,可洗涤所收集的微胶囊以去除交联剂,未交联的聚合物,乳化油和表面活性剂,任何其他未偶联的试剂,尺寸过大的微胶囊或其一部分,以及在微胶囊形成期间给予该微胶囊的、可潜在干扰本文所述方法和系统的使用的任何其他污染物。在一些方面,微胶囊将包含基本上纯的微胶囊组合物。基本上纯的微胶囊组合物是指,如上所述的微胶囊的单分散群体以及其相关的所需缓冲液和试剂将组成组合物的至少90%、组合物的至少95%、组合物的至少99%,并在许多情况下组成组合物的至少99.9%。一旦被洗涤,这些微胶囊可重悬在水溶液例如缓冲液和/或一种或多种选定的试剂中,以用于后续处理。根据上文,在生成上文所述的基本上纯的微胶囊时,可连续或交替使用多种不同的洗涤方案。举例而言,在一些情况下,该洗涤可包括简单的缓冲液交换洗涤,其中通过沉降、离心、过滤等将微胶囊从其支持液体中分离,然后重悬在新的缓冲溶液中,该新的缓冲溶液可以与最初含有该微胶囊的缓冲液相同或不同。可将这种类型的洗涤重复多次以从微胶囊中去除游离的污染物。在可替代或另外的洗涤步骤中,可采用更加严格的洗涤方法来从微胶囊中去除某些结合物质。例如,当微胶囊包含核酸、蛋白质或其他相关试剂时,可采用变性洗涤步骤来去除额外结合的过量蛋白质、核酸等。例如,在一些情况下,可在升高的温度下用离液剂如尿素洗涤微胶囊,以去除其他非共价结合的物质,例如,杂交的核酸等。在其他方面,可将洗涤步骤与提取技术结合,以便去除可能夹杂在微胶囊内部的物质。例如,在一些情况下,这些提取方法可包括电洗脱、渗透洗脱或其他技术,以从微胶囊内抽出非共价结合的物质。
在许多情况下,基本上纯的微胶囊组合物基本不含聚集的微胶囊,例如,粘附在一起的两个、三个、四个或更多个微胶囊。可通过包括例如基于大小或流动的分离技术(例如过滤)在内的多种方法进行聚集的微胶囊的分离。
虽然参考图1A和1B中示出的通道架构进行了描述,但应当理解,这些结构和架构的变化形式可以在本公开内容的范围内实施。例如,在一些情况下,水性流与分割流体的接口(interface)可与上述的特定架构不同。特别地,如图1A所示,通道区段112与通道区段104和106的相交提供了在通道区段102中的水性流体流与分割流体之间的接口。当水性流体被推动进入并通过该接口进入通道区段108时,液滴形成。然而,在一些情况下,接口可存在于流体装置内的开放空间或腔室或通道区段歧管内,使得接口作为分割流体的“壁”存在。这种类型的液滴生成交叉部的实例在图1C中示出。如图所示,第一通道区段122与形成液滴生成交叉部的一部分的流体歧管132流体连接。歧管132的结构设置为更大(即大于第一通道区段)的开放腔室,其具有离开该歧管的液滴分配通道134,通过该歧管,所形成的液体138通过分配通道或孔134排出至通道区段136。在一些情况下,还提供了与歧管132流体连接的附加的侧向通道区段124和126,如通道区段128和130一样。在操作时,使第一水性流体(例如,如参考图1B描述的水性聚合物前体流体,或参考下图3B描述的含微胶囊的水性流体)流入歧管132中。通过侧向通道128和130将不互溶的流体引入歧管中。在歧管132内,不互溶流体形成横穿歧管132至液滴分配端口的接口(如从通道区段128和130延伸至分配通道134的虚线示出的)。在一些情况下,通过侧向通道124和126将额外的水性流体引入歧管中。当流体流动通过液滴分配通道134时,聚集的水性流体,即,来自通道区段122且在一些情况下来自区段124和126的聚集的水性流体被来自通道区段128和130的不互溶的流体包围,并作为水性流体在不互溶流体乳液内的液滴138通过分配通道区段134排入通道区段136中。应当理解,控制液滴形成的速率,以及在这些类型的结构内的液滴中合并的流体的相对体积通过上文针对基本通道交叉口所述的许多相同的机制来实现。特别地,控制的流动可通过多种机制来实现,该机制包括,例如,控制被引入歧管中的流体的流速,控制通道进入歧管132时的几何形状例如通道形状、尺寸(深度和/或宽度)、交叉口轮廓和结构、以及与其他通道相比从歧管的后移。
另外,虽然在图1A中作为用于液滴生成的单个接口示出,但应当理解,本公开内容的装置和系统通常将包含多路液滴生成接口,以便提高通量,在该通量下,可以如本文其他各处所述产生用于微胶囊形成或用于分割微胶囊的液滴。例如,本公开内容的装置或系统可包含多个重复的具有图1A和/或1C中示出的架构的通道网络。而且,对于这样的多路装置或系统,就共同的储室或共同的通道或通道歧管而言,重复的通道网络内的各个通道区段中的一些可具有共同的流体来源,或可进料至共同的出口或储室。同样地,在备选架构的情况下,可提供与分割流体腔室连通的多个水性流体进料通道区段。
图2示意性地图示了用于产生上述微胶囊的微流体装置或装置模块。如图所示,该微流体装置通常包含包括其内部部分的主体结构200,即包含通道区段202、204、206和208的通道网络。这些通道区段全部与共同的通道交叉部210相连通。该装置主体结构还包含试剂储室212和214。如图所示,试剂储室212与通道区段202流体耦合,而试剂储室214与通道区段204和206流体耦合。第三出口储室以储室216示出,其与通道区段208流体连通。应当理解,可以在储室212中提供水性聚合物凝胶前体,而在储室214中提供分割流体和活化剂。这些流体通过交叉部210的流动产生如上文所述的微胶囊,该微胶囊流入储室216并从该储室216收获。
这些微流体装置或装置模块可以以多种常规方式中的任一种进行制造。例如,在一些情况下,该装置包含层状结构,其中第一层包含安置有与完成的装置中的通道网络对应的一系列通道或凹槽的平面表面。第二层包含在一侧上的平面表面,以及限定在相对的表面上的一系列储室,其中该储室作为通路连通至平面层,使得当第二层的平面表面与第一层的平面表面配对时,限定在第二层中的储室被定位为与第一层上的通道区段的末端流体连通。或者,可将储室和连接的通道结构两者制造成单个部件,其中储室设置在该结构的第一表面上,且储室的孔延伸至该结构的相对的表面。通道网络被制造成该第二表面中的一系列凹槽和特征。然后,在第二表面上提供较薄的层压层以进行密封,并提供通道网络的最终的壁和储室的底部表面。
这些层状结构可整体或部分地由聚合物材料,如聚乙烯或聚乙烯衍生物如环烯烃共聚物(COC)、聚甲基丙烯酸甲酯(PMMA)、聚二甲基硅氧烷(PDMS)、聚碳酸酯、聚苯乙烯、聚丙烯等制造,或者其可以整体或部分地由无机材料,如硅或其他基于二氧化硅的材料,例如,玻璃、石英、熔融石英、硼硅酸盐玻璃等制造。
可使用多种工艺中的任一种来制造聚合物装置组件,该工艺包括压印技术、显微机械加工例如激光加工,或在一些方面包含限定的通道结构以及其他结构(例如,储室、整合的功能组件等)的层组件的注射成型。在一些方面,包含储室和通道结构的结构可使用例如注射成型技术来制造,以产生聚合结构。在这样的情况下,可通过包括热层压、基于溶剂的层压、声波焊接等在内的容易获得的方法将层压层粘附至模制的结构化部件。
应当理解,还可使用已知的技术制造由无机材料组成的结构。例如,可使用标准的光刻技术,将通道和其他结构微加工至表面中或刻蚀至表面中。在一些方面,可通过使用三维打印技术制造装置和/或其离散组件的通道或其他结构来制造微流体装置或其组件。
如之前提到的,上述通道架构还可容易地用于将上述微胶囊例如包含封装的试剂的微胶囊分割在产生于不互溶流体如“油包水”(WO)乳液体系中的液滴内,其中水性溶液,特别是包含本文所述的封装的试剂的水性溶液,作为分割的液滴分散在不互溶分散液或分割流体如不互溶的油内。
图3示意性地图示了封装的试剂的分割。如图所示并参考图1A中示出的流体架构,包含有封装至少第一试剂的珠子的第一水性流体通过通道区段102流入通道交叉部110。该分散流体从侧向通道区段104和106流入交叉部110。然后,水性流体被分割至分散流体的流动流内的液滴中,其中单个液滴包含封装的试剂,并且在一些情况下仅含有单个试剂珠子或胶囊。
上述通道架构被包含在图3A中示出的通道系统示例中,用于将微胶囊(包括例如封装的试剂)与样品材料分割至例如油包水乳液体系中。如图所示,显示第一通道区段302与通道区段304、306和308在第一通道交叉部310处流体连接。第四通道区段308将第一通道交叉部310与第二通道交叉部322流体连接,该第二通道交叉部322还与通道区段324、326和328流体耦合。
在对封装的试剂进行分割的情形中,图3A的通道系统在图3B中示出。如图所示,含有可包含封装的试剂的微胶囊350(例如,诸如,如上文所述制备的微胶囊)、珠子等的第一水性流体312的第一流通过通道区段302流入通道交叉部310中。第二水性流体352和354的其他流从通道区段304和306引入至通道交叉部310中,以加入含有微胶囊350的第一水性流体312。通过通道区段304和306中的每一个添加的水性流体可以是彼此相同或不同以及与水性流312的流体部分相同或不同的。应当理解,各个通道区段通常将与将流动通过这些通道区段的流体的来源流体地耦合。这样的流体来源可包括整合在装置内或与装置接合的储室,或可包括与其他流体系统例如注射器、泵、流体网络等的其他接口,或与外部储室例如用于从管、小瓶、孔等抽取流体的外部流体加入系统,或甚至外部加工系统例如扩增系统、样品材料提取系统、过滤系统、分离系统、液相色谱系统等接合。
在一些方面,通过侧向通道304和306添加的其他水性流体可包含有待与包含在微胶囊内的封装试剂一起分割的样品材料。例如,第二水性流体可包含可与包含在微胶囊内的试剂一起分割至单独的液滴中的样品核酸,如条形码序列、功能序列等。还可以在第二水性流体中添加其他试剂。在一些情况下,例如,当封装的试剂将要用于核酸复制或合成反应时,其他流体可包括用于这样的反应的试剂,如DNA聚合酶、引物序列、核苷酸或核苷酸类似物、反应辅因子、缓冲液等,以及多种其他试剂中的任一种,例如,染料、标签、螯合剂、抑制剂、引发剂、底物等。
在一些情况下,添加的试剂可包括刺激封装的试剂释放至所产生的液滴中的试剂。例如,在一些情况下,可通过二硫键或其他可化学裂解的键将试剂与微胶囊缔合,或者可通过二硫键交联或其他可化学裂解的交联剂将微胶囊在结构上保持在一起。这样,还原剂如二硫苏糖醇(DTT)的添加可通过直接释放或通过微胶囊溶解或这两者,导致微胶囊上试剂的最终释放(参见,例如,于2014年2月14日提交的美国专利申请号61/940,318,该专利申请的全部公开内容通过引用以其整体并入本文用于所有目的)。可替代地或附加地,其他可裂解的键可用于交联微胶囊。这样的键的实例包括例如可光裂解或可化学裂解的键或交联体。
来自例如流体312、352和354的合并的水性流通过通道区段308流入通道交叉部322。将与从通道区段308流出的合并水性流不互溶的第三流体314从通道区段324和326中的每一个引入至通道交叉部312中,以形成包含微胶囊350的液滴356,以及一定量的合并的水性流体。在许多情况下,该第三不互溶流体包含如上文所述适合于形成具有稳定化所得液滴的油包水乳液的油,如含氟表面活性剂的氟化油。在一些情况下,其他合适的乳液体系可包括硅和烃油/表面活性剂体系。
如上文提到的,本文所述的装置对在不互溶流体中提供水性液滴内的微胶囊是有用的。应当理解,在多个应用中,在所形成的分区中提供所需水平的微胶囊占据是特别有利的。通常,这通过控制包含微胶囊的水性流与不互溶流体流的组合,使得多于所需数目的微胶囊被并入给定分区中的可能性为可接受的低水平来实现。这通常可以通过控制微胶囊的流动以及控制在分割区域(例如,图3中的交叉部322)中集合在一起的其他流体的流动来实现,以便基本上在每个分区提供所需数目的微胶囊。
在许多情况下,使用所述装置、系统和方法确保基本大多数占据的分区(例如,含有一个或多个微胶囊的分区)中的每个占据分区将包含不多于1个微胶囊。特别地,在一些情况下,控制分割过程,使得少于50%的占据分区含有多于一个微胶囊,少于45%的占据分区含有多于一个微胶囊,少于40%的占据分区含有多于一个微胶囊,少于35%的占据分区含有多于一个微胶囊,少于30%的占据分区含有多于一个微胶囊,少于25%的占据分区含有多于一个微胶囊,并且在许多情况下,少于20%的占据分区具有多于一个微胶囊,而在一些情况下,少于10%或甚至少于5%的占据分区中的每个分区将包含多于一个微胶囊。因此,在许多情况下,所得到的分区将导致至少50%的分区含有一个且仅含有一个微胶囊(即,单个微胶囊),至少55%的分区含有一个且仅含有一个微胶囊,至少60%的分区含有一个且仅含有一个微胶囊,至少65%的分区含有一个且仅含有一个微胶囊,至少70%的分区含有一个且仅含有一个微胶囊,至少75%的分区含有一个且仅含有一个微胶囊,至少80%的分区含有一个且仅含有一个微胶囊,至少80%的分区含有一个且仅含有一个微胶囊,至少85%的分区含有一个且仅含有一个微胶囊,至少90%的分区含有一个且仅含有一个微胶囊,并且在一些情况下至少95%的分区含有一个且仅含有一个微胶囊。
附加地或可替代地,在许多情况下,期望避免形成数目过多的空分区。虽然这可通过向分割区域中提供足够数目的微胶囊来实现,但预期泊松分布可增加可包含多个微胶囊的分区的数目。这样,根据本公开内容的方面,控制一个或多个微胶囊或被引导进入分割区域中的其他流体的流动,使得在许多情况下,不多于50%的所生成的分区将未被占据(即包含少于1个微胶囊),不多于25%的所生成的分区或不多于10%的所生成的分区将未被占据。此外,在一些方面,控制这些流动以便在提供低水平的未占据分区的同时呈现出单一占据分区的非泊松分布。重申一下,在一些方面,将实现上述提到的未占据分区的范围,同时仍提供以上所述的任何上述单一占据率。例如,在许多情况下,本公开内容的装置、系统和方法的使用形成了具有低于25%、低于20%、低于15%、低于10%,并且在许多情况下低于5%的多重占据率,同时具有低于50%、低于40%、低于30%、低于20%、低于10%,并且在一些情况下低于5%的未占据分区的所得分区。用于控制通道网络内的各种流动的方法、系统和装置配置在下文中进行了更详细的描述。
虽然上文就提供基本上单一占据的分区进行了描述,但在某些情况下,期望提供多重占据的分区,例如,在单个分区内含有两个、三个、四个或更多个微胶囊。因此,如上文提到的,可以控制含微胶囊流体和分割流体的流动特征,以提供这样的多重占据的分区。特别地,可以控制流动参数,以提供大于50%的分区、大于75%并在一些情况下大于80%、90%、95%或更高的期望占据率。
另外,在许多情况下,在单个分区内的多个微胶囊可包含封装在其中的不同试剂。在这样的情况下,通过进入共同通道或液滴生成交叉部的不同通道入口,从不同的微胶囊来源(即,含有不同封装试剂的)向这样的共同通道或液滴生成交叉部中引入不同的微胶囊可能是有利的。在这样的情况下,可以控制不同微胶囊向该通道或交叉部中的流动和频率,以提供所需比例的来自每个来源的微胶囊,同时确保这样的微胶囊向分区中的期望的配对或组合。
虽然通过两个交叉部及其相关的通道区段示出,但应当理解,可以在本公开内容的装置内提供额外的通道,以向上述的各个流体、胶囊和分区递送额外的组分。可以提供与本文所述的各个通道区段中的任一个相交的这些额外通道,以用于在不同的位置向在这些通道区段内流动的各种流体中的任一种或多种添加多种组分,用于不同的目的。例如,在一个方面,可提供与上述通道区段328相交的一个或多个额外的侧向通道,以实现向通道区段328内的分割的流体引入新流体、试剂或额外的分割流体的目的。
同样地,可以提供与通道区段302和/或308相交的额外的通道区段,以便在用分割流体将该流体流分离成液滴之前,向水性流中引入额外的流体。另外,可以提供与侧向通道区段例如通道区段304、306、324或326中的任一个相交的其他通道区段,以便向这些通道递送不同的流体。这样的系统可允许通过控制哪种流体通过各自的侧向通道提供,来实时改变引入到分割流中的流体,从而允许例如改变反应物,改变分割流体特征,或多种其他条件中的任一种。
在一些情况下,这些额外的流体可以用于通过向分区中引入新试剂来刺激分区内的不同反应的目的。例如,这些额外的流体可向分区或胶囊提供一种或多种活化剂,该活化剂在分割之前或之后的任何阶段导致一种或多种反应的引发。
这样的活化剂可以采取多种不同形式的任一种。例如,这些活化试剂可例如通过裂解微胶囊与试剂之间的键,或通过刺激微胶囊的分解及随后的试剂释放而导致分区或胶囊内试剂的释放,以使其可用于反应。可替代地或附加地,该活化试剂可包括期望反应的引发剂,如该期望反应缺少的关键试剂等。举例而言且为了说明的目的,在期望的反应包含核酸聚合酶介导的核酸复制的情况下,活化试剂可包括缺少的关键试剂,如混合物中缺乏的一种或多种核苷三磷酸,引物序列,或适合用于聚合酶反应的一种或多种反应辅因子,例如,二价金属离子如镁或锰。在许多情况下,用于控制给定反应的引发的目的的这类缺失体系或可激活试剂体系的使用被称为“热启动”试剂,其作为通用类别与本公开内容的系统结合是有用的。
活化试剂可以可替代地或附加地引发分区或胶囊自身或两者上的反应,例如,破坏胶囊或从这些胶囊释放试剂,使分区稳定或不稳定,以便例如分别减少或促进聚结。多种试剂体系可用于本公开内容的微胶囊的破坏或从中释放试剂。这包括如美国专利公开号2014/0378345中讨论的,使用上述化学刺激物断开化学交联或分子连接,该专利文献通过引用整体并入本文。
图4提供了用于如上所述分割封装的试剂的整个示例性微流体装置或装置模块的示意图。如图4所示,整个装置400提供了用于生成分割的微胶囊组合物的一个或多个通道网络模块450。如图所示,通道网络模块450包含与以上图3B所示的相似的基本架构。特别地,所示的通道网络模块包含连接通道区段402、404和406的第一通道交叉部410,以及将第一交叉部410与第二通道交叉部422连接的通道区段408。第二交叉部422还与通道区段424、426和428连接。
如图所示,通道区段402还与储室430流体耦合,储室430提供例如悬浮在水溶液中、可包含一种或多种封装试剂的微胶囊的来源。通道区段404和406中的每一个与流体储室432类似地流体耦合,储室432可提供例如样品材料以及将要与微胶囊一起分割的其他试剂的来源。如之前提到的,虽然以通道区段404和406都与同一储室432耦合的方式进行说明,但这些通道区段可以与用于引入将要与微胶囊一起分割的不同试剂或材料的不同储室耦合。
通道区段402、404和406中的每一个可设置有额外的流体控制结构,如被动流体阀436。这些阀可通过在阀结构中通道区段变宽处破坏将水性流体吸入装置中的毛细力,来提供整个装置的控制填充。简言之,首先将水性流体引入至储室430和432中的装置中,此时这些流体将通过毛细作用被吸入其各自的通道区段中。在到达阀结构时,变宽的通道将破坏毛细力,并且流体流动将会停止直到受到外力例如正压或负压的作用,从而驱使该流体进入并通过该阀结构。虽然以通道的宽度尺寸变宽的方式说明,但应当理解,被动阀结构可包括通道区域的任一个或多个截面尺寸的增加。例如,被动阀可以增加阀区处通道的阶梯式(stepped)深度。此外,当流体到达截面增大的通道区段时,毛细力将使流体保留在更浅的通道内。此外,如所提到的,截面尺寸的增加可以是任一个或多个截面尺寸的增加,并且可以是至少约5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%或甚至更大的截面增加。在许多情况下,其可以是约5%至约100%的截面增大,约5%至约50%、约5%至约20%的截面增加。虽然在特定的通道位置处进行了说明,但还应当理解,这些阀结构可以沿着微流体通道网络内的任何通道位置(包括在两个或更多个通道区段的交叉口处,或在单个通道内)定位。
在通道区段402中还示出了微胶囊漏斗结构452,该微胶囊漏斗结构452允许微胶囊从储室430的有效集中、微胶囊流动的调节(如在本文其他各处更详细描述的)以及减少由于通道堵塞造成的系统故障。同样如图所示,在一些情况下,通道区段402与储室430的连接处以及一个或多个或全部通道区段与其各自储室的交叉部可设置有附加的功能元件,如过滤结构454,例如柱、杆、曲折流体路径或其他阻塞结构,以防止不想要的微粒物质通过通道区段进入或行进。
交叉部410与第二交叉部422流体耦合。通道交叉部422还与通道区段424和426耦合,该通道区段424和426继而与储室438流体耦合,该储室438可提供例如与从交叉部410流出的水性流体不互溶的分割流体。此外,通道区段424和426被示为与相同的储室438耦合,但它们可与不同的储室耦合,例如,当期望每个通道区段向交叉部422递送不同的组合物,例如具有不同组成、包含不同试剂等的分割流体时。
在示例性操作中,储室430中提供的微胶囊通过通道区段402流入第一通道交叉部410。如下文更详细描述的,该微胶囊将流动通过阀436,该阀436除了提供被动流体阀结构之外,还作为微胶囊流动调节器运转。该微胶囊流动调节器确保微胶囊向交叉部410中以及通过交叉部410向通道区段408中的流动更加规律。在交叉部410内,水性微胶囊溶液与如通过通道区段404和406引入的来自储室432的水性流体接触。由于微流体通道网络的层流特征,并且不受任何特定操作理论的束缚,来自通道区段404和406的水性流体可与第二水性流体层一起包裹微胶囊组合物,其中这两种流体之间的主要相互作用是通过简单的扩散,即,基本上没有对流混合。
然后,水性流体流通过通道区段408流入第二交叉部422。在通道交叉部422内,流动通过通道区段408、包含规则间隔流动的微胶囊的水性流体流在从通道区段424和426引入的不互溶分割流体内形成液滴。在一些情况下,可进一步配置一个或两个分割交叉部例如交叉部422以及与该交叉部耦合的一个或多个通道区段例如通道区段408、424、426和428,以优化交叉部处的分割过程。
此外,如本文其他各处所述,虽然以交叉通道交叉口示出(其中水性流体通过通道区段408流入分割交叉部422以被来自通道区段424和426的不互溶流体分割,并流入通道区段428),但本公开内容的微流体装置内的分割结构可包含多种不同的结构。
如本文其他各处更详细描述的,控制微胶囊向交叉部422的流动,以及在一些情况下其他水性流体和/或分割流体通过交叉部410和422的每一个流动的速率,以提供所需水平的微胶囊分割,从而例如控制将会被分割在每个液滴中的微胶囊的数目、每个液滴中试剂的量,并控制装置的总体运行以便例如防止堵塞或其他破坏等。
一旦微胶囊被分割,则其流动通过通道区段428并进入回收结构或回收区,在该回收结构或回收区中可容易地将其收获。如图所示,该回收区包括例如出口储室438。或者,回收区可包含多种不同接口中的任一种,包括与管、孔、其他流体网络等的流体接口。在一些情况下,当回收区包含出口储室时,该出口储室的结构将设置为具有大于流入该储室的流体的预期体积的体积。就其最简单的含义而言,在一些情况下,该出口储室可具有等于或大于系统的输入储室(例如,储室430、432和434)的总体积的体积容量。
应当理解,单个微流体装置可包含多个基本相同的通道网络模块,该通道网络模块可各自具有独立的流体来源或可共享一个或多个流体储室。例如,包含多个通道网络模块的单个多路装置可包含分割流体、含微胶囊流体、一种或多种试剂流体以及样品流体中的一种或多种的单一来源。这样,可使用多个通道模块通过例如在多路装置中的每个模块450的相应储室中提供相同的流体分配(allocation),来生成大量相同类型的分割的微胶囊。然而,在某些方面,不同的通道网络模块将用于生成不同的分割的微胶囊。这样的不同的分割的组合物可包含被分配至分割的微胶囊的不同样品材料,被分配至相同或不同样品材料的不同的初始微胶囊,或向相同或不同样品材料和/或不同微胶囊应用不同试剂。如上文提到的,当相同的流体被引入至不同模块的通道区段中时,这样的通道区段与相同储室流体耦合可能是有效的。这些通道区段可以是每个模块中相同的相应通道区段,或者根据所需用途,它们可以是不同模块中的不同通道区段。
应当理解,无论是出于微胶囊生成的目的还是出于其后续分离至离散分区或液滴的目的,上述通道结构中不同流体聚在一起的速率可以对液滴生成产生影响。因此,在某些方面,本公开内容中使用的装置提供了对整合的通道网络内各种流体流动的控制。对通道网络内的流体流动的控制可通过多种机制实现。例如,可以在不同通道区段的起点处(例如,储室上)施加压力,以便控制该通道区段内的流体流动。通过利用基于压力的流动,可以能够通过将单独控制的压力源与不同通道区段耦合以在每个通道区段上施加差异压力梯度,来独立地控制不同通道区段内的流动。在这样的情况下,可通过例如接合的检测系统如光学检测器来监测不同通道区段内的流速,以提供流动控制方面的反馈,从而允许流动的调节。
或者,可通过例如将压力源耦合至与多个通道区段起点或储室同时连接的歧管,来同时将单个压力源与所有通道区段耦合。当在多个通道上施加单一压力时,将通过受流体粘度和通道尺寸(截面和长度)影响的每个通道内的阻力水平来控制这些通道内的流速。在这样的情况下,通过为通道区段提供适当的尺寸以在考虑到经过其的流体的粘度的情况下实现所需的流速,来实现流动控制。举例而言,为了实现相等的流速,可以为用于更加粘稠流体流动的通道提供比用于输送更低粘度流体的通道更宽和/或更短的通道区段。
虽然针对施加于通道起点的压力源进行了描述,但在一些方面,该压力源可包括真空(或负压)源,该真空源施加于通道网络的一个或多个出口端,例如末端储室,即,图4中的储室444。真空的施加提供了相对于正压驱动系统的多个优势,包括例如相对于若干个入口点在出口处提供与整合的通道网络的单点连接,缺少可能导致正压系统中的通道入口堵塞的微胶囊压缩等。
在一些情况下,为了分割微胶囊,可将真空源施加于与可以收获分割的微胶囊的区域不同的出口通道区段上的节点。特别地,当真空源施加在末端储室例如图4中的储室438时,可将该真空源与储室断开,以便从该末端储室收获分割的微胶囊。在一些情况下,通过将真空源接口节点与来自收获分割的微胶囊的区域的通道区段分离,可以不需要断开真空源及改善使用的方便性。在一些情况下,真空接口节点可包括末端储室,例如储室438,该末端储室可配置有用于与整合或离散的分割收获区接合的接口组件,该接口组件允许在不去除连接的真空源的情况下收获分区。在下文中更详细地描述了这些及其他接口组件。
III.其他改进的微流体系统组件
微胶囊的形成或后续分割中的精确处理和操控产生了微流体系统中的一些新的挑战,这些挑战被本公开内容的方面解决。特别地,流体系统,特别是微流体系统中微胶囊的流动可受到某些可变性的影响,这些可变性中的许多已在上文提到,包括变化的流速或分配频率、通道堵塞、可变的分割、取样或分配偏差等。本公开内容提供了用于解决这些问题中的许多问题的多种改进的组件、装置、方法和系统。
例如,在某些方面,本公开内容解决了例如来自储室中的微胶囊的取样偏差或可变性。特别地,在一些情况下,在本文所述的系统或装置中的、微胶囊沉积于其中的一个或多个储室(例如,图4中示出的储室430)被配置用于改善微胶囊向其连接的通道区段中的流动。
在一个实例中,用于提供微胶囊或其他试剂的储室可设置有圆锥形底表面,以允许微胶囊朝向与该储室连接的通道区段的入口汇集。这在图5A中示意性地示出,其显示了从侧向观察的储室500、502、504和506的示例。如图所示,储室500包含从微流体装置506的上表面512延伸出的侧壁510。该储室的内部空腔部分508延伸至微流体装置506中并设置为与流体通道516连通。如图所示,空腔部分508具有借助空腔508的会聚侧壁(converging wall)518形成的,如通过空腔508变窄限定的,朝向通道516的入口的逐渐变窄的或锥形形状。
在其他方面,可通过包含在储室与连接的流体通道之间的加宽的接口区或入口来提高微胶囊向通道区段中的装载。这样的一个实例在图4的通道网络中示出,其中通道区段402与储室430的接口设置有漏斗通道结构452,该漏斗通道结构452既提高了微胶囊向通道区段中的引入,又为进入通道区段的微胶囊提供了一些流动调节特征。还示出了提供针对较大微粒物质的障碍物的阻塞结构454,该较大颗粒物质可以是储室内的污染物并且可损害流体通过装置通道的流动。应当理解,各个储室可各自或全部在其中包含过滤或颗粒阻挡元件,该过滤或颗粒阻挡元件可以相同或不同,取决于安置在该储室中的流体。例如,在一些情况下,简单的结构障碍物,如图4中示出的柱结构(例如,结构454),可在与含微胶囊储室的通道接口中使用,而对于含有水溶液例如样品材料或试剂的那些储室,可在其中例如在储室的底部整合更严格或不那么严格的过滤组件,以便以更高或更低的程度原位过滤储室的内容物。包含例如膜过滤器、烧结过滤器(frits)或其他已知过滤器类型在内的多种过滤介质可容易地并入本公开内容的装置内的储室中。
与上述加宽的接口类似,该接口可包含来自给定储室的多个离散的通道入口,以确保微胶囊进入并通过通道区段的流动不容易中断或堵塞,以及确保安置在储室中的微胶囊在多个点处进入,而不是在单个点或通道入口处进入。特别地,对于给定的储室,可设置有将该储室与微流体装置内的单个通道区段(或流动调节交叉部,如下文更详细描述的)流体连接的多个通道入口。而且,如上所述,该多个通道入口可设置有上述功能元件中的一个或多个,例如,漏斗结构、过滤元件如柱、杆或曲折路径等。
如在上述微胶囊分割的讨论中提到的,可以控制微胶囊的流动和在分割区域(例如,图3中的交叉部322)中集合在一起的其他流体的流动,以便基本在每个分区提供所需数目的微胶囊。在许多情况下,基本上大多数占据的分区(例如,含有一个或多个微胶囊的分区)中的每个占据分区将包含不多于1个微胶囊,而在一些情况下还减少所形成的未占据分区的数目。
如上所述,本公开内容的方法、装置和系统通常通过微胶囊与分割或分散流体进入液滴的受控组合,例如,通过控制微胶囊和油进入微流体装置的液滴生成交叉部(即,如图3所示的交叉部312)的流速,来实现微胶囊向分区的所需水平的分配。
微胶囊从储室通过通道进入通道交叉部的流动可受到大量可变性的影响,因为这些微胶囊可以以由微胶囊进入通道区段时的偶然事件以及其通过该通道区段的流速限定的流速流动。因此,在某些方面,本公开内容的微流体系统可包含在适当的通道区段内的微胶囊流动调节器组件,以提供以更加明确的规律性流入液滴形成区中的这样的微胶囊。
包含在本文所述的通道系统内的微胶囊流动调节器通常将提供以相对规律的频率在通道内流动的微胶囊。特别地,在液滴生成的给定时间范围期间,例如,10秒窗口、30秒窗口、1分钟窗口、2分钟窗口、3分钟窗口,或在整个液滴生成运行的稳态操作(例如,不包含启动和关闭)期间,这些微胶囊流动的频率的变异系数通常将小于50%、小于40%、小于30%、小于20%、小于10%,以及在一些情况下小于5%。应当理解,微胶囊的流动频率反映了在一秒的时间段内流动经过导管中的给定点的微胶囊数目。频率测量通常可基于亚秒或一秒的间隔,但还可基于多秒、多分钟或更长的间隔,这取决于工艺的具体需求。
虽然在给定工艺中,使微胶囊以相对稳定的频率流动可能是期望的,但在一些方面,流动的微胶囊的频率可根据所需的应用、流动流体的性质等而不同。然而通常,流入分割交叉部或液滴生成交叉部的微胶囊以大于50Hz、大于100Hz、大于250Hz、大于500Hz、大于750Hz、大于1000Hz、大于1500Hz、大于2000Hz、或甚至大于5000Hz或甚至10,000Hz流动,同时仍达到期望的占据率和其他工艺目标。在某些情况下,可以在分割交叉部之后维持这些流动频率,使得分割的微胶囊以至少或大于50Hz、至少或大于100Hz、至少或大于500Hz、至少或大于750Hz、至少或大于1000Hz、至少或大于1500Hz、至少或大于2000Hz、或甚至至少或大于5000Hz或10,000Hz的频率流出该液滴生成交叉部。
可采用多种方法来调节本文所述装置的微流体通道区段内的珠子流动。例如,在一些情况下,这些调节器包含“集中区”,微胶囊将会流入该集中区中并在流出该集中区前进行集中。这些区被配置用于通过包含漏斗结构或通道轮廓以更好地测量单个微胶囊的流动,来更有效地测量微胶囊的流动。这样的结构的实例在上文中提到,并且在图4和图6B中示出。第一个实例包括以整合在通道区段402与储室430的接口内的漏斗区452示出的通道接口。
以类似的方式,可将微胶囊流动调节器整合在通道区段(例如,图4中的通道区段402)自身内,而非整合在与储室例如图4的储室430的接口处。该结构的实例包括图6A中示出的流动调节器结构600。应当理解,微胶囊流动调节结构460还可起到装置填充期间的被动流体阀例如阀436的作用,如上文关于通道区段402、404和406所描述的。与漏斗结构452一样,流动调节器600包含在区域604处的通道区段加宽区域602(在接口处以通道602a示出),该加宽区域在区域606处变窄直到其再次连接通道区段602的出口部分的截面尺寸(在接口处以区段602b示出)。当微胶囊进入扩张区602时,连续流动将允许多个微胶囊在整个集中区内集中或聚集。一旦聚集了足够数目的微胶囊,这些微胶囊将开始以计量且更受控的方式通过变窄的区域流入通道区段604。这在图6B中示意性地示出,其显示微胶囊以无规律的频率流入微胶囊流动调节结构中,并以更加规律的频率流出该调节器。应当理解,通道网络可包含连续或平行排列在给定流动路径内(例如,总网络中两个点之间的流体连接处)的一个或多个流动调节器。虽然这些流动调节器可包括具有如图6A和6B中示出的形状和配置的那些,但其还可以包含不同的形状和配置。例如,流动调节器的加宽区域可包含与图6A和6B中示出的类似的三角形形状,或可包含拉长的三角形形状。同样地,流动调节器的加宽区域可包含圆形、椭圆形或半圆形或半椭圆形形状,或可包含类似于本文其他各处描述的通道接口的锥形漏斗形状。应当理解,这些示例性流动调节器的基本结构组件是在流动进入调节器的点处的加宽的通道区,其具有流动进入后续通道或通道网络时的锥形、变窄或漏斗部分。这些加宽的区域通常将具有更宽的截面,该截面是流入该加宽区域中的通道区段的截面的1.1倍至20倍。在一些方面,这些加宽的区域为入口通道区段截面的2倍至10倍之间的任意值(与相同的截面量度相比,例如宽度比宽度、深度比深度等),并且在一些情况下为入口通道区段截面的2倍至5倍。在一些情况下,多于一种截面尺寸可在入口通道上变化,例如,宽度和深度都可以不同。此外,虽然在一些方面,当两种尺寸都变化时,它们将大于入口通道的尺寸,但在一些情况下,如果宽度和深度中的至少一个是增加的,则另一个尺寸可以是减小的,这取决于通过该流动调节器的期望的流动特征。
在其他实例中,多个含微胶囊的通道在集中区处汇聚在一起,以使更大数目的微胶囊进入交叉部以及其连接的流出物通道区段中。这允许在一个通道的微胶囊流动中的孔隙被从另一个通道流入的微胶囊填充。这些通道区段可包含作为集中区提供在通道网络内的单独的通道区段,或如上所述,其可包含与含微胶囊的储室流体连接的多个入口通道区段。此外,如上文提到的,这些通道区段可将来自单个微胶囊来源或群体的微胶囊递送至同一通道区段,或者其可将来自不同来源例如储室的微胶囊递送至共同的通道区段,其中这些不同的微胶囊包含不同的试剂。
如上文提到的,本公开内容的微流体装置和系统可包含对该装置和系统的运行有用的改进的接口组件,以及可能在微胶囊组合物和分割的组合物的处理和操控中特别有用的接口组件。
对微胶囊和分区操控有用的接口的实例包括对这样的组合物向这类装置沉积以及从这类装置收获该组合物中之一或两者有用的那些接口。例如,如上文提到的,溶液中微胶囊的移动和输送可能受到一些可变性的影响。在一些情况下,这种可变性可继续存在于这些溶液从产生该溶液的系统向其他系统和/或容器例如储存容器如管、孔、小瓶等中的输送中,或继续存在于该溶液从储存容器如管、孔、小瓶等向用于其后续处理的系统(例如,类似于上文描述的那些系统的微流体分割系统)的输送中。在一个实例中,将微胶囊溶液或悬浮液提供在包含可刺穿的壁或基底表面的储存容器内。相应的刺穿结构可提供在流体装置上的储室内。通过将储存容器插入至储室中,该可刺穿的壁被刺穿结构穿透,从而向储室释放微胶囊悬浮液。
这种类型的接口的实例在图7A和7B中示意性地示出。如图7A所示,提供了用于容纳流体试剂如微胶囊悬浮液704(如本文其他各处所述)的储存容器,如管702。容器的表面,例如基底表面706,作为可刺穿层提供。可刺穿层可以以多种不同配置中的任一种提供。例如,可刺穿层可简单地包含与该容器的其余部分相同材料的壁,但其足够薄以允许刺穿。这样的壁可以比容器中的其他壁更薄。或者,可刺穿的表面可包含与该容器的其余部分的材料不同的材料,如可刺穿隔膜(例如,硝化纤维素、PVDF、胶乳或任何其他类似使用的材料)、箔表面或多种其他可刺穿膜中的任一种。同样地,储存容器的表面可设置有可以是主动或被动的阀结构。在许多情况下,可以在储存容器的基底表面706中采用被动阀,如压力触发式止回阀。
如图7B所示,使用时,储存容器与装置710中的储室708配对。储室708配置有刺穿结构712,刺穿结构712被定位为在将储存容器插入至储室708中时接触并刺穿该容器的基底表面706。一旦插入,基底表面706破裂,并且使得包含在容器702中的微胶囊悬浮液704排出至储室708中。在一些情况下,容器702可设置有用于促进驱动悬浮液进入储室中的额外组件,如柱塞或其他加压装置,以迫使悬浮液从容器中流出。在其他情况下,可使用简单的重力流来转移悬浮液。在一些情况下,刺穿结构和容器的壁或基底组件可配制为通过包含在容器上的疏水性内部涂层、闪变抑制刺穿结构(flash-mitigating piercing structure)(例如,用于降低刺穿的表面的残余物可能阻挡悬浮液流出容器的可能性),来优化悬浮液从容器向储室的转移。在可替代的方面,可提供可溶解、可降解或可以其他方式激活的障碍物,以便允许悬浮液的控制分配。这样的障碍物包括例如这样的可溶解薄膜或膜,该可溶解薄膜或膜在施加刺激物时,被降解、溶解或变得足以被穿透以分配悬浮液。这样的障碍物可以在施加特定的化学、热、电磁或其他刺激时被降解。
与上述接口类似,在一些情况下,为了从装置收获微胶囊或分割的微胶囊或其他材料,这样的接口组件可包含例如用于收获储室(例如,图2中示出的储室216或图4中所示装置的储室438)的可刺穿基底层,以允许在不必去除接合的真空源的情况下从末端储室获取和去除分割的微胶囊。在操作中,在分割操作结束时,可刺穿末端储室的基底,并通过例如逆转真空源来向储室438施加压力,以驱使分割的微胶囊通过储室的刺穿的基底层,或通过重力驱使的流动,来去除生成的分区或允许其排入或流入等待器皿。可将该等待器皿整合在装置中,或定位为邻近微流体装置,以便接收分割的微胶囊。
在其他实例中,储室和储存容器之一或两者可配置用于提供彼此间有效的转移。例如,在一些情况下,包含微胶囊悬浮液的容器可设置有接口组件,该组件允许该器皿与接收储室直接配对、连接和/或耦合,以有效地转移其内容物。在一些情况下,该连接可以受到止回阀的约束以防止悬浮液移动,直到向该悬浮液施加适当的驱动力。
除了流体接口之外,本文所述的装置和系统还可包含多种机械或物理接口组件中的一种或多种。这样的组件包括,例如,用于促进装置的手动或自动化移动和处理的处理组件,用于确保装置在仪器、支架等上的恰当放置和对准的对准组件,以及用于允许装置内样品材料的其他操控的功能组件。处理组件的实例包括突出部(tabs)、壁或被定位为远离装置的关键或敏感表面(例如,光学窗口、易污染的表面等)的其他表面,以及被配置用于促进处理(手动或自动化),例如具有足够大小和/或纹理表面以确保抓握和控制的表面。
对准结构的实例包括确保装置与相应仪器对准的机械元件,或其他固定物如斜角、装置形状以及与其他固定物上的互补结构配对的整合的关键元件(例如,突出部、槽、杆等)。这样的对准组件还包括光学检测的组件,如登记标记或基准,条形码标签,或整合或附接到装置的其他机器可读组件。
还预想到很多种功能组件或功能组件接口,包括例如对装置的运行至关重要的那些接口组件。这样的接口组件的实例包括例如可整合到或单独地放置到一个或多个储室的上表面上的垫片结构,以确保压力或真空向本文所述装置的密封施加。在某些方面,这些垫片将被整合到装置中,或以单独的一次性组件提供而不是被整合到仪器中,以便将仪器污染的可能性最小化。功能接口组件的其他实例包括用于混合或搅拌储室内的组分的接口。在一些情况下,这样的组件对防止微胶囊组合物的沉降是有用的。这些接口可包含整合到装置中的实际搅拌组件,如压电、声学或机械振动组件,或者其可包含适合用于或被配置用于与相应仪器系统或其他固定物上的这些组件接合的表面。
虽然为了清楚和理解的目的已经相当详细地描述了上述发明,但通过阅读本公开内容本领域技术人员将会清楚,在不脱离本发明的真实范围的情况下,可以进行形式和细节上的各种改变。例如,上述所有技术和装置可以以各种组合的形式使用。例如,颗粒递送可以通过所述的阵列孔分级法来实施。本申请中引用的所有出版物、专利、专利申请和/或其他文献均通过引用以其整体并入本文用于所有目的,其程度如同单独且分别地指出每个单独的出版物、专利、专利申请和/或其他文献均通过引用并入本文用于所有目的。
- 还没有人留言评论。精彩留言会获得点赞!