用于多元分析物检测、富集或纯化的杆、配套件及其使用方法与流程
本发明涉及分析与检测技术领域,具体涉及一种用于多元分析物检测、富集或纯化的杆、配套件及其使用方法。
背景技术:
本部分向读者介绍可能与本发明的各个方面相关的背景技术,相信能够向读者提供有用的背景信息,从而有助于读者更好地理解本发明的各个方面。因此,可以理解,本部分的说明是用于上述目的,而并非构成对现有技术的承认。
于1983年张子文在他发表的“细胞与以矩阵排列格式结合在固体平面上的不同抗体反应”免疫方法学杂志j.immunol.methods65(1–2):217–23文章中已描述了多元分析物检测(多元检测)的概念或“从一个样本里检测多元分析物”的测定格式。多元检测的优势在于从一个样本里(例如:一个微阵列,一个孔或一个试管里)可检测多个像蛋白质,dna和rna的生物分子。多元检测减少了测定所需的样品和测试试剂的用量和样品数量,并实现了以更少的时间和成本出更多数据的目标。
这种多元检测的概念已经在后基因组时代广泛使用。安捷伦科技有限公司,亿明达公司、昂飞公司和生命技术公司
多元检测的关键步骤在于将每个信号与其相应的分析物相配对。微阵列芯片是运用行和列格式(矩阵),计算机软件可以很容易地跟踪位置和相应的分析物的信号。因此,安捷伦科技有限公司、亿明达公司、昂飞公司和生命技术公司和其他专门从事高密度微阵列芯片产品的公司依靠阵列/矩阵系统跟踪信号和相应分析物[如上文张子文的文章;司克纳,迈.;晓尔棱,帝.;戴威斯,阿.达.;布朗,匹.欧.(1995),“互补脱氧核糖核酸微阵列定量监测基因组表达量,”科学杂志270(5235):467–70]。除了微量诊断公司和其他公司,像路明克斯公司,纳米线公司,和质谱测序公司,这些专注于中低密度多元检测的公司,使用与阵列/矩阵系统不同的技术平台来跟踪信号和相应分析物。这三个公司似乎相同是因为他们都可以在一微孔的悬浮液中做多元检测。然而,他们在如何将信号与其相应的分析物相配对上是非常不同的。路明克斯公司有其自豪的液态芯片技术(
所有上述多元检测技术具有以下共同方面:它们都依赖于昂贵且易出故障的设备来检测信号和/或将信号与分析物相配对。研究人员们要购买每种技术所需的特有试剂。基本上,任何生命科学或临床实验室中的常用实验室设备,例如微孔板读数仪,都无法做这项工作。此外,在日常临床诊断中,医生们通常希望在当天内就能拿到病人样本测试结果,但以上所述技术平台在测试几个样品或少量分析物时并不是很精简或有效易的。而且,只有经过专门培训过的技术人员才能操作这些机器并解译原始数据。结果,大多数实验室日常不做多元检测或不得不使用核心实验室做这些实验。最终,多元检测的优点,例如节省时间或金钱,在终端用户层面并没有体现。此外,当前的高密度或低密度多元检测法是如此复杂,以致难以出重复性强的可通过fda规则的数据,从而无法应用到日常临床诊断测定上。
许多公司想出其它不依靠这些高端技术的解决方案。他们利用生命科学和临床实验室的基本工具,如微孔板、微孔板读数仪和qpcr仪器,来发明新的检测方法。那些测定法是用96孔板或384孔板测量几种分析物的单元测定法。主要公司有快捷公司和应用生物系统公司/生命技术公司。快捷公司已经生产了许多用于测量蛋白质或定量核酸的产品,如多元分析物阵列酶联免疫吸附测定法和阵列聚合酶链反应分析法,可用实验室日常设备,例如微孔板读数仪和qpcr仪器。基本上,该方法确实能够在一个板中测量多种分析物,并且也适宜于测量少量样品。然而,这些本质上还是单元检测,因此它们失去多元检测的优势,例如减少样品或试剂的用量以及节省时间和金钱。应用生物系统公司也制造了许多类似的pcr微阵列,其本质上具有与快捷公司有相同的问题。最近,应用生物系统公司确实引入了pcr微阵列的改进版本-可变微阵列。反应体积为33nl(纳升),这个平台确实减少了样品和试剂的用量,缩短了反应时间,高通量。然而,它也出现了与多元检测领域中的公司的相同的问题-机器昂贵不常用,专业技术人员操作,在测试几个样品或少量分析物时并不是很精简或有效易的。因此,上述解决方案无法保持多元检测的优势或将多元检测技术简单化,从而还是不能将多元检测技术推广到每个实验室使它成为实验室常用工具。
目前的靶向富集方法主要使用微球和/或离心方法。“快速染色质免疫沉淀方法的方案”是靶标富集方法的代表性实例[久欧帝尼尔圣,欧莱葛丹尼森克&凯柔波姆伺逖克,自然杂志方法学1,179-185(2006)]。商业公司,如罗氏公司的快易富集人类外显子组库试剂盒版本3.0安捷伦公司的保证靶向富集试剂盒,也依赖于微球和/或微珠方法达到靶向富集。长期以来一直有需求将靶标富集的方法简单化,尤其是将靶标富集变成多元化。
在后基因组时代,生命科学研究和临床应用正在朝着研究生物信息传递和生物标志物的方向发展。生物标志物可指导药物开发过程,并且它们在形成对于患者或个体化医疗的最佳治疗计划中也有至关重要的作用[“使用生物标志物指导药物开发,管理和临床实践:一个美国监管局的观点,”莎瑕埃墨等人,医用生物标志物杂志(2008)2(3),305–31]。用于临床研究或诊断和常规研究的验证过的生物标志物组通常含有少于10种分析物[“用多靶向检测粪便dna筛查结直肠癌”,新英格兰医学杂志2014,4,3;370(14):1287-97]。理想的生物标志物可以通过非侵入性方法测量,为此生物标志物最好存在于外周身体组织和/或体液,例如血液、尿液等中。此外,检测或测量生物标志物的方法需要是简单、快速、便宜,可重复和稳定[“越显重要性的生物标记物”,自然杂志生物技术28,431(2010)]。上述多元检测技术没有能满足这些标准。
美国专利3,932,141公开了一个用于测定抗原及其抗体的免疫测定的测试装置,其包括具有用于接收样品的多个孔的容器盘,用于接收和装球的通心棒,球表面覆有免疫物的球将被放置到所述容器盘的孔中,通心棒的上端有一个释放所述球的机关,通心棒的开口端有一个盖子。用此通心棒可在容器盘的每孔里放一个所述球。
世界卫生组织(who):“世界卫生组织体对一项体外诊断计划的资格预审的公共报告(whoprequalificationofinvitrodiagnosticsprogram)。产品:免疫梳状卡ii艾滋病1&2型(
一个改进的用于进行体外诊断测试的装置和方法。该方法采用一种固体装置,其表面覆有一种固定成分的物质,当插入一个容器中时,该固体装置将与流体样品接触。此改进在于以上固体装置可插入的容器,该容器的内表面上覆有与固体装置的表面相同的固定成分的物质。将流体样品先加入容器中,再将以上固体装置插入容器中,这样流体样品可与在容器内表面和固体装置表面覆有的一种固定成分的物质接触反应一段时间,流体样品中可与以上覆有的一种固定成分结合的物质的浓度可通过函数的变化来进行测试。
沃的利仪器(woodleyequipment)公司:1989年10月1日(1989-10-01)在“免疫梳状卡抗体检查”中发表“免疫梳状卡抗体测试”(“immunocombvaccichect”in“immunocombvaccicheck”)。沃的利仪器公司,博尔顿,英国(woodleyequipmentcompany,boltonuk),xp055233158,在第1-3页公开了免疫梳状卡
总之,以上所提发明还是不能解决以下市场所需。市场上急需一种好用,灵活,重复性强,便宜,低密度的,日常可用的多元检测技术,该技术可充分利用现代基因组信息来改善我们的生活。因此,本领域需要开发更简化的多元检测技术和多元靶向富集或纯化的方法,以使其成为生命科学研究和临床诊断中的常用实验室工具。本发明将能满足这些长期的,未解决的需求。
技术实现要素:
要解决的技术问题是如何提供一种用于多元分析物检测、富集或纯化的杆、配套件及其使用方法。
本发明申请涉及一个被简称为“移动阵列”(ma)系统,该系统包括用于多元分析物检测,富集或纯化的杆,配套件及其使用方法。所述的杆包括有独特的可被识别/可追踪的大颗粒/球,物质或化合物相互间作用/反应发生在大颗粒/球的表面上。此特点使多元化实验可在试管或微孔中进行。本发明保留了用路明克斯公司(luminex)液态芯片做多元化检测的优点,但本发明不依赖于昂贵和难于操作的设备。通过“移动阵列”系统,任何人可以使用酶标仪/微孔板读数仪做多元酶联免疫吸附测定(elisa)。“移动阵列”系统还可以将目前的免疫沉淀和靶向富集或纯化方法变成多元。“移动阵列”系统还可以结合到自动化过程中。这为将多元化实验概念推广到日常实验室,诊所检测,临床诊断,食品安全检查等中铺平了道路。
本发明的一方面包括用于多元分析物检测,富集或纯化的大颗粒/球,所述大颗粒/球表面可吸附一种物质,该球再与相对应的待分析物相互作用或反应便可提供检测,富集或纯化分析物的结果,本发明大颗粒/球与类似的大球本质不同点在于它可被识别/追踪性。
本发明的另一方面还包括用于多元分析物检测,富集或纯化的杆,所述杆包括附在上面的至少一个大颗粒/球,所述大颗粒/球表面可吸附一种物质,该球再与相对应的待分析物相互作用或反应便可提供检测,富集或纯化分析物的结果。
本发明另外一方面还包括子组合件和组合件,其包括上述的杆和其它配套组件,该组合可提高一元或多元分析物检测,富集或纯化的操作的便利和效率。
本发明再另外一方面还包括涉及用于分析,纯化或富集至少一种分析物的方法,所述方法包括将以上所述附在杆上或没附在杆上的大颗粒/球的表面吸附一种物质,将所述至少一个附有物质的大颗粒/球与待分析物相互作用或反应,该分析物可能与球面上的物质作用或反应,从而提供至少一种或一个待分析物的检测,富集或纯化的结果。检测的结果可以是定性或定量的。所述方法优先包括检测至少两种待分析物的多元分析物检测,富集或纯化的操作。此外,任何以上用于检测,纯化或富集的方法可与任何自动化过程结合。
附图说明
结合附图及简要说明阅读时,将会让你更好地理解前述发明摘要以及本发明的以下详细描述内容。为了解释本发明的目的,附图示出了目前优选的实施例。然而,应当明白,本发明并不只局限于所示的图案设计及尺寸。
在附图中:
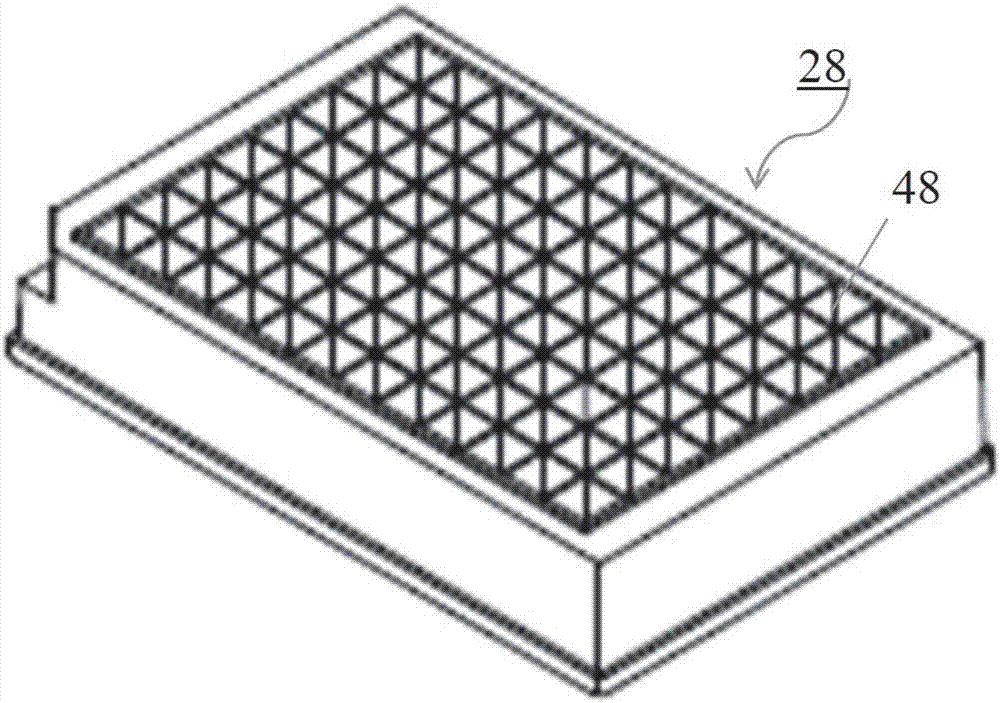
图1a是具有方形孔的标准96孔板的俯视图。
图1b是图1a的标准96孔板的等轴侧视图。
图2是在96孔板一个纵列里附带有8个大颗粒/球的杆的侧视图。
图3a是图2带有大颗粒/球的杆的俯视图。
图3b是图2带有大颗粒/球的杆的前端正视图。
图3c是带有大颗粒/球的杆的局部侧视图。
图3d是另一种设计的带有大颗粒/球的杆的前端正视图。
图4a是带有大颗粒/球的杆的若干不同设计模型或变型的侧视图。
图4b是另一种设计模型的带有大颗粒/球的杆的等轴侧视图。
图5a是一个实例96孔板的俯视图。
图5b是画有96孔板的三个孔的前正视图,并且其中一孔显示有四个带有大颗粒/球的杆的端视图。
图5c是96孔板的局部放大剖视图。
图5d是96孔板的局部放大俯视图。
图6a是架子的俯视图。
图6b是图6a的架子局部放大的正视图。
图6c是图6a的架子的等轴侧视图。
图7a是分隔件的仰视图。
图7b是图7a分隔件的正视图。
图7c是图7a分隔件的等轴侧视图。
图8是盖板的俯视图。
图9是图8盖板上加有对角支承杆的俯视图。
图10是移动阵列的分隔件放入架子内的仰视图。
图11a是移动阵列组合件的每个部件如何按步骤顺序组装成移动阵列组合件的一个实例图。
图11b是图11a所示的部件组装成的移动阵列组合件的一个实例的横截面图。
图11c是图11a所示的部件组装成的移动阵列组合件的另一种实例的横截面图。
图11d是图11a所示的大部分部件组装成的移动阵列组合件的另一实例的等轴侧视图。
图11e是图11d所示组装完毕的移动阵列组合件的等轴侧视图。
图12是一个单孔试剂槽的俯视图。
图13是几种常见类型的elisa测定的示意图。
图14a是一例在96孔板全板里使用移动阵列系统做4元elisa的温育步骤期间每个样品在96孔板中的位置图表。
图14b是图14a所示实验在检测/显色步骤期间每个样品在96孔板中的位置图表。
图15a是另一例只在96孔板一个纵列里使用移动阵列系统做4元elisa的温育步骤期间每个样品在96孔板中的位置图表。
图15b是图15a所示实验在检测/显色步骤期间每个样品在96孔板中的位置图表。
图16a-16d示意性地展示各种类型的移动阵列系统里带有大颗粒/球的杆用于大体积样品的多元分析物检测,富集或纯化的操作实例。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
除非另有定义,本文所使用的技术和科学术语与本发明所属领域的和普通技术人员通常理解的术语具有相同的含义。否则,本文使用的某些特殊术语具有说明书中所定义的含义。
如本文和所附权利要求书中所使用的,单数形式“一”,“一个”和“该”包括复数指代,除非上下文另有明确规定。
如本文所使用的,术语“分析物”是指被测量的生物或化学物质,或者它们是在样品中的待确定物质。分析物可以是蛋白质、核酸、细菌,病毒,细胞或其它将被测定的分子或颗粒。
如本文所用,术语“抗体”是指一种蛋白质其可识别将被测定的分析物,与其结合,或以其它方式形成相互作用。抗体可以是初级,次级或捕获抗体,并且可以是酶标抗体。
如本文所使用的,术语“试剂盒”是指进行从样品开始至获取最终原始数据所需的一组试剂和装置,并且还可以包括有关使用移动阵列系统的说明书。
本发明的一个目的是简化多元检测方法,但保持其多元的优点。本发明的另一个目的是让任何生命科学研究,食品安全检测和/或临床实验室在最少的培训或花费的情况下就可应用多元检测方法。本发明的再另一目的是使多元检测方法操作灵活,测试几个样品和许多样品都很方便高效。再再另一个目的是利用本发明将靶富集和/或纯化过程简单化和多元化。
本发明的优势在以下描述和权利要求中将变得显而易见。
本发明为实验室提供了可进行许多多元检测的杆,配套件及其使用方法。本文中的杆和配套件,它们的单数或复数的组件和系统,本发明简称为“移动阵列”“ma”系统将为简化实验室检测步骤发挥巨大作用,尤其和特别是可大大减少实验室多元检测,富集或纯化的时间,成本和对昂贵的专用实验室设备的需要。
微量滴定板(本文中也称为“板”,96孔板,或微孔板)和微孔板读数仪已经成为日常实验室中必不可少的工具。标准板可以具有以2:3矩形阵列格式排列的6,12,24,48,96,384或更多个孔。图1a是具有方形孔的标准96孔板的俯视图。图1a中板28所示是一个实例96孔板具有孔48/列34/行36的阵列布置。一个实例96孔标准板通常具有85.5mm的宽度和127.8mm的长度,其中宽度如图1a中所示标记30,长度标记32。
移动阵列系统里的杆和其它部件可被设计而适用于当今标准板,各种试管或任何其它形式的系统。物质或化合物之间在该系统里的可被识别/追踪的大颗粒/球的表面上发生相互作用/反应,这一特性使其能够将常规的平面固定阵列转化成可移动和可混合的液态阵列,类似luminex公司的液态芯片,但不需耗费其昂贵的成本。此外,移动阵列系统还能够将一个或多个样品的靶向富集或纯化步骤简单化和多元化,而luminex平台是做不到的。该说明书使用标准96孔板为例在下文里描述本发明中的移动阵列系统。为了将此发明合适配套地用于96孔板或其它板或试管或其它形式的系统,以下每个组件都可被修改和改变。
本发明的一个方面是图2,3a,3b,3c,3d,4a和4b所示的ma杆37,这里也称为“杆”,其中杆37包括杆构件40和至少一个大颗粒/球42,其可是球形或另一形状的颗粒,这里也可通称为“粒”,最好在半径,长度,宽度,高度,或直径上具有最小尺寸,例如等于或大于一毫米。然而,图3d所示的粒也就是球,其可具有任何其它合适的最小尺寸,例如半径等于或大于0.25mm,0.5mm,1mm,1.5mm,2mm等。图2是96孔板28纵列的孔48里容纳有附带8个大颗粒/球的杆37的横截面侧视图。一根杆37可带有一个大颗粒/球42或多个大颗粒/球42。例如,一根杆可带有1,2,3,4,5,6,7或8个大颗粒/球。另外,一根杆上带有的一个或多个大颗粒/球可被同时插入一个孔48里。在最佳实例中,每个在一根杆37上的大颗粒/球插入相对应的板28的每个孔48里。图2所示是含有八个大颗粒/球的一根杆37和图1a所示的板28的纵列34,其中每个大颗粒/球插入标准96孔板一个纵列8个孔里的每一个孔。大颗粒/球42可以直接附接到杆构件40(本文中也称为“杆”),附接到半刚性细丝44或刚性杆构件46从而连结到杆37。在一个实例中,大颗粒/球42连接到半刚性细丝44,其进一步附接到刚性杆构件46,刚性杆构件46再附接到杆37的杆构件40上。半刚性细丝44是为确保大颗粒/球42在吸附或相互作用过程中可与待测分析物在液相自由地和完全地混合。在最佳实例中,大颗粒/球42直接附接到刚性杆构件46,如图3d的前端视图所示和图4b的等轴视图所示。ma杆37具备将信号和特定分析物相配对的功能。这种可移动,可混合和可将信号和特定分析物配对的简单液体阵列系统可以很容易地应用于单试管,其它板或其它不同形式的反应器。每个大颗粒/球42实际上代表常规固定平面的阵列上的一个点。ma(移动阵列)系统使得相对应常规固定平面阵列上的一个点的每个大颗粒/球能够移动和混合。在ma系统的其它实例中,在必要时大颗粒/球42可以不附接到一个或多根杆37上,而是通过其它方式识别区分大颗粒/球42,例如颜色,图案,纹理,形状,或其任何组合等。大颗粒/球42,单独使用或附接到杆构件46或附接到杆37,或杆37的一个或多个部件上时,大颗粒/球42可以通过在杆37上的位置,颜色,图案,纹理,形状等或其任何组合来被识别区分,或者用户可以通过标记或标签杆37来识别区分大颗粒/球42。
大颗粒/球的材料可以是聚苯乙烯或其他材料,包括对分析物,例如蛋白质,核酸和其它生物品有优异结合能力和/或特异性的新合成材料。一些实例材料可以像邦斯实验室生产的材料,或快捷公司的各种树脂或珀金埃尔默仪器有限公司的阿法酶联免疫吸附测定
图3a是杆37的俯视图,杆37包括一根杆构件40和相邻其每个端部的一个标记区域38,但是为了便于说明,未示出大颗粒/球。标记区域38可以是正方形,圆形,圆圈,椭圆形,三角形或任何其它形状,但是最佳是矩形的并且可用来标记杆37。标记区域可以是杆37的延伸,例如杆构件40的延伸。图3b是杆37的前端正视图,包括至少一个大颗粒/球42,至少一个半刚性细丝44,和至少一个刚性杆构件46附接到杆37的杆构件40上。图3c是杆37的局部侧视图,包括在杆构件40的端部处的一个标记区域38,以及附接到一个半刚性细丝44的一个大颗粒/球42,其进一步通过刚性杆构件46连接到杆构件40。图3d是杆37的前端正视图,包括至少一个大颗粒/球42附接到至少一个刚性杆构件46,其再附接到杆37的杆构件40上。组合在杆37上的杆构件40,刚性杆构件46和半刚性细丝44是用于维持大颗粒/球42在整个制造和测试过程中的位点。制造杆构件40,刚性杆构件46和半刚性细丝44的最佳材料是非活性的,坚固的并且几乎没有吸附能力,例如聚丙烯或其它可用材料,但是也可以使用聚苯乙烯。最佳条件,杆构件,刚性杆构件是一体地形成在一起的,例如通过注塑成型工艺。
在一个实例中,杆构件的长度为85.5mm,或基本上等于板的宽度30。在最佳实例中,杆构件的长度大于板的宽度30。这样通过杆构件40的延伸端可抓住杆37。由于使用较长的杆构件,每根杆37可稍微移动使大颗粒/球可与液体更好地混合,这样也就不需要制造如图4a所示的不同模型号的杆37。杆构件40的高度最好为2.0mm,厚度为0.4mm。刚性杆构件46最好基本上与杆构件40的厚度相同0.4mm,宽度1.5mm和12.5mm的高度。半刚性长丝最好为6.0mm长,并且大颗粒/球的半径为1.0mm。所有尺寸要根据制造可行性,相对应的板或试管进行调整和改变,为此可确保大颗粒/球非常接近孔底部。本文所述的各组件尺寸形状可被调整和改变从而可与西格玛奥德里奇,赛默飞世尔科技公司,威达优尔国际公司等等公司所卖的各种形式的板,试管等配套使用。
前述杆37中的各部件/组件是为了形成一种可移动的,可混合的和可跟踪/识别的简单阵列系统,从而其可以多元的方式在液体中测试样品,富集或纯化待验物。以上可移动的,可混合的和可跟踪/识别的简单阵列系统的跟踪/识别功能也可通过视觉上的区别来达到,例如通过用颜色,图案,甚至小计算机芯片,其它电子设备来跟踪/识别杆37,杆构件40或大颗粒/球42。此外,杆37中的各部件/组件可以是松散部件,可以用粘合剂附接,或者整体注塑成。作为松散部件的杆或其它部件,其中一个示例是一个或多个球与装在任何容器里的液体反应作用,例如图16d中示意性示出的大颗粒/球与注射器主体配套使用。
在一个实例中,有三种模型的带大颗粒/球的杆37,大颗粒/球42直接或通过其它杆构件附接到杆构件40,例如上所述的半刚性细丝44和刚性杆构件46。大颗粒/球42在一根杆37的位置相对大颗粒/球42在另一根杆上的位置上有平行偏移,为此几根杆37可以同时插入板28的纵列34或行36中的孔。例如,图4a是该实例,模型i,模型ii和模型iii的杆37的三种变型的侧视图。在图4a中,当模型ii杆与模型i杆平行对齐时,模型ii杆上的大颗粒/球42都向右移动2.0mm。当与模型ii杆平行对齐时,模型iii杆也是如此。大颗粒/球位置变化的目的是使得从多根杆上来的大颗粒/球可很容易地装入每个孔。图4a中的大颗粒/球分布的示例性尺寸是可以修改的从而使多根杆可被装配到任何想用的板里。杆37可进一步修改以便与各式板的纵列和行里的孔相配,或与任形式的单个试管或注射器体相配。三种杆37的模型通常足以达到让多根杆上的大颗粒/球很容易地装入一个孔的目的,尽管还有其它变化可设计。在另一个实例中,杆37可以是相同模型,但杆37上的杆构件40比板28的宽度30或长度32更长,并且可以通过手动偏移大颗粒/球的位置或根本不偏移。
本发明的第二方面是与杆37配套使用的ma微孔板,在本文中也称为“板”,其中ma板包含至少一个孔。ma微孔板29基本上是如前所述的标准板28,具有一处或多处修改以便更好地与一个或多个杆37配套使用。图5a是板29的俯视图,其包括以纵列34和行36的阵列布置的多个孔48。在一个实例中,孔开口基本上是正方形。在另一个实例中,孔48具有凹形或圆形底部50。图5b-5d是如下所述的板29的局部放大图。
图5b是板29中的孔48的侧视图,其中中间孔包含四根不同模型杆37的端视图,例如模型i,ii,iii和i的平行排列的三个模型的杆37,通过如此排列,对齐的杆37上的大颗粒/球42可插入孔48中并且可以自由地与样品混合。图5c是板29的一部分的放大横截面。在另一个实例中,一个或多个孔壁52上有个加样口53,例如,微量移液管可通过此口将液体样品或试剂加入孔48中。例如,图5c在孔壁52的顶部上的倾斜平面形成一种微小加样口53。
图5d是板29的局部放大俯视图,示例了孔壁52上的加样口53的可能位置。
在又一个实例中,板29中的一些或所有孔底50可以有一个小过滤孔54,最好在孔底50的中心。图5a示出了板29的右下部分中的小过滤孔54的概念。小过滤孔可用于从孔48移除液体样品或试剂。过滤孔可以是直径为0.5mm,并且还可以有防止泄漏但允许抽真空的膜覆盖,例如紧密编织的尼龙膜。
在一最佳实例中,板29的长度为127.7mm,宽度为85.5mm,深度为20.0mm。对孔壁52具有1.0mm厚度的96孔板,每个孔可具有8.0mm×8.0mm的孔开口和19.0mm的孔深度。
本发明的第三方面是与杆37配套使用的ma试剂槽,在本文中也称为“试剂槽”。试剂槽是具有仅一个大孔的标准板28的改变。试剂槽可以包括板29的任何一个或多个前述特征。试剂槽最好用于以下步骤,大颗粒/球吸附分析物,洗涤大颗粒/球,或大颗粒/球与其它溶液孵育。图12是试剂槽82的俯视平面图。试剂槽可以具有任何期望的尺寸,最好它与架子56和分隔装置68的尺寸相配套。非限制性的示例性尺寸对于外口部宽度30可以是85.5mm,内口部宽度为81.5mm,外口部长度32为127.8mm,内口部长度为123.8mm。
本发明的第四方面是与杆37配套使用的ma架子,在本文中也被称为“架子”。图6a是架子56的俯视平面图。架子56,可以包括但不非要,在架子56的外周上的一个或多个把手60。把手有助于拿住架子,尤其是当有多个ma杆37在架子上时,它可以是正方形,圆形,椭圆形,三角形,最好是矩形。把手还可以提供如下所述用于将子组件或部件组件绑扎在一起的支撑的作用。架子56还可以包括一个或多个位于架子56的一个但最好四个角的孔66。或者如图6c所示,代替孔66,架子56可以包括一个或多个位于架子56的一个但最好四个角的竖立的棒67。棒67与架子56是整体地注塑出来的,以用于如下所述将移动阵列系统的部件绑扎在一起。架子56的外部尺寸,宽度30和长度32最好等于要与其配套使用的板29或试剂槽82的尺寸。内部开口57最好是矩形的,并且足够大以确保当架子56被放置在板上时,板29的孔48没有被架子56完全覆盖。
图6b是架子56的放大的局部侧视图。架子56还可包括狭槽58,其中每个狭槽可容纳杆37的一个或多个杆构件40。狭槽58最好是从架56的顶表面98向下延伸到架56的底表面100。或者如图6c所示,框架56可包括脊59,其中每个脊可分隔架子56上的空间,用于放置一个或多个杆37,每个空间最好与对应的一列或一行相配套。脊最好是从架子的顶表面98向上延伸,但是要比棒67短。脊59最好与架子56一整体地注塑出来的。在最佳实例中,架子的厚度1.5mm,架子的外部尺寸为85.5mm和127.7mm,或者基本上等于板29的最佳外部尺寸,并且架子内部开口的宽度77.5mm和长度119.8mm。
本发明的第五方面是一个与杆37配套使用的分隔件,其中,分隔件包括至少一个分隔构件。在最佳实例中,分隔构件在分隔件的底表面上彼此平行地排列,分隔构件间的距离与对应的装置,例如板29的每一纵列或每一行孔的距离配套一致,以便将在相邻的列或行里的多根杆37隔开。图7a和7c分别是底部仰视图和底部等轴侧视图,分隔件68包括沿宽72平行延伸的分隔构件70。分隔构件70可以和分隔件68一整体地注塑出来,分隔构件70从分隔件68的底表面延伸出。分隔件68最好为矩形。在最佳实例中,分隔件68的尺寸72和74略小于将与其配套使用的架子56的内开口57的相应尺寸。在最佳实例中,分隔件具有宽度为73.5mm,长度为109mm。
图7b是分隔件68的正视图。分隔构件70彼此从分隔件68的底表面110平行地延伸出来。在最佳实例中,分隔构件70的高度112至少足以容纳杆37,杆37与分隔构件70平行,并且接近分隔件68底表面110。
在最佳实例中,分隔构件70之间的空间102足以容纳板29的一纵列或一行孔48,为此当架子56中的分隔件68放在板29上时,球42可延伸到板29的孔48中与溶液混合。
本发明的第六方面是一个配套的盖板。图8是盖板76的俯视图。盖板76最好是矩形的,并且盖板76宽30和长32的尺寸最好等于板29,或试剂槽82,或架子56的外部的尺寸,从而它们可与盖板76配套使用。盖板76还可以包括孔78,其可以是或不是带螺纹的,并且位于盖板76的任何或最好所有的角部。孔78的尺寸上最好等于架56中的孔66,并且当盖板76放在架的顶部表面98时,孔78可与架中的螺钉孔66对齐。或者,孔78在尺寸上略大于架56上的棒67,并且当盖板76放在架的顶部表面98并对准时,架56上的棒67延伸穿过孔78。
此外,盖板可包括一个或多个支承杆或其它类似结构,例如具有内部延伸到角部和整体注塑形成的外围框架,其底表面在一个平面中,当盖板76与ma组件的一个或多个部件捆绑一起时(下面详细描述),上述外围框架可将盖板76的力均匀到组件的各部分。根据盖板的材料,若有足够刚性的话,可不需要支承杆或其它类似结构。图9是盖板76的俯视图,其中支承杆80对角地设置在盖板76上并从盖板76的对角相对的角延伸。支承杆或类似结构可以由金属制成,例如铝或其他刚性材料,例如工程聚合塑料材料,其具有足够的刚性,在多个上述部件捆绑一起时,螺钉或棒穿过盖板76的孔时,上述支承杆可平衡盖板76的力的分布。螺母64可以被拧到螺钉62上,将支承杆80固定盖板76的上表面。或者,盖板76的孔与架子上的棒67对准穿过,棒的端部可以是无螺纹的,或者螺纹以容纳螺母,如果需要的话。
本发明的第七方面是移动阵列组合体,在本文中也被称为“组合体”或“子组合体”,其中组件包括前述部件的任何实例中的两个或更多个,最好是全部。例如,组件可以包括至少一根杆37,板28或29,试剂槽82,架子56,分隔件68,盖板76和支承杆80。这些部件可以是以按预定顺序放置在彼此之上。该组件可以通过单独的螺钉,螺母或整体注塑的棒而捆绑在一起。除了螺钉或棒,还可以使用其它组件或者与螺钉或棒结合使用将两个或更多个部件捆绑在一起,例如弹簧夹夹在角部或组件的外围,或者用橡皮带扣在两个或多个螺钉或棒上。在简化的实例中,部件通过位于架上的棒67穿过孔78,再用橡皮带将各组件拴在一起。
在一个实例中,组件的一个或多个部件按11a和11d所示的顺序叠放在一起,并且如下所述:
(a)如图11a所示,将板28或最好ma板29放置在桌或其它支撑台面上,其中孔开口向上。
(b)架56放在板28上,架56底表面100与板28的顶部相邻。至少一个且最好四个螺钉62通过架56的底表面100并且延伸出架56的顶表面98而穿过架56的至少一个且最好四个孔66。螺钉62的头部63最好是埋在孔66里同时在架56的底部。或者,螺钉62可以被棒67替代,棒67是整体注塑而成的架子的一部分并具有与螺钉62相同的功能。
(c)至少一根,但最好多根杆37被平行地放置在架56的顶表面98上。一根个或多根杆37被容纳在狭槽58中或在脊59之间,杆37的每个大颗粒/球42穿过架开口57进入板28或29的孔48里。在一个实例中,在每个孔48里中具有一至十个大颗粒/球42其中每个大颗粒/球来自不同的杆37。在最佳实例中,在每个孔中有不超过8个大颗粒/球。在特佳实例中,每个孔中不超过四个大颗粒/球。
(d)如图10中最佳所示,分隔件68被放置在架口57内。根据本配置的最佳实例,其中分隔构件70与至少一根杆37平行,并且分隔构件70之间的空间102可容纳一个列34或行36孔中的所有杆37。分隔构件70的底表面108挨着板29的顶部并对齐,使得每个分隔构件70可分隔每个列34或行36的孔。
(e)盖板76放置在分隔件68的顶表面106上,其中盖板76的孔78与架子56的孔66对准,并且进一步将至少一个但最好四个螺钉62放置在至少一个但最好四个架子56螺钉孔66内,并且向上穿过盖板76的至少一个但最好四个螺钉孔78。或者,盖板孔78与架上的棒67对准从而棒穿过盖板的孔。
(f)支承杆80可以放置在盖板76上,并且它们的孔分别与盖板76孔78和架子56孔66对齐,或以类似的方式它们的孔分别与盖板76孔78和架子56上的棒67对齐。在一个实例中,支承杆80或类似结构被对角地放置在盖板76上,其包容有一些或全部先前列出的部件,在用螺母,夹子,橡皮带等将各部件紧固在一起时,支承杆可均衡盖板上力的分布。在最佳实例中,支承杆80将架子56,一根或多根杆37,分隔件68和盖板76紧固在一起。
(g)在一个实例中,至少一个但最好全部四个螺钉62用至少一个但最好全部四个螺母64分别紧固,将组件的以下部件紧固在一起,以形成子组件:架子56,杆37,分隔件68,盖板76以及支承杆80。在一个实例中,子组件可以通过带,例如橡皮带,代替或除了用坚硬的螺母。在最佳实例中,子组件通过架上的棒67和橡皮带紧固在一起。
图11b是如上文段落(a)-(g)中所述构造的部件的组合横截面图,并且其中放置有四根杆37,其中大颗粒/球42伸出分隔构件70的底表面108,使得它们可以进入孔48中的任何溶液内。分隔构件70的底表面108被示出为贴近板29的顶表面。图11c是组件的另一种横截面图,其中螺母64进一步拧紧在螺钉62上,使得架子56的顶表面98接近盖板76的底表面77。然而,如图11c所示,通过拧紧螺钉上的螺母,在架子56上的狭槽58或脊59内的杆37被推到贴近分隔件68的底表面110,并且子组件将杆37和大颗粒/球42还维持在分隔构件70之间。为此,子组件可以作为一个单元从板29的上部拿出,并且大颗粒/球42可被移到试剂槽82的孔中或板28或29的孔48中与其中的溶液进一步作用反应。图11d是各组件的另一种组合的等轴侧视图,其中架子56包括在四个角上的棒67。图11e是各组件的另一种组合的等轴侧视图,其中架子上的棒67已向上穿过盖板孔78。
本发明的第八方面是在颗粒/球的表面上进行多元酶联免疫吸附测定(elisa),所述颗粒/球最佳是在杆37上。简而言之,elisa是实验室溶液试验,其使用一种或多种抗体识别物质。elisa的三个实例如图13所示。在测定中,待测分析物86通过直接吸附固定到表面83,表面83可是板的孔壁或颗粒/球42的表面。待测分析物86也可被事先固定到表面83上的捕获抗体84有识别性地固定住。然后使用酶标一级抗体88(直接检测)或使用未标记的一级抗体88和其配套的二级酶标抗体90(间接检测)进行分析物的检测。在加入酶底物94之后,酶92催化化学反应并产生可见信号,其可以是例如可见的颜色变化(用于定性elisa),或通过分光光度计或elisa微孔板读数仪(酶标仪)在特定波长处读取的可见变化信号(定量elisa)。通过可见信号,可以确定样品中待测分析物86的浓度。如果没有产生可见信号,样品则不含有待测分析物。
利用本发明进行多元elisa的方法可以是捕获多元elisa,或称为“夹心”elisa。在捕获elisa中,捕获抗体84事先结合到表面,例如颗粒/球42的表面。捕获抗体84再与待测试样品反应后识别并结合待测分析物86。待测分析物可以如在直接elisa中进一步结合到酶标一级抗体88,或者如在间接elisa中结合到未标记的一级抗体88,再结合到和其配套的二级酶标抗体90。
利用本发明也可进行多元竞争性elisa。当分析物小且仅具有一个表位或抗体结合位点时,这是常用的方法。该方法的一种方式包括标记纯化的分析物而不是抗体。来自样品的未标记的分析物和标记的分析物竞争地与捕获抗体结合。与仅具有标记的分析物的测定孔相比,若来自纯化有标记的分析物的信号的降低则指示该孔中的样品有待测分析物的存在。
利用本发明进行多元elisa的方法包括把多个颗粒/球42放入一个待测试的样品里,从不同杆37上的来的每个颗粒/球吸附有不同的捕获抗体。吸附有不同捕获抗体的每个颗粒/球将识别结合样品里相对应的待测分析物。通过板的阵列系统和杆37的标记,每个颗粒/球42的信号可与相关的特定的待测分析物配对。此外,每个颗粒/球42或杆37也可以通过例如颜色或图案被识别区分。
图14a和14b显示了利用本发明进行一个定量多元elisa测试的典型步骤。标准浓度品和待测样品通常是一式三份进行测试。图14a显示孵育步骤的图谱。图14b示出了检测/显色步骤的图谱。对于4元试验(4种不同分析物的检测),在显色步骤时,将吸附有相同捕获抗体杆37按图谱分布在一个标准96孔板中,4元试验需要4个单独的96孔板,使用微孔板读数仪进行最终信号测量。
图15a和15b显示了利用本发明进行一个临床(病人)样品的定性测试的多元elisa步骤。可以是一式两份测试阳性对照(con+)和阴性对照(con-),(病人)样品可一式四份测试。图15a显示孵育步骤的图谱。图15b示了检测/显色步骤的图谱。对于4元测定(检测4种不同的分析物),按图谱,将4根在孵育步骤中来自标准96孔板一纵列的4根杆37分放入一个标准96孔板的4纵列中,以使用微孔板读数仪进行最终信号测量。
如何利用本发明的杆,配套件及其使用方法做多元实验请参考以下几个实例描述。然而,应当理解,本发明不是只局限于以下所示的具体参数和实例。
实例1-制备大量已结合有分析物的颗粒/球。当有需求大量在杆37上的颗粒/球42已结合有特定抗体或分析物时,它们可被用以下过程产生。移动阵列系统装置组合可用如先前所述和图11a-11e进行组装。螺钉62放置在架子的螺钉孔66中,螺钉的末端面向上。可用如图4a所示的不同模型的多根杆37,最好用杆构件40比孔板29的宽度长的杆37以便抓拿。将每根带有8个颗粒/球42的杆37整齐地放在孔板29上的架子56上。孔板29具有十二个纵使列34和八个行36,每列有8个孔,这样杆37上的8个颗粒/球42按列34可每球对应进入一孔,每列可如此放入多根杆37。第二至第十二列34以相同的方式填充。可移动的分隔件68放置在配套的架子56的内部开口57中,其中分隔构件70平行于杆37。盖板76被放上后,通过在盖板76上的支撑杆80将各组件固定。螺母64仅被拧紧到颗粒/球42还能在板29的孔48中为止。从板孔里将组装的杆拿出,通过把手60将架子56往上提直到杆37碰到分隔件68的底表面110。螺母64进一步紧固使杆37紧靠在分隔件68的底表面110。分隔件68的分隔构件70将每列的杆隔离。这可防止组合件散开并使所有的杆保持顺序,使得从架子56到支承杆80的子组件可作为一个单元移动,而不影响杆37或杆上的颗粒/球42的位置和顺序。
接下来,可以将整个ma子组件放在图12所示试剂槽82单孔里。所述试剂槽装有针对特定抗体或分析物的最佳缓冲液和最佳浓度的溶液。所使用的溶液的量应当浸没所有的颗粒/球42。整个组件可以被包起来,并根据特定抗体或分析物放在4℃过夜(on)或在室温(rt)温育。基本上,如果杆37是用于多元elisa,针对特定分析物已建立的单元elisa实验条件可用于加工准备杆37。在子组件组合好后,在试剂槽中进行特定抗体或分析物的结合和洗涤过程。之后,加工好的杆37被密封起来,例如用铝真空包装中,每个包装中具有一根或多根杆37用于长期存储。可以用上述相同的方式制备大量带有其它指定抗体或分析物的杆37。这些密封的杆37可以组装到多元测定试剂盒中。
实例2-制备少量已结合有分析物的颗粒/球。当有需求少量在杆37上的颗粒/球42已结合有特定抗体或分析物时,它们可被用以下过程产生。杆37可以与上述实施例1中所述相同的方式组装。这次,组件不需要从板上移除。在放上分隔件之前,将针对特定抗体或分析物的最佳缓冲液和最佳浓度的溶液加入到板29中的一列或两列孔中。例如,列1至3中的杆37结合抗体或分析物1,列4至6用于结合抗体或分析物2,列7至9用于结合抗体或分析物3,列10至12用于结合抗体或分析物4。可以使用多通道移液管通过加样口53添加。使用的溶液的量应浸没所有的颗粒/球42。这样,可以使用一个板29制备几种少量不同的结合有特定抗体或分析物的杆37。在添加完各相对应的试剂后,可移动的分隔件被放置在板29上,其中分隔构件与杆平行。放上盖板,子组件用螺钉和螺母紧固。整个子组件可以被包起来,根据相应抗体或分析物的最佳条件温育。
基本上,如果杆37是用于多元elisa,针对特定分析物已建立的单元elisa实验条件可用于加工准备杆37。在特定抗体或分析物的结合和洗涤之后,加工好的杆37被密封起来,例如用铝真空包装中,每个包装中具有一根或多根杆37用于长期存储。这些密封的杆37可以组装到多元测定试剂盒中。
实例3-事先组装好的96孔格式的移动阵列多元elisa试剂盒。制造商可事先组装好96孔格式的可测量4种蛋白质分析物(4元)的移动阵列elisa试剂盒。蛋白1捕获抗体结合在模型i杆上,蛋白2捕获抗体在模型ii杆上,蛋白3捕获抗体在模型iii杆上,蛋白4捕获抗体在模型i杆上(图4a)。制造商可用一个每列可容纳4根杆的架子。如此,每列34中的杆i,ii,iii,i,其相对应于四种不同的特定分析物。第2至12列将以与第1列相同的方式填充。杆将被按顺序地排列在移动阵列组件中(图11)。整个组件可以真空包装和密封,例如在用于长期存储的铝包装中。储存条件应当非常类似于当前的常规单元elisa板。此密封组件与其它试剂可组合成一个完整的96孔格式的移动阵列多元elisa试剂盒。
实例4-定制96孔格式的移动阵列多元elisa试剂盒。客户可以从制造商的网站订购他们想要的特定分析物的96孔格式的移动阵列多元elisa试剂盒。制造商可以组装那些单独包装的在杆37上的颗粒/球42已结合有特定抗体或分析物的杆。如果客户要求杆37已组合在96孔格式的移动阵列里,制造商可以使用与上述实例1-3中相同的程序组装试剂盒。如果客户希望自己组装,制造商可以向客户提供包括在杆37上的颗粒/球42已结合有特定抗体或分析物的杆,配套的板和所需的其它部件和说明书。用于客户自己组装定制96孔格式的移动阵列多元elisa试剂盒。
实例5-一个完整的96孔格式的移动阵列多元elisa试剂盒。为了生产完整的96孔格式的移动阵列多元elisa试剂盒,制造商可以将在96孔板中在杆37上的颗粒/球42已结合有特定抗体或分析物的杆和任何其它组件,下游试剂组合在一起以用来检测每个样品的多种待测分析物。下游试剂可包括但不限于两个对照样品,标准浓度样品,洗涤缓冲液,稀释剂,对应于分析物的辣根过氧化物酶(hrp)标记的检测抗体,显色底物例如3,3β,5,5'-四甲基联苯胺(tmb)。其它hrp底物也可用于测定。试剂盒中还包括描述试剂盒组分,测定原理和测定程序的小册子。
实例6-用96孔格式的移动阵列四元elisa试剂盒做实验。为了使用96孔格式的移动阵列四元elisa试剂盒做多元elisa实验,可根据图14a-14b按排实验。在该实例中,标记为1-4的4种蛋白质分析物将一式三份进行测量。列1,2和3用于7点(s1-s7)标准浓度和空白对照(b)。列
在标准品和样品孵育后,从板中取出整个子组件(从架子到盖板和支承杆)。这是通过把手将架子一直提到杆已碰到分隔件的底表面来完成的。螺丝上的螺母将被重新调整,以便进一步紧固子组件,如图11c所示。现在,来自分隔件的分隔构件将每列的杆隔离。这可防止组合件散开并使所有的杆保持顺序。将子组件置于有洗涤缓冲液试剂槽里,使得颗粒/球完全浸没在其液体中。子组件在洗涤缓冲液中上下移动几次,并转移到含有新鲜洗涤缓冲液的另一个试剂槽里。将该步骤重复多次,然后转移到含有与其相应的检测/酶标抗体液的试剂槽里。将整个子组件包起来并在板振荡器上在室温温育1小时。
在与检测/酶标抗体液孵育后,将整个子组件从试剂槽里取出并浸没在新的含有新鲜洗涤缓冲液的试剂槽里。该步骤在洗涤缓冲液中重复3次,再在底物tmb的缓冲液中重复1次。当颗粒/球仍然浸没在缓冲液中时,通过去除螺母,支承杆,盖板和分隔件来拆卸整个子组件。现在,所有的杆可以被拿出来。由于它是4元测定,将4个常规96孔板例如克司达elisa板放在试验台上。每个孔将加入50μl底物tmb的缓冲液。
将每根杆从第一列至最后一列从试剂槽里按顺序拿出,并且放入标记相应分析物的板的相应列中(图14b)。板1用于蛋白质1,板2用于蛋白质2,板3用于蛋白质3,板4用于蛋白质4。每个孔中有一个颗粒/球。当所有的杆已经正确的分配到各板的纵列时,使用多通道移液管一次一个板将50μl的2x底物tmb添加到每个孔中。将板在室温下温育5至30分钟。显色反应在杆拿出时终止。tmb的蓝色在620nm-650nm的波长下测量。这里,测量4个板并收集数据。
实例7-用96孔格式的散装移动阵列四元elisa试剂盒做实验。在该示例性实验中,仅有一个样品,例如患者咽喉棉签样品。目的是测试喉咙中是否存在4种类型的细菌。为了运行该实验,不需要整个96孔板。测试可以在一个纵列中进行。样品用于孵育和检测步骤中的排列如图15a-15b所示。对应于检测特定细菌的四根杆,所带颗粒/球表面已结合有特定细菌的捕获抗体,放置到有或没有架的的板的第一纵列中。在适当的缓冲液里,在孔中加入阳性对照(con+),阴性对照(con-)和一式四份咽喉棉签样品。反应体积可以是200μl或足以浸没所有颗粒/球。不需要使用子组件或组件的其它部件,因为只有一列杆。4根杆和板可以包起来,例如用铝纸或塑料膜包起来,并在室温下在板振荡器上温育2小时。
孵育后,将4根杆在洗涤缓冲液中洗涤3次,并在检测/酶标抗体缓冲液中洗涤1次,洗涤可在试剂槽里或板的一纵列里。将4根杆放入含有检测/酶标抗体溶液的一纵列里。4根杆和板可以包起来,例如用铝纸或塑料膜包起来,并在室温下在板振荡器上温育1小时。
孵育后,将4根杆在洗涤缓冲液中洗涤3次,再在试剂槽里或板的一纵列里使用底物tmb的缓冲液洗涤1次。然后,将4根杆放入一个costar板中检测(图15b所示)。每个孔将含有50μl用于底物tmb的缓冲液。每个列将有一根杆,因此板的列1-4含有杆。纵列1是用于检测1型细菌的杆,以此类推。当所有杆被分配到正确的纵列时,使用多通道移液管一次一个纵列将50μl的2x底物tmb加入每个孔中。将板在室温下温育5至30分钟。显色反应在杆拿出时终止。tmb的蓝色在620nm-650nm的波长下测量。这里,测量一个板中的4个纵列并收集数据。试剂盒中剩余的杆可用于其它实验。
实例8-使用已结合有特定抗体或分析物的杆在板里进行多元靶向富集或纯化的实验。例如,检测6个食物样品中的4种细菌,在进行pcr反应或其它检测测定之前首先富集细菌(参见图16a和16b),每个样品在6孔板中的一个孔与4个颗粒/球孵育,每个颗粒/球来源已结合有特定抗体或分析物的带有3个颗粒/球的杆。在另一个实例中,有六个样品,每个体积约有5ml。实验员想从每个样品中纯化4种不同的蛋白质。用已结合有特定抗体或分析物的带有3个颗粒/球的杆和6孔板格式做此实验最合适不过。在按如上所述的富集步骤之后,需要额外的洗涤步骤以纯化蛋白质。待富集或纯化的靶标也可以是核酸或其它感兴趣的分析物。
实例9-使用已结合有特定抗体或分析物的杆在注射器体中进行多元靶向富集或纯化的实验。在另一个实例中,液体食物或水样品可以是大体积但含有非常低浓度的细菌。已结合有特定抗体或分析物的带有一个颗粒/球42的杆37或散颗粒/球42可以被放置在注射器主体中。食物或水样品可以通过重力滴注入通过注射器主体(参见图16c和16d)从而富集细菌用于进一步研究。或者,实验员想从500ml细胞培养上清液中纯化4种不同的蛋白质。于其将样品分成4×125ml以进行单元纯化程序,可以使用已结合有特定抗体或分析物的带有一个颗粒/球42的杆37或散颗粒/球42和注射器体来达到用一个样品同时富集4种蛋白质的目的。需要加额外的洗涤步骤来纯化4种蛋白质。待富集或纯化的靶标也可以是核酸或其他感兴趣的分析物。
移动阵列系统的其它应用-上述实例仅是用于进行多元elisa,多元靶向富集或纯化的移动阵列系统和方法的一些应用。基于参考图13所示的elisa,用移动阵列系统做多元elisa的方法可以根据不同目的进一步地变化。用于多元靶向富集或纯化的方法也可以根据不同目的进一步地变化。可用于移动阵列系统的分析物或靶标可以是能够在颗粒/球表面上形成相互作用的蛋白质,核酸,细菌,病毒,细胞或其它分子或颗粒。此外,可以使用移动阵列系统装置的变型,例如有色颗粒/球或由包括计算机芯片或其它电子装置制成的颗粒/球,将带颗粒/球的杆与试管,48孔板或其它形式的容器配套。移动阵列系统装置还可以在任何需要的时候集成到任何自动化过程中。
本领域的技术人员都很明白,在不脱离本发明的情况下,可以对上述实例进行改变。因此,应当理解,本发明不仅仅限于所公开的特定实例,而是旨在包括与本发明相类似的实施例。应当理解,本发明不限于用于解释本发明的实例。应当理解,本发明不局限于用作描述本发明的实例中而使用的带有8个颗粒/球的杆。还应当理解,目前本发明中所述的尺寸可被进一步完善。还应当理解,为适应于不同的用途等,装置及其部件可被修改。此外,应当理解,本文所使用的术语或表达仅是为了描述特定实例的目的,而不是旨在限制本发明的范围。还应当理解,附图与实际装置的尺度不一定是全同的,它们主要用于提供一些实际装置的视觉。除非另有定义,否则本文使用的所有技术和科学术语具有与当前科学界所用的有相同的含义。
- 还没有人留言评论。精彩留言会获得点赞!