一种表面多功能化涂层及其制备方法与应用与流程
本发明涉及一种表面多功能化涂层及其制备方法与应用,属于分析化学领域。
背景技术:
传感芯片表面通常需要进行功能化修饰以用于探针分子的固定。然而,传感芯片如spri的金膜等,其单位面积可固载的目标分子的位点是固定、有限的并与被固定分子的尺寸有关。以小分子甘露糖的固定为例,若将甘露糖分子约化为正方体,则其边长模拟值约为
技术实现要素:
本发明的目的是提供一种表面多功能化涂层及其制备方法与应用;本发明具有操作简单,控制容易、灵活,修饰成本低,所得功能化层具有效果显著、稳定性良好且对生物分子识别干扰小的特点。
本发明提供的表面多功能化涂层,它包括基底、多羟基化合物、桥联分子、探针分子和去活化分子连接而成;
所述基底上修饰所述多羟基化合物;
所述多羟基化合物和所述探针分子通过所述桥联分子连接;
与所述多羟基化合物和所述探针分子连接后的所述桥联分子剩余的反应位点与所述去活化分子连接。
本发明中,所述多羟基化合物具有不易被水解和被生物分子识别的特点;所述桥联分子具有不改变表面亲疏水性质且具有可自由旋转的刚性骨架结构的特点;所述去活化分子能与剩余的所述桥联分子反应位点反应且不引入干扰基团。
上述的表面多功能化涂层中,所述多羟基化合物包括聚甲基丙烯酸羟乙酯、聚甲基丙烯酸羟丙酯、甲基丙烯酸羟乙酯与甲基丙烯酸羟丙酯的混聚产物、甲基丙烯酸羟乙酯与甲基丙烯酸寡聚乙二醇的混聚产物、甲基丙烯酸羟丙酯与甲基丙烯酸寡聚乙二醇的混聚产物、甲基丙烯酸羟乙酯与硫代甜菜碱丙烯酸甲酯的混聚产物和甲基丙烯酸羟丙酯与硫代甜菜碱丙烯酸甲酯的混聚产物中的至少一种;
所述多羟基化合物的分子量可为1500~300,000,具体可为30,000、30,000~300,000、1500~30,000或3000~200,000;
所述探针分子包括含羟基的分子和/或含氨基的分子。
上述的表面多功能化涂层中,所述含羟基的分子包括单糖、寡糖和多糖中的至少一种,具体可为葡萄糖;
所述含氨基的分子包括氨基酸、多肽和蛋白质中的至少一种,具体可为鸡卵蛋白。
上述的表面多功能化涂层中,所述桥联分子包括三聚氰氯(英文名称cyanuricchloride,简称cc);当所述桥联分子为三聚氰氯时,所述三聚氰氯上未与含羟基或含氨基的所述探针分子反应的n-cl键,cl能被所述去活化分子亲核取代,且不会引入干扰基团;
所述去活化分子包括h2o、乙二醇、乙醇胺和三乙醇胺中的至少一种。
上述的表面多功能化涂层中,所述基底包括金、银、二氧化硅和玻璃中至少一种。
本发明中,所述基底的厚度为本领域人员公知的厚度即可。
上述的表面多功能化涂层中,所述多羟基化合物中所含羟基与所述桥联分子、所述探针分子、所述去活化分子的物质的量之比可为1:0.001~1:0.001~1:0.01~1,具体可为12.6:0.1:0.1:1,且所述探针分子的量不为零。
本发明还提供了上述的表面多功能化涂层的制备方法,包括如下步骤:
1)在所述基底上修饰所述多羟基化合物;
2)修饰于所述基底表面的所述多羟基化合物与所述桥联分子发生亲核取代反应;
3)将步骤2)中反应后的所述桥联分子与所述探针分子发生亲核取代反应;
4)上述步骤3)反应后加入所述去活化分子反应,即得到所述表面多功能化涂层。
上述的制备方法中,步骤1)具体包括对所述基底修饰引发剂,然后加入所述多羟基化合物的单体原位引发生成所述多羟基化合物步骤:
(a)所述引发剂通过取代反应原位共价修饰于所述基底表面,室温条件下反应时间:10~120min,反应溶剂为四氢呋喃、二甲基甲酰胺、吡啶和乙腈中的至少一种;所述引发剂包括2-溴异丁酰溴、α-溴代异丁腈、n,n,n-三乙基(2-(2-溴-2甲基丙酰氧基))己基溴化铵、n-氯代丁二酰胺、1-溴乙基苯和α-溴代异丁酸乙酯中的至少一种;
(b)原位引发多羟基化合物生成:表面固定的所述引发剂在催化剂存在下引发所述多羟基化合物的单体聚合;室温条件下反应时间:10~240min;溶剂:甲醇、乙醇、水、甲醇水溶液、乙醇水溶液,反应在惰性气体中进行,所述惰性气体包括氮气或氩气;所述催化剂包括cubr、cucl或cui;所述引发剂、所述催化剂与所述多羟基化合物的单体的物质的量之比为0.01~0.3:0.01~0.1:1,具体可为0.067:0.025:1。
上述的制备方法中,步骤1)中,修饰的温度为室温,时间为20~360min;
步骤2)中,所述亲核取代反应的温度可为0~5℃,具体可为4℃、0~4℃或4~5℃,时间可为6~8h,具体可为8h或7~8h;
步骤3)中,所述亲核取代反应的温度可为20~25℃,具体可为25℃,时间可为8~12h,具体可为8h或8~10h;
步骤4)中,所述反应的温度可为20~100℃,具体可为20~25℃、90~100℃,时间为0.5~3h,具体可为3h。
本发明中,上述室温指的是本领域人员公知的常识,为10~30℃,具体可为25℃。
上述的制备方法中,步骤1)中反应溶剂选自水、乙醇、甲醇、四氢呋喃和二甲基甲酰胺中的至少一种;
步骤2)中反应溶剂选自冰水、丙酮、氯仿、苯、乙醚、乙腈和四氯化碳中的至少一种;
步骤3)和4)中反应溶剂为水、磷酸缓冲溶液、tris-hcl缓冲溶液、四氢呋喃、二甲基甲酰胺、二甲基亚砜、甲苯、苯、氯仿、二氯甲烷和四氯化碳中的至少一种;本发明制备生物样品点阵芯片时,采用水、磷酸缓冲溶液、和tris-hcl缓冲溶液中的至少一种作用溶剂。
本发明中,步骤1)-4)中反应得后处理均为本领域人员公知的常见操作。
本发明所述表面多功能化涂层在如下材料中的应用:
1)表面等离子体共振和成像的传感芯片;
2)高通量点阵芯片;
3)荧光成像分析材料。
本发明中,所述表面等离子体共振和成像的传感芯片用于分子间相互作用的直接检测。
本发明所述表面多功能化涂层在应用时,按照本领域常规的用法即可。
本发明具有以下优点:
(1)本发明通用性好,可实现多类分子(含氨基和羟基的分子)同时固定,可用于包含有多类探针的高通量点阵芯片制作;(2)稳定性好,分子骨架较天然葡聚糖对酸碱环境、微生物分解作用具有更强的耐受性;(3)对生物识别干扰小,经桥联分子固载的探针分子能完好的保持识别活性,天然葡聚糖为骨架的功能化层会干扰与葡聚糖有相互作用的分子识别研究;(4)借助cc的桥接能力,能用于spr及spri所用传感芯片的表面修饰以获得高灵敏度检测;功能扩展用于表面等离子体共振(spr)和成像(spri)测定以外领域,如荧光成像分析。
附图说明
图1为本发明实施1中在金膜表面制备功能化层的方法示意图;其中,
1表示金膜表面修饰多羟基化合物;
2表示表面修饰三聚氰氯;
3表示表面修饰糖分子;
4表示三聚氰氯活性位点去活化。
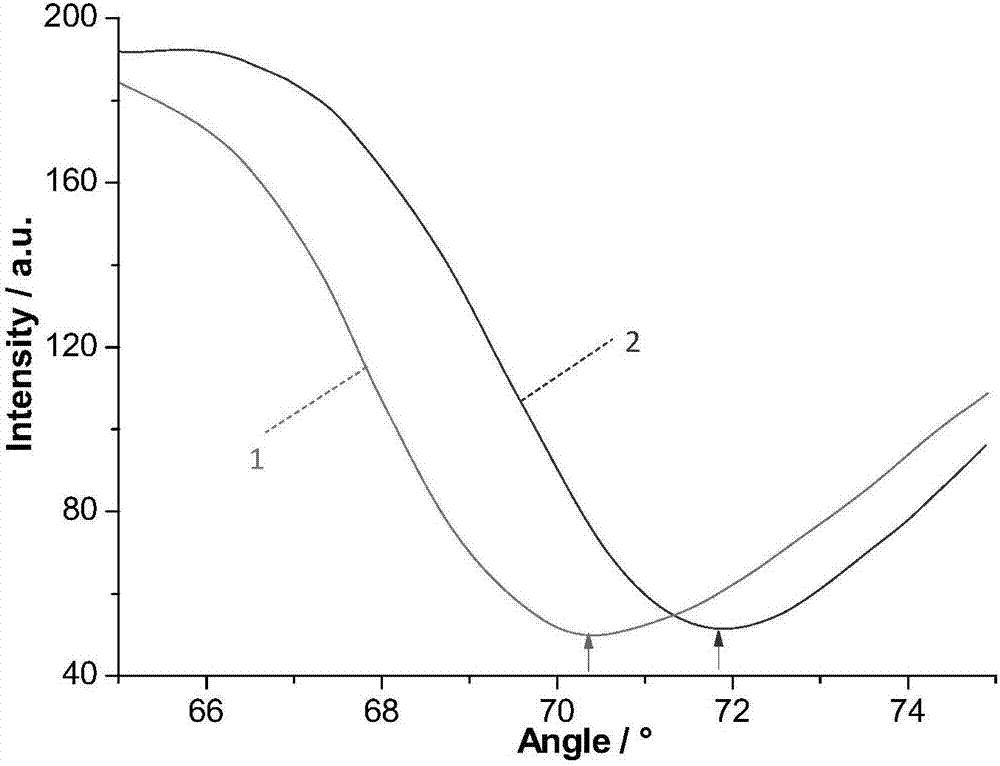
图2是本发明实施1中多羟基修饰过程spr共振角位移;其中,
1表示裸金膜共振角;
2表示经多羟基修饰的金膜共振角。
图3是本发明实施例1中金膜经多羟基及三聚氰氯修饰过程后接触角;其中,
1表示裸金膜表面;
2表示经多羟基修饰的金膜表面;
3表示经多羟基和三聚氰氯修饰的金膜表面。
图4是本发明实施例2固定有葡萄糖和鸡卵白蛋白功能化层与凝集素相互作用:(a)作用后与作用前的spri差减图;(b)spr实时曲线。
图5是本发明实施例2的玻璃制备功能化层的过程示意图和荧光成像图;其中,1代表玻璃表面修饰多羟基化合物;2代表玻璃表面修饰三聚氰氯;3代表玻璃表面修饰赖氨酸;4代表去活化过程;5代表荧光分子标记赖氨酸后的荧光成像图。
具体实施方式
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1、
以在金膜表面固定葡萄糖和鸡卵白蛋白(如图1所示),具体制备步骤如下:
一、具有葡萄糖和鸡卵白蛋白的功能化层在金膜表面的制备
1、金膜表面原位修饰引发剂
将金膜浸泡于10mmol/l、0.75ml的巯基十一醇(muoh)的乙醇溶液中,4℃反应12h,经乙醇清洗3次后,氮气吹干。将金膜置于合适的反应器,加入1ml四氢呋喃(13.7mmol)和84μl吡啶(1.0mmol),并逐滴加入124μl2-溴异丁酰溴(bibb,)(1.0mmol)。室温25℃反应30min,金膜用四氢呋喃清洗3次,氮气吹干。
2、聚甲基丙烯酸羟乙酯(phema,分子量约为30,000)于金膜表面原位聚合
phema原位聚合需要在惰性气体保护下进行。hema单体(12.6mmol)、二联吡啶(92.8mmol)和cubr(37.6mmol)溶于甲醇/水(0.5ml:0.5ml)溶液中,预脱气。加入氮气保护的反应器中,聚合反应结束,乙醇、水清洗金膜各3次,氮气吹干。本实施例中,通过控制聚合时间30min。经原位聚合后,如图2所示,spr共振角位移说明多羟基化合物在表面的成功修饰。如图3所示金膜经cc修饰表面亲水性显著提高。
3、phema与cc的反应对金膜表面进行功能化
经phema修饰的金膜用cc(0.1mmol)和n,n’-二甲基异丙基二胺(dipea,3.5μmol)的丙酮(1ml)溶液浸泡,4℃反应8h,丙酮清洗,氮气吹干,用于点阵制作。由图3可知,多羟基表面经cc修饰过程,表面亲疏水性无显著变化。
4、葡萄糖或鸡卵白蛋白点阵制作
采用简易点样仪将葡萄糖水溶液(100mm,0.1mmol)点至经cc功能化的金膜表面制作相应的点阵。室温25℃保湿孵育8h,水洗3次,氮气吹干。乙醇胺溶液(ph=8.6,1m,1ml)室温25℃封闭3h后,水洗3次,氮气吹干,-20℃保存。即得到本发明表面多功能化涂层。
二、相关测试与分析应用
为证明本发明实施例1制备得到的表面多功能化涂层是否具有生物识别活性,能否用于分子间相互作用直接测定,将探针分子与伴刀豆凝集素(cona)相互作用,采用表面等离子体共振成像仪进行检测,其操作方法如下:
1、利用spri进行葡萄糖与凝集素相互作用研究
采用25mm的tris-hcl缓冲溶液(含有1mm的cacl2、1mm的mncl2、及0.1%的tween-20)配置cona溶液。将缓冲溶液、cona溶液及缓冲溶液依次通入spri装置的流通池中,使得固定的葡萄糖与cona结合。由图4中spri净信号可得,本发明表面多功能化涂层具有生物识别活性且能用于分子间相互作用直接测定。
实施例2、
在玻璃表面固定赖氨酸,具体功能化层的制备步骤如下:
一、具有赖氨酸的功能化层在玻璃表面的制备
1、玻璃表面原位修饰引发剂
玻璃基底经等离子体清洗(70w,3min)立即浸没入0.75ml、3%(质量分数)3-氨基-三甲氧基硅烷(atpms)甲苯溶液中反应30min,经甲苯、丙酮超声清洗各3次后,氮气吹干。将金膜置于合适的反应器,加入(13.7mmol)四氢呋喃和1.0mmol)吡啶,并逐滴加入1.0mmol2-溴异丁酰溴(bibb)。反应30min,玻璃基底用四氢呋喃清洗3次,氮气吹干。
2、phema于玻璃表面原位聚合
phema原位聚合需要在惰性气体保护下进行。hema单体(12.6mmol)、二联吡啶(92.8mmol)和cubr(37.6mmol)溶于甲醇/水(0.5ml:0.5ml)溶液中,预脱气。加入氮气保护的反应器中,聚合反应结束,乙醇、水清洗金膜各3次,氮气吹干。本实施例中,通过控制聚合时间可以对表面羟基数量进行调控。
3、phema与cc的反应对玻璃表面进行功能化
经phema修饰的玻璃基底用cc(0.1mmol)和dipea(3.5μmol)的1ml丙酮溶液浸泡,4℃反应8h,丙酮清洗,氮气吹干,用于点阵制作。
4、赖氨酸点阵制作
采用简易点样仪将赖氨酸水溶液(100mm,0.1mmol)点至经cc功能化的玻璃基底表面制作相应的点阵。室温保湿孵育8h,水洗3次,氮气吹干。
5.荧光试剂原位标记赖氨酸
异硫氰酸荧光素(fitc,2.5mm)0.75ml浸泡点阵芯片,避光过夜反应,水洗3次,氮气吹干。即得到本发明表面多功能化涂层。
二、相关测试与分析应用
为证明本发明实施例2所得表面多功能化涂层能否用于荧光成像,其操作方法如下:
荧光成像分析:采用倒置荧光显微镜(olympus-ix71,λ=488nm)进行荧光成像分析。实验结果由图5表明,本发明表面多功能化涂层能用于荧光成像。
- 还没有人留言评论。精彩留言会获得点赞!