血清中脂蛋白a先后双试剂测定方法与流程
本发明属于一种脂蛋白a免疫比浊测定方法;或是利用可见光,通过测试反应的结果产生颜色变化来测试材料的方法,特别是涉及一种用生化分析仪检测血清中脂蛋白a的先后双试剂测定方法。
背景技术:
脂蛋白a(lpa)是心脑血管病的独立危险因素,其在动脉粥样硬化(as)与血栓形成中起着重要的桥梁和纽带作用,lpa具有明显的多态性,由于其结构的特殊性,使得目前测定lpa的不同方法、不同试剂、不同系统之间的结果缺乏可比性,需对其测定进行标准化。测定lpa的免疫化学检测法,如辐射状免疫扩散法(rid)、电免疫扩散法(eid)、放射免疫测定法(ria)、酶联免疫吸附试验(elisa)、免疫浊度法(包括免疫散射比浊法(ina)和免疫透射比浊法(ita)、解离增强配体荧光免疫测定法(delfia)等。rid法与eid法因操作简便,不需特殊设备,仍有一些基层单位实验室采用,但缺点是灵敏度低。ria法的缺点是操作复杂,有放射性核素污染。delfia法因需特殊仪器,国内也较少应用。各种lpa方法测定所得参考值相近,目前国内外所采用的判断标准基本相同。一般认为300mg/l为临界水平,大于300mg/l以上为病理水平,lpa的测定的临床应用价值已引起越来越多研究者的重视。
lpa测定的标准化数次国际性的lpa室间调查表明,不同实验室之间lpa结果差异很大,说明检测质量问题严重,急需进行标准化工作,lpa组成、大小、密度不均一性即lpa的多态性是lpa测定标准化的最大困难之一。试剂盒的分析性能差异、缺乏国际公认的二级参考材料、lpa的报告方式等也是影响lpa标准化的重要因素。
各种血清蛋白、补体、免疫球蛋白、急性反应蛋白、血凝蛋白及尿微量蛋白、lpa等都可在它们的特异性抗体存在下形成抗原(ag)-抗体(ab)复合物。这些免疫复合物可在不加标记的情况下,基于其散射光性质(light-scattering)通过透射比浊(turbidimetry)或散射比浊(nephelometry)方法直接参照标准(校正)物测定。
ag与其特异ab的结合是非共价的,按下述反应定律进行:
ag+ab→agabcomplex
结合常数是k。这种结合力的强弱决定于ag对ab的亲合力,参与结合的作用力包括氢键、范德华力(vanderwaalsbond)和疏水键等。在[ab]一定时,增加[ag],反应向ag-ab复合物形成方向进行。随着[ag]的增加,在[ab]过量区,随着[ag]增加免疫复合物形成增加,反应浊度升高,直至最高的反应平衡区;此后,进一步增加[ag]将导致沉淀增加,反应浊度反而下降,此为ag过剩区。这三个阶段出现的原因是:大多数ab是双价的(multivalent)。在反应的开始阶段,有较多的ab可被结合到抗原上。因此,ag上的所有结合位点都被ab结合,只有简单的可溶性ag-ab复合物,[agab]可通过光散射的性质被定量,经与标准(校正)物比较求出[ag],但在临床检验测定中,如何确认抗原浓度过剩而引起的测定结果出现偏差?。
技术实现要素:
:
为了解决现有技术中血清中lpa的测定方法存在lpa浓度过高而引起的测定结果出现偏差,本发明提供一种经济方便易行,准确性更高、能够通过实时反应曲线判定血清脂蛋白a测定中过剩的方法。
解决该技术问题采用的技术方案是:采用先后双试剂测定方法,试剂ⅰ和试剂ⅱ均为抗人脂蛋白a抗体试剂,血清中脂蛋白a与脂蛋白a测定试剂中抗体于37℃温浴3~5分钟形成抗原抗体复合物,使反应液出现浊度,然后再加入脂蛋白a测定试剂,当反应液中脂蛋白a过剩时,将再次出现反应峰,表明脂蛋白a抗原过剩;当出现平坦曲线时,则表明反应已达到了终点,仪器在334~340nm波长处检测,以第一步反应产生的浊度计算出脂蛋白a的含量。本发明检测时能够判断抗原过剩现象,经济方便易行,是一种准确性更高的脂蛋白a检测方法。
试剂ⅰ各组分浓度为:甘氨酸0.10~0.24mmol/l,氯化钠0.05~0.15mmol/l,包被抗lpa抗体的乳胶颗粒悬浮液2~8%,proclin-300防腐剂100μl~300μl;试剂ⅱ各组分浓度为:甘氨酸0.10~0.24mmol/l,氯化钠0.05~0.15mmol/l,包被抗lpa抗体的乳胶颗粒悬浮液2~8%,proclin-300防腐剂100μl~300μl。上述试剂ⅰ和试剂ⅱ中磷酸盐缓冲液的ph值为8.0±0.2。
上述测定中反应物的体积比为:样品∶试剂i∶试剂ii=1∶40~60∶5~10。
本方法的试剂虽与原有的lpa试剂组分相同,只是将采用先后双试剂测定方法,试剂ⅰ和试剂ⅱ均为抗人脂蛋白a抗体试剂,可以通过实时反应曲线监测到lpa过剩现象,测定效果明显不同。
本发明与现有技术相比有如下优点:原有的lpa测定方法不能监测到lpa过剩现象,而本发明方法可以监测到lpa过剩现象,是一种准确性更高的lpa检测方法。
附图说明
附图1.是单一试剂法实时反应曲线;
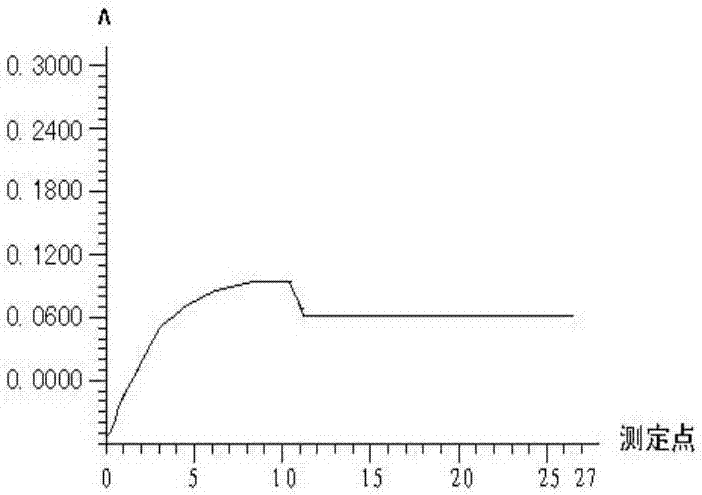
附图2是本发明方法已达到反应终点时实时反应曲线;
附图3是本发明方法抗原过剩时实时反应曲线。
具体实施方式:
下面通过实施例及附图对本发明做进一步详细说明。
实施例1
试剂的组成:
a.试剂ⅰ:
甘氨酸0.17mmol/l,氯化钠0.10mmol/l,包被抗-lpa抗体的乳胶颗粒悬浮液5%,proclin-300防腐剂200μl。
b.试剂ⅱ:
甘氨酸0.17mmol/l,氯化钠0.10mmol/l,包被抗-lpa抗体的乳胶颗粒悬浮液5%,proclin-300防腐剂200μl。
c.标准液:采用1000mg/l定值血清进行多点定标。
上述测定中反应物的体积比为:样品∶试剂i∶试剂ii=1∶50∶5。
实施例3
测定程序
研究对象住院及门诊患者45例进行空腹采血2.0ml,离心后分离血清进行lpa测定,应用单一试剂法和本发明方法进行lpa测定,并观察实时反应曲线,下面通过单一试剂法和本发明专利法进行说明本发明的检测效果
1.双试剂法:在日本olympusau2700全自动化生化分析仪上,仪器自动将5μl样品加入到250μl试剂ⅰ中混匀,37℃孵育3分钟,加入50μl试剂ⅱ混匀,37℃孵育5.1分钟,全自动分析仪在340nm波长处检测。仪器自动计算出lpa结果,具体见表1:
表1.本发明自动化生化分析仪测试条件
计算公式为:
odlpa=od2-od1
脂蛋白a浓度=f×odlpa
其中odlpa是脂蛋白a产生的吸光度,od1是样品加入前测得的吸光度,od2是加入试剂ⅰ反应后测得的吸光度,f是校正因数。
2.单一试剂法:在日本olympusau2700全自动化生化分析仪上,仪器自动将5μl样品加入到225μl试剂中混匀,37℃孵育3分钟,全自动分析仪在340nm波长处检测,仪器自动计算出lpa结果。
研究表明在lpa0.8~926.5mg/l时,两种方法测定结果无显著性差异,n=45,t=3.23,p=0.3338,实时反应曲线如图1,2所示,测定结果均可靠,本发明方法加入试剂ii后可出现平坦的曲线如图2;在lpa大于926.5mg/l时,单一试剂法测定结果显示926.5mg/l,本发明方法除计算出测定结果外,加入试剂ii后实时反应曲线可出现双峰现象,可提示lpa出现过剩,反应未达到终点,应稀释后重测方可报出准确结果,如图3所示。本发明方法在lpa过量与适量呈现出不同的实时反应曲线,如图2,3比较。
经过以上比较可看出,本发明虽与原配方组成相同,但因采用先后双试剂法,可以监测到抗原在反应液中过剩的现象,达到了准确检测的目的。
- 还没有人留言评论。精彩留言会获得点赞!