自组装有纳米金棒的碳纳米管的制备及利用其进行生物分子检测的方法与流程
本发明涉及纳米材料领域,特别是自组装有纳米金棒的碳纳米管的制备及利用其进行生物分子检测的方法。
背景技术:
随着生物技术的发展以及生物产品应用得越来越广泛,生物分子的检测方法也已发展成熟,各类检测技术早已经广泛应用于不同的生物分子检测领域。正是依赖于这些有效的检测手段才保证了我国食品、药品监测的准确性,保证了流通的安全。
现阶段的检测手段都是针对单一生物分子进行检测,并且都需要用荧光标记物或生物试剂盒等昂贵的试剂材料。目前生物分子检测存在的问题是:第一,检测成本高;第二,所需的检测仪器复杂;第三,检测手段普及率低,普及困难大。
技术实现要素:
本发明的目的是提供自组装有纳米金棒的碳纳米管的制备及利用其进行生物分子检测的方法,要解决现阶段生物检测制备不方便、成本高、分析速度有限、不易携带、普及推广困难的技术问题。
为实现上述目的,本发明采用如下技术方案:本发明提供自组装有纳米金棒的碳纳米管的制备,具体操作步骤如下:
步骤一:制备单壁碳纳米管,具体包括:
s1,将表面厚度为250nm-550nm的sio2的si基片手工裁成5mm×6mm的小片;
s2,用丙酮、乙醇和水进行超声清洗处理;
s3,以乙醇为碳源,fe为催化剂,在si基片表面生长出单壁碳纳米管;生长温度为850℃-950℃;
步骤二:制备碳纳米管微狭缝电极基片;
步骤三:制备纳米金棒;
步骤四:组装纳米金棒;将步骤二中制备好的碳纳米管微狭缝电极基片静置于纳米金棒溶液中,使其通过静电自组装,将自主装好的电极基片取出,用超纯水冲洗;
步骤五:通过探针台和电化学工作站测量出组装好纳米金棒碳管的电极间电导并记录。
进一步,纳米金棒沿着碳管横向或者纵向线性排列。
进一步,纳米金棒的粒径长度为107.5±7.2nm,直径14.7±0.6nm。
进一步,所述步骤二具体包括:
s1,在单壁碳纳米管基片上滴上pmma阻蚀剂;匀胶后,在热板上放置几分钟;
s2,通过ebl电子束曝光系统,将电子束打到基片上,电子束的组成的图案为电极形状,有单根碳管横跨过两极,两电极间距离为1μm;
s3,将曝光完成后的基片先置于显影液再置于定影液中,使电极图案暴露出来;显影时间为20s-30s,定影时间为20s-30s;
s4,使用真空蒸镀法将金膜镀到基片表面,将基片置于丙酮中,暴露出电极图案的位置的金膜会被保留,其他位置的金膜会随着pmma在丙酮中被溶解除去;
s5,被保留下的金膜及其狭缝间的单壁碳纳米管,即组成为单根单壁碳纳米管电极。
进一步,步骤二的s1中,pmma阻蚀剂规格为600k-900k;匀胶转速为3500-4000转/分钟;热板温度为140℃-160℃。
进一步,步骤二的s2中,两电极间距离为0.4μm-0.6μm。
进一步,所述步骤三具体包括:
s1,烧杯中,加入haucl4和ctab,搅拌至澄清透明后,然后将冰mnabh4的快速注入溶液中,溶液的颜色会由淡黄色转至茶色,静置,作为种子溶液备用;
s2,将ctab和naol溶于水中,搅拌至完全溶解;随后加入agno3溶液,搅拌至澄清透明;再加入haucl4溶液和浓盐酸,继续搅拌至澄清透明,作为生长液备用;
s3,将抗坏血酸溶液,与s1中制得的种子溶液加入到s2中制得的生长液内,静置,即可得到纳米金棒溶液。
进一步,步骤四:组装纳米金棒的时间为5-10min。
进一步,碳纳米管的长度为100um-50000um。
本发明另一方面提供利用上述自组装有纳米金棒的碳纳米管进行生物分子检测的方法,具体步骤如下:
步骤一,将制备好的自组装有纳米金棒的碳纳米管,通过探针台和电化学工作站可以测得其电极间的电导,此时由于纳米金棒已组装于碳管壁连接成线,此时测得的为大电流作为对照;
步骤二,将自组装有纳米金棒的碳纳米管浸泡于高浓度探针分子溶液中使其充分吸附探针分子,取出,用超纯水冲洗,氮气吹干;通过探针台和电化学工作站测量其电导;由于纳米金棒表面强大的吸附能力,纳米金棒表面会被探针分子紧密包裹住;
步骤三,将步骤二中的碳纳米管置于待测待检测样品溶液中一段时间,取出,用超纯水冲洗,氮气吹干;
步骤四,将其置于氯化铁和硫脲的溶液中一段时间,取出,用超纯水冲洗,氮气吹干;通过探针台和电化学工作站测量其电导,将结果与步骤一得到的对照电流进行比较;
步骤五,得出试验结论;样品溶液中有目标分子,则纳米金棒表面探针分子被清除,纳米金棒表面重新暴露出来,电流降低;样品溶液中无目标分子,则探针分子无法被清除,纳米金棒继续被包裹住,电流基本无变化。
进一步,生物分子为dna或者生物酶。
本发明的有益效果体现在:
1,自组装有纳米金棒的碳纳米管的制备方式设置合理,反应成功率高,制备方便,更为重要的是纳米金棒能够沿着碳管横向或者纵向线性排列在碳纳米管上,电流大。在单壁碳纳米管上原位生长单壁碳纳米管,然后通过静电吸附将纳米金棒组装于单壁碳纳米管壁。无需对碳纳米管进行基片转移,也无需任何化学方法将纳米金棒进行固定,方法简单。
2,本发明提供了自组装有纳米金棒的碳纳米管的制备及利用其进行生物分子检测的方法,以单壁碳纳米管为载体连接电极,由于碳纳米管自身导电能力较弱,能灵敏地检测到纳米金棒连接断开前后的变化,进而通过自身电导的改变实现电信号转化,进一步提高了单壁碳纳米管的灵敏度和检测下限。制备成本低廉,检测生物分子具有灵敏度高、分析速度快、仪器简单、成本低、结果可靠以及能实现原位实时检测等优点。并且易于批量化生产。
3,本发明提供了自组装有纳米金棒的碳纳米管的制备及利用其进行生物分子检测的方法,通过单壁碳纳米管中探针分子的改变,使得本发明提供的自组装有纳米金棒的碳纳米管可以适用于检测其他不同的目标分子,不需要用到荧光标记物及生物试剂盒等昂贵的试剂材料,具有普适性,能循环使用,经济廉价,更利于推广使用。
4,本发明提供的碳纳米管体积小、重量轻,便于携带,大大减轻了检测人员的工作负重。
本发明的其它特征和优点将在随后的说明书中阐述,并且部分地从说明书中变得显而易见,或者通过实施本发明而了解。本发明的主要目的和其它优点可通过在说明书中所特别指出的方案来实现和获得。
附图说明
下面结合附图对本发明做进一步详细的说明。
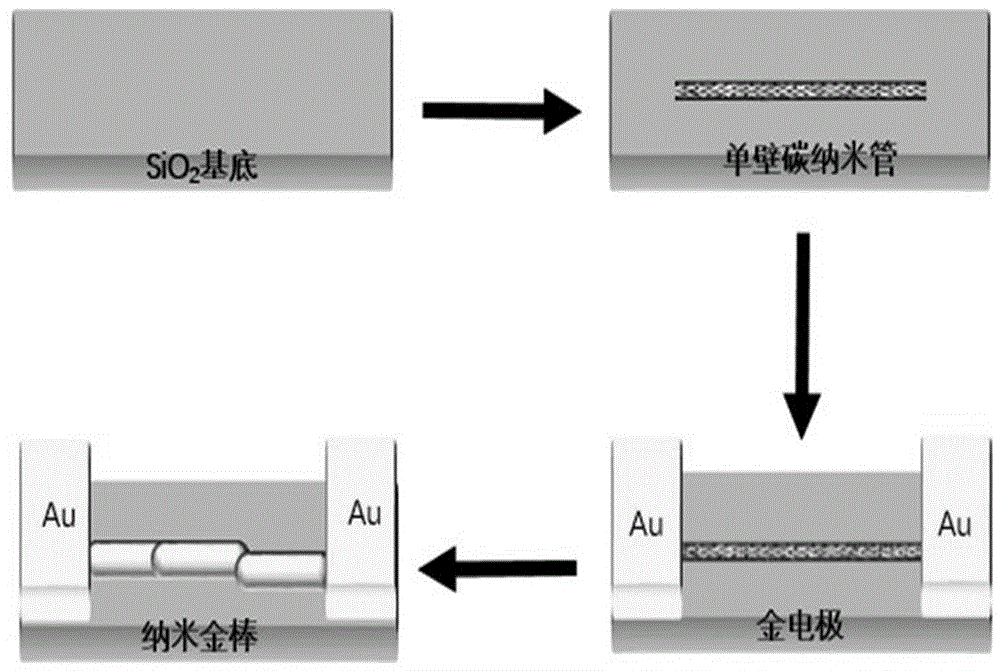
图1是自组装有纳米金棒的碳纳米管的制备的流程图;
图2是生物分子检测方法图;
图3是检测时电流变化示意图。
图4是自组装有纳米金棒的碳纳米管的电镜图。
具体实施方式
以下通过实施例来详细说明本发明的技术方案,以下的实施例仅仅是示例性的,仅能用来解释和说明本发明的技术方案,而不能解释为对本发明技术方案的限制。
目前,纳米材料被广泛地应用于生物单壁碳纳米管的研究和开发。其中,金纳米棒由于具有较强的光散射吸收效率、比表面积大、良好的光学稳定性、生物相容性、易加工制备等特点,已经广泛应用于生物传感、光学成像、基因和药物载体、热治疗等多个领域。基于纳米金棒的生物单壁碳纳米管具有低耗费、高灵敏以及小尺寸等优点,被广泛地应用于生物检测领域。
基于纳米金棒的电化学生物单壁碳纳米管,利用组装技术将纳米金棒固定在电极表面,不仅可以携带多个指示剂分子,还可以增加电极的有效表面积,从而大大提高了电化学检测的灵敏度。
实施例1
如图1所示,本发明提供自组装有纳米金棒的碳纳米管的制备,具体操作步骤如下:
步骤一:制备单壁碳纳米管,具体包括:
s1,将表面厚度为250nm-550nm的sio2的si基片手工裁成5mm×6mm的小片;
s2,用丙酮、乙醇和水进行超声清洗处理;
s3,以乙醇为碳源,fe为催化剂,在si基片表面生长出单壁碳纳米管;生长温度为850℃-950℃;
步骤二:制备碳纳米管微狭缝电极基片;具体包括:
s1,在单壁碳纳米管基片上滴上pmma阻蚀剂;匀胶后,在热板上放置几分钟;具体的pmma阻蚀剂规格为600k-900k;匀胶转速为3500-4000转/分钟;热板温度为140℃-160℃。
s2,通过ebl电子束曝光系统,将电子束打到基片上,电子束的组成的图案为电极形状,有单根碳管横跨过两极,两电极间距离为0.5μm。
s3,将曝光完成后的基片先置于显影液再置于定影液中,使电极图案暴露出来;显影时间为20s-30s,定影时间为20s-30s;
s4,使用真空蒸镀法将金膜镀到基片表面,将基片置于丙酮中,暴露出电极图案的位置的金膜会被保留,其他位置的金膜会随着pmma在丙酮中被溶解除去;
s5,被保留下的金膜及其狭缝间的单壁碳纳米管,即组成为单根单壁碳纳米管电极。
步骤三:制备纳米金棒;具体包括:
s1,在50ml烧杯中,加入5ml0.5mmhaucl4和5ml0.2mctab,搅拌至澄清透明后,然后将冰0.6ml0.01mnabh4的快速注入溶液中,溶液的颜色会由淡黄色转至茶色,静置30min,作为种子溶液备用;
s2,将7gctab和1.234gnaol溶于250ml水中,搅拌至完全溶解;随后加入24ml4mmagno3溶液,搅拌至澄清透明;再加入250ml1mmhaucl4溶液和4.8ml浓盐酸,继续搅拌至澄清透明,作为生长液备用;
s3,将1.25ml0.064m抗坏血酸溶液,与0.8mls1中合成的种子溶液加入到s2中的生长液,静置12h,即可得到纳米金棒溶液。
步骤四:组装纳米金棒;将步骤二中制备好的碳纳米管微狭缝电极基片静置于纳米金棒溶液中,使其通过静电自组装,将自主装好的电极基片取出,用超纯水冲洗;组装纳米金棒的时间为5-10min。参见如图4所示。
步骤五:通过探针台和电化学工作站测量出组装好纳米金棒碳管的电极间电导并记录。纳米金棒沿着碳管横向或者纵向线性排列。纳米金棒的粒径长度为107.5±7.2nm,直径14.7±0.6nm.
由于通过ebl法制备微狭缝电极,两极间的距离可以做到极小(小于1μm),因而电极间的金棒个数也极少(以长为100nm金棒为例,当电极间狭缝长为500nm左右时,只需5-6个金棒首尾相连即可连通电极)。所以,每个器件上所需被清除的探针分数也更少,所需的目标分子数也更少。这样更利于低浓度目标分子的检测。
依照上述步骤提供如下实验数据:
实施例1-4的各项参数明细
注:naol是油酸钠,一种表面活性剂。
如图2所示,本发明另一方面提供利用上述自组装有纳米金棒的碳纳米管进行生物分子检测的方法,生物分子为dna或者生物酶,将基片用含探针分子的溶液处理,使纳米金棒表面充分吸附探针分子,再将基片置于待检测样品溶液中。
步骤一,未经任何处理前,通过探针台和电化学工作站可以测得自组装有纳米金棒的碳纳米管的电极间的电导,此时由于纳米金棒已组装于碳管壁连接成线,此时测得的为大电流,将其作为对照。
步骤二,将自组装有纳米金棒的碳纳米管浸泡于高浓度探针分子溶液中使其充分吸附探针分子,取出,用超纯水冲洗,氮气吹干;通过探针台和电化学工作站测量其电导;由于纳米金棒表面强大的吸附能力,纳米金棒表面会被探针分子紧密包裹住。
步骤三,将步骤二中的碳纳米管置于待测待检测样品溶液中一段时间,取出,用超纯水冲洗,氮气吹干;
步骤四,将其置于氯化铁和硫脲的溶液中一段时间,取出,用超纯水冲洗,氮气吹干;通过探针台和电化学工作站测量其电导,将结果与步骤一得到的对照电流进行比较;
步骤五,得出试验结论;样品溶液中有目标分子,则纳米金棒表面探针分子被清除,纳米金棒表面重新暴露出来;样品溶液中无目标分子,则探针分子无法被清除,纳米金棒继续被包裹住。
只有当纳米金棒表面处于暴露状态下,纳米金棒才能被氯化铁和硫脲溶的液刻蚀变小至连接断开。通过对电极间电导能力的测试,完成刻蚀的电极间为小电流,未能完成刻蚀的电极间为大电流。电极间电流变小,说明纳米金棒完成刻蚀,即样品溶液中含有目标分子,从而实现对目标分子的电信号转化检测。
本发明提供的利用纳米金棒刻蚀条件电信号转换检测生物分子的单壁碳纳米管,电极间通过单根单壁碳纳米管连接,碳纳米管本身具有一定导电能力,纳米金棒的刻蚀导致碳纳米管的电导能力减弱,可以灵敏的通过电信号转化捕捉到,进一步提高了灵敏度和检测下限,同时能进行循环利用。
进一步,本发明构建了一根超长的单壁碳纳米管碳,纳米管的长度为100um-50000um。(碳纳米管在基片上生长,长度达到数百微米至数厘米),因而可以实现器件的并联使用,对同一样品,可以同时检测多个不同的目标分子,检测完毕后,纳米金棒可以重新组装,循环使用。
本发明还提供利用自组装有纳米金棒的碳纳米管进行生物分子检测的方法:
检测的目标物是可以为dna或者生物酶之类的生物分子,具体的检测实例:例如我们可以设计探针分子的核酸序列,从而检测出特定序列的目标核酸分子。例如,探针分子为:(5′→3′)ccacatcatccatatagct。能检测出目标分子序列agctatatggatgatgtgg。
采用实施例1中制得自组装有纳米金棒的碳纳米管,粒径长度约为108.7nm,直径约为15.1nm。通过探针台和电化学工作站可以测得其电极间的电导,此时由于纳米金棒已组装于碳管壁连接成线,此时测得的为大电流,该大电流读数参见图3所示,imax=1.6a,imax作为对照。
将其浸泡于高浓度探针分子溶液中使其充分吸附探针分子,测量电导约为imax。将单壁碳纳米管基片置于0.05mm氯化铁和1mm硫脲溶液中3h。取出并用氮气吹干,测量电导。结论:单壁碳纳米管基片检测目标分子具有极高的灵敏性。如果电极间的电导没有明显的变化,说明样品中没有目标分子,(imax=1.6a)。如果电极间电导明显减小,说明待测样品中有目标分子(imix=0.02a)。
本发明提供自组装有纳米金棒的碳纳米管的制备及利用其进行生物分子检测的方法,成功构建了单壁碳纳米管与纳米金棒组合器件,通过利用纳米金棒刻蚀的条件作为检测目标生物分子的开关。由于单壁碳纳米管本身具有一定导电能力,当纳米金棒被刻蚀后,减小的电导可以通过单壁碳纳米管被检测到,因而具有更高的灵敏度。
以上所述仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内所想到的变化或替换,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!