用于制备太阳能电池的光吸收层的前体及其制备方法与流程
本申请要求于2014年11月5日向韩国知识产权局提交的韩国专利申请No.10-2014-0152663和2015年5月13日向韩国知识产权局提交的韩国专利申请No.10-2015-0066497的权益,其公开内容通过引用整体并入本文。本发明涉及用于制备太阳能电池的光吸收层的前体及其制备方法。
背景技术:
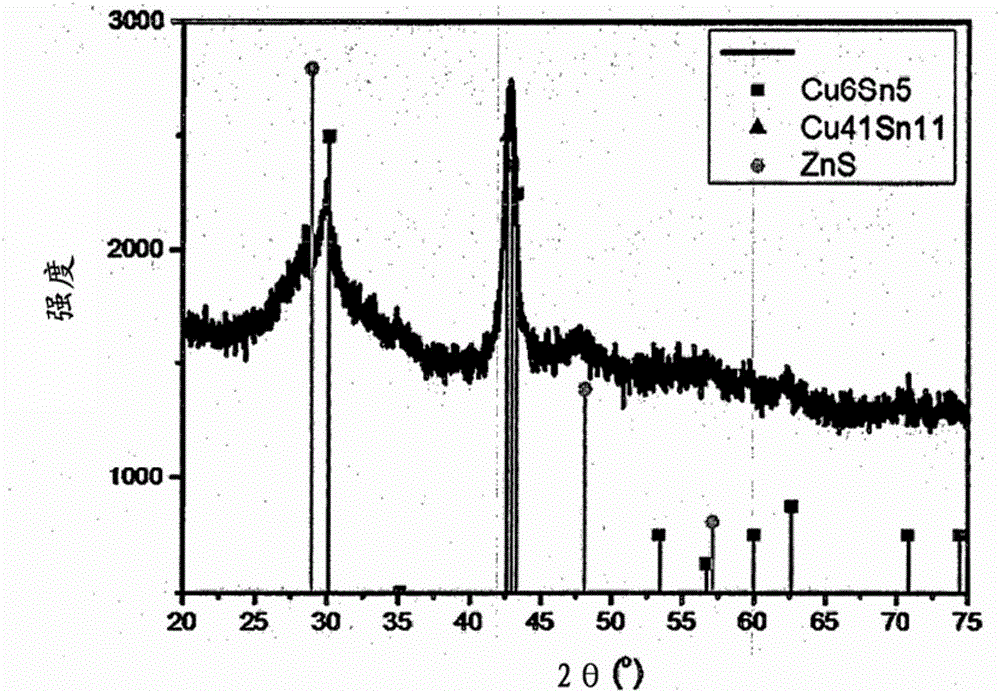
:从其发展的早期阶段开始就已经使用以高成本形成的光吸收层以及作为半导体材料的硅(Si)来制造太阳能电池。为了更经济地制造工业上可行的太阳能电池,已经开发了利用廉价的光吸收材料(例如铜铟镓(二)硒(CIGS)或Cu(In,Ga)(S,Se)2)的薄膜太阳能电池结构。这样的CIGS基太阳能电池通常包括背面电极层、n型结部件和p型光吸收层。含有这类CIGS层的太阳能电池的功率转换效率大于19%。然而,虽然CIGS基薄膜太阳能电池具有潜能,但是铟(In)的供应不足及成本是使用CIGS基光吸收层的薄膜太阳能电池的广泛适用性和可行性的主要障碍。因此,迫切需要开发使用无铟(In)或低铟(In)且低成本的普遍元素的太阳能电池。因此,作为CIGS基光吸收层的替代物,含有极廉价元素铜(Cu)、锌(Zn)、锡(Sn)、硫(S)或硒(Se)的CZTS(Cu2ZnSn(S,Se)4)基太阳能电池近来受到极大关注。有利地,CZTS具有约1.0eV至约1.5eV的直接带隙和104cm-1或更高的吸收系数,其储量相对高,且CZTS使用价格便宜的Sn和Zn。1996年首次报道了CZTS异质结PV电池,但CZTS基太阳能电池在技术上不如CIGS基太阳能电池先进,并且CZTS基太阳能电池的光电效率为10%或更低,这远低于CIGS基太阳能电池。CZTS的薄膜通过溅射、混合溅射、脉冲激光沉积、喷雾热解、电沉积/热硫化、电子束加工、Cu/Zn/Sn/热硫化和溶胶-凝胶法制造。同时,PCT/US/2010-035792公开了通过对使用包含CZTS/Se纳米颗粒的墨的基底进行热处理来形成薄膜。通常,当使用CZTS/Se纳米颗粒形成CZTS薄膜时,由于先前形成的小晶体而难以在随后的形成薄膜的过程中增大晶体尺寸。因此,当各晶粒小时,界面扩展并且在界面处发生电子损失。因此,效率不可避免地劣化。因此,薄膜中使用的纳米颗粒应包括Cu、Zn和Sn,并且不应是CZTS晶型。然而,不利地,由单一金属元素构成的金属纳米颗粒可能易被氧化,并且随后需要使用大量Se在高温下除去氧化物的附加工艺。此外,当分别合成包含各自金属的硫属化物并在制备墨的过程中组合使用或与金属纳米颗粒组合使用时,不均匀的金属组成比可能造成问题并且具有不同相的金属纳米颗粒之间的混合不充分可能导致在薄膜中形成次生相。因此,越来越需要开发用于薄膜太阳能电池的技术,所述薄膜太阳能电池包括对氧化稳定的高效光吸收层,包括足够量的第VI族元素,具有总体更均匀的组成,使薄膜中次生相的形成最小化并且具有增加的膜密度。技术实现要素:技术问题因此,进行本发明以解决尚未解决的上述问题和其他技术问题。作为各种广泛和深入的研究和实验的结果,本发明人开发了一种用于制备光吸收层的前体,所述前体包括:(a)聚集相复合体,其包括包含铜(Cu)-锡(Sn)双金属的第一相和包含含锌(Zn)硫属化物的第二相,或包括包含铜(Cu)-锡(Sn)双金属的第一相、包含含锌(Zn)硫属化物的第二相和包含含铜(Cu)硫属化物的第三相;或者(b)核-壳结构纳米颗粒,其包括包含铜(Cu)-锡(Sn)双金属纳米颗粒的核和包含含锌(Zn)硫属化物的壳或含锌(Zn)硫属化物和含铜(Cu)硫属化物的壳;或者(c)其混合物,并且发现,当使用所述前体制造薄膜时,薄膜可具有整体均匀的组成,可使其中次生相的形成最小化,对氧化稳定,并且由于掺入前体中的S或Se,可包含增加量的第VI族元素,因此具有高品质。基于这些发现完成了本发明。技术方案根据本发明的一个方面,提供了用于制备太阳能电池的光吸收层的前体,包括:(a)聚集相复合体,其包括包含铜(Cu)-锡(Sn)双金属的第一相和包含含锌(Zn)硫属化物的第二相,或者包括包含铜(Cu)锡(Sn)双金属的第一相、包含含锌(Zn)硫属化物的第二相和包含含铜(Cu)硫属化物的第三相;或者(b)核-壳结构纳米颗粒,其包括包含铜(Cu)-锡(Sn)双金属纳米颗粒的核和包含含锌(Zn)硫属化物的壳或含锌(Zn)硫属化物和含铜(Cu)硫属化物的壳;或者(c)其混合物。更具体地,根据本发明用于制备太阳能电池的光吸收层的前体可包括核-壳结构纳米颗粒,其包括包含铜(Cu)-锡(Sn)双金属纳米颗粒的核和包含含锌(Zn)硫属化物的壳或含锌(Zn)硫属化物和含铜(Cu)硫属化物的壳。更优选地,核-壳结构纳米颗粒对氧化稳定,使得在形成薄膜时晶粒表面上的氧化物的形成可最小化,因此可改善反应性,原因是铜(Cu)、锡(Sn)和锌(Zn)金属进一步均匀混合,并且包含铜(Cu)-锡(Sn)双金属的核被包含含锌(Zn)硫属化物的壳所保护。此外,优选地,所述壳还包括含铜(Cu)硫属化物,因为分布在颗粒中的元素的均匀性可以提高并且基于在整个颗粒中包含的Cu的量包含在核中的Cu/Sn的比例可以降低,使得在热处理时可使次生相的形成进一步最小化。具体地,比较了这样的事实:当所述壳不包含含铜(Cu)硫属化物时,基于全部颗粒中包含的Cu的量,核中包含的Cu/Sn比例为1.7至2.1,当所述壳包含含铜(Cu)硫属化物时,基于全部颗粒中包含的Cu的量,核中包含的Cu/Sn的比例降低到约1.2至约1.6。因此,可在热处理时使次生相的形成进一步最小化,并且可通过控制壳中含铜(Cu)硫属化物的含量来增加Cu的缺少量。在一个特定实施方案中,Cu-Sn双金属是指Cu和Sn的合金,其没有限制,只要具有1或更大的Cu/Sn比例(按摩尔计)即可,并且例如包括选自以下的一种或更多种:CuSn、Cu3Sn、Cu3.02Sn0.98、Cu10Sn3、Cu6.26Sn5、Cu6Sn5和Cu41Sn11。在一个特定实施方案中,“硫属化物”是指包括第VI族元素例如硫(S)和/或硒(Se)的物质,含锌(Zn)硫属化物可包括选自ZnS和ZnSe中的一种或更多种,含铜(Cu)硫属化物可包括选自CuxSy和CuxSey(其中0<x≤1,0<y≤2)中的一种或更多种,特别可以是CuS或CuSe。因此,在聚集相复合体的第二相和第三相或核-壳结构纳米颗粒的壳中,含锌(Zn)硫属化物和含铜(Cu)硫属化物中分别包含的Zn和Cu的Cu/Zn比(按摩尔计)可以根据核的Cu/Sn的比例而变化,但是特别可以为0≤Cu/Zn≤20,更特别地为0≤Cu/Zn≤2。在这种情况下,其中Cu/Zn的比例为0的情况意味着聚集相复合体不包含第三相,或者核壳结构的纳米颗粒的壳不包含含铜(Cu)硫属化物。在金属的组成不在该范围内的情况下,能够形成CZTS(e)的组成比例有很大的不同,因此形成过量的次生相例如ZnS、ZnSe、CuS、CuSe和/或Cu2SnS(e),不利地导致光电性能的劣化。同时,本文中使用的术语“聚集相复合体”是指由彼此均匀地聚集的包含第一相的颗粒、包含第二相的颗粒和包含第三相的颗粒构成的单元。因此,聚集相复合体的第一相、第二相和第三相可以独立地存在于单个复合体中。在这种情况下,复合体的形态不受限制并且可以是可变的。在一个特定实施方案中,第一相、第二相和第三相可以随机分布以构成各个区域。聚集相复合体可具有比包含各相的颗粒更大的粒径,因为如上所述其具有其中包括彼此聚集的各相的颗粒的结构。在一个特定实施方案中,聚集相复合体的粒径可为5纳米至500纳米。另一方面,作为根据本发明的用于制备太阳能电池的光吸收层的前体的另一个实施方案,每个核-壳结构纳米颗粒是具有其中Cu-Sn双金属纳米颗粒涂覆有含锌(Zn)硫属化物或含锌(Zn)硫属化物和含铜(Cu)硫属化物的结构的单个纳米颗粒。在这种情况下,核-壳结构纳米颗粒的粒径可为2纳米至200纳米。本发明人发现,当使用这样的聚集相复合体或核-壳结构纳米颗粒作为前体制造薄膜时,与在其中分别合成并混合包含各自元素的颗粒的情况,例如在其中Cu-Sn双金属纳米颗粒和锌(Zn)硫属化物纳米颗粒或含锌(Zn)硫属化物和含铜(Cu)硫属化物是分别合成以及随后混合,或铜(Cu)硫属化物、锌(Zn)硫属化物和锡(Sn)硫属化物纳米颗粒是分别合成以及随后混合的情况相比,在其任何情况下,在合成步骤中已均匀混合了金属和硫属化物元素,可改善组成的均匀性并且因此可获得次生相形成最小化的CZTS。在这种情况下,为了使CZTS最终薄膜发挥最大效率,聚集相复合体或核-壳结构纳米颗粒可具有满足0.5≤Cu/(Zn+Sn)≤1.5和0.5≤Zn/Sn≤2,特别地,0.7≤Cu/(Zn+Sn)≤1.2和0.7≤Zn/Sn≤1.8的金属组成。当金属的组成不在上述范围内时,大量的次生相形成并作为杂质存在,不利地导致光电效率的劣化。此外,相对于1摩尔的锌(Zn)或铜(Cu),在含锌(Zn)硫属化物和含铜(Cu)硫属化物中硫属化物元素的比例可以为0.5至3摩尔。当硫属化物元素的比例不在该范围内并且例如低于0.5摩尔时,不能供应足够的第VI族元素,并且可形成部分缺乏第VI族元素的膜,并且当该比例超过3摩尔时,由于薄膜中第VI族元素的不均匀分布,薄膜可能不均匀地生长,并且在制造薄膜的热处理期间第VI族源蒸发,不利地导致在最终薄膜中产生过量的孔。用于制备光吸收层的前体可通过包括以下步骤的方法制备:(i)制备包含还原剂的第一溶液和包含铜(Cu)盐和锡(Sn)盐的第二溶液;(ii)通过混合使所述第一溶液与所述第二溶液反应以合成铜(Cu)-锡(Sn)双金属纳米颗粒;以及(iii)通过混合使步骤(ii)的Cu-Sn双金属纳米颗粒的分散体与锌(Zn)-配体络合物反应。此外,该方法还可包括在步骤(iii)之后,向步骤(iii)的反应产物中添加铜(Cu)盐,通过Zn-Cu置换反应合成用于制备光吸收层的前体,以及纯化所述前体。如上所述,就整个颗粒的均匀组成和经济效率而言,优选锌(Zn)-配体络合物,原因是可引入含锌(Zn)硫属化物相,而不引入包含第VI族源的第三溶液和包含锌(Zn)盐的第四溶液。在一个特定实施方案中,对配体络合物中所包含的配体没有限制,只要其可用作第VI族元素源即可,并且配体包括例如选自以下化合物中的一种或更多种:在锌(Zn)-配体络合物中与Zn连接的配体的数目没有特别限制,例如为1至4,与Zn连接的配体的种类可以为一种或更多种。此外,用于制备光吸收层的前体可通过包括以下步骤的方法制备:(i)制备包含还原剂的第一溶液和包含铜(Cu)盐和锡(Sn)盐的第二溶液;(ii)通过混合使所述第一溶液与所述第二溶液反应以合成铜(Cu)-锡(Sn)双金属纳米颗粒;(iii)制备包含选自硫(S)、硒(Se)、含硫(S)化合物和含硒(Se)化合物的至少一种第VI族源的第三溶液和包含锌(Zn)盐的第四溶液;以及(iv)通过混合使第三溶液和第四溶液与步骤(ii)的Cu-Sn双金属纳米颗粒的分散体反应以合成用于制备光吸收层的前体,然后纯化所述前体。此外,该方法还可包括在步骤(iv)之后,向步骤(iv)的反应产物中添加铜(Cu)盐,通过Zn-Cu置换反应合成用于制备光吸收层的前体,以及纯化所述前体。在此,Zn-Cu置换反应是指其中通过锌(Zn)和铜(Cu)之间的还原电位的差异含锌(Zn)硫属化物的一部分被含铜(Cu)硫属化物代替的反应。如上所述,通过置换反应,Cu被引入到用于制备光吸收层的前体的第三相或壳中,因而基于在整个颗粒中所含的Cu的量,降低了核中所含的Cu/Sn的比例,并进一步抑制次生相的形成。这样产生的前体包括第一溶液至第四溶液的连续混合,并且如上所述,可以以以下形式合成:(a)聚集相复合体,其包括包含铜(Cu)-锡(Sn)双金属的第一相和包含含锌(Zn)硫属化物的第二相,或者包括包含铜(Cu)-锡(Sn)双金属的第一相、包含含锌(Zn)硫属化物的第二相、包含含铜(Cu)硫属化物的第三相;或(b)核-壳结构纳米颗粒,其包括包含铜(Cu)-锡(Sn)双金属纳米颗粒的核和包含含锌(Zn)硫属化物或含锌(Zn)硫属化物和含铜(Cu)的硫属化物的壳;或者(c)其混合物,而不是以分开独立的Cu-Sn双金属相和含锌(Zn)硫属化物相的颗粒的形式合成。在这种情况下,当将所述第一溶液与所述第二溶液混合时,当将Cu-Sn双金属纳米颗粒的分散体与所述锌(Zn)配体络合物或将所述第三溶液和所述第四溶液混合时以及当进行Zn-Cu置换反应时,可通过反应条件例如反应温度、反应浓度、反应时间和封端剂的类型来控制组成以及可通过控制混合后的溶液的当量比、铜(Cu)盐或配体络合物的含量、滴加速率、搅拌速率、反应温度、反应时间、封端剂的类型等来确保聚集相复合体或核-壳结构纳米颗粒的组成的均匀性和粒径。同时,当将第一溶液与第二溶液混合以制备混合物时,盐的总量与还原剂的混合比按摩尔计为例如1∶1至1∶20。当还原剂含量相对于盐的含量过低时,不能充分发生金属盐的还原,仅可获得过小尺寸的或少量的双金属纳米颗粒,或者难以获得具有期望元素比的颗粒。此外,当还原剂的含量超过盐的含量的20倍时,不利地,在纯化期间不易除去还原剂和副产物。在一个特定实施方案中,第一溶液中包含的还原剂可以是有机还原剂和/或无机还原剂,具体地可以是选自以下的任一种:LiBH4、NaBH4、KBH4、Ca(BH4)2、Mg(BH4)2、LiB(Et)3H、NaBH3(CN)、NaBH(OAc)3、N2H4、抗坏血酸和三乙醇胺。在一个特定实施方案中,第一溶液至第四溶液的溶剂不受限制,并且包括选自以下的一种或更多种:水、醇、二甘醇、油胺、乙二醇、三甘醇、二甲基亚砜、二甲基甲酰胺和N-甲基-2-吡咯烷酮(NMP)且醇溶剂具体地可以是C1-C8醇,例如甲醇、乙醇、丙醇、丁醇、戊醇、己醇、庚醇或辛醇。在一个特定实施方案中,铜(Cu)盐、锡(Sn)盐和锌(Zn)盐的盐可各自独立地选自以下的一种或更多种:氟化物、氯化物、溴化物、碘化物、硝酸盐、亚硝酸盐、硫酸盐、乙酸盐、柠檬酸盐、亚硫酸盐、乙酰丙酮化物、丙烯酸盐、氰化物、磷酸盐和氢氧化物。可使用任一种锡(Sn)盐,而不限于二价和四价盐。在一个特定实施方案中,第VI族源可包括选自以下的一种或更多种:Se、Na2Se、K2Se、CaSe、(CH3)2Se、SeO2、SeS2、Se2S6、Se2Cl2、Se2Br2、SeCl4、SeBr4、SeOCl2、H2SeO3、H2SeO4、S、Na2S、K2S、CaS、(CH3)2S、H2SO4、Na2S2O3和NH2SO3H、其水合物、HSCH2COOH、硫代乳酸、巯基乙醇、氨基乙硫醇、硫脲、硫代乙酰胺和硒脲。同时,第一溶液至第四溶液中的一种或更多种还可包含封端剂。如果需要,封端剂可在制备过程中单独添加。封端剂在溶液处理期间引入,从而控制合成的金属纳米颗粒和用于制备光吸收层的前体的尺寸和颗粒相。封端剂包含原子例如N、O和S,因此易于通过这些原子的孤对电子与金属纳米颗粒表面结合以环绕纳米颗粒表面,从而防止金属纳米颗粒的氧化。对封端剂没有特别限制。例如,封端剂可包括选自以下的一种或更多种:钠L-酒石酸二水合物、酒石酸钠钾、丙烯酸钠、聚(丙烯酸钠盐)、聚(乙烯吡咯烷酮)(PVP)、柠檬酸钠、柠檬酸三钠、柠檬酸二钠、葡糖酸钠、抗坏血酸钠、山梨醇、磷酸三乙酯、乙二胺、丙二胺、1,2-乙二硫醇、乙硫醇、氨基乙硫醇、巯基乙醇、巯基丙酸(MPA)、聚乙烯醇(PVA)和乙基纤维素。封端剂可以适当地存在于溶剂中,例如,相对于1摩尔的全部盐,以20摩尔或更少的量存在。当封端剂的含量超过全部盐的20倍时,不利地,难以纯化前体并且纯度劣化。此外,本发明提供了一种用于制备光吸收层的墨组合物,其包含分散在溶剂中的用于制备光吸收层的前体,以及使用用于制备光吸收层的前体制造薄膜的方法。根据本发明制造薄膜的方法包括:(i)将用于制备光吸收层的前体分散在溶剂中以制备墨,所述前体包括:(a)聚集相复合体,其包括包含铜(Cu)-锡(Sn)双金属的第一相和包含含锌(Zn)硫属化物的第二相,或者包括包含铜(Cu)-锡(Sn)双金属的第一相、包含含锌(Zn)硫属化物的第二相和包含含铜(Cu)硫属化物的第三相;或(b)核-壳结构纳米颗粒,其包括包含铜(Cu)-锡(Sn)双金属纳米颗粒的核和包含含锌(Zn)硫属化物的壳或含锌(Zn)硫属化物和含铜(Cu)硫属化物的壳;或者(c)其混合物;(ii)用墨涂覆设置有电极的基底;和(iii)将涂覆在设置有电极的基底上的墨干燥,并进行热处理。这样,当使用根据本发明的前体制造薄膜时,使用由已均匀混合元素合成的前体,使得薄膜可具有整体更均匀的组成,次生相的形成可最小化,由于在步骤(iii)的热处理期间通过由双金属构成的第一相或核掺入另外的第VI族元素可基于前体的体积增加生长高密度的光吸收层,由于包括S或Se的第二相或壳,可制造高品质的具有增加的VI族元素含量的最终薄膜。在一个特定实施方案中,可使用步骤(i)的溶剂而没有特别限制,只要其是通常使用的有机溶剂即可。溶剂可以是选自以下的有机溶剂或其组合:烷烃、烯烃、炔烃、芳族化合物、酮、腈、醚、酯、有机卤化物、醇、胺、硫醇、羧酸、膦、亚磷酸酯、磷酸酯、亚砜和酰胺。具体地,醇溶剂可以是选自以下的至少一种混合溶剂:乙醇、1-丙醇、2-丙醇、1-戊醇、2-戊醇、1-己醇、2-己醇、3-己醇、庚醇、辛醇、乙二醇(EG)、二乙二醇单乙醚(DEGMEE)、乙二醇单甲醚(EGMME)、乙二醇单乙醚(EGMEE)、乙二醇二甲醚(EGDME)、乙二醇二乙醚(EGDEE)、乙二醇单丙醚(EGMPE)、乙二醇单丁醚(EGMBE)、2-甲基-1-丙醇、环戊醇、环己醇、丙二醇丙醚(PGPE)、二乙二醇二甲醚(DEGDME)、1,2-丙二醇(1,2-PD)、1,3-丙二醇(1,3-PD)、1,4-丁二醇(1,4-BD)、1,3-丁二醇(1,3-BD)、α-萜品醇、二甘醇(DEG)、甘油、2-(乙基氨基)乙醇、2-(甲基氨基)乙醇和2-氨基-2-甲基-1-丙醇。胺溶剂可以是选自以下的至少一种混合溶剂:三乙胺、二丁胺、二丙胺、丁胺、乙醇胺、二亚乙基三胺(DETA)、三亚乙基四胺(TETA)、三乙醇胺、2-氨基乙基哌嗪、2-羟基乙基哌嗪、二丁基胺和三(2-氨乙基)胺。硫醇溶剂可以是选自以下的至少一种混合溶剂:1,2-乙二硫醇、戊硫醇、己硫醇和巯基乙醇。烷烃溶剂可以是选自以下的至少一种混合溶剂:己烷、庚烷和辛烷。芳族溶剂可以是选自以下的至少一种混合溶剂:甲苯、二甲苯、硝基苯和吡啶。有机卤化物溶剂可以是选自以下的至少一种混合溶剂:氯仿、二氯甲烷、四氯化碳、二氯乙烷和氯苯。腈溶剂可以是乙腈。酮溶剂可以是选自以下的至少一种混合溶剂:丙酮、环己酮、环戊酮和乙酰丙酮。醚溶剂可以是选自以下的至少一种混合溶剂:乙醚、四氢呋喃和1,4-二烷。亚砜溶剂可以是选自以下的至少一种混合溶剂:二甲基亚砜(DMSO)和环丁砜。酰胺溶剂可以是选自以下的至少一种混合溶剂:二甲基甲酰胺(DMF)和n-甲基-2-吡咯烷酮(NMP)。酯溶剂可以是选自以下的至少一种混合溶剂:乳酸乙酯、γ-丁内酯和乙酰乙酸乙酯。羧酸溶剂可以是选自以下的至少一种混合溶剂:丙酸、己酸、内消旋-2,3-二巯基琥珀酸、硫代乳酸和硫代乙醇酸。然而,溶剂作为实例给出,本发明不限于此。如果需要,可以向步骤(i)的墨中进一步加入添加剂。添加剂可包括例如选自以下的至少一种:分散剂、表面活性剂、聚合物、粘合剂、交联剂、乳化剂、消泡剂、干燥剂、填料、填量剂、增稠剂、膜调理剂、抗氧化剂、流化剂、流平剂和腐蚀抑制剂。特别地,添加剂可以包括选自以下的至少一种:聚乙烯吡咯烷酮(PVP)、聚乙烯醇(PVA)、Anti-terra204、Anti-terra205、乙基纤维素和DispersBYK110。例如,形成步骤(ii)的涂层的方法可包括选自以下的一种或更多种:湿法涂覆、喷涂、旋涂、刮刀涂覆、接触印刷、顶部进料反转印刷、底部进料反转印刷、喷嘴进料反转印刷、凹版印刷、微型凹版印刷、反向微型凹版印刷、辊涂、狭缝模头涂覆、毛细管涂覆、喷墨印刷、喷射沉积和喷雾沉积。步骤(iii)的热处理可在400℃至900℃的温度下进行。同时,该方法可任选地包括硒化以制备具有高密度的太阳能电池的薄膜。硒化可通过多种方法进行。在第一实例中,硒化可通过将颗粒形式的S和/或Se与步骤(i)的前体一起分散在溶剂中以制备墨并进行步骤(iii)的热处理来进行。在第二实例中,硒化可通过在S或Se的存在下进行步骤(iii)的热处理来进行。更具体地,S或Se的存在可通过供应H2S或H2Se气体或通过加热供应Se或S气体来实现。在第三实例中,硒化可在步骤(ii)之后,层合S或Se,随后进行步骤(iii)来进行。更具体地,层合可通过溶液法或沉积法进行。此外,本发明提供通过该方法制造的薄膜。薄膜可以具有0.5μm至3.0μm的厚度,更具体地,0.5μm至2.5μm的厚度。当薄膜的厚度小于0.5μm时,由于光吸收层的密度和量不足,不能获得期望的光电效率,当薄膜的厚度超过3.0μm时,随着载流子的移动距离增加,导致复合的可能性增加,从而发生效率的降低。此外,本发明提供使用所述薄膜制造的薄膜太阳能电池。制造薄膜太阳能电池的方法是本领域技术人员已知的,因此省略其详细说明。附图说明图1是根据实施例1的用于制备光吸收层的前体的SEM图像;图2是根据实施例1的用于制备光吸收层的前体的XRD图;图3是根据实施例3的用于制备光吸收层的前体的TEM图像;图4是使用图3的TEM图像的线扫描的组成分析图;图5是根据实施例11的用于制备光吸收层的前体的SEM图像;图6是根据实施例11的用于制备光吸收层的前体的XRD图;图7是根据实施例11的用于制备光吸收层的前体的TEM图像;图8是使用图7的TEM图像的线扫描的组成分析图;图9示出了根据实施例22的用于制备光吸收层的前体的组成的线扫描结果;图10是根据实施例22的用于制备光吸收层的前体的SEM图像;图11是根据实施例22的用于制备光吸收层的前体的XRD图;图12是根据实施例24的用于制备光吸收层的前体的SEM图像;图13是根据实施例24的用于制备光吸收层的前体的XRD图;图14是实施例35中制造的薄膜的SEM图像;图15是实施例35中制造的薄膜的XRD图;图16是实施例37中制造的薄膜的截面形状的SEM图像;图17是实施例43中制造的薄膜的SEM图像;图18是实施例43中制造的薄膜的XRD图;图19是实施例47中制造的薄膜的SEM图像;图20是实施例47中制造的薄膜的XRD图;图21是实施例48中制造的薄膜的SEM图像;图22是实施例48中制造的薄膜的EDX表;图23是比较例7中制造的薄膜的SEM图像;图24是比较例7中制造的薄膜的EDX表;图25是示出了测试例1中使用实施例37的薄膜制造的电池的性能的图;图26是示出了测试例1中使用实施例48的薄膜制造的电池的性能的图;以及图27是示出了测试例1中使用比较例7的薄膜制造的电池的性能的图。最佳实施方案现在,将参照以下实施例更详细地描述本发明。提供这些实施例仅仅用于说明本发明,而不应被解释为限制本发明的范围和精神。<实施例1>将含有18mmolCuCl2和10mmolSnCl2的四甘醇混合溶液缓慢地滴加到含有150mmolNaBH4的三甘醇混合溶液中,并使混合物在搅拌下反应3小时,然后纯化以制备包含Cu6Sn5和富Cu的Cu-Sn(Cn41Sn11)的混合物的Cu-Sn双金属金属纳米颗粒。将在50ml水中的5mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,随后搅拌1小时。然后,将在70ml蒸馏水中的10mmolNa2S的溶液滴加到搅拌的溶液中1小时,并使混合物反应3小时以制备包含由Cu6Sn5、Cu41Sn11相和ZnS相构成的聚集相复合体以及具有由Cu-Sn核和ZnS壳构成的结构的纳米颗粒的前体。所形成的前体的扫描电子显微镜(SEM)图像和XRD图分别示于图1和2中。从图1和图2可以看出,作为XRD分析的结果,颗粒以包含Cu6Sn5晶相和富Cu的Cu-Sn晶相的混合物的Cu-Sn双金属相与ZnS晶相的组合形式存在,或者颗粒以包含均匀分散的Cu-Sn和ZnS相的聚集相复合体,或者包括涂覆有ZnS的Cu-Sn的核-壳结构纳米颗粒的形式存在。<实施例2>将含有15mmolCuCl2和10mmolSnCl2的水溶液在50℃下缓慢滴加到150mmolNaBH4的蒸馏水溶液中,并使混合物在搅拌下反应3小时以制备包含Cu6Sn5和富Cu的Cu-Sn(例如Cu3Sn、Cu10Sn3或Cu41Sn11)的混合物的Cu-Sn双金属纳米颗粒。将在50ml蒸馏水中的11mmol乙酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,随后搅拌30分钟。然后,将在100ml蒸馏水中的20mmolNa2S的溶液一次性添加到搅拌的溶液中,并使混合物反应3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例3>将含有20mmolCuCl2和10mmolSnCl2的混合溶液在80℃下滴加到含有150mmolNaBH4的DMSO溶液中1小时,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备包含Cu6.26Sn5和Cu10Sn3的混合相的Cu-Sn双金属纳米颗粒。将在50ml乙醇中的1g聚乙烯吡咯烷酮的溶液添加到在乙醇中的Cu-Sn双金属纳米颗粒的分散体中,然后搅拌1小时。将在100ml乙醇中的12mmol乙酸锌的溶液添加到搅拌的混合物中,随后进一步搅拌1小时。将在50ml乙醇中的12mmol硫脲的溶液缓慢滴加到搅拌的混合物中1小时,使所得混合物加热至50℃以制备包含Cu-Sn双金属颗粒和ZnS相的核-壳结构纳米颗粒。所形成的前体的透射电子显微镜(TEM)图像和其TEM分析结果示于图3和4中。<实施例4>将含有18mmolCuCl2、10mmolSnCl2和50mmol柠檬酸三钠的混合水溶液缓慢滴加到含有120mmolNaBH4的水溶液中1小时,使混合物在搅拌下反应24小时,通过离心纯化所形成的颗粒以制备包含Cu6Sn5和Cu41Sn11的混合物的Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散在100ml蒸馏水中后,将含有11mmol乙酸锌的水溶液和含有12mmolNaHSe的水溶液依次滴加到分散体中以制备包含Cu-Sn相和ZnSe相的聚集相复合体。<实施例5>在1小时内将含有20mmolCuCl2和10mmolSnCl2的混合溶液滴加到含有80mmolNaBH4的DMSO溶液中,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散在200ml蒸馏水中后,将在100ml蒸馏水中的12mmolZnCl2和0.5gPVP的溶液滴加到分散体中。将Na2S的蒸馏水溶液缓慢滴加到所得混合物溶液中,随后搅拌5小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例6>将含有16mmolCuCl和10mmolSnCl4的混合水溶液滴加到含有120mmolNaBH4的水溶液中,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到丁氧基乙醇中后,将分别以11mmol和22mmol的浓度溶解的乙酸锌和硫脲的溶液添加到分散体中,并且使混合物在150℃下反应3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例7>在1小时内将含有16mmolCuCl2和10mmolSnCl4的混合水溶液滴加到含有120mmolNaBH4的水溶液中,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到乙醇中后,将在50ml乙醇中分别以11mmol、10mmol和22mmol的浓度溶解的乙酸锌、乙二硫醇和硫代乙酰胺的溶液添加到分散体中,并使混合物在150℃下反应3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例8>在1小时内将含有18mmolCuCl2和10mmolSnCl2的混合水溶液滴加到含有120mmolNaBH4的二甲基甲酰胺溶液中,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到异丙醇中后,将分别以10mmol和15mmol的浓度溶解的ZnCl2和硫代乙酰胺的溶液添加到分散体中,并使混合物在80℃下反应3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例9>在60℃下,将含有14mmolCu(NO3)2和10mmolSnCl4·5H2O的DMSO溶液滴加到含有80mmolNaBH4的DMSO溶液中1小时,使混合物在搅拌下反应6小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将15mmol乙基黄原酸锌溶解于分散体中,随后加热至78℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例10>在90℃下,将含有14mmolCu(NO3)2和10mmolSnCl4·5H2O的混合溶液滴加到含有80mmolNaBH4的NMP溶液中1小时,使混合物在搅拌下反应6小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例11>在室温下将含有17mmolCuCl2和10mmolSnCl4·5H2O的混合溶液滴加到80mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。所形成的颗粒的扫描电子显微镜(SEM)图像和XRD图示于图5和6中。此外,通过TEM分析的这些颗粒的形状和使用线扫描的其组成分析结果示于图7和8中。从图5和图6的XRD分析结果可以看出,颗粒以包含Cu6Sn5晶相和富Cu的Cu-Sn晶相的混合物的Cu-Sn双金属相与ZnS晶相的组合形式存在,或者以包含均匀分布的Cu-Sn和ZnS相的聚集相复合体或包含Cu-Sn和ZnS的核-壳结构纳米颗粒的形式存在。<实施例12>在室温下,将含有17mmolCu(NO3)2和10mmolSnCl4·5H2O的混合溶液滴加到80mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例13>在室温下,将含有17mmolCuCl2·2H2O和10mmolSnCl4·5H2O的混合溶液滴加到270mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解10mmol乙酸锌和20mmol硫代乙酰胺,随后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例14>在室温下,将含有17mmolCuCl2·2H2O和10mmolSnCl4·5H2O的混合溶液滴加到270mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将10mmol乙酸锌、20mmol硫代乙酰胺和10mmol半胱胺溶于该分散体中,随后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例15>在室温下,将含有17mmolCuCl2·2H2O和10mmolSnCl4·5H2O的混合溶液滴加到270mmolNaBH4和27mmol巯基乙醇的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将10mmol乙酸锌、20mmol硫代乙酰胺和10mmol巯基乙醇溶于该分散体中,然后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例16>在室温下,滴加含有280mmolNaBH4、18mmolCu(NO3)2、10mmolSnCl2和28mmol柠檬酸三钠的混合水溶液1小时,使混合物在搅拌下反应24小时,通过离心纯化所形成的颗粒以制备包含Cu6Sn5和Cu41Sn11的混合物的Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解10mmol乙酸锌、20mmol硫代乙酰胺和10mmol巯基乙醇,随后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例17>在室温下,将含有17mmolCuCl2·2H2O和10mmolSnCl4·5H2O的混合溶液滴加到270mmolNaBH4、27mmol半胱胺盐酸盐和27mmolNaOH的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL的蒸馏水中后,将10mmol乙酸锌和20mmol硫代乙酰胺溶于该分散体中,随后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例18>在室温下,将含有17mmolCuCl2·2H2O和10mmolSnCl1·5H2O的混合溶液滴加到270mmolNaBH4和27mmol的半胱胺盐酸盐的蒸馏水溶液中0.5小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL的蒸馏水中后,将10mmol乙酸锌、20mmol硫代乙酰胺和5mLNH4OH溶于该分散体中,随后加热至50℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例19>在室温下,将含有17mmolCuCl2·2H2O、10mmolSnCl2和28mmol柠檬酸三钠的混合溶液滴加到300mmolNaBH4和27mmol半胱胺盐酸盐的蒸馏水溶液中1小时,在搅拌下反应4小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将10mmol乙酸锌、20mmol硫代乙酰胺和10mmol巯基乙醇溶于该分散体中,然后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例20>在室温下,将含有17mmolCuCl2·2H2O、10mmolSnCl2·5H2O和28mmol柠檬酸三钠的混合溶液滴加到300mmolNaBH4和27mmol半胱胺盐酸盐的蒸馏水溶液中1小时,使混合物在搅拌下反应4小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将10mmol乙酸锌、20mmol硫代乙酰胺和10mmol半胱胺溶于该分散体中,随后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例21>在室温下,将含有17mmolCuCl2·2H2O、10mmolSnCl2和28mmol柠檬酸三钠的混合溶液滴加到300mmolNaBH4和27mmol半胱胺盐酸盐的蒸馏水溶液中1小时,使混合物在搅拌下反应4小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将10mmol乙酸锌、20mmol硫代乙酰胺和5mmol抗坏血酸溶于该分散体中,随后加热至70℃并搅拌3小时以制备包含Cu-Sn相和ZnS相的聚集相复合体。<实施例22>在60℃下,将含有14mmolCu(NO3)2和10mmolSnCl4·5H2O的DMSO溶液滴加到含有80mmolNaBH4的DMSO溶液中1小时,使混合物在搅拌下反应6小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时。洗涤后,将残余物分散到100mL乙醇中,将分散体滴加到50mL乙醇中的3mmolCuCl2的溶液中,并使混合物搅拌12小时以制备包含Cu-Sn相和ZnS-CuS相的聚集相复合体。所形成的颗粒的线扫描结果、扫描电子显微镜(SEM)图像和XRD图示于图9至11中。由线扫描分析结果可以看出,所述颗粒在壳部分富含Cu组分。由XRD分析结果,颗粒以包含Cu6Sn5晶相和富Cu的Cu-Sn晶相的混合物的Cu-Sn双金属相与ZnS-CuS晶相的组合的形式存在,或以包含均匀分布的Cu-Sn和ZnS-CuS相的聚集相复合体,或者以包含涂覆有ZnS和CuS的Cu-Sn的核-壳结构纳米颗粒的形式存在。<实施例23>在90℃下,将含有14mmolCu(NO3)2和10mmolSnCI4·5H2O的混合溶液滴加到含有80mmolNaBH4的NMP溶液中1小时,使混合物在搅拌下反应6小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时。洗涤后,将残余物分散在100mL乙醇中,将分散体滴加到50mL乙醇中的3mmolCuCl2的溶液中,并使混合物搅拌12小时以制备包含Cu-Sn相和ZnS-CuS相的聚集相复合体。<实施例24>在室温下,将含有17mmolCuCl2和10mmolSnCl4·5H2O的混合溶液滴加到80mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时。洗涤后,将残余物分散在100mL乙醇中,将分散体滴加到50mL乙醇中的3mmolCuCl2的溶液中,并使混合物搅拌12小时以制备包含Cu-Sn相和ZnS-CuS相的聚集相复合体。所形成的颗粒的扫描电子显微镜(SEM)图像和XRD图示于图12和13中。<实施例25>在室温下,将含有17mmolCu(NO3)2和10mmolSnCl4·5H2O的混合溶液滴加到80mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,在其中溶解15mmol乙基黄原酸锌,随后加热至78℃并搅拌3小时。洗涤后,将残余物分散在100mL乙醇中,将分散体滴加到50mL乙醇中的3mmolCuCl2溶液中,并使混合物搅拌12小时以制备包含Cu-Sn相和ZnS-CuS相的聚集相复合体。<实施例26>在室温下,将含有17mmolCu(NO3)2和10mmolSnCl4·5H2O的混合溶液滴加到80mmolNaBH4和27mmol半胱胺的蒸馏水溶液中1小时,使混合物在搅拌下反应5小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液滴加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,使所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,并使所得混合物在25℃下反应以制备包含具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例27>将含有18mmolCuCl2和10mmolSnCl2的四甘醇混合溶液缓慢滴加到含有150mmolNaBH4的三甘醇混合溶液中,并使混合物在搅拌下反应3小时并纯化以制备包含Cu6Sn5和富Cu的Cu-Sn(Cu41Sn11)的混合物的Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,使所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,并使所得混合物在25℃下反应以制备包含具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例28>在50℃下,将含有15mmolCuCl2和10mmolSnCl2的水溶液缓慢滴加到150mmolNaBH4的蒸馏水溶液中,并使混合物在搅拌下反应1小时并纯化以制备包含Cu6Sn5和富Cu的Cu-Sn(例如Cu3Sn、Cu10Sn3或Cu41Sn11)的混合物的Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,使所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,并使所得混合物在25℃下反应以制备包含具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例29>在80℃下,将含有20mmolCuCl2和10mmolSnCl2的混合溶液滴加到含有150mmolNaBH4的DMSO溶液中1小时,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备包含Cu6.26Sn5和Cu10Sn3的混合相的Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,将所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,使所得混合物在25℃下反应以制备包含具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例30>将含有18mmolCuCl2、10mmolSnCl2和50mmol柠檬酸三钠的混合水溶液滴加到含有120mmolNaBH4的水溶液中1小时,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备包含Cu6Sn5和Cu41Sn11的混合物的Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,将所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,使所得混合物在25℃下反应以制备包含具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例31>将含有16mmolCuCl2和10mmolSnCl4的混合水溶液滴加到含有120mmolNaBH4的水溶液中1小时,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,将所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,使所得混合物在25℃下反应以制备包含具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例32>将含有16mmolCuCl2和10mmolSnCl4的混合水溶液滴加到含有120mmolNaBH4的水溶液中1小时,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。将在50ml水中的15mmol硝酸锌的溶液添加到Cu-Sn双金属纳米颗粒的分散体中,使混合物搅拌1小时,将在70ml蒸馏水中的15mmolNa2S的溶液滴加到反应混合物中1小时,将所得混合物反应3小时,再向反应混合物中添加3mmolCuCl2,使所得混合物在25℃下反应以制备包括具有由Cu-Sn核和ZnS-CuS壳构成的结构的纳米颗粒的前体。<实施例33>将含有18mmolCuCl2和10mmolSnCl2的混合水溶液滴加到含有120mmolNaBH4的二甲基甲酰胺溶液中1小时,使混合物在搅拌下反应24小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到异丙醇中后,将10mmolZnCI2和15mmol硫代乙酰胺的溶液添加到分散体中,使混合物在80℃下反应3小时,再次向其中添加3mmolCuCl2并使所得混合物在25℃下反应以制备包含Cu-Sn相和ZnS-CuS相的聚集相复合体。<实施例34>在室温下,将含有17mmolCuCl2·2H2O、10mmolSnCl2和28mmol柠檬酸三钠的混合溶液滴加到300mmolNaBH4和27mmol半胱胺盐酸盐的蒸馏水溶液中1小时,使混合物在搅拌下反应4小时,并通过离心纯化所形成的颗粒以制备Cu-Sn双金属纳米颗粒。在将Cu-Sn双金属纳米颗粒分散到300mL乙醇中后,将10mmol乙酸锌、20mmol硫代乙酰胺和10mmol巯基乙醇溶于该分散体中,使混合物在80℃下反应3小时,再向其中添加3mmolCuCl2,并使所得混合物在25℃下反应以制备含有Cu-Sn相和ZnS-CuS相的聚集相复合体。<比较例1>将5mmol硝酸锌水溶液和10mmolNa2S各自溶于100ml的蒸馏水中,随后混合。然后,使混合物在室温下反应5小时,并通过离心纯化所形成的颗粒以制备ZnS纳米颗粒。<比较例2>将5mmol氯化铜水溶液和10mmolNa2S各自溶于100ml蒸馏水中,随后混合。然后,使混合物加热至50℃并反应2小时,通过离心纯化所形成的颗粒以制备CuS纳米颗粒。<比较例3>将5mmol氯化锡水溶液和10mmolNa2S各自溶于100ml的蒸馏水中,随后混合。然后,使混合物加热至50℃并反应2小时,通过离心纯化所形成的颗粒以制备SnS纳米颗粒。<比较例4>使100ml(5mmol)氯化锌水溶液与100ml(10mmol)NaHSe水溶液混合,然后在室温下反应5小时。通过离心纯化所形成的颗粒以制备ZnSe纳米颗粒。<实施例35>薄膜的制造将实施例1中制造的Cu-Sn/ZnS前体添加到包含乙醇、乙二醇单甲醚、乙酰丙酮,丙二醇丙醚、环己酮、乙醇胺、1,2-丙二醇、二乙二醇单乙醚、甘油和十二烷基硫酸钠的混合溶剂中,随后以21%的浓度分散以制备墨。将所得墨涂覆至已涂覆于玻璃上的Mo薄膜上并在200℃下干燥。在550℃下在Se的存在下对薄膜进行热处理以得到CZTS薄膜。所得薄膜的截面形状和XRD相示于图14和15中。如从图14和15可以看出,根据本发明的薄膜具有均匀的组成和高密度并包括良好生长的晶粒。<实施例36>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例2中制造的前体。<实施例37>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例3中制造的前体。所获得的薄膜的截面形状的SEM图像示于图16。从图16可以看出,根据本发明的薄膜具有高密度并且包括良好生长的晶粒。<实施例38>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例4中制造的前体。<实施例39>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例5中制造的前体。<实施例40>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例6中制造的前体。<实施例41>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例7中制造的前体。<实施例42>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例8中制造的前体。<实施例43>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例9中制造的前体。所获得的薄膜的截面形状的SEM图像和通过XRD图组成分析结果示于图17和18中。如从图17中可以看出,根据本发明的薄膜具有高密度并且包括良好生长的晶粒。<实施例44>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例10中制造的前体。<实施例45>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例11中制造的前体。<实施例46>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例12中制造的前体。<实施例47>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例22中制造的前体。所获得的薄膜的截面形状的SEM图像和XRD相示于图19和20中。<实施例48>薄膜的制造以与实施例35相同的方式获得CZTS薄膜,不同之处在于使用实施例24中制造的前体。所获得的薄膜的截面形状的SEM图像和EDX结果示于图21和22中。<比较例5>薄膜的制造将Cu-Sn金属纳米颗粒和比较例1中制造的ZnS纳米颗粒以满足Cu/(Zn+Sn)=0.9和Zn/Sn=1.2的比例进行混合,将混合物添加到含有乙醇、乙二醇单甲醚、乙酰丙酮、丙二醇丙基醚、环己酮、乙醇胺、1,2-丙二醇、二乙二醇单乙基醚、甘油和十二烷基硫酸钠的混合溶剂中,然后以21%的浓度分散以制备墨。将所获得的墨涂覆至已涂覆于玻璃上的Mo薄膜上,并在200℃下干燥。在Se的存在下,在550℃下对薄膜进行热处理以获得CZTS薄膜。<比较例6>薄膜的制造将Cu-Sn金属纳米颗粒和比较例4中制造的ZnSe纳米颗粒以满足Cu/(Zn+Sn)=0.8和Zn/Sn=1.1的比例进行混合,将混合物添加到含有乙醇、乙二醇单甲醚、乙酰丙酮、丙二醇丙基醚、环己酮、乙醇胺、1,2-丙二醇、二乙二醇单乙基醚、甘油和十二烷基硫酸钠的混合溶剂中,然后以21%的浓度分散以制备墨。将所获得的墨涂覆至已涂覆于玻璃上的Mo薄膜上并在200℃下干燥。在Se的存在下,在550℃下对薄膜进行热处理以获得CZTS薄膜。<比较例7>薄膜的制造将比较例1至3中制造的ZnS纳米颗粒、CuS纳米颗粒和SnS纳米颗粒以满足Cu/(Zn+Sn)=0.9和Zn/Sn=1.2的比例进行混合,将混合物添加到含有乙醇、乙二醇单甲醚、乙酰丙酮、丙二醇丙醚、环己酮、乙醇胺、1,2-丙二醇、二乙二醇单乙醚、甘油和十二烷基硫酸钠的混合溶剂中,然后以21%的浓度分散以制备墨。将所获得的墨涂覆至已涂覆于玻璃上的Mo薄膜上并在200℃下干燥。在Se的存在下,在550℃下对薄膜进行热处理以获得CZTS薄膜。所获得的薄膜的截面形状的SEM图像和EDX结果示于图23和24中。<测试例1>通过CBD在实施例35至37以及44至48和比较例5至7中制造的各CZTS薄膜上形成CdS缓冲层,通过溅射在其上依次沉积ZnO和Al:ZnO,并且通过丝网印刷在其上层合Ag电极以制造电池。电池的特性示于表1中。此外,从使用实施例37和48的薄膜的电池的特性获得的图和从比较例7获得的IV特性图示于图25、26和27中。表1Jsc(mA/cm2)Voc(V)FF(%)光电效率(%)实施例3527.370.4142.74.8实施例3624.460.3440.693.4实施例3731.830.3735.444.2实施例4427.870.3335.643.3实施例4528.110.3338.903.6实施例4631.670.3333.983.5实施例4729.50.3143.914.0实施例4833.830.3544.085.3比较例518.90.2033.41.3比较例612.70.1536.10.7比较例719.60.2328.401.3图25至27和表1中所示的确定太阳能电池效率的参数Jsc是指电流密度,Voc是指在零输出电流下测量的开路电压,光电效率是指电池功率相对于入射到太阳能电池板上的能量量的比率,以及填充因子(FF)是指通过用在最大功率下的电流密度和电压的乘积获得的值除以Voc和Jsc的乘积而计算的值。此外,Vmp是指最大功率点的电压,Jmp是最大功率点的电流。从图25至27和表1可以看出,与通过分别制备金属纳米颗粒或金属硫属化物、然后混合制造的比较例5至7的薄膜相比,使用本发明制造的前体的实施例35至37和44至48的CZTS薄膜表现出高的电流密度和电压,因此具有优异的光电效率。此外,即使对于具有相同核-壳结构的前体,与使用在壳部分中不包含Cu的前体制造的实施例35至37和44至46的CZTS薄膜相比,使用在壳部分中包含Cu的前体制造的实施例47和48的CZTS薄膜特别地表现出改善的FF,因此必须出优异的光电效率。尽管出于说明的目的公开了本发明的优选实施方案,但是本领域技术人员将理解,在不脱离如所附权利要求中公开的本发明的范围和精神的情况下,可以进行各种修改、添加和替换。工业实用性从前述可以明显看出,根据本发明的用于制备光吸收层的前体包括:(a)聚集相复合体,其包括包含铜(Cu)-锡(Sn)双金属的第一相和包含包含锌(Zn)硫属化物的第二相,或者包括包含铜(Cu)-锡(Sn)双金属的第一相、包含含锌(Zn)硫属化物的第二相和包含含(Cu)硫属化物的第三相;或者(b)核-壳结构纳米颗粒,其包括包含铜(Cu)-锡(Sn)双金属纳米颗粒的核和包含含锌(Zn)硫属化物的壳或含锌(Zn)硫属化物和含铜(Cu)硫属化物的壳;或者(c)其混合物。当使用所述前体制造薄膜时,可以由已均匀混合的元素合成前体,使得薄膜可具有整个更均匀的组成、可以使次生相的形成最小化、由于在通过由双金属构成的第一相或核的热处理期间添加的另外的第VI族元素可以基于增加的前体体积生长高密度的光吸收层,并且可制造出具有增加的第VI族元素含量的高品质的最终薄膜,原因是前体包括包含S或Se的第二相或壳。特别地,核-壳结构纳米颗粒具有这样的结构,其中包含铜(Cu)-锡(Sn)双金属的核被包含含锌(Zn)硫属化物和含铜(Cu)硫属化物的壳所保护,从而有利地使构成核的Cu-Sn双金属颗粒表面上的氧化物的形成最小化以提高反应性。特别地,基于全部颗粒中相同量的Cu,与仅包含含锌硫属化物的颗粒相比,通过用Cu置换含锌硫属化物颗粒获得的包含含锌硫属化物和含铜硫属化物二者的颗粒可具有包含在核中的低Cu/Sn比,从而改善颗粒中的铜元素的均匀性,抑制热处理时次生相的形成并改善薄膜品质。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1