用于锂/硫电池的硫化锂‑氧化石墨烯复合材料的制作方法
对相关申请的交叉引用
本申请依照35u.s.c.§119要求2014年8月12日提交的临时申请号62/036,390的优先权,该临时申请的公开内容以引用的方式并入本文。
本公开提供了用于生成硫化锂氧化石墨烯复合材料的方法。
背景技术:
常规的可再充电的锂离子电池没有满足所有挑战来满足市场需求。举例来说,开发先进的电动车辆需要高达400wh/kg的高比能量,但是当前的锂离子电池仅可以提供约200wh/kg(在理论上是580wh/kg)。
技术实现要素:
本公开提供了一种包含纳米颗粒球体的组合物,所述纳米颗粒球体具有嵌入有氧化石墨烯的硫化锂(li2s/go)。在一个实施方案中,所述组合物进一步包含围绕所述li2s/go的保形碳涂层。因此,在一个实施方案中,本公开提供了一种组合物,所述组合物包含硫化锂氧化石墨烯核心和保形碳涂层。在前述实施方案中任一个的另一个实施方案中,所述硫化锂核心包含嵌入的氧化石墨烯。在又另一个或替代的实施方案中,所述氧化石墨烯和硫化锂是不均匀分散的。在再另一个实施方案中,所述氧化石墨烯和硫化锂是基本上均匀分散的。在前述实施方案中任一个的另一个实施方案中,所述硫化锂氧化石墨烯核心具有约200nm至1400nm的宽度或直径。在前述实施方案中任一个的又另一个实施方案中,所述硫化锂氧化石墨烯核心具有约800nm的平均宽度或直径。在再另一个实施方案中,所述保形碳涂层包含围绕所述硫化锂氧化石墨烯核心的壳层。在另一个实施方案中,所述保形碳涂层约5nm-45nm厚。在再另一个实施方案中,所述保形碳涂层的平均厚度是约25nm。
本公开还提供了一种合成如本文和上文所述的硫化锂-氧化石墨烯复合材料的方法。所述方法包括将在非极性有机溶剂中包含元素硫的第一溶液添加到在分散溶剂中包含分散的氧化石墨烯的第二溶液中并且添加强锂基还原剂以制成反应混合物;以及通过将所述反应混合物在高温加热2分钟至30分钟来从所述反应混合物中沉淀所述li2s-go材料。在另一个实施方案中,所述方法进一步包括从所述反应混合物中收集所述沉淀的li2s-go材料,洗涤所述li2s-go材料以及干燥所述li2s-go材料。在再另一个实施方案中,所述非极性有机溶剂选自戊烷、环戊烷、己烷、环己烷、辛烷、苯、甲苯、氯仿、四氯乙烯、二甲苯、1,2-二氯苯、1,4-二
本公开还提供了一种由如上文所述的方法制备的li2s/go材料。本公开还提供了一种由上文所述的方法制备的li2s/go@c材料。
本公开还提供了一种电极,所述电极包含本公开的li2s/go材料。
本公开提供了一种锂/硫电池,所述锂/硫电池包括本公开的包含li2s/go材料的电极。
本公开还提供了一种电极,所述电极包含本公开的li2s/go@c材料。
本公开还提供了一种锂/硫电池,所述锂/硫电池包括包含li2s/go@c材料的电极。
本公开提供了一种合成硫化锂-氧化石墨烯复合材料的方法,所述方法包括:将在非极性有机溶剂中包含元素硫的第一溶液添加到包含分散的氧化石墨烯的第二溶液中并且添加强锂基还原剂以制成反应混合物;通过将所述反应混合物在高温加热2分钟至30分钟来从所述反应混合物中沉淀所述li2s-go材料。在一个实施方案中,所述方法进一步包括:从所述反应混合物中收集所述沉淀的li2s-go材料;洗涤所述li2s-go材料;以及干燥所述li2s-go材料。在前述实施方案中任一个的又另一个实施方案中,所述非极性有机溶剂选自戊烷、环戊烷、己烷、环己烷、苯、甲苯、氯仿、1,4-二
本公开还提供了一种由前述实施方案中的任一个所述的方法制备的复合li2s-go材料。
在另一个实施方案中,本公开提供了一种电极,所述电极包含本公开的li2s-go材料。
本公开还提供了一种锂/硫电池,所述锂/硫电池包括本公开的电极。
附图说明
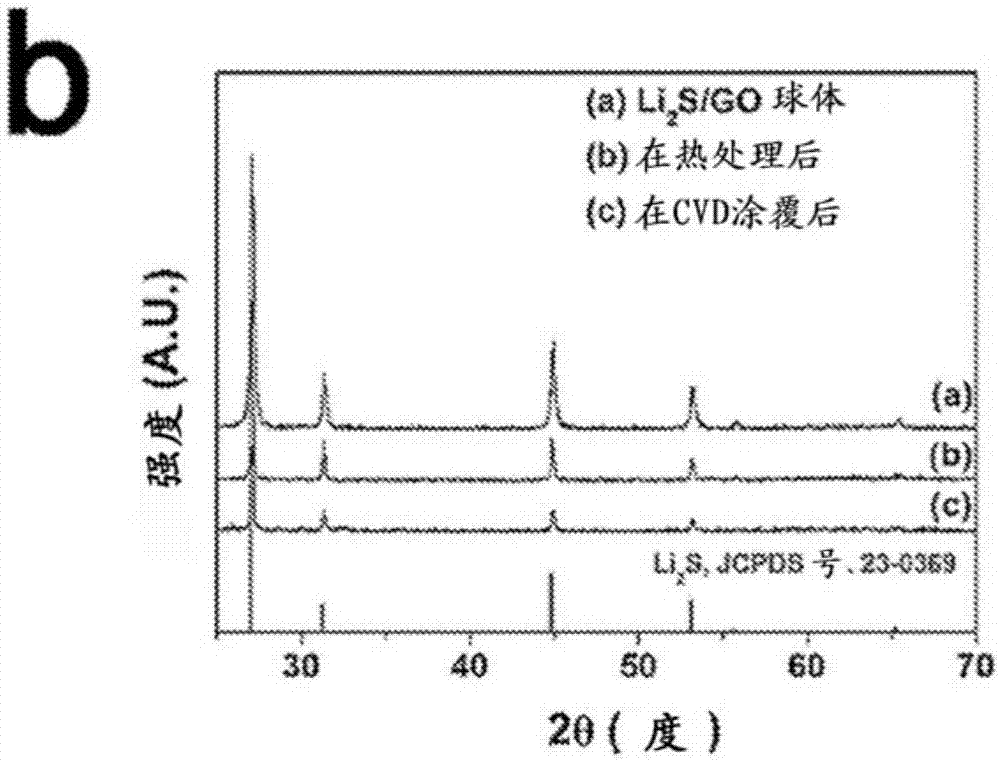
图1a-e示出了li2s/go@c纳米球的合成方案和表征。(a)本公开的合成方法的示意图;在每一个步骤时(b)xrd图和(c)拉曼光谱(ramanspectra)。(d)示意性地描绘了本公开的li2s/go@c纳米球。(e)描绘了li2s/go核心材料。
图2a-e:(a)合成态li2s/go、(b)热处理过的li2s/go、以及(c)li2s/go@c纳米球的sem图像。(d)基于能量过滤式透射电子显微镜(eftem,插图:li2s/go@c纳米球的零损失图像)的li2s/go@c纳米球的元素分布分析。(e)中空碳纳米球的tem图像,所述中空碳纳米球包括通过从li2s/go@c纳米球中去除li2s所获得的于自身结构的go。
图3a-c示出了合成的li2s、li2s/go、li2s/go@c-nr、以及li2s/go@c电极的电化学测试结果。(a)在0.2c倍率下电极的电压曲线。(b)在0.2c下电极的循环性能的比较。(c)针对以0.2c进行50次循环的电极的测试时间与放电容量的关系图。
图4示出了使用常规的cvd方法和使用旋转炉的cvd的碳沉积工艺的示意图。
图5a-e示出了li2s/go@c电极的电化学性能。以各种倍率循环的电极的(a)电压曲线和(b)循环性能。(c)以2.0c放电和以1.0c充电的电极的电压曲线。(d)在数百次循环之后在0.05c下电极的电压曲线。(e)针对1500次循环的电极的长期循环性能。
图6示出了以各种c倍率循环的li2s/go@c电极的库仑效率。
图7示出了对应于图5c中所示的电压曲线的li2s/go@c电极的微分电容图(dcp)。
具体实施方式
除非上下文另外明确规定,否则如本文和所附权利要求书中所用的单数形式“a/an(一)”和“所述”包括复数指代对象。因此,举例来说,提到“一种li2s材料”时,包括多种这样的材料,并且提到“所述氧化石墨烯”时,包括提到本领域技术人员已知的一种或多种氧化石墨烯材料和其等同物,诸如此类。
此外,除非另外说明,否则使用“和”意指“和/或”。类似地,“包含(comprise/comprises/comprising)”以及“包括(include/includes/including)”是可互换的并且不意具有限制性。
应当进一步了解的是,在对各种实施方案的说明使用术语“包含”的情况下,本领域技术人员应当了解,在一些特定情况下,可以使用语言“基本上由……组成”或“由……组成”来替代性地描述一个实施方案。
本说明书中所提到的所有公开、专利、以及专利申请均以引用的方式并入本文,其引用的程度就如同各公开、专利、或专利申请被具体地并且单独地指示为以引用的方式并入本文一般。本说明书中所提到的所有公开、专利、和专利申请以及其中所引用的任何参考文献以引用的方式整体并入本文。
除非另外定义,否则本文所用的所有技术术语和科学术语所具有的含义与本领域的普通技术人员通常所了解的含义相同。尽管许多方法和试剂类似于或等同于本文所述的那些,但在本文介绍了示例性方法和材料。
由于当前的锂离子电池的限制,因此研究继续尝试并且提高它们的性能。许多研究人员一直在尝试开发先进的电池系统,如锂/硫电池和氧化还原液流电池。在它们当中,锂/硫电池是代替当前的锂离子电池的强有力的候选者之一,这是因为它具有2680wh/kg的高理论比能量。这一高理论比能量是因为硫阴极的高理论比容量(1675mah/g),这是用于锂离子电池的常规阴极材料的理论比容量的差不多10倍。硫阴极与锂离子的反应如下:
考虑到硫阴极的挑战,完全锂化的硫,即硫化锂(li2s)是一种用于锂/硫(li/s)电池的有吸引力的阴极材料,它具有1166mahg-1的理论比容量。它可以与不同种类的无锂金属材料,如高容量硅阳极配对。此外,与硫相比,li2s具有更高的熔点并且处在最大体积状态,因此可以在更高的温度对li2s材料进行改性并且表面涂层可以是更稳定的。然而,li2s阴极仍存在低电子导电性以及多硫化物在许多电解质中的溶解性的问题。因此,使用包括氧化石墨烯的含碳复合材料、控制粒度以及为li2s活性材料提供保护是要被考虑到的重要的考虑因素。
尽管具有高理论比容量,但是必须克服几个问题,如在循环期间大的体积变化、多硫化物向有机电解质中的溶解以及硫的低导电性。在硫与锂反应(方程式1)期间,发生高达80%的活性材料的体积变化并且这一大的体积变化可能导致电极粉碎。此外,诸如li2s8、li2s6以及li2s4的中间物质可溶于大多数的有机电解质中,这是在循环期间容量衰减的主要原因之一。此外,用作锂/硫电池的阳极材料的锂金属通常在常规的有机液体电解质中在再充电期间形成枝晶,从而导致电池的短路。
常规使用液体电解质,它具有高的对锂多硫化物和硫化物的溶解性。在含有液体电解质的电池中硫的利用率取决于这些硫物质在所述液体电解质中的溶解度。此外,除了在完全充电状态下之外,正极(例如阴极)中的硫可以溶解以形成多硫化物在电解质中的溶液。在放电期间,在正极处多硫化物物质sn2-(n大于4)的浓度一般高于在负极(例如阳极)处的浓度,并且在负极处sn2-(n小于4)的浓度一般高于在正极处的浓度。多硫化物物质的浓度梯度驱动在电极之间固有的多硫化物穿梭。多硫化物穿梭(扩散)在两个电极之间来回运送硫物质,其中硫物质可以始终在电池内迁移。多硫化物穿梭导致不佳的可循环性、高的自放电、以及低的充放电效率。此外,一部分的多硫化物转化成硫化锂(li2s),所述硫化锂可以沉积在负极上。“化学短路”导致活性材料从硫电极损失、含锂负极(即阳极)的腐蚀、以及低的库仑效率。此外,移动的硫物质导致硫在电池中重新分布并且对电池施以差的循环寿命,其中差的循环寿命与电极的微观结构变化直接相关。这一沉积过程在每一次充电/放电循环中发生,并且最终导致硫正极的容量的完全损失。硫化锂的沉积还由于硫化锂的绝缘性质而导致电池内的内阻的增加。由于连续循环中电池电阻的增加,因此充电电压的逐渐增加和放电电压的降低在锂/硫化物(li/s)电池中是常见的现象。因此,能量效率随着循环次数的增加而降低。
li2s阴极具有非常差的电子导电性、多硫化物溶解以及穿梭效应,这导致低的s利用率、低的库仑效率、以及在循环期间快速衰减。因此,还至关重要的是,防止多硫化物溶解到液体电解质中以及为li2s阴极材料提供良好的电通路以实现锂/硫电池的高倍率和长期循环性能。一些最新的研究已经进行来解决这些问题;例如涂有各种材料,如碳(参见例如wo2015103305,其以引用的方式并入本文)、二维层状过渡金属二硫化物、以及导电聚合物的li2s阴极。举例来说,各种方法和组合物提供了被封装在聚合物材料或石墨烯中的li2s。
石墨烯是一种由紧密堆积成二维蜂窝晶格的碳原子构成的含碳材料。本公开的方法和组合物中所用的石墨烯可以是纯的石墨烯或官能化的石墨烯。纯的石墨烯指的是包括碳原子而不含其它官能团的石墨烯。官能化的石墨烯可以包括与石墨烯的碳原子连接的一个或多个官能团。官能化的石墨烯(有时被称为石墨烯衍生物)可以是共价官能化的或非共价官能化的(如由于电价键、氢键、和/或π-π键)。所述一个或多个官能团可以包括例如含氧官能团、含氮官能团、含磷官能团、含硫官能团、含烃官能团、以及含卤素官能团。官能化的石墨烯的一个实例是氧化石墨烯。氧化石墨烯包含含氧官能团。所述含氧官能团可以包括例如羧基、羰基、羟基、酯基、醛基、以及环氧基。可以使用单层石墨烯或可以将多层石墨烯层压在一起并且使用。本公开的石墨烯片可以包含层压在一起的1层-10层石墨烯。
与包含被封装在第二材料中的li2s的其它组合物相对比,本公开提供了一种包含li2s/go的核心材料,其中氧化石墨烯或石墨烯衍生物嵌入li2s颗粒中(例如不是围绕li2s材料,而是在li2s材料中)。举例来说,“嵌入”指的是元素存在于周围物质中而不是存在于周围物质“上”。应当认识到的是,“嵌入”可以指一部分被嵌入,然后被周围物质与嵌入该周围物质中的相似材料隔开(例如周围物质中的补片)。嵌入还指的是材料(例如氧化石墨烯)处于周围物质内部。
本公开提供了制备li2s/go纳米颗粒的组合物、用途以及方法,其中氧化石墨烯或石墨烯衍生物嵌入li2s材料中。举例来说,图1e示出了li2s/go核心10,该核心包含嵌入有氧化石墨烯或石墨烯衍生物140的li2s150。氧化石墨烯或石墨烯衍生物140可以分散于或嵌入li2s材料内。这与li2s由石墨烯封装相反。
li2s/go颗粒可以通过将硫(例如元素硫或其它硫源)在溶剂中与分散的氧化石墨烯混合,继而添加锂基还原剂(例如三乙基硼氢化锂、正丁基锂、以及氢化锂铝)来获得。在一个实施方案中,将硫添加到非极性有机溶剂(例如戊烷、环戊烷、己烷、环己烷、苯、甲苯、氯仿、1,4-二
本领域已知的许多方法可以用于生成本文所公开的li2s材料。在一个具体的实施方案中,本公开的li2s核心材料可以通过使元素硫与强锂基还原剂在许多非水性溶剂(例如甲苯和thf)中进行基于溶液的反应并且收集沉淀物来制备,所述还原剂诸如超氢化物(即li(ch2ch3)3bh)、正丁基锂、或氢化锂铝。在一个实施方案中,所述强锂基还原剂是li(ch2ch3)3)bh。在某个实施方案中,一种合成li2s材料的方法包括:将元素硫溶解在非极性有机溶剂(例如甲苯)中以形成含有硫的溶液;将所述含有硫的溶液添加到分散的氧化石墨烯悬浮液中;添加强锂基还原剂以形成反应混合物;以及通过将所述混合物在高温(例如90℃)加热2分钟-30分钟以蒸发具有良好的对li2s的溶解性的溶剂(例如thf)来从所述反应混合物中沉淀li2s-go材料。在一个具体的实施方案中,将反应物在90℃加热长达2分钟、长达3分钟、长达4分钟、长达5分钟、长达6分钟、长达7分钟、长达8分钟、长达9分钟、长达10分钟、长达11分钟、长达12分钟、长达13分钟、长达14分钟或长达15分钟。在另一个实施方案中,所述非极性有机溶剂选自戊烷、环戊烷、己烷、环己烷、苯、甲苯、氯仿、1,4-二
在另一个具体的实施方案中,将硫粉溶解在甲苯中,继而添加分散于四氢呋喃(thf)中的市售的单层氧化石墨烯(slgo)以制备均匀的s/slgo复合溶液。然后将这一s/slgo复合溶液添加到三乙基硼氢化锂(liet3bh)在thf中的溶液中并且在搅拌下加热以去除thf直到形成稳定的li2s/go球体为止。
可以通过机械搅拌或超声搅拌将石墨烯片或衍生物(例如氧化石墨烯(go))分散于溶剂中以形成分散的悬浮液。所述溶剂应当能够允许石墨烯分散。在一个实施方案中,所述溶剂能够在加热步骤期间完全蒸发。在一个具体的实施方案中,所述溶剂是thf。
可以将硫源溶解在与用于分散石墨烯或氧化石墨烯的溶剂相同或不同的适当的溶剂中。用于本公开的方法和组合物中的硫源可以是例如硫的盐、酸、或氧化物。举例来说,硫源可以是硫代硫酸盐、硫代碳酸盐、亚硫酸盐、金属硫化物(mxsy)、二氧化硫、三氧化硫、硫化氢、硫代硫酸、硫代碳酸、亚硫酸、或其组合。所述硫代硫酸盐可以是硫代硫酸钠、硫代硫酸钾、硫代硫酸锂以及硫代硫酸铵中的至少一种。所述金属硫化物可以是硫化钠、硫化钾、以及硫化锂中的至少一种。
然后可以将所形成的li2s/go颗粒进一步改性(例如封装在聚合物、碳或其它材料中)并且使用。举例来说,本公开提供了一种复合活性材料,所述材料包含具有嵌入的氧化石墨烯(go)的li2s以用于硫阴极中,所述硫阴极克服了当前有关锂/硫电池应用的问题。在这个实施方案中,go不仅用作固定剂以保持s,而且还可以提供循环期间稳定的电通路,从而使得电极的循环性能和倍率性能提高。如所提到的那样,li2s阴极具有高的理论比容量并且它可以与无锂金属阳极配对,所述阳极诸如碳基、硅基以及锡基阳极。此外,li2s(熔点:1372℃)具有比s(熔点:115℃)高得多的熔点并且处在最大体积状态,因此可以容易地在更高的温度下在li2s颗粒的表面上进行改性并且表面涂层可以相对更稳定。
本公开还提供了制备在表面上具有保形碳涂层的li2s/go纳米球(li2s/go@c)的组合物、用途以及方法。使用li2s/go@c提高电池性能的策略如下:(i)所述保形碳涂层不仅通过防止li2s与液体电解质之间的直接接触来阻止多硫化物溶解到电解质中,而且还用作电通路,从而使得电极电阻降低;(ii)亚微米尺寸颗粒的球形可以提供短的固态li扩散途径和循环期间碳壳层的更好的结构稳定性;(iii)在充电期间,在碳壳层内将形成空隙空间,这提供了足够的空间以容纳放电期间高达80%的体积膨胀。因此,可以确保碳壳层的更好的结构稳定性,这是因为碳壳层在循环期间将不需要膨胀;以及(iv)即使一定百分比的碳壳层由于物理缺陷而破裂,所述颗粒中的go也可以由于其s固定性质而用作多硫化物溶解的第二抑制剂。
图1d描绘了li2s/go@c复合材料120的一个具体的实施方案,所述复合材料包含li2s/go核心材料10。“核心材料”是li2s/go基材料(还参见图1e中的10)。如本文所用的术语“复合材料”表示所述核心材料进一步包含一种或多种涂层材料。在一些实施方案中,复合材料120包含li2s/go核心材料10、与核心材料10直接接触并且封装核心材料10的第一涂层30、以及与第一涂层30直接接触并且封装第一涂层30的任选的第二涂层90。在另一个实施方案中,li2s/go核心材料10具有直径d1,其中d1是100nm至1500nm、200nm至1400nm、300nm至1300nm、400nm至1200nm、500nm至1100nm、或约600nm至1μm(应当显而易见的是,本公开涵盖了100nm至1500nm的任何值);平均来说,li2s/go核心材料具有约800nm的平均宽度或直径。在另一个实施方案中,本文所公开的包含li2s/go核心材料10和第一层30的li2s/go@c复合材料具有直径d1+d3,其中d3是1nm至50nm、5nm至45nm、10nm至40nm、15nm至35nm、或20nm至30nm的直径。在一个实施方案中,第一层30具有约25nm的平均厚度(d3)。在又另一个实施方案中,本文所公开的包含li2s/go核心材料10、第一层30以及第二层90的li2s/go@c复合材料具有直径d2。d2可以是102nm至1700nm以及其间的任何数。
在一些实施方案中,阴极包含li2s/go@c复合材料120。包含li2s/go@c复合材料120的阴极适用于电池,如锂/硫(li/s)电池中。在另一个实施方案中,所述阴极包含li2s/go@c,其中所述li2s/go@c具有核心li2s/go10、保形碳层30以及任选的一个或多个另外的导电聚合物层。
在某个实施方案中,li2s/go核心材料10是通过使用本领域已知的标准技术制备的。举例来说,可以通过使元素硫和go与强锂基还原剂进行基于溶液的反应并且收集沉淀物来制备li2s/go核心材料10,所述还原剂诸如超氢化锂(例如li(ch2ch3)3)bh)、正丁基锂、或氢化锂铝。
在某些实施方案中,li2s/go@c复合材料120包含保形碳材料的第一涂层30。可以涂布第一涂层30以使所述涂层均匀地涂覆li2s/go核心材料10或可选择地,涂布所述涂层以使所述涂层不均匀地涂覆li2s/go材料10(即其中所述涂层较厚的部分和其中所述涂层较薄的部分,包括多孔涂层)。或者,可以将第一涂层在li2s/go材料10上图案化,例如通过使用基于平版印刷术的方法。举例来说,可以使用数字平版印刷术(例如参见wang等,nat.matter3:171-176(2004),所述方法并入本文)或软式平版印刷术(例如参见granlund等,adv.mater12:269-272(2000),所述方法并入本文)将第一涂层在li2s/go材料10上图案化。在另一个实施方案中,可以涂布第二涂层90。在一个实施方案中,第二涂层90是多孔电子导电涂层。
在一个具体的实施方案中,第一涂层30包含碳。可以通过使用各种技术将包含碳的第一涂层30涂布到li2s/go核心材料10上。举例来说,在一个实施方案中,可以通过使用化学气相沉积(cvd)工艺将碳基涂层涂布到li2s/go材料10上。在一个替代的实施方案中,可以通过使用碳化工艺将碳基涂层涂布到li2s/go材料10上。举例来说,可以通过制备包含导电碳基聚合物的混合物,将所述混合物涂布到li2s/go材料10上,然后通过热解将所述碳基聚合物碳化来碳涂覆li2s/go材料10。所述碳基前体化合物的热解通常是在非氧环境中进行的,并且通常是在惰性气流,例如像氩气流下进行的。
在某个实施方案中,使用碳化工艺通过使碳基前体化合物热解来在li2s/go材料10上涂覆碳。在热解步骤期间,发生化学和物理重排,常常伴有残余溶剂和副产物物质的排放,然后可以将它们去除。如本公开中所用的术语“基于碳化的碳涂层”意指碳涂层是通过使合适的碳基前体化合物热解成无定形热解碳来产生。可以通过本领域已知的许多方法来将合适的前体碳化合物(例如碳基聚合物)涂布到li2s/go材料上。举例来说,可以将li2s/go材料浸渍或浸泡在包含碳基前体化合物的混合物、溶液、或悬浮液中。或者,可以通过喷涂、分配、旋涂、沉积、印刷等将包含碳基前体化合物的混合物、溶液、或悬浮液涂布到li2s/go材料上。然后可以通过将前体化合物在合适的温度下、在适当的气氛中加热一段合适的时间以使碳基前体化合物经历热分解为碳来将所述碳基前体化合物碳化。
通过碳化产生的碳基第一涂层可以通过使碳基前体化合物在例如坩埚的反应容器中在约300℃至800℃的温度下热解而产生。通常,碳基前体化合物的热解是在至少200℃并且最高700℃的温度下进行最多48小时的时间段,其中一般来说,更高的温度需要更短的处理时间来实现相同的效果。在某个实施方案中,碳基前体化合物的碳化是通过使所述碳前体在至少425℃并且最高600℃的温度下热解最多48小时的时间段来进行的。在不同的实施方案中,热解步骤中所用的温度是200℃、250℃、300℃、350℃、400℃、450℃、500℃、550℃、600℃、650℃、或700℃、或在由前述示例值中的任何两个所界定的温度范围内。对于这些温度中的任一个或其中的范围,处理时间(即在一定温度或在一定的温度范围内处理碳基前体化合物的时间)可以例如精确地是至少或不超过15分钟、30分钟、1小时、2小时、3小时、4小时、5小时、6小时、12小时、18小时、24小时、30小时、36小时、42小时、48小时、或在由前述示例值中的任何两个所界定的时间范围内。产生第一涂层30的碳化可以包括用碳基前体化合物进行的多个重复的热解步骤。在每一个步骤之间,可以将聚集体研磨至基本均匀,继而用额外的碳基前体化合物进一步热解。碳基涂层30的厚度可以通过许多手段来调节,包括(i)使用利用碳基前体化合物的重复的热解步骤;(ii)增加涂布到li2s/go材料上的碳基前体的量;以及(iii)碳基前体化合物的类型。可以通过测量在将涂层涂布到li2s/go材料上之前和之后重量的变化来确定沉积为涂层30的碳的量。
可以用于本文所公开的碳化法中的典型的碳基前体化合物包括碳基聚合物。举例来说,可以使用廉价的碳基聚合物,如聚苯乙烯(ps)、聚丙烯腈(pan)、以及聚甲基丙烯酸甲酯(pmma)。不同于爆炸性气态原料碳源,碳基聚合物操作安全且相对便宜。
在替代的实施方案中,涂层30是通过使用化学气相沉积(cvd)工艺所产生的碳基涂层。cvd是一种用于产生高纯度、高性能固体材料的化学工艺。对于本文所公开的li2s/go@c复合材料120,可以通过将li2s/go核心材料10放置在包含碳基前体化合物,如乙炔的气氛下,并且在一定温度加热以使所述前体化合物热解来使碳基涂层30沉积到li2s/go核心材料10上。在一个具体的实施方案中,可以通过将li2s/go材料转移到手套箱中的封闭炉管中并且以限定的标准立方厘米/分钟(sccm)流速引入惰性气体和碳基前体化合物(例如烃)来使碳基涂层30沉积到li2s/go核心材料10上。在另一个实施方案中,以限定的比率引入sccm流速的惰性气体与碳基前体化合物。在一个具体的实施方案中,以如下sccm流速比引入惰性气体与碳基前体化合物:1:10至10:1、1:9至9:1、1:8至8:1、1:7至7:1、1:6至6:1、1:5至5:1、1:4至4:1、1:3至3:1、或1:2至2:1。举例来说,在一个具体的实施方案中,以70sccm引入氩气,而以10sccm引入乙炔,从而使得sccm流速比为7:1。在另一个实施方案中,cvd处理利用选自甲烷、乙烯、乙炔、苯、二甲苯、一氧化碳、或其组合的碳基前体化合物。根据具体的碳基前体化合物,可以使用质量流量控制器将流速调节到期望值。碳涂层的厚度可以通过调节li2s/go材料暴露于碳基前体化合物的时间长度、改变碳基前体化合物的流速、和/或改变沉积温度来调节。为了实现更均匀的碳涂层,可以定期将li2s/go材料从热中取出并且研磨以破碎任何结块。然后将li2s/go材料与碳基前体化合物一起再加热。沉积的碳的量可以通过li2s/go材料重量的变化来确定。
在一个具体的实施方案中,通过化学气相沉积工艺(cvd)涂布碳涂层。在这个实施方案中,使氩气中的碳前体(例如乙炔)流入旋转炉中并且加热到约700℃。在一个实施方案中,所述工艺是在低氧或无氧、低或无水分的环境中进行的,这是因为li2s对水分敏感。在一个实施方案中,水分和氧气低于0.1ppm。
li2s/go@c复合材料120可以任选地包含另一涂层90,它可以有助于防止多硫化物物质的迁移。第二涂层90可以被涂布以使所述涂层均匀地封装第一涂层30或被涂布以使所述涂层不均匀地涂覆第一涂层30(即其中所述涂层较厚的部分和其中所述涂层较薄的部分)。或者,可以将第二涂层90在第一涂层30上图案化,例如通过使用基于平版印刷术的方法。
在一个实施方案中,第二涂层90是选自以下各项的导电聚合物:聚吡咯(ppy)、聚(3,4-亚乙基二氧噻吩)-聚(苯乙烯磺酸盐)(pedot:pss)、聚苯胺(pani)、聚吡咯(ppy)、聚噻吩(pth)、聚乙二醇、聚苯胺多硫化物(span)、支链淀粉、或其组合。
在一个替代的实施方案中,第二涂层90是导电聚合物,例如聚(3,4-亚乙基二氧噻吩)-聚(苯乙烯磺酸盐)(pedot:pss)。可以通过将所述聚合物涂布到复合材料上并且将所述聚合物干燥以去除水来将导电聚合物第二涂层90涂布到包含li2s/go核心材料10和第一涂层30的复合材料(例如li2s/go@c组合物)上。举例来说,可以将所述聚合物作为胶凝颗粒在水中的分散体、胶凝颗粒在丙二醇中的分散体、或通过将聚合物旋涂到复合材料上来将所述聚合物涂布到复合材料上。包含导电聚合物的第二涂层90的复合材料的导电性可以通过用各种化合物处理所述复合材料来进一步提高,所述化合物诸如乙二醇、二甲亚砜(dmso)、盐、两性离子、共溶剂、酸(例如硫酸)、偕二醇、两亲性氟化合物、或其组合。
值得指出的是,可以使用cvd涂覆工艺,用实验室设计的旋转管式炉来容易地形成保形碳保护层。本文所提供的li2s/go@c阴极具有电化学性能,包括例如在2.0c放电倍率(1.0c=每克li2s1.163a)下延长的循环寿命(1500次循环),具有每克li2s650ma·h(对应于每克s942ma·h)的高初始容量以及在以2.0c放电进行400次循环之后在0.05c下每克li2s699ma·h(每克s1012ma·h);在以各种放电c倍率(2.0c、3.0c、4.0c、以及6.0c放电倍率)进行150次循环之后超过84%的优良容量保持率以及高达99.7%的高库仑效率。
本文所公开的合成方法可以被改动以通过调整反应时间和/或增加或减少添加到反应混合物中的硫溶剂的量来产生具有不同尺寸的颗粒。举例来说,可以通过使用更短的反应时间和减少添加到反应混合物中的硫溶剂的量来产生小尺寸的颗粒;反之亦然,可以通过使用更长的反应时间和增加添加到反应混合物中的硫溶剂的量来产生更大的颗粒。
本公开的li2s/go@c纳米球可以如图1a中所示来合成。简言之,将硫粉溶解在甲苯中,继而添加分散于四氢呋喃(thf)中的市售的单层氧化石墨烯(slgo)以制备均匀的s/slgo复合溶液。将这一s/slgo复合溶液添加到三乙基硼氢化锂(liet3bh)在thf中的溶液中并且在搅拌下加热以去除thf直到形成稳定的li2s/go球体为止。形成li2s的反应化学如下:
s+2liet3bh→li2s+2et3b+h2(方程式2)
在上述化学反应中形成的li2s不均匀沉积在go表面上,继而获得li2s/go纳米球。然后通过例如cvd涂覆处理,使用实验室设计的旋转管式炉涂布保形碳涂层以在li2s/go纳米球的表面上简单地形成保形碳保护层。在cvd工艺期间,旋转卧式炉管以连续地混合li2s/go粉末,并且li2s/go粉末的新鲜表面可以由碳覆盖,从而使得在li2s/go纳米球的表面上形成保形碳涂层。li2s:go:c的重量比是约85:2:13。然而,可以容易地调整所述比率以使得li2s占70%-90%,go占1%-10%并且碳占5%-20%。详细的合成和表征程序在以下实施例中举例说明。如图1b中所示,每一个样品的所有xrd峰均对应于li2s(立方晶系,jcpds号:23-0369),这表明在上述化学反应之后成功地形成li2s并且在随后的热处理和cvd碳涂覆步骤期间没有发生副反应。没有观测到与go相关的xrd峰,这是因为片材沿堆垛方向的排序不佳。然而,合成态li2s/go球体的拉曼光谱(图1c)清楚地证实了go的存在,该拉曼光谱显示在1377cm-1和1588cm-1附近的两个拉曼位移,它们分别对应于碳的d带和g带,存在一些有机残余物(s-o键)。对应于所述有机残余物的拉曼峰由在氩气(ar)气氛下在500℃进行的热处理过程成功去除(标记为li2s/go-500℃)。基于拉曼光谱的变化和粉末的颜色变化(浅灰色→深灰色),有机残余物在热处理过程期间被完全碳化。在涂覆碳之后,在约370cm-1处li2s的拉曼峰几乎消失并且粉末的颜色变得几乎为黑色,这表明由cvd工艺沉积的碳成功地覆盖了li2s的表面并且阻挡了li2s的拉曼信号。
当合成li2s/go纳米球时,嵌入li2s球体中的go的片尺寸、甲苯的量以及go与s之间的重量比可以影响产物的尺寸和形状。因此,可以使用具有500nm-800nm片尺寸的相对少量的slgo(2mg)获得球形li2s/go纳米颗粒。成功地获得了具有约800nm的粒度的球形的li2s/go,如通过图2a中所示的扫描电子显微镜(sem)图像所确认。在分别在500℃和700℃进行的热处理和cvd涂覆工艺之后,由于li2s的高熔点(1372℃),颗粒保持球形,但是在cvd涂覆工艺之后互连,这表明连续的碳壳层形成。热处理过的li2s/go纳米球的能量色散x射线光谱学(eds)结果证实了颗粒上s(对应于基于li2s/go的xrd图的li2s)和c(go或由有机残余物的碳化所获得的碳)的存在。还检测到氧光谱,但是这主要是因为li2s对水分的高敏感性和在将li2s/go纳米球转移到sem室中期间少量lioh的形成。暴露于空气的li2s/go纳米球的xrd图确认了lioh的形成。
本公开进一步提供了本文所公开的li2s/go@c材料或由其制成的复合材料可以用于多种应用中,包括用于锂/硫电池中。与常规的锂/硫电池相比,包含li2s/go@c材料的锂/硫电池具有更高的能量密度、更低的材料成本、以及更好的循环性能。因此,包含li2s/go@c材料的锂/硫电池可以用于车辆、电子器件、电子栅格等中的高性能电池中。在一个具体的实施方案中,一种电池包含本文所公开的li2s/go@c材料或由其制成的复合材料。在另一个实施方案中,所述电池是可再充电的锂/硫电池。在又另一个实施方案中,包含本文所公开的li2s/go@c材料或由其制成的复合材料的电池用于消费类电子器件、电动车辆、或航空航天应用中。
“碳材料”指的是基本上包含碳的材料或物质。碳材料包括超纯以及无定形和结晶碳材料。碳材料的实例包括但不限于活性炭、热解干燥聚合物凝胶、热解聚合物冷冻凝胶、热解聚合物干凝胶、热解聚合物气凝胶、活化干燥聚合物凝胶、活化聚合物冷冻凝胶、活化聚合物干凝胶、活化聚合物气凝胶等。对于所公开的复合材料,“碳材料”在本文还被称为“碳壳层”。
本公开的li2s/go@c纳米球通过将go片嵌入li2s纳米球中并且在表面上沉积保形碳涂层而提供了一种用于锂/硫电池的高倍率和长寿命的阴极材料。由于在初始阶段li2s颗粒相对于s占据它们的最大体积,因此li2s/go纳米球上的碳壳层在循环期间维持良好的结构稳定性。所述碳壳层不仅物理地围绕li2s/go纳米球以防止li2s与电解质之间直接接触,而且还提供了循环期间的导电性。此外,嵌入li2s@c中的go片由于它的s固定性质而用作第二屏障以防止多硫化物溶解。这种li2s/go@c电极表现出在0.2c下每克li2s964ma·h的非常高的初始放电容量(对应于每克s1397ma·h),具有高达99.7%的高库仑效率。以各种c倍率证实高倍率循环性能,例如当电极以2.0c、3.0c、4.0c以及6.0c放电时,在150次循环之后放电容量分别是每克li2s584ma·h、477ma·h、394ma·h以及185ma·h(每克s845ma·h、691ma·h、571ma·h以及269ma·h),具有高达99.7%的优良库仑效率。在长期循环测试中,所述li2s/go@c电极表现出在以2.0c放电进行400次循环之后在0.05c下每克li2s699ma·h(每克s1012ma·h)的比容量,以及对于1500次循环,每次循环仅0.046%的非常低的容量衰减率。通过这些对高硫利用率、高倍率性能、以及长循环寿命的论证,结合简单的制造工艺,所述li2s/go@c阴极可以被认为是用于高级的锂/硫电池中的强有力的候选者。
本文所提供的结果证实li2s@c核壳型颗粒提供高比容量和稳定的循环性能这两者。以下实施例意在说明而不是限制本公开。虽然它们是可能使用典型程序,但是可以可选地使用本领域技术人员已知的其它程序。
实施例
材料制备:使用超声发生器将1ml可商购获得的于thf中的单层氧化石墨烯(slgo)分散体(cheaptube,2mg/ml)超声处理1小时。将3.5ml的甲苯和64mg的s(阿法埃莎公司(alfaaesar),约325目)添加到go分散体中并且搅拌1小时以制备溶解的s-go混合物。然后将这一混合物添加到4.2ml的1.0m于四氢呋喃中的三乙基硼氢化锂(1mliet3bh于thf中,西格玛-奥德里奇公司(sigma-aldrich))中。在室温搅拌2分钟之后,将溶液在连续搅拌下加热到90℃,持续7分钟-8分钟直到形成稳定的li2s/go纳米球为止。在使用离心用thf和己烷洗涤之后,获得了涂覆li2s的go粉末。将所制备的涂覆li2s的go粉末在500℃在ar气氛下加热约30分钟以去除有机残余物并且使用研钵和研杵碾磨。使用离心将li2s-go用thf和己烷洗涤。然后将li2s/go纳米球在500℃在ar气氛下热处理30分钟并且使用研钵和研杵碾磨。通过洗涤方法证实li2s/go纳米球中li2s与go之间的重量比是约98:2。称取li2s-go粉末并且放入蒸馏水和乙醇(1:2比率v/v)的混合物中并且将溶液以5000rpm离心10分钟。收集上清液并且检查上清液的ph值。重复这一程序直到上清液的ph值达到7为止(请注意:当li2s与h2o反应时,形成lioh,这会增加ph值)。一旦上清液的ph值达到7,就收集粉末并且将所述粉末在真空烘箱中在60℃干燥过夜。通过比较原始粉末和洗涤过的粉末的重量来估计li2s与go之间的重量比。为了获得核壳型结构化的li2s/go@c纳米球,使用实验室设计的旋转炉,利用石英管旋转,在700℃进行cvd碳涂覆程序,持续30分钟。分别以100sccm(标准立方厘米/分钟)和10sccm的流速供应ar和乙炔(c2h2,碳前体)混合物。在cvd涂覆工艺之前和之后将样品称重以估计由cvd涂覆工艺所获得的c的量(获得约13%的c)。由于li2s对水分高度敏感,因此在具有低于0.1ppm的水分和氧含量的填充有氩气的手套箱中进行包括炉管组装在内的所有合成过程。为了比较,制备li2s球体(1μm)。简言之,将64mg的硫(阿法埃莎公司,硫粉,约325目,99.5%)溶解在3ml甲苯中,然后将s-甲苯溶液添加到4.2ml于thf中的1.0mliet3bh中。在室温搅拌2分钟之后,将溶液加热到90℃,持续7分钟。收集li2s粉末并且通过离心方法洗涤所述粉末。还使用典型的cvd涂覆方法,在相同的涂覆条件但无石英管旋转的情况下制备li2s/go@c-nr样品。所获得的碳量与li2s/go@c纳米球的碳量相同(约13%)。
表征:在具有低于0.1ppm的水分和氧含量的填充有氩气的手套箱中进行用于表征的样品的所有制备。使用x射线衍射仪(xrd,brukeraxsd8discovergadds微衍射仪),以无空气xrd夹持器保护li2s避免水分来对晶体结构进行研究。在共聚焦后向散射配置中以488nm的激发波长收集样品的拉曼光谱(labram,horibajobinyvonusa公司)。为了将样品保持在惰性气氛中,应用具有恒定氩气流量的linkam池。使用场致发射扫描电子显微镜(fesem,jeoljsm-7500f)来观测粉末样品的形态,使用能量色散x射线光谱学(eds,oxford公司)进行元素分布分析。使用jeoltem仪器(hrtem,jeol2100-f)收集高分辨率透射电子显微镜图像,使用能量过滤式tem(eftem)进行元素分布分析。对于多硫化物溶解测试,将1mg的li2s、li2s/go@c-nr、li2s/go@c球体添加到包含溶解在1.5mlthf/甲苯混合溶液(1:1,v/v)中的7mgs的测试溶液中。
电化学测试:为了制造电极,将60%的li2s、35%的碳材料(包括go、由cvd获得的碳以及作为导电剂的炭黑(superp))以及作为粘合剂的5%的聚乙烯吡咯烷酮(pvp;分子量约1,300k)混合,然后将浆液滴注到用作集电器的碳纤维纸(河森电气有限公司(hesenelectricalltd),hcp010n;0.1mm厚度,75%孔隙率)上并且干燥。电极中li2s的质量负载是0.7mgcm-2-0.9mgcm-2。制备于n-甲基-n-丁基吡咯烷
首先将溶解硫的甲苯和于四氢呋喃(thf)中的氧化石墨烯(go)分散体混合,然后添加到三乙基硼氢化锂(liet3bh)于四氢呋喃(thf)中的溶液中。在通过热处理完全去除thf之后,获得涂有li2s的go的1μm直径的颗粒。
涂有li2s的go的xrd衍射图示于图1中。如所述xrd图中所示,成功地获得了li2s峰(jcpds号:23-0369),而不能观测到slgo的峰,这是因为氧化石墨烯片沿堆垛方向的排序不佳。
图2示出了市售的slgo和涂有li2s的go的sem图像和eds分布分析。图2a中所示的slgo片的大部分粒度小于1μm。在li2s涂覆处理之后,获得1μm的涂有li2s的go球体。为了确认li2s和go的存在,进行eds分布分析。结果显示这些元素是均匀分布的,其分别表明了go和li2s的存在。
为了证实li2s/go@c纳米球的表面上的碳壳层,使用能量过滤式tem(eftem),用对应于lik缘和ck缘的所选能量窗来进行元素分布分析。使用三窗方法(前缘、1、2、以及后缘图像)来扣除背景。如图2d中所示,li2s/go@c纳米球的零损失图像(图2d的插图)中的暗壳层区域与围绕li2s的li区域的c区域一致,这证实了具有约25nm厚的碳壳层的li2s/go@c纳米球的核壳型结构。此外,在从li2s/go@c纳米球去除li2s之后在中空碳壳层的内部观测到非常薄的go片(图2e),并且通过高分辨率tem验证了go的典型石墨结构。这证明在被设计成提高li2s基阴极的电化学性能的合成过程期间,薄层go成功地嵌入li2s颗粒中。
为了验证这些材料改性对电化学性能的影响,制造li2s(1μm)、li2s/go、以及通过典型的cvd涂覆工艺所获得的li2s/go@c(li2s/go@c-nr)和li2s/go@c电极。获得所制备的li2s球体(1μm)和li2s/go@c-nr的xrd图和sem图像并且验证了合成的li2s和li2s/go@c-nr颗粒的晶体结构和形态。为了制造电极,将60%的li2s、35%的碳材料(包括go、通过cvd获得的碳、以及作为导电剂的炭黑)以及作为粘合剂的5%的聚乙烯吡咯烷酮(pvp)在nmp中混合,然后将浆液滴注到碳纤维纸集电器上。电解质由含有1mlitfsi和1重量%的lino3的pyr14tfsi/dol/dme(2:1:1v/v/v)的混合物构成。将lino3添加到电解质中是为了通过钝化li金属表面以对抗多硫化物穿梭来提高库仑效率。将所制造的电极和电解质用于具有li箔作为负极的2325型纽扣电池中。在ar气氛下进行所有的制造程序。在首先以0.05c充电到4.0v以活化li2s之后,将所制造的电池以0.2c倍率在1.5v与2.8v之间的电压范围循环,并且结果示于图3中。
沉积在氧化石墨烯上的li2s成功地显示出提供了比没有go的li2s电极更好的性能和循环稳定性。go不仅用作固定剂以保持s,而且还提供循环期间稳定的电通路,从而使得电极的循环性能和倍率性能提高。
如电压曲线(图3a)中所示,在所有电极当中,li2s/go@c电极表现出最低的充电和放电超电位,甚至低于li2s/go@c-nr电极,这表明通过cvd工艺使用旋转炉获得的碳涂层可以提供良好的电通路以克服li2s和s的绝缘性质。在比较电极的循环性能(图3b)中,li2s电极和li2s/go电极显示出每克li2s约740ma·h的相似的初始比容量。然而,li2s电极在第二次放电时表现出显著的容量降低(每克li2s528ma·h),而li2s/go电极显示出相对平缓的容量损失(每克li2s665ma·h)。这主要是因为go的s固定性质,这可以有助于通过抑制多硫化物溶解到电解质中来使循环性能稳定。相反,两种涂有碳的电极li2s/go@c和li2s/go@c-nr在第一次放电时分别显示出高达每克li2s964ma·h和每克li2s896ma·h(对应于每克s1397ma·h和每克s1298ma·h)的比放电容量,这比无涂层电极的那些要高得多。这两种电极的高s利用率可以归因于碳壳层的存在,所述碳壳层不仅用作保护以通过防止li2s与电解质之间的直接接触来抑制多硫化物溶解到电解质中,而且还提供更好的电通路以弥补li2s和s的绝缘性质。此外,与li2s/go@c-nr电极相比,li2s/go@c电极针对50次循环显示出好得多的可循环性,具有高达99.7%的高库仑效率。这意味着使用旋转炉获得的碳涂层比li2s/go@c-nr电极的碳涂层更加有效抑制循环期间多硫化物溶解到液体电解质中。由多硫化物溶解到液体电解质中所引起的容量衰减可以更清楚地在放电容量与累积测试时间的关系图(图3c)中看到,这是因为从阴极到液体电解质中溶解的多硫化物的量具有时间依赖性。多硫化物溶解得越快,图的斜率越陡。如图3c中所示,li2s/go@c电极在所有电极当中表现出最高的容量保持率,而裸li2s电极在最初30小时内显示出非常陡的斜率。在200小时之后,li2s/go@c电极的比放电容量是每克li2s约760ma·h,但是所有其它电极分别仅显示出每克li2s425ma·h、每克li2s465ma·h、以及每克li2s520ma·h。还值得注意的是,li2s/go电极比裸li2s电极表现出相对更好的容量保持率,这验证了go作为s固定剂的作用。
为了验证li2s/go@c纳米球和li2s/go@c-nr纳米球的碳保护作用,使用由thf(li2s微溶于thf中)和溶解有s的甲苯(s可溶于甲苯中)构成的溶液进行多硫化物溶解测试。如果li2s颗粒没有受到保护并且与测试溶液直接接触,那么多硫化物将形成并且测试溶液的颜色将发生变化。当将裸li2s放入测试溶液中(样品a)时,测试溶液的颜色立即变成淡橙色,这表明裸li2s与溶解的s快速反应并且形成多硫化物。在4小时之后,在样品a中没有保留li2s的固体颗粒,但是碳涂覆的样品的测试溶液没有显示任何颜色变化。在6天之后,li2s/go@c-nr的测试溶液(样品b)表现出橙色,而li2s/go@c的测试溶液(批料c)仍是透明和无色的。在一个月之后,样品c显示出轻微的颜色变化,而样品a和样品b这两者表现出深橙色。这验证了li2s/go@c的保形碳壳层成功地阻止了li2s溶解到测试溶液中。多硫化物溶解测试的结果强烈地支持了图3中所示的电化学测试结果并且表明li2s/go@c电极的优良可循环性是通过使用本文所述的方法所形成的保护性碳层实现的。如图4中所示,在典型的cvd涂覆工艺中,石英管中的碳前体气体主要流过li2s/go纳米球床的顶部,并且由所述前体气体形成的碳主要沉积在li2s/go纳米球的顶层上。因此,可以使用多个c沉积步骤来获得均匀的碳涂层。相反,在cvd涂覆期间,在旋转炉中,li2s/go纳米球经由“上升和下降”过程连续混合。在这一过程期间,碳可以均匀地沉积在li2s/go纳米球上。这一单步保形碳涂覆有助于材料制备过程并且将大幅降低生产成本。
还研究了li2s/go@c电极的高倍率和长期循环性能,并且结果示于图5中。对于高倍率循环测试,使li2s/go@c电极以各种充电c倍率(1.0c、1.5c、2.0c、以及3.0c)和放电c倍率(2.0c、3.0c、4.0c、以及6.0c)恒电流循环150次循环(1.0c=每克li2s1.136a)。如图5a中所示,对应于li2s的形成和分解的放电平台和充电平台分别保持在1.7v-1.9v和2.3v-2.5v的电压范围,尽管放电超电位和充电超电位随着施加电流(c倍率)增加而明显增加。这表明即使当将电极以高达6.0c的放电c倍率恒电流循环时,li2s/go@c电极也能够发生可逆的氧化还原反应。当以2.0c、3.0c、4.0c、以及6.0c将电极放电时,li2s/go@c电极在150次循环之后分别表现出每克li2s584ma·h、477ma·h、394ma·h、以及185ma·h(每克s845ma·h、691ma·h、571ma·h、以及269ma·h)的放电容量,具有超过84%的容量保持率和高达99.7%的非常高的库仑效率(图6)。还以2.0c放电倍率和1.0c充电倍率进行1500次循环来证实li2s/go@c电极的长期循环性能,并且定期以0.05c循环(每200次循环)以检查在低c倍率下的s利用率(图5c-e)。在图5c中,在第一次放电过程期间没有观测到对应于高度可溶的高级多硫化物(li2sn,n≥4)形成的显著的第一平台,并且它显示随第二次放电于约2.3v开始。这很可能表明碳保护层对于第一次循环非常有效地阻止s与电解质之间的直接接触,但是它在循环期间部分降解。对应于图5c中的电压曲线的微分电容图(dcp)(图7)更清楚地显示了这一变化。图5d示出了在第200次、第400次、第600次以及第1000次循环时以0.05c循环的li2s/go@c电极的电压曲线。在200次循环和1000次循环之后分别观测到每克li2s812ma·h(每克s1176ma·h)和441ma·hg-1(每克s640ma·h)的高放电比容量。图5d中充电容量低于放电容量的原因是在以0.05c进行充电过程之前以高放电c倍率(2.0c)循环所引起的有限的li2s形成。在1500次循环期间,li2s/go@c电极表现出每次循环0.046%的非常低的容量衰减率(图5e),库仑效率高于99.5%,这与先前关于锂/硫电池的长期循环性能所报道的结果是有竞争力的。
在另一个实施方案中,可以如下制备本公开的组合物:使用超声发生器分别将7.5ml、10ml以及12.5ml可商购获得的于thf中的单层氧化石墨烯(slgo)分散体(cheaptube,2mg/ml)超声处理1小时。将3ml的甲苯和64mg的s(阿法埃莎公司,约325目)添加到go分散体中并且搅拌1小时以制备溶解有s的go混合物。然后将这些混合物各自添加到4.2ml的1.0m于四氢呋喃中的三乙基硼氢化锂(1m于thf中的liet3bh,西格玛-奥德里奇公司)中并且分别在室温搅拌过夜。在用己烷洗涤之后获得li2s与go之间不同重量比的涂覆li2s的go粉末样品。将所制备的涂覆li2s的go粉末样品在500℃在ar气氛下加热30分钟以去除有机残余物。
在本文已经对多个实施方案作了描述。然而,将了解的是,可以作出各种改动而不脱离本公开的精神和范围。因此,其它实施方案也落入以下权利要求书的范围内。
- 还没有人留言评论。精彩留言会获得点赞!