MACF1基因在成骨细胞中条件性敲除的小鼠模型的构建及应用的制作方法
本发明属于生物医学领域,特别涉及一种macf1基因在成骨细胞中条件性敲除的小鼠模型的构建及应用。
背景技术:
成骨细胞(osteoblast,ob)是骨形成和修复的主要功能细胞。成骨细胞能合成、分泌胶原与糖蛋白形成骨基质,并促进基质矿化形成骨组织;同时,成骨细胞还参与破骨细胞性骨吸收的调控作用,维持骨的代谢平衡。因此,成骨细胞的功能状态与骨骼生长、塑造、再造有着极其密切的联系。任何抑制成骨细胞生成和分化,促进其凋亡的因素均可使骨形成降低,骨再建失衡,导致骨量减少。成骨细胞成骨是一个受多基因调控的复杂过程,目前仍有许多相关机制尚未被阐明。
微管微丝交联因子1(macf1)是一种新型的细胞骨架交联分子。作为骨架交联蛋白超家族成员之一,它既能与微管连接,也能与微丝相连,而且能选择性地限制自身与微丝微管之间的相互作用,在协调细胞的发育及维持组织的完整性中具有重要作用。已有研究发现:macf1在前成骨细胞内广泛表达,并与纤维型肌动蛋白和微管部分共定位,在成骨细胞响应力学环境刺激时,这种共定位分布会发生改变(qianar,etal.[j].bioelectromagnetics,2009oct.30(7):545–555);低表达macf1的前成骨细胞增殖和分化功能受到抑制(hulf,etal.[j].bmbrep.2015oct.48(10):583-588.)。
这些结果证明了macf1参与成骨细胞分化过程,在骨形成过程中可能具有重要作用。目前关于macf1对骨形成抑制作用的研究仅限于细胞水平,常用的模型例如在前成骨细胞系mc3t3-e1中使macf1低表达的稳定细胞株(骞爱荣等.抑制小鼠macf1基因表达的shrna序列及其应用[p].北京:cn104531700a,20150422.)等。然而细胞水平的实验并不能完全反应体内的真实情况,需要进行体内实验验证。因此,本领域急需一种动物模型,以便在动物水平上研究macf1基因在成骨细胞中的功能及其在骨形成过程中的作用。
技术实现要素:
为了克服现有技术的不足,本发明提供一种macf1基因在成骨细胞中条件性敲除的小鼠模型的构建及应用。本发明利用cre-loxp系统,通过macf1fl/fl小鼠与成骨细胞特异性表达cre重组酶的sp7-cre转基因小鼠交配,获得成骨细胞特异性敲除macf1的小鼠模型(sp7-cre;macf1fl/fl)。所述模型因macf1基因的条件性敲除造成小鼠骨形成能力降低。该模型可以用于研究macf1基因在成骨细胞中的功能及其在骨形成过程中的作用,同时还可以作为骨质疏松症及其它骨形成相关疾病发病/发生机制研究的动物模型,并用于筛选预防、治疗或改善此类疾病的药物。
本发明解决其技术问题所采用的技术方案:一种macf1基因在成骨细胞中条件性敲除的小鼠模型的构建方法,其特点是包括以下步骤:
步骤一、选用macf1fl/+小鼠自交,扩繁获得纯合子macf1fl/fl小鼠;
步骤二、将获得的macf1fl/fl小鼠与sp7-cre转基因小鼠交配,获得半敲sp7-cre;macf1fl/+小鼠;
步骤三、选用sp7-cre转基因小鼠与spf级c57bl/6j小鼠交配,获得sp7-cre转基因小鼠。
步骤四、将获得的半敲sp7-cre;macf1fl/+小鼠自交,获得macf1基因在成骨细胞中条件性敲除小鼠模型,即全敲sp7-cre;macf1fl/fl小鼠。
其中,所述步骤一、二所得到的小鼠利用特异性引物通过pcr方法进行基因型的鉴定。
步骤一所得到的小鼠基因型鉴定的引物为:
macf1-ap179:5'-aaagaaacggaaatactggcc-3';
macf1-ap180:5'-gcagcttaattctgccaaattc-3'。
步骤二所得到的小鼠基因型鉴定的引物为:
sp7-icre-wt-f:5'-taccagaagcgaccacttgagc-3';
icre-mut-r:5'-gcacacagacaggagcatcttc-3'。
所述步骤三、四所得到的小鼠通过双重pcr方法筛选鉴定,基因型鉴定所用的引物为:
macf1-ap179:5'-aaagaaacggaaatactggcc-3';
macf1-ap180:5'-gcagcttaattctgccaaattc-3'
和
sp7-icre-wt-f:5'-taccagaagcgaccacttgagc-3';
icre-mut-r:5'-gcacacagacaggagcatcttc-3'。
一种macf1基因在成骨细胞中条件性敲除的小鼠模型的应用,其特点是:
其一,macf1基因在成骨细胞中条件性敲除的小鼠模型作为研究macf1基因在成骨细胞中的功能及其在骨形成过程中的作用的动物模型。包括以下内容中的一种或几种:
(1)对macf1基因在成骨细胞中条件性敲除的小鼠模型与对比动物的成骨细胞的增殖、分化和矿化能力进行检测;
(2)对macf1基因在成骨细胞中条件性敲除的小鼠模型与对比动物的成骨细胞成骨分化过程中的标记基因的表达进行检测;
(3)采用qrt-pcr技术对macf1基因在成骨细胞中条件性敲除的小鼠模型与对比动物的骨组织成骨分化相关基因的表达进行检测;
(4)采用钙黄绿素双标法对macf1基因在成骨细胞中条件性敲除的小鼠模型与对比动物的骨形成速率进行检测;
(5)利用micro-ct扫描对macf1基因在成骨细胞中条件性敲除的小鼠模型与对比动物的骨密度及骨组织微结构进行分析。
其二,macf1基因在成骨细胞中条件性敲除的小鼠模型作为研究骨质疏松症及其它骨形成相关疾病发病/发生机制的动物模型。macf1基因在成骨细胞中条件性敲除的小鼠模型可自发的产生骨形成相关疾病的表型特征。
其三,macf1基因在成骨细胞中条件性敲除的小鼠模型作为筛选预防、治疗或改善骨质疏松症及其它骨形成相关疾病的药物的动物模型。其包括以下步骤:
(1)给macf1基因在成骨细胞中条件性敲除的小鼠模型施用待筛选的测试药物;
(2)检测macf1基因在成骨细胞中条件性敲除的小鼠模型中的骨密度及骨组织微结构,并与对照组进行比较。
本发明的有益效果是:本发明利用cre-loxp系统,通过macf1fl/fl小鼠与成骨细胞特异性表达cre重组酶的sp7-cre转基因小鼠交配,获得成骨细胞特异性敲除macf1的小鼠模型(sp7-cre;macf1fl/fl)。所述模型因macf1基因的条件性敲除造成小鼠骨形成能力降低。该模型可以用于研究macf1基因在成骨细胞中的功能及其在骨形成过程中的作用,同时还可以作为骨质疏松症及其它骨形成相关疾病发病/发生机制研究的动物模型,并用于筛选预防、治疗或改善此类疾病的药物。
首次建立了macf1基因在成骨细胞中条件性敲除的小鼠模型;
运用该模型可在体内验证macf1基因在成骨细胞中的功能及其在骨形成过程中的作用;
为骨质疏松症及其它骨形成相关疾病发病/发生机制的研究及预防、治疗或改善此类疾病的药物的筛选提供一个可信的动物模型。
因此,macf1基因在成骨细胞中条件性敲除的小鼠模型将具有广阔的应用前景。
下面结合附图和具体实施方式对本发明作详细说明。
附图说明
图1是本发明实施例1中macf1基因条件性敲除小鼠模型的构建策略示意图;
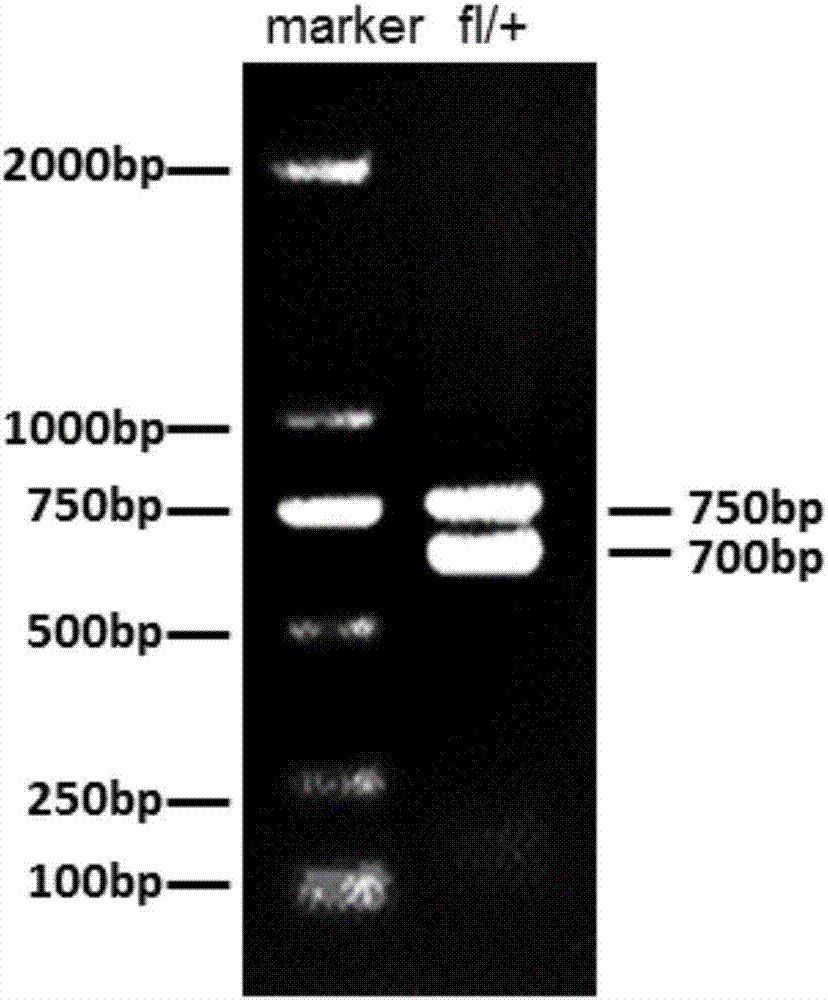
图2是本发明实施例1中最初引入的macf1fl/+小鼠的pcr基因型鉴定结果图;
图3是本发明实施例1中最初引入的sp7-cre小鼠的pcr基因型鉴定结果图;
图4是本发明实施例1中最终获得的sp7-cre;macf1fl/fl(cko)小鼠的pcr基因型鉴定结果图;
图5是本发明实施例2中对cko小鼠的成骨细胞中macf1的表达鉴定结果图;
图6是本发明实施例3中对cko小鼠的成骨细胞中相关成骨基因的表达鉴定结果图;
图7是本发明实施例4中利用microct对cko小鼠股骨进行骨密度扫描的结果图;
图8是本发明实施例4中利用钙黄绿素双标法检测cko小鼠的骨形成速率的结果图。
具体实施方式
以下实施例参照图1-8。
实施例1:构建macf1基因在成骨细胞中条件性敲除的小鼠模型。
1.1实验动物。
macf1fl/+小鼠与sp7-cre转基因小鼠的饲养。
macf1fl/+小鼠与sp7-cre转基因小鼠经隔离观察未见异常后进入饲养区,饲养按照spf动物饲养标准执行,实验操作严格按照spf动物管理相关规定进行。
1.2macf1fl/+小鼠基因型鉴定
剪取小鼠脚趾,提取macf1fl/+小鼠基因组dna,采用引物进行小鼠基因型鉴定;以小鼠macf1基因序列为模板,具体设计引物序列如下:
ap179:5’-aaagaaacggaaatactggcc-3’;
ap180:5'-gcagcttaattctgccaaattc-3’。
参照图2,pcr鉴定结果显示扩增出700bp和750bp两条带,证明为杂合子macf1fl/+小鼠。
1.3sp7-cre转基因小鼠基因型鉴定。
剪取小鼠脚趾,提取sp7-cre转基因小鼠基因组dna,采用引物进行小鼠基因型鉴定;根据cre基因序列为模板引物序列具体设计如下:
sp7-icre-wt-f:5'-taccagaagcgaccacttgagc-3';
icre-mut-r:5'-gcacacagacaggagcatcttc-3'。
参照图3,pcr鉴定结果显示扩增得一条445bp的条带,证明为sp7-cre转基因小鼠。
1.4参照图1,构建macf1基因在成骨细胞中条件性敲除纯合子小鼠模型。
(1)选用macf1fl/+小鼠自交,获得纯合子macf1fl/fl小鼠。
(2)选用sp7-cre转基因小鼠与spf级c57bl/6j小鼠交配,获得sp7-cre转基因小鼠。
(3)将获得的macf1fl/fl小鼠与sp7-cre转基因小鼠交配,获得macf1基因在成骨细胞中条件性敲除的杂合子小鼠,即半敲sp7-cre;macf1fl/+小鼠;再利用sp7-cre;macf1fl/+小鼠进行自交,获得macf1基因在成骨细胞中条件性敲除的纯合子小鼠,即全敲sp7-cre;macf1fl/fl小鼠,其基因型通过双重pcr方法筛选鉴定。参照图4,分别获得750bp和445bp两个条带,表明获得了全敲sp7-cre;macf1fl/fl小鼠。
(4)将获得的sp7-cre;macf1fl/fl小鼠与macf1fl/fl小鼠进行交配,获得更多的sp7-cre;macf1fl/fl小鼠与macf1fl/fl小鼠,然后对7-9天龄子代小鼠剪脚趾提取基因组dna,用双重pcr筛选鉴定基因型,理论上产生的后代有1/2的macf1fl/fl子鼠和1/2的sp7-cre;macf1fl/fl子鼠。子鼠基因型确定后,用于macf1基因在成骨细胞中条件性敲除小鼠模型的表型鉴定。
实施例2:检测条件性敲除的小鼠模型的成骨细胞中macf1的表达情况。
取新生小鼠颅骨成骨细胞,并提取其rna进行sybrgreenreal-timequantitativepcr(简称qrt-pcr),检测macf1在mrna水平的表达情况,以验证macf1在macf1基因在成骨细胞中条件性敲除的小鼠模型的成骨细胞中低表达,从而确定动物模型构建成功。
参照图5,macf1在sp7-cre;macf1fl/fl小鼠的成骨细胞中的表达量显著低于macf1fl/fl小鼠,说明macf1基因在成骨细胞中条件性敲除的小鼠模型构建成功。
实施例3:成骨细胞中敲除macf1对小鼠成骨细胞中相关成骨基因表达的影响。
取新生小鼠颅骨成骨细胞,提取其rna进行qrt-pcr,检测成骨分化标志基因(alp、runx2、col-i、ocn)的表达情况。
参照图6,结果表明,与macf1fl/fl小鼠相比,sp7-cre;macf1fl/fl小鼠成骨细胞中相关成骨基因的表达量均显著降低,说明在成骨细胞中敲除macf1降低了成骨细胞的分化能力。
实施例4:macf1基因在成骨细胞中条件性敲除的小鼠模型表型的鉴定
发现macf1基因在成骨细胞中条件性敲除的小鼠股骨骨小梁结构稀疏、骨形成能力降低。
4.1成骨细胞中敲除macf1对小鼠股骨发育的影响。
选取3月龄的sp7-cre;macf1fl/fl小鼠和macf1fl/fl小鼠,取血处死后,剥离取出股骨,去除骨表面的软组织,用70%乙醇固定后,采用小动物micro-ct扫描,获取数据后,用siemensinveonresearchworkplace软件进行三维重建处理。
参照图7,与macf1fl/fl小鼠相比,sp7-cre;macf1fl/fl小鼠的股骨骨组织骨小梁数量明显减少。说明在成骨细胞中敲除macf1降低了小鼠骨密度,并改变了骨组织微结构。
4.2成骨细胞中敲除macf1对小鼠骨形成能力的影响。
选取3月龄的sp7-cre;macf1fl/fl小鼠和macf1fl/fl小鼠,分别于处死前10天和3天进行腹腔注射钙黄绿素(25mg/kg)。取胫骨,40%乙醇固定,树脂包埋,选择10μm胫骨树脂切片浸泡于乙酸乙二醇乙醚溶液中避光脱脂过夜;无水乙醇漂洗后避光室温晾干,中性树胶封片;荧光显微镜495nm波长下进行双标观察、测量,形态计量。
参照图8,与macf1fl/fl小鼠相比,sp7-cre;macf1fl/fl小鼠的骨形成速率明显降低,说明在成骨细胞中敲除macf1使小鼠的骨形成能力降低。
sequencelisting
<110>西北工业大学
<120>macf1基因在成骨细胞中条件性敲除的小鼠模型的构建及应用
<130>说明书,权利要求书
<160>4
<170>patentinversion3.5
<210>1
<211>21
<212>dna
<213>人工序列
<400>1
aaagaaacggaaatactggcc21
<210>2
<211>22
<212>dna
<213>人工序列
<400>2
gcagcttaattctgccaaattc22
<210>3
<211>22
<212>dna
<213>人工序列
<400>3
taccagaagcgaccacttgagc22
<210>4
<211>22
<212>dna
<213>人工序列
<400>4
gcacacagacaggagcatcttc22
序列表
1
- 还没有人留言评论。精彩留言会获得点赞!