一种混合益生菌片剂及其低温包衣制备方法与流程
本发明属于益生菌片剂领域,具体涉及一种混合益生菌片剂及其低温包衣制备方法。
背景技术:
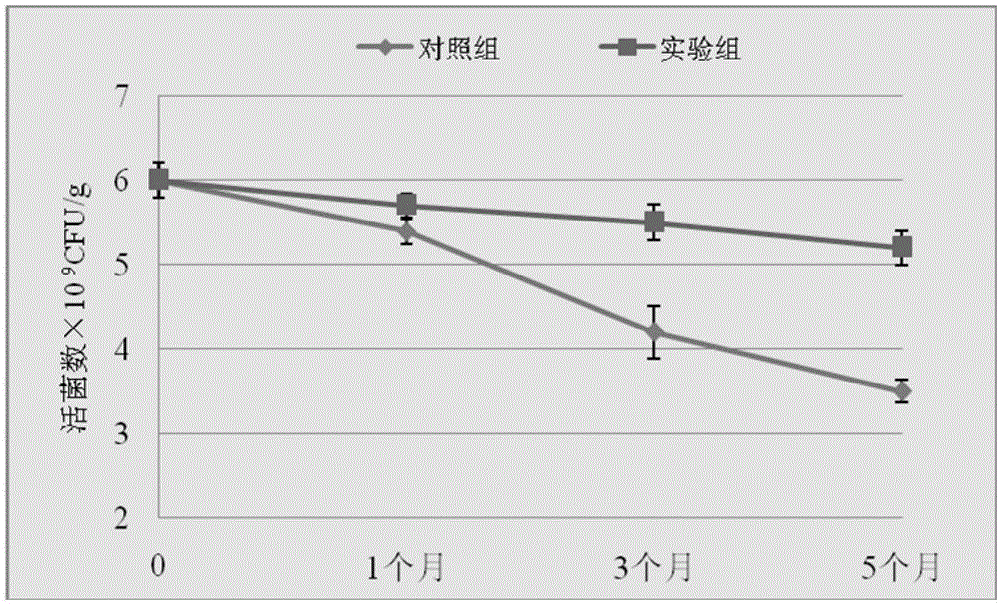
:益生菌被定义为“摄取足够数量可对宿主提供有益作用的活的微生物”。益生菌具有多种生理功能,包括改善人体肠道功能、抑制有害菌生长、减少肠道疾病、缓解乳糖不耐症、促进糖、蛋白质及钙、镁等营养物质的吸收、降胆固醇、调节免疫系统、抗肿瘤、预防癌症等。但要想获得益生功效,要求益生菌在产品和宿主中都保持活性和代谢稳定,且达到一定数量(通常认为是每克或毫升产品中不低于107CFU)。然而,在生产、贮藏、运输等过程中,益生菌将受到诸如食品组分(酸、氧、添加剂等)、储存温度及宿主消化系统(胃酸、胆盐、酶)等的影响,常导致活菌数大幅下降,最终定植于肠道中的活菌数低于理论上能够发挥生理作用的最小值。申请号为200910253872.8的发明专利公开了“一种益生菌片剂及其制备方法”,其特征为以葡萄糖、乳糖、微品纤维素等为原料制备颗粒,再混合活性成份益生菌粉末及硬脂酸镁进行压片。该发明的优点在于:制备的益生菌片剂因其活菌存活率高,服用方便,便于吸收,治疗效果明显。申请号为201410129017.7的发明专利公开了“一种益生菌微生态片剂及其制备方法”,其特征为益生菌微生态片剂按质量计为益生菌菌粉90%~98%,低聚果糖1%~9%,硬脂酸镁0.1%~1%。制备是将双歧杆菌进行活化,并制备开菲尔发酵剂;再将二者经混合发酵、低温浓缩干燥、混料压片制得。混合发酵是将益生菌混合菌种进行接种,28~36℃条件下发酵16~24小时,混合菌种中开菲尔发酵剂与双歧杆菌的比例1~3:1。本发明将开菲尔发酵剂和双歧杆菌进行高密度混合发酵,菌种多样,储存稳定,片剂中的活菌数分别达到20亿cfu/g以上;不仅可以提高消化能力,同时还增强了益生菌在肠道中的定植能力;具有营养价值高,风味独特等特点。申请号为201410709383.X的的发明专利公开了“一种益生菌微生态片剂及其制备方法”,其特征为以植物乳杆菌等益生菌粉剂为主要原料,科学复配改性膳食纤维、果蔬粉、低聚糖、植物提取物、蛋白粉、茶叶提取物、中草药提取物等,提高了对益生菌群具有真正意义的可溶性纤维素的含量,增强了纤维素的生理活性,进而在增加肠道益生菌菌群种类的同时,显著增强了内源和外源益生菌在人体肠道内的定植能力及定植时间,有效抑制了肠道有害菌尤其是革兰氏阴性菌的生长及繁殖,充分调节了肠道益生菌菌群的组成,制备的益生菌片剂生物活性高、在人体肠道定植时间长、减肥效果显著并且适宜人群广泛。但综上,由于益生菌片剂是一种携带方便、含有高浓度益生菌活菌数的产品,因益生菌的存活稳定性极易受到贮藏温度的影响,目前市场上的益生菌片剂均不能实现在常温下贮藏,而且生产的益生菌片剂表面粗糙,运输过程中相互摩擦容易掉粉,严重影响产品的美观。因此,本发明通过新的技术手段,制备了一种混合益生菌片剂,并在避免益生菌菌在制备过程中造成损失的同时提高益生菌在产品货架期内的贮藏稳定性。同时提高混合益生菌片剂的附加值,以及其在机体内的耐受性,保持较高的活力,同时在提高机体消化吸收率,改善机体胃肠道环境,调节机体免疫,有效预防缓解腹泻等方面进行进一步优化。技术实现要素:本发明所解决的技术问题是克服上述现有技术中混合益生菌片剂在制备过程以及在产品货架期内益生菌体活性易受损失的缺陷,同时提高混合益生菌片剂的附加值,提高混合菌剂在机体的耐受性,保持较高的活力,同时在提高机体消化吸收率,改善机体胃肠道环境,调节机体免疫,有效预防缓解腹泻等方面均有显著的效果。为了达到上述目的,本发明采用以下技术方案:一种混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂2-7份、干酪乳杆菌Zhang菌剂2-7份、动物双歧杆菌乳亚种V9菌剂2-7份、植物乳杆菌P-8菌剂2-7份、低聚半乳糖10-40份、葡萄糖10-30份、微晶纤维素10-30份、可溶性大豆多糖0.1-0.7份。优选地,所述混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂2-5份、干酪乳杆菌Zhang菌剂2-5份、动物双歧杆菌乳亚种V9菌剂2-5份、植物乳杆菌P-8菌剂2-5份、低聚半乳糖20-30份、葡萄糖10-20份、微晶纤维素10-20份、可溶性大豆多糖0.1-0.5份。更优选地,所述混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂3份、干酪乳杆菌Zhang菌剂3份、动物双歧杆菌乳亚种V9菌剂3份、植物乳杆菌P-8菌剂3份、低聚半乳糖25份、葡萄糖15份、微晶纤维素15份、可溶性大豆多糖0.3份。进一步地,所述嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂以及植物乳杆菌P-8菌剂的制备,包括如下步骤:分别取一环活化后的嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌P-8菌的斜面菌体,各自分别接种至MRS培养基中,在相同温度33~37℃,相同转速50~100rpm条件下培养18~24h,分别得到一级种子液;将培养好的一级种子液按接种量3%~10%(v/v)再次转接入MRS培养基进行二次活化,活化时间18~24h后得二级种子液;将二级种子液分别按照相同接种量3%~10%(v/v)分别各自接入到不同的发酵罐培养基中,温度均为33~37℃,转速均为50~100rpm,通风量均为0.3~1L/min,发酵全程调节发酵液相同pH值为5.6~6.2条件下培养8~12小时,分别得到最终嗜酸乳杆菌KT-A1发酵液、最终干酪乳杆菌Zhang发酵液、最终动物双歧杆菌乳亚种V9发酵液以及最终植物乳杆菌P-8发酵液,将得到的上述最终发酵液分别经5000~12000rpm,5~15min离心收集菌体;向经离心后的嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的菌体中分别按照各自菌体与保护剂溶液质量比1:(5~10)的比例添加保护剂溶液,混匀获得菌悬液,将所述菌悬液经冷冻干燥,分别得到嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的冻干菌剂。进一步地,所述嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的发酵液的各自活菌数均达到1010CFU/ml以上。进一步地,所述嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的冻干菌剂各自的活菌总数均达到2×1011CFU/g以上。所述发酵罐培养基(g/L):蔗糖50~80,酵母粉20~40,大豆蛋白胨8~20,MgSO4.7H2O1.5~2.0,MnSO4.5H2O0.08~0.12,吐温-800.8~1.0,余量为水,pH7.0。所述保护剂溶液的配方如下(g/L):脱脂乳10-15,海藻糖8~15,余量为蒸馏水。本发明的另一目的在于提供上述混合益生菌片剂的低温包衣技术制备方法,包括如下步骤:原料混合:将嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂、植物乳杆菌P-8菌剂与低聚半乳糖、葡萄糖、微晶纤维素、可溶性大豆多糖按比例复配混合,利用三维多向运动混合机,在转速为5-15rpm的条件下充分混匀,混合时间10-30min,获得益生菌混合料;压片:将所述益生菌混合料采用压片机压片,片重0.7-0.9g/片,硬度达到7N/cm2以上;获得片状益生菌混合料;低温包衣:通过包衣机采用可溶性大豆多糖将所述片状益生菌混合料进行低温包衣,包衣温度45-55℃,包衣时间2-4小时,即获得混合益生菌片剂。优选地,所述混合益生菌片剂的低温包衣技术制备方法,包括如下步骤:原料混合:将嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂、植物乳杆菌P-8菌剂与低聚半乳糖、葡萄糖、微晶纤维素按比例复配混合,利用三维多向运动混合机,在转速为10rpm的条件下充分混匀,混合时间20min,获得益生菌混合料;压片:将所述益生菌混合料采用压片机压片,片重0.7-0.9g/片,硬度8N/cm2,;获得片状益生菌混合料;低温包衣:通过包衣机采用可溶性大豆多糖将所述片状益生菌混合料进行低温包衣,包衣温度50℃,包衣时间3小时,即获得混合益生菌片剂。进一步地,所述混合益生菌片剂中的总活菌数达到5×109CFU/g以上。所述嗜酸乳杆菌KT-A1,已于2016年9月8日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称CGMCC),菌种保藏号:CGMCCNo.12951,保藏地址为:中国北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编:100101,分类命名为嗜酸乳杆菌(Lactobacillusacidophilus)。所述干酪乳杆菌zhang,已于2011年11月18日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称CGMCC),保藏号为CGMCCNo.5469,保藏地址为:中国北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编:100101,分类命名为干酪乳杆菌(Lactobacilluscasei)。该菌株是2001年分离自内蒙古锡林郭勒盟正蓝旗草原上自然发酵酸马奶(Komiss)中的一株具有优良益生特性的干酪乳杆菌。所述动物双歧杆菌乳亚种V9,已于2011年11月18日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称CGMCC),保藏号为CGMCCNo.5470,保藏地址为:中国北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编:100101,分类命名为动物双歧杆菌乳亚种(Bifidobacteriumanimalissubsp.lactis)。该菌株是2005年分离自内蒙古草原上健康蒙古族儿童肠道中的一株具有优良益生特性的动物双歧杆菌乳亚种。所述植物乳杆菌P-8,已于2012年06月28日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称CGMCC),保藏号为CGMCCNo.6312,保藏地址为:中国北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编:100101,分类命名为植物乳杆菌(Lactobacillusplantarum)。该菌株是2003年从内蒙古自治区牧民家庭中的自然发酵酸牛奶中分离并筛选出的一株具有优良益生特性的乳酸菌株。有益效果:本发明分别分离自酸牛乳、健康儿童肠道和酸马奶样品中的L.acidophilusKT-A1、L.plantarumP-8、B.lactisV9和L.caseiZhang益生菌株制备混合益生菌片剂,上述益生菌具有优异的抗胃肠道消化液耐受能力;改善人体肠道菌群结构的能力,提高机体消化吸收率;调节血脂代谢,对高血脂症肝脏具有保护修复作用,增强机体抗氧化能力;对机体免疫具有调节作用;有效预防缓解腹泻、便秘、腹痛、腹胀等肠易激综合症;有效预防肿瘤生长和Ⅱ型糖尿病的发生等功效。通过低温包衣技术制备的混合益生菌片剂不仅避免了益生菌在制片过程造成的菌体损失,而且大大地提高了益生菌在产品货架期内的贮藏稳定性,在37℃下贮藏5个月,产品中益生菌总活菌数保持不低于5×109CFU/g;产品片重0.7-0.9g/片,硬度达到7N/cm2,表面光滑,没有掉粉现象。附图说明下面结合附图及具体实施例对本发明作进一步说明:附图1是实验组与对照组中混合益生菌片剂硬度比较;附图2是混合益生菌片剂在37℃贮藏5个月总益生菌活菌数的变化。具体实施方式下面通过具体的实施方案叙述本发明。除非特别说明,本发明中所用的技术手段均为本领域技术人员所公知的方法。另外,实施方案应理解为说明性的,而非限制本发明的范围,本发明的实质和范围仅由权利要求书所限定。对于本领域技术人员而言,在不背离本发明实质和范围的前提下,对这些实施方案中的物料成分和用量进行的各种改变或改动也属于本发明的保护范围。实施例1:四钟菌剂的发酵制备方法嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂以及植物乳杆菌P-8菌剂的发酵制备,包括如下步骤:分别取一环活化后的嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌P-8菌的斜面菌体,各自分别接种至MRS培养基,在相同温度37℃,相同转速100rpm条件下培养18h,分别得到一级种子液;将培养好的一级种子液按接种量3%(v/v)再次转接入MRS培养基进行二次活化,活化时间18h后得二级种子液;将二级种子液分别按照相同接种量3%(v/v)分别各自接入至3L发酵罐培养基的5L发酵罐中,温度均为37℃,转速均为100rpm,通风量均为0.3L/min,发酵全程调节发酵液相同pH值为6.2条件下培养10小时,分别得到最终嗜酸乳杆菌KT-A1发酵液、最终干酪乳杆菌Zhang发酵液、最终动物双歧杆菌乳亚种V9发酵液以及最终植物乳杆菌P-8发酵液,将得到的上述最终发酵液分别经8000rpm,5min离心收集菌体;向经离心后的嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的菌体中分别按照各自菌体与保护剂溶液质量比1:5的比例添加保护剂溶液,混匀获得菌悬液,将所述菌悬液经冷冻干燥,分别得到嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的冻干菌剂。嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的发酵液的各自活菌数均达到1010CFU/ml以上。嗜酸乳杆菌KT-A1、干酪乳杆菌Zhang、动物双歧杆菌乳亚种V9以及植物乳杆菌的冻干菌剂各自的活菌总数均达到2×1011CFU/g以上。发酵罐培养基(g/L):蔗糖50~80,酵母粉20~40,大豆蛋白胨8~20,MgSO4﹒7H2O1.5~2.0,MnSO4.5H2O0.08~0.12,吐温-800.8~1.0,余量为水,pH7.0;保护剂溶液的配方如下(g/L):脱脂乳10-15,海藻糖8~15,余量为蒸馏水。以下实施例2-5所用嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂以及植物乳杆菌P-8菌剂均由实施例1制备。实施例2:混合益生菌片剂的制备一种混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂2份、干酪乳杆菌Zhang菌剂2份、动物双歧杆菌乳亚种V9菌剂2份、植物乳杆菌P-8菌剂2份、低聚半乳糖10份、葡萄糖10份、微晶纤维素10份、可溶性大豆多糖0.1份。本发明的另一目的在于提供上述混合益生菌片剂的低温包衣技术制备方法,包括如下步骤:原料混合:将嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂、植物乳杆菌P-8菌剂与低聚半乳糖、葡萄糖、微晶纤维素按比例复配混合,利用三维多向运动混合机,在转速为5rpm的条件下充分混匀,混合时间10min,获得益生菌混合料;压片:将所述益生菌混合料采用压片机压片,片重0.7g/片,硬度7.7N/cm2,;获得片状益生菌混合料;低温包衣:通过包衣机采用可溶性大豆多糖将所述片状益生菌混合料进行低温包衣,包衣温度45℃,包衣时间2小时。所述混合益生菌片剂中的总活菌数为5.8×109CFU/g。实施例3;混合益生菌片剂的制备一种混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂7份、干酪乳杆菌Zhang菌剂7份、动物双歧杆菌乳亚种V9菌剂7份、植物乳杆菌P-8菌剂7份、低聚半乳糖40份、葡萄糖30份、微晶纤维素30份、可溶性大豆多糖0.7份。本发明的另一目的在于提供上述混合益生菌片剂的低温包衣技术制备方法,包括如下步骤:原料混合:将嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂、植物乳杆菌P-8菌剂与低聚半乳糖、葡萄糖、微晶纤维素按比例复配混合,利用三维多向运动混合机,在转速为15rpm的条件下充分混匀,混合时间30min,获得益生菌混合料;压片:将所述益生菌混合料采用压片机压片,片重0.9g/片,硬度9N/cm2,;获得片状益生菌混合料;低温包衣:通过包衣机采用可溶性大豆多糖将所述片状益生菌混合料进行低温包衣,包衣温度55℃,包衣时间4小时。所述混合益生菌片剂中的总活菌数为6.9×109CFU/g。实施例4;混合益生菌片剂的制备一种混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂3.5份、干酪乳杆菌Zhang菌剂3.5份、动物双歧杆菌乳亚种V9菌剂3.5份、植物乳杆菌P-8菌剂3.5份、低聚半乳糖25份、葡萄糖15份、微晶纤维素15份、可溶性大豆多糖0.3份。混合益生菌片剂的低温包衣技术制备方法,包括如下步骤:原料混合:将嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂、植物乳杆菌P-8菌剂与低聚半乳糖、葡萄糖、微晶纤维素按比例复配混合,利用三维多向运动混合机,在转速为10rpm的条件下充分混匀,混合时间20min,获得益生菌混合料;压片:将所述益生菌混合料采用压片机压片,片重0.8g/片,硬度7.96N/cm2,;获得片状益生菌混合料;低温包衣:通过包衣机采用可溶性大豆多糖将所述片状益生菌混合料进行低温包衣,包衣温度50℃,包衣时间3小时。混合益生菌片剂中的总活菌数不低于6.4×109CFU/g。实施例5:混合益生菌片剂的制备一种混合益生菌片剂,主要由以下重量份数的原料制备:嗜酸乳杆菌KT-A1菌剂5份、干酪乳杆菌Zhang菌剂5份、动物双歧杆菌乳亚种V9菌剂5份、植物乳杆菌P-8菌剂5份、低聚半乳糖30份、葡萄糖20份、微晶纤维素20份、可溶性大豆多糖0.5份。本发明的另一目的在于提供上述混合益生菌片剂的低温包衣技术制备方法,包括如下步骤:原料混合:将嗜酸乳杆菌KT-A1菌剂、干酪乳杆菌Zhang菌剂、动物双歧杆菌乳亚种V9菌剂、植物乳杆菌P-8菌剂与低聚半乳糖、葡萄糖、微晶纤维素按比例复配混合,利用三维多向运动混合机,在转速为10rpm的条件下充分混匀,混合时间25min,获得益生菌混合料;压片:将所述益生菌混合料采用压片机压片,片重0.85g/片,硬度为8.4N/cm2,;获得片状益生菌混合料;低温包衣:通过包衣机采用可溶性大豆多糖将所述片状益生菌混合料进行低温包衣,包衣温度50℃,包衣时间3小时。所述混合益生菌片剂中的总活菌数不低于6.6×109CFU/g。实施例6:嗜酸乳杆菌KT-La9的部分抑菌特性和耐受性测试嗜酸乳杆菌KT-La9分离自自然发酵的饲料样品中,可有效抑制人体肠道大肠杆菌、金黄色葡萄球菌、志贺氏菌、沙门氏菌、单胞李斯特氏菌等致病菌的生长和繁殖,耐受动物胃肠道的酸性和碱性环境,在人体肠道内存活和定植。抑菌特性实验:嗜酸乳杆菌KT-A1菌株在MRS液体培养基中37℃培养24h后,在12000转条件下进行离心15min,得到的上清液经过滤除菌得到无细胞提取液,然后在温度-80℃下保藏待用;准备带有致病菌平板:把20mL灭菌MRS琼脂培养基冷却到45℃,再与200μL105-106CFU/mL致病菌菌悬液(大肠杆菌、金黄色葡萄球菌、志贺氏菌、沙门氏菌、单胞李斯特氏菌)一起倒在琼脂平板上混匀;待冷却凝固后,使用打孔器在平板上打出直径0.8cm的孔;每个孔加入100μL上述无细胞提取液,于温度4℃冰箱中扩散12h后在温度37℃下进行培养24h;待出现明显抑菌圈后使用游标卡尺记录抑菌圈扩散直径mm。嗜酸乳杆菌KT-La9的部分抑菌特性(抑菌圈大小)和耐受性见下表。表1嗜酸乳杆菌KT-La9的部分抑菌特性(抑菌圈大小)和耐受性实施例7;混合益生菌片剂的硬度以及活菌稳定性测试对照组为市售的普通混合益生菌片剂,试验组为利用实施例4制备的混合益生菌片剂。根据本实施例4制备混合益生菌片剂,不仅避免了益生菌在制片过程造成的菌体损失,而且大大地提高了益生菌在产品货架期内的贮藏稳定性,在37℃下贮藏5个月,产品中益生菌总活菌数保持不低于5×109CFU/g;产品片重0.7-0.9g/片。由表2可以看出,混合益生菌片剂硬度达到7N/cm2以上,且较对照组,表面光滑,没有掉粉现象。表2实验组与对照组中益生菌片剂硬度比较对照组7.51N/cm2试验组7.96N/cm2表3混合益生菌片剂在37℃贮藏5个月总益生菌活菌数的变化分组初始(0个月)1个月3个月5个月对照组6.02×109CFU/g5.41×109CFU/g4.32×109CFU/g3.52×109CFU/g试验组6.02×109CFU/g5.86×109CFU/g5.53×109CFU/g5.14×109CFU/g由表3可以明显地看出,试验组通过低温包衣制备的混合菌剂在初始放置1个月时,其菌体活力比对照组明显地高出0.43×109CFU/g。随着货架期的延长,在放置3个月后,试验组的菌体活力略有下降,较初始益生菌活菌数仅下降了8.86%,但依然保持较高的菌体活力,益生菌活菌数依然保持较高的水平,而对照组经过3个月的放置后,其益生菌活菌数有显著的下降趋势,共下降了1.7×109CFU/g,较初始益生菌活菌数显著下降了28.24%,菌体活力有明显地下降趋势,较试验组的菌体活力下降比率显著提高了19.38%。在放置5个月后,试验组的菌体活力略有下降,下降幅度较对照组并不明显,仅下降了0.88×109CFU/g,而对照组的益生菌活菌数则有更为显著的下降趋势,较初始值显著下降了2.5×109CFU/g。由图2即可明显地看出,益生菌片剂经过1、3、5个月的放置,试验组的益生菌活菌数相比对照组,略有下降,且下降速率较为缓慢,以此说明试验组的菌株活力有较为显著的稳定性。而相比于试验组,对照组的益生菌活菌数有显著的下降趋势,较初始益生菌活菌数显著下降了41.52%,课件对照组的益生菌片剂经过5个月的放置,其益生菌活菌数几乎丧失一半,菌种活力也几乎仅存初始益生菌剂菌活力的一半。需要说明的是:本发明实施例2-3、5制备的混合益生菌片剂同样具有上述实验效果,各实施例之间及与上述实验效果差异性不大。实施例8混合益生菌片剂在人体内部的耐受性对照组为市售的普通混合益生菌片剂,试验组为利用实施例4制备的混合益生菌片剂。表4混合益生菌片剂在人体的耐受性测试需要说明的是:本发明实施例2-3、5制备的混合益生菌片剂同样具有上述实验效果,各实施例之间及与上述实验效果差异性不大。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1