白细胞的细胞外诱捕网形成抑制剂的制作方法
本发明涉及以类似乳铁蛋白(lactoferrin)的肽片段为有效成分的白细胞的细胞外诱捕网形成抑制剂以及用于治疗与白细胞的细胞外诱捕网形成相关的疾病的组合物。另外,本发明涉及一种使用所述抑制剂或组合物治疗与白细胞的细胞外诱捕网形成相关的疾病的方法。
背景技术:
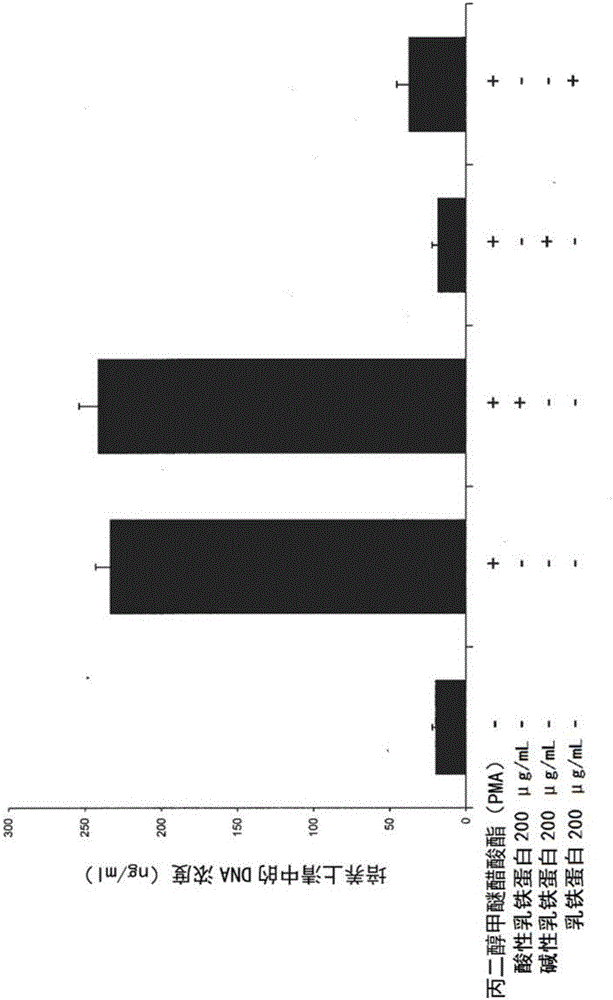
:中性粒细胞胞外诱捕网(NeutrophilExtracellularTraps,NETs)是一种细胞外结构,因细菌感染而引起中性粒细胞被激活,分叶核的形态、染色质的分布变得不清晰,然后核膜消失,染色质结构中混合有细胞质、颗粒成分,细胞膜破裂,此时,所述中性粒细胞胞外诱捕网释放网状结构,捕获细菌、真菌、寄生虫、病毒,发挥抗菌作用。NETs以DNA为中心,组蛋白3(H3)、弹性蛋白酶在上述作用中发挥重要作用。NETs形成使得有效杀死微生物的抗菌分子聚集在局部。由于产生NETs,所以导致中性粒细胞死亡(NETosis),但其分子机制尚不明确,因肿瘤坏死因子-α(TumorNecrosisFactor-α,TNF-α)、丙二醇甲醚醋酸酯(PMA)、脂多糖(Lipopolysaccharides,LPS)、白介素-8(Interleukin-8,IL-8)等的刺激而产生,此时产生的细胞死亡表现出与经典的坏死或产生半胱氨酸蛋白酶(caspase)的激活、DNA片段化这样的情况的细胞凋亡(Apoptosis)不同的方式。若中性粒细胞被LPS、PMA刺激,则产生自噬,同时,生成活性氧。由此,产生核膜破裂、染色质解凝缩、组蛋白瓜氨酸化,引起细胞死亡(非专利文献1和2)。已报告了随着NETs的形成,中性粒细胞通过脱颗粒分泌大量蛋白质,特别是嗜苯胺蓝颗粒、第二颗粒中含有的抗菌蛋白质,也分泌与细胞结构相关的蛋白质等(非专利文献2)。这些蛋白质也被称为NETs结构蛋白质,已报告了中性粒细胞弹性蛋白酶、组蛋白、髓过氧化物酶、F-肌动蛋白、乳铁蛋白、基质金属蛋白酶9、LL37、组织蛋白酶G、杀菌/渗透性增加蛋白(Baetericidal/PermeabilityIncreasingprotein,BPI)、蛋白酶3、钙卫蛋白、天青杀素(azurocidin)、溶菌酶C、防御素、过氧化氢酶等(非专利文献3)。对于乳铁蛋白而言,其被包含在中性粒细胞的第二颗粒中,中性粒细胞形成NETs,最终脱颗粒,释放到周围(非专利参考文献1)。对于乳铁蛋白而言,在哺乳动物中保存良好,其在功能上没有明显物种差异。另外,目前作为牛乳成分的蛋白质,其生理活性受到关注,在市场上有售。然而,已报告了牛乳对牛的中性粒细胞的NETs形成未表现出抑制效果(非专利文献4)。NETs也参与血栓的增大、成长,释放NETs后,其中含有的组蛋白具有使血小板凝缩的作用,基于NETs形成血小板血栓。另外,NETs中含有的中性粒细胞弹性蛋白酶、组织蛋白酶G使组织因子途径抑制因子分解,促进血液凝固反应。通过上述作用也表现出将微生物等限定在局部的作用(非专利文献5)。NETs本来的作用是捕捉革兰氏阳性菌、革兰氏阴性菌、真菌等外来微生物并限制在局部,进行杀菌。由于具有这种作用,所以在感染病中常见,但也有报告称随着感染病等转为慢性,即使在不存在外来微生物的情况下也观察到NETs的形成。众所周知的是,作为慢性且难治性的自身免疫性疾病之一的系统性红斑狼疮(SystemicLupusErythematosus,SLE)形成了针对自身DNA、相关蛋白质的自身抗体,由此,在组织、脏器中引发炎症。SLE的特征观察结果显示在损伤部位存在大量中性粒细胞。已知在SLE患者的血清中存在抗菌肽LL37和NETs中的DNA(非专利文献6和7)。这些DNA作为自身抗原被B细胞识别而产生自身抗体。另外,SLE患者的中性粒细胞比健康人的中性粒细胞更容易引起NETosis(非专利文献6)。认为这些主要因素会诱发慢性炎症。另外,已报告了在作为因自身抗体导致的疾病的抗中性粒细胞细胞质抗体(Anti-NeutrophilCytoplasmicAntibody,ANCA)相关血管炎中,与健康人的免疫球蛋白G(ImmunoglobulinG,IgG)组分相比,患者血清中的IgG组分形成中性粒细胞NETs的能力约高两倍(非专利文献8和9)。自2004年Brinkman等报告(非专利文献1)以来,NETs的形成与疾病的相关性最近才受到关注,将来,因NETs的形成而导致的新疾病可能会变得明确。如此地,NETs的形成在生物体的感染防御中发挥重要的作用,但根据病情,考虑到病情的改善需要抑制NETs的形成的情况。已报告了作为抑制NETs形成的物质,肺炎链球菌、金黄色葡萄球菌等革兰氏阳性球菌的链球菌在菌体外使脱氧核糖核酸酶(DNase)表达以使释放的DNA网分解。另外,作为针对组蛋白的抗体、抑制超氧化物产生的物质,已报告了二亚苯基烟碱氯化物(DiphenyleneIodoniumChloride,DPI)、过氧化氢酶(非专利文献10)。除此以外,已知髓过氧化物酶(Myeloperoxidase,MPO)活性影响NETosis(非专利文献11),中性粒细胞形成NETs而出现细胞死亡的现象即NETosis是与细胞凋亡、坏死不同的过程(非专利文献10)等。存在以来自乳的碱性蛋白质组分为有效成分预防I型糖尿病、类风湿关节炎的自身免疫性疾病的现有技术(专利文献1),但其特别指明了调节以淋巴细胞为中心的免疫细胞、抑制炎性细胞因子等内容,而与抑制NETs形成的作用无关。目前,尚未报告治疗因NETs的形成而导致的疾病的药剂。现有技术文献专利文献专利文献1:日本特开2008-189637。非专利文献非专利文献1:VolkerBrinkmann等,2004Science,303:1532-1535;非专利文献2:QRemijsen等,2011,CellDeathandDifferentiation,18:581-588;非专利文献3:MarenvonKoeckritz-Blickwede等,2008,Blood,111:3070-3080;非专利文献4:JohnD.Lippolis等,2006,VeterinaryImmunologyandImmunopathology,113:248-255;非专利文献5:FuchsTA等,2010,ProcNatlAcadSciUSA,107:15880-15885;非专利文献6:Garcia-RomoGS等,2011SciTranslMed,3:73ra20;非专利文献7:LandeR等,2011SciTranslMed,3:73ra19;非专利文献8:KessenbrockK等,2009,NatMed,6:623-625;非专利文献9:BoschX,2009,JAmSocNephrol,8:1654-1656;非专利文献10:TobiasA.Fuchs等,2007,JCellBiol,176:231-241;非专利文献11:K.Akong-Moore等,2012,PLOSONE,7:e42984;非专利文献12:内藤真等,2010,生物试样分析,33:329-338。技术实现要素:本发明的目的在于,提供一种因白细胞的细胞外诱捕网形成而导致发作的疾病的根治性治疗药,特别是,提供一种适用于长期进行维持缓解(抑制复发)的安全且有效的治疗药及治疗方法。本发明人等为了解决上述问题进行了精心研究,其结果发现,乳铁蛋白片段显著发挥抑制NETs形成的效果,能够对与NETs相关的疾病进行根治性治疗。即,本发明提供以下技术方案。[1]一种白细胞的细胞外诱捕网形成抑制剂,包含作为有效成分的含有由X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9表示的氨基酸序列的肽。[在上述氨基酸序列中,X1=S、T、F、A、K、E或Q;X2=R、F、S、Y、A或L;X3=Q、R、K或M;X4=W或F;X5=R、W、V、N、S或E;X6=R、N、E、K或M;X7=M、L或I;X8=R、K或N;且X9=K或R。][2]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X1=S或T。[3]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X2=R、F、S、Y或A。[4]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X3=Q、R或K。[5]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X4=W。[6]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X5=R。[7]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X6=R或N。[8]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X7=M或L。[9]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X8=R或K。[10]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X9=K。[11]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X1=S。[12]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X3=Q。[13]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X7=M。[14]如上述[1]所述的细胞外诱捕网形成抑制剂,在所述氨基酸序列中,X8=R。[15]如上述[1]所述的细胞外诱捕网形成抑制剂,在残基X1的N末端侧还含有残基X0,X0=A、M、W、G、S、E或Y。[16]如上述[15]所述的细胞外诱捕网形成抑制剂,X0=A。[17]如上述[1]~[16]中任一项所述的细胞外诱捕网形成抑制剂,在残基X9的C末端侧还含有氨基酸序列X10-X11-X12-P-X13-X14-X15-C-X16-X17-X18-X19-X20,[在上述氨基酸序列中,X10=V、L、T、A,优选X10=V、L,更优选X10=V;X11=G、R、N,优选X11=G、R,更优选X11=G;X12=G、A、V,优选X12=G、A,更优选X12=G;X13=S、P、I、L,优选X13=S、P,更优选X13=S;X14=V、I、L、M,优选X14=V、I,更优选X14=V;X15=S、T、F、R,优选X15=S、T,更优选X15=S;X16=I、V、T、A,优选X16=I、V,更优选X=I;X17=R、K,优选X17=R;X18=R、K,优选X18=R;X19=A、T、D、S、Y,优选X19=A、T;X20=S、F,优选X20=S。][18]如上述[1]~[14]中任一项所述的细胞外诱捕网形成抑制剂,所述肽由选自由序列号6~16所示的各氨基酸序列组成的组中的任意一个氨基酸序列构成。[19]如上述[1]~[18]中任一项所述的抑制剂,将所述肽制备成0.001~10g/kg/天的量。[20]如上述[1]~[19]中任一项所述的抑制剂,所述白细胞是选自由中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、单核细胞、巨噬细胞和肥大细胞组成的组中的任意一种。[21]如上述[1]~[20]中任一项所述的抑制剂,所述白细胞为中性粒细胞。[22]一种用于治疗与白细胞的细胞外诱捕网形成相关的疾病的组合物,其包含作为有效成分的含有由X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9表示的氨基酸序列的肽。[在上述氨基酸序列中,X1=S、T、F、A、K、E或Q;X2=R、F、S、Y、A或L;X3=Q、R、K或M;X4=W或F;X5=R、W、V、N、S或E;X6=R、N、E、K或M;X7=M、L或I;X8=R、K或N;且X9=K或R。][23]如上述[22]所述的组合物,将所述肽制备成0.001~10g/kg/天的量。[24]如上述[22]或[23]所述的组合物,所述白细胞是选自由中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、单核细胞、巨噬细胞和肥大细胞组成的组中的任意一种。[25]如上述[22]或[23]所述的组合物,所述白细胞为中性粒细胞。[26]如上述[22]~[25]中任一项所述的组合物,所述疾病是选自由血管炎综合征、ANCA相关性血管炎、系统性红斑狼疮、局部性施瓦兹曼(Shwartzman)反应、伴有缺血再灌注损伤的急性肾损伤(AcuteKidneyInjury,AKI)以及弥散性血管内凝血组成的组中的任意一种。[27]如上述[22]~[26]中任一项所述的组合物,其为食品的形式。[28]如上述[22]~[26]中任一项所述的组合物,其为注射剂的形式。[29]如上述[22]~[26]中任一项所述的组合物,其为口服给药的组合物。[30]如上述[22]~[26]中任一项所述的组合物,其为经皮给药的组合物。本发明能够提供一种针对因白细胞的细胞外诱捕网形成而产生的疾病、副作用少的治疗方法。另外,由于副作用少,所以具有能够安心用于广范围的患者和患者后备军的优点。本发明的抑制剂和组合物能够广泛用于老年人、荷瘤患者等免疫低下的受试者、有感染病并发症例、有结核病史的受试者等广泛的受试者群体。另外,本发明提供一种即使长期使用副作用也少的、与白细胞的细胞外诱捕网形成相关的疾病的治疗药以及治疗方法。特别是,在治疗所述疾病中需要长期使用药剂的情况下,作为受试者在急性期症状已缓解后的抑制复发的药剂以及在所述疾病转为慢性的情况下的治疗药,是有用的。附图说明图1是表示来自各种动物的乳铁蛋白的氨基酸序列的比对的图。图2是表示人乳铁蛋白片段的抑制NETs形成的能力的图表。图3是表示人乳铁蛋白片段的抑制NETs形成的能力的图表。具体实施方式下面,详细地说明本发明。下述实施方式是用于说明本发明的示例,并非旨在将本发明仅限定于所述实施方式。在不脱离主旨的范围内,本发明能够以各种形式实施。需要说明的是,在本说明书中引用的全部文献、公开公报、专利公报以及其他专利文献均作为参照引入本说明书中。另外,本说明书包括2014年10月8日申请的作为本申请要求优先权基础的日本专利申请(特愿2014-207415号)的说明书和附图记载的内容。在本说明书中,在没有特别说明的情况下,将碱基序列的5’末端记载于左侧、将3’末端记载于右侧。另外,将氨基酸序列的氨基末端(N末端)记载于左侧、将羧基末端(C末端)记载于右侧。另外,各氨基酸由如下所示的单字母代码或三字母代码表示。表1氨基酸名称单字母代码三字母代码丙氨酸AAla精氨酸RArg天冬酰胺NAsn天冬氨酸DAsp半胱氨酸CCys谷氨酰胺QGln谷氨酸EGlu甘氨酸GGly组氨酸HHis异亮氨酸IIle亮氨酸LLeu赖氨酸KLys蛋氨酸MMet苯丙氨酸FPhe脯氨酸PPro丝氨酸SSer苏氨酸TThr色氨酸WTrp酪氨酸YTyr缬氨酸VVal1.白细胞的细胞外诱捕网形成抑制剂作为第一实施方式,本发明提供一种包含乳铁蛋白片段的白细胞的细胞外诱捕网形成抑制剂(以下,称为“本发明的抑制剂”)。已报告了细胞外诱捕网由各种白细胞形成,例如由中性粒细胞(Brinkmann,V.等,Science2004;303:1532-1535.)、嗜碱性粒细胞(Yousefi,S.等,NatMed2008;14:949-953.)、肥大细胞(vonKoeckritz-BlickwedeM等,Blood2008;111:3070-3080.)、单核细胞(WebsterSJ等,JImmunol2010;185:2968-2979)例如巨噬细胞(Chow,O.A等,CellHost&Microbe,Volume8,Issue5,445-454,18November2010))等生成。已报告了所述白细胞所形成的细胞外诱捕网具有释放以DNA和颗粒蛋白质(granuleprotein)为主要成分的纤维成分的共同特征(Simon,D.等,Allergy68(2013)409-416)。相对于此,本发明的抑制剂使所述纤维成分凝缩和/或缩合,由此能够抑制该纤维成分的释放。因此,可知若使用本发明的抑制剂,不仅实施例中使用的中性粒细胞,而且由其他白细胞(例如,嗜碱性粒细胞、肥大细胞、单核细胞(例如,巨噬细胞))形成细胞外诱捕网时释放的纤维成分也凝缩和/或缩合,由此,能够抑制所述白细胞的细胞外诱捕网形成。作为本发明抑制剂的有效成分的乳铁蛋白片段,只要是来自哺乳动物(例如,猴、牛、山羊、绵羊、人、骆驼、马、狗、猫、小鼠和大鼠)的乳汁的乳铁蛋白片段,就没有特别的限定,优选来自人能够摄取的哺乳动物的乳汁(例如,牛、山羊、绵羊、人的乳汁)的乳铁蛋白片段,更优选来自人乳汁的乳铁蛋白片段。或者,乳铁蛋白及其片段也可以来自所述哺乳动物的中性粒细胞。来自各种哺乳动物的乳铁蛋白的氨基酸序列是公知的(参照下述表2)。表2乳铁蛋白的来源基因银行登记号序列号人NP_001186078.11牛NP_851341.12绵羊ACT76166.13山羊AAA97958.14马CAA09407.15作为乳铁蛋白片段,只要是将乳铁蛋白的全长分段得到的片段,就没有特别的限定,可以是包含许多酸性氨基酸残基的酸性片段(acidicfraction)或包含许多碱性氨基酸残基的碱性片段(basicfraction)。在一实施方式中,乳铁蛋白片段是用胃蛋白酶将乳铁蛋白的全长分解而得到的片段,优选为碱性片段,进一步地,在又一实施方式中,乳铁蛋白片段为乳铁蛋白素(Lactoferricin,Lfcin)。此处,酸性氨基酸残基是指从天冬氨酸(D)和谷氨酸(E)中选出的氨基酸残基。另外,碱性氨基酸残基是指从精氨酸(R)、组氨酸(H)和赖氨酸(K)中选出的氨基酸残基。在一实施方式中,用于本发明抑制剂的肽是包含以下氨基酸序列的乳铁蛋白片段。X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9[在上述氨基酸序列中,X1=S、T、F、A、K、E或Q;X2=R、F、S、Y、A或L;X3=Q、R、K或M;X4=W或F;X5=R、W、V、N、S或E;X6=R、N、E、K或M;X7=M、L或I;X8=R、K或N;且X9=K或R。]下面,将由“X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9”构成的氨基酸序列称为“共有序列”。另外,以下,将用于本发明抑制剂的肽即乳铁蛋白片段称为“本发明的LF片段”。在共有序列中,X1优选为X1=S或T,更优选为X1=S。X2优选为X2=R、F、S、Y或A。X3优选为X3=Q、R或K,更优选为X3=Q。X4优选为X4=W。X5优选为X5=R。X6优选为X6=R或N。X7优选为X7=M或L,更优选为X7=M。X8优选为X8=R或K,更优选为X8=R。X9优选为X9=K。根据情况,本发明的LF片段可以是包含“X1-K-C-X2-X3-X4-Q-X5-X6”(9聚体)或“X1-K-C-X2”(4聚体)的片段,或者是由所述氨基酸序列构成的片段。即,本发明的LF片段可以是包含选自由“X1-K-C”(3聚体)、“X1-K-C-X2”(4聚体)、“X1-K-C-X2-X3”(5聚体)、“X1-K-C-X2-X3-X4”(6聚体)、“X1-K-C-X2-X3-X4-Q”(7聚体)、“X1-K-C-X2-X3-X4-Q-X5”(8聚体)、“X1-K-C-X2-X3-X4-Q-X5-X6”(9聚体)、“X1-K-C-X2-X3-X4-Q-X5-X6-X7”(10聚体)、“X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8”(11聚体)以及“X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9”(12聚体)组成的组中的任意一个氨基酸序列的片段,或者是由所述氨基酸序列构成的片段,无论在上述哪种情况下,均具有抑制白细胞的细胞外诱捕网形成的活性(对于该活性而言,参照下述情况)在上述3聚体~9聚体的各氨基酸序列中,X1~X9如上所述。在一实施方式中,本发明的LF片段可以在上述共有序列的残基X1的N末端侧还包含残基X0。在此情况下,本发明的LF片段包含以下氨基酸序列。X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9“在上述氨基酸序列中,X1~X9如上所述,X0=A、M、W、G、S、E或Y,优选X0=A”或者,本发明的LF片段还可以在上述共有序列的残基X9的C末端侧包含氨基酸序列X10-X11-X12-P-X13-X14-X15-C-X16-X17-X18-X19-X20。在此情况下,本发明的LF片段包含以下氨基酸序列。X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9-X10-X11-X12-P-X13-X14-X15-C-X16-X17-X18-X19-X20“在上述氨基酸序列中,X1~X9如上所述,X10=V、L、T、A,优选X10=V、L,更优选X10=V;X11=G、R、N,优选X11=G、R,更优选X11=G;X12=G、A、V,优选X12=G、A,更优选X12=G;X13=S.P.I.L,优选X13=S、P,更优选X13=S;X14=V、I、L、M,优选X14=V、I,更优选X14=V;X15=S、T、F、R,优选X15=S、T,更优选X15=S;X16=I、V、T、A,优选X16=I、V,更优选X=I;X17=R、K,优选X17=R;X18=R、K,优选X18=R;X19=A、T、D、S、Y,优选X19=A、T;X20=S、F,优选X20=S”。另外,在另一实施方式中,本发明的LF片段也可以在上述共有序列的残基X0的N末端侧和残基X20的C末端侧中的任意一侧或两侧还包含氨基酸序列X。在此情况下,本发明的LF片段包含以下氨基酸序列。X-X0-X1-K-C-X2-X3-X4-Q-X5-X6-X7-X8-X9-X10-X11-X12-P-X13-X14-X15-C-X16-X17-X18-X19-X20-X“在上述氨基酸序列中,X0~X20如上所述,X为由1~16个任意氨基酸残基构成的氨基酸序列。”在又一实施方式中,本发明的LF片段由选自由序列号6~16所示的各氨基酸序列组成的组中的任意一个氨基酸序列构成。其中,序列号6~16是来自各种动物的乳铁蛋白的氨基酸序列(参照下表3)。表3来自各种动物的乳铁蛋白的氨基酸序列物种序列号牛6人7猴8山羊9绵羊10马11骆驼12狗13小鼠14猪15大鼠16如图1所示,序列号6~16所示的氨基酸序列能够通过上述共有序列概括地表示。如以下实施例所示,上述乳铁蛋白片段具有抑制白细胞的细胞外诱捕网形成的活性。此处,对“抑制白细胞的细胞外诱捕网形成的活性”而言,白细胞为来自形成白细胞的细胞外诱捕网的生物的白细胞,优选为来自脊椎动物的白细胞。进一步优选为来自哺乳动物的白细胞。作为哺乳动物的例子,可举出猴、牛、山羊、绵羊、人、骆驼、马、狗、猫、小鼠和大鼠,优选为人。另外,白细胞为来自上述生物的白细胞,同时,优选为选自由中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、单核细胞、巨噬细胞和肥大细胞组成的组中的任意一种,更优选为选自由中性粒细胞、嗜碱性粒细胞、单核细胞、巨噬细胞和肥大细胞组成的组中的任意一种,进一步优选为中性粒细胞。在存在以及不存在上述乳铁蛋白片段即本发明的LF片段的条件下培养上述白细胞,通过显微镜对所述培养体系进行观察,确认在存在本发明的LF片段的条件下细胞外诱捕网的形成减少,从而能够确认抑制白细胞的细胞外诱捕网形成的活性。在确认上述活性的试验中,在添加本发明的LF片段前,优选用细胞外诱捕网形成促进剂(丙二醇甲醚醋酸酯(PMA)、脂多糖(LPS)等)对上述白细胞进行处理。或者,回收上述培养体系的培养上清,测定该上清中的DNA浓度,从而能够确认其抑制白细胞的细胞外诱捕网形成的活性。对于如上所述的DNA浓度而言,其主要源于形成细胞外诱捕网时释放到培养上清中的DNA。在细胞外诱捕网的形成受到本发明的LF片段的抑制的情况下,上清中的DNA浓度与不存在本发明的LF片段的条件相比下降。在此情况下,也优选在添加本发明的LF片段前,用细胞外诱捕网形成促进剂(丙二醇甲醚醋酸酯(PMA)、脂多糖(LPS)等)对上述白细胞进行处理。对于DNA浓度而言,能够用市售的试剂盒(Picogreen双链DNA定量检测试剂(P11496,美国英杰生命技术公司(Invitrogen)))简单地测定。对于各白细胞的培养条件、细胞外诱捕网的确认方法而言,能够参照以下文献:中性粒细胞(Brinkmann,V.等,Science2004;303:1532-1535.)、A.KGupta.FEBSletters2010;584:3193-3197,DJNovo.AntimicrobAgentsChemother.2000;44(4):827-34.)、嗜碱性粒细胞(Yousefi,S.等,NatMed2008;14:949-953.)、肥大细胞(vonM等,Blood2008;111:3070-3080.)、单核细胞(WebsterSJ等,JImmunol2010;185:2968-2979)例如巨噬细胞(Chow,O.A.等,CellHost&Microbe,Volume8,Issue5,445-454,2010年11月18日))。另外,本发明的LF片段也可以用化合物修饰。例如,本发明的LF片段可以是结合了聚乙二醇的修饰蛋白质(日本专利第4195486号、日本专利第4261531号、国际公开公报WO2009/113743)、融合了其他蛋白质或其片段(例如,血中稳定蛋白质IgG、白蛋白或其片段等)的融合蛋白质(特愿2012-98085号)。2.治疗方法通过使用本发明的抑制剂,能有效地抑制白细胞的细胞外诱捕网的形成。即,通过使用本发明的抑制剂,能够治疗与白细胞的细胞外诱捕网形成相关的疾病(以下,称为“本发明的治疗方法”)。本说明书中使用的“治疗”的用语通常是指改善人以及人以外的哺乳动物的症状。另外,“改善”的用语是指,例如与不给药本发明的LF片段的情况相比,疾病的程度减轻的情况以及不恶化的情况,也包含预防的意思。在此情况下,治疗对象(患者)是患有与白细胞的细胞外诱捕网形成相关的疾病或具有患该病风险的生物,优选为脊椎动物,进一步优选为哺乳动物。作为哺乳动物的例子,可举出选自由人、牛、马、山羊、绵羊、狗和猫组成的组中的哺乳动物,进一步优选为人。在本发明的治疗方法中,“与白细胞的细胞外诱捕网形成相关的疾病”只要是可观察到患者体内白细胞的细胞外诱捕网的形成增加的疾病,就没有特别的限定。作为这种疾病,例如,可举出血管炎综合征、ANCA相关性血管炎(韦格纳肉芽肿、显微镜下多血管炎、变应性肉芽肿性血管炎等)、伴有缺血再灌注损伤的急性肾损伤(AKI)、系统性红斑狼疮(SLE)、阑尾炎、曲霉菌感染、肺炎、肺炎双球菌感染、坏死性筋膜炎、链球菌感染、败血症、子痫前期、克罗恩病、血吸虫病、牙周炎、结核病、乳腺炎、疟疾、囊性纤维化病以及深静脉栓塞(vonBruhl,M.L.等,JExpMed.2012年4月9日;209(4):819-35)、心肌梗塞(deBoer,O.J.,ThrombHaemost.2013年2月;109(2):290-7)、肿瘤相关的血栓栓塞(Demers,M.,ProcNatlAcadSciUSA.2012年8月7日;109(32):13076-81)以及弥散性血管内凝血(DisseminatedIntravascularCoagulation,DIC)(TobiasA.等,blood,2011年9月29日,vol.118,no.13,p.3708-3714)等血栓性疾病等(非专利文献2和12)。血管炎综合征根据其发病血管的尺寸而分为大血管炎、中血管炎、小血管炎。上述ANCA相关性血管炎、SLE等与NETs相关的疾病被归类为小血管炎,但在作为中血管炎的重症结节性多动脉炎(心血管疾病的诊断和治疗相关的指导原则(2006-2007年度合同研究班报告))、败血症、实体癌症中也经常合并DIC。对于这些疾病而言,因白细胞的细胞外诱捕网(例如,NETs)的形成而产生的细胞毒性造成血管内皮损伤,因此,产生脏器功能不全。另外,在上述血栓性疾病中,白细胞的细胞外诱捕网(例如,NETs)的形成为诱因,促进了形成血栓的级联反应。认为本发明的LF片段通过抑制白细胞的细胞外诱捕网(例如,NETs)的形成以及释放、扩散,从而预防血管内皮损伤,进一步地通过抑制形成血栓的级联反应,从而表现出保护脏器的作用,发挥治疗上述疾病的效果。作为本发明治疗方法的对象的疾病优选为血管炎综合征、ANCA相关性血管炎(韦格纳肉芽肿、显微镜下多血管炎、变应性肉芽肿性血管炎等)、系统性红斑狼疮、局部性施瓦兹曼(Shwartzman)反应以及伴有缺血再灌注损伤的急性肾损伤(AKI),进一步优选为伴有血中髓过氧化物酶特异性抗中性粒细胞胞质抗体(MyeloperoxidaseSpecificAnti-neutrophilCytoplasmicAntibody,MPO-ANCA)的抗体效价增加的显微镜下多血管炎、变应性肉芽肿性血管炎或弥散性血管内凝血(DIC)。需要说明的是,也报告了使用乳铁蛋白治疗I型糖尿病、类风湿关节炎的自身免疫性疾病(专利文献1),由于白细胞的细胞外诱捕网的形成不被视为I型糖尿病、类风湿关节炎等自身免疫性疾病的主要病因,因此,可以认为在所述报告涉及的治疗中,乳铁蛋白不通过细胞外诱捕网的形成而发挥作用的可能性高。即,可以认为在本发明中,乳铁蛋白片段通过全新的机制即抑制白细胞的细胞外诱捕网形成的机制对上述疾病表现出治疗作用。对于SLE的治疗、因ANCA导致的疾病的治疗而言,使用类固醇、免疫抑制剂等,但是,在所述治疗方法中,除了伴随有患者的身体负担(副作用等)、给患者强加痛苦以外,还存在诱发其他疾病(感染病)的风险高的问题。相对于此,在本发明中,由于使用以往食品中所含的乳铁蛋白片段作为有效成分,因此,具有副作用少、不会给患者强加痛苦、诱发其他疾病的风险也低的优点。3.组合物作为本发明的另一实施方式,提供包含本发明的LF片段、用于治疗与白细胞的细胞外诱捕网形成相关的疾病的组合物(以下记作“本发明的组合物”)。此处,“组合物”的用语是指含有在本发明的有用活性成分(本发明的乳铁蛋白片段)的制备中使用的载体等添加物的组合物。在本发明的组合物中,“本发明的LF片段”以及“与白细胞的细胞外诱捕网形成相关的疾病”如上所述。对本发明的组合物的给药途径而言,只要是通常采用的途径,就没有特别的限定,作为具体例,可举出口服、舌下、经鼻、经肺、经消化道、经皮、滴眼、静脉注射、皮下注射、肌肉注射、腹腔注射、局部注射、外科植入,优选为口服给药和静脉给药。作为本发明的组合物,可以为胶囊、片剂、粉末等固体制剂,也可以为溶液、混悬液或乳液等溶液剂、或者为软膏、霜或膏等半液体制剂。本发明在口服给药的情况下,组合物优选为固体制剂。另外,在注射剂的情况下,其为加入了冷冻干燥方法等的固体制剂或溶液剂。在经皮给药的情况下,组合物可以制备成溶液、混悬液或乳液等溶液剂(包括喷雾剂)、或软膏、霜或膏等半液体制剂、或者也可以制备成湿敷剂。本发明的LF片段也可以添加在食品、饲料中,以食品或饲料的方式被人或除人以外的对象动物摄取。这种食品或饲料的制造方法也是本领域普通技术人员公知的。另外,也可以制备成溶液制剂、注射剂。进一步地,可以将本发明的LF片段直接添加到营养剂、饮食品等中、或者在制成制剂后添加到营养剂、饮食品等中。本发明的LF片段可以单独使用、或者也可以与药理学上可容许的其他成分一同调配。例如,在制备成粉末剂、颗粒剂、片剂、胶囊剂等口服给药用组合物的情况下,通过常用方法使用淀粉、乳糖、白糖、甘露醇、羧甲基纤维素、玉米淀粉、无机盐类等制成制剂。在这种组合物中,除了所述赋形剂以外,还能够适当使用包衣剂、粘合剂、崩解剂、表面活性剂、润滑剂、流动性促进剂、着色剂、香料等。本发明的组合物能包含治疗上有效量的作为有效成分的乳铁蛋白片段。此处,“治疗上有效量”是指,与不给药乳铁蛋白片段的情况相比,通过将该量的有效成分给药于对象从而使与白细胞的细胞外诱捕网形成相关的疾病的症状减轻的情况以及不恶化的量,也包含有效预防的量。例如,在口服给药的情况下,治疗上有效量能够设为0.001~10g/kg/天、0.005~10g/kg/天、0.01~10g/kg/天、0.01~5g/kg/天。在对人给药的情况下,作为治疗上有效量,通常为每天10mg~15000mg、10mg~12000mg、10mg~10000mg、20mg~10000mg、20mg~8000mg、30mg~8000mg、30mg~6000mg的量。另外,在经皮给药的情况下,治疗上有效量能够设为0.001~10g/kg/天、0.005~10g/kg/天、0.01~10g/kg/天、0.01~5g/kg/天。在对人给药的情况下,作为治疗上有效量,通常为每天10mg~15000mg、10mg~12000mg、10mg~10000mg、20mg~10000mg、20mg~8000mg、30mg~8000mg、30mg~6000mg的量。能够将如上所述的每天的用量一次或分几次地对需要治疗与白细胞的细胞外诱捕网形成相关的疾病的患者进行给药。需要说明的是,本发明的组合物的给药量和给药频率依赖于对象的物种、体重、性别、年龄、肿瘤疾病的进展程度、给药途径这样的各种主要因素而变化,医师、兽医师、牙科医师或药剂师等本领域普通技术人员能够考虑各种主要因素来决定给药量。作为上述治疗上有效量、给药量和给药频率,列举了典型的数值,也充分考虑大于或小于该数值的数值也发挥治疗效果的情况。因此,即使是大于或小于上述治疗上有效量、给药量和给药频率的数值,也被包含在本发明的组合物的治疗上有效量、给药量和给药频率中。下面,使用实施例详细地说明本发明,但本发明并不限定于实施例所记载的实施方式。实施例下面,使用实施例详细地说明本发明,但本发明并不限定于实施例所记载的实施方式。来自乳铁蛋白的肽片段前处理引起的抑制健康人末梢血中性粒细胞的NETs形成刺激的效果1.人中性粒细胞的分离方法用含有乙二胺四乙酸(EthyleneDiamineTetraaceticAcid,EDTA)的注射器(18~22G针)从健康人中采集15ml~20ml的末梢血以用于一次实验。采血后,在加入了3ml的单聚分解培养基(Mono-PolyResolvingMedium)(货号DSBN100,DS医药生物医学公司(DSPharmaBiomedical))的15ml锥形管中,使下层的单聚分离培养基和3.5ml全血静静地分层。在室温(15~30℃)条件下用摇摆式离心分离机(スイング式の遠心分離機)将15ml锥形管在400×g的条件下离心20分钟,轻轻地取出锥形管。用吸气器(アスピレーター)等除去最上部的褐色血浆层和与其邻接的下层的淋巴细胞/单核细胞层。另外,尽可能地除去淋巴细胞/单核细胞层的下层的透明层。用巴斯德吸管吸取位于透明层的下层的淡粉色层,并转移至加入了磷酸缓冲生理盐水(磷酸盐缓冲液(PhosphateBuffersolution,PBS)(-);氯化钠137mM、氯化钾2.7mM、磷酸氢二钠十二水合物8.1mM、磷酸二氢钾1.47mM)的试管以洗涤中性粒细胞。在室温(15~30℃)条件下将加入了中性粒细胞的试管在200×g的条件下离心10分钟。取出试管,弃去上清。在试管中,将4℃的灭菌水加入到中性粒细胞中,在冰上静置30秒,使混有的红细胞溶血。溶血后,加入45ml的PBS(-),在200×g的条件下离心10分钟。取出试管,弃去上清,使沉淀物混悬于杜尔贝科(Dulbecco)改良伊格尔(Eagle)培养基(Dulbecco'sModifiedEagle'sMedium,DMEM)+2%人血清白蛋白(Serumhumanalbumin;产品编号A9080西格玛(SIGMA)+4mM的L-谷氨酰胺)中,使用前保存在8℃的条件下。能分离的中性粒细胞的数量为1×106个/ml~1×107个/ml,关于纯度,对经细胞离心涂片机(cytospin)处理后的检体进行姬姆萨(Giemsa)染色处理并目视计数,纯度为95~98%。2.中性粒细胞的前处理方法(抑制NETs形成)和Netosis(NETs形成)的诱导方法在进行上述“1.人中性粒细胞的分离方法”中记载的中性粒细胞分离后约1小时后进行中性粒细胞的前处理。在μ-Slide8孔腔室载玻片(8well-μslide)(货号ib80826Ibidi(注册商标))中,将中性粒细胞以约1.0×105个细胞/孔的方式撒在400μl的培养基DMEM+2%人血清白蛋白(Serumhumanalbumin;产品编号A9080西格玛(SIGMA)+4mM的L-谷氨酰胺)中,添加乳铁蛋白肽片段,在室温下进行30分钟的前处理。3.培养上清中的DNA浓度测定方法回收培养上清,在200×g的条件下离心10分钟,将上清转移至新的微型离心管中。使用Picogreen双链DNA定量检测试剂(P11496,美国英杰生命技术公司(Invitrogen)),按照附带的实验方案对DNA量进行测定。对人乳铁蛋白进行前处理后,浓度依赖性地降低培养上清中的DNA浓度,抑制了因NETs引起的DNA释放。4.来自牛乳铁蛋白的碱性肽和酸性肽的制备方法将牛乳铁蛋白溶解在无菌水中以使最终量成为5%(w/v),用盐酸将水溶液的pH降低至2.5。然后,在乳铁蛋白溶液中加入胃蛋白酶(E/S=1/50),在37℃的条件下静置5分钟。用氢氧化钠将水溶液配制成pH=7.0,从而使乳铁蛋白的水解停止。使用AKTAExplorer10S(通用电气医疗集团日本公司(GEヘルスケア·ジャパン))对乳铁蛋白的碱性肽进行分离纯化。作为洗脱梯度,采用加入有2M氯化钠的20mM磷酸钠缓冲液(pH=7.0)、加入有2M氯化铵的20mM磷酸缓冲液(pH=7.0)洗脱乳铁蛋白的碱性肽(序列号6)以除去杂质和乳铁蛋白未消化物。对于乳铁蛋白的酸性肽(由美国国立生物技术信息中心(NationalCenterofBiotechnologyInformation,NCBI)蛋白质数据库登记号3IAZ_A、3IB1_A、3IB0_A、3IB2_A、4OQO_A和4OQO_B所示的各氨基酸序列的第316~332位氨基酸残基构成的各肽)而言,使用ABI433A多肽合成仪(美国生命技术公司(ライフテクノロジー社))按照F-MOC法(9-芴甲氧羰基法)进行化学合成。采用PPSQ-21A型蛋白质测序仪(株式会社岛津制作所)对制备肽的氨基酸序列进行解析。5.碱性肽的制备其他碱性肽(序列号6和7)的制备委托给日本PH公司。6.结果来自乳铁蛋白的酸性肽并不抑制NETs。对于碱性肽(序列号6)而言,能够观察到其对编码乳铁蛋白区域的抑制效果(图2)。另外,编码乳铁蛋白的肽区域(序列号6和7)剂量依赖性地抑制NETs的形成(图3)。工业实用性本发明能够提供一种针对因白细胞的细胞外诱捕网形成而产生的疾病的、副作用少的治疗方法。另外,由于副作用少,所以具有能够安心用于广范围的患者和患者后备军的优点。另外,由于确认了本发明在非自身免疫性疾病模型中对白细胞的细胞外诱捕网的形成的抑制能力,因此,可以认为在本发明中,乳铁蛋白片段通过不同于过去已报告的作用机制(专利文献1)的全新作用机制表现出治疗作用。序列表<110>NRL制药股份有限公司学校法人庆应义塾川上浩<120>白细胞的细胞外诱捕网抑制剂<130>G1239WO<150>JP2014-207415<151>2014-10-08<160>16<170>PatentInversion3.5<210>1<211>666<212>蛋白质<213>智人<400>1MetArgLysValArgGlyProProValSerCysIleLysArgAspSer151015ProIleGlnCysIleGlnAlaIleAlaGluAsnArgAlaAspAlaVal202530ThrLeuAspGlyGlyPheIleTyrGluAlaGlyLeuAlaProTyrLys354045LeuArgProValAlaAlaGluValTyrGlyThrGluArgGlnProArg505560ThrHisTyrTyrAlaValAlaValValLysLysGlyGlySerPheGln65707580LeuAsnGluLeuGlnGlyLeuLysSerCysHisThrGlyLeuArgArg859095ThrAlaGlyTrpAsnValProIleGlyThrLeuArgProPheLeuAsn100105110TrpThrGlyProProGluProIleGluAlaAlaValAlaArgPhePhe115120125SerAlaSerCysValProGlyAlaAspLysGlyGlnPheProAsnLeu130135140CysArgLeuCysAlaGlyThrGlyGluAsnLysCysAlaPheSerSer145150155160GlnGluProTyrPheSerTyrSerGlyAlaPheLysCysLeuArgAsp165170175GlyAlaGlyAspValAlaPheIleArgGluSerThrValPheGluAsp180185190LeuSerAspGluAlaGluArgAspGluTyrGluLeuLeuCysProAsp195200205AsnThrArgLysProValAspLysPheLysAspCysHisLeuAlaArg210215220ValProSerHisAlaValValAlaArgSerValAsnGlyLysGluAsp225230235240AlaIleTrpAsnLeuLeuArgGlnAlaGlnGluLysPheGlyLysAsp245250255LysSerProLysPheGlnLeuPheGlySerProSerGlyGlnLysAsp260265270LeuLeuPheLysAspSerAlaIleGlyPheSerArgValProProArg275280285IleAspSerGlyLeuTyrLeuGlySerGlyTyrPheThrAlaIleGln290295300AsnLeuArgLysSerGluGluGluValAlaAlaArgArgAlaArgVal305310315320ValTrpCysAlaValGlyGluGlnGluLeuArgLysCysAsnGlnTrp325330335SerGlyLeuSerGluGlySerValThrCysSerSerAlaSerThrThr340345350GluAspCysIleAlaLeuValLeuLysGlyGluAlaAspAlaMetSer355360365LeuAspGlyGlyTyrValTyrThrAlaGlyLysCysGlyLeuValPro370375380ValLeuAlaGluAsnTyrLysSerGlnGlnSerSerAspProAspPro385390395400AsnCysValAspArgProValGluGlyTyrLeuAlaValAlaValVal405410415ArgArgSerAspThrSerLeuThrTrpAsnSerValLysGlyLysLys420425430SerCysHisThrAlaValAspArgThrAlaGlyTrpAsnIleProMet435440445GlyLeuLeuPheAsnGlnThrGlySerCysLysPheAspGluTyrPhe450455460SerGlnSerCysAlaProGlySerAspProArgSerAsnLeuCysAla465470475480LeuCysIleGlyAspGluGlnGlyGluAsnLysCysValProAsnSer485490495AsnGluArgTyrTyrGlyTyrThrGlyAlaPheArgCysLeuAlaGlu500505510AsnAlaGlyAspValAlaPheValLysAspValThrValLeuGlnAsn515520525ThrAspGlyAsnAsnAsnGluAlaTrpAlaLysAspLeuLysLeuAla530535540AspPheAlaLeuLeuCysLeuAspGlyLysArgLysProValThrGlu545550555560AlaArgSerCysHisLeuAlaMetAlaProAsnHisAlaValValSer565570575ArgMetAspLysValGluArgLeuLysGlnValLeuLeuHisGlnGln580585590AlaLysPheGlyArgAsnGlySerAspCysProAspLysPheCysLeu595600605PheGlnSerGluThrLysAsnLeuLeuPheAsnAspAsnThrGluCys610615620LeuAlaArgLeuHisGlyLysThrThrTyrGluLysTyrLeuGlyPro625630635640GlnTyrValAlaGlyIleThrAsnLeuLysLysCysSerThrSerPro645650655LeuLeuGluAlaCysGluPheLeuArgLys660665<210>2<211>708<212>蛋白质<213>牛<400>2MetLysLeuPheValProAlaLeuLeuSerLeuGlyAlaLeuGlyLeu151015CysLeuAlaAlaProArgLysAsnValArgTrpCysThrIleSerGln202530ProGluTrpPheLysCysArgArgTrpGlnTrpArgMetLysLysLeu354045GlyAlaProSerIleThrCysValArgArgAlaPheAlaLeuGluCys505560IleArgAlaIleAlaGluLysLysAlaAspAlaValThrLeuAspGly65707580GlyMetValPheGluAlaGlyArgAspProTyrLysLeuArgProVal859095AlaAlaGluIleTyrGlyThrLysGluSerProGlnThrHisTyrTyr100105110AlaValAlaValValLysLysGlySerAsnPheGlnLeuAspGlnLeu115120125GlnGlyArgLysSerCysHisThrGlyLeuGlyArgSerAlaGlyTrp130135140IleIleProMetGlyIleLeuArgProTyrLeuSerTrpThrGluSer145150155160LeuGluProLeuGlnGlyAlaValAlaLysPhePheSerAlaSerCys165170175ValProCysIleAspArgGlnAlaTyrProAsnLeuCysGlnLeuCys180185190LysGlyGluGlyGluAsnGlnCysAlaCysSerSerArgGluProTyr195200205PheGlyTyrSerGlyAlaPheLysCysLeuGlnAspGlyAlaGlyAsp210215220ValAlaPheValLysGluThrThrValPheGluAsnLeuProGluLys225230235240AlaAspArgAspGlnTyrGluLeuLeuCysLeuAsnAsnSerArgAla245250255ProValAspAlaPheLysGluCysHisLeuAlaGlnValProSerHis260265270AlaValValAlaArgSerValAspGlyLysGluAspLeuIleTrpLys275280285LeuLeuSerLysAlaGlnGluLysPheGlyLysAsnLysSerArgSer290295300PheGlnLeuPheGlySerProProGlyGlnArgAspLeuLeuPheLys305310315320AspSerAlaLeuGlyPheLeuArgIleProSerLysValAspSerAla325330335LeuTyrLeuGlySerArgTyrLeuThrThrLeuLysAsnLeuArgGlu340345350ThrAlaGluGluValLysAlaArgTyrThrArgValValTrpCysAla355360365ValGlyProGluGluGlnLysLysCysGlnGlnTrpSerGlnGlnSer370375380GlyGlnAsnValThrCysAlaThrAlaSerThrThrAspAspCysIle385390395400ValLeuValLeuLysGlyGluAlaAspAlaLeuAsnLeuAspGlyGly405410415TyrIleTyrThrAlaGlyLysCysGlyLeuValProValLeuAlaGlu420425430AsnArgLysSerSerLysHisSerSerLeuAspCysValLeuArgPro435440445ThrGluGlyTyrLeuAlaValAlaValValLysLysAlaAsnGluGly450455460LeuThrTrpAsnSerLeuLysAspLysLysSerCysHisThrAlaVal465470475480AspArgThrAlaGlyTrpAsnIleProMetGlyLeuIleValAsnGln485490495ThrGlySerCysAlaPheAspGluPhePheSerGlnSerCysAlaPro500505510GlyAlaAspProLysSerArgLeuCysAlaLeuCysAlaGlyAspAsp515520525GlnGlyLeuAspLysCysValProAsnSerLysGluLysTyrTyrGly530535540TyrThrGlyAlaPheArgCysLeuAlaGluAspValGlyAspValAla545550555560PheValLysAsnAspThrValTrpGluAsnThrAsnGlyGluSerThr565570575AlaAspTrpAlaLysAsnLeuAsnArgGluAspPheArgLeuLeuCys580585590LeuAspGlyThrArgLysProValThrGluAlaGlnSerCysHisLeu595600605AlaValAlaProAsnHisAlaValValSerArgSerAspArgAlaAla610615620HisValLysGlnValLeuLeuHisGlnGlnAlaLeuPheGlyLysAsn625630635640GlyLysAsnCysProAspLysPheCysLeuPheLysSerGluThrLys645650655AsnLeuLeuPheAsnAspAsnThrGluCysLeuAlaLysLeuGlyGly660665670ArgProThrTyrGluGluTyrLeuGlyThrGluTyrValThrAlaIle675680685AlaAsnLeuLysLysCysSerThrSerProLeuLeuGluAlaCysAla690695700PheLeuThrArg705<210>3<211>708<212>蛋白质<213>绵羊<400>3MetLysLeuPheValProAlaLeuLeuSerLeuGlyAlaLeuGlyLeu151015CysLeuAlaAlaProArgLysAsnValArgTrpCysAlaIleSerPro202530ProGluGlySerLysCysTyrGlnTrpGlnArgArgMetArgLysLeu354045GlyAlaProSerIleThrCysValArgArgThrSerAlaLeuGluCys505560IleArgAlaIleAlaGlyLysLysAlaAspAlaValThrLeuAspSer65707580GlyMetValPheGluAlaGlyLeuAspProTyrLysLeuArgProVal859095AlaAlaGluIleTyrGlyThrGluLysSerProGlnThrHisTyrTyr100105110AlaValAlaValValLysLysGlySerAsnPheGlnLeuAspGlnLeu115120125GlnGlyGlnLysSerCysHisMetGlyLeuGlyArgSerAlaGlyTrp130135140AsnIleProMetGlyIleLeuArgProPheLeuSerTrpThrGluSer145150155160AlaGluProLeuGlnGlyAlaValAlaArgPhePheSerAlaSerCys165170175ValProCysValAspGlyLysAlaTyrProAsnLeuCysGlnLeuCys180185190LysGlyValGlyGluAsnLysCysAlaCysSerSerGlnGluProTyr195200205PheGlyTyrSerGlyAlaPheLysCysLeuGlnAspGlyAlaGlyAsp210215220ValAlaPheValLysGluThrThrValPheGluAsnLeuProGluLys225230235240AlaAspArgAspGlnTyrGluLeuLeuCysLeuAsnAsnThrArgAla245250255ProValAspAlaPheLysGluCysHisLeuAlaGlnValProSerHis260265270AlaValValAlaArgSerValAspGlyLysGluAsnLeuIleTrpGlu275280285LeuLeuArgLysAlaGlnGluLysPheGlyLysAsnLysSerGlnArg290295300PheGlnLeuPheGlySerProGlnGlyGlnLysAspLeuLeuPheLys305310315320AspSerAlaLeuGlyPheValArgIleProSerLysValAspSerAla325330335LeuTyrLeuGlySerArgTyrLeuThrAlaLeuLysAsnLeuArgGlu340345350ThrAlaGluGluValLysAlaArgCysThrArgValValTrpCysAla355360365ValGlyProGluGluHisSerLysCysGlnGlnTrpSerGluGlnSer370375380GlyGlnAsnValThrCysAlaMetAlaSerThrThrAspAspCysIle385390395400AlaLeuValLeuLysGlyGluAlaAspAlaLeuSerLeuAspGlyGly405410415TyrIleTyrThrAlaGlyLysCysGlyLeuValProValMetAlaGlu420425430AsnArgGluSerSerLysTyrSerSerLeuAspCysValLeuArgPro435440445ThrGluGlyTyrLeuAlaValAlaValValLysLysAlaAsnGluGly450455460LeuThrTrpAsnSerLeuLysGlyLysLysSerCysHisThrAlaVal465470475480AspArgThrAlaGlyTrpAsnIleProMetGlyLeuIleAlaAsnGln485490495ThrGlySerCysAlaPheAspGluPhePheSerGlnSerCysAlaPro500505510GlyAlaAspProLysSerSerLeuCysAlaLeuCysAlaGlyAspAsp515520525GlnGlyLeuAsnLysCysValProAsnSerLysGluLysTyrTyrGly530535540TyrThrGlyAlaPheArgCysLeuAlaGluAspValGlyAspValAla545550555560PheValLysAsnAspThrValTrpGluAsnThrAsnGlyGluSerSer565570575AlaAspTrpAlaLysAsnLeuAsnArgGluAspPheArgLeuLeuCys580585590LeuAspGlyThrThrLysProValThrGluAlaGlnSerCysTyrLeu595600605AlaValAlaProAsnHisAlaValValSerArgSerAspArgAlaAla610615620HisValGluGlnValLeuLeuHisGlnGlnAlaLeuPheGlyLysAsn625630635640GlyLysAsnCysProAspGlnPheCysLeuPheLysSerGluThrLys645650655AsnLeuLeuPheAsnAspAsnThrGluCysLeuAlaLysLeuGlyGly660665670ArgProThrTyrGluLysTyrLeuGlyThrGluTyrValThrAlaIle675680685AlaAsnLeuLysLysCysSerThrSerProLeuLeuGluAlaCysAla690695700PheLeuThrArg705<210>4<211>708<212>蛋白质<213>山羊<400>4MetLysLeuPheValProAlaLeuLeuSerLeuGlyAlaLeuGlyLeu151015CysLeuAlaAlaProArgLysAsnValArgTrpCysAlaIleSerLeu202530ProGluTrpSerLysCysTyrGlnTrpGlnArgArgMetArgLysLeu354045GlyAlaProSerIleThrCysIleArgArgThrSerAlaLeuGluCys505560IleArgAlaIleAlaGlyLysAsnAlaAspAlaValThrLeuAspSer65707580GlyMetValPheGluAlaGlyLeuAspProTyrLysLeuArgProVal859095AlaAlaGluIleTyrGlyThrGluLysSerProGlnThrHisTyrTyr100105110AlaValAlaValValLysLysGlySerAsnPheGlnLeuAspGlnLeu115120125GlnGlyGlnLysSerCysHisMetGlyLeuGlyArgSerAlaGlyTrp130135140AsnIleProValGlyIleLeuArgProPheLeuSerTrpThrGluSer145150155160AlaGluProLeuGlnGlyAlaValAlaArgPhePheSerAlaSerCys165170175ValProCysValAspGlyLysAlaTyrProAsnLeuCysGlnLeuCys180185190LysGlyValGlyGluAsnLysCysAlaCysSerSerGlnGluProTyr195200205PheGlyTyrSerGlyAlaPheLysCysLeuGlnAspGlyAlaGlyAsp210215220ValAlaPheValLysGluThrThrValPheGluAsnLeuProGluLys225230235240AlaAspArgAspGlnTyrGluLeuLeuCysLeuAsnAsnThrArgAla245250255ProValAspAlaPheLysGluCysHisLeuAlaGlnValProSerHis260265270AlaValValAlaArgSerValAspGlyLysGluAsnLeuIleTrpGlu275280285LeuLeuArgLysAlaGlnGluLysPheGlyLysAsnLysSerGlnSer290295300PheGlnLeuPheGlySerProGluGlyArgArgAspLeuLeuPheLys305310315320AspSerAlaLeuGlyPheValArgIleProSerLysValAspSerAla325330335LeuTyrLeuGlySerArgTyrLeuThrAlaLeuLysAsnLeuArgGlu340345350ThrAlaGluGluLeuLysAlaArgCysThrArgValValTrpCysAla355360365ValGlyProGluGluGlnSerLysCysGlnGlnTrpSerGluGlnSer370375380GlyGlnAsnValThrCysAlaThrAlaSerThrThrAspAspCysIle385390395400AlaLeuValLeuLysGlyGluAlaAspAlaLeuSerLeuAspGlyGly405410415TyrIleTyrThrAlaGlyLysCysGlyLeuValProValMetAlaGlu420425430AsnArgLysSerSerLysTyrSerSerLeuAspCysValLeuArgPro435440445ThrGluGlyTyrLeuAlaValAlaValValLysLysAlaAsnGluGly450455460LeuThrTrpAsnSerLeuLysGlyLysLysSerCysHisThrAlaVal465470475480AspArgThrAlaGlyTrpAsnIleProMetGlyLeuIleAlaAsnGln485490495ThrGlySerCysAlaPheAspGluPhePheSerGlnSerCysAlaPro500505510GlyAlaAspProLysSerSerLeuCysAlaLeuCysAlaGlyAspAsp515520525GlnGlyLeuAspLysCysValProAsnSerLysGluLysTyrTyrGly530535540TyrThrGlyAlaPheArgCysLeuAlaGluAspValGlyAspValAla545550555560PheValLysAsnAspThrValTrpGluAsnThrAsnGlyGluSerSer565570575AlaAspTrpAlaLysAsnLeuAsnArgGluAspPheArgLeuLeuCys580585590LeuAspGlyThrThrLysProValThrGluAlaGlnSerCysTyrLeu595600605AlaValAlaProAsnHisAlaValValSerArgSerAspArgAlaAla610615620HisValGluGlnValLeuLeuHisGlnGlnAlaLeuPheGlyLysAsn625630635640GlyLysAsnCysProAspGlnPheCysLeuPheLysSerGluThrLys645650655AsnLeuLeuPheAsnAspAsnThrGluCysLeuAlaLysLeuGlyGly660665670ArgProThrTyrGluLysTyrLeuGlyThrGluTyrValThrAlaIle675680685AlaAsnLeuLysLysCysSerThrSerProLeuLeuGluAlaCysAla690695700PheLeuThrArg705<210>5<211>695<212>蛋白质<213>马<400>5LeuGlyLeuCysLeuAlaAlaProArgLysSerValArgTrpCysThr151015IleSerProAlaGluAlaAlaLysCysAlaLysPheGlnArgAsnMet202530LysLysValArgGlyProSerValSerCysIleArgLysThrSerSer354045PheGluCysIleGlnAlaIleAlaAlaAsnLysAlaAspAlaValThr505560LeuAspGlyGlyLeuValTyrGluAlaGlyLeuHisProTyrLysLeu65707580ArgProValAlaAlaGluValTyrGlnThrArgGlyLysProGlnThr859095ArgTyrTyrAlaValAlaValValLysLysGlySerGlyPheGlnLeu100105110AsnGlnLeuGlnGlyValLysSerCysHisThrGlyLeuGlyArgSer115120125AlaGlyTrpAsnIleProIleGlyThrLeuArgProTyrLeuAsnTrp130135140ThrGlyProProGluProLeuGlnLysAlaValAlaAsnPhePheSer145150155160AlaSerCysValProCysAlaAspGlyLysGlnTyrProAsnLeuCys165170175ArgLeuCysAlaGlyThrGluAlaAspLysCysAlaCysSerSerGln180185190GluProTyrPheGlyTyrSerGlyAlaPheLysCysLeuGluAsnGly195200205AlaGlyAspValAlaPheValLysAspSerThrValPheGluAsnLeu210215220ProAspGluAlaAspArgAspLysTyrGluLeuLeuCysProAspAsn225230235240ThrArgLysProValAspAlaPheLysGluCysHisLeuAlaArgVal245250255ProSerHisAlaValValAlaArgSerValAspGlyArgGluAspLeu260265270IleTrpArgLeuLeuHisArgAlaGlnGluGluPheGlyArgAsnLys275280285SerSerAlaPheGlnLeuPheLysSerThrProGluAsnLysAspLeu290295300LeuPheLysAspSerAlaLeuGlyPheValArgIleProSerGlnIle305310315320AspSerGlyLeuTyrLeuGlyAlaAsnTyrLeuThrAlaThrGlnAsn325330335LeuArgGluThrAlaAlaGluValAlaAlaArgArgGluArgValVal340345350TrpCysAlaValGlyProGluGluGluArgLysCysLysGlnTrpSer355360365AspValSerAsnArgLysValAlaCysAlaSerAlaSerThrThrGlu370375380GluCysIleAlaLeuValLeuLysGlyGluAlaAspAlaLeuAsnLeu385390395400AspGlyGlyPheIleTyrValAlaGlyLysCysGlyLeuValProVal405410415LeuAlaGluAsnGlnLysSerGlnAsnSerAsnAlaProAspCysVal420425430HisArgProProGluGlyTyrLeuAlaValAlaValValArgLysSer435440445AspAlaAspLeuThrTrpAsnSerLeuSerGlyLysLysSerCysHis450455460ThrGlyValGlyArgThrAlaAlaTrpAsnIleProMetGlyLeuLeu465470475480PheAsnGlnThrGlySerCysLysPheAspLysPhePheSerGlnSer485490495CysAlaProGlyAlaAspProGlnSerSerLeuCysAlaLeuCysVal500505510GlyAsnAsnGluAsnGluAsnLysCysMetProAsnSerGluGluArg515520525TyrTyrGlyTyrThrGlyAlaPheArgCysLeuAlaGluLysAlaGly530535540AspValAlaPheValLysAspValThrValLeuGlnAsnThrAspGly545550555560LysAsnSerGluProTrpAlaLysAspLeuLysGlnGluAspPheGlu565570575LeuLeuCysLeuAspGlyThrArgLysProValAlaGluAlaGluSer580585590CysHisLeuAlaArgAlaProAsnHisAlaValValSerGlnSerAsp595600605ArgAlaGlnHisLeuLysLysValLeuPheLeuGlnGlnAspGlnPhe610615620GlyGlyAsnGlyProAspCysProGlyLysPheCysLeuPheLysSer625630635640GluThrLysAsnLeuLeuPheAsnAspAsnThrGluCysLeuAlaGlu645650655LeuGlnGlyLysThrThrTyrGluGlnTyrLeuGlySerGluTyrVal660665670ThrSerIleThrAsnLeuArgArgCysSerSerSerProLeuLeuGlu675680685AlaCysAlaPheLeuArgAla690695<210>6<211>26<212>蛋白质<213>牛<400>6MetPheLysCysArgArgTrpGlnTrpArgMetLysLysLeuGlyAla151015ProSerIleThrCysValArgArgAlaPhe2025<210>7<211>49<212>蛋白质<213>智人<400>7GlyArgArgArgArgSerValGlnTrpCysAlaValSerGlnProGlu151015AlaThrLysCysPheGlnTrpGlnArgAsnMetArgLysValArgGly202530ProProValSerCysIleLysArgAspSerProIleGlnCysIleGln354045Ala<210>8<211>26<212>蛋白质<213>台湾猕猴<400>8AlaThrLysCysSerGlnTrpGlnArgAsnLeuArgArgValArgGly151015ProProValSerCysIleLysArgAlaSer2025<210>9<211>26<212>蛋白质<213>山羊<400>9TrpSerLysCysTyrGlnTrpGlnArgArgMetArgLysLeuGlyAla151015ProSerIleThrCysIleArgArgThrSer2025<210>10<211>26<212>蛋白质<213>绵羊<400>10GlySerLysCysTyrGlnTrpGlnArgArgMetArgLysLeuGlyAla151015ProSerIleThrCysValArgArgThrSer2025<210>11<211>26<212>蛋白质<213>马<400>11AlaAlaLysCysAlaLysPheGlnArgAsnMetLysLysValArgGly151015ProSerValSerCysIleArgLysThrSer2025<210>12<211>26<212>蛋白质<213>单峰驼<400>12SerSerLysCysAlaGlnTrpGlnArgArgMetLysLysValArgGly151015ProSerValThrCysValLysLysThrSer2025<210>13<211>26<212>蛋白质<213>家犬<400>13AlaLysLysCysSerLysPheGlnValAsnMetLysLysValGlyGly151015ProIleValSerCysThrArgLysAlaSer2025<210>14<211>26<212>蛋白质<213>小家鼠<400>14GluGluLysCysLeuArgTrpGlnAsnGluMetArgLysValGlyGly151015ProProLeuSerCysValLysLysSerSer2025<210>15<211>26<212>蛋白质<213>家猪<400>15TyrSerLysCysArgGlnTrpGlnSerLysIleArgArgThrAsnPro151015MetPheCysIleArgArgAlaSerProThr2025<210>16<211>26<212>蛋白质<213>大白鼠<400>16AlaGlnLysCysPheMetTrpGlnGluMetLeuAsnLysAlaGlyVal151015ProLysLeuArgCysAlaArgLysTyrPhe2025当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种RNA抑制剂及其在肿瘤中的应用的制作方法与工艺
- 固氮鱼腥藻细胞受ALS抑制剂类除草剂损伤的修复方法与流程
- 一种修复细胞DNA损伤的抑制剂及其制作方法和应用与流程
- 一种修复细胞DNA损伤的抑制剂及其制作方法和应用与流程
- TLR3抑制剂在制备防治肿瘤转移产品中的应用的制作方法与工艺
- 一种提高酵母细胞对复合抑制剂耐受能力的方法与流程
- 免疫检查点抑制剂在中枢神经系统肿瘤中的用途的制造方法与工艺
- 作为MIDH1抑制剂用于治疗肿瘤的1‑环己基‑2‑苯基氨基苯并咪唑的制造方法与工艺
- 具有细胞渗透性的BCL‑XL抑制剂的抗体药物缀合物的制造方法与工艺
- 用于增强干细胞功能的内含抑制素纳米粒子制剂、以及含有其的功能增强干细胞及其制备方法与流程