靶向B‑细胞成熟抗原的抗体及其用途的制作方法
相关申请的交叉引用
本申请要求2014年12月5日提交的序列号为62/088,246的美国临时专利申请的优先权,在此将其全部内容引入本文以供参考,并要求其优先权。
本发明公开的主题涉及与b-细胞成熟抗原(bcma)结合的抗体及其使用方法。
背景技术:
bcma涉及b细胞分化和信号传导,已知在非恶性分化b细胞和浆细胞上表达。已经证实若干组bcma在多发性骨髓瘤(mm)上有表面表达,发现一组是cd138的替代物,其作为来自新鲜或冷冻患者骨髓样品的恶性浆细胞的facs标记物,其平均相对平均荧光强度(mfi)为9-16(n=35)(frigyesi,i.等人,robustisolationofmalignantplasmacellsinmultiplemyeloma.blood123,1336-1340(2014);tai,y.t.等人,novelafucosylatedanti-bcellmaturationantigen-monomethylauristatinfantibody-drugconjugate(gsk2857916)inducespotentandselectiveanti-multiplemyelomaactivity.blood(2014))。考虑到bcma在多发性骨髓瘤中的重要作用,期望识别bcma的抗体及使用该药剂的方法。
技术实现要素:
本发明公开的主题在于提供与b-细胞成熟抗原(bcma)结合的抗体及其使用方法。
在某些实施方式中,本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:包括与选自seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61和65的氨基酸序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸序列的重链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:包括与选自seqidno:2、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62和66的氨基酸序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸序列的轻链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。而且,本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:(a)包括与选自seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61和65的氨基酸序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸序列的重链可变区;和(b)包括与选自seqidno:2、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62和66的氨基酸序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸序列的轻链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。
此外,本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:包括选自seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61、65的氨基酸序列及其保守修饰的重链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:包括选自seqidno:2、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62、66的氨基酸序列及其保守修饰的轻链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。而且,本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:(a)包括选自seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61、65的氨基酸序列及其保守修饰的重链可变区;和(b)包括选自seqidno:、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62、66的氨基酸序列及其保守修饰的轻链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。
本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括重链可变区和轻链可变区,其中重链可变区和轻链可变区选自:(a)包括序列与seqidno:1所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:2所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(b)包括序列与seqidno:5所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:6所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(c)包括序列与seqidno:9所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:10所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(d)包括序列与seqidno:13所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:14所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(e)包括序列与seqidno:17所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:18所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(f)包括序列与seqidno:21所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:22所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(g)包括序列与seqidno:25所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:26所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(h)包括序列与seqidno:29所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:30所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(i)包括序列与seqidno:33所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:34所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(j)包括序列与seqidno:37所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:38所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(k)包括序列与seqidno:41所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:42所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(l)包括序列与seqidno:45所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:46所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(m)包括序列与seqidno:49所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:50所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(n)包括序列与seqidno:53所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:54所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(o)包括序列与seqidno:57所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:58所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;(p)包括序列与seqidno:61所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:62所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区;和(q)包括序列与seqidno:65所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的重链可变区,和包括序列与seqidno:66所述序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸的轻链可变区,其中抗体或其抗原结合片段与人bcma特异性结合。
在某些实施方式中,抗体或其抗原结合片段包括:(a)包括具有seqidno:1所示序列的氨基酸的重链可变区,和包括具有seqidno:2所示序列的氨基酸的轻链可变区;(b)包括具有seqidno:5所示序列的氨基酸的重链可变区,和包括具有seqidno:6所示序列的氨基酸的轻链可变区;(c)包括具有seqidno:9所示序列的氨基酸的重链可变区,和包括具有seqidno:10所示序列的氨基酸的轻链可变区;(d)包括具有seqidno:13所示序列的氨基酸的重链可变区,和包括具有seqidno:14所示序列的氨基酸的轻链可变区;(e)包括具有seqidno:17所示序列的氨基酸的重链可变区,和包括具有seqidno:18所示序列的氨基酸的轻链可变区;(f)包括具有seqidno:21所示序列的氨基酸的重链可变区,和包括具有seqidno:22所示序列的氨基酸的轻链可变区;(g)包括具有seqidno:25所示序列的氨基酸的重链可变区,和包括具有seqidno:26所示序列的氨基酸的轻链可变区;(h)包括具有seqidno:29所示序列的氨基酸的重链可变区,和包括具有seqidno:30所示序列的氨基酸的轻链可变区;(i)包括具有seqidno:33所示序列的氨基酸的重链可变区,和包括具有seqidno:34所示序列的氨基酸的轻链可变区;(j)包括具有seqidno:37所示序列的氨基酸的重链可变区,和包括具有seqidno:38所示序列的氨基酸的轻链可变区;(k)包括具有seqidno:41所示序列的氨基酸的重链可变区,和包括具有seqidno:42所示序列的氨基酸的轻链可变区;(l)包括具有seqidno:45所示序列的氨基酸的重链可变区,和包括具有seqidno:46所示序列的氨基酸的轻链可变区;(m)包括具有seqidno:49所示序列的氨基酸的重链可变区,和包括具有seqidno:50所示序列的氨基酸的轻链可变区;(n)包括具有seqidno:53所示序列的氨基酸的重链可变区,和包括具有seqidno:54所示序列的氨基酸的轻链可变区;(o)包括具有seqidno:57所示序列的氨基酸的重链可变区,和包括具有seqidno:58所示序列的氨基酸的轻链可变区;(p)包括具有seqidno:61所示序列的氨基酸的重链可变区,和包括具有seqidno:62所示序列的氨基酸的轻链可变区;或者(q)包括具有seqidno:65所示序列的氨基酸的重链可变区,和包括具有seqidno:66所示序列的氨基酸的轻链可变区。
本发明公开的主题还提供一种分离的抗体或其抗原结合片段,其包括:包括cdr1、cdr2和cdr3结构域的重链可变区;和包括cdr1、cdr2和cdr3结构域的轻链可变区,其中重链可变区和轻链可变区cdr3结构域选自:
(a)包括具有seqidno:91所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:94所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(b)包括具有seqidno:97所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:100所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(c)包括具有seqidno:103所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:106所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(d)包括具有seqidno:109所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:112所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(e)包括具有seqidno:115所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:118所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(f)包括具有seqidno:121所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:124所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(g)包括具有seqidno:127所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:130所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(h)包括具有seqidno:133所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:136所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(i)包括具有seqidno:139所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:142所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(j)包括具有seqidno:145所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:148所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(k)包括具有seqidno:151所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:154所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(l)包括具有seqidno:157所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:160所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(m)包括具有seqidno:163所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:166所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(n)包括具有seqidno:169所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:172所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(o)包括具有seqidno:175所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:178所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
(p)包括具有seqidno:181所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:184所示序列的氨基酸及其保守修饰的轻链可变区cdr3;和
(q)包括具有seqidno:187所示序列的氨基酸及其保守修饰的重链可变区cdr3;和包括具有seqidno:190所示序列的氨基酸及其保守修饰的轻链可变区cdr3;
其中抗体或其抗原结合部分与人bcma特异性结合。
在某些实施方式中,抗体或其抗原结合部分的重链可变区和轻链可变区cdr2结构域选自:
(a)包括具有seqidno:90所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:93所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(b)包括具有seqidno:96所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:99所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(c)包括具有seqidno:102所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:105所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(d)包括具有seqidno:108所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:111所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(e)包括具有seqidno:114所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:117所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(f)包括具有seqidno:120所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:123所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(g)包括具有seqidno:126所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:129所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(h)包括具有seqidno:132所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:135所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(i)包括具有seqidno:138所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:141所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(j)包括具有seqidno:144所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:147所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(k)包括具有seqidno:150所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:153所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(l)包括具有seqidno:156所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:159所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(m)包括具有seqidno:162所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:165所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(n)包括具有seqidno:168所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:171所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(o)包括具有seqidno:174所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:177所示序列的氨基酸及其保守修饰的轻链可变区cdr2;
(p)包括具有seqidno:180所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:183所示序列的氨基酸及其保守修饰的轻链可变区cdr2;和
(q)包括具有seqidno:186所示序列的氨基酸及其保守修饰的重链可变区cdr2;和包括具有seqidno:189所示序列的氨基酸及其保守修饰的轻链可变区cdr2。
在某些实施方式中,抗体或其抗原结合部分的重链可变区和轻链可变区cdr1结构域选自:
(a)包括具有seqidno:89所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:92所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(b)包括具有seqidno:95所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:98所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(c)包括具有seqidno:101所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:104所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(d)包括具有seqidno:107所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:110所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(e)包括具有seqidno:113所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:116所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(f)包括具有seqidno:119所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:122所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(g)包括具有seqidno:125所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:128所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(h)包括具有seqidno:131所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:134所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(i)包括具有seqidno:137所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:140所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(j)包括具有seqidno:143所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:146所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(k)包括具有seqidno:149所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:152所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(l)包括具有seqidno:155所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:158所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(m)包括具有seqidno:161所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:164所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(n)包括具有seqidno:167所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:170所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(o)包括具有seqidno:173所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:176所示序列的氨基酸及其保守修饰的轻链可变区cdr1;
(p)包括具有seqidno:179所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:182所示序列的氨基酸及其保守修饰的轻链可变区cdr1;和
(q)包括具有seqidno:185所示序列的氨基酸及其保守修饰的重链可变区cdr1;和包括具有seqidno:188所示序列的氨基酸及其保守修饰的轻链可变区cdr1。
在某些实施方式中,一个或多个cdr序列具有至多3个氨基酸取代。在某些实施方式中,一个或多个cdr序列具有至多5个氨基酸取代。
而且,本发明公开的主题提供一种分离的抗体或其抗原结合部分,其包括:
(a)包括具有seqidno:89所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:90所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:91所示序列的氨基酸的重链可变区cdr3;
(b)包括具有seqidno:95所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:96所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:97所示序列的氨基酸的重链可变区cdr3;
(c)包括具有seqidno:101所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:102所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:103所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:107所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:108所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:109所示序列的氨基酸的重链可变区cdr3;
(e)包括具有seqidno:113所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:114所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:115所示序列的氨基酸的重链可变区cdr3;
(f)包括具有seqidno:119所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:120所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:121所示序列的氨基酸的重链可变区cdr3;
(g)包括具有seqidno:125所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:126所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:127所示序列的氨基酸的重链可变区cdr3;
(h)包括具有seqidno:131所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:132所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:133所示序列的氨基酸的重链可变区cdr3;
(i)包括具有seqidno:137所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:138所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:139所示序列的氨基酸的重链可变区cdr3;
(j)包括具有seqidno:143所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:144所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:145所示序列的氨基酸的重链可变区cdr3;
(k)包括具有seqidno:149所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:150所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:151所示序列的氨基酸的重链可变区cdr3;
(l)包括具有seqidno:155所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:156所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:157所示序列的氨基酸的重链可变区cdr3;
(m)包括具有seqidno:161所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:162所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:163所示序列的氨基酸的重链可变区cdr3;
(n)包括具有seqidno:167所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:168所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:169所示序列的氨基酸的重链可变区cdr3;
(o)包括具有seqidno:173所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:174所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:175所示序列的氨基酸的重链可变区cdr3;
(p)包括具有seqidno:179所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:180所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:181所示序列的氨基酸的重链可变区cdr3;或者
(q)包括具有seqidno:185所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:186所示序列的氨基酸的重链可变区cdr2;和包括具有seqidno:187所示序列的氨基酸的重链可变区cdr3。
此外,本发明公开的主题提供一种分离的抗体或其抗原结合部分,其包括:
(a)包括具有seqidno:92所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:93所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:94所示序列的氨基酸的轻链可变区cdr3;
(b)包括具有seqidno:98所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:99所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:100所示序列的氨基酸的轻链可变区cdr3;
(c)包括具有seqidno:104所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:105所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:106所示序列的氨基酸的轻链可变区cdr3;
(d)包括具有seqidno:110所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:111所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:112所示序列的氨基酸的轻链可变区cdr3;
(e)包括具有seqidno:116所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:117所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:118所示序列的氨基酸的轻链可变区cdr3;
(f)包括具有seqidno:122所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:123所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:124所示序列的氨基酸的轻链可变区cdr3;
(g)包括具有seqidno:128所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:129所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:130所示序列的氨基酸的轻链可变区cdr3;
(h)包括具有seqidno:134所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:135所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:136所示序列的氨基酸的轻链可变区cdr3;
(i)包括具有seqidno:140所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:141所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:142所示序列的氨基酸的轻链可变区cdr3;
(j)包括具有seqidno:146所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:147所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:148所示序列的氨基酸的轻链可变区cdr3;
(k)包括具有seqidno:152所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:153所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:154所示序列的氨基酸的轻链可变区cdr3;
(l)包括具有seqidno:158所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:159所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:160所示序列的氨基酸的轻链可变区cdr3;
(m)包括具有seqidno:164所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:165所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:166所示序列的氨基酸的轻链可变区cdr3;
(n)包括具有seqidno:170所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:171所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:172所示序列的氨基酸的轻链可变区cdr3;
(o)包括具有seqidno:176所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:177所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:178所示序列的氨基酸的轻链可变区cdr3;
(p)包括具有seqidno:182所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:183所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:184所示序列的氨基酸的轻链可变区cdr3;或者
(q)包括具有seqidno:188所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:189所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:190所示序列的氨基酸的轻链可变区cdr3。
本发明公开的主题还提供一种分离的抗体或其抗原结合部分,其包括:
(a)包括具有seqidno:89所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:90所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:91所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:92所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:93所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:94所示序列的氨基酸的轻链可变区cdr3;
(b)包括具有seqidno:95所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:96所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:97所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:98所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:99所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:100所示序列的氨基酸的轻链可变区cdr3;
(c)包括具有seqidno:101所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:102所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:103所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:104所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:105所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:106所示序列的氨基酸的轻链可变区cdr3;
(d)包括具有seqidno:107所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:108所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:109所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:110所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:111所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:112所示序列的氨基酸的轻链可变区cdr3;
(e)包括具有seqidno:113所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:114所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:115所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:116所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:117所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:118所示序列的氨基酸的轻链可变区cdr3;
(f)包括具有seqidno:119所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:120所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:121所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:122所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:123所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:124所示序列的氨基酸的轻链可变区cdr3;
(g)包括具有seqidno:125所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:126所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:127所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:128所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:129所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:130所示序列的氨基酸的轻链可变区cdr3;
(h)包括具有seqidno:131所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:132所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:133所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:134所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:135所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:136所示序列的氨基酸的轻链可变区cdr3;
(i)包括具有seqidno:137所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:138所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:139所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:140所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:141所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:142所示序列的氨基酸的轻链可变区cdr3;
(j)包括具有seqidno:143所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:144所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:145所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:146所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:147所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:148所示序列的氨基酸的轻链可变区cdr3;
(k)包括具有seqidno:149所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:150所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:151所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:152所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:153所示序列的氨基酸的轻链可变区cdr2;包括具有seqidno:154所示序列的氨基酸的轻链可变区cdr3;
(l)包括具有seqidno:155所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:156所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:157所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:158所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:159所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:160所示序列的氨基酸的轻链可变区cdr3;
(m)包括具有seqidno:161所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:162所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:163所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:164所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:165所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:166所示序列的氨基酸的轻链可变区cdr3;
(n)包括具有seqidno:167所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:168所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:169所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:170所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:171所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:172所示序列的氨基酸的轻链可变区cdr3;
(o)包括具有seqidno:173所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:174所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:175所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:176所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:177所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:178所示序列的氨基酸的轻链可变区cdr3;
(p)包括具有seqidno:179所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:180所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:181所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:182所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:183所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:184所示序列的氨基酸的轻链可变区cdr3;或者
(q)包括具有seqidno:185所示序列的氨基酸的重链可变区cdr1;包括具有seqidno:186所示序列的氨基酸的重链可变区cdr2;包括具有seqidno:187所示序列的氨基酸的重链可变区cdr3;包括具有seqidno:188所示序列的氨基酸的轻链可变区cdr1;包括具有seqidno:189所示序列的氨基酸的轻链可变区cdr2;和包括具有seqidno:190所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体或其抗原结合部分以大约1x10-9m至大约1x10-8m的结合亲合力(kd)与人bmca结合。在某些实施方式中,抗体或其抗原结合部分与包括seqidno:71所示氨基酸序列的人bcma结合。在某些实施方式中,抗体或其抗原结合部分与包括seqidno:71的氨基酸14-22的表位区结合。例如,抗体或其抗原结合部分包括:包括具有seqidno:21所示序列的氨基酸的vh和包括具有seqidno:22所示序列的氨基酸的vl,例如,抗体或其抗原结合部分包括:包括具有seqidno:119所示序列的氨基酸的vhcdr1、包括具有seqidno:120所示序列的氨基酸的vhcdr2、包括具有seqidno:121所示序列的氨基酸的vhcdr3、包括具有seqidno:122所示序列的氨基酸的vlcdr1、包括具有seqidno:123所示序列的氨基酸的vlcdr2、和包括具有seqidno:124所示序列的氨基酸的vlcdr3。
本发明公开的主题提供一种分离的抗体或其抗原结合部分,其与任意上述抗体或其抗原结合部分交叉竞争结合人bcma。本发明公开的主题提供一种分离的抗体或其抗原结合部分,其在人bcma上结合与任意上述抗体或其抗原结合部分相同的表位。
而且,本发明公开的主题提供一种分离的抗体或其抗原结合部分,其与包括以下重链可变区和轻链可变区的参考抗体或其参考抗原结合部分交叉竞争结合人bcma:(a)包括具有seqidno:1所示序列的氨基酸的重链可变区,和包括具有seqidno:2所示序列的氨基酸的轻链可变区;(b)包括具有seqidno:5所示序列的氨基酸的重链可变区,和包括具有seqidno:6所示序列的氨基酸的轻链可变区;(c)包括具有seqidno:9所示序列的氨基酸的重链可变区,和包括具有seqidno:10所示序列的氨基酸的轻链可变区;(d)包括具有seqidno:13所示序列的氨基酸的重链可变区,和包括具有seqidno:14所示序列的氨基酸的轻链可变区;(e)包括具有seqidno:17所示序列的氨基酸的重链可变区,和包括具有seqidno:18所示序列的氨基酸的轻链可变区;(f)包括具有seqidno:21所示序列的氨基酸的重链可变区,和包括具有seqidno:22所示序列的氨基酸的轻链可变区;(g)包括具有seqidno:25所示序列的氨基酸的重链可变区,和包括具有seqidno:26所示序列的氨基酸的轻链可变区;(h)包括具有seqidno:29所示序列的氨基酸的重链可变区,和包括具有seqidno:30所示序列的氨基酸的轻链可变区;(i)包括具有seqidno:33所示序列的氨基酸的重链可变区,和包括具有seqidno:34所示序列的氨基酸的轻链可变区;(j)包括具有seqidno:37所示序列的氨基酸的重链可变区,和包括具有seqidno:38所示序列的氨基酸的轻链可变区;(k)包括具有seqidno:41所示序列的氨基酸的重链可变区,和包括具有seqidno:42所示序列的氨基酸的轻链可变区;(l)包括具有seqidno:45所示序列的氨基酸的重链可变区,和包括具有seqidno:46所示序列的氨基酸的轻链可变区;(m)包括具有seqidno:49所示序列的氨基酸的重链可变区,和包括具有seqidno:50所示序列的氨基酸的轻链可变区;(n)包括具有seqidno:53所示序列的氨基酸的重链可变区,和包括具有seqidno:54所示序列的氨基酸的轻链可变区;(o)包括具有seqidno:57所示序列的氨基酸的重链可变区,和包括具有seqidno:58所示序列的氨基酸的轻链可变区;(p)包括具有seqidno:61所示序列的氨基酸的重链可变区,和包括具有seqidno:62所示序列的氨基酸的轻链可变区;或者(q)包括具有seqidno:65所示序列的氨基酸的重链可变区,和包括具有seqidno:66所示序列的氨基酸的轻链可变区。
此外,本发明公开的主题提供一种分离的抗体或其抗原结合部分,其在人bcma上结合与包括以下重链可变区和轻链可变区的参考抗体或其参考抗原结合部分相同的表位:(a)包括具有seqidno:1所示序列的氨基酸的重链可变区,和包括具有seqidno:2所示序列的氨基酸的轻链可变区;(b)包括具有seqidno:5所示序列的氨基酸的重链可变区,和包括具有seqidno:6所示序列的氨基酸的轻链可变区;(c)包括具有seqidno:9所示序列的氨基酸的重链可变区,和包括具有seqidno:10所示序列的氨基酸的轻链可变区;(d)包括具有seqidno:13所示序列的氨基酸的重链可变区,和包括具有seqidno:14所示序列的氨基酸的轻链可变区;(e)包括具有seqidno:17所示序列的氨基酸的重链可变区,和包括具有seqidno:18所示序列的氨基酸的轻链可变区;(f)包括具有seqidno:21所示序列的氨基酸的重链可变区,和包括具有seqidno:22所示序列的氨基酸的轻链可变区;(g)包括具有seqidno:25所示序列的氨基酸的重链可变区,和包括具有seqidno:26所示序列的氨基酸的轻链可变区;(h)包括具有seqidno:29所示序列的氨基酸的重链可变区,和包括具有seqidno:30所示序列的氨基酸的轻链可变区;(i)包括具有seqidno:33所示序列的氨基酸的重链可变区,和包括具有seqidno:34所示序列的氨基酸的轻链可变区;(j)包括具有seqidno:37所示序列的氨基酸的重链可变区,和包括具有seqidno:38所示序列的氨基酸的轻链可变区;(k)包括具有seqidno:41所示序列的氨基酸的重链可变区,和包括具有seqidno:42所示序列的氨基酸的轻链可变区;(l)包括具有seqidno:45所示序列的氨基酸的重链可变区,和包括具有seqidno:46所示序列的氨基酸的轻链可变区;(m)包括具有seqidno:49所示序列的氨基酸的重链可变区,和包括具有seqidno:50所示序列的氨基酸的轻链可变区;(n)包括具有seqidno:53所示序列的氨基酸的重链可变区,和包括具有seqidno:54所示序列的氨基酸的轻链可变区;(o)包括具有seqidno:57所示序列的氨基酸的重链可变区,和包括具有seqidno:58所示序列的氨基酸的轻链可变区;(p)包括具有seqidno:61所示序列的氨基酸的重链可变区,和包括具有seqidno:62所示序列的氨基酸的轻链可变区;或者(q)包括具有seqidno:65所示序列的氨基酸的重链可变区,和包括具有seqidno:66所示序列的氨基酸的轻链可变区。
在某些实施方式中,交叉竞争抗体或其抗原结合部分与包括seqidno:71所示氨基酸序列的人bcma结合。在某些实施方式中,交叉竞争抗体或其抗原结合部分与包括seqidno:71的氨基酸14-22的表位区结合。例如,参考抗体或其抗原结合部分包括:包括具有seqidno:21所示序列的氨基酸的vh和包括具有seqidno:22所示序列的氨基酸的vl,例如,参考抗体或其抗原结合部分包括:包括具有seqidno:119所示序列的氨基酸的vhcdr1、包括具有seqidno:120所示序列的氨基酸的vhcdr2、包括具有seqidno:121所示序列的氨基酸的vhcdr3、包括具有seqidno:122所示序列的氨基酸的vlcdr1、包括具有seqidno:123所示序列的氨基酸的vlcdr2、和包括具有seqidno:124所示序列的氨基酸的vlcdr3。
本发明公开的主题还提供一种分离的抗体或其抗原结合片段,其包括选自seqidno:72-88的氨基酸序列。
在某些实施方式中,抗体或其片段包括人可变区构架区。在某些实施方式中,抗体或其片段是全长人抗体或其抗原结合片段。在某些实施方式中,抗体或其片段是嵌合抗体或其抗原结合片段。在某些实施方式中,抗体或其片段是人源化抗体或其抗原结合片段。在某些实施方式中,抗体或其片段是fab、fab'、f(ab')2、fv或单链fv(scfv)。
本发明公开的主题还提供一种组合物,其包括本文公开的抗体或其抗原结合片段,和药学上可接受的载体。
此外,本发明公开的主题提供一种免疫缀合物,其包括本文公开的抗体或其抗原结合片段,其与治疗剂连接。在某些实施方式中,治疗剂是药物、细胞毒素或放射性同位素。本发明公开的主题还提供一种组合物,其包括上述免疫缀合物和药学上可接受的载体。
而且,本发明公开的主题提供一种双特异性分子,其包括本文公开的抗体或其抗原结合片段,其与第二功能部分连接。在某些实施方式中,第二功能部分具有与抗体或其抗原结合片段不同的结合特异性。在某些实施方式中,第二功能部分具有免疫细胞结合特异性。在某些实施方式中,第二功能部分具有cd3结合特异性。本发明公开的主题还提供一种组合物,其包括该双特异性分子和药学上可接受的载体。
此外,本发明公开的主题提供编码本文公开的抗体或其抗原结合片段的分离的核酸、包括该核酸分子的表达载体、以及包括该表达载体的宿主细胞。
而且,本发明公开的主题提供一种检测全细胞或组织中bcma的方法。在某些实施方式中,该方法包括:使细胞或组织与本文公开的抗体或其抗原结合片段接触,其中上述抗体或其抗原结合片段包括可检测标记;和通过测量与上述细胞或组织缔合的可检测标记的量,确定与上述细胞或组织结合的标记的抗体或其抗原结合片段的量,其中结合的抗体或其抗原结合片段的量显示上述细胞或组织中bcma的量。
而且,本发明公开的主题提供一种治疗受试者的肿瘤的方法。在某些实施方式中,该方法包括:对受试者施用有效量的本文公开的抗体或其抗原结合片段,从而诱导受试者的肿瘤细胞死亡。在某些实施方式中,该方法减少肿瘤细胞的数量。在某些实施方式中,该方法减小肿瘤的大小。在某些实施方式中,该方法根除受试者中的肿瘤。在某些实施方式中,受试者是人。
此外,本发明公开的主题提供本文公开的抗体或其抗原结合片段在治疗肿瘤中的用途,以及本文公开的抗体或其抗原结合片段在治疗受试者的肿瘤中的用途。
而且,本发明公开的主题提供一种用于治疗肿瘤的药盒,其包括本文公开的抗体或其抗原结合片段。在某些实施方式中,药盒进一步包括使用抗体或其抗原结合片段治疗患有肿瘤的受试者的书面说明书。
在某些实施方式中,肿瘤选自多发性骨髓瘤、非霍奇金淋巴瘤、霍奇金淋巴瘤、慢性淋巴细胞性白血病(cll)、成胶质细胞瘤和waldenstrom氏巨球蛋白血症。在某些实施方式中,肿瘤是多发性骨髓瘤。
附图说明
以下可以结合附图理解以举例方式给出的具体实施方式,但无意于将本发明限定为所描述的具体的实施方式。
图1描述不同组织中的人bcma表达。
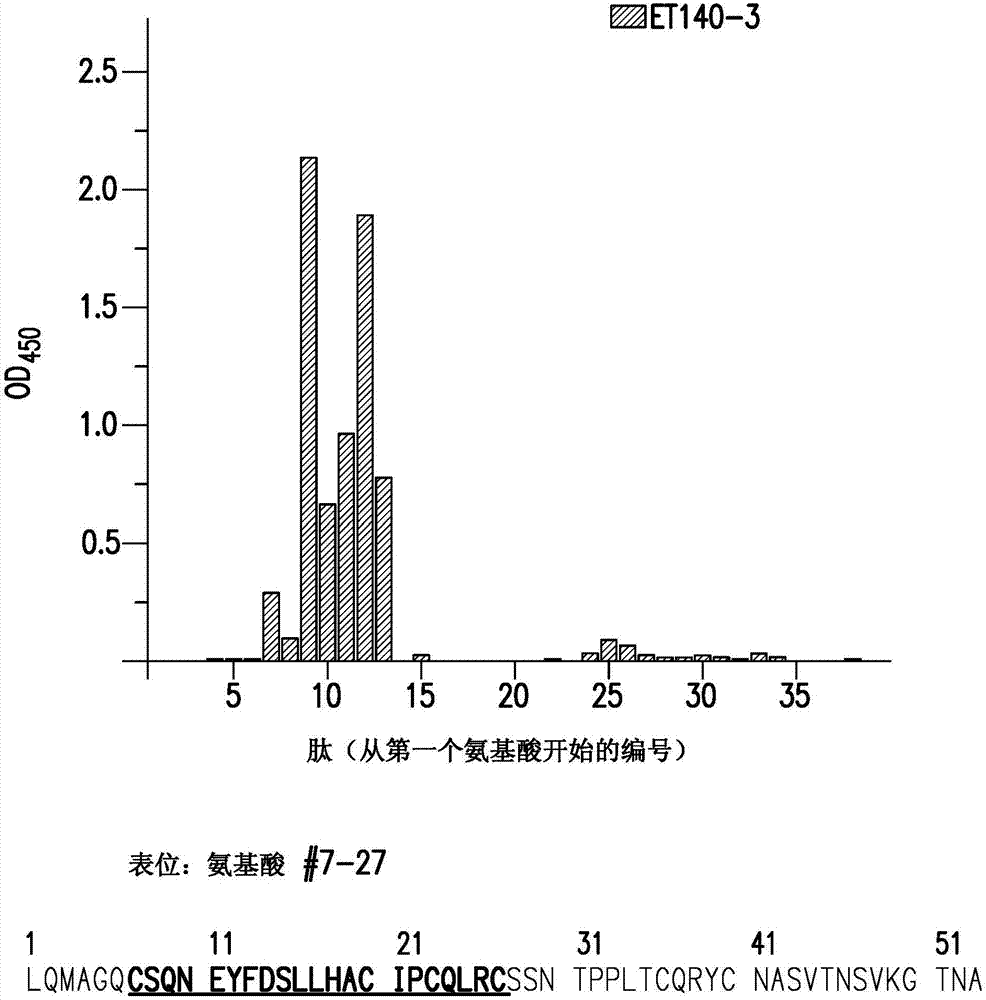
图2描述et140-3的表位定位。
图3描述et140-24的表位定位。
图4描述et140-54的表位定位。
图5描述et140-3、et140-24和et140-54的表位定位。
图6描述et140-3、et140-24、et140-37、et140-40和et140-54的elisa筛选数据。
图7描述et140-3、et140-24、et140-37、et140-40和et140-54的fcas筛选数据。
具体实施方式
本文引用的所有出版物、专利和其他参考文献均全文并入本发明公开内容作为参考。
在实施本发明公开的主题时,使用本领域技术内的分子生物学、微生物学、细胞生物学、生物化学和免疫学的许多常规技术。例如,这些技术在以下文献中得以更详细的说明:molecularcloning:alaboratorymanual3rdedition,j.f.sambrookandd.w.russell编,coldspringharborlaboratorypress2001;recombinantantibodiesforimmunotherapy,melvynlittle编,cambridgeuniversitypress2009;“oligonucleotidesynthesis”(m.j.gait编,1984);“animalcellculture”(r.i.freshney编,1987);“methodsinenzymology”(academicpress,inc.);“currentprotocolsinmolecularbiology”(f.m.ausubel等人编,1987,以及定期更新);“pcr:thepolymerasechainreaction”(mullis等人编,1994)“apracticalguidetomolecularcloning”(perbalbernardv.,1988);“phagedisplay:alaboratorymanual”(barbas等人,2001)。这些参考文献以及含有标准方案的其他参考文献的内容是本领域技术人员广泛知晓的,并取决于本领域技术人员,其包括制造商说明书,在此将其并入作为本公开内容的一部分作为参考。
定义
在以下说明中,在术语用法将遵照某些惯例。通常,本文使用的术语是要理解成含义与本领域技术人员所知晓的含义一致。
“抗原结合蛋白质”是包括抗原结合区或抗原结合部分的蛋白质或多肽,即,与其所结合的另一分子具有强亲合力。抗原结合蛋白质包括抗体、嵌合抗原受体(car)和融合蛋白。
“抗体”和“多种抗体”如本领域所知,是指免疫系统的抗原结合蛋白质。如本文所用,术语“抗体”包括具有抗原结合区的完整全长抗体及其保留“抗原结合部分”或“抗原结合区”的任意片段,或者其单链,例如单链可变片段(scfv)。天然“抗体”是包括通过二硫键互相连接的至少两个重(h)链和两个轻(l)链的糖蛋白。每个重链包括重链可变区(在此简称作vh)和重链恒定(ch)区。重链恒定区包括三个结构域ch1、ch2和ch3。每个轻链包括轻链可变区(在此简称作vl)和轻链恒定cl区。轻链恒定区包括一个结构域cl。vh和vl区可以进一步细分成称作互补决定区(cdr)的超变区,分散有更加保守的称作框架区(fr)的区域。每个vh和vl由以如下顺序从氨基端到羧基端排列的三个cdr和四个fr组成:fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。重链和轻链的可变区含有与抗原相互作用的结合结构域。抗体的恒定区可以介导免疫球蛋白与宿主组织或因子的结合,包括各种免疫系统细胞(例如效应细胞)和经典补体系统的第一成分(clq)。
如本文所用,术语“人抗体”是包括其中框架区和cdr区二者均源自人种系免疫球蛋白序列的具有可变区的抗体。而且,如果抗体含有恒定区,恒定区也源自人种系免疫球蛋白序列。本发明公开主题的人抗体可以包括并非由人种系免疫球蛋白序列编码的氨基酸残基(例如,通过体外随机或定点突变或者通过体内体细胞突变引入的突变)。
如本文所用,术语“单克隆抗体”是指由基本上均一的抗体群体得到的抗体,即,构成该群体的各个抗体是相同和/或结合相同表位,可能的变体抗体除外,例如,包括天然产生的突变或者在单克隆抗体制备生产过程中发生,例如,这样的变体通常以微小的量存在。与通常包括导向不同决定簇(表位)的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂的每个单克隆抗体导向抗原上的单个决定簇。因此,修饰“单克隆”是指当获自基本上同源的抗体群体时抗体的性质,而不是要理解成要求抗体通过任何特定方法制造。例如,根据本发明公开主题所使用的单克隆抗体可以通过许多种技术制造,包括但不限于杂交瘤方法、重组dna方法、噬菌体展示方法和利用含有全部或部分人免疫球蛋白基因座的转基因动物的方法,例如本文所述的制造单克隆抗体的这些方法和其他示例性方法。
如本文所用,术语“重组人抗体”包括所有通过重组方式制备、表达、产生或分离的人抗体,例如,(a)自用人免疫球蛋白基因进行转基因或转染色体的动物(例如小鼠)或由其制备的杂交瘤分离的抗体(在以下更详细描述),(b)自转化成表达人抗体的宿主细胞例如转染瘤分离的抗体,(c)自重组、组合人抗体文库分离的抗体,和(d)通过包括剪接人免疫球蛋白基因至其他dna序列的任意其他方式制备、表达、产生或分离的抗体。这些重组人抗体具有可变区,其中框架区和cdr区源自人种系免疫球蛋白序列。但是,在某些实施方式中,这些重组人抗体可以进行体外突变(或者,当使用人ig序列对动物进行转基因时,体内的体细胞突变),因此,重组抗体vh和vl区的氨基酸序列是尽管源自人种系vh和vl序列并与其相关、但在体内在所有的人抗体种系内均不可能天然存在的序列。
术语“人源化抗体”是指将源自其他哺乳动物物种例如小鼠种系的cdr序列接到人框架序列上的抗体。可以在人框架序列内进行额外的框架区修饰。
术语“嵌合抗体”是指可变区序列源自一物种、恒定区序列源自另一物种的抗体,例如,其中可变区序列源自小鼠抗体、恒定区序列源自人抗体的抗体。
如本文所用,“与人bcma特异性结合”的抗体是指以大约5x10-7m或更低、大约1x10-7m或更低、大约5x10-8m或更低、大约1x10-8m或更低、大约5x10-9m或更低、大约1x10-9m或更低、大约5x10-10m或更低、大约1x10-10m或更低、大约5x10-11m或更低、或大约1x10-11m或更低的kd与人bcma结合的抗体。
与结合例如bcma的抗原的参考抗体“竞争结合的抗体”或“交叉竞争结合的抗体”是指在竞争检验中阻断参考抗体与抗原(例如bcma)结合50%或更多的抗体,以及相反地,在竞争检验中参考抗体阻断抗体与抗原(例如bcma)结合50%或更多。示例性竞争检验描述于:“antibodies”,harlowandlane(coldspringharborpress,coldspringharbor,ny)。
如本文所用,“表型”是指由重链恒定区基因编码的抗体类别(例如igm或iggl)。
在本文中,术语“识别抗原的抗体”和“抗原特异性抗体”与术语“与抗原(例如bmca多肽)特异性结合的抗体”可互换地使用。如本文所用,术语“抗原结合部分”或“抗原结合区”是指抗体与抗原结合并使抗体具有抗原特异性的区域或部分;抗原结合蛋白质片段,例如抗体包括一个或多个保持特异性结合抗原(例如bcma多肽)的能力的抗体片段。已经知道全长抗体的片段能够显示抗体的抗原结合功能。抗体的“抗体片段”术语内包括的抗原结合片段的例子包括由vl、vh、cl和ch1结构域组成的单价片段即fab片段;包括在铰链区通过二硫键连接的两个fab片段的二价片段即f(ab)2片段;由vh和ch1结构域组成的fd片段;由抗体单臂的vl和vh结构域组成的fv片段;由vh结构域组成的dab片段(ward等人,1989nature341:544-546);和分离的互补决定区(cdr)。
而且,尽管fv片段的两个结构域vl和vh分别由不同的基因编码,可以使用重组技术通过能够成为其中vl和vh区成对形成单价分子的单一蛋白质链的合成接头(linker)连接。这些称作单链fv(scfv);参见:例如,bird等人,1988science242:423-426;和huston等人,1988proc.natl.acad.sci.85:5879-5883。使用本领域技术人员已知的常规技术得到这些抗体片段,并以与完整抗体相同的方式对片段进行用途筛选。
“分离的抗体”或“分离的抗原结合蛋白质”是已经鉴别并从其天然环境中分离和/或回收者。“合成抗体”或“重组抗体”通常使用重组技术或使用本领域技术人员已知的合成技术产生。
术语“bcma”和“b-细胞成熟抗原”可互换地使用,其包括人bcma的变体、同种型、物种同源物和与bcma(例如人bcma)具有至少一个相同表位的类似物。示例性的人bcma序列可以见于entrezgene编号:np_001183。
如本文所用,术语“单链可变片段”或“scfv”是免疫球蛋白(例如小鼠或人)的重链(vh)和轻链(vl)的可变区的融合蛋白,其共价连接形成vh::vl异二聚体。重链(vh)和轻链(vl)直接连接或通过肽-编码接头(例如,10、15、20、25个氨基酸)连接,其将vh的n端与vl的c-端连接或将vh的c端与vl的n端连接。接头通常富含表现柔性的甘氨酸以及表现溶解性的丝氨酸或苏氨酸。接头可以连接细胞外抗原结合结构域的重链可变区和轻链可变区。接头的非限定性例子公开于shen等人,anal.chem.80(6):1910-1917(2008)和wo2014/087010,将其内容全文并入作为参考。在某些实施方式中,接头是g4s接头。在某些实施方式中,接头包括具有如下文所提供的seqidno:191所示序列的氨基酸:
ggggsggggsggggs[seqidno:191]。
在某些实施方式中,编码氨基酸序列seqidno:191的核苷酸序列在下面提供的seqidno:192中给出:
ggtggaggtggatcaggtggaggtggatctggtggaggtggatct[seqidno:192]。
在某些实施方式中,接头包括具有如下提供的seqidno:69中所示序列的氨基酸。
srggggsggggsggggslema[seqidno:69]。
在某些实施方式中,编码氨基酸序列seqidno:69的核苷酸序列在下面提供的seqidno:70中给出:
tctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggcc[seqidno:70]。
在某些实施方式中,接头包括具有以下序列ggggs[seqidno:193]的氨基酸。
在某些实施方式中,接头包括具有以下序列sggsggs[seqidno:194]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsgggs[seqidno:195]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsggggs[seqidno:196]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsggggsgggggggs[seqidno:197]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsggggsggggsggggs[seqidno:198]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsggggsggggsggggsggggs[seqidno:199]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsggggsggggsggggsggggsggggs[seqidno:200]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsggggsggggsggggsggggsggggsggggs[seqidno:201]的氨基酸。
在某些实施方式中,接头包括具有以下序列epkscdkthtcppcp[seqidno:202]的氨基酸。
在某些实施方式中,接头包括具有以下序列ggggsgggsepkscdkthtcppcp[seqidno:203]的氨基酸。
在某些实施方式中,接头包括具有以下序列elktplgdtthtcprcpepkscdtpppcprcpepkscdtpppcprcpepkscdtpppcprcp[seqidno:204]的氨基酸。
在某些实施方式中,接头包括具有以下序列gsgsgs[seqidno:205]的氨基酸。
在某些实施方式中,接头包括具有以下序列aaa[seqidno:206]的氨基酸。
尽管去除了恒定区并引入了接头,scfv蛋白质保留了原始免疫球蛋白的特异性。单链fv多肽抗体可以由包括vh-和vl-编码序列的核酸表达,如huston等人所述(proc.nat.acad.sci.usa,85:5879~5883,1988)。还可参见美国专利号5,091,513、5,132,405和4,956,778;以及美国专利公开号20050196754和20050196754。具有抑制活性的拮抗性scfv已有描述(参见:例如,zhao等人,hyrbidoma(larchmt)200827(6):455~51;peter等人,jcachexiasarcopeniamuscle2012年8月12日;shieh等人,jimunol2009183(4):2277~85;giomarelli等人,thrombhaemost200797(6):955~63;fife等人,jclininvst2006116(8):2252~61;brocks等人,immunotechnology19973(3):173~84;moosmayer等人,therimmunol19952(10:31~40)。具有刺激活性的激动性scfv已有描述(参见:例如,peter等人,jbioichern200325278(38):36740~7;xie等人,natbiotech199715(8):768~71;ledbetter等人,critrevimmunol199717(5-6):427~55;ho等人,biochimbiophysacta20031638(3):257~66)。
如本文所用,“f(ab)”是指结合抗原的抗体结构的片段,但其是单价的并且不具有fc部分,例如,由木瓜蛋白酶消化抗体产生两个f(ab)片段和一个fc片段(例如,重(h)链恒定区;不结合抗原的fc区)。
如本文所用,“f(ab')2”是指由胃蛋白酶消化完整igg抗体产生的抗体片段,其中该片段具有两个抗原结合(ab')(二价)区,其中每个(ab')区包括两条分开的氨基酸链,h链的一部分通过s-s键与轻(l)链连接,用于结合抗原,其中,h链的剩余部分连接在一起。“f(ab')2”片段可以分裂成两个单独的fab'片段。
如本文所用,术语“载体”是指任何遗传元件,比如质粒、噬菌体、转座子、黏粒、染色体、病毒、病毒颗粒等,其当关联有适当的控制元件时能够复制,并且其可以将基因序列转移到细胞中。因此,该术语包括克隆和表达载体,以及病毒载体和质粒载体。
“cdr”定义为抗体的互补决定区氨基酸序列,其为免疫球蛋白重链和轻链的高变区。参见:例如,kabat等人,sequencesofproteinsofimmunologicalinterest,4thu.s.departmentofhealthandhumanservices,nationalinstitutesofhealth(1987)。如本文所用,术语“高变区”或“hvr”是指抗体可变结构域的各个区,其在序列上是高度可变的(“互补决定区”或“cdr”)和/或形成结构限定的回环(“高变环”)和/或含有抗原接触残基(“抗原接触”)。通常,抗体在可变区中包括三个重链和三个轻链cdr或cdr区。cdr提供了大多数使抗体与抗原或表位结合的接触残基。
“分离的抗体”是已经与其天然环境的组分分离的抗体。在某些实施方式中,抗体提纯至纯度大于95%或99%,例如,通过电泳(例如,sds-page、等电点聚焦(ief)、毛细管电泳)或色谱(例如,离子交换或反相hplc)测定。对于抗体纯度评价方法的综述,参见:例如flatman等人,j.chromatogr.b848:79-87(2007)。
“分离的核酸”是已经与其天然环境的组分分离的核酸分子。分离的核酸包括通常含有核酸分子的细胞中含有的核酸分子,但是核酸分子存在于染色体外,或者存在于不同于其天然染色体位置的染色体位置处。
“分离的编码抗体的核酸”(包括提及特异性抗体,例如,抗klb抗体)是指编码抗体重链和轻链(或其片段)的一种或多种核酸分子,其包括单一载体、单独的载体中的该核酸分子以及宿主细胞中在一个或多个位置处存在的该核酸分子。
如本文所用,术语“载体”是指能够使与其连接的另一核酸分子增殖的核酸分子。该术语包括作为自复制核酸结构的载体以及插入到其被导入的宿主细胞的基因组中的载体。某些载体能够引导与其可操作连接的核酸的表达。这种载体在本文中称作“表达载体”。
“免疫缀合物”是与一个或多个包括但不限于细胞毒素的异源分子缀合的抗体。
药剂例如抗bcma抗体或其抗原结合片段、包括其的药物组合物的“有效量”是指以必需的剂量和期间有效地实现所需的治疗或预防效果例如治疗肿瘤(例如多发性骨髓瘤)的量。
“个体”或“受试者”是哺乳动物。哺乳动物包括但不限于饲养的动物(例如,牛、绵羊、猫、狗和马)、灵长类动物(例如,人和非人灵长类动物例如猴)、兔子和啮齿类动物(例如小鼠和大鼠)。在某些实施方式中,个体或受试者是人。
如本文所用,“治疗(及其语法变化形式例如“treat”或“treating”)是指试图改变被治疗个体的自然进程的临床干预,并且可以用于预防或在临床病理过程期间进行。治疗的合意效果包括但不限于预防疾病的发生或复发、症状的缓解、疾病的任何直接或间接病理学后果的减少、预防转移、降低疾病进展的速度、减轻或缓和疾病状态以及缓解或改善预后。在某些实施方式中,本发明公开主题的抗体用于延缓疾病的发生或者减慢疾病的进展,例如肿瘤(多发性骨髓瘤)。
如本文所用,术语“约”或“大约”是指在由本领域普通技术人员确定的特定值的可接受误差范围内,这将部分地取决于如何测量或确定该值,即测量系统的局限性。例如,根据本领域的惯例,“约”可以指在3个或多于3个标准偏差内。或者,“约”可以表示给定值的高达20%、优选高达10%、更优选高达5%、进一步更优选高达1%的范围。或者,特别是关于生物系统或过程,该术语可以表示在数值的一个数量级内、优选在5倍以内、更优选在2倍以内。
如本文所述,除非另外指出,任何浓度范围、百分比范围、比例范围或整数范围要理解成包括所引范围内的任意整数值,当适当时,包括其分数(例如整数的十分之一和百分之一)。
抗bcma抗体
本发明公开主题的抗体特征在于抗体的特定功能特征或特性。例如,抗体与bcma特异性结合(例如,与人bcma结合,并可以与来自其他物种例如小鼠的bcma交叉反应)。在某些实施方式中,本发明公开主题的抗体以高亲合力与bcma结合,例如,kd为1x10-6m或更低,例如,大约1x10-7m或更低,大约1x10-8m或更低,大约1x10-9m或更低,大约1x10-10m或更低,大约1x10-11m或更低。在某些实施方式中,本发明公开的抗bcma抗体以大约1x10-11m至大约1x10-6m例如大约1x10-11m至大约1x10-10m、大约1x10-10m至大约1x10-9m、1x10-9m至大约1x10-8m、大约1x10-8m至大约1x10-7m或者大约1x10-7m至大约1x10-6m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约1x10-8m或更低的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约1x10-9m至大约1x10-8m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约1x10-9m至大约1.5x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约1.2x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约4x10-9m至大约5x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约5x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约4.8x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约8x10-9m至大约9x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约8x10-9m的kd与bcma(例如,人bcma)结合。在某些实施方式中,本发明公开的抗bcma抗体以大约8.1x10-9m的kd与bcma(例如,人bcma)结合。
本发明公开主题的抗体的重链和轻链可以是全长的(例如,抗体可以包括至少一个(例如,一个或两个)完整的重链和至少一个(例如,一个或两个)完整的轻链),或者可以包括抗原结合部分(fab、f(ab')2、fv或单链fv片段(“scfv”)。在某些实施方式中,抗体重链恒定区选自例如igg1、igg2、igg3、igg4、igm、iga1、iga2、igd和ige,特别是选自例如igg1、igg2、igg3和igg4,更具体地,igg1(例如人igg1)。在另一实施方式中,抗体轻链恒定区选自例如κ或λ,特别是κ。
1.单链可变片段(scfv)
在一些实施方式中,本发明公开的主题包括具有与一个或多个恒定结构域融合的scfv序列,以形成具有人免疫球蛋白fc区的抗体,产生二价蛋白质,增加抗体总的亲和力和稳定性。此外,fc部分允许在抗体上直接缀合有其他分子,其包括但不限于荧光染料、细胞毒素、放射性同位素等,例如,用于抗原定量研究、将抗体固定化用于亲合力测量、用于治疗剂的靶向输送、使用免疫效应细胞的fc-介导的细胞毒性测试以及许多其他用途。
本文所示的结果突出之处在于本发明的抗体在靶向bcma多肽方面的特异性、敏感性和应用。
本发明的分子基于使用噬菌体展示对单链可变片段(scfv)进行识别和选择,其氨基酸序列使得分子对于所关注的bcma多肽具有特异性,并形成本公开内容所有抗原结合蛋白质的基础。因此,scfv可以用于设计“抗体分子”的多样化阵列,其包括,例如,全长抗体,其片段例如fab和f(ab')2,微抗体,融合蛋白,包括scfv-fc融合物,多价抗体,即对于相同抗原或不同抗原具有一种以上特异性的抗体,例如双特异性抗体、三价抗体等(参见:cuesta等人,multivalentantibodies:whendesignsurpassesevolution.trendsinbiotechnology28:355-3622010)。
在某些实施方式中,抗原结合蛋白质可以是全长抗体,本发明公开主题抗体的重链和轻链可以是全长的(例如,抗体可以包括至少一个、优选两个完整的重链和至少一个、优选两个完整的轻链),或者可以包括抗原结合部分(fab、f(ab')2、fv或单链fv片段(“scfv”)。在某些实施方式中,抗体重链恒定区选自例如igg1、igg2、igg3、igg4、igm、iga1、iga2、igd和ige。在某些实施方式中,免疫球蛋白同种型选自igg1、igg2、igg3和igg4,更具体地,igg1(例如人igg1)。抗体同种型的选择可以取决于设计抗体要引起的免疫效应功能。
在构建重组免疫球蛋白时,不同免疫球蛋白同种型恒定区的适当氨基酸序列和广泛的一系列抗体的产生方法是本领域技术人员已知的。
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:72的抗原结合区,并特异性结合具有氨基酸序列seqidno:71的bcma多肽(例如,具有以下提供的氨基酸序列的bcma多肽,或其片段),其命名为et140-192(也称作“et140-42”)。
mlqmagqcsqneyfdsllhacipcqlrcssntppltcqrycnasvtnsvkgtnailwtclglsliislavfvlmfllrkinseplkdefkntgsgllgmanidleksrtgdeiilprgleytveectcedcikskpkvdsdhcfplpameegatilvttktndyckslpaalsateieksisar[seqidno:71]
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:1所示序列的氨基酸的重链可变区和包括具有seqidno:2所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表1的vh和vl区或cdr的scfv-fc融合蛋白或全长人igg。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:1所示序列的氨基酸的vh,如表1所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:2所示序列的氨基酸的vl,如表1所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:1所示序列的氨基酸的vh和包括具有seqidno:2所示序列的氨基酸的vl,如表1所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:89所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:90所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:91所示序列的氨基酸或其保守修饰的vhcdr3,如表1所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:92所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:93所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:94所示序列的氨基酸或其保守修饰的vlcdr3,如表1所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:89所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:90所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:91所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:92所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:93所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:94所示序列的氨基酸或其保守修饰的vlcdr3,如表1所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:89所示序列的氨基酸的vhcdr1、包括具有seqidno:90所示序列的氨基酸的vhcdr2、包括具有seqidno:91所示序列的氨基酸的vhcdr3、包括具有seqidno:92所示序列的氨基酸的vlcdr1、包括具有seqidno:93所示序列的氨基酸的vlcdr2、和包括具有seqidno:94所示序列的氨基酸的vlcdr3。
表1
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:73的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-197(也称作“et140-47”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:5所示序列的氨基酸的重链可变区和包括具有seqidno:6所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表2的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:5所示序列的氨基酸的vh,如表2所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:6所示序列的氨基酸的vl,如表2所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:5所示序列的氨基酸的vh和包括具有seqidno:6所示序列的氨基酸的vl,如表2所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:95所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:96所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:97所示序列的氨基酸或其保守修饰的vhcdr3,如表2所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:98所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:99所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:100所示序列的氨基酸或其保守修饰的vlcdr3,如表2所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:95所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:96所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:97所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:98所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:99所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:100所示序列的氨基酸或其保守修饰的vlcdr3,如表2所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:95所示序列的氨基酸的vhcdr1、包括具有seqidno:96所示序列的氨基酸的vhcdr2、包括具有seqidno:97所示序列的氨基酸的vhcdr3、包括具有seqidno:98所示序列的氨基酸的vlcdr1、包括具有seqidno:99所示序列的氨基酸的vlcdr2、和包括具有seqidno:100所示序列的氨基酸的vlcdr3。
表2
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:74的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-180(也称作“et140-30”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:9所示序列的氨基酸的重链可变区和包括具有seqidno:10所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表3的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:9所示序列的氨基酸的vh,如表3所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:10所示序列的氨基酸的vl,如表3所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:9所示序列的氨基酸的vh和包括具有seqidno:10所示序列的氨基酸的vl,如表3所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:101所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:102所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:103所示序列的氨基酸或其保守修饰的vhcdr3,如表3所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:104所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:105所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:106所示序列的氨基酸或其保守修饰的vlcdr3,如表3所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:101所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:102所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:103所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:104所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:105所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:106所示序列的氨基酸或其保守修饰的vlcdr3,如表3所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:101所示序列的氨基酸的vhcdr1、包括具有seqidno:102所示序列的氨基酸的vhcdr2、包括具有seqidno:103所示序列的氨基酸的vhcdr3、包括具有seqidno:104所示序列的氨基酸的vlcdr1、包括具有seqidno:105所示序列的氨基酸的vlcdr2、和包括具有seqidno:106所示序列的氨基酸的vlcdr3。
表3
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:75的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-172(也称作“et140-22”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:13所示序列的氨基酸的重链可变区和包括具有seqidno:14所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表4的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:13所示序列的氨基酸的vh,如表4所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:14所示序列的氨基酸的vl,如表4所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:13所示序列的氨基酸的vh和包括具有seqidno:14所示序列的氨基酸的vl,如表4所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:107所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:108所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:109所示序列的氨基酸或其保守修饰的vhcdr3,如表4所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:110所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:111所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:112所示序列的氨基酸或其保守修饰的vlcdr3,如表4所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:107所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:108所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:109所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:110所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:111所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:112所示序列的氨基酸或其保守修饰的vlcdr3,如表4所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:107所示序列的氨基酸的vhcdr1、包括具有seqidno:108所示序列的氨基酸的vhcdr2、包括具有seqidno:109所示序列的氨基酸的vhcdr3、包括具有seqidno:110所示序列的氨基酸的vlcdr1、包括具有seqidno:111所示序列的氨基酸的vlcdr2、和包括具有seqidno:112所示序列的氨基酸的vlcdr3。
表4
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:76的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-157(也称作“et140-7”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:17所示序列的氨基酸的重链可变区和包括具有seqidno:18所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表5的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:17所示序列的氨基酸的vh,如表5所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:18所示序列的氨基酸的vl,如表5所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:17所示序列的氨基酸的vh和包括具有seqidno:18所示序列的氨基酸的vl,如表5所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:113所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:114所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:115所示序列的氨基酸或其保守修饰的vhcdr3,如表5所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:116所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:117所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:118所示序列的氨基酸或其保守修饰的vlcdr3,如表5所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:113所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:114所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:115所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:116所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:117所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:118所示序列的氨基酸或其保守修饰的vlcdr3,如表5所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:113所示序列的氨基酸的vhcdr1、包括具有seqidno:114所示序列的氨基酸的vhcdr2、包括具有seqidno:115所示序列的氨基酸的vhcdr3、包括具有seqidno:116所示序列的氨基酸的vlcdr1、包括具有seqidno:117所示序列的氨基酸的vlcdr2、和包括具有seqidno:118所示序列的氨基酸的vlcdr3。
表5
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:77的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-153(也称作“et140-3”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:21所示序列的氨基酸的重链可变区和包括具有seqidno:22所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表6的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:21所示序列的氨基酸的vh,如表6所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:22所示序列的氨基酸的vl,如表6所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:21所示序列的氨基酸的vh和包括具有seqidno:22所示序列的氨基酸的vl,如表6所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:119所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:120所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:121所示序列的氨基酸或其保守修饰的vhcdr3,如表6所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:122所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:123所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:124所示序列的氨基酸或其保守修饰的vlcdr3,如表6所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:119所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:120所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:121所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:122所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:123所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:124所示序列的氨基酸或其保守修饰的vlcdr3,如表6所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:119所示序列的氨基酸的vhcdr1、包括具有seqidno:120所示序列的氨基酸的vhcdr2、包括具有seqidno:121所示序列的氨基酸的vhcdr3、包括具有seqidno:122所示序列的氨基酸的vlcdr1、包括具有seqidno:123所示序列的氨基酸的vlcdr2、和包括具有seqidno:124所示序列的氨基酸的vlcdr3。
表6
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:78的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-201(也称作“et140-51”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:25所示序列的氨基酸的重链可变区和包括具有seqidno:26所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表7的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:25所示序列的氨基酸的vh,如表7所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:26所示序列的氨基酸的vl,如表7所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:25所示序列的氨基酸的vh和包括具有seqidno:26所示序列的氨基酸的vl,如表7所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:125所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:126所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:127所示序列的氨基酸或其保守修饰的vhcdr3,如表7所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:128所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:129所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:130所示序列的氨基酸或其保守修饰的vlcdr3,如表7所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:125所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:126所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:127所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:128所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:129所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:130所示序列的氨基酸或其保守修饰的vlcdr3,如表7所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:125所示序列的氨基酸的vhcdr1、包括具有seqidno:126所示序列的氨基酸的vhcdr2、包括具有seqidno:127所示序列的氨基酸的vhcdr3、包括具有seqidno:128所示序列的氨基酸的vlcdr1、包括具有seqidno:129所示序列的氨基酸的vlcdr2、和包括具有seqidno:130所示序列的氨基酸的vlcdr3。
表7
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:79的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-167(也称作“et140-17”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:29所示序列的氨基酸的重链可变区和包括具有seqidno:30所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表8的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:29所示序列的氨基酸的vh,如表8所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:30所示序列的氨基酸的vl,如表8所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:29所示序列的氨基酸的vh和包括具有seqidno:30所示序列的氨基酸的vl,如表8所示。在某些实施方式中,抗bcma包括:包括具有seqidno:131所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:132所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:133所示序列的氨基酸或其保守修饰的vhcdr3,如表8所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:134所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:135所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:136所示序列的氨基酸或其保守修饰的vlcdr3,如表8所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:131所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:132所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:133所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:134所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:135所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:136所示序列的氨基酸或其保守修饰的vlcdr3,如表8所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:131所示序列的氨基酸的vhcdr1、包括具有seqidno:132所示序列的氨基酸的vhcdr2、包括具有seqidno:133所示序列的氨基酸的vhcdr3、包括具有seqidno:134所示序列的氨基酸的vlcdr1、包括具有seqidno:135所示序列的氨基酸的vlcdr2、和包括具有seqidno:136所示序列的氨基酸的vlcdr3。
表8
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:80的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-163(也称作“et140-13”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:33所示序列的氨基酸的重链可变区和包括具有seqidno:34所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表9的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:33所示序列的氨基酸的vh,如表9所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:34所示序列的氨基酸的vl,如表9所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:33所示序列的氨基酸的vh和包括具有seqidno:34所示序列的氨基酸的vl,如表9所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:137所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:138所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:139所示序列的氨基酸或其保守修饰的vhcdr3,如表9所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:140所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:141所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:142所示序列的氨基酸或其保守修饰的vlcdr3,如表9所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:137所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:138所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:139所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:140所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:141所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:142所示序列的氨基酸或其保守修饰的vlcdr3,如表9所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:137所示序列的氨基酸的vhcdr1、包括具有seqidno:138所示序列的氨基酸的vhcdr2、包括具有seqidno:139所示序列的氨基酸的vhcdr3、包括具有seqidno:140所示序列的氨基酸的vlcdr1、包括具有seqidno:141所示序列的氨基酸的vlcdr2、和包括具有seqidno:142所示序列的氨基酸的vlcdr3。
表9
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:81的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-207(也称作“et140-57”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:37所示序列的氨基酸的重链可变区和包括具有seqidno:38所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:98所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表10的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:37所示序列的氨基酸的vh,如表10所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:38所示序列的氨基酸的vl,如表10所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:37所示序列的氨基酸的vh和包括具有seqidno:38所示序列的氨基酸的vl,如表10所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:143所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:144所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:145所示序列的氨基酸或其保守修饰的vhcdr3,如表10所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:146所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:147所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:148所示序列的氨基酸或其保守修饰的vlcdr3,如表10所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:143所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:144所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:145所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:146所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:147所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:148所示序列的氨基酸或其保守修饰的vlcdr3,如表10所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:143所示序列的氨基酸的vhcdr1、包括具有seqidno:144所示序列的氨基酸的vhcdr2、包括具有seqidno:145所示序列的氨基酸的vhcdr3、包括具有seqidno:146所示序列的氨基酸的vlcdr1、包括具有seqidno:147所示序列的氨基酸的vlcdr2、和包括具有seqidno:148所示序列的氨基酸的vlcdr3。
表10
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:82的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-165(也称作“et140-15”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:41所示序列的氨基酸的重链可变区和包括具有seqidno:42所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表11的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:41所示序列的氨基酸的vh,如表11所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:42所示序列的氨基酸的vl,如表11所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:41所示序列的氨基酸的vh和包括具有seqidno:42所示序列的氨基酸的vl,如表11所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:149所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:150所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:151所示序列的氨基酸或其保守修饰的vhcdr3,如表11所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:152所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:153所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:154所示序列的氨基酸或其保守修饰的vlcdr3,如表11所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:149所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:150所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:151所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:152所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:153所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:154所示序列的氨基酸或其保守修饰的vlcdr3,如表11所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:149所示序列的氨基酸的vhcdr1、包括具有seqidno:150所示序列的氨基酸的vhcdr2、包括具有seqidno:151所示序列的氨基酸的vhcdr3、包括具有seqidno:152所示序列的氨基酸的vlcdr1、包括具有seqidno:153所示序列的氨基酸的vlcdr2、和包括具有seqidno:154所示序列的氨基酸的vlcdr3。
表11
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:83的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-188(也称作“et140-38”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:45所示序列的氨基酸的重链可变区和包括具有seqidno:46所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表12的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:45所示序列的氨基酸的vh,如表12所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:46所示序列的氨基酸的vl,如表12所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:45所示序列的氨基酸的vh和包括具有seqidno:46所示序列的氨基酸的vl,如表12所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:155所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:156所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:157所示序列的氨基酸或其保守修饰的vhcdr3,如表12所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:158所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:159所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:160所示序列的氨基酸或其保守修饰的vlcdr3,如表12所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:155所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:156所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:157所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:158所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:159所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:160所示序列的氨基酸或其保守修饰的vlcdr3,如表12所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:155所示序列的氨基酸的vhcdr1、包括具有seqidno:156所示序列的氨基酸的vhcdr2、包括具有seqidno:157所示序列的氨基酸的vhcdr3、包括具有seqidno:158所示序列的氨基酸的vlcdr1、包括具有seqidno:159所示序列的氨基酸的vlcdr2、和包括具有seqidno:160所示序列的氨基酸的vlcdr3。
表12
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:84的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-196(也称作“et140-46”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:49所示序列的氨基酸的重链可变区和包括具有seqidno:50所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表13的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:49所示序列的氨基酸的vh,如表13所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:50所示序列的氨基酸的vl,如表13所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:49所示序列的氨基酸的vh和包括具有seqidno:50所示序列的氨基酸的vl,如表13所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:161所示序列或其保守修饰的vhcdr1、包括具有seqidno:162所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:163所示序列的氨基酸或其保守修饰的vhcdr3,如表13所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:164所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:165所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:166所示序列的氨基酸或其保守修饰的vlcdr3,如表13所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:161所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:162所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:163所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:164所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:165所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:166所示序列的氨基酸或其保守修饰的vlcdr3,如表13所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:161所示序列的氨基酸的vhcdr1、包括具有seqidno:162所示序列的氨基酸的vhcdr2、包括具有seqidno:163所示序列的氨基酸的vhcdr3、包括具有seqidno:164所示序列的氨基酸的vlcdr1、包括具有seqidno:165所示序列的氨基酸的vlcdr2、和包括具有seqidno:166所示序列的氨基酸的vlcdr3。
表13
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:85的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-204(也称作“et140-54”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:53所示序列的氨基酸的重链可变区和包括具有seqidno:54所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表14的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:53所示序列的氨基酸的vh,如表14所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:54所示序列的氨基酸的vl,如表14所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:53所示序列的氨基酸的vh和包括具有seqidno:54所示序列的氨基酸的vl,如表14所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:167所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:168所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:169所示序列的氨基酸或其保守修饰的vhcdr3,如表14所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:170所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:171所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:172所示序列的氨基酸或其保守修饰的vlcdr3,如表14所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:167所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:168所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:169所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:170所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:171所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:172所示序列的氨基酸或其保守修饰的vlcdr3,如表14所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:167所示序列的氨基酸的vhcdr1、包括具有seqidno:168所示序列的氨基酸的vhcdr2、包括具有seqidno:169所示序列的氨基酸的vhcdr3、包括具有seqidno:170所示序列的氨基酸的vlcdr1、包括具有seqidno:171所示序列的氨基酸的vlcdr2、和包括具有seqidno:172所示序列的氨基酸的vlcdr3。
表14
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:86的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-190(也称作“et140-40”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:57所示序列的氨基酸的重链可变区和包括具有seqidno:58所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表15的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:57所示序列的氨基酸的vh,如表15所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:58所示序列的氨基酸的vl,如表15所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:57所示序列的氨基酸的vh和包括具有seqidno:58所示序列的氨基酸的vl,如表15所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:173所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:174所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:175所示序列的氨基酸或其保守修饰的vhcdr3,如表15所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:176所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:177所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:178所示序列的氨基酸或其保守修饰的vlcdr3,如表15所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:173所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:174所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:175所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:176所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:177所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:178所示序列的氨基酸或其保守修饰的vlcdr3,如表15所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:173所示序列的氨基酸的vhcdr1、包括具有seqidno:174所示序列的氨基酸的vhcdr2、包括具有seqidno:175所示序列的氨基酸的vhcdr3、包括具有seqidno:176所示序列的氨基酸的vlcdr1、包括具有seqidno:177所示序列的氨基酸的vlcdr2、和包括具有seqidno:178所示序列的氨基酸的vlcdr3。
表15
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:87的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-187(也称作“et140-37”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:61所示序列的氨基酸的重链可变区和包括具有seqidno:62所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表16的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:61所示序列的氨基酸的vh,如表16所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:62所示序列的氨基酸的vl,如表16所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:61所示序列的氨基酸的vh和包括具有seqidno:62所示序列的氨基酸的vl,如表16所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:179所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:180所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:181所示序列的氨基酸或其保守修饰的vhcdr3,如表16所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:182所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:183所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:184所示序列的氨基酸或其保守修饰的vlcdr3,如表16所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:179所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:180所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:181所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:182所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:183所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:184所示序列的氨基酸或其保守修饰的vlcdr3,如表16所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:179所示序列的氨基酸的vhcdr1、包括具有seqidno:180所示序列的氨基酸的vhcdr2、包括具有seqidno:181所示序列的氨基酸的vhcdr3、包括具有seqidno:182所示序列的氨基酸的vlcdr1、包括具有seqidno:183所示序列的氨基酸的vlcdr2、和包括具有seqidno:184所示序列的氨基酸的vlcdr3。
表16
在某些实施方式中,抗体或其他抗原结合蛋白质是抗bcmascfv或其抗原结合片段,其具有包括氨基酸序列seqidno:88的抗原结合区,并特异性结合bcma多肽(例如,具有氨基酸序列seqidno:71的bcma多肽或其片段),其命名为et140-174(也称作“et140-24”)。
在某些实施方式中,抗bcmascfv抗体包括:包括具有seqidno:65所示序列的氨基酸的重链可变区和包括具有seqidno:66所示序列的氨基酸的轻链可变区,其任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,抗bcmascfv抗体是具有选自表17的vh和vl区或cdr的scfv-fc融合蛋白或人igg全长。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:65所示序列的氨基酸的vh,如表17所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:66所示序列的氨基酸的vl,如表17所示。在某些实施方式中,抗bcmascfv包括有包括具有seqidno:65所示序列的氨基酸的vh和包括具有seqidno:66所示序列的氨基酸的vl,如表17所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:185所示序列或其保守修饰的vhcdr1、包括具有seqidno:186所示序列的氨基酸或其保守修饰的vhcdr2、和包括具有seqidno:187所示序列的氨基酸或其保守修饰的vhcdr3,如表17所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:188所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:189所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:190所示序列的氨基酸或其保守修饰的vlcdr3,如表17所示。在某些实施方式中,抗bcmascfv包括:包括具有seqidno:185所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:186所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:187所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:188所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:189所示序列的氨基酸或其保守修饰的vlcdr2、和包括具有seqidno:190所示序列的氨基酸或其保守修饰的vlcdr3,如表17所示。在某些实施方式中,细胞外抗原结合区域包括:包括具有seqidno:185所示序列的氨基酸的vhcdr1、包括具有seqidno:186所示序列的氨基酸的vhcdr2、包括具有seqidno:187所示序列的氨基酸的vhcdr3、包括具有seqidno:188所示序列的氨基酸的vlcdr1、包括具有seqidno:189所示序列的氨基酸的vlcdr2、和包括具有seqidno:190所示序列的氨基酸的vlcdr3。
表17
本发明公开的主题进一步提供包括重链可变区、轻链可变区、重链可变区与轻链可变区之间的接头肽和his标记和ha标记的抗bcmascfv抗体。在某些实施方式中,his标记和ha标记的氨基酸序列包括氨基酸序列seqidno:246,其提供如下:
tsgqagqhhhhhhgaypydvpdyas[seqidno:246]
编码seqidno:246的核苷酸序列是seqidno:247,其提供如下:
actagtggccaggccggccagcaccatcaccatcaccatggcgcatacccgtacgacgttccggactacgcttct[seqidno:247]
2.单克隆抗体
本发明公开的主题提供特异性结合bcma(例如人bcma)的人抗体(例如,人单克隆抗体),其如实施例2所示被分离并进行结构鉴定。人抗bcma抗体et140-192(也称作“et140-42”)、et140-197(也称作“et140-47”)、et140-180(也称作“et140-30”)、et140-172(也称作“et140-22”)、et140-157(也称作“et140-7”)、et140-153(也称作“et140-3”)、et140-201(也称作“et140-51”)、et140-167(也称作“et140-17”)、et140-163(也称作“et140-13”)、et140-207(也称作“et140-57”)、et140-165(也称作“et140-15”)、et140-188(也称作“et140-38”)、et140-196(也称作“et140-46”)、et140-204(也称作“et140-54”)、et140-190(也称作“et140-40”)、et140-187(也称作“et140-37”)和et140-174(也称作“et140-24”)的vh氨基酸序列分别示于seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61和65。et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174的vl氨基酸序列分别示于seqidno:2、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62和66。
只要et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体各自均可以结合bcma,vh和vl序列可以“混合并匹配”,以产生其他的抗bcma结合分子。这些“混合并匹配”的抗体的bcma结合可以使用本领域已知的结合检验测试,其包括例如elisa、蛋白质免疫印迹、ria、biacore分析。优选地,当vh和vl链混合并匹配时,将来自特定vh/vl配对的vh序列用结构上类似的vh序列代替。类似地,来自特定vh/vl配对的vl序列用结构上类似的vl序列代替。
在某些实施方式中,本发明公开的主题提供一种分离的抗体或其抗原结合部分,其包括:(a)包括选自seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61和65的氨基酸序列的重链可变区;和(b)包括选自seqidno:2、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62和66的氨基酸序列的轻链可变区;其中抗体特异性结合bcma,例如人bcma。
优选的重链和轻链组合包括:
(a)包括具有seqidno:1所示序列的氨基酸的重链可变区,和包括具有seqidno:2所示序列的氨基酸的轻链可变区;
(b)包括具有seqidno:5所示序列的氨基酸的重链可变区,和包括具有seqidno:6所示序列的氨基酸的轻链可变区;
(c)包括具有seqidno:9所示序列的氨基酸的重链可变区,和包括具有seqidno:10所示序列的氨基酸的轻链可变区;
(d)包括具有seqidno:13所示序列的氨基酸的重链可变区,和包括具有seqidno:14所示序列的氨基酸的轻链可变区;
(e)包括具有seqidno:17所示序列的氨基酸的重链可变区,和包括具有seqidno:18所示序列的氨基酸的轻链可变区;
(f)包括具有seqidno:21所示序列的氨基酸的重链可变区,和包括具有seqidno:22所示序列的氨基酸的轻链可变区;
(g)包括具有seqidno:25所示序列的氨基酸的重链可变区,和包括具有seqidno:26所示序列的氨基酸的轻链可变区;
(h)包括具有seqidno:29所示序列的氨基酸的重链可变区,和包括具有seqidno:30所示序列的氨基酸的轻链可变区;
(i)包括具有seqidno:33所示序列的氨基酸的重链可变区,和包括具有seqidno:34所示序列的氨基酸的轻链可变区;
(j)包括具有seqidno:37所示序列的氨基酸的重链可变区,和包括具有seqidno:38所示序列的氨基酸的轻链可变区;
(k)包括具有seqidno:41所示序列的氨基酸的重链可变区,和包括具有seqidno:42所示序列的氨基酸的轻链可变区;
(l)包括具有seqidno:45所示序列的氨基酸的重链可变区,和包括具有seqidno:46所示序列的氨基酸的轻链可变区;
(m)包括具有seqidno:49所示序列的氨基酸的重链可变区,和包括具有seqidno:50所示序列的氨基酸的轻链可变区;
(n)包括具有seqidno:53所示序列的氨基酸的重链可变区,和包括具有seqidno:54所示序列的氨基酸的轻链可变区;
(o)包括具有seqidno:57所示序列的氨基酸的重链可变区,和包括具有seqidno:58所示序列的氨基酸的轻链可变区;
(p)包括具有seqidno:61所示序列的氨基酸的重链可变区,和包括具有seqidno:62所示序列的氨基酸的轻链可变区;或者
(q)包括具有seqidno:65所示序列的氨基酸的重链可变区,和包括具有seqidno:66所示序列的氨基酸的轻链可变区。
在某些实施方式中,本发明公开的主题提供包括et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体的重链和轻链cdr1、cdr2和cdr3的抗体。et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174的vhcdr1的氨基酸序列分别示于seqidno:89、95、101、107、113、119、125、131、137、143、149、155、161、167、173、179和185。et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体的vhcdr2的氨基酸序列分别示于seqidno:90、96、102、108、114、120、126、132、138、144、150、156、162、168、174、180和186。et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体的vhcdr3的氨基酸序列分别示于seqidno:91、97、103、109、115、121、127、133、139、145、151、157、163、169、175、181和187。
et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体的vlcdr1的氨基酸序列分别示于seqidno:92、98、104、110、116、122、128、134、140、146、152、158、164、170、176、182和188。et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体的vlcdr2的氨基酸序列分别示于seqidno:93、99、105、111、117、123、129、135、141、147、153、159、165、171、177、183和189。et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体的vlcdr3的氨基酸序列分别示于seqidno:94、100、106、112、118、124、130、136、142、148、154、160、166、172、178、184和190。使用kabat系统对cdr区加以界定(kabat,e.a.等人,(1991)sequencesofproteinsofimmunologicalinterest,fifthedition,u.s.departmentofhealthandhumanservices,nihpublicationno.91-3242)。
只要这些抗体各自均与bcma结合,并且抗原结合特异性主要由cdr1、cdr2和cdr3区提供,vhcdr1、cdr2和cdr3序列和vlcdr1、cdr2和cdr3序列可以“混合并匹配”(即,来自不同抗体的cdr可以混合并匹配,尽管各个抗体必须含有vhcdr1、cdr2和cdr3以及vlcdr1、cdr2和cdr3),以产生其他的抗bcma结合分子。这些“混合并匹配”的抗体的bcma结合可以使用上述的结合检验测试。当vhcdr序列混合并匹配时,将来自特定vh序列的cdr1、cdr2和/或cdr3序列用结构上类似的cdr序列代替。类似地,当vlcdr序列混合并匹配时,将来自特定vl序列的cdr1、cdr2和/或cdr3序列优选地用结构上类似的cdr序列代替。本领域技术人员很容易显而易见地得出,通过将一个或多个vh和/或vlcdr区序列用来自本文公开的抗体et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174的cdr序列的结构上类似的序列代替,可以产生新的vh和vl序列。
在某些实施方式中,本发明公开的主题提供一种分离的抗体或其抗原结合片段,其包括:
(a)包括选自seqidno:89、95、101、107、113、119、125、131、137、143、149、155、161、167、173、179和185的氨基酸序列的重链可变区cdr1;
(b)包括选自seqidno:90、96、102、108、114、120、126、132、138、144、150、156、162、168、174、180和186的氨基酸序列的重链可变区cdr2;
(c)包括选自seqidno:91、97、103、109、115、121、127、133、139、145、151、157、163、169、175、181和187的氨基酸序列的重链可变区cdr3;
(d)包括选自seqidno:92、98、104、110、116、122、128、134、140、146、152、158、164、170、176、182和188的氨基酸序列的轻链可变区cdr1;
(e)包括选自seqidno:93、99、105、111、117、123、129、135、141、147、153、159、165、171、177、183和189的氨基酸序列的轻链可变区cdr2;和
(f)包括选自seqidno:94、100、106、112、118、124、130、136、142、148、154、160、166、172、178、184和190的氨基酸序列的轻链可变区cdr3;
其中抗体特异性结合bcma,例如人bcma。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:89所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:90所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:91所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:92所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:93所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:94所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:95所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:96所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:97所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:98所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:99所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:100所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:101所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:102所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:103所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:104所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:105所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:106所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:107所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:108所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:109所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:110所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:111所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:112所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:113所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:114所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:115所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:116所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:117所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:118所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:119所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:120所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:121所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:122所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:123所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:124所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:125所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:126所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:127所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:128所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:129所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:130所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:131所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:132所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:133所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:134所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:135所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:136所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:137所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:138所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:139所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:140所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:141所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:142所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:143所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:144所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:145所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:146所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:147所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:148所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:149所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:150所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:151所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:152所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:153所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:154所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:155所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:156所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:157所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:158所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:159所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:160所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:161所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:162所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:163所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:164所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:165所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:166所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:167所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:168所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:169所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:170所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:171所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:172所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:173所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:174所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:175所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:176所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:177所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:178所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:179所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:180所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:181所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:182所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:183所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:184所示序列的氨基酸的轻链可变区cdr3。
在某些实施方式中,抗体包括:
(a)包括具有seqidno:185所示序列的氨基酸的重链可变区cdr1;
(b)包括具有seqidno:186所示序列的氨基酸的重链可变区cdr2;
(c)包括具有seqidno:187所示序列的氨基酸的重链可变区cdr3;
(d)包括具有seqidno:188所示序列的氨基酸的轻链可变区cdr1;
(e)包括具有seqidno:189所示序列的氨基酸的轻链可变区cdr2;和
(f)包括具有seqidno:190所示序列的氨基酸的轻链可变区cdr3。
本文公开的抗bcma抗体的恒定区/框架区可以通过例如氨基酸取代改变,以修饰抗体特性(例如,增加或降低以下的一种或多种:抗原结合亲合力、fc受体结合、抗体糖水化合物例如糖基化、岩藻糖基化等、半胱氨酸残基的数量、效应细胞功能、效应细胞功能、互补功能或引入缀合位点)。
在某些实施方式中,本发明公开的抗bcma抗体是全长人抗体,例如,et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174中的任意一种。优选全长人mabs用于人的治疗用途,因为鼠科动物抗体导致称作hama(人抗鼠抗体,humananti-mouseantibodies)反应的免疫原性反应(azinovici等人,survivalbenefitassociatedwithhumananti-mouseantibody(hama)inpatientswithb-cellmalignancies.cancerimmunolimmunother2006;55(12):1451-8;tjandrajj等人,developmentofhumananti-murineantibody(hama)responseinpatients.immunolcellbiol1990;68(6):367-76),当对人施用时,导致严重的副反应,包括过敏和超敏反应。这一免疫原性反应通过人免疫细胞将由于与天然人抗体的氨基酸序列的稍许不同的鼠源抗体识别成异物来触发。可以使用本领域已知的人源化方法(riechmannl等人,reshapinghumanantibodiesfortherapy.nature1988;332(6162):332:323;queenc等人,ahumanizedantibodythatbindstotheinterleukin2receptor.procnatlacadsciusa1989;86(24):10029-33),来降低鼠源抗体的免疫原性(gerdr等人,serologicalanalysisofhumananti-humanantibodyresponsesincoloncancerpatientstreatedwithrepeateddosesofhumanizedmonoclonalantibodya33.cancerres2001;61,6851–6859)。
使用噬菌体展示文库使得能够对大量的所有ab进行选择得到对于非常确定的表位的独特、稀有的ab(噬菌体展示方面详见mccafferty等人,phageantibodies:filamentousphagedisplayingantibodyvariabledomains.nature,348:552-554)。因此,对来自肿瘤抗原的肽-mhc复合物分子具有高度特异性的人fab或单链fv(scfv)片段的快速识别成为可能(19-22)。最近,通过将黑色素瘤agmart-126-35/a2或gp100280-288/a2特异性的tcr样fab与截短形式的假单胞菌内毒素融合产生的免疫毒素已经显示出在体外和体内抑制黑色素瘤的生长(klechevskye等人,antitumoractivityofimmunotoxinswitht-cellreceptor-likespecificityagainsthumanmelanomaxenografts.cancerres2008;68(15):6360-6367)。此外,通过使用fab片段改造全长mab,可以绕开开发治疗性mab通常需要的耗时数月的工作直接产生治疗性人mab。本发明公开的主题涉及开发全长人mab,其识别例如人bcma多肽(例如具有seqidno:71所示氨基酸序列的多肽)用于癌症治疗。
3.同源抗体
在某些实施方式中,本发明公开主题的抗体包括:包括与本文所述抗体(例如,et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体)的氨基酸序列同源的氨基酸序列的重链和轻链可变区,其中抗体保留本发明公开主题的抗bcma抗体的所需功能特性。
例如,本发明公开的主题提供一种分离的抗体或其抗原结合部分,其包括重链可变区和轻链可变区,其中:
(a)包括与选自seqidno:1、5、9、13、17、21、25、29、33、37、41、45、49、53、57、61和65的氨基酸序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸序列的重链可变区;和
(b)包括与选自seqidno:2、6、10、14、18、22、26、30、34、38、42、46、50、54、58、62和66的氨基酸序列的同源性为至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%的氨基酸序列的轻链可变区;并且
其中抗体以1x10-7m或更低的kd与人bcma结合。
在某些实施方式中,vh和/或vl氨基酸序列与上述序列的同源性可以是至少大约80%、大约81%、大约82%、大约83%、大约84%、大约85%、大约86%、大约87%、大约88%、大约89%、大约90%、大约91%、大约92%、大约93%、大约94%、大约95%、大约96%、大约97%、大约98%或大约99%。具有与上述序列的vh和vl区具有高度同源性(即,80%或更高)的vh和vl区的抗体可以通过突变得到(例如,定点突变或pcr-介导的突变),然后使用本文所述的结合检验测试所编码的改变后的抗体保留的功能(即,结合亲合力)。
如本文所用,氨基酸序列之间的同源性百分比等于两个序列之间的同一性百分比。两个序列之间的同一性百分比或同源性是序列共享的相同位置的数量的函数(即,%同源性=相同位置的#/总的位置#x100),其考虑到对两个序列进行最优对比需要引入的间隙数量和各间隙的长度。序列的对比和两个序列之间同一性百分比的确定可以使用数学算法完成,如以下非限定性例子中所述。
两个氨基酸序列之间的同源性百分比可以使用e.meyers和w.miller的算法确定(comput.appl.biosci.,4:11-17(1988)),其已并入align程序(2.0版)中,使用pam120重量残基表,间隙长度补偿12,间隙补偿4。此外,氨基酸序列之间的同源性百分比可以使用needleman和wunsch算法确定(j.mol.biol.48:444-453(1970)),其已经并入到gcg软件包的gap程序中(可获自www.gcg.com),使用blossum62矩阵或pam250矩阵,间隙重量16、14、12、10、8、6或4,长度重量1、2、3、4、5或6。
额外地或另外可选地,本发明公开主题的蛋白质序列可以进一步用作“查询序列”,以对公开数据库进行搜索,例如,识别相关的序列。这样的搜索可以使用altschul等人(1990)j.mol.biol.215:403-10的xblast程序进行(2.0版)。blast蛋白质搜索可以用xblast程序进行,分值=50,字长=3,以得到与本发明抗体分子同源的氨基酸序列。为出于比较目的得到间隙对比,可以使用gappedblast,如altschul等人,(1997)nucleicacidsres.25(17):3389-3402所述。当使用blast和gappedblast程序时,可以使用各个程序(例如xblast和nblast)的缺省参数。(参见www.ncbi.nlm.nih.gov)。
4.具有保守修饰的抗体
在某些实施方式中,本发明公开主题的抗体包括:包括cdr1、cdr2和cdr3序列的重链可变区和包括cdr1、cdr2和cdr3序列的轻链可变区,其中这些cdr序列中的一个或多个包括基于本文所述优选抗体(例如,et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体)的特定氨基酸序列或其保守修饰,其中抗体保留本发明公开主题的抗bcma抗体所需的功能特性。本发明公开的主题提供一种分离的抗体或其抗原结合部分,其包括:包括cdr1、cdr2和cdr3序列的重链可变区和包括cdr1、cdr2和cdr3序列的轻链可变区,其中:
(a)重链可变区cdr3序列包括选自seqidno:91、97、103、109、115、121、127、133、139、145、151、157、163、169、175、181和187的氨基酸序列及其保守修饰;
(b)轻链可变区cdr3序列包括选自seqidno:94、100、106、112、118、124、130、136、142、148、154、160、166、172、178、184和190的氨基酸序列及其保守修饰;并且抗体以1x10-7m或更低的kd与人bcma结合。
在某些实施方式中,重链可变区cdr2序列包括选自seqidno:90、96、102、108、114、120、126、132、138、144、150、156、162、168、174、180和186的氨基酸序列及其保守修饰;轻链可变区cdr2序列包括选自seqidno:93、99、105、111、117、123、129、135、141、147、153、159、165、171、177、183和189的氨基酸序列及其保守修饰。
在某些实施方式中,重链可变区cdr1序列包括选自seqidno:89、95、101、107、113、119、125、131、137、143、149、155、161、167、173、179和185的氨基酸序列及其保守修饰;轻链可变区cdr1序列包括选自seqidno:92、98、104、110、116、122、128、134、140、146、152、158、164、170、176、182和188的氨基酸序列及其保守修饰。
如本文所用术语“保守序列修饰”是指不会显著影响或改变含有氨基酸序列的抗体的结合特征的氨基酸修饰。这种保守修饰包括氨基酸取代、添加和缺失。可以通过本领域已知的标准技术,比如定点突变和pcr介导的突变,将修饰引入本发明的抗体中。
保守氨基酸取代是其中氨基酸残基被具有类似侧链的氨基酸残基替换的取代。本领域中对具有类似侧链的氨基酸残基家族已有定义。示例性保守氨基酸取代示于表18。可以将氨基酸取代引入到所关注的抗体中,筛选具有所需活性例如保留/提高抗原结合、降低免疫原性或者提高adcc或cdc的产品。在某些实施方式中,本文公开的序列例如cdr序列、vh序列或vl序列可以具有至多大约1个、至多大约2个、至多大约3个、至多大约4个、至多大约5个、至多大约6个、至多大约7个、至多大约8个、至多大约9个或至多大约10个修饰和/或取代的氨基酸残基。
表18
氨基酸可以根据共同的侧链特性加以分组:
●疏水性:正亮氨酸、met、ala、val、leu、ile;
●中性亲水性:cys、ser、thr、asn、gln;
●酸性:asp、glu;
●碱性:his、lys、arg;
●影响链取向的残基:gly、pro;
●芳香性:trp、tyr、phe。
非保守性取代将会使得这些类型中的一个成员变更为另一个类型中的成员。
5.与本发明的抗bcma抗体交叉竞争结合bcma的抗bcma抗体
本发明公开的主题提供与公开的任意抗bcma抗体交叉竞争结合bcma(例如,人bcma)的抗体。例如,且无意于进行限定,交叉竞争抗体可以结合与本发明公开主题的任意抗bcma抗体相同的表位区,例如相同表位、相邻表位或者重叠。在某些实施方式中,用于交叉竞争研究的参考抗体可以是任意一种本文所公开的抗bcma抗体,例如,et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体。
在某些实施方式中,交叉竞争抗体与包括seqidno:71的14-22氨基酸的表位区结合。在某些实施方式中,交叉竞争抗体与选自seqidno:71的氨基酸8-22、9-23、10-24、11-25、12-26、13-27、14-28和8-28的1个、2个、3个、4个、5个、6个或7个表位区结合。
这些交叉竞争抗体可以在标准bcma结合检验中基于其与任意一种本发明公开的抗bcma抗体交叉竞争的能力加以识别。例如,可以使用biacore分析、elisa检验或流式细胞术来演示与本发明公开主题的抗体的交叉竞争。测试抗体抑制例如任意一种本发明公开的抗bcma抗体(例如,et140-192、et140-197、et140-180、et140-172、et140-157、et140-153、et140-201、et140-167、et140-163、et140-207、et140-165、et140-188、et140-196、et140-204、et140-190、et140-187和et140-174抗体)的结合人bcma的能力说明测试抗体可以与任意一种本发明公开的抗bcma抗体竞争结合人bcma,因此在人bcma上结合与任意一种本发明公开的抗bcma抗体相同的表位。在某些实施方式中,交叉竞争抗体在人bcma上结合与本发明公开的抗bcma抗体相同的表位。
6.结合抗原的抗体的鉴定
本发明公开主题的抗体可以通过例如标准elisa测试与bcma的结合。为了确定选择的抗bcma抗体是否与特定表位结合,可以使用市售试剂(pierce,rockford,il)对各抗体进行生物素酰化。如上文所述,使用bcma涂覆的elisa板,可以使用未标记的单克隆抗体和生物素酰化的单克隆抗体进行竞争研究。生物素酰化的mab结合可以用链霉素-亲和素-碱性磷酸酶探针检测。
为了确定提纯的抗体的同种型,可以使用特定同种型抗体的特异性试剂进行同种型elisa。抗bcma人igg可以进一步通过蛋白质免疫印迹测试与bcma抗原的反应性。
在某些实施方式中,kd通过同位素标记的抗原结合检验(ria)测量。在某些实施方式中,ria以fab形式的所关注抗体及其抗原进行。例如,fab对于抗原的溶液结合亲合力通过以下方法测量:在滴定系列未标记抗原的存在下将fab用最小浓度的(125i)标记抗原平衡,然后用抗fab抗体涂覆的板捕获结合的抗原(参见:例如,chen等人,j.mol.biol.293:865-881(1999))。
在某些实施方式中,kd使用
表位定位
在某些实施方式中,本发明公开的抗bcma抗体结合包括seqidno:71所示氨基酸序列的人bcma多肽。在某些实施方式中,本发明公开的抗bcma抗体结合seqidno:71所示氨基酸序列的一个或多个部分。在某些实施方式中,本发明公开的抗bcma抗体结合包括seqidno:71的氨基酸14-22的表位区。在某些实施方式中,本发明公开的抗bcma抗体结合选自seqidno:71的氨基酸8-22、9-23、10-24、11-25、12-26、13-27、14-28和8-28的1、2、3、4、5、6或7个表位区。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:9所示序列的氨基酸的重链可变区和包括具有seqidno:10所示序列的氨基酸的轻链可变区,任选地在重链可变区和轻链可变区之间具有(iii)接头序列,例如接头多肽。在某些实施方式中,接头包括具有seqidno:69所示序列的氨基酸。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括与seqidno:21所示氨基酸序列的同源性为至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的氨基酸序列的vh。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:21所示序列的氨基酸的vh。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括与seqidno:22所示氨基酸序列的同源性为至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的氨基酸序列的vl。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:22所示序列的氨基酸的vl。本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:21所示序列的氨基酸的vh和包括具有seqidno:22所示序列的氨基酸的vl。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:119所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:120所示序列的氨基酸或其保守修饰的vhcdr2和包括具有seqidno:121所示序列的氨基酸或其保守修饰的vhcdr3。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:122所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:123所示序列的氨基酸或其保守修饰的vlcdr2和包括具有seqidno:124所示序列的氨基酸或其保守修饰的vlcdr3。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:119所示序列的氨基酸或其保守修饰的vhcdr1、包括具有seqidno:120所示序列的氨基酸或其保守修饰的vhcdr2、包括具有seqidno:121所示序列的氨基酸或其保守修饰的vhcdr3、包括具有seqidno:122所示序列的氨基酸或其保守修饰的vlcdr1、包括具有seqidno:123所示序列的氨基酸或其保守修饰的vlcdr2和包括具有seqidno:124所示序列的氨基酸或其保守修饰的vlcdr3。在某些实施方式中,本发明公开的结合包括seqidno:71的氨基酸14-22的表位区的抗bcma抗体包括:包括具有seqidno:119所示序列的氨基酸的vhcdr1、包括具有seqidno:120所示序列的氨基酸的vhcdr2、包括具有seqidno:121所示序列的氨基酸的vhcdr3、包括具有seqidno:122所示序列的氨基酸的vlcdr1、包括具有seqidno:123所示序列的氨基酸的vlcdr2和包括具有seqidno:124所示序列的氨基酸的vlcdr3。在某些实施方式中,本发明公开的抗bcma抗体是et140-3(或“et140-153”)。
7.免疫缀合物
本发明公开的主题提供一种缀合有治疗部分例如细胞毒素、药物(例如,免疫抑制剂)或放射性毒素的抗bcma抗体或其片段。这些缀合物在本文中称作“免疫缀合物”。包括一种或多种细胞毒素的免疫缀合物称作“免疫毒素”。细胞毒素或细胞毒性药剂包括任何不利于(例如杀死)细胞的药剂。例子包括紫杉醇(例如,蓖麻毒素、白喉毒素、白树毒素)、松胞菌素b、短杆菌肽d、溴化乙锭、吐根碱、丝裂霉素、表鬼臼素、表鬼臼素噻吩糖苷、长春新碱、长春花碱、秋水仙素、阿霉素、柔红霉素、二羟基炭疽菌素二酮、米托蒽醌、光神霉素、放线菌素d、1-去氢睾酮、糖皮质激素、普鲁卡因、丁卡因、利多卡因、心得安(propranolol)和嘌呤霉素及其类似物或同源物。例如,治疗药剂还可以包括例如卡奇霉素(calecheamicin)、aureastatin、抗代谢物(例如,氨甲碟呤、6-巯基嘌呤、6-硫鸟嘌呤、阿糖胞苷、5-氟尿嘧啶氨烯咪胺(5-fluorouracildecarbazine)、烷基化试剂(例如,氮芥、三胺硫磷苯丁酸氮芥(thioepachlorambucil)、苯丙氨酸氮芥、卡莫司汀(bsnu)和洛莫司汀(ccnu)、环磷酰胺、白消安、二溴甘露醇、链脲菌素、丝裂霉素c和顺二氯二胺铂(ii)(ddp)顺铂)、蒽环类(例如,柔红霉素(前道诺霉素)和阿霉素)、抗生素(例如,更生霉素(前放线菌素)、博来霉素、光神霉素和安曲霉素(anthramycin,amc))和抗有丝分裂药(例如,长春新碱和长春花碱)。
其他可以缀合在本文公开的抗bcma抗体上的治疗性细胞毒素的例子包括倍癌霉素(duocarmycins)、卡奇霉素(calicheamicins)、美登素(maytansines)和阿里他汀(auristatins)及其衍生物。卡奇霉素抗体缀合物的例子是市售的(mylotargtm;wyeth-ayerst)。
可以使用本领域可提供的接头技术将细胞毒素与抗bcma抗体缀合。已经用于将细胞毒素与抗体缀合的接头类型包括但不限于腙、硫醚、醚、二硫化物和含肽接头。接头可以选择成例如易于在溶酶体区室内通过低ph切割,或者易于通过蛋白酶例如优先在肿瘤组织中表达的蛋白酶例如组织蛋白酶(如组织蛋白酶b、c、d)切割。用于细胞毒素类型、接头和将治疗剂与抗体缀合的方法的详述另外参见saito,g.等人,(2003)adv.drugdeliv.rev.55:199-215;trail,p.a.等人(2003)cancerimmunol.immunother.52:328-337;payne,g.(2003)cancercell3:207-212;allen,t.m.(2002)nat.rev.cancer2:750-763;pastan,i.和kreitman,r.j.(2002)curr.opin.investig.drugs3:1089-1091;senter,p.d.和springer,c.j.(2001)adv.drugdeliv.rev.53:247-264。
本发明公开主题的抗bcma抗体还可以与放射性同位素缀合,以产生细胞毒性放射性药物,也称为放射性免疫缀合物。可以与抗体缀合用于诊断或治疗用途的放射性同位素的例子包括但不限于90y、131i、225ac、213bi、223ra和227th。放射性免疫缀合物的制备方法是本领域已建立的。放射性免疫缀合物的例子是市售的,包括zevalintm(idecpharmaceuticals)和bexxartm(corixapharmaceuticals),类似的方法可以用于使用本发明的抗体制备放射性免疫缀合物。
本发明公开主题的抗体缀合物可以用于修饰指定的生物反应,药物部分不应理解成限于经典的化学治疗剂。例如,药物部分可以是具有所需生物活性的蛋白质或多肽。这样的蛋白质可以包括例如酶促活性毒素或其活性片段,例如相思豆毒素、蓖麻毒素a、假单胞菌外毒素或白喉毒素;例如肿瘤坏死因子(tnf)或干扰素-γ的蛋白质;或生物反应修饰剂,例如,如淋巴因子、白介素-1(“il-1”)、白介素-2(“il-2”)、白介素-6(“il-6”)、粒细胞-巨噬细胞集落刺激因子(“gm-csf”)、粒细胞集落刺激因子(“g-csf”)或其他生长因子。
用于将这些治疗部分与抗体缀合的技术是公知的,参见:例如,arnon等人,"monoclonalantibodiesforimmunotargetingofdrugsincancertherapy",inmonoclonalantibodiesandcancertherapy,reisfeldetal.(eds.),pp.243-56(alanr.liss,inc.1985);hellstrom等人,"antibodiesfordrugdelivery",incontrolleddrugdelivery(2nded.),robinson等人(eds.),pp.623-53(marceldekker,inc.1987);thorpe,"antibodycarriersofcytotoxicagentsincancertherapy:areview",inmonoclonalantibodies'84:biologicalandclinicalapplications,pincheraetal.(eds.),pp.475-506(1985);"analysis,results,andfutureprospectiveofthetherapeuticuseofradiolabeledantibodyincancertherapy",inmonoclonalantibodiesforcancerdetectionandtherapy,baldwinetal.(eds.),pp.303-16(academicpress1985);和thorpe等人,"thepreparationandcytotoxicpropertiesofantibody-toxinconjugates",immunol.rev.,62:119-58(1982)。
8.双特异性分子
本发明公开的主题提供包括本文公开的抗bcma抗体或其片段的双特异性分子。本发明公开主题的抗体或其抗原结合部分可以衍生化或连接在另一功能分子例如另一多肽或蛋白质(例如另一抗体或受体配体)上,以产生与至少两种不同结合位点或目标分子结合的双特异性分子。本发明公开主题的抗体实际上可以衍生化或连接在一种以上其他功能分子上,以产生于两种以上不同结合位点和/或目标分子结合的多特异性分子;如本文所用,这些多特异性分子也要包括在术语“双特异性分子”内。为了产生双特异性分子,可以将本发明公开的抗bcma抗体功能性地与一种或多种其他结合分子例如另一抗体、抗体片段、多肽或结合模拟物连接(例如,通过化学偶联、基因融合、非共价缔合等),使得产生双特异性分子。
本发明公开的主题提供至少包括bcma第一结合特异性和第二目标表位的第二结合特异性的双特异性分子。第二目标表位可以是bcma表位或非bcma表位,例如,不同的抗原。在某些实施方式中,双特异性分子是多特异性的,分子可以进一步包括第三结合特异性。当双特异性分子的第一部分在例如肿瘤细胞上与抗原结合、并且双特异性抗体的第二部分识别出人免疫效应细胞表面上的抗原时,抗体能够通过与人免疫效应细胞上的效应抗原结合募集该效应细胞的活性。在某些实施方式中,双特异性抗体因此能够在效应细胞例如t细胞和肿瘤细胞之间形成连接,从而提高效应器功能。在某些实施方式中,本公开内容的双特异性部分包括至少与bcma的第一结合和至少与免疫细胞的第二结合。例如,且无意于进行限定,本公开内容的双特异性分子包括至少与bcma的第一结合和至少与免疫细胞例如cd3表面上存在的受体的结合。
使用本领域已知方法,通过缀合组分结合特异性,可以制备本发明公开主题的双特异性分子。例如,可以分别产生双特异性分子的各个结合特异性,然后彼此缀合。当结合特异性为蛋白质或肽时,可以使用多种偶联剂或交联剂用于共价缀合。交联剂的例子包括蛋白质a、碳化二亚胺、n-琥珀酰亚胺基-s-乙酰基-硫代乙酸酯(sata)、5,5'-二硫代双(2-硝基苯甲酸)(dtnb)、邻苯撑双马来酰亚胺(opdm)、n-琥珀酰亚胺基-3-(2-吡啶基二硫代)丙酸酯(spdp)和磺基琥珀酰亚胺基4-(n-马来酰亚胺甲基)环己烷-l-甲酸酯(sulfo-smcc)(参见:例如,karpovsky等人,(1984)j.exp.med.160:1686;liu等人,(1985)proc.natl.acad.sci.usa82:8648)。其他方法包括以下文献中所述的方法:paulus(1985)behringins.mitt.no.78:118-132;brennan等人,(1985)science229:81-83;和glennie等人,(1987)j.immunol.139:2367-2375)。优选的缀合剂为sata和磺基-smcc,二者均可获自piercechemicalco.(rockford,il)。
当结合双特异性为抗体时,可以通过两个重链c-端铰链区的巯基键使他们缀合。在某些实施方式中,在缀合之前,将铰链区修饰成含有奇数个巯基残基,优选1个。
可选地,可以在相同载体中编码两种结合特异性,并在相同宿主细胞中表达和组装。在双特异性分子为mabxmab、mabxfab、fabxf(ab')2或配体xfab融合蛋白时,该方法特别有用。
例如,通过酶联免疫吸附检验(elisa)、放射性免疫检验(ria)、facs分析、生物检验(例如,生长抑制)或蛋白质印迹检验,可以确认双特异性分子与其特异性目标的结合。这些检验各自通常通过使用对所关注复合物有特异性的标记试剂(例如抗体),检测所具体关注的抗原-抗体复合物的存在。可选地,复合物可以使用多种其他免疫检验中任意检验来检测。例如,抗体可以进行放射性同位素标记,并用于放射性免疫检验(ria)(参见:例如,weintraub,b.,principlesofradioimmunoassays,seventhtrainingcourseonradioligandassaytechniques,theendocrinesociety,march,1986,在此将其并入作为参考)。放射性同位素可以通过例如使用γ计数器或闪烁计数器或通过放射自显影的方式检测。
9.选择针对bcma多肽的高亲合力scfv
下一步是从不结合或以较低亲合力结合的人噬菌体展示文库中选择与所关注的目标抗原以高亲合力结合的噬菌体。这一点通过以下方式实现:将噬菌体与结合在固体载体例如小珠或哺乳动物细胞上的抗原反复结合,然后除去未结合的噬菌体,并洗脱特异性结合的噬菌体。在某些实施方式中,首先将抗原生物素酰化,用于固定在例如链霉亲和素缀合的dynabeadsm-280上。将噬菌体文库与细胞、小珠或其他固体载体一起孵育,通过洗涤除去非结合噬菌体。选择并测试结合的克隆。
一经选择,通过流式细胞术测试阳性scfv克隆在活的3t3细胞表面上与bcma(人bcma)的结合。简言之,将噬菌体克隆与过度表达bcma的3t3细胞一起孵育。将细胞洗涤,然后与小鼠抗m13山羊蛋白质mab一起孵育。再次将细胞洗涤,并在流式细胞术之前用fitc-山羊抗小鼠ig标记。
在其他实施方式中,抗bcma抗体可以包括一个或多个设计成提高蛋白质稳定性、抗体结合、表达水平或者引入治疗剂缀合位点的框架区氨基酸取代。然后使用这些scfv根据本领域技术人员已知的方法制造重组人单克隆ig。
10.使用选择的scfv片段改造全长mab
噬菌体展示技术使得可以迅速选择并产生抗原特异性scfv和fab片段,该抗原特异性scfv和fab片段自身有用,或者其可以进一步开发成提供完整的抗体、抗原结合蛋白质或其抗原结合部分。具有fc结构域的完整mab相对于scfv和fab抗体具有若干优势。首先,只有全长ab发挥例如通过fc结构域介导的cdc和adcc的免疫学功能。第二,二价mab提供比单体fabab更强的抗原结合亲合力。第三,血浆半衰期和肾脏清除将不同于fab和二价mab。各自具体的特性和优势可以匹配给计划的效应器策略。第四,二价mab可以以与scfv和fab不同的速率内化,改变免疫功能或载体功能。例如,α发射体不需要内化成杀死目标,但许多药物和毒素将受益于免疫复合物的内化。在某些实施方式中,因此,当由噬菌体展示文库获得bcma特异性scfv克隆时,产生使用scfv片段的全长iggmab。
为了在中国仓鼠卵巢(cho)细胞中产生重组人单克隆igg,可以基于本领域技术人员已知的方法对全长iggmab进行改造(tomomatsu等人,productionofhumanmonoclonalantibodiesagainstfceriabyamethodcombininginvitroimmunizationwithphagedisplay.bioscibiotechnolbiochem73(7):1465-14692009)。简言之,可以将抗体可变区亚克隆到具有匹配λ或κ轻链恒定序列和igg1子类fc(例如)的哺乳动物表达载体中(lidijap等人,anintegratedvectorsystemfortheeukaryoticexpressionofantibodiesortheirfragmentsafterselectionfromphagedisplaylibraries.gene1997;187(1):9-18;lisajh等人crystallographicstructureofanintactlgg1monoclonalantibody.journalofmolecularbiology1998;275(5):861-872)。可以使用动力学结合分析(yasminana等人,probingthebindingmechanismandaffinityoftanezumab,arecombinanthumanizedanti-ngfmonoclonalantibody,usingarepertoireofbiosensors.proteinscience2008;17(8):1326-1335),以确认全长igg以毫微摩尔级kd与bcma特异性结合。
药物组合物和治疗方法
本发明公开主题的抗bcma抗体可以足以防止、抑制或降低肿瘤发展的量对患有肿瘤(例如,多发性骨髓瘤)的患者施用,用于治疗性治疗。发展包括例如肿瘤的生长、浸润、转移和/或复发。该用途的有效量将取决于疾病的严重程度和患者自身免疫系统的一般状况。剂量方案另外随着疾病状态和患者状态而变化,通常典型范围从单次灌注(singlebolus)剂量或连续输注至每天多次给药(例如,每4-6小时),或者由治疗医师和患者状况指示。
在本领域技术人员的能力和知识以内能够识别本发明公开主题的抗bcma抗体可治疗的医疗状况。例如,患有多发性骨髓瘤或者处于发生多发性骨髓瘤风险中的人个体适合于施用本发明公开的抗bcma抗体。如果个体是该治疗的候选者,例如,本领域临床医师可以很容易地通过临床测试、物理检查和医疗/家族史确定。
在某些实施方式中,本发明公开的主题提供一种通过将本发明公开的抗bcma抗体与一种或多种其他药剂组合给药以治疗肿瘤的方法。例如,本发明公开的主题提供一种通过将本发明公开的抗bcma抗体与抗肿瘤药剂组合给药以治疗肿瘤的方法。抗bcma抗体可以与一种或多种抗肿瘤药剂化学或生物合成地连接。
合适的肿瘤的非限定性例子包括多发性骨髓瘤、非霍奇金淋巴瘤、霍奇金淋巴瘤、慢性淋巴细胞性白血病(cll)、成胶质细胞瘤和waldenstrom氏巨球蛋白血症。在某些实施方式中,肿瘤是多发性骨髓瘤。
可以使用任何适当的方法或途径施用本发明公开的抗bcma抗体,并任选地一起施用抗肿瘤药剂。给药途径包括例如口服、静脉内、腹膜内、皮下或肌内给药。但是,应当强调的是,本发明公开的主题不限于任何具体的给药方法或途径。
应当注意到,本发明公开的抗bcma抗体可以作为与受体特异性结合、并在配体-毒素内化之后释放毒性的、致死的负载(payload)的缀合物给药。
应当理解到,本发明公开主题的抗bcma抗体可以以额外地包括药学上可接受载体的形式给药。合适的药学上可接受载体包括例如一种或多种的水、盐水、磷酸盐缓冲液、葡萄糖、甘油、乙醇等及其组合。药学上可接受的载体可以进一步包括少量的辅助物质,例如润湿剂或乳化剂、防腐剂或缓冲剂,其提高结合蛋白质的保质期或有效性。如本领域公知,注射组合物可以配制成在对哺乳动物施用之后提供迅速、持久或延迟的活性成分的释放。
本发明公开的主题另外提供抗体和编码上述抗体的核酸在治疗肿瘤(例如,多发性骨髓瘤)、诊断和预防应用以及在检测细胞和组织中bcma的研究工具中的用途。包括公开的抗体和核酸的药物组合物也包括在本发明公开的主题内。用于通过载体化免疫疗法的基于抗体的治疗的包括本发明公开主题的核酸的载体也根据在本发明公开的主题预期。载体包括能够表达和分泌抗体的表达载体,以及引导抗原结合蛋白例如嵌合抗原受体的细胞表面表达的载体。
包括核酸的细胞例如已经用本发明的载体转染的细胞也包括在本发明公开的主题内。
药盒
本发明公开的主题提供用于治疗或预防肿瘤(例如,多发性骨髓瘤)的药盒。在某些实施方式中,药盒包括以单位剂型含有有效量抗bcma抗体的治疗组合物。在一些实施方式中,药盒包括容纳治疗性或预防性疫苗的无菌容器;这样的容器可以是盒子、安瓿、瓶子、小瓶、管、袋、小袋、泡罩包装或其他本领域已知的容器形式。这些容器可以由塑料、玻璃、金属箔或者其他适于保存药物的材料制成。
如果需要,抗bcma抗体可以与用于将细胞对患有肿瘤(例如,多发性骨髓瘤)或者处于发展肿瘤风险中的受试者施用的说明书一起提供。说明书通常包括有关组合物用于治疗或预防肿瘤(例如,多发性骨髓瘤)的用途的信息。在其他实施方式中,说明书包括至少一种以下内容:治疗剂的说明;用于治疗或预防瘤形成(例如,多发性骨髓瘤)或其症状的剂量方案和给药;警示;适应症;禁忌症;用药过量信息;不良反应;动物药理学;临床研究;和/或参考文献。说明书可以直接印在容器上(如果存在),或者作为应用于容器的标签,或者作为在容器中或者与容器一起提供的纸张、小册子、卡片或文件夹。
方法
流式细胞术分析.对于细胞表面染色,可以将细胞与适当的mab一起在冰上孵育30分钟,洗涤,如果需要,将其与第二抗体试剂一起孵育。流式细胞术数据可以用facscalibur(bectondickinson)收集,并用flowjov8.7.1和9.4.8软件分析。
bcma特异性scfv的选择和鉴定.使用人scfv抗体噬菌体展示文库进行mab克隆的选择。简言之,首先可以将生物素酰化的抗原与人scfv噬菌体文库混合,然后通过链霉亲和素缀合的dynabeadsm-280通过磁分离架拉下抗原-scfv抗体复合物。然后将结合的克隆洗脱,并用于感染大肠杆菌(e.coli)xl1-blue。可以对细菌中表达的scfv噬菌体进行提纯(yasminana等人,probingthebindingmechanismandaffinityoftanezumab,arecombinanthumanizedanti-ngfmonoclonalantibody,usingarepertoireofbiosensors.proteinscience2008;17(8):1326-1335;robertswk等人,vaccinationwithcd20peptidesinducesabiologicallyactive,specificimmuneresponseinmice.blood2002:99(10):3748-3755)。筛选可以进行3-4轮,以富集特异性结合bcma的scfv噬菌体克隆。阳性克隆可以针对生物素酰化的单链bcma通过标准elisa方法来鉴定。阳性克隆可以进一步通过流式细胞术使用bcma+细胞系3t3测试其在活细胞表面上与bcma的结合。可以将细胞洗涤,然后可以按照以下步骤进行染色。
首先可以将细胞用提纯的scfv噬菌体克隆染色,然后用小鼠抗m13mab染色,最后将山羊抗小鼠ig与fitc缀合。每个染色步骤可以在冰上进行30-60分钟,每个染色步骤之间可以将细胞洗涤两次。
使用选择的scfv片段改造全长mab.可以在hek293和中国仓鼠卵巢(cho)细胞系中产生所选噬菌体克隆的全长人igg1,如(caronpc,classk,lairdw,coms,queenc,scheinbergda.engineeredhumanizeddimericformsofiggaremoreeffectiveantibodies.jexpmed176:1191-1195.1992)所述。简言之,可以将抗体可变区亚克隆到哺乳动物表达载体中,将人λ或κ轻链恒定区与人igg恒定区序列匹配。提纯的全长igg抗体的分子量可以在还原和非还原条件下通过电泳测量。
用于bcma的全长人igg的鉴定.最初,全长人iggmab对bmca的特异性可以通过以下方法确定:将转导成过量表达bcma的3t3细胞染色,然后将第二山羊抗人iggmab与pe或fitc缀合。荧光强度可以通过流式细胞术测量。可以使用相同的方法确定mab与新鲜肿瘤细胞和细胞系的结合。
抗体依赖性细胞毒性(adcc).用于adcc的目标细胞可以是过量表达bcma的3t3细胞。可以将不同浓度的抗bcma抗体或其对照人igg与目标细胞和新鲜的pbmc以不同的效应器︰目标(e:t)比例一起孵育16小时。可以收获上清液,细胞毒性可以使用获自promega的cytotox96非放射性药盒按照其说明书通过ldh释放检验测量。细胞毒性也可以通过标准的4小时51cr-释放检验测量。
实施例
提供以下实施例,以便为本领域普通技术人员提供如何制造和使用本发明公开主题的抗体、双特异性分子、包括其的组合物、筛选和治疗方法的完整的公开和说明,其无意于对发明人视作本发明公开主题的范围进行限定。应当理解到,给予上文提供的概述,可以实施许多种其他的实施方式。
实施例1-不同组织中的bcma表达
通过考察数据库例如癌细胞系大全和biogps中的基因表达图谱,在各种恶性和正常组织中评价人bcma的表达。如图1所示,人在淋巴瘤和多发性骨髓瘤中高度表达,但在其他恶性组织中没有。正常表达似乎限于b-细胞和血浆细胞。基于发明人对cd19靶向cart细胞的患者经验,这些正常细胞类型潜在的bcma靶向cart细胞根除可能没有显著的不良反应。任何生理抗体产生的缺乏可以用静脉内免疫球蛋白治疗来解决。
实施例2-使用全人噬菌体展示文库选择bcma特异性scfv
针对bcma噬菌体展示进行3轮筛选,以富集特异性结合bcma的scfv噬菌体克隆。针对过量表达bcma的3t3细胞用12个不同的噬菌体文库进行独立筛选,识别出186个克隆。各个bcma阳性scfv噬菌体克隆通过elisa测定,对具有独特dna编码序列的克隆进行进一步鉴定。为了测试scfv是否与活细胞上的bcma结合,测试阳性噬菌体克隆与bcma-阳性细胞系3t3的结合。测序之后,从79个测序的阳性克隆中发现57个独特的bcma-fc阳性克隆;独特克隆率为72%。从噬菌体抗体克隆对bcma-3t3和亲代3t3细胞系的facs分析确认了25个独特的阳性克隆。
实施例3-抗bcma抗体的筛选数据
elisa筛选:图6显示了使用特异性scfv噬菌体抗体克隆(et140-3、et140-24、et140-37、et140-40和et140-54)对bcma抗原进行蛋白质elisa筛选的代表性结果。将板分别用人bcmaecd-fc融合蛋白、对照-fc融合蛋白或者作为空白对照的单独的pbs涂覆。将来自对bcmaecd-fc融合蛋白的富集的噬菌体展示筛选池的各个噬菌体克隆在涂覆的板中孵育。通过hrp-缀合的抗m13抗体检测噬菌体克隆的结合,并使用tmb底物显色。在450nm下读取吸收。
facs筛选:图7显示了bcma特异性噬菌体抗体克隆et140-3、et140-24、et140-37、et140-40和et140-54的代表性facs分析结果。将噬菌体克隆与3t3-bcma细胞系一起孵育,然后与抗m13小鼠抗体一起孵育。最后,再次洗涤之后,将apc标记的抗小鼠igg第二抗体加入到反应中。通过facs测量结合,并表达为平均荧光强度(mfi)。将细胞与单独的第二抗体、与m13k01辅助噬菌体一起孵育、以及仅细胞用作阴性对照。
实施例4-抗bcma抗体的表位定位
基于具有n-端生物素+sgsg接头+具有1个氨基酸间隔的15个氨基酸的ecd序列对bcma多肽进行排序。肽库示于表19中。
表19
将肽以pbst(pbs+0.05%tween-20)中2ug/ml涂覆在链霉亲和素板上。洗涤并用3%bsa阻断之后,洗涤之后,分别向孔中加入1ug/mlet140-3、et140-24、et140-54或et901migg1。所有实施例中使用的“migg1”表示可变区是全长人序列且fc部分是小鼠igg1。然后将hrp抗小鼠igg检测抗体加入到每个孔中。最后,使用tmb底物显色。记录a450用于数据分析。结果示于图2-5。如图2和图5所示,et140-3与seqidno:71的多肽7-13(即,氨基酸8-22、9-23、10-24、11-25、12-26、13-27和14-28)结合。如图3和图4所示,对于et140-24或et140-54没有发现线性表位。
总结:将3et140抗体(migg1)与同种型对照et901migg1一起测试其对bcma-ecd的结合表位。使用由39种肽(n-端生物素+sgsg接头+15氨基酸,1氨基酸偏移)组成的肽库用于表位定位elisa。这使得可以搜索bcma-ecd的线性结合表位。使用et901migg1作为每个肽的背景参考。仅et140-3可以识别其表位区:包括seqidno:71的氨基酸14-22的区域,例如seqidno:71的氨基酸8-28。
et140-24和et140-54没有显示任何显著的对肽库的结合。这表明这两种抗体识别构象表位,而不是bcma的线性表位。
实施例5-通过表面等离子体共振的抗bcma抗体重组抗原
et140-153migg1(或“et140-3migg1”)、et140-174migg1(或“et140-24migg1”)、et140-204migg1(或“et140-54migg1”)和bcma重组抗原之间相互作用的动力学使用biacorex100仪器测量。简言之,通过使biotincapture试剂以2μl/min流过流动池5分钟,将50μg/ml修饰的链霉亲和素固定在传感芯片chipcap上。将10ug/ml生物素酰化bcma-fc蛋白质以30μl/min的速率上样到流动池上3分钟。按照动力学标准方案,进行0.6至15μg/ml的esk1系列注射,每一步由以30μl/min注射3分钟和解离3分钟组成。之后,将表面用由75%v/v8m胍-hcl和25%v/v1mnaoh组成的溶液再生2分钟。使用biacorex100评价软件(2.0.1版)通过全局拟合(1:1langmuir结合模型)得出动力学常数。结合亲合力数据示于表20。
表20
尽管前述本发明公开的主题已经出于清楚理解的目的通过说明和实施例进行了相当程度的说明,说明书和实施例均不应当理解成对本发明公开的主题进行限定。在此将本文引用的所有专利和科学文献的公开内容明确地全文并入作为参考。
- 还没有人留言评论。精彩留言会获得点赞!