导管稳定性指示的制作方法
背景技术:
1.技术领域
本发明涉及组织消融系统。更具体地,本发明涉及对侵入式探头与体内的组织之间的接触的监测。
2.相关领域的描述
当心脏组织的区域向相邻组织异常地传导电信号时,发生心律失常诸如心房纤颤,从而扰乱正常的心动周期并造成心律不齐。
用于治疗此类心律失常的手术包括以手术形式来破坏造成心律失常的信号源,以及破坏用于此类信号的传导通路。通过经由导管施加能量来选择性地消融心脏组织,有时可终止或更改不想要的电信号从心脏的一部分传播到另一部分。该消融方法通过形成非传导性消融灶来破坏无想要的电通路。
验证与目标组织的物理电极接触和接触稳定性对于控制消融能量的递送而言非常重要。本领域已针对验证电极与组织接触进行了大量尝试,并且已提出多种技术。例如,美国专利no.6,695,808描述了用于治疗所选择的患者组织或器官区域的设备。探头具有可推抵该区域的接触表面,从而产生接触压力。压力换能器测量接触压力。手术过程中的医疗器械必须牢固放置但是不与解剖表面过度接触,该装置据信通过向医疗器械的使用者提供用于指示接触力的存在和量值的信息来满足手术过程的需要。
又如,美国专利no.6,241,724描述了使用分段电极组件来在身体组织内产生消融灶的方法。在一个实施方案中,导管上的电极组件携带压力换能器,该压力换能器感测与组织的接触并向压力接触模块传送信号。该模块识别与压力换能器信号相关联的电极元件并指导能量发生器将射频(rf)能量传送到这些元件而不传送到仅与血液接触的其他元件。
美国专利no.6,915,149中提供了另一个示例。该专利描述了使用具有测量局部电活动的末端电极的导管来标测心脏的方法。为了避免可能因末端与组织接触不良而产生的伪像,使用压力传感器测量末端与组织之间的接触压力,以确保稳定接触。
美国专利申请公布2007/0100332描述了用于评估组织消融的电极组织接触的系统和方法。导管轴内的机电传感器产生电信号,该电信号对应于导管轴的远侧部分内的电极的移动量。输出装置接收用于评估电极和组织之间的接触水平的电信号。
本领域已知的用于评估导管组织接触的基于阻抗的方法通常依赖于对导管上电极与体表电极之间的阻抗的量值的测量。当量值低于某个阈值时,电极被视为与组织接触。这种二元接触对于体表电极与皮肤之间的阻抗变化是敏感的。
sauarav等人的以引用方式并入本文的美国专利申请公布no.2008/0288038和no.2008/0275465描述了可包括适于施加电能的电极的电极导管系统。当电极靠近目标组织时,可在电极与接地部之间实现适于测量阻抗的测量电路。可实现处理器或处理单元以确定目标组织的接触状态,该接触状态至少部分地基于由测量电路所测量的阻抗的电抗。在另一个实施方案中,接触状态可基于阻抗的相位角。
技术实现要素:
新型心脏导管包括温度感测元件,该温度感测元件提供有关导管末端的温度分布和导管组织接合的相对取向的信息。该信息使得能够对消融灶的尺寸进行估计。发明人已发现,在递送消融能量之前,可利用与目标消融位点的策略性施加的冷却冲洗结合的此类温度信息来确定导管组织接合为稳定的或不稳定的。
使用消融能量(例如,射频能量)消融心脏组织的已知的困难在于控制组织的局部加热。在期望形成足够大的消融灶以有效地消融异常组织病灶或阻断异常传导模式与过度局部加热的不期望效应之间存在权衡。如果射频装置形成太小的消融灶,则医疗手术可能不太有效,或者可能需要太多的时间。另一方面,如果过度加热组织,则可存在由于过热而引起的局部炭化效应、凝固物、和或爆炸性蒸汽爆裂。此类过热区域可形成高阻抗,并且可形成热量通道的功能性屏障。使用较慢的加热可更好地控制消融,但会不当地延长手术。通常,冲洗在消融过程之前。冲洗降低接合处的温度,因为冲洗流体比血液和组织更冷。
在导管相对于组织稳定时和不稳定时,瞬态温度模式及其稳态有所不同,其中当导管稳定时,仅有限的区域被冷却,而不稳定的导管接合由冲洗流体的相对较分散的分布来表征。本文更详细描述的温度现象为可观察到的,前提条件是冲洗流体比血液/组织温度更冷。在这种约束条件下,冲洗流体的温度及其流量主要影响差分信号的量值及其信噪比。
根据本发明的实施方案,提供了一种方法,该方法为通过以下步骤来进行:将其远侧部分上的具有温度传感器的探头引入到受检者的流体填充的体腔中,并且传送冲洗流体流过探头,其中冲洗流体在其远侧部分处离开探头,并且其中冲洗流体的温度不同于体腔的温度。当传送冲洗流体时,该方法还通过以下步骤来进行:记录温度传感器的温度读数,根据温度读数作出探头与体腔的内壁之间的预先确定的接触标准得以满足的确定,并且随后警告操作者该接触标准得以满足。
根据该方法的另一方面,以不同流量多次执行传送冲洗流体。
所述方法的另一方面包括根据相应流量下的温度读数来导出血液温度和冲洗流体温度。
根据所述方法的一个方面,该接触标准包括探头与体腔的内壁之间的稳定接触的标准。
根据该方法的另一方面,该接触标准包括探头与体腔的内壁之间的不稳定接触的标准。
根据该方法的另一方面,该接触标准包括探头与体腔的内壁之间的不接触的标准。
根据所述方法的一个方面,该探头具有多个温度传感器,并且记录温度读数是利用温度传感器同时执行的。
该方法的另一方面包括使温度传感器与流过探头的冲洗流体热绝缘。
根据该方法的另一方面,该温度传感器被设置在探头的外表面上。
根据该方法的另一方面,该温度传感器被设置在探头内部。
根据该方法的另一方面,探头上的消融电极在记录温度读数时被激活。
在该方法的另一方面,记录温度读数包括记录第一温度读数,并且随后记录第二温度读数。接触标准在第二温度读数低于第一温度读数时得以满足,该方法包括记录探头与内壁之间的接触。
根据该方法的另一方面,第二温度读数比第一温度读数低至少1℃。
根据该方法的另一方面,第二温度读数比第一温度读数低至少4℃。
根据该方法的另一方面,第二温度读数还包括0.3秒至5秒之间的持续时间的1℃至4℃之间的瞬态升高,该方法包括记录探头和内壁之间的间断接触。
该方法的另一方面包括对温度读数滤波,以去除心率变化和呼吸波动的影响。
根据本发明的实施方案,还提供了一种设备,该设备包括适于插入到受检者的流体填充的体腔中的探头,该探头包括位于该探头的远侧部分上的温度传感器。该设备包括用于传送冲洗流体流过探头的泵,其中该冲洗流体在远侧部分处离开探头,并且其中该冲洗流体的温度不同于体腔的温度;以及处理器,该处理器操作用于当泵正在传送冲洗流体时,记录温度传感器的温度读数,根据温度读数作出探头与体腔的内壁之间的预先确定的接触标准得以满足的确定,并且随后向操作者警告接触标准得以满足。
消融电极被设置在探头的远侧部分上,该消融电极可在记录温度读数时被激活。
附图说明
为了更好地理解本发明,以举例的方式引用本发明的详细说明,本发明的详细说明应结合以下附图来阅读,附图中相同的元件被赋予相同的参考编号,并且其中:
图1为根据本发明的实施方案的用于执行诊断和治疗手术的系统的图解说明图;
图2为根据本发明的实施方案的沿着心脏导管远侧段的长度的剖面图;
图3为根据本发明的另选实施方案的心脏导管的远侧段的一部分的详细视图;
图4为根据本发明的实施方案的用于导管的插件的等轴视图;
图5为根据本发明的实施方案的确定导管-组织接合稳定性的方法的流程图;
图6为示出根据本发明的实施方案的校准过程的图示;
图7为根据本发明的实施方案的指示执行图5的过程时的典型温度描记线的图示;
图8为根据本发明的实施方案的显示示例性数据的图示;
图9为根据本发明的实施方案的示出随冲洗流体的流速而变化的平均温度测量的曲线图;
图10为根据本发明的实施方案的示出随冲洗流体的流速而变化的平均温度测量的曲线图;
图11为根据本发明的实施方案的对图9和图10所示的曲线图进行比较的复合显示图;
图12为根据本发明的实施方案的示出从图11中的数据获取的导管和组织在接触和不接触期间的温度之间的差值的曲线图;并且
图13为根据本发明的另选实施方案的确定导管和组织之间的接触的方法的流程图。
具体实施方式
为了全面理解本发明的各种原理,在以下说明中阐述了许多具体细节。然而,对于本领域的技术人员将显而易见的是,并非所有这些细节都是实施本发明所必需的。在此示例中,未详细示出熟知的电路、控制逻辑、以及用于常规算法和过程的计算机程序指令的细节,以免不必要地模糊一般概念。
本发明的多个方面可被体现为软件编程代码,该软件编程代码通常被保持在永久性存储装置诸如计算机可读介质中。在客户端/服务器环境中,此类软件编程代码可被存储在客户端或服务器上。软件编程代码可被实施在与数据处理系统一起使用的多种已知非临时性介质诸如磁盘、硬盘驱动器、电子介质或cd-rom中的任一者上。代码可被分布于此类介质上,或者可通过某些类型的网络从一个计算机系统的存储器或存储装置向其他计算机系统上的存储装置分发给使用者,以供此类其他系统的使用者使用。
系统综述
现在转到附图,首先参见图1,其为用于在活体受检者心脏12上评估电活动并且执行消融手术的系统10的图解说明图,该系统10是根据本发明的公开实施方案构造和操作的。该系统包括导管14,该导管14由操作者16经由皮肤穿过患者的血管系统插入心脏12的腔室或血管结构中。通常为医师操作者16使导管的远侧末端18例如在消融目标部位处与心壁接触。可根据公开于美国专利no.6,226,542和no.6,301,496中和公开于共同转让的美国专利no.6,892,091中的方法来制备电活动标测图,这些专利的公开内容以引用方式并入本文。一种体现系统10的元件的商品可以商品名
可通过施加热能对例如通过评价所述电活动图而被确定为异常的区域进行消融,例如通过将射频电流通过导管中的金属线传导到远侧末端18处的一个或多个电极,这些电极将射频能量施加到心肌。能量在组织中被吸收,从而将组织加热到组织永久性地失去其电兴奋性的点(通常为约50℃)。此手术成功后,在心脏组织中形成非传导性消融灶,这些消融灶可中断导致心律失常的异常电通路。本发明的原理可应用于不同的心脏腔室,以诊断并治疗多种不同的心律失常。
导管14通常包括柄部20,该柄部20上具有合适的控制器以使得操作者16能够按消融过程所需对导管的远侧端部进行操纵、定位和定向。为了协助操作者16,导管14的远侧部分包含向位于控制台24中的处理器22提供信号的位置传感器(未示出)。处理器22可履行如下所述的若干个处理功能。
可使消融能量和电信号经由电缆34穿过位于远侧末端18处或附近的一个或多个消融电极32在心脏12和控制台24之间来回传送。可通过电缆34和电极32将起搏信号和其他控制器信号从控制台24传送到心脏12。另外连接到控制台24的感测电极33被设置在消融电极32之间并且已连接到电缆34。
线连接件35将控制台24与体表电极30和用于测量导管14的位置和取向坐标的定位子系统的其他部件进行链接。处理器22或另一个处理器(未示出)可为定位子系统的元件。如授予govari等人的美国专利no.7,536,218中所教导的那样,电极32和体表电极30可用于在消融位点处测量组织阻抗,该专利以引用方式并入本文。通常为热电偶或热敏电阻器的温度传感器(未示出)可被安装在电极32中的每个电极上或附近。传感器的位置可为变化的。例如,传感器可位于导管14的外部或内部。在任何情况下,传感器使用任何常规绝缘材料来与流过导管的冲洗流体热绝缘。
控制台24通常包括一个或多个消融功率发生器25。导管14可适于使用任何已知的消融技术来将消融能量(如,射频能量、超声能量和激光产生的光能)传导到心脏。共同转让的美国专利no.6,814,733、no.6,997,924和no.7,156,816中公开了此类方法,这些专利以引用方式并入本文。
在一个实施方案中,定位子系统包括磁定位跟踪构造,该磁定位跟踪构造使用用于生成磁场的线圈28通过以预先确定的工作容积生成磁场并感测导管处的这些磁场来确定导管14的位置和取向。定位子系统在以引用方式并入本文的美国专利no.7,756,576以及上述美国专利no.7,536,218中有所描述。
如上所述,导管14联接到控制台24,这使得操作者16能够观察并调节导管14的功能。控制台24包括处理器,优选为具有适当信号处理电路的计算机。处理器被联接以驱动监视器29。信号处理电路通常接收、放大、滤波并数字化来自导管14的信号,该信号包括由传感器诸如电传感器、温度传感器和接触力传感器和位于导管14远侧的多个位置感测电极(未示出)生成的信号。控制台24和定位系统接收并使用数字化信号,以计算导管14的位置和取向并分析来自电极的电信号。
为了生成电解剖标测图,处理器22通常包括电解剖标测图发生器、图像配准程序、图像或数据分析程序和被构造成能够在监视器29上呈现图形信息的图形用户界面。
通常,系统10包括为了简洁起见未在图中示出的其他元件。例如,系统10可包括心电图(ecg)监视器,该心电图(ecg)监视器被联接以接收来自一个或多个体表电极的信号,以便为控制台24提供ecg同步信号。如上所述,系统10通常还包括基准定位传感器,该基准定位传感器位于附接到受检者身体外部的外部施加基准贴片上,或者位于被插入到心脏12中并相对于心脏12被保持在固定位置的内置导管上。提供用于使液体循环穿过导管14以冷却消融位点的常规泵和管路。系统10可接收来自外部成像模态诸如mri单元等的图像数据并且包括图像处理器,该图像处理器可被结合在处理器22中或由处理器22调用以用于生成并显示图像。
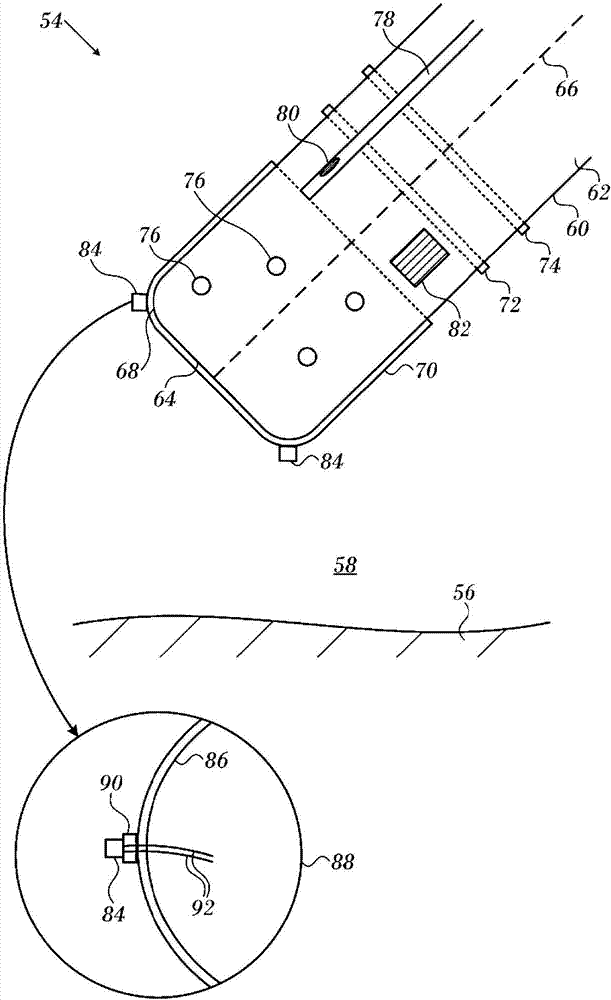
现在参见图2,其为根据本发明的实施方案的沿心脏导管的远侧段54的长度的剖视图。远侧段54邻近组织56,并且被假定被浸没在流体58中,使得组织56的表面29接触流体。流体58通常包括血液和盐水溶液的混合物。以举例的方式,本文假定远端段54由绝缘基材60形成,该绝缘基材60具有圆柱体62的形状,并且一端被基本上平坦的表面64封闭。圆柱体62具有对称轴线66。如图2所示,弯曲段68连接平坦表面64和圆柱体62。圆柱体62的典型直径为2.5mm,并且弯曲段68的典型半径为0.5mm。
远侧段54包括三个电极70,72,74,这些电极彼此绝缘。电极70,72,74通常包括被成形于绝缘基材60上方的薄金属层。典型地,远侧末端具有与电极70,72,74绝缘的其他电极,为简单起见未在图中示出。末端电极70具有平底杯形形状,因此在本文中也被称为杯形电极。杯形电极70通常具有约0.1mm至约0.230mm范围内的厚度。第二电极70和第三电极72通常呈环形形式,并且也称为环形电极。
电极70,72,74通过线(未示出)连接到控制台24(图1)中的控制器。电极中的至少一个电极用于消融组织56。典型地,在消融过程中,在消融电极和周围区域中产生热量。为了散热,在杯形电极中具有小冲洗孔76。孔76通常具有约0.1mm-0.2mm范围内的直径。冲洗管78向孔76供应盐水溶液,并且盐水溶液流过孔76(使流体58成为血液和盐水溶液的混合物)的流量受到控制台24中的冲洗模块(未示出)的控制(图1)。盐水的流量通常在约2cc/min–20cc/min的范围内,但可高于或低于此范围。
盐水温度传感器80(通常为热电偶)位于管78内,并向控制台24(图1)模块56中的电路提供信号,以使得控制台24能够测量进入孔76的盐水溶液的温度ts。尽管盐水溶液可以环境室温(例如,在约19-25℃的范围内)来提供,但该溶液可在其流过该导管期间被略微加热,使得最终冲洗温度可为略高的。
典型地,一个或多个位置感测装置82可被结合在远侧末端中。装置82被构造成能够向处理器22(图1)提供信号,使得该系统能够确定远侧段54的位置和/或取向。
在一个实施方案中,远端段54包括一个或多个大致相似的温度传感器84(以举例的方式,图中示出了两个),它们通过绝缘体牢固连接在杯形电极70的外表面上,以便从表面伸出。传感器84具有约0.3mm的典型直径和约1.5mm的长度。在一个实施方案中,传感器84为由generalelectriccompany(schenectady,newyork)生产的热敏电阻器ntc型ab6。在另选的实施方案中,传感器84包括由semitecusacorporation(torrance,15california)生产的“f”型热敏电阻器。以举例的方式,以下描述假定存在相对于轴51对称分布并位于杯形电极的弯曲段86上的三个传感器84。杯形电极的弯曲段86覆盖远侧末端的弯曲段68。弯曲段86为部分圆环面形状,通常为具有大约0.5mm的管半径的部分圆环面。
图2的放大部分88更详细地示出了传感器84中的一个传感器。如放大部分88中所示,绝缘体90将传感器84与杯形电极70的弯曲段86隔开。绝缘体90被选择以提供良好的绝热和电绝缘性能,并且在一些实施方案中,绝缘体90可包括将传感器84粘合到弯曲段86的粘合剂。线9290将传感器84连接到控制台24(图1)。
通过使传感器84从杯形电极70的外表面伸出,传感器84能够紧密接触组织56。处理器22(图1)因此能够使用来自传感器84的信号,以提供组织56的直接温度测量。在一个实施方案在,传感器84从电极70的外表面伸出不超过0.7mm,并且通常伸出约0.5mm。
现在参见图3,其为根据本发明的另选实施方案的心脏导管的远侧段的一部分的详细视图。在该实施方案中,传感器并未伸出顶盖电极的外表面或探头的外表面。在图3的代表性示例中,传感器94与外表面96齐平并且通过绝缘材料100与流过内腔98的流体绝缘。该实施方案的优点为降低了在传感器94的表面上形成血栓的可能性。
现在参见图4,其为根据本发明的实施方案的用于导管的插件102的等轴视图。插件102适于由类似于电极70(图2)的导管中的顶盖电极封盖,为清楚起见,省略顶盖电极。
如图可见,突起104包括被构造成能够接合消融电极的内表面的环形肩部106。肩部106可具有与顶盖电极的内表面适当互补的表面。肩部106的宽度可由基部部分108的直径和内部部分110的直径之间的差值限定。内部部分110的直径的尺寸设定成与传感器孔(未示出)配合。突起104被构造成能够从顶盖电极的外表面向外延伸或者与顶盖电极的外表面齐平。相似地,环形肩部106从插件102的表面径向向外延伸,使得基部部分108的深度建立顶盖电极的内表面与插件102的主体上的表面112之间的最小间距。
在该实施方案中,插件102包括三个纵向延伸的臂114,每个臂具有中空内部部分以允许引线和线材穿行到传感器116。臂114在远侧冠部部分118处连接在一起。通道120可形成于臂114之间以及由冠部部分118中的中心开口形成。根据所提供的传感器的预期用途和数量,插件102的构型可例如根据需要诸如通过具有两个或四个臂的特征进行调整。在一个方面,臂114可包括至少两个突起104以容纳至少两个传感器,诸如一个近侧传感器和一个远侧传感器。
传感器116可为温度传感器(例如,热敏电阻器、热电偶、荧光探头等等)或电传感器(例如微电极)的任何组合。任何温度传感器结点位于突起104的端部处或附近并且可利用导热粘合剂进行灌封。与传感器116相关联的任何线材或引线可被适当地引导穿过臂114。应当理解,这种构型使传感器116与顶盖电极和冲洗流体隔离。在一个方面,插件102用于使传感器116热绝缘。因此,通过降低来自顶盖电极或循环冲洗流体的偏差可获得组织温度和环境温度的更的准确的测量。在另一方面,插件102也可用于使传感器116电绝缘,以实现更准确的测量。相似地,任何线材和/或引线也是绝热和电绝缘的,并且被密封起来以免受到冲洗流体的腐蚀。在一个方面,通过突起104定位的传感器116中的每个传感器可被构造成能够感测多个测量。例如,一个或多个传感器116可用作微热敏电阻器和微电极。根据一个实施方案,热敏电阻器线以及电极引线可连接到传感器116中的每个传感器的壳体顶盖电极。诸如通过在放置传感器116之后采用合适的非导电和非热绝缘材料填充臂114的内部,每根线可通过任何合适的技术彼此隔离。
插件102通过部分118被固定在顶盖电极内,该部分118包括圆盘状基座122和远侧突出键124。基座122可具有与顶盖电极的内径对应的直径并且可以任何合适的方式进行固定诸如通过焊接126。键124被构造成能够适配在由臂114的近侧部分形成的插件102的凹槽128内,以稳定插件102以抵制传感器116的轴向旋转和可能的移位。当从延伸穿过导管主体的内腔引导与顶盖电极、传感器116相关联的导线和线材、以及冲洗流体时,部分118可与顶盖电极提供不透流体的密封。例如,中心管道130可与导管的内腔连通以将冲洗流体引导到通道120,以用于顶盖电极的内部内的循环以及通过孔诸如孔76(图2)的最终流出。
参考图2和图4所述的类型的导管更详细地描述于以下专利中:govari等人的共同转让的美国专利申请no.2014/0171821、bar-tal等人的共同转让的美国专利申请no.2011/0224664、以及名称为irrigatedablationcatheterwithmultiplesensors的共同未决的美国专利申请no.14/551,229,这些专利申请以引用方式并入本文。
操作
现在参见图5,其为根据本发明的实施方案的确定导管-组织接合稳定性的方法的流程图。在本文的附图中,为了呈现清楚起见,以具体的线性顺序示出了过程步骤。然而,将显而易见的是,这些步骤中的多个步骤可并行地、异步地、以具有反馈回路的形式或以不同的顺序执行。本领域的技术人员还应当理解,另选地,过程可例如在状态图示中被表示为多个相互联系的状态或事件。此外,可能并非全部所示出的过程步骤需要用来实施该过程。
在下文的讨论中,冲洗流体的温度低于血液的温度。典型室温(25℃)下的冲洗流体为合适的。然而,加以必要的变更,本发明的原理适用于冲洗流体比血液热的情况。
在初始步骤132处,使用熟知的方法来将心脏导管引入到受检者的心脏中。在这一阶段,导管仍游离于心腔中并且不与心脏的壁接触。现在可执行任选的校准。校准的目标为建立用于区分以下两种状态的温度阈值:a)导管处于血池中;和b)导管与组织接触(中等或不接触)。知道血液温度、冲洗流体温度为必要的。可假定或测量这些温度。知道冲洗流体的流量也为必要的。
现在参见图6,其为根据本发明的实施方案的示出任选校准过程的图示。血液和冲洗流体基线温度分别由虚线134,136表示。在下文相对于图5所述的过程期间测量的温度发生在位于基线温度之间的操作区域138中。可在导管的引入期间并且在启动冲洗之前使用导管末端中的传感器来确定血液温度(线134)。流体温度的测量可在冲洗管线上执行或者可通过将冲洗流体以已知的流量提供到导管并且测量观察的温度来导出。可使用以下两个过程中的任一个过程来确定冲洗流体温度(线134)。两个过程均建立表示冲洗流体的温度的基线。
返回到图5,在框140所示的第一校准选项中,在导管的引入之后,在步骤142处启动冲洗。然后,在步骤144处,可直接从患者体外的冲洗流体管线中的传感器获得基线温度读数。这些读数不受血液温度的影响。
除此之外或作为另外一种选择,在步骤142中,冲洗流体基线读数可同时利用导管末端中的多个温度传感器来获取并且应持续预先确定的时间间隔例如2秒-5秒,以便建立可靠的变化模式。预先确定的时间间隔并非关键性的,并且可针对具体应用进行改变。在该时间过去之后,可期望利用冲洗流体来冲刷导管。这种替代方案提供了用于以下状态的基线,其中导管游离于心腔中并且正以典型的速率进行冲洗。所获得的值通常与第一替代方案不同,因为存在环境血液温度的一些影响。
在框146所示的第二选项中,通过在步骤148处通常利用盐水以2毫升/秒至20毫升/秒的不同流量冲刷导管并且在步骤150处在每次冲刷期间读取一个或多个温度传感器来设定冲洗流体基线温度。冲刷的每次流动可利用下述方程来表达,该方程依赖于两个已知量(给定的流量和导管构造/设计)和两个未知量(血液和流体温度)。通过提供若干次流动,可通过求解一系列此类方程来获得血液和流体温度。导管设计的几何结构和其他方面为重要的,因为它们影响参数。方程的参数因此为经验性的和导管特异性的。显著的导管设计问题包括传感器位置(如何感测流速)和冲洗孔的设计。这些方程的解同时提供有关流体和血液温度的数据。预校准过程可用于这些方程。
在冲刷期间,温度从环境水平快速下降到阈值(线134;图6),该阈值接近用于冲刷的流体的温度。除此之外或作为另外一种选择,一个或多个附加传感器(未示出)可沿导管进行定位,以便在盐水进入导管时监测盐水温度并且测量血液的温度。使用由附加传感器提供的信息并且求解上述方程,可以在确定组织与导管接触之前估计血液池中的温度传感器152的预期温度读数。
在框140,146中所述的过程中的任一个过程中,一旦冲洗开始,来自导管末端的温度读数便从血液温度基线(线136;图6)下降。例如,一旦观察到低于预先确定的阈值的温度读数例如,32℃,便可断定冲洗已开始。在完成步骤144或步骤150之后,控制程序前进到步骤154。
在一些实施方案中,框140,146的程序被省略,因为下文例如在图8的讨论中描述的转变可在不参考基线或阈值读数的情况下来实现。可例如基于经验或已知信息来假定基线值。如果患者发热或者体温过低,则基线值将从其他模态得知。在这种情况下,控制程序从初始步骤132直接前进到步骤154,如由线156所示。
接下来,在步骤154处,在组织与消融电极之间建立接触,该消融电极在导管到达新位置时通常位于远侧末端处。这可通过任何已知的方法完成,例如上述方法以及名称为“contactassessmentbasedonphasemeasurement”的美国专利申请no.20130172875和名称为“machinelearningindeterminingcatheterelectrodecontact”的美国专利申请no.20140051959中教导的方法,这两份专利申请均与本发明共同转让并且以引用方式并入本文。冲洗在步骤158处开始。当已建立接触时,温度读数位于血液基线与冲洗流体基线中间(参见图8;时间160)。
接下里,在步骤162处,当继续冲洗时,获得温度读数的记录。在步骤162中考虑温度记录的统计值(例如,平均温度、方差)和结构。如果导管组织接合不稳定,则读数将为不稳定的、甚至突发性的(当与特定位置的接触形成并且丧失、或者当接触点在组织上移动时)。在前一情况下,导管末端暴露于周围血液。在后一情况下,导管接触未冷却的组织。在任一种情况下,当接触以不稳定的方式丧失并且重新建立时,温度将上升或下降。通常,当接触为间断的或不稳定时,可在0.3秒至5秒之间的持续时间内观察到1℃至4℃之间的瞬态升高。此类波动可归因于呼吸(通常5秒/周期)、心跳(0.3秒/周期-1秒/周期)和0.3秒/周期至5秒/周期范围内的泵脉动。
接下来,在确定步骤164处,确定基于步骤162的分析的稳定接触标准是否得到满足。标准可根据冲洗流量以及冲洗流体和血液的温度来经验性地逐一确定。如果确定步骤164处的确定为肯定的,则控制程序前进到步骤166。报告稳定的导管组织接合,并且消融可开始。
如果确定步骤164处的确定为否定的,则在确定步骤168处确定是否获得不稳定或突发性温度读数。如果确定步骤168处的确定为肯定的,则控制程序前进到步骤170。报告不稳定的电极组织接合。
如果确定步骤168处的确定为否定的,则控制器前进到最终步骤172。断定导管末端游离于血池中。
在执行最终步骤166,170,172中的一个最终步骤之后,电极被分类为稳定接触、间断接触或不接触。每个电极的分类可仅仅依赖于传感器数据或得自若干个传感器的特性。当存在多个消融电极时,可针对每个电极执行步骤142之后的序列并且针对它们中的每一者来报告相应的接触状态。
现在参见图7,其为指示当根据本发明的实施方案执行图5的过程时并且当导管定位在心脏中时预期的典型温度描记线的图示。在时间间隔174期间,当导管的末端游离于血池中并且不接触组织时,三个温度传感器记录到相对较高的温度并且存在极小的波动。如上所述,温度传感器的实际数量可在不同实施方案中有所变化。在时间间隔176期间,存在与组织的间断接触。相比于时间间隔174,温度较低并且存在较高程度的波动。观察到高频波动,因为导管在接触状态与不接触状态之间交替。这些交替为导管靠近组织的指示。重要的是,这证明存在与组织的不牢固接触。在这种情况下,可向操作者产生警告。这种情况下中的波动与心脏壁的机械运动相关联,因为当心脏搏动时心脏壁抵靠导管而运动。在时间间隔178期间,导管与组织强力接触。在时间间隔174,176,178中,该温度为最低的并且波动为中间的。据信,该温度是最低的,因为从导管流动的冲洗流体正冷却组织并且分离的传感器测量组织温度。在导管相对于组织稳定时和不稳定时,瞬态温度模式及其稳态有所不同,其中当导管稳定时,仅有限的区域被冷却,而不稳定的导管接合由冲洗流体的相对较分散的分布来表征。当导管组织接合稳定时和当其不稳定时,在目标位点处观察到不同的测量温度。本文更详细描述的温度现象为可观察到的,前提条件是冲洗流体比血液/组织温度更冷。在这种约束条件下,冲洗流体的温度及其流量主要影响差分信号的量值及其信噪比。
第一另选实施方案
在该实施方案中,从温度传感器获得的信号可使用系统10(图1)的信号处理电路进行滤波,例如通过对信号求平均、或者将熟知的滤波器应用到泵脉动频率、心率变化和呼吸波动(这些情况将模糊其他显著的温度波动)。在第一实施方案中,高频波动有意不进行滤波,因为它们的存在为与组织的间断接触的优异指示。然而,在间断接触的持续时间期间,滤波操作模式为有利的,如下述实施例所示。
实施例1
此仿真实施例示出了沿着组织拖动电极的效果。其包括得自测试系统的数据,在测试系统中,心脏腔室中的血液由水填充的玻璃缸(温度34℃)来仿真。通过导管(例如,图1、图2所示的具有远侧温度传感器的导管)泵送24℃温度的水以仿真消融位点冲洗。通过使操作者的手接触导管的远侧部分来仿真组织接触。
现在参见图8,其为根据本发明的实施方案的显示得自此实施例的数据的图示。从导管上的三个温度传感器记录数据。相对于时间来绘制温度。在时间180之前,导管的末端游离于玻璃缸中,并且传感器记录到34℃并且具有极小变化的温度。在时间180处启动冲洗。温度快速地下降到25℃-30℃的范围内,并且与时间180之前相比具有略微较高的变化。在此实施例中,心率和呼吸影响被不可避免地省略。
在时间160处,建立导管与组织的接触。因此,温度急剧下降约4℃至约26℃,并且其后较缓慢地下降,由此在略高于24℃处达到平衡。
在时间182处,通过沿着手滑动导管来仿真不稳定的导管组织接合。这导致瞬态升高,即持续时间小于约2秒的约4℃的温度尖峰,因为导管接触未冷却的组织。温度随后逐渐地下降并且接近冲洗流体的温度。在时间184,186处重复这种操作。时间182,184,186处的尖峰反映出导管末端从一个位置处的相对稳定方位的移位。当末端通过滑动到另一位置而重新定位时,存在末端不再与组织稳定接触的持续时间。在该持续时间期间,温度瞬态上升。然后,当达到新的相对较稳定位置时,温度按照在时间182,184,186观察到的尖峰模式急剧下降。应当指出的是,如果不对传感器信号进行滤波,则时间182,184,186的尖峰将被由上述伪影引起的波动(例如,发生在时间间隔176期间的波动;图7)模糊。
然后,将导管保持在适当的位置,直至时间188。温度保持平衡在冲洗流体的温度附近,并且满足可通过已知方法建立的预先确定的稳定性标准,例如,偏移在给定时间间隔内小于阈值。然后在时间188处,从组织突然移除导管。这种操作与中等温升和波动的描记线模式相关联。
不受理论的约束,下述讨论被提供为所观察到的效果的可能解释,以便有利于本发明的理解。当导管处于血池中时,其暴露于温暖的循环血液(来自心脏工作或者来自循环冲洗流体和血液的组合),该循环血液将导管保持在相对较高的温度(通常约34°-35°)。由传感器读取的低温指示正被导管冷却的组织,此时导管靠近心内膜表面。冷却发生在相对较小的局部禁闭空间中。因此,当导管在组织上滑动时,其暴露于血池的较高温度和/或未被流体冷却的组织;因此在时间182出现尖峰。当导管在接触与血池之间交替时,其显示出时间间隔176的尖峰模式(图7)。
实施例2
该实施例示出了接触、不接触与流量之间的关系。使用具有图f4所示的构造并且具有六个热电偶传感器和接触力传感器的开口冲洗导管对猪进行插管和麻醉、以及导管插入。测试的状态为接触和不接触,即导管的末端游离于血池中。通过得自接触力传感器的读数并且通过carto标测来确认接触状态。在接触状态和不接触状态下,测量三个不同的冲洗流速(2毫升/秒、10毫升/秒、25毫升/秒)。
现在参见图9,其为根据本发明的实施方案的曲线图,该曲线图示出了当在导管末端与组织之间不存在接触时得自6个传感器的随室温下的冲洗流体的流速而变化的平均温度测量。显而易见的是,测量的温度随着流量的增加而下降。描记线190,192和193分别对应于2毫升/秒、10毫升/秒和25毫升/秒的流量。在2毫升/秒速率下,测量的温度并不显著不同于血液温度。在25毫升/秒下观察到较显著的下降,并且在10毫升/秒下具有中等下降。
现在参见图10,其为根据本发明的实施方案的曲线图,该曲线图示出了当在导管末端与组织之间存在接触时得自6个传感器的随室温下的冲洗流体的流速而变化的平均温度测量。使用与图9中相同的条件。描记线194,196,198分别对应于2毫升/秒、10毫升/秒和25毫升/秒的流量。当接触力传感器读取到超过15克的力时,接触得到确认。如同图9,观察到随流量增加的温度下降进程。
现在参见图11,其为根据本发明的实施方案的比较图9和图10所示的曲线图的复合显示图。在极低的流量下,流量变化具有最小的影响。描记线190,192几乎相同。在中等流量下,观察到剩余的组织冷却证据。因此,在接触和不接触状态下,温度为几乎相同的。然而,流速越高,温度影响越大(即,描记线198,193(25毫升/秒)之间的差值大于描记线196,192之间的差值)。
现在参见图12,其为根据本发明的实施方案的示出从图11中的数据获取的导管和组织在接触和不接触期间的温度之间的差值的曲线图。示出了非线性关系。实际关系可根据所涉及的导管和组织的特性而变化;然而,温度差值与流量之间的大体非线性增加可被预期到存在于大多数(即使并非全部)情况中。
第二另选实施方案
现在参见图13,其为根据本发明的另选实施方案的确定导管与组织之间的接触的方法的流程图。该方法应参考实施例2和图12来理解。
该过程开始于初始步骤200。将导管引入腔室内且与组织形成不接触关系。如上所述在零流量下确定血液温度。在该方法中的此步骤和后续步骤中,使用上文在图6的讨论中描述的过程中的一个过程来获取温度测量。
接下来,在步骤202处,当导管与组织保持不接触关系时,以第一流量传送冲洗流体。这可为如上所述的10毫升/秒,但可替换成其他速率。
接下来,在步骤204处,当导管与组织保持不接触关系时,以第二流量传送冲洗流体。这可为如上所述的25毫升/秒,但可替换成其他速率。
接下来,在步骤206处,使导管与目标组织(通常为心腔的壁)形成假定接触。
接下来,在步骤208处,当导管与组织保持假定接触时,以第一流量传送冲洗流体,如同步骤202。
接下来,在步骤210处,当导管与组织保持假定接触时,以第二流量传送冲洗流体,如同步骤204。
接下来,在步骤212处,针对第一流量和第二流量计算不接触和假定接触期间的测量的相应温度差值。
接下来,在确定步骤214处,确定在步骤212中计算的差值是否显著。这可通过利用名称为machinelearningindeterminingcatheterelectrodecontact的共同转让的专利申请序列no.13/589,347的教导内容(加以必要的变更)优化图12所示类型的曲线的品质因数来完成,该专利申请以引用的方式并入本文。用于此类优化的其他技术在本领域中为熟知的。另选地,对于在步骤212中计算的差值中的一个或两个差值而言,当差值超过阈值时,假定接触便可被确认。用于阈值的实际值依赖于应用,如上所述。此外另选地,可将温度差值的其他特征用作确定标准,例如,图12的曲线图中的δ(温度)/δ(流速)的最大值。
如果确定步骤214处的确定为肯定的,则控制程序前进到步骤216。报告导管与组织之间的假定接触的确认。
如果确定步骤214处的确定为否定的,则控制器前进到最终步骤218。导管与组织之间的假定接触不能被确认。推测导管末端仍游离于腔室中。
当确定接触的常规技术失效或不可用时,例如当在手术期间发生接触力传感器中的故障或者标测处理器或电路中的失灵时,这种确定接触的方法为尤其可用的。此外,实施例2和图13中所述的方法可用于预测图8中的温度阈值。
本领域的技术人员应当理解,本发明并不限于上文中特别示出和描述的内容。相反,本发明的范围包括上文所述各种特征的组合与子组合两者,以及不在现有技术范围内的其变型和修改,所属领域的技术人员在阅读上述说明时应当想到这些变型和修改。
- 还没有人留言评论。精彩留言会获得点赞!