高致病性猪葡萄球菌分泌蛋白在作为亚单位疫苗中的应用的制作方法
本发明涉及生物医学技术领域,具体是涉及高致病性猪葡萄球菌分泌蛋白在作为亚单位疫苗中的应用。
背景技术:
猪渗出性表皮炎是哺乳仔猪或早期断乳仔猪因感染猪葡萄球菌而引起的一种急性致死性浅表脓皮炎,以全身油脂样渗出性皮炎为特征并具有高度传染性的疾病。世界上大多数国家的哺乳仔猪和断奶仔猪都有渗出性皮炎,发病率10%~90%,死亡率5%~90%。近年来猪渗出性皮炎在国内外猪场的发生率也逐渐增高,虽然国内外对猪葡萄球菌的研究己有不少,但它的毒力及其致病机理至今仍不十分明确。
本实验室于2011年从增城某猪场分离得到一株高致病性猪葡萄球菌(S.hycius,命名为ZC-4),之后对其致病性以及分子机理进行了较深入的研究。目前我们用免疫蛋白质组学的方法,筛选得到了多个具有免疫原性的猪葡萄球菌蛋白,经过筛选,发现了其分泌蛋白enolase具有较好的免疫原性。而目前对猪葡萄球菌的研究主要基于基因水平和细胞水平,在蛋白水平上的研究较少,而对于猪葡萄球菌在蛋白水平上的研究也未见相关报道。
技术实现要素:
本发明解决的技术问题是:提供一种高致病性猪葡萄球菌(S.hycius,命名为ZC-4)的分泌蛋白在作为亚单位疫苗中的应用,该分泌蛋白具有较好的免疫保护能力,能够预防猪葡萄球菌感染。
本发明的技术方案是:一种高致病性猪葡萄球菌的分泌蛋白在作为亚单位疫苗中的应用。
进一步地,所述的分泌蛋白在作为预防猪葡萄球菌感染的亚单位疫苗中的应用。
进一步地,所述分泌蛋白的氨基酸序列如SEQ ID NO:1所示。
进一步地,制备所述的高致病性猪葡萄球菌的分泌蛋白亚单位疫苗的方法,其特征在于:将猪葡萄球菌的分泌蛋白中加入佐剂、赋形剂、冻干稳定剂,搅拌均匀,即成。
更进一步地,所述的佐剂为水性佐剂或油性佐剂或其他佐剂混合使用,如本领域常见的白油佐剂、铝胶佐剂、弗氏佐剂等等。所述赋形剂选自氨基乙酸。
进一步地,所述高致病性猪葡萄球菌的分泌蛋白的制备为重组蛋白的原核表达,具体步骤如下:
1)细菌培养;
2)基因组DNA提取;
3)Enolase基因克隆:PCR扩增;
4)Enolase表达载体构建:所用原核表达载体为pET32a;
5)Enolase重组蛋白表达;
6)重组Enolase过镍柱纯化。
本发明的有益效果是:高致病性猪葡萄球菌(S.hycius,命名为ZC-4)其分泌蛋白enolase具有较好的免疫原性,保护率达到60%,免疫小鼠和仔猪后能诱导较高抗体水平。攻毒保护力实验表明该蛋白能够增强小鼠和仔猪对猪葡萄球菌的抵抗力,将其作为亚单位疫苗能够预防猪葡萄球菌感染。
附图说明
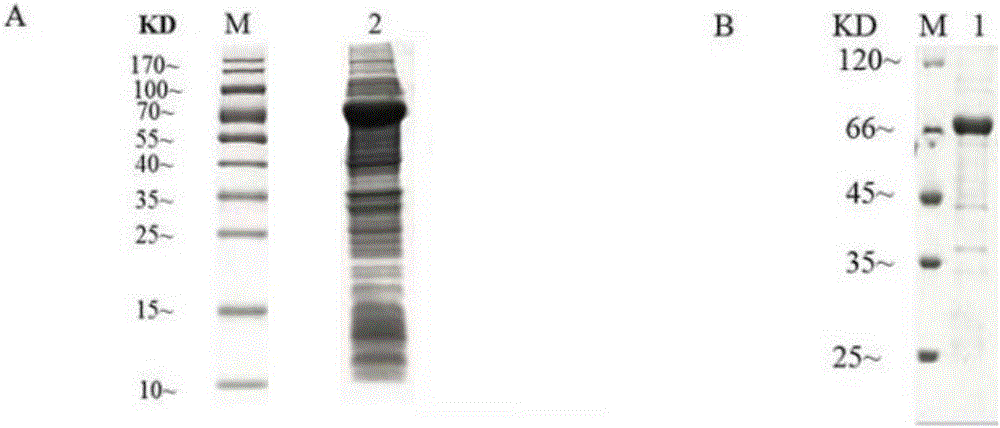
图1A为猪葡萄球菌分泌蛋白ENO的IPTG诱导表达及其免疫原性分析结果;
图1B为分离纯化后的Enolase重组蛋白ENO。
图2为用纯化的Enolase重组蛋白(ENO)处理后的BALB/c小鼠的血清细胞因子水平,其中,图2C为注射ENO第3小时的结果;图2D为注射ENO第24小时的结果。
图3A,第一次免疫后28天Enolase重组蛋白(ENO)的抗体的水平;
图3B,Enolase重组蛋白ENO免疫应答小鼠的存活率。
具体实施方式
一种高致病性猪葡萄球菌的分泌蛋白在作为预防猪葡萄球菌感染引起的猪渗出性表皮炎的亚单位疫苗中的应用。所述分泌蛋白的氨基酸序列如SEQ IDNO:1所示。
制备所述的高致病性猪葡萄球菌的分泌蛋白亚单位疫苗的方法为:将猪葡萄球菌的分泌蛋白中加入弗氏佐剂、赋形剂、冻干稳定剂,搅拌均匀,即成。
所述高致病性猪葡萄球菌的分泌蛋白的制备方法为重组蛋白的原核表达,具体步骤如下:
1)细菌培养:将冻存的猪葡萄球菌(S.hycius,命名为ZC-4)菌种划线接种于LB平板上,37℃振荡培养约12小时;
2)基因组DNA提取:将上述培养菌液按照细菌基因组提取试剂方法提取基因组DNA;
3)Enolase基因克隆:以上述DNA为模板进行PCR扩增,反应体系:10×PCR buffer缓冲液2.5-5ul,Mg2+试剂5-10ul,PCR引物5-10ul,Taq DNA聚合酶2-5ul,加纯化水补足至25ul;反应条件为:94℃3min;94℃30s、45℃30s、72℃40s,30个循环;72℃10min,得到PCR扩增产物;
4)Enolase表达载体构建:以pET32a为载体,经过酶切连接转化得到重组质粒,得到含目的基因的重组质粒;
5)Enolase重组蛋白表达:用上述重组质粒转化BL21(DE3),用IPTG诱导,表达重组蛋白;
6)重组Enolase过镍柱纯化。
实验验证
1.猪葡萄球菌的分泌蛋白的免疫原性验证:
鉴定蛋白质的免疫原性验证为了验证鉴定通过免疫蛋白质组学分析获得蛋白质的免疫原性,取猪葡萄球菌分泌蛋白(烯醇化酶)ENO进行生物功能验证。通过SDS-PAGE分析,该ENO蛋白在大肠杆菌中高度正确地表达,如图3所示。通过Western blot分析证明分泌蛋白ENO可与针对ZC-4的猪血清反应,如图3A所示。这表明这种蛋白表现出免疫原性。
使用Ni2+的琼脂糖凝胶柱对重组蛋白ENO进行进一步的分离纯化后的免疫原性,结果如图3B所示。
图1A中,泳道:M,10kDa的-170kDa的预染蛋白分子量标记;2,通过1mM IPTG诱导重组ENO;3,重组蛋白ENO的免疫印迹分析(与S.hycius感染的阳性血清反应)。
图1B中,泳道:M,10kDa的-170kDa的预染蛋白分子量标记;1,重组ENO的纯化。
2.猪葡萄球菌分泌蛋白对小鼠的免疫功能验证:
用纯化的猪葡萄球菌的分泌蛋白对小鼠进行注射,收集小鼠血液样本,并对收集的小鼠血液样本的细胞因子水平进行测定,并在第3小时和第24小时通过蛋白质芯片测定白细胞介素(IL)-6,IL-8,IL-12和INF-γ,在第3小时和第24小时这两组小鼠G-CSF和MCP-5的水平显著升高(P<0.05),IL-12p40p70显著增加(P<0.05)。
用纯化蛋白注射BALB/c小鼠,并在3小时和24小时后测定所收集血液样品的细胞因子水平。
3.ENO作为对S.hycius亚单位疫苗在小鼠体内的血免疫保护试验:
于0,7,14,21和28天从免疫小鼠和对照小鼠的尾静脉收集血液,通过ELISA测量这些时间抗体的水平。28天第一次免疫后得到的值。结果表明,治疗组的抗体水平明显高于PBS中的抗体水平,PBS组的血清是作为阴性对照,HIS治疗组和PBS组无显著差异(P<0.05)。
为了评估针ENO蛋白疫苗对S.hycius ZC-4感染的效果,用300uL 2.8×109CFU/毫升ENO对S.hycius小鼠进行免疫应答。PBS和他组小鼠在免疫12小时死亡,24小时后,两组有83.3%(5/6)和80%(4/5)的死亡率。而在ENO免疫组小鼠开始挑战后24小时后死亡,36小时后,他们有40%(2/5)的死亡率。ENO,HIS和对照组有5只小鼠,PBS组有6只小鼠,对照组不感染S.hycius ZC-4,于免疫后0,6,20,48,60,72小时观察到的生命或死亡情况。
上述结果表明,用ENO免疫小鼠后可以预防小鼠感染猪葡萄球菌S.hyciusZC-4。
以上述依据本发明的理想实施例为启示,通过上述的说明内容,相关工作人员完全可以在不偏离本项发明技术思想的范围内,进行多样的变更以及修改。本项发明的技术性范围并不局限于说明书上的内容,必须要根据权利要求范围来确定其技术性范围。
- 还没有人留言评论。精彩留言会获得点赞!