一种靶向肺癌的偶联药物cdGIGPQc‑ScFvαvβ3的制作方法
本发明属于生物医药领域,具体涉及一种靶向肺癌的偶联药物cdGIGPQc-ScFvαvβ3。
背景技术:
肺癌是世界范围内最常见、致死人数最多的恶性肿瘤之一,其发病率增长速度亦高居各恶性肿瘤之首。目前肺癌的主要治疗模式还是多学科的综合治疗,但总体效果不尽人意。分子靶向治疗已成为当今肺癌临床治疗学的重要研究课题之一。
分子靶向治疗,是指在细胞分子水平上,针对已经明确的致癌位点(该位点可以是肿瘤细胞的一个蛋白分子,也可以是一个基因片段),来设计相应的治疗药物,药物进入体内会特异地选择致癌位点相结合发生作用,使肿瘤细胞特异性死亡,而不会波及肿瘤周围的正常组织细胞。
研究证实整合素αvβ3在肺癌等病理性血管生成的过程中发挥了重要的作用,而新生血管的形成是肿瘤侵袭和转移的标志。因此以整合素αvβ3为靶点,抑制肿瘤血管生成,使肿瘤细胞无法得到所需的血液、氧和其它养分,从而促进了细胞凋亡。针对αvβ3的单克隆抗体新药已进入临床试验阶段,然而由于单克隆抗体分子较大,难以进入实体瘤内部;体内清除慢,易产生抗-抗体,副作用较大等缺点,因而研发更易透过毛细血管,能进入实体肿瘤内部的小分子肿瘤抑制剂具有重大意义。
本发明是利用单链抗体(scFvαvβ3)替代上述单克隆抗体,并将小分子肽cdGIGPQc和整合素αvβ3单链抗体ScFvαvβ3结合起来,得到靶向肺癌的偶联药物cdGIGPQc-ScFvαvβ3来解决上述问题。
技术实现要素:
本发明的目的在于提供一种靶向肺癌的偶联药物cdGIGPQc-ScFvαvβ3。
本发明所采取的技术方案是:
一种靶向肺癌的偶联药物,是小分子肽cdGIGPQc和整合素αvβ3的单链抗体ScFvαvβ3通过偶联得到,记名为cdGIGPQc-ScFvαvβ3。
优选的,小分子肽cdGIGPQc中,c表示D型半胱氨酸,d表示D型天冬氨酸,G表示L型甘氨酸,I代表L型异亮氨酸,P代表L型脯氨酸,Q代表L型谷氨酰胺。
优选的,整合素αvβ3单链抗体ScFvαvβ3的氨基酸序列如SEQ ID NO:1所示。
优选的,编码整合素αvβ3单链抗体ScFvαvβ3的核苷酸序列如SEQ ID NO:2所示。
优选的,所述肺癌为非小细胞肺癌。
偶联药物cdGIGPQc-ScFvαvβ3在制备治疗癌症药物中的应用。
优选的,所述癌症为肺癌。
优选的,所述肺癌为非小细胞肺癌。
本发明的有益效果是:
本发明利用整合素αvβ3的单链抗体(scFvαvβ3)替代单克隆抗体。本发明中整合素αvβ3的单链抗体是把单克隆抗体重链的可变区(VH)和轻链的可变区(VL)基因在DNA水平克隆出来,再用一段连接肽(GGGGS)3的基因把VH和VL的羧基端和氨基端以VH-linker-VL的形式连接起来,表达后即得到单链抗体ScFvαvβ3片段,记名为ScFvαvβ3。此外,利用小分子肽cdGIGPQc与整合素αvβ3单链抗体ScFvαvβ3进行偶联,得到靶向肺癌的偶联药物cdGIGPQc-ScFvαvβ3。
本发明所获得的偶联药物cdGIGPQc-ScFvαvβ3是小分子,容易透过毛细血管,能迅速在肺癌靶细胞集聚;cdGIGPQc和ScFvαvβ3无免疫原性,不会产生抗-抗体,不存在过敏的危险,安全性好;体内清除快,对机体无毒副作用;cdGIGPQc-ScFvαvβ3对非小细胞肺癌的靶向性强,小分子肽能与体内任何部位的非小细胞肺癌(NSCLC)细胞发生特异性的结合,疗效不受肿瘤的生长部位的限制,更适合于远处器官转移的晚期肺癌患者,而对正常细胞无影响。
本发明所获得的偶联药物cdGIGPQc-ScFvαvβ3对肺癌移植瘤的抑制率约为ScFvαvβ3和cNAQAEQc-ScFvαvβ3的1.40倍和1.56倍,也优于αvβ3单克隆抗体(mAb)。
附图说明
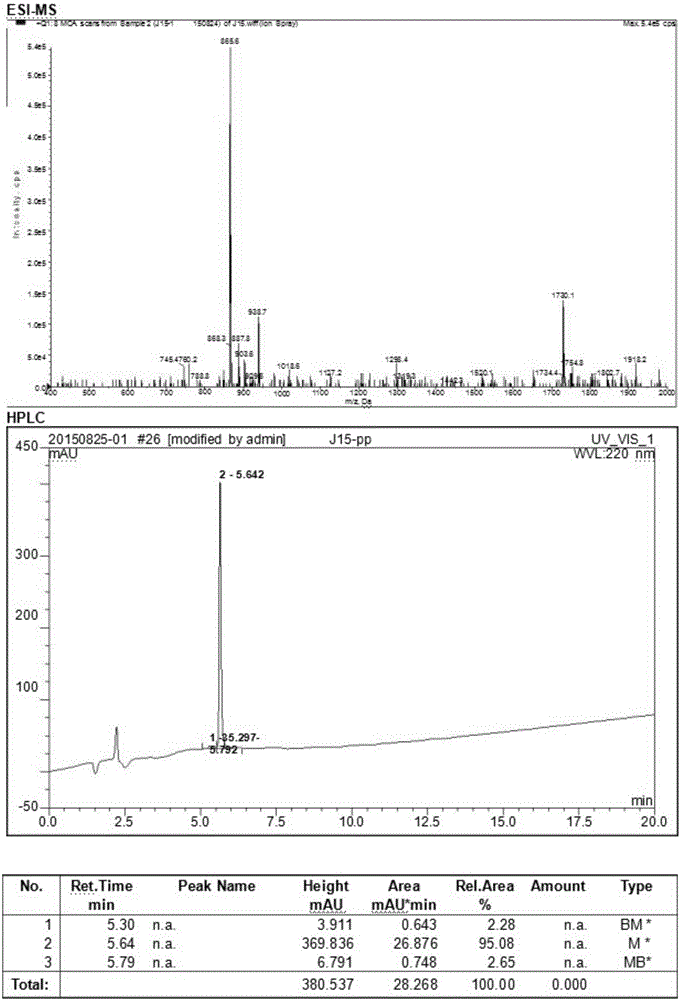
图1为小分子肽cdGIGPQc的合成及分析;
图2为小分子肽cNAQAEQc的合成及分析;
图3为ScFvαvβ3蛋白的表达与纯化;
图4为体外分析cdGIGPQc-ScFvαvβ3和cNAQAEQc-ScFvαvβ3对肺癌细胞的结合能力;
图5为cdGIGPQc-ScFvαvβ3体外的抗原结合能力及肿瘤生长抑制作用;
图6为cdGIGPQc-ScFvαvβ3的体内抗肿瘤疗效;
图7为H&E染色和免疫组化结果;
图8为A549动物移植瘤模型经治疗后重要脏器的H&E染色;
图9为L78动物移植瘤模型经治疗后重要脏器的H&E染色。
具体实施方式
本发明的技术方案是:
(1)、cdGIGPQc-ScFvαvβ3的设计和合成
发明人利用PCR方法及分子生物学基因克隆技术,构建cdGIGPQc-ScFvαvβ3,初步阐明其对肺癌细胞增殖和转移的影响。
(2)、小分子肽-ScFvαvβ3的靶向性分析
将荧光素Alexa标记小分子肽(前期工作已完成),构建Alexa-cdGIGPQc-ScFvαvβ3。建立人裸鼠肺癌动物模型,于鼠尾静脉注射Alexa-cdGIGPQc-ScFvαvβ3,利用荧光扫描仪动态观察在荷瘤小鼠各脏器中的分布,分析其特异性。
(3)、cdGIGPQc-ScFvαvβ3的生物相容性及毒性分析
①选择SD大鼠和实验犬通过异常毒性或急性毒性试验观察分子探针体内静脉给药的安全性。
②选择大鼠和实验犬通过长期毒性试验观察cdGIGPQc-ScFvαvβ3体内静脉给药的安全性。
③观察记录的内容包括皮肤、粘膜、毛色、眼睛、呼吸、循环、自主及中枢神经系统行为表现等。
④对所有实验动物的重要组织器官如心脏、肝脏、肺脏、肾脏等作常规病理组织学和电镜检查,观察分子探针对细胞有无毒性作用。
⑤分析常规血液指标如红、白细胞计数及血红蛋白等改变;血液生化自动仪测定谷丙转氨酶、谷草转氨酶等常规生化指标。
(4)、cdGIGPQc-ScFvαvβ3对体内抑瘤疗效
通过比较cdGIGPQc-ScFvαvβ3与对照组(ScFvαvβ3、cNAQAEQc-ScFvαvβ3、空白组)对肺癌细胞和人裸鼠肺癌动物模型的瘤体治疗效果,评价cdGIGPQc-ScFvαvβ3对肺癌瘤体的抑瘤疗效。
下面结合具体实验对本发明作进一步的说明,但并不局限于此。
一、cdGIGPQc-ScFv的构建与分析
采用自动多肽合成仪常规固相法(SPPS)合成肺癌特异性小分子肽cdGIGPQc(简写为cd)和非相关小分子肽cNAQAEQc(简写为cN),小分子肽由8个不同的氨基酸组成的短肽。其中,c表示D型半胱氨酸,d表示D型天冬氨酸,G表示L型甘氨酸,I代表L型异亮氨酸,P代表L型脯氨酸,Q代表L型谷氨酰胺,N代表L型天冬酰胺,A代表L型丙氨酸,E代表L型谷氨酸。
小分子肽经固相合成法(SPPS)合成后,利用电喷雾电离质谱(ESI-MS)分析其结构,并通过高效液相层析(HPLC)加以纯化。cdGIGPQc和cNAQAEQc的分子结构及纯度见图1和图2,cdGIGPQc(图1)和cNAQAEQc(图2)的HPLC报告中的峰值,提示其纯度分别为96.45%、95.08%。
本发明利用整合素αvβ3的单链抗体(scFvαvβ3)替代单克隆抗体,所述单链抗体是把单克隆抗体重链的可变区(VH)和轻链的可变区(VL)基因在DNA水平克隆出来,再用一段连接肽(GGGGS)3的基因把VH和VL的羧基端和氨基端以VH-linker-VL的形式连接起来,表达后即得到ScFv片段,记名为ScFvαvβ3。
整合素αvβ3单链抗体ScFvαvβ3的氨基酸序列下所示:
QVQLQQSGAELARPGTSVKWSCRTSGYTFTSFGIAWVKQRSGQGLEWIGEIFPRSGNTYYNEKFTGKATLTADTSSSTAYMELRSLTSEDSAVYFCATYTSYGAMDYWGQGTSVTVSSGGGGSGGGGSGGGGSEIVLTQSPTTMAASRGEKITITCSANSSISSNHLHWYQQKSGFSPKFLIYRTSILASGVPARFSGSGSGTSYSLTIDTMEAEDVATYYCQQGSSKPYTFGGGTKLEIKRAHHHHHH(SEQ ID NO:1)。
编码整合素αvβ3单链抗体ScFvαvβ3的核苷酸序列如下所示:
CAGGTGCAGTTACAGCAGTCTGGTGCTGAATTAGCCCGTCCGGGTACAAGCGTTAAGTGGAGTTGTCGCACGTCAGGCTATACCTTTACGAGCTTTGGCATTGCCTGGGTTAAACAGCGCTCTGGCCAGGGCTTAGAGTGGATCGGCGAAATCTTTCCTCGCTCAGGCAATACTTATTATAACGAAAAGTTCACGGGCAAAGCCACACTGACCGCCGATACAAGTAGCTCAACCGCATATATGGAACTGCGTAGCCTGACGAGTGAAGATTCTGCTGTGTATTTTTGTGCGACATATACGAGCTATGGTGCGATGGATTATTGGGGTCAGGGCACCAGTGTGACCGTGTCTTCAGGTGGCGGTGGTAGCGGTGGTGGCGGTTCAGGCGGCGGTGGTTCAGAAATCGTGTTAACACAGAGTCCGACAACGATGGCCGCGTCACGCGGCGAAAAAATTACAATCACATGTAGTGCTAATAGTTCAATCTCTAGTAATCATCTGCATTGGTATCAGCAGAAAAGTGGCTTTTCTCCTAAATTTCTGATCTATCGCACCTCTATCTTAGCAAGCGGCGTTCCTGCACGCTTTTCTGGCAGCGGCTCAGGCACCTCTTATAGTTTAACCATTGATACGATGGAAGCCGAAGATGTTGCCACATATTATTGCCAGCAGGGCTCAAGTAAACCGTATACGTTTGGCGGTGGGACAAAACTGGAAATTAAACGCGCCCATCATCATCATCATCATTAA(SEQ ID NO:2)。
为了获得纯化的ScFvαvβ3蛋白,在转染E.coli BL21(DE3)之前,先通过限制性酶切分析鉴定重组质粒pET-28a-ScFv(图3A)。筛选出具有卡那霉素抗性的克隆进一步培养,利用镍柱亲和层析纯化上清中的ScFvαvβ3蛋白。纯化后的ScFvαvβ3经SDS-PAGE电泳和考马斯亮蓝染色,结果见图3B。
图3B中,M:蛋白分子量标志(KDa);BI:诱导前;AI:诱导后;P:沉淀;FT:穿透;E1、E2、E3:纯化后条带;R:复性后。在分子量26.5KDa处出现单一条带,为纯化后的ScFvαvβ3条带。
小分子肽cdGIGPQc和ScFvαvβ3之间的偶联,是通过偶联剂SMCC实现的。蛋白和多肽偶联SDS-PAGE检测结果见图3C,其中1,2:ScFvαvβ3-非相关肽偶联产物;3,4:ScFvαvβ3-相关肽偶联产物;5:蛋白分子量标志(KDa);6:ScFvαvβ3。重组的cdGIGPQc-ScFv经SDS-PAGE分析,其分子量略高于ScFvαvβ3。
非相关小分子肽cNAQAEQc与ScFvαvβ3的偶联,也是通过同样的方法完成的,其分子量与cdGIGPQc-ScFvαvβ3相似。
二、cdGIGPQc-ScFvαvβ3的肺癌细胞结合特性
为了探究cdGIGPQc-ScFvαvβ3是否保留了cdGIGPQc原有的肺癌细胞结合特性,利用免疫荧光试验加以验证。首先,将A549和L78细胞以5000个/孔的密度接种在96孔板中,孵箱孵育24h使其贴壁。次日,经4%多聚甲醛固定30min、5%BSA封闭1h后,避光加入100μl FITC-cdGIGPQc-ScFvαvβ3(15μg/mL)或FITC-cNAQAEQc-ScFvαvβ3(15μg/mL)4℃孵育过夜。PBS洗3次,去除未结合的荧光抗体。用DAPI(1:200,复能基因,广州,中国)复染核后,PBS洗3次,在荧光显微镜下观察结果。等体积的PBS和FITC-cdGIGPQc(1μg/mL)分别作为阴性对照和阳性对照。以上实验重复3次。
另外,又利用流式细胞术,进一步评估重组蛋白对肺癌细胞的结合能力。经PBS洗3次后,收集并重悬2×106的A549和L78细胞,避光加入100μl FITC-cdGIGPQc-ScFv(15μg/mL)或FITC-cNAQAEQc-ScFv(15μg/mL),室温孵育20min,同样以PBS和FITC-cdGIGPQc作为对照。用BD FACSVerseTM检测,并用FlowJo软件分析试验结果。结果见图4。
图4中,免疫荧光图片反映了FITC-cdGIGPQc-ScFvαvβ3和FITC-cNAQAEQc-ScFvαvβ3与A549细胞(A)及L78细胞(B)的结合。比例尺:100μm;用流式细胞术定量分析cdGIGPQc-ScFvαvβ3和cNAQAEQc-ScFvαvβ3对肺癌细胞A549(C)及L78(D)的亲和性;其中,红线代表阴性对照,蓝线代表经FITC-cdGIGPQc,FITC-cdGIGPQc-ScFvαvβ3或FITC-cNAQAEQc-ScFvαvβ3处理过的肺癌细胞。
免疫荧光组图(图4A、4B)说明:FITC-cdGIGPQc-ScFvαvβ3可以同阳性对照FITC-cdGIGPQc一样,特异性结合A549(图4A)和L78(图4B)肺癌细胞,其亲和性明显高于FITC-cNAQAEQc-ScFvαvβ3。在流式细胞术中,也得出了一致的的结果:加入FITC-cdGIGPQc-ScFvαvβ3和FITC-cdGIGPQc孵育的细胞,呈现出相似的近100%的阳性率,而FITC-cNAQAEQc-ScFvαvβ3处理组的阳性率约50%,其无论在阳性率或荧光强度上均明显低于前两者(图4C、4D)。由此可见,与cdGIGPQc偶联后,ScFvαvβ3与非小细胞肺癌的结合能力约提高了1倍。cdGIGPQc-ScFvαvβ3靶向非小细胞肺癌时,cdGIGPQc结合非小细胞肺癌上的整合素α3,ScFvαvβ3结合非小细胞肺癌的整合素αvβ3,拮抗αvβ3,使αvβ3失去生物学功能,从而抑制肿瘤新生血管的形成,使瘤细胞得不到充分养分而凋亡,同时通过血液转移也受到抑制.综上所述,这些结果表明:cdGIGPQc与ScFvαvβ3的偶联,不但没有影响cdGIGPQc部分的肺癌细胞结合特性,还增强了ScFvαvβ3对肺癌细胞的结合。
三、ScFvαvβ3和cdGIGPQc-ScFvαvβ3与αvβ3抗原的结合能力
利用Western Blot实验,验证ScFvαvβ3和cdGIGPQc-ScFvαvβ3对人整合素αvβ3的抗原识别能力。首先,将人整合素αvβ3蛋白(抗原)和上样缓冲液混合煮沸,在10%SDS-PAGE上电泳并转到PVDF膜。作为一抗,ScFvαvβ3和cdGIGPQc-ScFvαvβ3均能通过抗原抗体反应,有效地识别整合素αvβ3,表现为与αvβ3单抗一致的条带(图5A)。
这些结果清楚地表明:重组后的ScFvαvβ3片段,并未丢失其作为单克隆抗体时原有的抗原结合能力,这一能力也同样未因与cdGIGPQc偶联而有所影响。
四、cdGIGPQc-ScFvαvβ3在体外抑制肺癌细胞增殖
cdGIGPQc-ScFvαvβ3对肺癌细胞的增殖抑制作用,是通过CCK8实验验证的。将A549和L78细胞以5000个/孔的密度接种到96孔板中,24h后更换为无血清培养基饥饿12h。以等分子量的ScFvαvβ3为阳性对照,加入从50pM到5μM不同浓度的cdGIGPQc-ScFvαvβ3和cNAQAEQc-ScFvαvβ3作用24h。PBS洗涤之后,加入CCK8溶液37℃孵育1-4h,用酶标仪读出OD450值,用SPSS 20.0软件计算对肿瘤细胞增殖的相对抑制率和半数抑制浓度IC50。实验重复三次。
图5B、5C分别代表A549和L78细胞三次重复实验的一次结果。cdGIGPQc-ScFvαvβ3的IC50值较低,说明有活力的细胞较少,也就意味着更显著的抑瘤效应。ScFvαvβ3和cNAQAEQc-ScFvαvβ3具有相似的浓度效应曲线及抑瘤作用。在相同浓度下,与ScFvαvβ3和cNAQAEQc-ScFvαvβ3相比,cdGIGPQc-ScFvαvβ3可以更显著地抑制肿瘤生长。微摩尔浓度的cdGIGPQc-ScFvαvβ3即可有效抑制肺癌细胞增殖。由图可知,在5μM的浓度下,ScFvαvβ3和cNAQAEQc-ScFvαvβ3仅能抑制约40%的肺癌细胞,而cdGIGPQc-ScFvαvβ3则可达到大于90%的抑制率。
五、cdGIGPQc-ScFvαvβ3的体内抑瘤疗效
为了评估cdGIGPQc-ScFvαvβ3在体内的抑瘤效果,构建了A549(图6A,B)和L78((图6C,D))两种肺癌裸鼠移植瘤模型。当瘤子的平均体积达到100mm3,将裸鼠随机分为4组(n=6),每四天经尾静脉注射10μg的ScFvαvβ3(ScFv组)、cdGIGPQc-ScFvαvβ3(cd-ScFv组)和cNAQAEQc-ScFvαvβ3(cN-ScFv组),每4天1次,共3次;注射等体积的PBS作为阴性对照,定期用游标卡尺测量瘤子大小,并用公式:体积=(长×宽2)/2计算瘤子体积;用分析天平称量瘤子的最后质量;结果用“均值±标准差”表示;利用非配对t检验分析实验数据;*,p<0.05。
给药两周后,A549和L78模型的肿瘤生长曲线如图6A、6C所示,与PBS组相比,ScFv、cd-ScFv和cN-ScFv三组的瘤子体积均明显缩小。在A549模型中,各组的平均最终瘤重分别为982.9±111mg(PBS组)、636.3±30.42mg(ScFv组)、429.9±85.32mg(cd-ScFv组)、631.1±141.07mg(cN-ScFv组)(图6B)。各给药组相对于PBS组,对肿瘤生长的抑制率分别为:35.26%(ScFv组)、56.27%(cd-ScFv组)、35.80%(cN-ScFv组)。同样地,在L78模型中,平均最终瘤重分别为530.8±72.50mg(PBS组),250.1±28.68mg(ScFv组),185.8±48.99mg(cd-ScFv组)and 305.5±100.45mg(cN-ScFv组)(图6D)。各给药组相对于PBS组,对肿瘤生长的抑制率分别为:52.89%(ScFv组)、64.99%(cd-ScFv组)、42.45%(cN-ScFv组)。
总而言之,ScFvαvβ3和cNAQAEQc-ScFvαvβ3具有相近的抗肿瘤活性,而cdGIGPQc-ScFvαvβ3则呈现出更优于两者的疗效,其对肺癌移植瘤的抑制率约为ScFvαvβ3和cNAQAEQc-ScFvαvβ3的1.40倍和1.56倍。除此之外,当瘤子尚小就出现明显破溃的现象仅见于cdGIGPQc-ScFvαvβ3,也就是在肿瘤尚小的时候cdGIGPQc-ScFvαvβ3就开始起抑瘤作用。已经有文献报道过:ScFvαvβ3的抑瘤效果相当于αvβ3的单克隆抗体mAbαvβ3(Liu D,Wang C,Li C,Zhang X,Zhang B,Mi Z,An X,Tong Y:Production and characterization of a humanized single-chain antibody against human integrin alphav beta3protein.J BIOL CHEM 2011;286:24500-24507.),则可以推测本发明的偶联药物cdGIGPQc-ScFvαvβ3效果优于mAbαvβ3。
综上所述,ScFvαvβ3偶联肺癌特异性小分子肽cdGIGPQc,而非cNAQAEQc之类的非相关肽,可以增强ScFvαvβ3的抗肿瘤效应,体现为更小的肿瘤体积及质量。另外,与传统的化疗药物不同的是,在使用cdGIGPQc-ScFvαvβ3治疗的过程中,裸鼠的体重及一般情况均无明显变化。在A549模型中,cdGIGPQc-ScFvαvβ3组裸鼠给药前的平均体重为17.13g,给药2周后平均体重为18.57g;L78模型中,给药前的平均体重为19.37g,给药2周后平均体重为20.8g。从而提示了其在体内具有良好耐受性。
六、cdGIGPQc-ScFv的疗效及毒性
通过H&E染色,直观地描述了A549和L78两种移植瘤的肿瘤本质,结果见图7,其中左边代表A549模型,右边代表L78模型。
图7A中,裸鼠经ScFvαvβ3,cdGIGPQc-ScFvαvβ3和cNAQAEQc-ScFvαvβ3处理2周后,肿瘤的病理学特征及抗CD31和抗Ki67的代表性组化图片,免疫组化CD31反映肿瘤血管生成情况,Ki67则反映肿瘤细胞增殖。比例尺:100μm。
图7B中,抗CD31和抗Ki67组化图片的IOD/Area值,是利用Image-Pro Plus软件分析计算得出的。每组至少包括9张图片用以定量分析及数据统计。采用非配对t检验进行数据分析。*,p<0.05。cdGIGPQc-ScFv组CD31和Ki67的IOD/Area值明显低于其他组(图7B)。CD31和Ki67的同步减少趋势,进一步明确了cdGIGPQc-ScFv的抗肿瘤机制。该实验表明:cdGIGPQc-ScFvαvβ3能够更显著地降低肿瘤的微血管密度并抑制肿瘤细胞的增殖,从而说明其疗效更优于ScFvαvβ3和cN-ScFvαvβ3。图8、图9为动物移植瘤模型经治疗后重要脏器的H&E染色结果,显示cdGIGPQc-ScFv对重要脏器无明显影响或毒性作用,仅少数个体存在轻微的炎症反应,从而反映了其低毒性。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
SEQUENCE LISTING
<110> 南方医科大学珠江医院
<120> 一种靶向肺癌的偶联药物cdGIGPQc- ScFvαvβ3
<130>
<160> 2
<170> PatentIn version 3.5
<210> 1
<211> 249
<212> PRT
<213> 人工序列
<400> 1
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Thr
1 5 10 15
Ser Val Lys Trp Ser Cys Arg Thr Ser Gly Tyr Thr Phe Thr Ser Phe
20 25 30
Gly Ile Ala Trp Val Lys Gln Arg Ser Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Phe Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Thr Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Thr Tyr Thr Ser Tyr Gly Ala Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Thr Thr Met
130 135 140
Ala Ala Ser Arg Gly Glu Lys Ile Thr Ile Thr Cys Ser Ala Asn Ser
145 150 155 160
Ser Ile Ser Ser Asn His Leu His Trp Tyr Gln Gln Lys Ser Gly Phe
165 170 175
Ser Pro Lys Phe Leu Ile Tyr Arg Thr Ser Ile Leu Ala Ser Gly Val
180 185 190
Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr
195 200 205
Ile Asp Thr Met Glu Ala Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Gly Ser Ser Lys Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
225 230 235 240
Lys Arg Ala His His His His His His
245
<210> 2
<211> 750
<212> DNA
<213> 人工序列
<400> 2
caggtgcagt tacagcagtc tggtgctgaa ttagcccgtc cgggtacaag cgttaagtgg 60
agttgtcgca cgtcaggcta tacctttacg agctttggca ttgcctgggt taaacagcgc 120
tctggccagg gcttagagtg gatcggcgaa atctttcctc gctcaggcaa tacttattat 180
aacgaaaagt tcacgggcaa agccacactg accgccgata caagtagctc aaccgcatat 240
atggaactgc gtagcctgac gagtgaagat tctgctgtgt atttttgtgc gacatatacg 300
agctatggtg cgatggatta ttggggtcag ggcaccagtg tgaccgtgtc ttcaggtggc 360
ggtggtagcg gtggtggcgg ttcaggcggc ggtggttcag aaatcgtgtt aacacagagt 420
ccgacaacga tggccgcgtc acgcggcgaa aaaattacaa tcacatgtag tgctaatagt 480
tcaatctcta gtaatcatct gcattggtat cagcagaaaa gtggcttttc tcctaaattt 540
ctgatctatc gcacctctat cttagcaagc ggcgttcctg cacgcttttc tggcagcggc 600
tcaggcacct cttatagttt aaccattgat acgatggaag ccgaagatgt tgccacatat 660
tattgccagc agggctcaag taaaccgtat acgtttggcg gtgggacaaa actggaaatt 720
aaacgcgccc atcatcatca tcatcattaa 750
- 还没有人留言评论。精彩留言会获得点赞!