含索拉非尼和GSK2656157的药物组合物及用途的制作方法
本发明属于生物医药领域,具体涉及含索拉非尼和gsk2656157抑制剂的药物组合物及用途。
背景技术:
世界卫生组织调查报告表明,全球癌症状况日益严重,今后20年新患者的人数将由目前的每年1000万增加到1500万,因癌症而死亡的人数也将由每年的600万增加至1000万。随着生活水平的提高,饮食结构的改变,食管癌的发病率呈逐年上升趋势;其中原发性肝癌为发生在肝细胞与肝内胆管上皮细胞的癌变,是人类最常见的恶性肿瘤之一;肺癌为常见的恶性肿瘤,源于各级支气管上皮,分为细胞肺癌和非小细胞肺癌。这些癌症的治疗虽然以手术为主,但由于早期患者一般无明显症状,在首次被确诊的癌症患者中,很多已为中晚期,失去了手术切除的机会,故非手术治疗(如化疗)在肿瘤的综合治疗中有着十分重要的地位。化疗是利用化学药物阻止癌细胞的增殖、浸润、转移,直至最终杀灭癌细胞的一种治疗方式。它是一种全身性治疗手段,和手术、放疗一起,并称为癌症的3大治疗手段。
目前已上市的抗肿瘤药物较多,如烷化剂药物、抗代谢药物、抗肿瘤抗生素、免疫调节剂等,但是大多药物普遍存在选择性低,毒性较大,病人不耐受等缺点。随着对肿瘤的发生发展的分子机制研究越来越清楚,分子靶向治疗多种恶性肿瘤受到了广泛的关注和高度重视。分子靶向药物选择性高、广谱有效,其安全性优于细胞毒性化疗药物,是目前肿瘤治疗领域发展的新方向。
索拉非尼(sorafenib)是一个多靶向药物,它通过抑制raf/mek/erk介导的细胞信号传导通路而直接抑制肿瘤细胞的增殖,又通过作用于egfr和pdgfr来阻断肿瘤新生血管的形成,间接抑制肿瘤生长。该药物对包括肝癌在内的多种恶性肿瘤均有明显的抑制作用,但却只能将肿瘤无进展期的基线控制在6个月内,且其对人体毒性较大,服用后容易导致皮疹、血压升高、手掌或足底部发红、疼痛、肿胀或出现水疱等不良症状。如何进一步提高索拉非尼抗肿瘤活性的同时保持较低的毒副作用,无疑也是目前临床试验急待研究解决的问题。
目前已有将索拉非尼和其他药物联用在体内和体外抗肿瘤的例子。如中国专利申请cn102438608a公开了抗血管药ave8062和索拉非尼之间的组合,并证实了该组合可有效治疗癌症,特别是实体瘤,尤其是对肉瘤、肺癌、卵巢癌、肝癌或肾癌具有抑制效果。中国专利申请cn102836160a公开了淋巴癌药物abt-263和索拉非尼之间的组合,并证实了该组合可有效治疗多种癌症。但是上述组合物联合使用时的毒副作用较强。
越来越多的证据表明,内质网应激与肿瘤细胞的药物敏感性密切相关,而perk/eif2α通路是内质网应激下游的重要传感通路。gsk2606414是一种口服具有生物活性的、有效的、选择性perk抑制剂,比测试的其他eif2aks选择性至少高100倍。
目前,并无gsk2606414和索拉非尼联用的报道。
技术实现要素:
为了解决现有技术中存在的技术问题,本发明的目的在于提供一种含索拉非尼和gsk2656157的药物组合物,提高了索拉非尼对肿瘤的抑制效果,并有效地改善了索拉非尼的毒副作用。
本发明提供了一种含索拉非尼和gsk2656157的药物组合物,所述药物组合物包含有效量的甲苯磺酸索拉非尼和有效量的gsk2656157。
所述的甲甲苯磺酸索拉非尼,cas号为475207-59-1,所述gsk2656157,cas号为1337532-29-2,其结构式如下:
作为本发明最佳的实施方案,所述药物组合物中甲苯磺酸索拉非尼和gsk2656157的摩尔浓度比为5~40∶1~10,优选地,所述药物组合物中甲苯磺酸索拉非尼和gsk2656157的摩尔浓度比为10∶5,其结构式如下:
优选地,可将本发明中所述药物组合物按照本领域常规技术制备成注射制剂或口服制剂,本发明优选将本发明中所述药物组合物制备成口服制剂,所述口服制剂优选为口服胶囊。根据制剂形式,本发明所述药物组合物在制剂中的含量可以以质量计为1~99%,优选为5~90%;制剂使用的辅料可采用本领域常规的辅料,以不和本发明药物组合物发生反应或不影响本发明药物的疗效为前提;制剂的制备方法可以采用本领域常规的制备方法进行制备。
本发明中的药物组合物的给药剂量根据给药对象、给药途径或药物的制剂形式不同可以进行适当的变化,但以保证该药物组合物在哺乳动物体内能够达到有效的血药浓度为前提。
上述药物组合物可有效治疗癌症,特别是肺癌、食管癌或肝癌,更特别是用于治疗食管癌。
本发明另一个目的是提供上述的药物组合物在制备预防和/或治疗肿瘤中的用途。其中,所述肿瘤为肺癌、食管癌或肝癌,更优选地,所述肿瘤为食管癌。
与现有技术相比,本发明药物组合物具有以下优势:
本发明含甲苯磺酸索拉非尼和gsk2656157的药物组合物有效地改善了索拉非尼的副作用问题,使药物的生物利用度提高,同时,甲苯磺酸索拉非尼和gsk2656157的联合在治疗肺癌、肝癌和食管癌上可使药效产生协同增效的作用,明显优于单药使用,这一点在本发明抗肿瘤作用和试验结果中得到证实。特别地,当甲苯磺酸索拉非尼和gsk2656157的摩尔浓度比10∶5时,这种协同作用非常好,并且药物对正常细胞的毒副作用最小。
附图说明
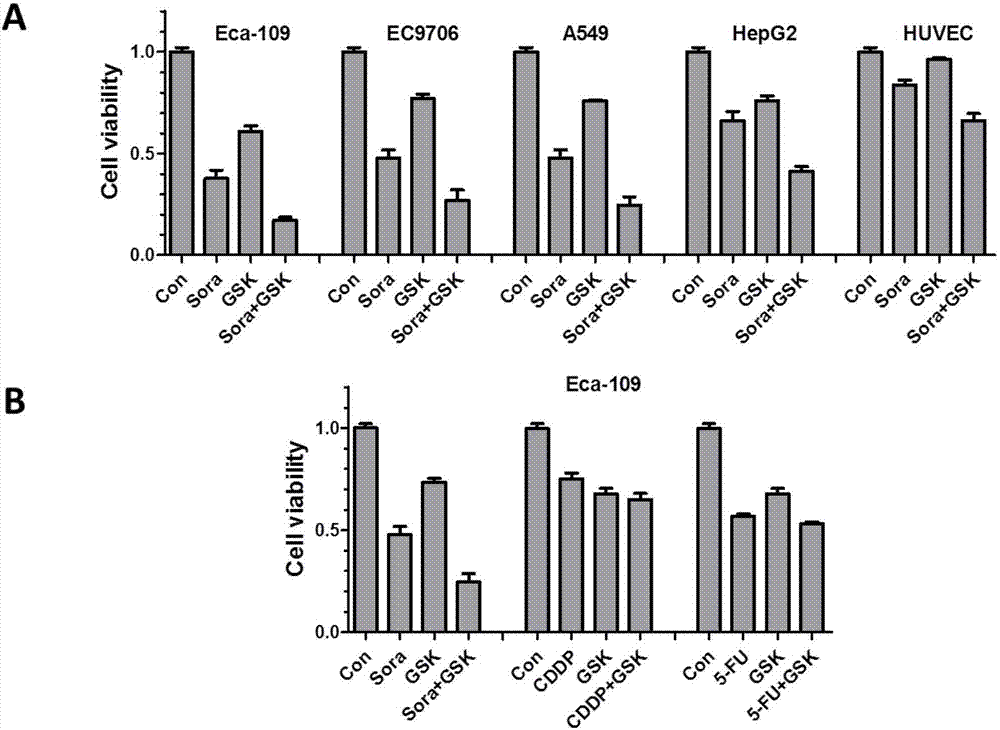
图1显示了甲苯磺酸索拉非尼与gsk2656157单独使用对肿瘤细胞生长的影响;
图2显示了甲苯磺酸索拉非尼、顺铂、5-氟尿嘧啶分别与gsk2656157联合作用对肿瘤细胞生长的影响;
图3显示了甲苯磺酸索拉非尼与gsk2656157联合作用对肿瘤细胞凋亡的影响;
图4显示了甲苯磺酸索拉非尼与gsk2656157联合作用对肿瘤细胞克隆形成的影响。
具体实施方式:
以下通过具体实施方式的描述对本发明作进一步说明,但这并非是对本发明的限制,本领域技术人员根据本发明的基本思想,可以做出各种修改或改进,但是只要不脱离本发明的基本思想,均在本发明的范围之内。
实施例1、本发明药物组合物的原料配方
组合物1:甲苯磺酸索拉非尼和gsk2656157,甲苯磺酸索拉非尼和gsk2656157的摩尔浓度比10∶5。
组合物2:甲苯磺酸索拉非尼和gsk2656157,甲苯磺酸索拉非尼和gsk2656157的摩尔浓度比5∶1。
组合物3:甲苯磺酸索拉非尼和gsk2656157,甲苯磺酸索拉非尼和gsk2656157的摩尔浓度比40∶10。
实施例2、抗肿瘤作用和试验
研究1:甲苯磺酸索拉非尼和gsk2656157单独使用对肿瘤细胞增殖的影响(图1)
1.1实验方法
将细胞以每孔3000~6000个细胞的数量接种到96孔板,待细胞贴壁(24h)后,将甲苯磺酸索拉非尼与gsk2656157药物分别稀释成一定的梯度浓度,每浓度设5复孔,分实验组及调零组加药。48h后采用mtt法进行细胞活力检测,每孔加入10μlmtt溶液,继续培养4h,小心吸除孔内液体,避免接触孔内结晶物,每孔加入100μl的dmso,于恒速摇床上避光摇晃。待结晶物充分溶解后,在酶标仪上读取od值(波长570nm,参考波长630nm),测得吸光度a值。细胞活力(cellviability)的计算公式为:细胞活力=od实验组/od对照组。根据各浓度的抑制率可作图得到剂量反应柱状图,作图软件为graphpad。
从图1可以看出,甲苯磺酸索拉非尼与gsk2656157对肿瘤细胞都有一定的生长抑制作用,其中甲苯磺酸索拉非尼在10μm对四株肿瘤细胞eca-109,ec9706,a549和hepg2的存活率分别为31%,48%,45%和74%,而gsk2656157在5μm对四株肿瘤细胞的存活率分别为60%,76%,74%和73%。
研究2:甲苯磺酸索拉非尼和gsk2656157组合对肿瘤细胞增殖的影响(图2a)
将肿瘤eca-109、ec9706、a549和hepg2细胞以每孔3000-6000个细胞的数量接种到96孔板,待细胞贴壁后,加空白对照组、甲苯磺酸索拉非尼单药组、gsk2656157单药组及联合用药组药物(10μm甲苯磺酸索拉非尼+5μmgsk2656157),培养48h后,每孔加入10μl浓度为5mg/ml的mtt溶液,继续培养4h,然后弃去培养液每孔加入100μl的dmso,于恒速摇床上避光摇晃。待结晶物充分溶解后,在酶标仪上读取od值(波长570nm,参考波长630nm),读取每孔的吸光值,计算两药合用后的细胞存活及抑制率。
采用金氏修正式评价两种药物联合用药时对肿瘤细胞的联用效果,具体步骤为,按照生长抑制率(%)=(1-od实验组/od对照组)×100%的公式,计算出a药在某种条件下对肿瘤细胞的抑制率为ea,计算出b药在某种条件下对肿瘤细胞的抑制率为eb,再计算出两者联合给药的抑制率为ec,通过以下公式计算联合用药指数q值,q=ec/(eb+ea-eb*ea),当q值>1.15为协同效应,0.85<q<1.15为相加效应,q<0.85为拮抗效应。通过上述联合用药指数的计算进一步判断两种药物联合用药的最终药效。经过计算甲苯磺酸索拉非尼与gsk2656157联合用药在eca-109,ec9706,a549和hepg2肿瘤细胞的q值分别为1.27,1.23,1.16,1.18。表明10μm甲苯磺酸索拉非尼与5μmgsk2656157在肿瘤细胞中联合使用具有很好的协同作用。
研究3:甲苯磺酸索拉非尼、顺铂、5-氟尿嘧啶分别与gsk2656157组合对食管癌细胞增殖的影响(图2b)
按照研究2中所述方法,探索甲苯磺酸索拉非尼、顺铂、5-氟尿嘧啶分别与gsk2656157组合对食管癌细胞增殖的影响。食管癌eca-109细胞铺板,分组如下:对照组、甲苯磺酸索拉非尼组、gsk2656157组、甲苯磺酸索拉非尼+gsk2656157组、顺铂组、顺铂+gsk2656157组、5-氟尿嘧啶组、5-氟尿嘧啶组+gsk2656157组。经过计算,10μm甲苯磺酸索拉非尼与5μmgsk2656157联合用药在eca-109中的q值为1.27;0.5μg/ml顺铂与5μmgsk2656157联合用药在eca-109中的q值为0.85;2μg/ml5-氟尿嘧啶与5μmgsk2656157联合用药在eca-109中的q值为0.75。表明甲苯磺酸索拉非尼与gsk2656157在抑制食管癌细胞生长中的联合使用效果强于顺铂、5-氟尿嘧啶与gsk2656157联合使用。
研究4:甲苯磺酸索拉非尼和gsk2656157组合对肿瘤细胞凋亡的影响(图3)
将eca-109细胞分别以每孔2×105个细胞的密度接种至6孔板。待细胞贴壁后,按研究2分组给药,共同处理48h后。利用westernblot方法检测经甲苯磺酸索拉非尼与gsk2656157分别单独处理及联合处理后食管癌细胞eca-109细胞内凋亡蛋白parp的表达情况。westernblot方法按照研究2进行。
结果如图3所示,在eca-109细胞中,当用甲苯磺酸索拉非尼与gsk2656157单独及联合用药处理时,凋亡标志蛋白parp的剪切条带明显上调,并且联合组与各个单药组相比表达具有明显的差异,这说明甲苯磺酸索拉非尼与gsk2656157联合用药能够显著引起食管癌细胞发生凋亡。
研究5:甲苯磺酸索拉非尼和gsk2656157组合对肿瘤细胞克隆形成的影响(图4)
将eca-109和ec9706细胞接种到6孔板,待细胞贴壁过夜后,加入空白对照组、10μm甲苯磺酸索拉非尼、5μmgsk2656157及联合用药组药物,孵育7天,检测细胞平板克隆形成情况。结果如图4所示,与对照组以及单药组相比,联合用药对细胞克隆形成具有明显的协同抑制作用,联合用药组已不能观察到明显的细胞克隆。
实施例3、联合用药急性毒性试验
本实验以昆明小鼠为研究对象,研究甲苯磺酸索拉非尼和gsk2656157组合药物对小鼠的急性毒性的影响,为甲苯磺酸索拉非尼和gsk2656157药物组合物进一步研究开发提供初步安全性评价参考。
急性毒性试验按gb1519.3-2003《食品急性毒性试验》中最大耐受剂量法进行试验。取18只清洁小白鼠,随机分为3组:空白对照组(a组)、甲苯磺酸索拉非尼和gsk2656157(摩尔浓度比为10∶5)联用组(b组)、甲苯磺酸索拉非尼单独用药组(c组),每组6只(n=6),雌雄各3只。根据食品安全性评价中的急性毒性分级标准,实验前小鼠禁食10h,以0.5ml/只灌胃给药,24h内给药2次,日用量为15g/kg,空白对照组小鼠灌胃相同剂量的生理盐水。给药后,观察小鼠72h内是否死亡,以及未来一周内的体重变化。所有试验结果均以“x±s”表示,用t检验方法检验差异显著性,结果见表1。
从表1可知,小鼠在喂养期间的体重是不断增加的,甲苯磺酸索拉非尼单独供药组(c组)相对于空白对照组(a组)体重有显著的下降,而甲苯磺酸索拉非尼和gsk2656157联用组(b组)相对于空白对照组(a组)体重虽有所下降,但幅度不大。说明,甲苯磺酸索拉非尼和gsk2656157联用组联用的毒性较甲苯磺酸索拉非尼单独用药的毒性有降低,即甲苯磺酸索拉非尼和sk2656157联用能使甲苯磺酸索拉非尼对人体的毒副作用减少。
表1用药期间小鼠的体重变化情况(n=6)
注:与a组相比,**p<0.01。
将上述小鼠,称重后,处死解剖,用肉眼观察心脏、肝、脾、肾、脑以及胸腺情况,记录观察结果。结果显示:甲苯磺酸索拉非尼单独用药组以及甲苯磺酸索拉非尼和gsk2656157联用组小鼠各器官均有不同程度的病变。
将取出的各内脏器官,用生理盐水洗涤,去除脏器表面的残留血液与结缔组织,用吸水纸擦干,准确称重,计算脏器指数(脏器指数=脏器重量体/体重*100%),结果见表2。
从表2可以看出,与空白对照组相比,甲苯磺酸索拉非尼单独用药组小鼠脏器指数有显著性差异;甲苯磺酸索拉非尼和gsk2656157联用组小鼠脏器指数差异不显著。
表2各组小鼠脏器指数(n=6)
注:与a组相比,*p<0.05,**p<0.01。
脏器指数可近似反映该脏器的生理指标,反映动物总的营养状态和内脏器官的病变情况。脏器系数增大时表明有充血水肿增生肥大等变化,脏器系数减小时表明脏器可能出现萎缩退行性等变化。本发明根据脏器指数判断小鼠内脏器官是否发生病变。
血清总胆固醇、甘油三酯是反映生物体内血脂水平的重要指标,血清谷丙转氨酶、谷草转氨酶是肝功能的主要检测指标,而尿素氮和肌酐是肾功能的主要检测指标。本发明通过小鼠的血清指标考察索拉非尼和gsl2656157复合药物的毒副性,结果见表3。
由表3可知,甲苯磺酸索拉非尼单独用药组的血清生化指标与对照组相比有显著性地差异,而甲苯磺酸索拉非尼和gsk2656157联用组小鼠的血清指标与对照组相比差异不显著,影响明显小于甲苯磺酸索拉非尼单独用药组。
表3各组小鼠的血清生化指标(n=6)
注:与a组相比,*p<0.05,**p<0.01。
- 还没有人留言评论。精彩留言会获得点赞!