青蒿素衍生物治疗炎症性肠病的医学用途的制作方法
本发明涉及药物领域,具体地,本发明提供了4个青蒿素衍生物具有抗炎免疫抑制活性作为治疗炎症性肠病的医学新用途。在硫酸葡聚糖(dss)诱导的溃疡性结肠炎小鼠动物模型中的实验研究结果证明了所述化合物灌胃给药能够有效改善实验动物的体重下降、腹泻、便血等溃疡性结肠炎临床症状,减轻结肠组织的病理学损伤,抑制实验小鼠炎症细胞对结肠组织的浸润,下调相关促炎性细胞因子的水平,药效药理学研究证实该类化合物具有良好的免疫抑制活性和较高的安全性,可作为治疗和辅助治疗炎症性肠病的药物及医学用途。
背景技术:
炎症性肠病(ibd),是累及回肠、直肠、结肠的特发性、慢性肠道炎症性疾病,包括溃疡性结肠炎(uc)和克罗恩病(cd)等,并发症多,近年来该类疾病的发病率和患病率呈整体上升趋势。慢性结肠炎、溃疡性结肠炎是一种病因尚不明确的慢性非特异性肠道炎症性疾病,其病变部位累及直肠和结肠,反复性发作,临床主要表现为腹泻、腹痛和黏液脓血便。该类疾病不仅影响患者的生活质量,甚至易诱发结直肠癌。目前临床上治疗炎症性肠病的药物主要为抗炎和免疫抑制类化合物或生物制剂,包括氨基水杨酸类、激素、环孢素和肿瘤坏死因子单抗等。这些药物附带的肾脏毒性、固醇类依赖性等毒副作用导致了它们临床应用上的局限性。因此,研发高效、低毒的治疗炎症性肠病的药物具有广泛的临床需求。
青蒿素是从中药青蒿(植物黄花蒿artemisiaannual.)提取的抗疟有效成分,一种罕见的含有过氧基团的倍半萜内酯。它不仅具有卓越的抗疟作用,还发现具有良好的抗炎免疫抑制活性。我们自2000年开始针对青蒿素类化合物开展了以免疫抑制活性为导向的药物化学与生物学相结合的系统研究,合成了多系列的新型青蒿素衍生物,发现了一批具有更强抗炎免疫抑制活性以及口服给药顺应性好的新衍生物。针对上述的研究发现,我们申请两个专利并获得授权。其中,中国专利第200680002368.5号公开了青蒿素衍生物、其制备方法和应用以及包含该衍生物的药物组合物;中国专利第200680026325.0号公开了水溶性青蒿素衍生物、制法、药物组合物及用途。
通过对系列的青蒿素衍生物的抗炎免疫抑制活性的成药性研究评价,于2006年我们最终确定了代表性化合物马来酸蒿乙醚胺(β-aminoarteethermaleate,sm934)作为治疗自身免疫性疾病系统性红斑狼疮的候选新药。sm934是水溶性青蒿素衍生物,具有强烈的免疫抑制活性和新颖的作用机制,sm934高效、低毒、口服吸收好,成药性高,具有良好应用前景。sm934获2项中国、2项美国和1项日本专利授权。该研究得到国际同行的关注,mini-reviewsinmedicinalchemistry(2007,7,411-422.)认为我们研发的青蒿素衍生物毒性低,不良反应少,作用机制与csa和fk506完全不同,是极具前景的免疫抑制药物;chemicalsocietyreviews.(2010,39(2):435-454)认为水溶性青蒿素的发现是青蒿素类化合物在免疫学领域的成功拓展和应用。机理研究证实:青蒿素类化合物以th17细胞功能为作用中心,对免疫细胞的异常活化信号转导途径进行交互调控。这项工作不仅研发具有自主知识产权的免疫抑制新药,同时发挥我国青蒿素的资源优势,拓展青蒿素类化合物的应用范围,具有重要的科学意义和应用价值。
技术实现要素:
本发明的目的是发现和提供青蒿素类衍生物或其药学上可接受的盐用于制备治疗或辅助治疗炎症性肠病的药物中的用途。
一方面,本发明提供了青蒿素类衍生物或其药学上可接受的盐在制备用于治疗或辅助治疗炎症性肠病的药物中的用途,其中,所述青蒿素类衍生物选自以下化合物:
本发明研究证明了上述青蒿素衍生物能够有效地抑制炎性细胞对结肠组织的浸润,下调结肠组织中促炎性细胞因子的水平,可用于制备治疗或辅助治疗炎症性肠病的药物。
因此,本发明还提供了上述青蒿素类衍生物或其药学上可接受的盐在制备用于抑制炎性细胞对结肠组织的浸润和下调结肠组织中促炎性细胞因子的水平的药物中的用途。
优选地,上述用途中,所述青蒿素类衍生物药学上可接受的盐选自以下化合物:
优选地,上述用途中,所述药物可以为片剂、胶囊剂、冲剂、口服或灌肠液体制剂、或静脉或肌肉注射剂等剂型。
此外,本发明还提供了一种治疗或辅助治疗炎症性肠病的方法,该方法包括向有此需要的受试者提供治疗有效量的上述青蒿素类衍生物或其药学上可接受的盐。
此外,本发明还提供了一种抑制炎性细胞对结肠组织的浸润和下调结肠组织中促炎性细胞因子的水平的方法,该方法包括向有此需要的受试者提供治疗有效量的上述青蒿素类衍生物或其药学上可接受的盐。
本发明还涉及用于治疗或辅助治疗炎症性肠病的上述青蒿素类衍生物或其药学上可接受的盐。
本发明还涉及用于抑制炎性细胞对结肠组织的浸润和下调结肠组织中促炎性细胞因子的水平的上述青蒿素类衍生物或其药学上可接受的盐。
本发明还涉及一种用于治疗或辅助治疗炎症性肠病的药物组合物,其包含上述青蒿素类衍生物或其药学上可接受的盐作为活性成分。
本发明还涉及一种用于抑制炎性细胞对结肠组织的浸润和下调结肠组织中促炎性细胞因子的水平的药物组合物,其包含上述青蒿素类衍生物或其药学上可接受的盐作为活性成分。
本发明中,优选地,所述炎症性肠病可以包括溃疡性结肠炎、克罗恩病、慢性肠炎等慢性肠道炎症性疾病。
附图说明
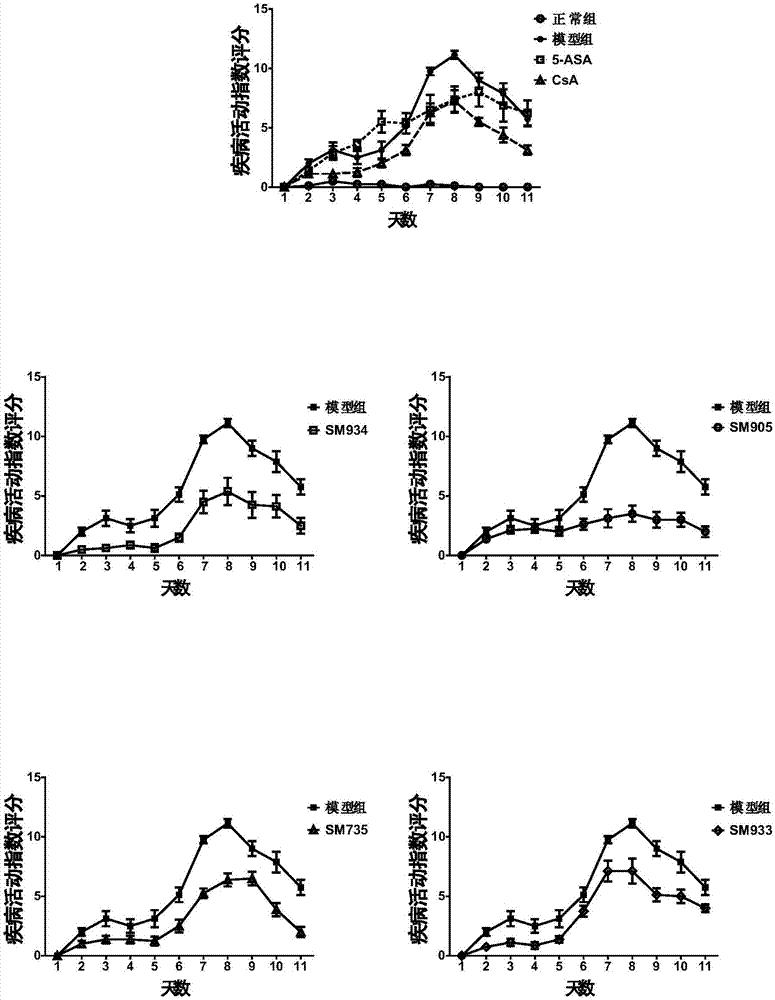
图1为显示实验期间各组小鼠的疾病活动指数评分的图。
图2a为实验终点的各组小鼠结肠组织的照片。
图2b为显示实验终点的各组小鼠结肠长度的图。与模型对照组比较,*,p<0.05;**,p<0.01。
图2c为显示实验终点取小鼠结肠组织,截取远端结肠固定于福尔马林中,石蜡包埋切片、h&e染色制作病理学切片的图。
图3为显示实验终点取各组小鼠肠系膜淋巴结和脾脏制备单细胞悬液,用相应荧光抗体对细胞标记,进行流式细胞术分析的结果的图。图3a是对分离的肠系膜淋巴结细胞,图3b是对分离的脾脏淋巴细胞,分别进行了抗f4/80抗体+抗cd11b抗体的染色(双阳性细胞被识别为巨噬细胞),抗gr-1抗体+抗cd11b抗体的染色(双阳性细胞被识别为中性粒细胞)。
图4为显示实验终点对各组小鼠结肠中段进行冷冻切片后,应用dapi荧光抗体对细胞核进行染色,抗cd11b抗体对单核淋巴细胞进行染色,在荧光共聚焦显微镜下拍照分析的结果的图。
图5为显示各组小鼠结肠组织中促炎性细胞因子水平检测结果的图。与模型对照组比较,*,p<0.05;**,p<0.01;***,p<0.001。
具体实施方式
实验实施例
对4个青蒿素衍生物(sm934,sm905,sm933和sm735)开展了治疗慢性炎症性肠病的药效学及相关机制研究。
一、实验材料
实验动物:纯系balb/c雌性小鼠,8周龄左右,上海斯莱克实验动物有限责任公司。
试剂:硫酸葡聚糖(dss,美国mpbiomedicals生物医学公司产品),环孢素a(csa,中国药品生物制品检定所),5-氨基水杨酸(5-asa,sigma-aldrich公司),流式细胞抗体购自bdpharmingen公司。
sm934和sm905的具体制备方法可参照发明人之前的专利(zl89109562.4,zl93112454.9)和已发表的论文j.med.chem,2000,43:1635-1640.。
sm934:
与马来酸成盐。白色结晶。熔点:139-141℃
元素分析(c21h33no9):
计算值:c56.87h7.50n3.16
实测值:c56.84h7.59n3.10
sm905:
与马来酸成盐。白色结晶。熔点:171-173℃
元素分析(c26h43no10):
计算值:c58.96h8.18n2.64
实测值:c58.92h7.91n2.59
sm933和sm735的具体制备方法可参照发明人之前的专利(zl94113982.4、zl01113407.0)和申请号为99807416专利申请中的内容。
sm735:
元素分析(c25h32o9·1/2h2o):
计算值:c61.84h6.85
实测值:c62.09h6.86
sm933:
元素分析(c26h36o8):
计算值:c65.53h7.61
实测值:c65.46h7.66
二、实验方法
[一]dss诱导溃疡性结肠炎小鼠模型建立及药效学评价
1.小鼠随机分为正常对照组、模型组、环孢素a(csa)(20mg/kg)治疗组、5-氨基水杨酸(5-asa)(50mg/kg)治疗组、以及具有抗炎免疫抑制活性作用的青蒿素衍生物sm934,sm905,sm933和sm735(各自10mg/kg)治疗组,每组8只小鼠。除正常对照组的小鼠以外,其他各组包括模型组、环孢素a治疗组、5-氨基水杨酸治疗组,4个青蒿素衍生物治疗组小鼠的饮用水中均加入了5%dss连续7天进行肠道炎症模型的诱导造模。
2.自小鼠诱导造模日开始至实验终点,各治疗组分别给予环孢素a、5-氨基水杨酸5-asa和4个青蒿素衍生物(10mg/kg)灌胃给药进行治疗干预。
3.疾病活动指数评价
实验期间对各组小鼠进行每天称取小鼠重量,检测粪便隐血,根据如下表格对每只小鼠疾病活动进行评分。
疾病活动指数(dai)评分表
表1.体重减轻分成5级(0,体重没有下降或上升;1,下降1-5%;2,下降5-10%;3,下降10-20%;4,下降超过20%);粪便硬度分成3级(0,正常;2,软便;4,稀便);粪便隐血分成5级(0,阴性;1,+;2,++;3,+++;4,肛周出血)。
[二]小鼠结肠组织整体及微观病理学变化
实验终点取小鼠结肠组织,量取长度,截取远端结肠固定于福尔马林中,石蜡包埋切片、h&e染色制作病理学切片。
[三]致炎性细胞检测
1.实验终点取小鼠脾脏和淋巴结制备单细胞悬液,用相应荧光抗体对细胞标记,进行流式细胞术分析。
2.结肠中段进行冷冻切片后,相应荧光抗体进行染色,在荧光共聚焦显微镜下拍照分析。
[四]结肠组织中促炎性细胞因子水平检测
1.取各组小鼠相同节段结肠组织进行匀浆,离心后,bca试剂盒对匀浆上清进行蛋白定量
2.elisa方法检测上清中促炎性细胞因子的含量,以单位总蛋白中细胞因子的含量显示
三、实验研究发现和结果:
图1实验结果显示给予本发明的青蒿素衍生物灌胃治疗可明显改善dss诱导的炎症性肠病小鼠疾病症状,改善体重减轻、腹泻、便血等临床症状。图2a至2c实验结果显示给予本发明的青蒿素衍生物治疗可显著抑制由dss诱导炎症所致的结肠长度缩短和结肠病理学损伤。结肠病理切片he染色发现,肠炎组小鼠的结肠局部腺体结构紊乱,黏膜及黏膜下中性粒细胞及单核细胞和多核细胞等炎性细胞浸润,黏膜局部糜烂,部分隐窝破坏,而治疗组小鼠的上述变化得到明显缓解。图3a和图3b实验结果显示给予sm934治疗降低了肠系膜淋巴结和脾脏中巨噬细胞(抗f4/80+和cd11b+双阳性细胞)和中性粒细胞(gr-1+和cd11b+双阳性细胞)的比例;图4实验结果显示给予sm934治疗降低了单核淋巴细胞(cd11b+细胞)对结肠组织的浸润。致炎细胞因子(tnf-α,il-1,il-6,il-17等等)在调节肠道炎症免疫反应中起关键作用,参与炎症性肠病的发生发展过程。图5实验结果显示给予sm934治疗降低了结肠组织中促炎性细胞因子的水平。
因此,上述代表性化合物在硫酸葡聚糖(dss)诱导的炎症性肠病小鼠动物模型中的实验研究结果表明:灌胃给药能够有效改善实验动物的体重下降、腹泻、便血等结肠炎的临床症状,减轻结肠组织的病理学损伤,抑制实验小鼠炎症细胞对结肠组织的浸润,下调相关促炎性细胞因子的水平,药效药理学研究证实该类型化合物具有良好的抗炎免疫抑制活性和较高的安全性,在临床治疗和辅助治疗炎症性肠病方面具有良好的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!