NKILA作为靶点在筛选或制备治疗肿瘤的药物中的用途的制作方法
本发明涉及nkila的用途,具体涉及kila作为靶点在筛选或制备治疗肿瘤的药物中的用途。
背景技术:
免疫治疗包括过继性免疫效应细胞治疗以及免疫检查点抑制剂等,是近十多年肿瘤免疫治疗中十分活跃的研究领域,主要有以下方案:
1.肿瘤浸润性淋巴细胞(tumorinfiltratinglymphocyte,til)治疗,是从肿瘤组织分离具有抗肿瘤活性的淋巴细胞,体外经il-2培养增殖,再重新输入患者体内的细胞疗法。目前仅成功用于转移性黑素瘤的治疗,因为从其他类型的瘤组织中采集肿瘤特异性t细胞比较困难。
2.t细胞受体(t-cellreceptor,tcr)治疗,是收集患者t细胞,采用基因工程的手段导入可识别肿瘤抗原的tcr序列,使其识别特异性肿瘤抗原并杀伤肿瘤细胞。主要问题是tcr必须与患者的免疫类型匹配。有研究报道,导入mart-1及ny-eso-1分别在黑素瘤和滑膜细胞瘤患者中取得一定疗效。
3.嵌合抗原受体治疗(chimaericantigenreceptor,car),采用基因工程手段,在t细胞内导入可以与肿瘤细胞表面抗原结合的抗体样蛋白的编码基因,可以是常见癌症抗原的抗体、细胞受体片段或t细胞增殖刺激因子,优点是不需要与患者的免疫类型相匹配。目前有靶向b细胞上cd19蛋白的cart细胞治疗在小规模临床试验中有阳性结果,因为正常细胞上也表达cd19蛋白,因此副作用的产生不可避免。
4.免疫检查点抑制剂:目前研究和应用最广泛的免疫检查点抑制剂包括ctla-4、pd-1以及其配体pd-l1的抑制剂。利用免疫检查点抑制剂恢复t细胞的激活状态,借助人体免疫系统释放毒性因子等达到杀灭肿瘤目的的治疗策略,在黑色素瘤等恶性肿瘤中有一定的治疗效果。
目前恶性肿瘤的免疫节点抑制剂治疗效果仍不理想。例如在乳腺癌等多种恶性肿瘤中免疫节点抑制剂仍未显示出明显疗效;并且,目前的免疫治理药物针对靶点在正常组织中广泛表达,无差别地耗竭免疫抑制细胞极易造成自身免疫反应等严重副作用。一项对抗pd-1(nivolumab)单抗和抗ctla-4单抗联合治疗晚期黑色素瘤的研究中,有高达23%的患者因为治疗副反应停药,1例患者出现治疗相关性死亡(结肠炎导致的多器官衰竭)。而针对改善tcr及构建car-t的方法,有研究指出肿瘤内血管表达fasl,诱导t细胞发生凋亡,使具有功能的淋巴细胞无法到达肿瘤局部。
技术实现要素:
针对上述缺点,本发明的目的是为了解决具有杀肿瘤功能淋巴细胞无法到达肿瘤局部这一问题,通过改善淋巴细胞的生存,增加杀肿瘤的能力,增加免疫治疗的效果。
为实现上述目的,所采取的技术方案:nkila作为靶点在筛选或制备抑制t细胞凋亡的药物中的用途。
本发明提供了nkila作为靶点在筛选或制备治疗肿瘤的药物中的用途。
本发明提供了沉默nkila表达的shrna在制备抑制t细胞凋亡的药物中的用途。
本发明提供了沉默nkila表达的shrna在制备治疗肿瘤的药物中的用途。
优选地,所述shrna的核苷酸序列如seqidno:1或seqidno:2所示。
本发明提供了nkila表达被沉默的t细胞在制备治疗肿瘤的药物中的用途。
优选地,所述肿瘤为乳腺癌。
本发明的有益效果在于:本发明提供了nkila作为靶点在改善肿瘤特异淋巴细胞的生存从而抑制乳腺癌的生长和转移中的应用。所述nkila是一条与nfκb相互作用的长非编码rna,被鉴定为可抑制nfκb通路的激活,使t淋巴细胞易于发生凋亡,是一种新的抑制乳腺癌免疫逃逸、生长、转移的靶点。通过靶向抑制nkila,可抑制t细胞凋亡,促进乳腺癌的免疫反应,抑制乳腺癌的生长。
附图说明
图1为本发明实施例1中沉默t细胞的nkila可抑制aicd的相关图片;
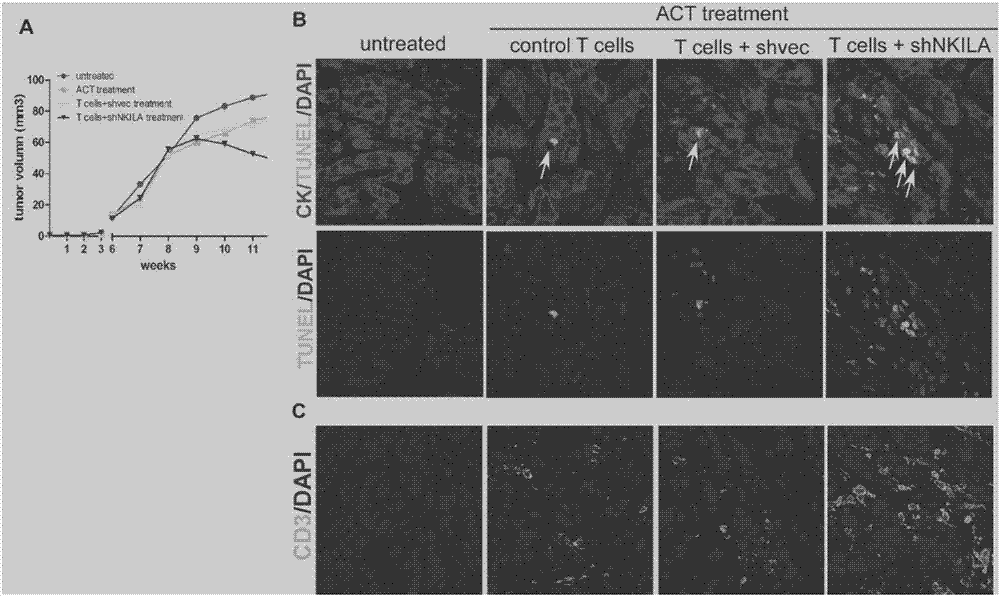
图2为本发明实施例2中过继性回输沉默nkila的t细胞,可使肿瘤局部浸润的t细胞数目增多,并抑制肿瘤生长的相关图片;
图3为肿瘤特异t细胞更易发生aicd的相关图片;
图4为t细胞诱导过程中,nfκb通路的活性决定了aicd的状态的相关图片;
图5为长非编码rnankila在t细胞诱导活化过程中上调的相关图片。
具体实施方式
为更好的说明本发明的目的、技术方案和优点,下面将结合具体实施例对本发明作进一步说明。
本发明实施例中所述沉默nkila表达的shrna的序列为:
本发明首次提出长非编码rnankila在t淋巴细胞表达,并在nfκb通路激活后上调,与nfκb激活呈负相关,说明nkila通过抑制iκb的磷酸化,抑制nfκb的活性,导致t细胞凋亡。通过靶向抑制nkila,可抑制t细胞凋亡,促进乳腺癌的免疫反应,抑制乳腺癌的生长。
实施例1:沉默t细胞的nkila可抑制aicd
图1为沉默t细胞的nkila可抑制aicd的相关图片,从图1中a可以看出沉默nkila可抑制aicd,从图1中b可以看出沉默nkila可增加t细胞杀伤肿瘤细胞的能力;
从图1的体外细胞实验证明沉默t细胞中的nkila,可解除nfκb的抑制,有效减少淋巴细胞的凋亡,增加其杀肿瘤的能力。
实施例2
图2为过继性回输沉默nkila的t细胞,可使肿瘤局部浸润的t细胞数目增多,并抑制肿瘤生长的相关图片;从图2中a可以看出过继性回输沉默nkila的t细胞使肿瘤明显缩小,从图2中b可以看出过继性回输沉默nkila的t细胞使肿瘤细胞凋亡增加;从图2中c可以看出过继性回输沉默nkila的t细胞后,肿瘤局部浸润的t细胞数目较对照组增多。
从图2的动物实验证明在小鼠皮下种植病人来源的移植瘤,同时收集同一个病人的外周血,分离出t淋巴细胞,并用慢病毒沉默nkila,成瘤后过继性回输同一个病人的t淋巴细胞,发现肿瘤明显缩小,肿瘤局部浸润的t细胞数目明显增多。
为使本发明更加容易理解,下面结合原理,进一步阐述本发明。
1.在诱导肿瘤特异效应t细胞的过程中,t细胞会发生活化诱导的细胞凋亡(activationinducedcelldeath,aicd)。前期t细胞的杀伤功能较弱,同时处于aicd耐受期,这一时期受到再次刺激,不会发生凋亡;后期t细胞的杀伤功能较强,同时处于aicd敏感期,在fasl的处理下迅速发生凋亡,如图3所示,从图3中a可以看出t细胞激活后,有杀肿瘤的能力,图3中b可以看出t细胞激活后,肿瘤特异t细胞发生aicd。
2.在肿瘤特异淋巴细胞诱导过程中,激活了nfκb通路,转录了抗凋亡的基因,使t细胞进入aicd耐受期;后期,由于iκb的磷酸化被抑制,nfκb的活性降低,t细胞进入aicd敏感期,如图4所示,从图4中a、b可以看出nfκb在aicd耐受期被激活,在aicd敏感期被抑制,主要因为抑制了iκb的磷酸化水平,导致p65入核减少,nfκb下游基因转录减少。
3.在肿瘤特异淋巴细胞诱导过程中,长非编码rnankila上调,且稳定在aicd敏感期高表达,定位在胞浆,如图5所示,图5中a.qrt-pcr显示nkila在t细胞诱导第4天明显上调;图5中b:fish显示nkila定位于t细胞胞浆;图5中c.northernblot显示nkila在t细胞aicd敏感期明显上调。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
序列表
<110>中山大学孙逸仙纪念医院
<120>nkila作为靶点在筛选或制备治疗肿瘤的药物中的用途
<130>2017
<160>2
<170>patentinversion3.3
<210>1
<211>19
<212>rna
<213>人工序列
<400>1
gggcaguaggaaaggagaa19
<210>2
<211>19
<212>rna
<213>人工序列
<400>2
ccuugcaaguagaggagaa19
- 还没有人留言评论。精彩留言会获得点赞!